暨南大学无机化学
暨南大学2015生科院复试名单及分数

暨南大学生科院2015年硕士生入学复试方案学院(公章):生命科学技术学院各专业复试考生名单海洋生物学与生物技术复试考生名单第一志愿生物工程(待补充)考生号考生姓名政治理论外国语业务课一业务课二初试总分初试排名105595210001831 揭辉洋64 59 133 103 359 1 105595210007427 文涛71 70 129 88 358 2 105595210008514 杨银64 63 130 95 352 3 105595210001832 李腾70 64 136 82 352 3105595210005377 刘俊伟62 62 120 102 346 5 105595210005573 钟思婷60 54 127 96 337 6 105595210008752 刘宇坤60 50 133 83 326 7 105595210002827 李广蒙68 46 121 91 326 7 105595210007426 刘艳梅56 61 111 96 324 9 105595210001503 彭德莲66 51 110 83 310 10 105595210000399 张钰65 65 107 64 301 11105595210004843 郭婷72 60 103 104 339 校内调剂105595210007222 陈俊良74 59 92 95 320 校内调剂105595210004669 刘玲67 53 74 106 300 校内调剂105595210003512 王文成64 51 100 82 297 校内调剂105595210001091 陈祥泰57 41 96 102 296 校内调剂105595210005436 许锡玲65 47 84 95 291 调剂生物医药考生号考生姓名政治理论外国语业务课一业务课二初试总分初试排名105595210002679 张甜甜67 51 129 117 364 1 105595210002565 王天翔68 48 117 116 349 2 105595210001746 王昆65 54 112 103 334 3 105595210004289 刘传68 48 111 103 330 4 105595210003740 冷洋73 48 105 102 328 5 105595210004958 陈静63 51 110 102 326 6 105595210000864 杜丽萍60 52 104 105 321 7 105595210002967 肖兴69 54 96 102 321 7 105595210007174 林舒莹63 54 108 94 319 9105595210000170 王楠楠62 57 96 102 317 10 105595210001744 邓朋飞63 47 104 102 316 11 105595210005700 林镇旺66 56 100 93 315 12 105595210005996 叶慧颖69 61 97 87 314 13 105595210007166 叶立坤65 50 109 90 314 13 105595210001743 董扬扬68 45 103 98 314 13 105595210003741 党诗莹60 55 102 96 313 16 105595210001464 秦秋平63 61 88 95 307 18 105595210007170 邹立功68 49 93 97 307 18细胞生物学考生号考生姓名政治理论外国语业务课一业务课二初试总分初试排名105595210003044 毛晓彤72 58 121 119 370 1 105595210001124 胡刘兵74 40 121 104 339 2 105595210007136 黄家荣60 42 110 101 313 3 105595210002019 王敏珍57 63 99 91 310 5 105595210002965 郭燕可59 49 119 83 310 5 105595210008444 洪文宾63 41 104 101 309 7 105595210004955 卢雪萍56 43 107 101 307 8 105595210001394 颜亮59 37 106 100 302 9 105595210003866 陈少敏71 37 99 92 299 10 105595210005992 莫亦佳65 53 85 90 293 11 105595210005563 莫善仪62 57 86 88 293 11 105595210004666 龙彦宇53 51 98 86 288 13 105595210005991 邓艳62 49 94 82 287 14 105595210001463 吴栋雄62 40 88 94 284 15 105595210007134 吴杰64 43 89 85 281 16水生所专业参加复试考生的名单(待继续补充)一、水生生物学考生号考生姓名政治理论外国语业务课一业务课二初试总分初试排名105595210008574 刘惠茹68 56 118 118 360 1 105595210003041 孟鸽67 58 119 110 354 2 105595210003865 张辉杰60 45 118 97 320 3 105595210003735 陈飞66 55 89 108 318 4 105595210003814 张玲丽59 70 108 80 317 5 105595210001726 朱忆秋65 54 105 91 315 6 105595210007124 陈爱玲66 50 104 93 313 7 105595210008215 刘洪65 54 80 112 311 8 105595210005686 李丽梅63 58 104 83 308 9 105595210003552 杨思远61 45 96 105 307 10 105595210008443 徐梓钧55 45 99 101 300 12 105595210000788 李凌云70 36 90 101 297 13 105595210002071 曾俊67 40 91 94 292 14 105595210004212 韩诺63 58 70 94 285 15 105595210002673 赵彦花58 41 105 75 279 16 105595210005685 卓泉龙67 51 79 80 277 17 105595210007182 阮紫曦64 56 112 79 311 调剂105595210002336 袁朝杰66 51 112 84 313 调剂105595210002121 何崇单62 37 133 79 311 调剂105595210003936 江小璐66 56 111 76 309 调剂105595210002157 邱小芳61 46 108 92 307 调剂105595210008679 张悦64 45 113 84 306 调剂105595210007183 温旭66 36 118 86 306 调剂105595210002680 张振华65 44 118 70 297 调剂二、生态学考生号考生姓名政治理论外国语业务课一业务课二初试总分初试排名105595210001913 杜小琴64 59 142 98 363 1 105595210001747 甘磊62 50 138 98 348 2105595210000356 傅宝珠62 53 137 96 348 2 105595210003561 杨洋63 56 135 92 346 4 105595210003194 郭菁菁64 52 134 94 344 5 105595210005702 龙艾虹67 53 129 94 343 6 105595210003560 肖晗67 53 133 88 341 7 105595210000397 苏玲64 50 131 94 339 8 105595210007180 梁采莹66 49 135 89 339 8 105595210002451 黄镇宇66 52 122 95 335 10 105595210008751 吴梓钊72 42 134 84 332 11 105595210003742 刘磊66 62 131 69 328 12 105595210000970 张依70 45 132 79 326 13 105595210008711 丁西飞59 46 129 87 321 15 105595210003223 吴中奎65 56 116 79 316 16 105595210001748 杨瑜芬63 46 116 91 316 16 105595210002120 王璐畇54 43 139 80 316 16 105595210007178 樊静静65 47 120 80 312 21 105595210000321 李瑾66 47 109 73 295 32三、环境科学考生号考生姓名政治理论外国语业务课一业务课二初试总分初试排名105595210002122 黄琦62 54 84 132 332 1 105595210008874 成凯63 41 76 134 314 2发育生物学再生医学专业复试考生:生物医学工程专业学位(085230)复试名单(待补充)生物医学工程专业学位调剂考生复试名单:动物学复试名单:(待补充)遗传学复试考生名单:二、化学系各专业参加复试考生的名单。
2014暨南大学复试方案 名单
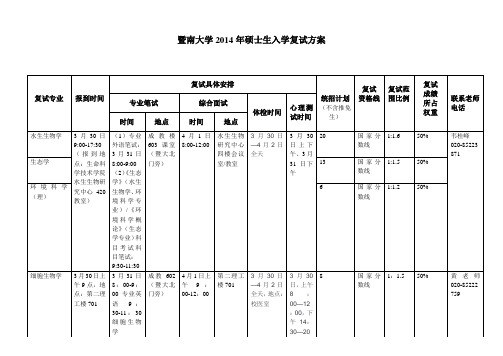
暨南大学2014年硕士生入学复试方案二、各专业参加复试考生的名单1、水生生物学(待继续补充)2、生态学(待继续补充)3、环境科学(待继续补充)4、生物医药考生号考生姓名性别政治理论外国语业务课一业务课二初试总分105594210001787 吴旭鹏男76 68 118 123 385 105594210007387 王得华女62 68 117 126 373 105594210007386 李曾丽女69 55 116 131 371 105594210005869 张光林男66 57 114 125 362 105594210008982 杨阳女63 55 120 121 359 105594210007393 余文佳女65 53 109 127 354105594210000140 刘艳婷女59 68 112 115 354 105594210002564 解展志女62 55 111 125 353 105594210002641 方思南男71 52 109 119 351 105594210007391 胡伟雄男71 53 113 114 351 105594210005171 黄云娜女62 56 118 113 349 105594210002361 覃锦红女63 65 104 114 346 105594210000371 韩磊男67 56 109 112 344 105594210002981 王继重男72 45 108 118 343 105594210006125 陈铭锋男74 43 107 119 343 105594210005680 邓颖莎女59 53 112 118 342 105594210008318 韦焕男60 50 114 114 338 105594210002705 李艳伟女61 67 110 100 338 5、细胞生物学(待继续补充)考生号考生姓名性别政治理论外国语业务课一业务课二初试总分105594210004926 肖旭晖女63 61 113 126 363 105594210008432 安春景女72 45 113 118 348 105594210007356 郑迪威男57 50 112 129 348 105594210001780 王丽芳女61 61 108 116 346 105594210004441 魏红霞女57 57 106 121 341 105594210007358 田华健男60 62 109 109 340 105594210002689 张宇女63 55 104 109 331 105594210001199 刘鸽女61 48 114 107 330 105594210005456 何六一男65 50 94 103 312 105594210001944 吴杰男55 53 96 95 2996、生物工程(待继续补充)考生号考生姓性别政治理外国语业务课业务课初试总备注名论一二分105594210000501 胡超智男58 45 142 106 351105594210003751 吴皓男65 52 113 120 350105594210002872 田璐女57 63 109 108 337105594210003362 徐海朋男57 56 115 107 335105594210002913 赵志磊男70 58 105 92 325105594210002301 宋莹女60 57 104 94 315105594210007629 李子毅男64 56 100 94 314105594210005881 陈耀男58 49 108 93 308105594210006147 张卓男61 48 95 85 289105594210002362 周生玉女58 48 105 124 335 生物医药调剂105594210006123 陈纯女67 55 100 107 329 生物医药调剂105594210001786 王海龙男66 50 101 97 314 生物医药调剂105594210007388 王璐女59 55 96 97 307 生物医药调剂7、免疫学(生科院)免疫学(生物医学转化研究院)调剂中9、发育生物学10、动物学(待继续补充)11、生物化学与分子生物学12、遗传学13、再生医学14、海洋生物学与生物技术15、生物医学工程复试考生的名单(待继续补充)16、分析化学17、无机化学18、物理化学19、有机化学20、高分子化学与物理21、应用化学2014年生命科学技术学院调剂复试名单。
暨南大学无机化学下期末试卷

暨南大学无机化学下期末试卷姓名: 班别:学号:一、选择题: 请把正确答案的字母填在各小题前的( )内。
(15分)( B ) 1. 键能大小正确的顺序是A. B-B > C-C > Si-SiB. C-C > B-B > Si-SiC. Si-Si > B-B > C-CD. C-C > Si-Si > B-B( D ) 2. 下列各组元素中,性质最相似的两种元素是A. Co和NiB. Mg和AlC. B和SiD. Mo和W( C ) 3. 用氢氧化钠熔融法分解矿石时最合适用的容器是A. 铂坩埚B. 石英坩埚C. 镍坩埚D. 铁坩埚( D ) 4. 过量氨水加于Hg2Cl2,生成A. Hg(OH)2B. Hg(NH3) 2+C. Hg(NH3) 42+D. HgNH2Cl + Hg ( A ) 5. 可以用于治疗癌症的含铂药物是A. cis-PtCl2(NH3)2B. PtCl4C. H2PtCl6D. trans-PtCl2(NH3)2 ( D ) 6. 下列各组元素中,都可以形成多酸的是A. V,Ag,ZnB. Fe,Co,NiC. B,N,PD. Mo,Si,P( A ) 7. 可用PdCl2溶液检测的气体是A. COB. CO2C. O3D. Cl2( B ) 8. 下列化学方程式正确的是A. SiO2(s) + 2Cl2(g) = SiCl4(l) + O2(g)B. 2H2S(aq) + SnCl4(aq) = SnS2(s) + 4HCl(g)C. 2H2S(aq) + PbCl4(aq) = PbS2(s) + 4HCl(g)D. Cu2+(aq) + 4I-(aq) = [CuI4]2-(aq)( C ) 9. 既可溶于NaOH,又可溶于氨水的是A. Ni(OH)2B. Fe(OH)3C. Zn(OH)2D. Al(OH)3( A ) 10. 某金属离子在八面体弱场中的磁矩为4.9 B.M.,而在八面体强场中的磁矩为0 B.M.,该金属离子可能是A. Co3+B. Mn2+C. Cr3+D. Fe3+( C ) 11. 下列各对配合物稳定性顺序不正确的是A. [Fe(CN)6]3- > [Fe(H2O)6]3+B. [Fe(CN)6]4- <[Fe(CN)6]3-C. [HgCl4]2- > [HgI4]2-D. [Al(OH)4]- <[Zn(OH)4]2-( C ) 12. 下列配合物中,不满足“有效原子序规则”的是A. Fe(CO)5B. Mn2(CO)10C. V(CO)5D. Fe(C5H5)2( B ) 13. 以Fe2O3(s)为原料制备高铁酸盐应选择的试剂是A. NaClO + 稀H2SO4B. KNO3+ KOHC. H2O2 + 稀H2SO4D. 浓H2SO4 + Cl2(g) ( D ) 14. 下列配离子中, 分裂能O最大的是A. [Fe(CN)6]4B. [Fe(H2O)6]2+C. [Ru (CN)6]4D. [Os(CN)6]4( A ) 15. 63 Eu3+ 离子是许多发光材料中的激活离子,其基态价电子构型是A. 4f 6B. 4f56s1C. 4f55d 1D. 4f45d 16s1二、填空题 (15分)1. TlCl3(s) 在313 K分解,相应的化学方程是 TlCl3(s) = TlCl(s) + Cl2(g) ,化学式为TlI3(s)的化合物存在,其中Tl元素的氧化数是 +1 ;上述现象说明 Tl(III)的强氧化性,是由6s2惰性电子对效应引起。
暨南大学-2018年-硕士学位研究生入学考试真题-710无机化学

考试科目:710无机化学
考生注意:所有答案必须写在答题纸(卷)上,写在本试题上一律不给分。
一、选择题(选择一个正确答案,每小题3分,20题共60分)
1.液体沸腾过程中,下列物理量中数值增大的是····························()
A.摩尔熵B.摩尔自由能
C.蒸气压D.液体质量
A.平衡向左移动B.平衡向右移动
C.平衡不发生移动D.条件不足,不能判断
15.根据价层电子对互斥理论,SO32-的空间构型为····························()
A.平面三角形B. V形C.正四面体D.三角锥形
16.下列配体与过渡金属形成配位化合物时,有可能形成反馈π键的配体是······()
A、s区B、d区C、p区D、ds区
19.下列阴离子的水溶液,若浓度相同,碱性最强的是························()
A.F-(HF, pKa=3.18)-(HCN, pKa=9.21)
C.Ac-(HAc, pKa=4.74)D.S2-(H2S, pKa1=6.88, pKa2=12.92)
A. Zr, Hf B. Mg, Al C. Li, Be D. Co, Ni
4.下列哪个轨道上的电子在xy平面上出现的概率为0·····················()
A. 3pzB. 3dx2-y2C. 3s D. 3dz2
5.下列物质中,中心原子采取不等性杂化的是····························()
20.以下元素的原子半径递变规律正确的是································()
A.B<C<Al<SiB.C<B<Si<Al
无机化学排名

070301 无机化学研究元素、单质和无机化合物的来源、制备、结构、性质、变化和应用的一门化学分支。
对于矿物资源的综合利用,近代技术中无机原材料及功能材料的生产和研究等都具有重大的意义。
当前无机化学正处在蓬勃发展的新时期,许多边缘领域迅速崛起,研究范围不断扩大。
已形成无机合成、丰产元素化学、配位化学、有机金属化学、无机固体化学、生物无机化学和同位素化学等领域。
无机化学是研究无机物质的组成、性质、结构和反应的科学,它是化学中最古老的分支学科。
无机物质包括所有化学元素和它们的化合物,不过大部分的碳化合物除外。
|(除二氧化碳、一氧化碳、二硫化碳、碳酸盐等简单的碳化合物仍属无机物质外,其余均属于有机物质。
)无机化学是除碳氢化合物及其衍生物外,对所有元素及其化合物的性质和他们的反应进行实验研究和理论解释的科学,是化学学科中发展最早的一个分支学科。
过去认为无机物质即无生命的物质,如岩石、土壤,矿物、水等;而有机物质则是由有生命的动物和植物产生,如蛋白质、油脂、淀粉、纤维素、尿素等。
1828年德意志化学家维勒从无机物氰酸铵制得尿素,从而破除了有机物只能由生命力产生的迷信,明确了这两类物质都是由化学力结合而成。
现在这两类物质是按上述组分不同而划分的。
排名学校名称等级1 南京大学A+2 吉林大学 A+3 南开大学A+4 北京大学A+5 中国科学技术大学 A南京大学:http:/NewsSpecialDetailsInfo.aspx?SID=19944 吉林大学:http:/NewsSpecialDetailsInfo.aspx?SID=5431 南开大学:http:/NewsSpecialDetailsInfo.aspx?SID=1161 北京大学:http:/NewsSpecialDetailsInfo.aspx?SID=20 中国科学技术大学:http:/NewsSpecialDetailsInfo.aspx?SID=6643北京大学--化学与分子工程学院-- 无机化学中国人民大学--化学系-- 无机化学北京科技大学--应用科学学院-- 无机化学北京师范大学--化学学院-- 无机化学南开大学--化学学院-- 无机化学天津大学--理学院-- 无机化学中国石油大学(北京)--化工科学与工程学院-- 无机化学天津师范大学--化学与生命科学学院-- 无机化学河北大学--化学学院-- 无机化学河北师范大学--化学与材料科学学院-- 无机化学山西大学--分子所-- 无机化学山西师范大学--化学与材料科学学院-- 无机化学内蒙古师范大学--化学与环境科学学院-- 无机化学大连理工大学--化工学院-- 无机化学东北大学--理学院-- 无机化学辽宁大学--化学院-- 无机化学辽宁师范大学--化学化工学院-- 无机化学吉林大学--化学学院-- 无机化学东北师范大学--化学学院-- 无机化学延边大学--理学院-- 无机化学长春理工大学--化学与环境工程学院-- 无机化学哈尔滨工业大学--理学院-- 无机化学武汉大学--化学与分子科学学院-- 无机化学复旦大学--化学系-- 无机化学中国科学技术大学--化材院化学系-- 无机化学中国科学技术大学--合肥智能机械研究所-- 无机化学黑龙江大学--化学化工与材料学院-- 无机化学复旦大学--先进材料与技术研究院-- 无机化学哈尔滨师范大学--理化学院-- 无机化学华东理工大学--化学与分子工程学院-- 无机化学华东师范大学--化学系-- 无机化学齐齐哈尔大学--化学与化学工程学院-- 无机化学上海大学--理学院-- 无机化学上海师范大学--生命与环境科学学院-- 无机化学同济大学--化学系-- 无机化学安徽大学--化学化工学院-- 无机化学安徽师范大学--化学与材料科学学院-- 无机化学安庆师范学院--化学化工学院-- 无机化学淮北煤炭师范学院--化学系-- 无机化学福建师范大学--化学与材料学院-- 无机化学福州大学--化学化工学院-- 无机化学华侨大学--材料科学与工程学院-- 无机化学厦门大学--化学系-- 无机化学华南理工大学--化学科学学院-- 无机化学华南师范大学--化学-- 无机化学暨南大学--生命科学技术学院-- 无机化学汕头大学--理学院-- 无机化学中山大学--化学与化学工程学院-- 无机化学广西师范大学--化学工学院-- 无机化学河南大学--化学化工学院-- 无机化学河南师范大学--化学与环境科学学院-- 无机化学郑州大学--化学系-- 无机化学湖北大学--化学与材料科学学院-- 无机化学华中科技大学--化学系-- 无机化学四川省社会科学院--理学院-- 无机化学中南民族大学--化学与材料科学学院-- 无机化学湖南师范大学--化学化工学院-- 无机化学湘潭大学--化学学院-- 无机化学中南大学--化学化工学院-- 无机化学南昌大学--理学院-- 无机化学济南大学--化学化工学院-- 无机化学聊城大学--化学化工学院-- 无机化学青岛科技大学--化学院-- 无机化学青岛科技大学--材料学院-- 无机化学曲阜师范大学--化学科学学院-- 无机化学山东大学--化学与化工学院-- 无机化学山东大学--晶体材料研究所-- 无机化学山东师范大学--化学、化工与材料科学学院-- 无机化学中国海洋大学--化学化工学院-- 无机化学四川大学--化学学院-- 无机化学四川大学--生物材料研究工程中心-- 无机化学四川大学--原子核科学技术研究所-- 无机化学西南科技大学--材料科学与工程学院-- 无机化学西南大学--化学化工学院-- 无机化学西南师范大学--化学化工学院-- 无机化学兰州大学--化学化工学院-- 无机化学兰州交通大学--化学与生物工程学院-- 无机化学西北师范大学--化学化工学院-- 无机化学贵州大学--理学院-- 无机化学青海师范大学--化学系-- 无机化学陕西科技大学--化学与化工学院-- 无机化学陕西师范大学--化学与材料科学学院-- 无机化学西北大学--化学系-- 无机化学华中师范大学--化学学院-- 无机化学南京大学--化学化工学院-- 无机化学南京工业大学--化学化工学院-- 无机化学南京理工大学--化工学院-- 无机化学南京农业大学--化学化工学院-- 无机化学南京师范大学--化学与环境科学学院-- 无机化学南京艺术学院--化学化工学院-- 无机化学苏州大学--化学化工学院-- 无机化学苏州科技大学--化学化工学院-- 无机化学宁波大学--材化学院-- 无机化学武汉理工大学--理学院-- 无机化学。
考研真题:广东暨南大学2022年[无机化学]考试真题
![考研真题:广东暨南大学2022年[无机化学]考试真题](https://img.taocdn.com/s3/m/f3335a70bf23482fb4daa58da0116c175e0e1e44.png)
考研真题:暨南大学2022年[无机化学]考试真题一、选择题1、根据质子酸碱理论,下列物质中既是酸又是碱的是()。
A、Ac-B、HCO3-C、PO43-D、NH4+2、液体沸腾过程中,下列物理量中数值增大的是()。
A、摩尔熵B、蒸气压C、摩尔自由能D、液体质量3、1.0 mol·L-1 NH4HF2(p Kθa1 = 3.18 和p Kθa2 = 4.74)溶液的pH值是()。
A、1.59B、6.22C、3.18D、9.264、下列纯物质中,哪个单质的标准摩尔生成焓不等于零()。
A、Br2 (l)B、Fe (s)C、金刚石D、石墨5、对于一个给定的条件下的反应,随着反应的进行()。
A、速率常数k变小B、平衡常数K变大C、正反应速率降低D、正反应速率增加6、在乙酸溶液中加入下列物质,会使乙酸的解离度降低的是()。
A、KClB、HClC、NaNO3D、CaCl27、1 mol O2 (g) 与2 mol H2 (g) 完全反应生成2 mol H2O (g),反应进度ξ为()。
A、0.5 molB、1 molC、2 molD、无法判断8、增加相同温度时,反应速率增加幅度大的是()。
A、多分子反应B、双分子反应C、活化能大的反应D、活化能小的反应9、多电子原子中,各电子具有下列量子数,其中能量最高的电子是()。
A、1,1,-1,1/2B、2,0,0,1/2C、4,1,-1,-1/2D、3,2,-1,-1/210、过量AgCl溶解在下列物质中,Ag+离子浓度最小的是()。
A、100 mL水B、100 mL 0.2 mol·L-1的KCl溶液C、500 mL水D、500 mL 0.7 mol·L-1的KNO3溶液11、在配离子[Co(en)(C2O4)2]-中,中心离子的配位数是()。
A、6B、5C、4D、312、[Co(NH3)6]3+是内轨型配合物,中心离子未成对电子数和杂化轨道类型是()。
2019年暨南大学考研真题710无机化学A

三、计算题(共3题,每题10分,共30分)
(2)在1 mol/L的氨水溶液中,Co(III)能否将水氧化?
四、完成反应方程式并配平(共4题,每题4分,共16分)
1.将AgBr溶于Na2S2O3溶液中;
2.用N2H4还原AgBr;
3.金溶于王水;
4. Mg3N2与水反应。
五、简答题(共3题,每题8分,共24分)
1.硅胶干燥剂中常加入CoCl2(蓝色),吸水后变为粉红色,试用晶体场理论解释变色的原理。
2019年招收攻读硕士学位研究生入学考试试题
********************************************************************************************
招生专业与代码:无机化学、分析化学、有机化学、物理化学、高分子化学与物理
15.某晶体的晶胞参数满足关系a=b=c,α=β=γ,则下列判断正确的是()
(A)一定属于立方晶系(B)一定属于三方晶系
(C)一定属于六方晶系(D)属于立方晶系或三方晶系
16.由两元素的电负性数值,可以预测()
(A)配位数(B)分子的偶极矩(C)分子的极性(D)键的极性
17.反应N2(g) + 3H2(g) 2NH3(g)在恒压下进行时,若向体系中通入一定量的氩气,则氨气的产率()
1/2 Cl2+Fe2+→Cl+Fe3+ ,
暨南大学2017硕士生入学复试方案

51
128
109
348
41
105597210005122
黄弘毅
男
有机化学
55
71
98
122
346
42
105597210007639
林兆廷
男
无机化学
68
44
118
115
345
43
105597210012476
李代春
男
有机化学
65
59
116
105
345
44
105597210010257
关灼斌
男
有机化学
60
65
96
98
319
8
105597210012800
张旭
男
化学工程
63
56
109
85
313
9
105597210007949
吴浩萍
女
化学工程
62
69
68
112
311
10
105597210003265
赖洁
女
化学工程
64
62
80
103
309
11
105597210007346
王海林
男
化学工程
77
67
87
76
307
12
105597210010701
林盛繁
男
化学工程
71
70
64
88
293
13
105597210003742
熊才艺
男
化学工程
59
61
70
暨南大学考研各专业参考书目汇总-暨大各专业考研指定教材是什么?-暨南大学考研参考书目如何获得?

2019暨南大学考研各专业参考书目汇总——暨南大学各专业考研指定教材是什么?暨南大学2018年有一些专业在考试大纲里面指定了参考书,鸿知暨大考研网在下文为各位考生整理了这些专业的官方指定参考书目,如果考生报考的专业没有官方指定参考书目,可以登入,鸿知暨大考研网()免费向暨南大学研一研二学长学姐或考研老师咨询。
同时鸿知暨南大学考研网还提供海量暨大考研真题答案,需要的同学可以点击查看2018年暨南大学240基础日语主要参考书目:1.《中日交流标准日本语(新版)》(初级),上册,北京:人民教育出版社,2005.2.《中日交流标准日本语(新版)》(初级),下册,北京:人民教育出版社,2005.3.《中日交流标准日本语(新版)》(中级),上册,北京:人民教育出版社,2008.2018年暨南大学280法语参考书目孙辉,《简明法语教程》(上、下册),北京:商务印书馆,2008年。
陈振尧,《新编法语语法》,北京:外语教学与科研出版社,1993年。
2018年暨南大学308护理综合参考书目1.《基础护理学》(第5版,李小寒主编,人民卫生出版社,2013年)2.《内科护理学》(第5版,尤黎明主编,人民卫生出版社,2013年)3.《外科护理学》(第5版,曹伟新主编,人民卫生出版社,2013年)4.《妇产科护理学》(第5版,郑修霞主编,人民卫生出版社,2013年)5.《儿科护理学》(第5版,崔焱主编,人民卫生出版社,2013年)鸿知暨大考研网链接地址:/暨大考研真题答案链接地址:/kaoyan/2018年暨南大学352口腔综合参考书目主要参考书目以卫生部“十一五”规划教材、全国高等学校教材、供口腔医学类专业用为主。
①《口腔解剖生理学》,皮昕主编,第六版②《口腔组织病理学》,于世凤主编,第六版③《口腔颌面外科学》,邱蔚六主编,第六版④《口腔修复学》,赵铱民主编,第六版⑤《牙体牙髓病学》,樊明文主编,第三版⑥《牙周病学》,孟焕新主编,第三版⑦《口腔黏膜病学》,陈谦明主编,第三版2018年暨南大学353卫生综合参考书目1.《卫生学》(第7版,仲来福主编,人民卫生出版社,2008年)2.《流行病学》(第6版,王建华主编,人民卫生出版社,2005年)3.《卫生统计学》(第6版,方积乾主编,人民卫生出版社,2005年)2018年暨南大学432应用统计参考资料1.《统计学原理》(第七版)韩兆洲主编,暨南大学出版社2010年12月。
无机化学

无机化学一、专业介绍1、概述:无机化学是化学下属的二级学科,是以实验为基础的一门基础性学科,是研究无机物质的组成、性质、结构和反应的科学,是化学中最古老的分支学科。
近年来,无机化学的研究与发展越来越受到化学界的重视,现已从最早的理论性研究逐步地进入到人类社会的现代化建设中。
无机化学是我国最早设置的化学专业之一。
2、研究方向:无机化学的研究方向主要有01无机合成化学02能源材料化学03无机纳米材料04化学电源05功能性配合物化学06生物无机化学(注:各大院校的研究方向有所不同,以南开大学为例)3、培养目标:本专业硕士学位获得者应具有较深厚的近代无机化学和结构化学等基础理论知识;熟悉并掌握近代无机合成技术以及对化合物进行表征的常用近代物理研究方法、现代化学实验技术;了解相关领域在国内外的现状和发展趋势,能够适应我国经济、科技、教育发展需要;具有较好的实验技能和总结归纳分析问题的能力,能独立进行科研工作;有严谨的学风;至少掌握一门外国语,具有较熟练的阅读能力以及一定的写作和听说能力。
毕业后可胜任高校、科研院所和企业单位的教育、科研和应用开发或管理工作。
4、研究生入学考试科目:①101思想政治理论②201英语一③708综合化学④820无机化学(注:各大院校的考试科目有所不同,以南开大学为例)5、相关专业与无机化学专业相关的二级学科有:分析化学、有机化学、物理化学、高分子化学与物理二、专业素质要求及就业无机化学是化学科学中发展最早的一个分支学科。
它承担着研究所有元素的单质和化合物(碳氢化合物及衍生物除外)的组成、结构、性质和反应的重大任务。
当前无机化学的发展有两个明显趋势,即在广度上的拓宽和深度上的推进。
它与现代文明的三大支柱:能源、信息和材料紧密相联。
随着各学科的相互渗透及其自身的新成就,无机化学学科已发展到一个新阶段,在新材料的制备及应用上,已具有了相当重要的战略地位,具有广阔的发展前景,同步于材料科学、生命科学以及信息、能源的发展,是各类交叉学科的源始学科,特别是材料科学的发展强烈地依赖于无机化学。
2023年暨南大学710 无机化学考研真题试卷

2023年招收攻读硕士学位研究生入学考试试题********************************************************************************************招生专业与代码:化学一级学科0703考试科目名称及代码:710无机化学考生注意:所有答案必须写在答题纸(卷)上,写在本试题上一律不给分。
一、选择题(选择一个正确答案,每小题2分,20题共40分)1. 下列最稳定的化合物是:(A) CsF (B)CsCl (C) CsBr (D) CsI2.当基态原子的第六电子层只有2个电子时,则原子的第五电子层的电子数为:(A) 8 (B) 18 (C) 8 ~ 18 (D) 8 ~ 323. 下列固体碳酸盐分解温度最低的是:(A) 碳酸镁(B) 碳酸钙(C) 碳酸锶(D) 碳酸钡4. 一级反应的半衰期与反应物初始浓度的关系为:(A) 成正比(B) 成反比(C) 无关(D) 立方根成正比5. 将1.0 mol/L NaAc与0.10 mol/L H3BO3等体积混合,所得溶液pH是:[p K a(HAc) = 4.74, p K a(H3BO3) = 9.24](A) 6.49 (B) 6.99 (C) 7.49 (D) 9.226.下列分子中属于极性分子的是:(A) SO3(B) CO2(C) O3(D) C2H47. 浓度相同的下列物质水溶液的pH最高的是:(A) NaCl (B) NaHCO3(C) NH4Cl (D) Na2CO38. 在等压下,无论用什么手段进行一个A+B=C的反应,若⊿r H m 0,则该反应一定为:(A)吸热反应(B)放热反应(C)视反应手段而定(D)无热量变化9. 在刚性密闭容器中,有下列理想气体反应达平衡,A(g) + B(g)C(g),若在恒温下加入一定量惰性气体,则平衡将:(A)向右移动(B)向左移动(C)不移动(D)无法确定10. 含有下列离子的溶液,与Na2S溶液反应不生成黑色沉淀的一组是:(A) Fe2+,Bi3+(B) Cd2+,Zn2+(C) Fe3+,Cu2+(D) Mn2+,Pb2+考试科目:无机化学共4 页,第 1 页考试科目:无机化学共4 页,第 2 页二、填空题(6小题,每空1分,共25分)1.第二周期同核双原子分子或离子具有以下分子轨道电子排布,X2:(σ1s)2(σ1s*)2(σ2s)2(σ2s*)2(σ2p)2(π2py)2(π2pz)2 (π2py*)1 (π2pz*)1, Y2-:(σ1s)2(σ1s*)2 (σ2s)2(σ2s*)2(π2py)2 (π2pz)2(σ2p)2(π2py*)1, 这两种元素分别是(X) 和(Y) 。
暨南大学(已有10全套试题)

暨南大学〔2021全套〕经济学院西方经济学2002——2005,2021,2021〔均为回忆版〕金融学根底〔联考〕2002——2021〔2002——2007有答案〕概率论与数理统计2005〔回忆版〕概率统计2001统计学原理2001管理学院西方经济学2002——2005,2021,2021〔均为回忆版〕产业经济学2005心理统计与心理测量2005〔回忆版〕会计学〔一〕1998——2002〔其中2002为回忆版〕会计学〔二〕1998——2002〔其中2002为回忆版〕会计学2003〔回忆版〕,2006〔回忆版〕管理学1996——2001,2003——2005〔其中2003和2005为回忆版〕微观与宏观经济学2004——2005管理学与微观经济学〔会计学、企业管理、旅游管理专业〕2021〔回忆版〕行政管理学2005教育经济学2005公共政策2021〔回忆版〕公共管理学2021〔回忆版〕法学院国际经济法2003〔回忆版〕国际法2003国际关系学2002——2003国际政治与国际关系2001国际关系史2002——2003,2021,2021〔2021为回忆版〕国际政治、国际关系专业综合考试2001国际关系专业经济方向试题〔专业根底〕2003世界经济1998——2002法学综合(宪法、国际法)2021〔回忆版〕法学专业根底(经济法、民法)2021〔回忆版〕文学院美学原理2021〔回忆版〕美学评论与写作2021〔回忆版〕文学理论2003〔回忆版〕中国古代文学史2003〔回忆版〕欧美文学史2005〔回忆版〕现当代文学2021〔回忆版〕文学理论2021〔回忆版〕中国通史2004,2006〔均为回忆版〕世界通史2004,2006〔均为回忆版〕华文学院语言学综合(含语言学概论、古代汉语和写作) 2004——2006〔均为回忆版〕现代汉语A 2004——2007〔均为回忆版〕语言文学根底理论2021〔回忆版〕外国语学院〔无此专业试卷〕新闻与传播学院传播理论2002传播业务2005〔回忆版〕,2006〔回忆版〕,2007〔回忆版〕传播史论2005〔回忆版〕,2006〔回忆版〕,2007〔回忆版〕新闻传播理论1995——2001〔答案有:2001〕新闻传播史论2003,2021〔2021为回忆版〕新闻传播业务2021〔回忆版〕新闻理论2002〔回忆版〕新闻业务1995——2001,2002〔回忆版〕,2003〔回忆版〕,2005〔回忆版〕,2006〔回忆版〕,2007〔回忆版〕新闻史论2005〔回忆版〕,2006〔回忆版〕,2007〔回忆版〕中外新闻事业史1995——2001,2002〔回忆版〕暨南大学期末考试试卷:〔以下试卷每份10元〕:1、新闻采访学2001-2002学年度第一学期考试试卷A卷2、新闻采访学2001-2002学年度第一学期考试试卷B卷〔缺页〕3、中国新闻史2001-2002学年度第二学期考试试卷A卷4、中国新闻史2001-2002学年度第二学期考试试卷B卷5、传播学概论2001-2002学年度第一学期考试试卷A卷6、传播学概论2001-2002学年度第一学期考试试卷B卷7、新闻学概论2001-2002学年度第一学期考试试卷A卷8、外国新闻史期末考试试卷1份9、播送电视概论2001-2002学年度第一学期考试试卷1、?播送电视概论?教学大纲〔彭伟步老师编〕共91页,85元。
化学类专业及院校介绍

化学类专业及院校介绍1.化学主干学科:化学主要课程:无机化学、分析化学(含仪器分析)、有机化学、物理化学(含结构化学)、化学工程基础等。
包括生产实习、毕业论文等,一般安排10~20周。
培养目标本专业培养具备化学的基础知识、基本理论和基本技能,能在化学及与化学相关的科学技术和其它领域从事科研、教学、技术及相关管理工作的高级专门人才。
培养要求本专业学生主要学习化学方面的基础知识、基本理论和基本技能与方法,受到科学思维和科学实验的训练,具有一定的科学研究、应用研究及科技管理的能力。
就业方向1.掌握数学、物理等方面的基本理论和基本知识;2.掌握无机化学、分析化学(含仪器分析)、有机化学、物理化学(含结构化学)及化学工程的基础知识、基本原理和基本实验技能;3.了解相近专业的一般原理和知识;4.了解国家关于科学研究、化学相关产业的政策,国内外知识产权等方面的法律法规;5.了解化学某些领域的理论前沿、应用前景和最新发展动态以及化学相关产业发展状况:6.掌握中外文资料查询、文献检索及运用现代信息技术获取相关信息的基本方法;具有一定的实验设计,创造实验条件,归纳、整理、分析实验结果,撰写论文,参与学术交流的能力。
开设院校[北京]清华大学[广东]中山大学[上海]复旦大学[北京]北京理工大学[北京]中国人民大学[河南]郑州大学[吉林]吉林大学[江苏]苏州大学[天津]南开大学[湖南]湖南大学[重庆]西南大学[山东]中国海洋大学[四川]成都理工大学[山东]青岛科技大学[北京]北京师范大学[广东]广州大学[北京]中国农业大学[上海]华东师范大学[甘肃]兰州大学[陕西]西北大学[河北]河北大学[辽宁]辽宁大学[安徽]安徽大学[四川]西南石油大学[辽宁]大连大学[河南]河南大学[北京]中央民族大学[江苏]扬州大学[天津]天津师范大学[四川]四川师范大学[广东]华南师范大学[湖北]华中师范大学[浙江]宁波大学[湖南]湘潭大学[山东]山东师范大学[江苏]南京工业大学[江苏]江苏大学[湖南]湖南师范大学[上海]上海师范大学[江苏]南京师范大学[云南]云南大学[广西]广西大学[黑龙江]黑龙江大学[吉林]东北师范大学[浙江]浙江师范大学[陕西]陕西师范大学[新疆]石河子大学[陕西]陕西科技大学[黑龙江]东北林业大学[浙江]杭州师范大学2.应用化学主干学科:化学主要课程:无机化学、分析化学(含仪器分析)、有机化学、物理化学(含结构化学)、化学工程基础及化工制图。
2021年暨南大学710无机化学 考研真题

2021年暨南大学710无机化学考研真题2021年招收攻读硕士学位研究生入学考试试题******************************************************************************************** 招生专业与代码:无机化学、分析化学、有机化学、物理化学、高分子化学与物理考试科目:共页,第页考试科目:共页,第页2. 已知: CuS (s) + H 2 (g) → Cu (s) + H 2S (g)θ∆f m H / kJ mol 1 -53.1 0 0 -20.6m S θ/ J mol -1 K -1 66.5 130.57 33.15 205.7 试求:1)该反应正向自发进行的最低温度;2)该反应在298 K 的标准平衡常数K 。
3. 已知 E (MnO 2/Mn 2+) = 1.229 V ,E (Cl 2/Cl -) = 1.360 V 。
试通过计算判断反应MnO 2 (s) + 4 HCl (aq) → MnCl 2 (aq) + Cl 2 (g) + 2 H 2O (l) 在298 K 时的标准态下能否正向自发进行。
并通过计算说明实验室中为什么能用浓盐酸(c = 12 mol/L )来制取氯气。
四、论述题(8分)请选取你所熟悉的当今无机化学领域的某一研究方向,简要论述该方向的研究内容、最新进展和研究意义。
五、简答题(3小题,共11分)1. 某A 3B 型离子化合物(A 代表阳离子,B 代表阴离子)由四种元素组成,一种为氢,另有两种第二周期元素和一种第三周期元素。
阴、阳离子分别由两种元素构成且均呈正四面体构型。
写出该化合物的化学式。
(4分)2. 铁元素是地壳中含量次高的金属元素(仅次于铝)。
在地球漫长的演化过程中,溶解在海洋中Fe 2+被空气氧化转变成针铁矿FeO(OH)而沉积。
写出该反应配平的离子方程式。
(3分)3. 228Bi Cl -离子中铋原子的配位数为5,每个铋中心采取四方锥几何构型。
《无机及分析化学》(第四版)教材的编写体会

《无机及分析化学》(第四版)教材的编写体会摘要:“无机及分析化学”是为实现课程结构和教学内容整合、优化而由原无机化学和分析化学两大基础课程合并而成的一门基础理论课程。
它又是近化学类专业一门重要的基础课程,是建立相关技术人才整体知识结构、能力结构的重要组成部分。
陈荣三教授主编的《无机及分析化学》是我国最早正式出版的教材,2006年该书的第四版作为普通高等教育“十五”国家级规划教材正式出版。
本文对该书第四版的编写进行了简要介绍。
为适应当前教学改革的形势,编者在修订中遵循“加强基础,趋向前沿,反映现代,注意交叉”的现代课程建设理念,力求与生产实践密切结合。
关键词:无机及分析化学;教材;编写;课程建设;教学对于近化学专业如生命科学、材料、环境、农学、医学及药学等专业的学生而言,学习无机及分析化学课程对他们学习基础知识和专业知识都是不可或缺的。
将无机化学和分析化学两门课程合并为无机及分析化学一门课,经过二十多年的探索和实践已逐渐得到教育界的广泛认可。
由南京大学陈荣三教授主编的《无机及分析化学》是我国最早正式出版的教材,2006年本书的第四版作为普通高等教育“十五”国家级规划教材正式出版。
本文对该教材第四版的编写进行简要介绍,提出一些肤浅的体会和大家交流,以期起到抛砖引玉的作用。
一、《无机及分析化学》教材编写的回顾由陈荣三教授主编、黄孟健教授等人参编的《无机及分析化学》一书,从1975年由南京大学自编讲义,到1978年人民教育出版社作为全国高等学校生物系通用教材正式出版至今已有三十年的历史了,这是1977年恢复高考后国内第一本《无机及分析化学》教材,最初主要供生物系及农医等院校相近专业使用。
它首次将四大滴定融入四大平衡中讲授。
由于生物及相关学科发展的需要,以及全国读者对这本书的厚爱,在教育部有关部门和高等教育出版社的大力支持下,全国许多综合大学和师范院校,如北京大学、南开大学、复旦大学、厦门大学、兰州大学、四川大学、武汉大学、山东大学、暨南大学、西北大学、华东师范大学、南京师范大学、华中师范大学、福建师范大学、河北师范大学等数十所高校任课教师成立了“全国高校‘无机及分析化学’课程建设与教学研讨会”。
暨南大学2018年《812有机化学A》考研专业课真题试卷
2016年招收攻读硕士学位研究生入学考试试题
********************************************************************************************
学科、专业名称:无机化学、分析化学、有机化学、物理化学、高分子化学与物理、应用化
学
研究方向:各个方向
考试科目名称:812有机化学A
考生注意:所有答案必须写在答题纸(卷)上,写在本试题上一律不给分。
一、写出下列化合物的名称(用系统命名法)或结构式(10分)
1、2、
3、4、5、
6、2-乙基吡咯
7、三甲基苄基氯化铵
8、丁二酸酐
9、5-硝基萘磺酸10、苯肼
二、回答下列问题(共23分)
1、用化学方法鉴别下列化合物(共10分)
丁烷、环丙烷、1-丁烯、氯化苄、1-氯丁烷、乙醛、葡萄糖、乙酰乙酸乙酯、丙酮、苯胺、N-甲基苯胺
2、比较顺-1-溴-4-叔丁基环己烷与反-1-溴-4-叔丁基环己烷与NaSCH3发生取代反应的反应速度,并进行合理的简单解释。
(6分)
3、将下面Newman投影式转变为Fischer投影式,并标明R、S构型,然后画出其对映体的Fischer 投影式(7分)
考试科目:812有机化学A 共5 页,第 1 页。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2008暨南大学无机(二)选择题 (选择一个正确答案,每小题2分, 25题共 50分 )1.CO 2晶体升华时,需要克服的作用力主要是……………………………()(A)离子键(B)氢键(C)共价键(D)范德华力2.Fe(CO)5的中心离子采用dsp 3杂化, 试问其的空间构型 ………………( )(A) 正四体形 (B)三角双锥形 (C) 平面四边形 (D) V 形3.N 2分子中存在的共价键为…………………………………………………( )A. 只有σ键B. 只有π键C. 一个σ键和二个π键D. 二个σ键和一个π键4.在[Co(en)(NH 3)4]3+配离子中,中心离子的配位数为……………………( )A. 3B. 4C. 5D. 65.下列反应的平衡常数可以用K p = 1/表示的 …………………………(2H p )(A) H 2(g) + S(g)H 2S(g)(B) H 2(g) + S(s)H 2S(g)(C) H 2(g) + S(s)H 2S(l) (D) H 2(l) + S(s)H 2S(s)6.下列元素属于ds 区元素的是………………………………………………( )A. 4d 105s 1B. 4s 24p 6C. 4s 2D. 3d 14s 27.过量AgCl 溶解在下列各物质中,问哪种溶液中Ag +浓度最小…………( )(A) 100 cm 3水 (B) 1000 cm 3水(C) 100cm 3 0.2mol ·dm -3 KCl 溶液 (D) 1000 cm 3 0.5mol ·dm -3 KNO 3溶液8.在工业上欲除去ZnSO 4溶液中的Fe 3+ 杂质,需加入最合适的试剂是……( )(A) NaOH (B) Na 2CO 3 (C) ZnCO 3 (D) Zn9.H 2O(l , 100℃, 101.3 kPa)H 2O(g, 100℃, 101.3 kPa),设H 2O(g)为理想气−→−体,则由始态到终态体系所吸收的热量Q 为……………………………………( )(A) >ΔH (B) <ΔH (C) =ΔH (D) =ΔU10.Li 、Be 、B 原子失去一个电子,所需要的能量相差不是很大, 但最难失去第二个电子的原子估计是……………………………………………………… ( )(A) Li (B) Be (C) B (D) 都相同11.性质最相似的两种元素是…………………………………………………( )(A) Zr 和Hf (B) Ru 和Rh (C) Mn 和Mg (D) Cu 和Cr12.pH 计上所用的指示电极是………………………………………………( )(A) 饱和甘汞电极 (B) 铂电极(C) 氯化银电极 (D) 玻璃电极13.下列分子和离子中,中心原子的价层电子对几何构型为四面体,且分子(离子)空间构型为角形(V 形)的是……………………………………………………( )(A) (B) SO 2 (C) H 3O + (D) OF 2+4NH 14.CrO 5中Cr 的氧化数为 ………………………………………………… ( )(A) 4 (B) 6 (C) 8 (D) 1015.由下列反应设计的电池不需要惰性电极的是……………………………( )(A) H 2(g) + Cl 2(g) = 2HCl(aq) (B) Ce 4+ + Fe 2+ = Ce 3+ + Fe 3+(C) Zn + Ni 2+ = Zn 2+ + Ni (D) Cu + Br 2 = Cu 2+ + 2Br -16.在FeCl 3与KSCN 的混合液中加入过量NaF ,其现象是…………………( )(A) 产生沉淀 (B) 变为无色 (C) 颜色加深 (D) 无变化17.含有下列离子的溶液,与Na 2S 溶液反应不生成黑色沉淀的一组是……( )(A) Fe 2+,Bi 3+ (B) Cd 2+,Zn 2+ (C) Fe 3+,Cu 2 (D) Mn 2+,Pb 2+18.0.50 mol ·dm -3 HAc 的电离度是(K a = 1.8 ⨯ 10-5)……………………………( )(A) 0.60 % (B) 0.90 % (C) 0.030 % (D) 1.3 %19.已知,(Sn 4+ / Sn 2+) = 0.14 V ,(Fe 3+ / Fe 2+) = 0.77 V ,则不能共存于同 ϕ ϕ一溶液中的一对离子是…………………………………………………………… ()(A) Sn4+,Fe2+(B) Fe3+,Sn2+(C) Fe3+,Fe2+(D) Sn4+,Sn2+20.下列物质的酸性强弱顺序正确的是………………………………………()(A) HF> HI > HCl (B) HF> HCl > HI(C) HI > HF > HCl (D) HI > HCl >HF21.273 K 时, 蒸气压最高的物质是……………………………………………( )(A) 汽油(B) 甘油(C) 冰(D) 食盐22.下列量子数合理的一组是…………………………………………………()(A) n= 1 l = 0 m= 1 (B) n= 1 l = 1 m= 1(C) n= 3 l = 2 m= 1 (D) n= 2 l = 1 m= 223.某中心离子d5在八面体场中处于高自旋,由公式(n为未成μ=+n n()2对电子数)计算的数据应为………………………………………………………()(A) 5.48 (B) 0(C) 5.92 (D) 不能计算24.能生成氮气的方法是……………………………………………………()(A) 将硝酸铵(NH4NO3)加热(B) 将亚硝酸铵(NH4NO2)加热(C) 将氯气与氨混合(D) B和C25.下列各组混合液中,能作为缓冲溶液的是……………………………()(A) 10 cm3 0.2 mol·dm-3 HCl和10 cm3 0.1 mol·dm-3 NaCl(B) 10 cm3 0.2 mol·dm-3 HAc和10 cm3 0.1 mol·dm-3 NaOH(C) 10 cm3 0.2 mol·dm-3 HAc和10 cm3 0.3 mol·dm-3 NaOH(D) 10 cm3 0.2 mol·dm-3 HCl和10 cm3 0.2 mol·dm-3 NaOH二、填空题(1、5题每空2分,其余每空1分,共33分)1. 在Al3+和Cu2+的混合溶液中加入过量的NH3· H2O,生成的沉淀是________。
2.Cr原子(Z=24)基态时电子组态________________________________________,价层上的电子数为_______________, 属于第_____周期第_____族元素。
3. (1) BBr 3熔点-46℃,属________晶体,微粒之间的作用力为_________。
(2) KF 熔点880℃,属________晶体,微粒之间的作用力为________。
(3) Si 熔点1423℃,属________晶体,微粒之间的作用力为_______。
4. N 2 +H 2NH 3 = -46 kJ ·mol -12123m r H ∆气体混合物处于平衡时,N 2生成NH 3的转化率将会发生什么变化? (1) 压缩混合气体_____________; (2) 升温___________________;(3) 引入H 2__________________; (4) 恒压下引入惰性气体_________;(5) 恒容下引入惰性气体____________________。
6. 配平下列方程式:(1).( )Cu +( )HNO 3 —( )Cu (NO 3)2 + ( )NO + ( )H 2O (2).( )P 4 +( )HClO 3 + ( ) H 2O —( )H 3PO 4+ ( )HCl 7. 下列物质,,Ac -中,属于质子酸的是______________,其共轭碱HCO 3-NH 4+是________________。
属于质子碱的是________________,其共轭酸是_________________。
三、问答题 (共4题,共22分 )1.5分,试用分子轨道理论写出N 2的分子轨道结构式,说明是否具有磁性?并计算键级。
2. 5分,试给下配合物命名或写出化学式:(1)[Cu (NH 3)4]SO 4 , (2)[Co (en )3]Cl 3,(3)Li[AlH 4](4)氯化二氯一水三氨合钴(Ⅲ),(5)六氯合铂(Ⅳ)酸钾3. 6分,将Zn+ Cu 2+ = Cu + Zn 2+ 氧化还原反应设计为一个原电池。
试写出电池的负极和正极发生的半反应以及原电池符号的表达式?已知(Zn 2+ / Zn) = -ϕ0.76 V ,(Cu 2+ / Cu) = 0.34 V ,则原电池的电动势和分别是多少? ϕ E m r G ∆4.6分,已知反应FeO(s) + CO(g)Fe(s) + CO2(g)的 = 0.5 (1273K)。
C K 若起始浓度CO =0.05mol ·L -1, CO 2 =0.01mol ·L -1,问:(1) 反应物,生成物的平衡浓度各是多少?(2) 增加FeO 是否对平衡有影响?(简单说明道理)四、计算题 ( 共3题,每题15分,共45分)1. 某化工厂生产中需用银作催化剂,它的制法是将浸透AgNO 3溶液的浮石在一定温度下焙烧,使发生下列反应:AgNO 3(s)Ag(s) + NO 2(g) +O 2(g)−→−21试从理论上估算AgNO 3分解成金属银所需的最低温度。
已知:AgNO 3(s) 的= -123.14 kJ ·mol -1,= 140 J ·mol -1·K -1m f H ∆ m S NO 2(g) 的= 35.15 kJ ·mol -1,= 240.6 J ·mol -1·K -1m f H ∆ m SAg(s) 的= 42.68 J ·K -1·mol -1,O 2(g) 的= 205 J ·mol -1·K -1m S m S 2. 计算AgCl 在6mol ·L -1氨水中的溶解度。
(已知:K 稳[Ag(NH3)2]+=1.6×107,中K sp,AgCl =1.7×10-10)3. 3.25g 固体KCN 溶于水配成500mL 水溶液,试计算该溶液的酸度。
