碳族和硼族元素练习
高三化学专题训练(碳族元素) doc

高三化学专题训练(碳族元素)座号_________姓名____________一、选择题1.1985年,科学家发现了一种新的单质碳系列—碳笼,其中最丰富的是C60。
根据其结构特点,科学家称之为“足球烯”,这是一种分子晶体。
据此推测下列说法中不正确的是()A.金刚石、石墨、足球烯都是碳的同素异形体 B.一定条件下,足球烯可发生加成反应C.石墨、足球烯均可作为高温条件下的润滑材料D.足球烯在苯中的溶解度比在酒精中的溶解度大2.用适量的原料经玻璃熔炉反应后制取的普通玻璃中,含钠9.6%,含钙8.4%,含硅35.1%。
习惯上可用下列哪个化学式来表示该玻璃的组成()A.Na2O·CaO·SiO2 B.2Na·CaO·6SiO2C.Na2O·CaO·6SiO2 D.Na2O·CaO·5SiO23.2MgO·SiO2中的酸根阴离子是()A.SiO32- B.Si2O64- C.SiO44- D.Si2O32-4.将足量CO2气体通入水玻璃中,然后加热蒸干,再在高温下充分燃烧,最后所得的固体物质是()A.Na2SiO3 B.Na2CO3、Na2SiO3 C.Na2CO3、SiO2 D.SiO25.下列说法正确的是(N A表示阿佛加德罗常数)()A. 常温下常压下,3g甲醛气体含有的原子数是0.4N AB. 7.59gCuO被CO完全还原,转移的电子数为0.2N AC. 100mL1mol/L的Na3PO4溶液中含有离子数多于0.4N AD.60gSiO2和12g金刚石中各含有4N A个Si—O键和4N A个C—C键6.2002年12月31日,世界上第一条商业磁悬浮铁路在上海投入运营。
磁悬浮的核心技术是利用超导体的反磁性,以Y2O3、BaCO3和CuO为原料,经研磨烧结可合成一种高温超导物质YBa2Cu3O x。
现欲合成0.5mol此高温超导物质,理论上需取Y2O3、BaCO3和CuO的物质的量(mol)分别是()A.0.50、0.50、0.50 B.0.50、1.0、1.5C.0.25、1.0、1.5 D.1.0、0.25、0.177. 砖瓦是用含铁元素等杂质的粘土隔绝空气烧制而成的。
元素知识点

一、学习要点1一、学习要点1. 氮族、碳族和硼族元素的通性。
2. 碳、硅、硼的基本性质和成键特征。
3. HNO2及其盐的制备和性质,HNO3的结构、制法和性质,硝酸盐的化学性质。
4. CO、CO2、CO32--和乙硼烷的结构。
5. 碳酸、碳酸盐、硅酸、硅酸盐、锡、铅氢氧化物及其盐的性质。
6. 乙硼烷、硼酸、硼砂、氢氧化铝及其盐的性质。
7. 磷的氧化物、含氧酸(正、焦、偏、亚、次)及其盐的化学性质。
8. 砷,锑,铋氧化物及其水合物的性质和递变规律。
二、练习题1.Ag+分别与NaH2PO4和Na2HPO4溶液作用,将生成什么沉淀?2. 为什么单质铝不溶于水,却易溶于浓Na2CO3和NH4Cl溶液中?3.试说明下列现象的原因:(1)有水玻璃的试剂瓶长期敞开瓶口,水玻璃变浑浊。
(2)CO2和SiO2的组成相似,在常温常压下CO2为气体而SiO2为固体。
4.碳和氧的电负性差很大,但CO分子的偶极矩却很小,为什么?5. 配制纯净的SnCl2溶液时,应如何防止它被氧化和水解?6. 硼酸为何具有酸性?是几元酸?通常如何增强它的酸性?7.排列出下列磷的含氧酸酸度由强到弱的顺序:H3PO4、H3PO2、H3PO3、H4P2O78. 说明上述酸各是几元酸?9. 什么是“三中心两电子”键,它与通常的共价键有什么不同?10. 为什么PCl5可以稳定存在,但现在却未制得NCl5?11. 给出下列碳酸盐的热稳定性顺序:⑪BeCO3,MgCO3 , CaCO3 , SrCO3 , BaCO3⑫Na2CO3,NaHCO3,H2CO312. 什么是对角线规则?并说明锂和镁的相似性,铍和铝的相似性。
13. 完成下列化学反应方程式:《无机化学》第十章(碱金属和碱土金属)学习要点和练习题答案二、练习题1. 写出分子式生石膏CaSO4·2H2O 重晶石BaSO4方解石CaCO3天青石SrSO4明钒KAl(SO4)2·12H2O2. 根据碱金属的性质的递变规律,预测钫的下列性质:主要物理性质(密度、硬度、熔点);在空气中燃烧的主要产物;与水反应的情况;FrClO4在水中的溶解性如何?答:1、钫的密度不大,与铯接近;硬度很小,很容易用刀子切割;熔点很低,室温下即可熔化。
高三上学期化学单元测试—— 碳族元素

高三上学期化学单元测试——碳族元素注意事项:1.本试题分为第Ⅰ卷和第Ⅱ卷两部分,第Ⅰ卷为选择题,共48分;第Ⅱ卷为非选择题,共52分。
满分100分,考试时间为90分钟。
2.答第Ⅰ卷前务必将自己的姓名、考号、考试科目涂写在答题卡上。
考试结束,试题和答题卡一并收回。
3.第Ⅰ卷每题选出答案后,都必须用2B铅笔把答题卡上对应题目的答案标号(ABCD)涂黑,如需改动,必须先用橡皮擦干净,再改涂其它答案。
第Ⅰ卷(选择题,共48分)一、选择题(每题只有一个正确选项)1.1985年,科学家发现了一种新的单质碳形成:碳笼,其中最丰富的是C60,根据其结构特点,科学家称之为“足球烯”,它是一种分子晶体,据此推测下列说法中不正确的是()A.金刚石、石墨、足球烯都是碳的同素异形体B.一定条件下,足球烯可发生加成反应C.石墨、足球烯均可作为高温条件下的润滑材料D.足球烯在苯中的溶解度比在酒精中的溶解度大2.下列关于硅和硅的化合物叙述不正确的是()①硅晶体的结构和金刚石相似,都是原子晶体;②硅是地壳中含量最多的元素;③单晶硅是良好的半导体材料;④二氧化硅是制造光导纤维的重要原料;⑤二氧化硅分子是由两个氧原子和一个硅原子组成的;③二氧化硅是酸性氧化物,它不溶于任何酸。
A.①②③B.①⑤⑥C.③④⑤D.②⑤⑥3.生石灰中往往含有CaCO3和SiO2杂质,若检验是否存在这两种杂质,最适宜的试剂是()A.氟化氢B.浓硫酸C.盐酸D.苛性钠4.某氧化物X难溶于水,能熔于熔融态的烧碱,生成易溶于水的化合物Y,将少量Y溶液滴入盐酸中,最终能生成一种白色的胶状沉淀,则X是()A. MgOB. Al2O3C. SiO2D. P2O55.将一定量的二氧化碳通入含有7.4g Ca(OH)2的澄清溶液中,最后得到5.0g白色沉淀,则通入的二氧化碳的物质的量可能是()A. 0.05molB. 0.10molC. 0.15molD. 1.0mol6.10g含杂质的碳酸钙和足量的盐酸反应,产生标况下2.24升CO2,试推断杂质的组成是()A.碳酸镁和二氧化硅B.碳酸镁和碳酸氢钾C.碳酸钾和二氧化硅D.碳酸氢钾和二氧化硅7.石榴石是石榴石族矿物的总称,颜色随成分的不同而变化,其组成可以表示为A3B2(SiO4)3,式中A、B均为金属元素,则A、B对应的化合价依次为()A.+2,+3B.+3,+2C.+2,+2D.+3,+38.石棉在使用不当时,也会污染环境,使吸入石棉纤维者易患肺癌。
高三化学训练题碳族元素训练题(1) 习题精练

质对市爱慕阳光实验学校高三化学训练题碳族元素训练题(1)一.选择题〔包括5小题,每题只有一个正确答案〕1.在玻璃、水泥工业生产中,都需要用的原料是〔〕A. 石灰石B. 纯碱C. 粘土D. 石英2.玻璃的性质是〔〕A. 没有固的熔点B. 能耐骤冷、骤热的变化C. 肯有固的熔点D. 有效弱的导电性3.四种晶体:①干冰②氯化钠③钠④二氧化硅,它们的熔点由低到高的顺序是〔〕A. ④②③①B. ①②③④C. ③①②④D. ①③②④4. 以下表达正确的选项是〔〕A. SiO2溶于水显酸性B. CO2通入硅酸钠溶液中可以得到原硅酸C. SiO2是酸性氧化物,不溶于任何酸D. 硅酸的酸性强于碳酸 5.同温同压下,质量的二氧化硫和二氧化碳相比,以下表达正确的选项是〔〕A. 与过量石灰水都生成同物质的量沉淀B.密度比为16:11C. 体积比为1:1D. 原子个数比为2:3二、选择题〔此题包括15小题,每题有一个或两个选项符合题意〕6.以下能发生的反中,离子方程式正确的选项是( )A. 氢氧化钡溶液跟稀硫酸混合:Ba2++SO42—= BaSO4↓B. 氯化镁溶液中通人二氧化碳:Mg2++CO2十H2O=MgCO3↓+2H+C. 足量氯气通人溴化亚铁溶液中:2Fe2++4Br—+3Cl2= 2Fe3++2Br2+6Cl—D. 碳酸钙和盐酸混合:CaCO3+2H+=Ca2++CO2↑+H2O7.在反SiO2+2C 高温Si+2CO↑中,氧化剂和复原剂的质之比是〔〕A. 2:1B. 5:2C. 1:2D. 1:18.以下物质:①SiO2 ②晶体硅③石④CH4⑤NH4+⑤CHCl3⑦NH3,其中晶体或分子的空间结构均不属于正四面体的是( )A. ①③⑤B. ②④⑥C. ①⑥⑦D. ⑥⑦9.通入以下气体后,溶液不会产生浑浊的是( )A.CaCl2溶液中通入SO2B. 氢硫酸中通入Cl2气C. Na2SiO3溶液中通入CO2D. BaCl2溶液通入CO210.生产水泥的过程中,在熟料里参加适量的石膏,其作用是〔〕A.调节水泥的硬化速率 B.增加水泥的强度C.使水泥变得软些 D.增加水泥的可塑性11. 能证明SO2有漂白性的是〔〕A.将SO2通人酸性KMnO4溶液后紫色稍失B.向显的酚酞溶液中通入SO2后,消失C. 向品红溶液中通入SO2通后,消失D. 将SO2通入溴水后,橙色消失12. 以下说法正确的选项是〔〕A. 将H2S通入CuSO4溶液后,无任何变化B. SO2跟H2O2反生成H2SO4,反中SO2表现出复原性C. 除去SO2中少量SO3,可将混合气通过水D.氨催化氧化制HNO3时,吸收塔的尾气用稀H2SO4处理13. 处于固态物质的四氯化硅,以下四项性质的表达正确的选项是〔〕A. 由分子间力结合,熔点很低B. 电的良导休,熔点在1000C左右C. 由共价键组成的状晶体熔点很高D. 非导电体,但熔融后可以导电14.可以说明常温下SiO2是坚硬固体而CO2是气体的原因是〔〕A. 硅的非金属性比碳弱B.SiO2是原子晶体,CO2是分子晶体C. SiO2里硅与氧结合的化学键和CO2中碳与氧结合的化学键不同D. Si-O键比C=O键能大15以下物质①活性炭②氯气③二氧化硫④漂白粉⑤过氧化钠,都能使品红溶液褪色,但褪色过程不是氧化-复原反的是〔〕A. ①③B. ①④⑤C. ②③D. ③⑤16.一量氯酸钾参加到浓盐酸中发生如下反:KC1O3+6HC1=KCl+3Cl2↑+3H2O,其中被氧化的元素和被复原的元素间质量比为〔〕A. 6:1B. 1:6C. 5:1D.3:217,a、b、c是元素周期表中相邻的三种短周期元素,a、b同周期,b、c同主族,它们的核电荷数按a、b、c顺序增大,其质子总数为28,那么这三种元素是〔〕A. Li、Be、MgB. B、C、SiC. C、N 、PD. O、F、Cl18. 无色透明的酸性溶液中,可以大量共存的离子组是〔〕A. NO3—、SiO32—、Na+B. HCO3—、Cl—、SO42—C. Na+、MnO4—、NO3—D. Al3+、SO42—、Mg2+19,能说明碳酸的酸性比硅酸强的事实是〔〕A . CO2通入Na2SiO3溶液中生成白色状沉淀B. CO2溶于水可生成碳酸而SiO2不溶于水,也不跟水反生成硅酸C. 碳酸易溶于水而硅酸难溶于水、D. SiO2和Na2CO3在高温下反生成Na2SiO3和CO220. 大气中CO2增多,会引起“温室效〞你认为目前大气中的CO2主要来源是〔〕A.植物的呼吸与植物腐败放出CO2B.人口增长呼出CO2气体量增大C.工业上大量燃烧含碳燃料D. 建筑工业的开展使大量碳酸盐分解三. 选择题〔此题包括6小题,每题只有一个正确答案〕2l.以下说法正确的选项是〔〕A.二氧化硅是原子晶体,所以“SiO2〞仅表示晶体中Si原子与O原子的个数比为1:2.而不是分子式B. 石英玻璃的膨胀系数是玻璃的1/18.故不能经受温度的剧变C. 二氧化硅是酸性氧化物是硅酸酸酐,所以二氧化硅与水化合可生成硅酸D. 二氧化硅的熔点比二氧化碳高,原因是:要使二氧化硅熔化或气化必须克服Si-O共价键,而使CO2熔化或气化只克服范德华力就可以了22.以下说法正确的选项是( )①假设证明生石灰中是否混有石英和石灰石,可向混和物中参加足量盐酸,看是否有气体生成和是否有剩余固体存在,此剩余固体可溶于热的浓NaOH溶液②水玻璃是一种矿物,既不能燃烧又不能受腐蚀,在工业上可用作粘剂和耐火材料。
碳族元素练习25题

碳族元素练习25题1、下列碳酸盐中最容易热分解的是()A、CaCO 3B、BaCO 3C、MgCO 3D、SrCO 3正确答案:C解析:离子极化2、下列化合物中最易水解的是()A、SiCl 4B、CCl 4C、CF 4D、SiF 62-正确答案:A解析:非金属化合物的水解机理解释3、在下列氧化物中,氧化性最强的是()A、CO 2B、PbO 2C、GeO 2D、SnO 2正确答案:B解析:惰性电子对效应4、下列各组化合物热稳定性关系正确的是()A、Na 2CO 3>Na 2SO 4B、K 2CO 3>Ag 2CO 3C、NaHCO 3>Na 2CO 3D、(NH 4)2CO 3>ZnCO 3正确答案:B解析:离子极化5、下列分子中偶极矩为零的是()A、SO 2B、CS 2C、PBr 3D、SF 4正确答案:B解析:通过预测分子的空间结构,判断是否非极性分子6、下列盐中热稳定性顺序正确的是()A、NaHCO 3<Na 2CO 3<BaCO 3B、Na 2CO 3<NaHCO 3<BaCO 3C、BaCO 3<NaHCO 3<Na 2CO 3D、NaHCO 3<BaCO 3<Na 2CO 3正确答案:D解析:离子极化7、ⅣA 族元素从Ge 到Pb,下列性质依次增大的是()A、+2氧化态的稳定性B、二氧化物的酸性C、单质的熔点D、氢化物的稳定性正确答案:A8、下列硫化物中能溶于Na 2S 溶液中的是()A、SnSB、SnS 2C、PbSD、Bi 2S 3正确答案:B9、下列各组中正确表示了两对物质还原性强弱的是()A、Cu +<CuCl;Pb 2+<Sn 2+B、Cu +>CuCl;Pb 2+<Sn 2+C、Cu +<CuCl;Pb 2+>Sn 2+D、Cu +>CuCl;Pb 2+>Sn 2+正确答案:B解析:CuCl 是难容盐,Cu+的浓度低,据nest 方程,Cu2+/CuCl 的E>Cu2+/Cu+的E 10、下列各组物质的性质递变顺序正确的是()A、FeCl 2<FeCl 3(熔点)B、Pb(Ⅱ)>Pb(Ⅳ)(稳定性)C、Si<P 4(硬度)D、Na>Al(密度)正确答案:B解析:A 错误:Fe3+离子极化强11、在下述溶解度大小的关系中,不正确的是()A、AgF>AgClB、Ca(H 2PO 4)2>CaHPO 4C、NaHCO 3>Na 2CO 3D、Ba(OH)2>Mg(OH)2正确答案:C12、配制SnCl 2溶液时,必须加入()A、足量的水B、盐酸C、碱D、Cl 2正确答案:B解析:防止Sn2+水解13、不能用H 2S(在0.3mol·L -1HCl 溶液中)分离的离子对是()A、Bi 3+、Pb2+B、Zn 2+、Cu2+C、Ni 2+、Cd 2+D、Ni 2+、Cu 2+正确答案:A解析:硫化物的溶解性14、铅易溶于稀的()A、醋酸B、硫酸C、盐酸D、磷酸正确答案:A解析:在B、C、D 中生成沉淀15、在下列物质中,水解度最大的是()A、FeCl 3B、FeCl 2C、BeCl 2D、BCl 3正确答案:D16、在下列盐中,能与碳酸钠溶液作用,生成沉淀,而且沉淀又能溶于氢氧化钠溶液的是()A、AgNO 3B、FeCl 2C、AlCl 3D、Ba(NO 3)2正确答案:C17、下列碳酸盐的热稳定性顺序正确的是()A、CaCO 3>K 2CO 3>ZnCO 3>(NH 4)2CO 3B、ZnCO 3>K 2CO 3>CaCO 3>(NH 4)2CO 3C、K 2CO 3>CaCO 3>ZnCO 3>(NH 4)2CO 3D、CaCO 3>K 2CO 3>(NH 4)2CO 3>ZnCO 3正确答案:C18、碳最多能与四个氟原子形成CF 4,而硅却能与六个氟原子形成SiF 62-,对于这点不同合理的解释是()A、硅的电离能比碳小B、硅的化学活泼性比碳强C、硅原子具有空的外层d 轨道,而碳原子没有D、化合前碳原子的d 轨道是充满的,而硅原子的d 轨道是空的正确答案:C19、SiCl 4在潮湿空气中冒“白烟”,这是因为()A、SiCl 4不稳定而分解为Cl 2和SiB、SiCl 4发生水解,生成SiO 2和HCl 气体C、SiCl 4发生水解,生成H 4SiO 4和HCl 气体D、SiCl 4化学活性很大,被O 2氧化为SiO 2和Cl 2O正确答案:C20、分子筛是一类多孔性的()A、碱金属硅酸盐B、碱金属铝酸盐C、铝硅酸盐D、硅烷衍生物正确答案:C21、下列气体中能用氯化钯(PdCl 2)稀溶液检验的是()A、O 3B、CO 2C、COD、N 2正确答案:C22、常温下不能稳定存在的是()A、GaCl 4-B、SnCl 4C、PbCl 4D、GeCl 4正确答案:C解析:惰性电子对效应23、下列物质中,酸性最强的是()A、H 2SnO 3B、Ge(OH)4C、Sn(OH)2D、Ge(OH)2正确答案:B24、下列化学式中代表金刚砂的是()A、Al 2O 3B、CaC 2C、SiO 2D、SiC正确答案:D25、某黄色固体化合物,不溶于热水,溶于热的稀盐酸,生成一橙色溶液,当所得溶液冷却时,有一白色沉淀析出,加热该溶液后白色沉淀又消失。
7.24-碳族元素练习

碳族元素复习-练习题一、单项选择题1.根据统计数字表明,全球气候逐年变暖,其后果是气候异常,生态平衡被破坏,海平面升高。
造成这种变化的“罪魁”是 ( )A .SO 2B .CO 2C .COD .Cl 22.除去SiO 2中混有的石灰石和生石灰,下列试剂中最适宜的是( )A .盐酸B .NaOH 溶液C .水玻璃D .浓硫酸3.下列各溶液中分别通入过量CO 2气体后,仍产生沉淀的是( )A .水玻璃溶液B .石灰水C .CaCl 2溶液D .漂白粉溶液4.光纤通信70年代后期发展起来的一种新型通信技术,目前长距离光纤通信系统已投入使用,光纤通信的光学纤维是由下列哪种物质经特殊工艺制成的….…………( )A .碳 B. 石英 C. 锗 D. 硅5.能证明硅酸的酸性弱于碳酸酸性的实验事实是……………………………….…( )A. CO 2溶于水形成碳酸,SiO 2难溶于水B. CO 2通入可溶性硅酸盐中析出硅酸沉淀C. 高温下SiO 2与碳酸盐反应生成CO 2D. 氯化氢通入可溶性碳酸盐溶液中放出气体,通入可溶性硅酸盐溶液中生成沉淀6.下列试剂能贮存在磨口玻璃塞的试剂瓶里的是……………….…………….…( )A. HF 溶液B. KOH 溶液C. 盐酸D. 水玻璃7.碳酸氢钠受热容易分解为碳酸钠。
现加热5.00g 的碳酸钠和碳酸氢钠的混合物,使碳酸 氢钠完全分解,混合物质量减少了0.31g ,则原混合物中碳酸钠的质量为 ..( )A.3.38gB. 4.58gC. 4.16gD. 4.41g8.下列离子方程式的书写正确的是…………..…………………..………….…..( )A .实验室用大理石和稀盐酸制取CO 2:2H + + CO 32- = CO 2↑+ H 2OB .铁和稀硝酸反应:Fe + 2H + = H 2↑+ Fe 2+C .向AlCl 3溶液中加入过量的NaOH 溶液:Al 3+ + 3OH - = Al(OH)3↓D .NaHCO 3溶液与NaOH 溶液反应: OH - + HCO 3- = CO 32- + H 2O9.下列物质的变化,不能通过一步化学反应完成的是 ( )A .CO 2→H 2CO 3B .SiO 2→Na 2SiO 3C .Na 2O 2→Na 2CO 3D .SiO 2→H 2SiO 310.下列各组中的离子,能在溶液中大量共存的是( )A .K +、Mg 2+、NO 3-、Cl -B .Ba 2+、H +、HCO 3-、 Cl -C .Mg 2+、Ba 2+、OH -、HCO 3-D .H +、 K +、 CO 32-、 SO 42-11.标准状况下,将20LCO 2和CO 的混合气体通过足量的Na 2O 2粉未,充分反应后,在相同状况下气体体积减少至16L ,原混合气中CO 的体积是 ( )A. 16LB. 12LC. 8LD. 4L12.等量的小苏打制取CO 2,①煅烧法②与酸作用,两种方法得到CO 2的量哪个多( )A. 无法比较B. 相等C. ①少于②D. ①多于②13. 某无色混合气体可能含有O H CO CO 22、、(水蒸气)、2H 中的一种或几种,依次进行如下处理(假设每次处理均反应完全);① 通过碱石灰,气体体积变小;② 通过赤热的氧化铜时,固体变为红色;③ 通过白色硫酸铜粉末时,粉末变为蓝色;④ 通过澄清石灰水时,溶液变时浑浊。
第12章 氮族碳族和硼族元素 习题参考答案

第12章氮族、碳族和硼族元素习题参考答案1. (1)解:3 + HClNH4Cl NH 3 + NH4HSO4(NH4)2SO4 NH 2O3 + N2 + 4H2O (NH4)2Cr2O7 Cr(2)解:2KNO3 2KNO2 + O2 2Cu(NO3)2 2CuO + 4NO2 + O22AgNO3 2Ag + 2NO2 + O25NO3- + 2Mn2+ + 3H2O2.解:(1) 5NO2-+ 2MnO4- + 6H+2? 3NO2-+ Cr2O7+ 8H+ →3NO3- +2Cr3++7H2O(2) 2NO2- + 2I- + 4H+(3) HNO2+NH33.解:(1) NH4Cl (NH4)2SO4(2)KNO2H2SO4 2NO↑+ I2 + 2H2O N2+ 2H2OBaCl2无现象产生白色沉淀(BaSO4)产生蓝色溶液(N2O3)、红棕色气体(NO2)无现象产生黄色沉淀(As2S3) KNO3(3)AsCl3SbCl3H2S产生橙红色沉淀(Sb2S3)产生黑色沉淀(Bi2S3) BiCl34.解:(1)S +2HNO3(浓) (2)4Zn + 10HNO3(很稀) (3)3CuS + 8HNO3 (4)PCl5+4H2OH2SO4 + 2NO↑4Zn(NO3)2 + NH4NO3 + 3H2O3Cu(NO3)2 + 3S↓ + 2NO↑ + 4H2OH3PO4+ 5HCl(5)2AsO33- + 3H2S + 6H+(6)AsO43- + 2I- + 5H+(8)Sb2S3 + 3S2-5.解:(1)NH4+NaOHH2SO4NH3O2Pt As2S3↓ + 6H2O H3AsO3 + I2 + H2O2MnO4- + 5Bi3+ + 5Na+ + 7H2O(7)2Mn2+ + 5NaBiO3 + 14H+ 2SbS33-NOO2 H2(Fe)纯O2高温高压燃烧N2NH3NO2Cu(浓HOHNO3)2Zn(稀HNO3)HNO3NH3N2OKIHNO2Cu(稀HNO3)NH4NO3H2SO4H2SO4(浓)NaOHO2NaNO2NaNO3H3AsO4H2S(HCl)As2S5Na2SHClNa3AsS4(2)AsCl3H2SNa3AsS3HClNa2SAs2S3H2O浓HClH3AsO3I2(pH=5~9)KI(pH<0.5)(3)Na3SbO3HCl(适量)NaOHSb(OH)3HClNaOH(过量)SbCl3H2SH2OHClNa2SHClSbOCl (4)Cl2(NaOH)NaBiO3Sb2S3Na3SbS3(NaOH)MnSO4 Cl2(HNO3)Bi(OH)3HNO3NaOHBi(NO3)3H2OHNO3BiONO36.解:A是AsCl3,B是AgCl,C是[Ag(NH3)2]Cl,D是As2S3,E是(NH4)3AsS4,F是As2S5,G是H2S。
元素化学 硼族、碳族元素

(2)B、C族元素的成键特征 ) 、 族元素的成键特征
元素 B 成键特征 Al3+ sp CO、CO2 、 sp2
石墨, 石墨,大π
Al
C
Si
离子键
sp2 BF3 共价键
sp2 AlCl3
sp3 SiO2 硅氧四面体, 硅氧四面体, 巨型分子
缺电子特征: 缺电子特征: 桥键 配位键
(作为中心离子) 作为中心离子)
(1)性质 )
大多数硼烷易挥发(但B10H14的熔、沸点都较高 大多数硼烷易挥发( 的熔、 在常温下为固体) , 在常温下为固体); • 所有挥发性硼烷都有毒; 所有挥发性硼烷都有毒 有毒; 稳定性很 • 多氢的硼烷BnHn+6热稳定性很低; 多氢的硼烷B • 少氢的BnHn+4对热较稳定; 少氢的B 对热较稳定; • 几乎所有硼烷都对氧化剂极为敏感; 几乎所有硼烷都对氧化剂极为敏感; • 除B10H14 不溶于水且几乎不与水作用外 , 其他 不溶于水且几乎不与水作用外, 所有硼烷在室温都与水反应而产生硼酸和氢 ; •BnHn2 - 阴离子的化学性质比相应的中性硼烷稳 B 定。
2.B、Al的缺电子性质及对比: 、 的缺电子性质及对比 及对比: • 单质 的多中心键(缺电子之故); 单质B的多中心键 缺电子之故); 的多中心键( • 硼烷中的氢桥键与多中心少电子键; 硼烷中的氢桥键与多中心少电子键; • 硼酸的酸式电离: 硼酸的酸式电离: OH
B(OH)3 +H2O → [HO-B ← OH]- +H+
OH • 卤化硼和卤化铝的特征:为路易斯酸,可以形 卤化硼和卤化铝的特征:为路易斯酸, 成加合物。酸性: 成加合物。酸性:BF3>BCl3>BBr3>BI3(?)
大学无机化学第17章 硼族元素习题解答
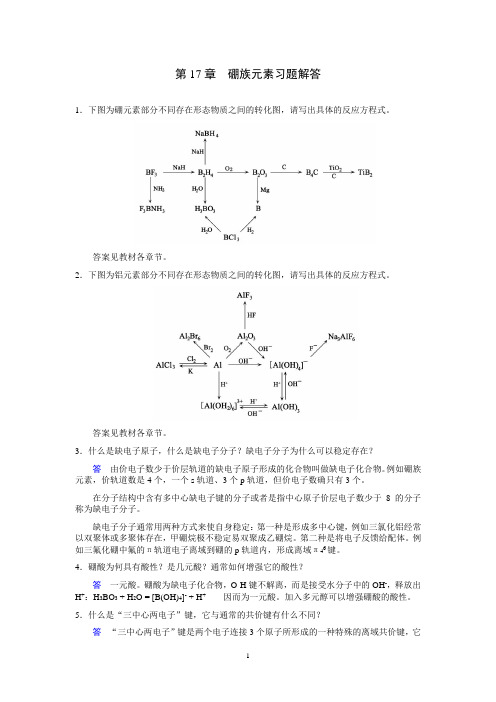
第17章硼族元素习题解答1.下图为硼元素部分不同存在形态物质之间的转化图,请写出具体的反应方程式。
答案见教材各章节。
2.下图为铝元素部分不同存在形态物质之间的转化图,请写出具体的反应方程式。
答案见教材各章节。
3.什么是缺电子原子,什么是缺电子分子?缺电子分子为什么可以稳定存在?答由价电子数少于价层轨道的缺电子原子形成的化合物叫做缺电子化合物。
例如硼族元素,价轨道数是4个,一个s轨道、3个p轨道,但价电子数确只有3个。
在分子结构中含有多中心缺电子键的分子或者是指中心原子价层电子数少于8的分子称为缺电子分子。
缺电子分子通常用两种方式来使自身稳定:第一种是形成多中心键,例如三氯化铝经常以双聚体或多聚体存在,甲硼烷极不稳定易双聚成乙硼烷。
第二种是将电子反馈给配体。
例如三氟化硼中氟的π轨道电子离域到硼的p轨道内,形成离域π46键。
4.硼酸为何具有酸性?是几元酸?通常如何增强它的酸性?答一元酸。
硼酸为缺电子化合物,O-H键不解离,而是接受水分子中的OH-,释放出H+:H3BO3 + H2O = [B(OH)4]- + H+因而为一元酸。
加入多元醇可以增强硼酸的酸性。
5.什么是“三中心两电子”键,它与通常的共价键有什么不同?答“三中心两电子”键是两个电子连接3个原子所形成的一种特殊的离域共价键,它是缺电子原子的一种成键特征。
它与通常的共价键的区别,在于它是一种缺电子的桥键,而一般的共价键是由两个原子共用两个电子所形成的。
6.铝在什么情况下生成致密的钝化膜,其应用如何?钝化膜又在什么情况下容易被破坏?答铝在空气中由于表面会生成致密的氧化膜而阻止进一步的反应,不易受到腐蚀,常被用来制造化学反应器、医疗器械、冷冻装置、石油精炼装置、石油和天然气管道等。
铝但遇到冷的浓硝酸或浓硫酸时,由于在金属表面生成薄而极其致密的氧化物薄膜,而发生钝化。
食盐可腐蚀铝表面的氧化膜,因此铝制器皿不宜长期存放咸的菜品等。
铝置于水中会生成紧密而很难溶解的氢氧化铝层。
高三化学训练题碳族元素训练题(2)习题精练

质对市爱慕阳光实验学校高三化学训练题碳族元素训练题(2)一、选择题〔此题包括五小题,每题只有一个选项符合题意〕1.为除去CO2中混有的少量SO2最好选用〔〕A.水 B.NaOH溶液 C.饱和Na2CO3溶液 D.饱和NaHCO3溶液 2.碳酸只能存在于稀溶液中,这主要因为〔〕A.碳酸是一种挥发性的酸 B.碳酸是一种弱酸C.二氧化碳在水中的溶解度很小 D.碳酸不稳,极易分解3.能证明 SiO2是酸性氧化物的事实是〔〕A.常温下能跟水反生成对的酸——原硅酸B.高温下能跟生石灰反生成硅酸钙C.二氧化硅是非金属氧化物 D.二氧化硅属分子晶体4.在含有 a molCa(OH)2的石灰水中,逐渐通入b molCO2,过程中沉淀逐渐增多,后又消失。
如果CO2充分被吸收,那么最后得到的白色沉淀是 ( ) A . 100〔2a—b〕g B.100〔b—a〕g C.100〔a-b〕g D.100〔2b—a〕g5.要除去CO2中混有的CO、H2S、HCI水蒸气杂质,得到纯洁枯燥的CO2,混合气通过的顺序是〔〕①灼热的氧化铜②NaHCO3溶液③CuSO4溶液④浓 H2SO4A.①②③④ B②④③① C.③②①④ D.②③①④二.选择题【此题包括15小题,每题有一个或2个选项符合题意〕6.最近家研制出一种的分子,它具有空心的类似足球状结构,化学式为C60,以下说法正确的选项是〔〕A.C60是一种型的化合物 B.C60和石墨都是碳的同素异形体C.C60中含有离子键 D.C60的式量是1207.以下说法正确的选项是〔〕A.SiO2是酸性氧化物不跟任何酸反B.水玻璃敞口存放,可能有白色状沉淀析出C.高温时SiO2能跟Na2CO3反放出CO2,所以硅酸的酸性比碳酸强D.SiO2和CO2化学性质虽然相似,但两者的结构完全不同8.在Na2SiO3溶液中,存在的各种离子浓度之间的关系正确的选项是〔〕A.[Na+]=2[SiO32—] B.[Na+]:[SiO]=2:1C.[Na+]>[SiO32—]>[H+]>[OH—] D.[Na+ ]>[SiO32—]>[OH —]>[H+]9.碳化硅〔SiC〕的一种晶体具有类似石的结构,其中碳原子和硅原子的位置是交替的。
全国化学竞赛 碳族元素和硼族元素

碳族元素和硼族元素第1题(共6分) 实验室制备少量硅一般采用镁粉还原SiO2的方法,然后用稀盐酸洗涤产品以除去杂质。
某同学在进行上述操作时,在制得的产品中加HCl洗涤时突然起火。
(1)请用化学方程式解释:①稀盐酸洗涤产品可除去哪些主要杂质?②为什么加HCl洗涤时突然起火?(2)请设计一个实验来验证你的解释。
(不必画出装置图,也不必指出具体化学药品,不要写方程式,只要简明指出方法。
)1.(共6分) (1) ① 2HCl+MgO H2O+MgCl22HCl+Mg H2↑+MgCl2② SiO2+4Mg Mg2Si +2MgOMg2Si+4HCl SiH4+2MgCl2SiH4+2O2SiO2+2H2O(2) 在N2保护下(或惰性气体),对硅烷气体进行检验。
SiH4+2KMnO4H2+K2SiO3+2MnO2↓+ H2O (不要求)(方程式各1分,检验1分)第2题(8分) C60的发现开创了国际科学的一个新领域,除C60分子本身具有诱人的性质外,人们发现它的金属掺杂体系也往往呈现出多种优良性质,所以掺杂C60成为当今的研究热门领域之一。
经测定C60晶体为面心立方结构,晶胞参数a=1420pm。
在C60中掺杂碱金属钾能生成盐,假设掺杂后的K+填充C60分子堆积形成的全部八面体空隙,在晶体中以K+和C60-存在,且C60-可近似看作与C60分子半径相同的球体。
已知C的范德华半径为170pm,K+的离子半径133pm。
11-1 掺杂后晶体的化学式为;晶胞类型为;如果为C60-顶点,那么K+所处的位置是;处于八面体空隙中心的K+到最邻近的C60-中心的距离是pm。
11-2 实验表明C60掺杂K+后的晶胞参数几乎没有发生变化,试给出理由。
11-3 计算预测C60球内可容纳的掺杂原子的半径。
第11题(8分)11-1 KC60面心立方晶胞体心和棱心710pm (各1分,共4分)11-2 C60分子形成面心立方最密堆积,由其晶胞参数可得C60分子的半径:pm aC r 50222142022)(60=== 所以C 60分子堆积形成的八面体空隙可容纳的球半径为:r(容纳)=0.414×r(堆积)=0.414×502=208pm这个半径远大于K +的离子半径133pm ,所以对C 60分子堆积形成的面心立方晶胞参数几乎没有影响(2分)11-3 因r(C 60)=502pm ,所以C 60球心到C 原子中心的距离为:502-170=332 pm所以空腔半径,即C 60球内可容纳原子最大半径为:332-170=162 pm第3题 (共11分)2005年1月美国科学家在Science 上发表论文,宣布发现了Al 的超原子结构,并预言其他金属原子也可能存在类似的结构,这是一项将对化学、物理以及材料领域产生重大影响的发现,引起了科学界的广泛关注。
化学奥赛无机元素化学习题 硼 族 元 素(含答案)

【高中化学奥林匹克竞赛辅导】无机元素化学习题第十一章硼族元素1.下列为有关硼酸的一些反应的图解,试写出其反应方程式,并指出反应条件。
B 2H 6 ?Mg 2B 2O 5·H 2O ?Na 2B 4O 7·10H 2O ?BF 3?H[BF 4] ?H 2SO 4B 2O 3?HBO 2?H 3BO 3?BPO 4 CH2-HO -CB -CH 2-O2.(1)3.B 2H 64.为什么5.6.硼酸H 37.×10-10)8.9.10.11.12.已知-1672(1)(2)若用(3)13.,如何解释?14.为什么不能制得TlI 3和Tl 2S 3?15.虽然TlI 与KI 是同晶型的,但为什么TlI 不溶于水?16.铊的化学性质,在某些方面相似于铝,在一些方面相似于IA 金属,试用化学事实来说明上述叙述。
17.今有K 2SO 4、Pb(NO 3)2、SnC12、SbC13、A12(SO 4)3和Bi(NO 3)3等六瓶溶液,如何用最方便的化学方法来区别它们?写出现象及有关离于方程式。
18.一单质A 难溶于浓硝酸,与NaOH 溶液作用放出气体B ,得到溶液C ,C 用盐酸酸化后得到白色沉淀D ,D 溶于过量的盐酸,若将A 与盐酸反应也能放出气体B ,同时生成溶液E ,用NaOH 将E 小心碱化,也能得到沉淀D ,D 溶于过量的NaOH ,如果在E 中加入Na 2CO 3或(NH 4)2S 也能得到沉淀D ,问A ?E 各是何物?写出有关反应式。
19.已知气态化合物(HNBCl)3(环状)的?H ?f =-1012kJ ?mol -1,气态单原子的B 、Cl 、N 和H 的标准生成焓分别为590kJ ?mol -1,122kJ ?mol -1,472kJ ?mol -1和218kJ ?mol -1,E (B-Cl)=456kJ ?mol -1,E (N-H)=390kJ ?mol -1,试计算此化合物中E (B-N)值。
大连理工大学无机化学教研室《无机化学》(第6版)笔记和课后习题(含考研真题)详解(13-18章)【圣

2.p 区元素特征 (1)各族元素性质自上而下呈规律性变化 同族自上而下:原子半径↑,金属性↑,非金属性↓。 (2)多种氧化值 ns2np1~6 的价电子构型使大部分 p 区元素具有多种氧化值。 (3)电负性大 电负性:p 区元素>s 区元素。 (4)第二周期元素具有反常性 第二周期元素单键键能(N、O、F)<第三周期元素单键键能(P、S、Cl)。 (5)第四周期元素表现出异样性 d 区元素的插入,使第四周期元素的原子半径显著减小,性质展现出特殊性。
圣才电子书
十万种考研考证电子书、题库视频学习平台
第 13 章 p 区元素(一)
13.1 复习笔记
一、p 区元素概述 1.p 区元素 p 区元素:除 H 以外的所有非金属元素和部分金属元素。 惰性电子对效应:同族元素,自上而下,氧化值低的化合物的稳定性高于氧化值高的化 合物的现象。
圣才电子书 十万种考研考证电子书、题库视频学习平台
③加合反应:B2H6+2NH3→[BH2·(NH3)2]++[BH4]- 【注意】①乙硼烷自燃和水解放热较大,可用于制作火箭燃料。②乙硼烷是剧毒物质, 空气中其最高允许含量为 0.1µg/g。 (2)硼的含氧化合物 ①三氧化二硼 B2O3 a.物理性质 颜色:白色固体;密度:2.55g·cm-3;熔点:450C。 b.化学性质 被碱金属还原:B2O3+3Mg→2B+3MgO 与水反应:
B 2 O 3 HH 22OO 2 H B O 2 HH 22OO 2 H 3 B O 3
②硼酸 H3BO3 化学性质:硼酸为一元弱酸(固体酸);与多羟基化合物发生加合反应;受热易分解。 ③硼砂 硼砂:硼酸盐的一种,水解呈碱性;溶液中,n(H3BO3)=n(B(OH)4-),具有缓冲 作用。 (3)硼的卤化物 ①三卤化硼 BX3 BX3 在湿空气中发生水解反应 BX3+3H2O→B(OH)3+3HX ②氟硼酸 H[BF4] H[BF4]的酸性比 HF 强,可利用 BF3 的水解制备,反应方程为
硼族和碳族元素习题

一、选择题1 硼的独特性质表现在: (D)(A) 能生成正氧化态化合物如BN,其它非金属则不能(B) 能生成负氧化态化合物,其它非金属则不能(C) 能生成大分子(D) 在简单的二元化合物中总是缺电子的2 二氧化硅: (A)(A) 与NaOH共熔反应生成硅酸钠(B) 是不溶于水的碱性氧化物(C) 单质是分子晶体,与CO2晶体相似(D) 属AB2型的化合物,晶体结构属CaF2型3 CO与金属形成配合物的能力比N2强的原因是: (D)(A) C原子电负性小易给出孤对电子(B) C原子外层有空d轨道易形成反馈键(C) CO的活化能比N2低(D) 在CO中由于C-←O+配键的形成,使C原子负电荷偏多,加强了CO 与金属的配位能力6 下列无机酸中能溶解酸性氧化物SiO2的是: (C)(A) HCl (B) H2SO4(浓) (C) HF (D) HNO3(浓)7 下列元素性质最相似的是: (A)(A) B和Al (B) B和Si (C) B和Mg (D) B和C二、简答题:1 为什么SiCl4水解而CCl4不水解?要点:SiCl4具有空的3d轨道可接受H2O:中的孤电子对而水解,CCl4无空的价轨道不能接受H2O:中的孤电子对,因此不能水解.2 为什么说H3BO3是一个一元弱酸?要点:H3BO3是一个一元弱酸,它的酸性是由于B的缺电子性而加合了来自H2O中氧原子上的孤电子对成配键,而释放出H+,使溶液的[H+]大于[OH-]的结果:B(OH)3 + H2O ←→B(OH)4- + H+3、等电子原理是什么?与CO互为等电子体的有哪些?与CO2互为等电子体的有哪些?要点:核外电子总数相等的分子或离子; N2, NO+; NO2+ ,N2O,N3-三、推断题14mg某黑色固体A,与浓NaOH共热时产生无色气体B 22.4ml(标况下)。
A燃烧的产物为白色固体C,C与氢氟酸反应时,能产生一无色气体D,D通入水中时产生白色沉淀E及溶液F。
第12章氮族,碳族和硼族习题解

第12章氮族,碳族和硼族习题解第12章氮族,碳族和硼族思考题解析1.NH4NO3,(NH4)2Cr2O7属于具有氧化性酸的铵盐,它们的分解产物是氮⽓或氮的氧化物⽽不是氨;NH4HCO3在常温下即可分解,产物虽有氨⽓,但同时还有CO2。
NH4NO3→NO2↑+2H2O↑或2NH4NO3→2N2↑+O2↑+4H2O↑(NH4)2Cr2O7→N2↑+Cr2O3+4H2O↑NH4HCO3→NH3↑+CO2↑+H2O2.(1) 4NH3(g) + 5O2 (g) → 4NO(g) + 6H2O(g)f G m/(kJmol-1) -16.45 0 86.55 -228.572r G m=[4×(86.55)+6×(-228.572)-4×(-16.45)]kJmol-1=-959.43 kJ?mol-1因?r G m?<0,故该反应在常温下可以⾃发进⾏。
(2)4NH3(g) + 5O2 (g) → 4NO(g) + 6H2O(g)f H m/(kJmol-1) -46.11 0 90.25 -241.818S m?/(J?mol-1?K-1) 192.45 205.138 210.761 188.825r H m=[4×90.25+6×(-241.818)-4×(-46.11)] kJmol-1=-905.47 kJ?mol-1r S m=[(4×210.761+6×188.825)-(4×192.45+5×205.138)] Jmol-1K-1=180.50 J?mol-1?K-1因为?r H m?<0,?r S m?>0,温度升⾼不会使该反应反向进⾏,但温度升⾼可使反应速率加快,所以⽣产上⼀般选择反应温度在800℃左右。
3⾦属与浓稀硝酸反应产物不同,可能是由于存在下列平衡:NO+2HNO33NO2+H2O可以看出:硝酸浓度越⼩,平衡越向左移动,则氮(V)被还原的程度越⼤;也有认为浓硝酸可进⼀步氧化低氧化数的还原产物,所以这与浓稀硝酸的氧化能⼒强弱并不⽭盾。
第16章-硼族元素习题

第16章硼族元素习题1.选择题16-1硼族元素最重要的特征是…………………………………………………( ) (A) 共价性特征 (B) 缺电子性特征(C) 共价性和缺电子性特征 (D) 易形成配合物和自身聚合的特征16-2 硼成键为sp2杂化,且含三个单键, 1 个π46键的化合物是………….. ( )(A) B2O3(B) BF4-(C) BO33-(D) B2H616-3硼的独特性质表现在………………………………………………………( )(A) 能形成正氧化态化合物,如BN ,其它非金属则不能(B) 能生成大分子(C) 能形成负氧化态化合物,其它金属则不能(D) 在简单的二元化合物中总是缺电子的16-4在 菱形硼的B12单元中,表现硼原子是缺电子原子性质的原子个数是( )(A) 3个(B) 6个(C) 9个(D) 12个16-5 下列关于单质硼性质的描述,错误的是………………………………..( )(A) 常温下不活泼,但高温下可与许多非金属反应(B) 与碳相似,炽热的硼可与水蒸气反应(C) 可与盐酸反应 (D) 可与碱反应16-6 硼与浓NaOH反应,所得的含硼产物是………………………………..( )(A) NaBO2(B) Na3BO3(C) B2O3(D) H3BO316-7 硼与浓硝酸反应,所得的含硼产物是…………………………………( )(A) B(NO3)3(B) H3BO3(C) BN (D) B2O316-8 下列对硼酸性质的描述不正确的是…………………………………( )(A) 硼酸是三元酸(B) 硼酸是一元路易斯酸(C) 硼酸与多元醇反应,生成配合物,使酸性增强(D) 硼酸的溶解度小16-9 硼砂的水溶液呈…………………………………………………….( )(A) 碱性(B) 中性(C) 酸性(D) 弱酸性16-10用盐酸滴定硼砂水溶液至恰好中和时,溶液呈……………………( )(A) 中性(B) 弱酸性(C) 弱碱性(D) 强碱性16-11下列关于硼酸结构的叙述错误的是……………………………….( )(A) 硼酸为白色片状晶体,其结构单元为B(OH)3三角形(B) 硼原子通过sp3杂化轨道与氧原子成键(C) 分子间通过氢键形成接近于六角形的对称层状结构(D) 层与层间以范德华力联系16-12在分析化学中,硼砂被用来作标准溶液是因为它………………………( )(A) 易水解(B) 在干燥空气中易风化(C) 溶融态时可溶解金属氧化物(D) 稳定,易提纯16-13 CO2泡末灭火器的反应原理是…………………………………………..( )(A) HCO3-离子的水解(B ) Al3+水解(C) HCO3-Al3+双水解,相互促进(D) 反应生成Al(HCO3)3,然后水解16-14 下列物质中水解并放出H2的是………………………………………()(A) B2H6(B) N2H4(C) NH3 (D) PH316-15 硼的缺电子性表现在……………………………………………………( )(A) 易形成缺电子多中心键及配合物(B) 易形成含桥键的化合物(C) 易形成不同类型杂化,形成化合物(D) 易形成共价化合物16-16 可形成下面几种类型化合物的X元素是………………………………( ) (XH3)2;X2O3;XCl3;XO2-;XF3·HF(A) P (B) Al (C) B (D) S16-17铝在空气中燃烧时,生成……………………………………………….( )(A)单一化合物Al2O3 (B) Al2O3和Al2N3(C)单一化合物Al2N3 (D) Al2O3和AlN16-18下列含氧酸中属于三元酸的是…………………………………………. ( )(A) H3BO3(B) H3PO2(C) H3PO3(D) H3A s O416-19BF3通入过量的Na2CO3溶液,得到的产物是………………………()(A) HF和H3BO3(B) HBF4和B(OH)3(C) NaBF4和NaB(OH)4(D) HF 和B2O316-20 BF3,B2H6,Al2Cl6都是稳定的化合物,BH3,AlCl3则相对不稳定,其原因是……………………………………………………………………….( )(A) 前者形成大π键,后者缺电子(B) 前者通过大π键、多中心键、配位键补偿了缺电子,后者缺电子(C) 前者缺电子,后者有多中心键(D) 前者有配位键,后者缺电子16-21 铊可以生成氟化铊、氯化铊和碘化铊,Tl在这三种化合物中的氧化态是( )(A) 与F 结合为Tl(+III) (B)与Cl 结合为Tl(+III)(C) 与I 结合为Tl(+I)与F,Cl结合为Tl(+III) (D) 全部为Tl(+III)16-22 InCl2为反磁性化合物,其中In 的氧化数为…………………………….()(A) +1 (B) +2 (C) +3 (D) +1和+316-23三氯化铝经常以(AlCl3)2 形式存在。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(A) 三中心二电子键 (C) 二个单电子 键(B) 一个 键(D) 一个 键和一个 键碳族和硼族元素练习、选择题 ( 共 17 题 34 分 )1. (7643)与 Na 2CO 3溶液作用全部都生成碱式盐沉淀的一组离子是⋯ ⋯⋯⋯⋯⋯⋯⋯( )2+ 3+ 2+ 2+ 3+ 2+ 2+ 2+(A) Mg ,Al ,Co ,Zn (B) Fe ,Co ,Ni , Cu2+ 2+ 2+ 2+ 2+ 2+ 2+ 2+(C) Mg2+,Mn2+,Ba2+,Zn2+(D) Mg2+,Mn2+,Co2+,Ni2+2. (7462) 下列说法不正确的是⋯ ⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯ ⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯ ( )(A) SiCl 4在与潮湿的空气接触时会冒“白烟” (B) NF 3因会水解,不能与水接触 (C) SF 6在水中是稳定的 (D) PCl 5不完全水解生成 POCl 33. (3718) 铅蓄电池在充电时,阳极反应是⋯ ⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯( )+2 2(A) PbSO 4 + H 2O = PbO 2 + 4H + SO 42 + 2e(B) Pb + SO 42 = PbSO 4 + 2e+ 2(D) PbO 2 + 4H + SO 24 + 2e = PbSO 4 + 2H 2O4. (0545) 已知在一定温度下SnO 2(s) + 2H 2(g)Sn(s) + 2H 2O(g) K c = 21.0 CO(g) + H 2O(g)CO 2(g) + H 2(g) K c = 0.0340因此下列反应 SnO 2(s) + 2CO(g)Sn(s) + 2CO 2(g) 的 K c 值⋯⋯⋯⋯⋯⋯⋯⋯⋯()(A) 21.0 (B) 0.714 (C) 0.0243 (D) 21.15. (7476) 分离 SnS 和 PbS ,应加的试剂为⋯ ⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯( )(A) 氨水 (B) 硫化钠 (C) 硫酸钠 (D) 多硫化铵4+ 2+6. (7475) 鉴别 Sn 4+和 Sn 2+离子,应加的试剂为⋯ ⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯( ) (A) 盐酸 (B) 硝酸 (C) 硫酸钠 (D) 硫化钠 (过量 )7. (7466)下列分子中, C 与 O 之间键长最短的是⋯ ⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯( ) (A) CO (B) Ni(CO) 4 (C)CO 2(D) CH 3COOH8. (7363) 将过量 SiF 4通入 NaOH 溶液中,主要产物是⋯ ⋯ ⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯()(A) H 4SiO 4, NaF (B) Na 2SiO 3,NaF(C) Na 2SiO 3,Na 2SiF 6(D) SiO 2,HF9. (4370)下列说法不正确的是⋯ ⋯⋯⋯⋯⋯ ⋯⋯⋯⋯⋯⋯⋯ ⋯⋯⋯⋯⋯⋯ ⋯⋯⋯ ( )(B) NaHCO 3 的热稳定性不如 NaCO 3高 (D) 所有碱金属碳酸盐都是易溶于水的210. (4308)CO 32的几构型是⋯(A) 平面三角形(B) 三角锥形 (C) T 形 (D) 直线形11. (1460) 下列硫化物,能溶于 Na 2S 溶液生成硫代酸盐的是⋯ ⋯⋯⋯⋯⋯⋯⋯⋯⋯( ) (A) SnS (B)SnS 2(C) PbS(D) Bi 2S 312. (1456) 试判断 Ge 、Sn 、Pb 分别与浓 HNO 3作用时,正确的说法是⋯ ⋯⋯⋯⋯⋯( ) (A) 三元素都被氧化成 +2 价 (B) 三元素都被氧化成 +4 价(C) Ge 和Sn 被氧化成 +4价,但 Pb 却被氧化成 +2价(D) Ge 被氧化成 +4 价,但 Sn 和Pb 只却被氧化成 +2 价13. (1451) IVA 族元素从 Ge 到 Pb ;下列性质随原子序数的增大而增加的是⋯⋯⋯⋯( )(A) +2 氧化态的稳定性(B) 二氧化物的酸性(C) 单质的熔点 (D) 氢化物的稳定性14. (7354)从分子轨道理论出发,可以认为在 B 2分子中存在的化学键是⋯ ⋯⋯⋯⋯⋯( )2 (C) PbSO 4 + 2e = Pb + SO 24(A) HCO 3 可通过氢键形成双聚离子(C) BeCO 在热水中就可发生分解15. (4403) BF3通入过量的Na 2CO3溶液,得到的产物是⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯( )(A) HF和H3BO3 (B) HBF4和B(OH)3 (C) NaBF4和NaB(OH) 4 (D) HF和B4O316. (4333) 下列含氧酸中属于三元酸的是⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯ ( )(A) H3BO3 (B) H3PO2 (C) H3PO3 (D) H 3AsO417. (1478) 铝在空气中燃烧时,生成⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯⋯( )(A) 单一化合物Al2O3 (B) Al2O3和Al2N3 (C) 单一化合物Al2N3 (D) Al2O3和AlN二、填空题( 共18 题36 分)18. (1509)将适量的SnCl2溶液加入HgCl2溶液中,有 ________ 产_生,其化学反应程式为:19. (7419) HF 腐蚀SiO2玻璃的反应程式为20. (1439) 在Sn(II)的强碱溶液中加入硝酸铋溶液,发生变化的化学程式为:21. (1281) 期表(主族元素)中具有对角线关系的元素是_________________________ ;___22. (7445) 由粗硅经氯化硅制备纯硅的反应程式是23. (7440) K1 2CO3与HCl(aq) ,Na2SiO3与酸反应的化学程式分别是和。
24. (7336)当CO2通入灰水时,根据CO2 和Ca(OH) 2物质的量的比值不同可能生成不同的产物,≤1 时,其产物为,当n CO 2 / n Ca(OH)2 ≥2时,其产物当n CO2 / n Ca(OH) 2为;当 1 < n CO2/ n Ca(OH) 2< 2 时,其产物为。
25. (4455) 完成并配平二氧化铅与硫酸反应的化学程式:氧化剂是________________ ;__氧_ 化产物是__________________ 。
__26. (4408) 将Cl2 通入Pb(II) 的碱性溶液中,这时发生的反应是。
27. (4365) 两种区别开NaHCO 3和Na2CO3的法是:(1) _______________________________________________ ;________(2) _______________________________________________ 。
________28. (1468) C 和O 的电负性相差较大,但CO 分子的偶极矩却很小。
其原因是29. (1455) 用> 或< 号表示下列各对碳酸盐热稳定性的大小。
(1) Na 2CO3 ____ BeCO3 ;(2) NaHCO 3 _____ Na2CO3;3 MgCO 3 ____ BaCO3;(4) PbCO 3 _____ CaCO3。
30. (1450) 由于SnCl2极易 __________ 和_ ___ ,_所以在配制SnCl2水溶液时,必须先将SnCl2 溶于________ 中_,而后还要加入少量________ 。
_31. (1447) 用> 或< 号表示下列化合物中键的离子性大小:(1) PbO __ P bS (2) SnS _____ SnS 2 32. (7325)试指出在 IIIA 和 IVA 族元素中:(1) 金属和非金属元素: ;(2) 在自然界中能以氧化物形式存在的元素: 。
33. (7474)BF 3 与 BCl 3的水解程式分别为 和。
34. (7369)BF 3 的几构型为,而 BF 4 的几构型为 。
中的 B — F 键长比 中的键要短。
35. (1477) H 3BO 3 是极弱的一元酸, 在定量分析中不能直接用强碱滴定, 如果加一定量的 __________________ ,__生_成 ______________________ 后__,__因_ 酸性大为增强, 则就可滴定 了。
三、计算题 ( 共 1 题 5 分 )2+36. (4412)利用金属电极电势,通过计算说明,用 Sn 从Pb 2+ 盐溶液中置换 Pb 的过程,四、问答题 ( 共 20 题 100 分 )37. (1722)有人估计具有 114 个质子和 184 个中子的原子核可以稳定存在。
试估计: (1) 该元素的近似相对原子质量; (2) 该元素的价层电子排布; (3) 它和哪种元素的性质最相似。
38. (1653) 拟出准确鉴别标签不清的二氧化锰、二氧化铅、四氧化三铁三瓶黑色固体试 剂的简要步骤,并写出主要化学程式。
39. (7355)碳与硅为同族元素, SiCl 4和 CCl 4结构相似,且根据:1CCl 4(l) + 2H 2O(l) = CO 2(g) + 4HCl(g) rG m = -377 kJ ·mol 11SiCl 4(l) + 2H 2O(l) = SiO 2(s) + 4HCl(g)r G m = -282 kJ ·mol 1CCl 4(l)的水解比 SiCl 4(l) 的水解在热力学上趋势更大。
然而,在实际上, SiCl 4能激烈水解, 而 CCl 4 不发生水解,试阐明理由。
40. (4465)某元素 A 能直接与 VIIA 族某元素 B 反应生成 A 的最高氧化态化合物, 在此化合物中 B 的含量占 83.5 %,而在与此相应的氧化物中,氧的质量则占 53.3 %, 又它与 B 形 成的此化合物为一无色透明的液体, 沸点为 57.6℃,其蒸气对空气的相对密度约为 5.87 倍。
回答下列问题:(1) 该元素的名称,并指出属于第几期第几族;(2) 该元素与 B 元素所生成的此化合物及此元素氧化物的分子式; (3) A 与 B 的化合物的构型、极性大小。
41. (4418) 除去酒中酸味的一种法是:把在空气中加热过的铅投入酒中,加盖,不久酒 的酸味消失并具有甜味。
(1) 写出有关的反应程式, (2) 请评价这个法。
42. (4413) SnCl 4和 SnCl 2水溶液均为无色,如加以鉴别?说明原理,写出反应式。
43. (4395)有一种白色固体,可能是 SnCl 2、SnO 2、PbCl 2、PbSO 4中的一种,由下列实验判断,该白色固体是什么化合物?写出有关程式。
(1) 加水生成悬浊液; (2) 将该白色固体加入盐酸中溶解后,滴加碘淀粉溶液可以 褪色; (3) 通 H 2S 于白色固体的盐酸溶液中, 得到棕色沉淀, 沉淀与 H 2O 2反应又析出白 色沉淀。
