奥美沙坦酯杂质汇总列表
奥美沙坦酯片的合成工艺研究

作为临床常用的降压药物,奥美沙坦酯片在降压 效果、安全性方面具有明显优势 [1]。随着这种血管紧张 素Ⅱ1 型受体(AT1)拮抗剂效果的证实,奥美沙坦酯 片的合成工艺逐渐引起了人们的广泛关注 [2]。因此, 分析奥美沙坦酯片的合成工艺具有一定的必要性。
(2)合成 2- 丙基咪唑 -4,5- 二腈。取 48 g 原 丁 酸 三 甲 酯、32 g 2,3- 二 氨 基 顺 丁 烯 二 腈,混 于 50 g DMF 溶液中。充分混匀后,将混合溶液加热至 100 ℃,充分反应(反应时长为 10 h)。反应结束时,
作者简介:赵振鑫(1991—),男,山东烟台人,本科,研究实习员,研究方向:生物技术。
Abstract: Objective: To analyze the Synthesis process of olmesartan medoxomil tablets. Method: The olmesartan medoxomil was prepared by treating the raw materials of 2,3-diaminomaleonitrile with de-alcoholization, esterification and Grignard reaction. Results: The refined content of olmesartan medoxomil was 99.7%. Conclusion: The process of dealcoholation, ring closure, hydrolysis, esterification and Grignard reaction is used for the synthesis of olmesartan medoxomil.
抗高血压药奥美沙坦酯合成新路线和相关杂质的研究

抗高血压药奥美沙坦酯合成新路线和相关杂质的研究吴泰志1,刘晓华2,张福利13,谢美华1(1.上海医药工业研究院,上海200437;2.青岛国风药业股份有限公司,山东青岛266510)摘要:目的 研究奥美沙坦酯的新合成方法,并对合成中产生的主要杂质进行结构确证和有效控制。
方法 42(12羟基212甲基乙基)222丙基咪唑252羧酸乙酯水解,环合成4,42二甲基222丙基24,62二氢呋喃并[3,42d ]咪唑262酮,与42[22(22三苯甲基四唑252基)苯基]苄基溴缩合,经分离纯化,皂化成钠盐,与42氯甲基252甲基222氧代21,32二氧杂环戊烯成酯,脱保护基得奥美沙坦酯。
对缩合反应的主要杂质应用X 2ray 单晶衍射谱确证其结构为咪唑位置异构体,并用其合成奥美沙坦酯的咪唑位置异构体。
通过优化反应条件抑制异构体的量,从而保证奥美沙坦酯的质量。
结果 用新路线合成了奥美沙坦酯,总收率60%,纯度大于9910%;成品中异构体含量小于011%。
结论 本文合成路线是奥美沙坦酯的新合成方法,并首次报道奥美沙坦酯的咪唑位置异构体。
关键词:奥美沙坦酯;合成;异构体中图分类号:R916.41 文献标识码:A 文章编号:0513-4870(2006)06-0537-07收稿日期:2005211203.3通讯作者 Tel:86-21-55514600,Fax:86-21-65169893,E 2mail:zhangfl@si p i A novel synthesis of ol m es art an medoxo m il and exam i n ati onof its rel ated i m puriti esWU Tai 2zhi 1,L I U Xiao 2hua 2,ZHANG Fu 2li 13,X I E Mei 2hua1(1.Shanghai Institute of Phar m aceutical Industry,Shanghai 200437,China;2.Q ingdao Gro w ful Phar m aceutical Co .L td .,Q ingdao 266510,China )Abstract:A i m T o devel op a ne w synthetic r oute for ol m esartan medoxom il .M ethods O l m esartanmedoxom il was p repared fr om ethyl 42(12hydr oxy 212methylethyl )222p r opyli m idaz ole 252carboxylate via hydr olysis and lact onizati on t o aff ord 4,42di m ethyl 222p r opyl 24,62dihydr ofur o [3,42d ]21H 2i m idaz ole 262one which was condensed with 22(tri phenyl m ethyl )252[4′2(br omomethylbi phenyl )222yl]tetraz ole,f oll owed by esterificati on with 42chl or o methyl 252methyl 21,32di ox ol 222one,and dep r otecti on .The che m ical structure of the maj or i m purity in condensati on reacti on is the regi o 2is omer in the i m idaz ole moiety,and confir med by single crystal X 2ray diffracti on .The corres ponding regi o 2is omer of ol m esartan medox om il was synthesized fr om the i m purity by si m ilar method .Op ti m izati on of the condensati on conditi ons reduced the i m purity t o a negligible quantity .Results Synthesis of ol m esartan medoxom il by the ne w r oute gave a p r oduct of 60%yield and above 9910%purity .The content of ol m esartan medoxom il regi o 2is omer was effectively contr olled t o less than 011%.Conclusi on A novel synthetic r oute f or ol m esartan medoxom il was devel oped successfully .The ol m esartan medoxom il regi o 2is omer is reported for the first ti m e .Key words:ol m esartan medoxom il;synthesis;regi o 2is omer 奥美沙坦酯(ol m esartan medoxom il,1)是由日本三共(Sankyo )株式会社开发成功的新的Ang II 受体拮抗剂。
气相色谱-质谱联用测定奥美沙坦酯中基因毒性杂质4-氯甲基-5-甲基-1,3-二氧杂环戊烯-2-酮

气相色谱-质谱联用测定奥美沙坦酯中基因毒性杂质4-氯甲基-5-甲基-1,3-二氧杂环戊烯-2-酮刘勇军;熊学武;巢燕芳;杨铁金【摘要】A gas chromatograph-mass spectrometric (GC-MS) method was developed for the determination of 4-(chloromethyl)-5-methyl-1,3-dioxol-2-ketone,which is classified as genotoxic impurity and may present in Olmesartan medoxomil drug substance (API) in trace level.The 4,5-dimethyl-1,3-dioxol-2-one (DMDO)is selected as internal standard.In order to avoid matrix interference,the Olmesartan medoxomil test sample was firstly dissolved in-dichloromethane (DCM) with the aid of 1% formic acid,then n-hexane was added to allow the Olmesartan medoxomil to precipitate completely.The supernatant obtained was injected into the DB-624 column (30m × 0.32mm × 1.8μm),and separated by using helium as carrier gas a t flow rate of 2mL/min and split ratio of 1 ∶ 1 under temperature programming mode.The detection of the DMDO-Cl was performed by mass spectrometry (MS) under Single Ion Monitoring (SIM) Mode.Selective ion monitors were set at m/z 113 for DMDO-Cl and m/z 114 for DMDO.The method was proved to be of good reproducibility,high sensitivity,accuracy and reliability.%通过气相色谱-质谱联用(GC-MS)法,测定奥美沙坦酯原料药中基毒杂质4-氯甲基-5-甲基-1,3-二氧杂环戊烯-2-酮(4-(chloromethyl)-5-methyl-1,3-dioxol-2-one,DMDO-C1).选用4,5-二甲基-1,3-二氧杂环戊烯-2-酮(DMDO)为内标物,奥美沙坦酯原料药经1%甲酸的二氯甲烷溶解后,加入正庚烷使奥美沙坦酯析出.取上述清液,用DB-624色谱柱(30m×0.32mm×1.8 μm)分离,使用氦气为载气,流速2mL/min,分流比1∶1,程序升温模式,进行测定.用电子轰击(EI)质谱,在离子选择(SIM)模式下,监控m/z 113与m/z 114离子进行检测,测定痕量DMDO-C1.研究记过表明,该检查方法具有重现性好、灵敏度高、准确可靠的特点.【期刊名称】《合成材料老化与应用》【年(卷),期】2017(046)003【总页数】5页(P91-95)【关键词】奥美沙坦酯;基因毒性杂质;气质联用;杂质痕量检测【作者】刘勇军;熊学武;巢燕芳;杨铁金【作者单位】齐齐哈尔大学化学与化学工程学院,黑龙江齐齐哈尔161000;东阳光药物研究院,广东东莞443300;东阳光药物研究院,广东东莞443300;东阳光药物研究院,广东东莞443300;齐齐哈尔大学化学与化学工程学院,黑龙江齐齐哈尔161000【正文语种】中文【中图分类】O657奥美沙坦酯(Olmesartan medoxomil)是一种血管紧张素Ⅱ受体拮抗剂类药物[1],主要用于高血压的治疗。
奥美拉唑杂质列表及其合成路线

奥美拉唑原料药杂质列表序号名称结构合成路线及操作1 奥美拉唑杂质I 详见第2页2 奥美拉唑杂质H详见第2页3 奥美拉唑杂质F/G详见第3页4 奥美拉唑杂质E 详见第3页5 奥美拉唑杂质D 详见第4页6 奥美拉唑杂质C 详见第4页7 奥美拉唑杂质B详见第5页8 奥美拉唑杂质A 详见第5页奥美拉唑杂质合成路线及合成操作奥美拉唑杂质I4-methoxy-2-(((6-methoxy-1H-benzo[d]imidazol-2-yl)sulfonyl)methyl)-3,5-dimethylpyridine 1-oxide杂质I合成路线杂质I合成操作:取18g硫醇化合物及18.5g苄氯化合物,加入200ml无水乙醇,加热升温至40~50℃溶解,保温40~50℃条件下加入氢氧化钠水溶液(氢氧化钠质量分数为25%),氢氧化钠溶液加入完毕后,反应5‐6h,反应结束后,加入饮用水200ml,析出大量固体物质,过滤,滤饼使用无水乙醇精制两次,得到目标化合物中间体;取10g中间体,加入无水乙醇溶解,加入3当量过氧化氢;缓慢加热升温至70~80℃,保持70~80℃反应5~6小时,TLC监控,反应结束后,用硫代硫酸钠水溶液淬灭反应,淬灭完成后,加入乙酸乙酯萃取三次,每次100ml,合并有机相,将有机相浓缩至干,加入无水乙醇精制,过滤,滤饼送制备液相进行制备;奥美拉唑杂质H2-(((4-chloro-3,5-dimethylpyridin-2-yl)methyl)sulfinyl)-6- methoxy-1H-benzo[d]imidazole杂质H合成路线:杂质H合成操作:取18g硫醇化合物及20g苄氯化合物,加入200ml无水乙醇,加热升温至40~50℃溶解,保温40~50℃条件下加入氢氧化钠水溶液(氢氧化钠质量分数为25%),氢氧化钠溶液加入完毕后,反应5‐6h,反应结束后,加入饮用水200ml,析出大量固体物质,过滤,滤饼使用无水乙醇精制两次,得到目标化合物中间体;取10g目标化合物中间体加入200ml二氯甲烷,搅拌溶解至‐10~‐15℃;在‐10~‐15℃条件下,缓慢加入20g间氯过氧苯甲酸,TLC监控,保温反应4‐5小时,加入硫代硫酸钠水溶液淬灭,升温至20‐30℃,搅拌10‐12小时,静置分液,取二氯甲烷相浓缩,拌硅胶柱层析分离,收集主成分;将主成分使用乙醇重结晶,得到淡黄色固体物质‐杂质H;奥美拉唑杂质F/奥美拉唑杂质G9-methoxy-1,3-dimethyl-12-thioxobenzo[4',5']imidazo[2',1':2,3]imidazo[1,5-a]pyridin-2(12H)-one AND 8-methoxy-1,3-dimethyl-12-thioxobenzo[4',5']imidazoNNNOSO杂质G杂质F及杂质G 合成路线:杂质F 及杂质G 合成操作:取5g 奥美拉唑于100ml 单口瓶中,加入20ml 浓盐酸,加热升温至50~60℃反应,保温反应1.5~2小时,TLC 监控(取样,调节pH 值至中性后监控),反应结束后,将反应液加入氢氧化钠溶液(氢氧化钠质量分数为25%)中,调节pH 值至中性后,过滤,取滤饼送制备液相进行制备分离;奥美拉唑杂质 E4-methoxy-2-(((5-methoxy-1H-benzo[d]imidazol-2-yl)sulfinyl)methyl)-3,5-dimethylpyridine1-oxide杂质E 合成路线:杂质E 合成操作:取18g 硫醇化合物及18.5g 苄氯化合物,加入200ml 无水乙醇,加热升温至40~50℃溶解,保温40~50℃条件下加入氢氧化钠水溶液(氢氧化钠质量分数为25%),氢氧化钠溶液加入完毕后,反应5‐6h ,反应结束后,加入饮用水200ml ,析出大量固体物质,过滤,滤饼使用无水乙醇精制两次,得到目标化合物中间体杂质C ;取10g 目标化合物中间体加入200ml 四氢呋喃,搅拌溶解至0~10℃;在0~10℃℃条件下,缓慢加入20g 双氧水,TLC 监控,保温反应4‐5小时,加入硫代硫酸钠水溶液淬灭,升温至20‐30℃,搅拌10‐12小时,加入乙酸乙酯萃取三次,每次100ml ,合并有机相,浓缩拌硅胶柱层析分离,收集主成分;将主成分使用乙醇重结晶,得到淡黄色固体杂质E ;奥美拉唑杂质 D6-methoxy-2-(((4-methoxy-3,5-dimethylpyridin-2-yl)methyl)sulfonyl)-1H-benzo[d]imidazole杂质D 合成路线:N HNOSHNClON HNOS NO+NaOHCH 3CH 2OH/H 2ONaClO/THFN HN OS NOO O杂质D杂质C 杂质ACAS 号:84006-10-0CAS 号:88546-55-8杂质D 的合成操作:在反应瓶中加入65.00g 奥美拉唑硫醚,加入200ml 四氢呋喃和19.2g 氢氧化钠水溶液(氢氧化钠质量分数为75%),20~30℃下搅拌至溶清后,再降温至-20~-15℃,加入催化剂七钼酸铵59.3g (0.06mol ),控制温度为-20~-15℃,在60min 内缓慢滴加198.7g 次氯酸钠(有效氯为10%,0.56mol )溶液,滴加完毕后保持温度为-20~-15℃,继续搅拌反应5小时,TLC检测反应完全。
奥美沙坦酯项目简介

奥美沙坦酯一、基本信息1、项目名称:奥美沙坦酯原料药、片剂英文名称:Olmesartan Medoxomil Tablets商品名称:傲坦(上海第一三共制药)化学名称:4-(1-羟基-1-甲基乙基)-2-丙基-1-{4-[2-(四唑-5-基)苯基]苯基}甲基咪唑-5-羧酸(5-甲基-2-氧代-1,3-二氧杂环戊烯-4-基)甲基酯分子式:C29H30N6O6分子量:558.592、剂型:原料药、片剂3、注册分类:化药6+64、规格:20mg、40mg5、适应症:适用于高血压的治疗。
6、用法用量:剂量应个体化。
在血容量正常的患者中作为单一治疗的药物,通常推荐起始剂量为20mg,每日一次。
对进行2周治疗后仍需进一步降低血压的患者,剂量可增至40mg。
剂量大于40mg没显示出更大的降压效果。
当日剂量相同时,每日2次给药与每日1次给药相比没有显示出优越性。
无论进食与否,本品都可以服用。
本品可以与其他利尿剂合用,也可以与其他抗高血压药物联合使用。
7、是否医保:否8、零售价:20mg*7片¥/盒58.80元二、国内外上市申报情况国外上市情况由日本DAIICHI Sankyo公司研发,于2002年5月获得美国FDA批准上市,商品名为Banicar。
2002年8月在德国获批准上市,商品名Olmetec。
三、政策法规行政保护:无新药保护:无专利保护:化合物专利是1991年由日本三共株式会社申请的,专利号为:EP0503785,专利优先国为日本;国内无化合物专利。
四、产品特点:【药理作用】在血管紧张素转化酶(ACE,激酶Ⅱ)的催化下,血管紧张素I(ATⅠ)转化形成血管紧张素Ⅱ(ATⅡ)。
血管紧张素Ⅱ是肾素-血管紧张素系统的主要升压因子,其作用包括收缩血管、促进醛固酮的合成和释放、刺激心脏以及促进肾脏对钠的重吸收。
奥美沙坦酯是一种前体药物,经胃肠道吸收水解为奥美沙坦。
奥美沙坦为选择性血管紧张素Ⅱ1型受体(AT1)拮抗剂,通过选择性阻断血管紧张素Ⅱ与血管平滑肌AT1受体的结合而阻断血管紧张素Ⅱ的收缩血管作用,因此它的作用独立于ATⅡ合成途径之外。
奥美沙坦酯片(傲坦)的说明书

奥美沙坦酯片(傲坦)的说明书为什么中年以上的人群容易得血管病呢?心脏和血管是传输人体能量的纽带,心脏动力足,血液流通的财会,血管通常,才能顺利供血,因此治疗心血管疾病很重要,那么老年人应该如何选择用药呢?现在有一款叫做奥美沙坦酯片(傲坦)的治疗心脑血管疾病的药物在众多药物中效果突出,那么它到底好在哪呢?【药品名称】通用名称:奥美沙坦酯片商品名称:奥美沙坦酯片(傲坦)拼音全码:AoMeiShaTanZhiPian(AoTan)【主要成份】奥美沙坦酯。
化学名:4-(1-羟基-1-甲基乙基)-2-丙基-1-{4-[2-(四唑-5-基)苯基]苯基}甲基咪唑-5-羧酸(5-甲基-2-氧代-1,3-二氧杂环戊烯-4-基)甲基酯。
分子式:C29H30N6O6分子量:558.59【性状】傲坦为白色或类白色片。
【适应症/功能主治】本品适用于高血压的治疗。
【规格型号】20mg*7s【用法用量】剂量应个体化。
在血容量正常的患者中作为单一治疗的药物,通常推荐起始剂量为20mg,每日一次。
对进行2周治疗后仍需进一步降低血压的患者,剂量可增至40mg。
剂量大于40mg没显示出更大的降压效果。
当日剂量相同时,每日2次给药与每日1次给药相比没有显示出优越性。
无论进食与否,傲坦都可以服用。
傲坦可以与其他利尿剂合用,也可以与其他抗高血压药物联合使用。
儿童:还没有在18岁以下人群中进行奥美沙坦药代动力学研究。
老年人:奥美沙坦的最大血浆浓度在年轻成人和老年人(≥65岁)中相似。
在多次用药的老年人中观察到了奥美沙坦的轻度蓄积;平均稳态药时曲线下面积(AUCss)在老年人中要高33%,相应的肾清除率(CLR)则减少30%。
肝功能不全:中度肝功能损害患者的AUC0→∞和最大血药浓度(Cmax)都增高,AUC增加了约60%。
肾功能不全:严重肾功能损害(肌酐清除率小于20ml/分钟)的患者多次给药后的药时曲线下面积(AUC)大约为肾功能正常人的3倍。
非诺贝特全套杂质汇总
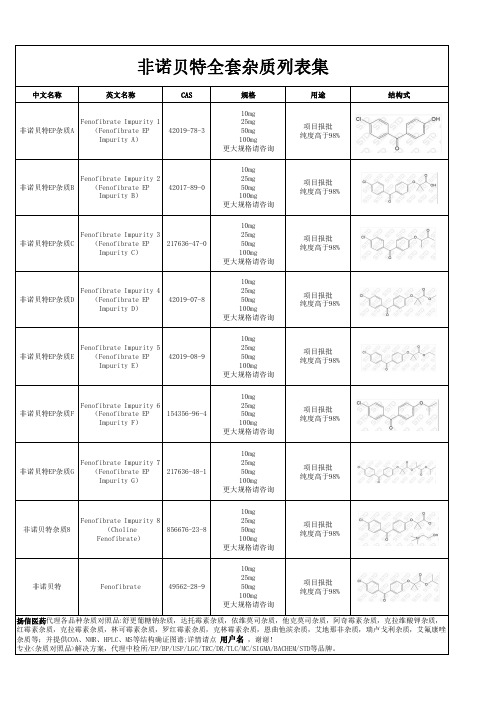
Fenofibrate Impurity 8
非诺贝特杂质8
(Choline
856676-23-8
Fenofibrate)
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
非诺贝特
Fenofibrate
49562-28-9
10mg 25mg 50mg 100mg 更大规格请咨询
非诺贝特EP杂质B (Fenofibrate EP
42017-89-0
Impurity B)
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
Fenofibrate Impurity 3 非诺贝特EP杂质C (Fenofibrate EP 217636-47-0
Impurity C)
项目报批 纯度高于98%
扬信医药代理各品种杂质对照品:舒更葡糖钠杂质,达托霉素杂质,依维莫司杂质,他克莫司杂质,阿奇霉素杂质,克拉维酸钾杂质, 红霉素杂质,克拉霉素杂质,林可霉素杂质,罗红霉素杂质,克林霉素杂质,恩曲他滨杂质,艾地那非杂质,瑞卢戈利杂质,艾氟康唑 杂质等;并提供COA、NMR、HPLC、MS等结构确证图谱;详情请点 用户名 ,谢谢! 专业<杂质对照品>解决方案,代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGMA/BACHEM/STD等品牌。
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
Fenofibrate Impurity 4
非诺贝特EP杂质D (Fenofibrate EP
42019-07-8
Impurity D)
10mg 25mg 50mg 100mg 更大规格请咨询
奥美沙坦酯氨氯地平片 标准

奥美沙坦酯氨氯地平片Aomeishatanzhi Anlüdiping PianOlmesartan Medoxomil and Amlodipine Besylate Tablets本品含奥美沙坦酯(C29H30N6O6)与苯磺酸氨氯地平(以C20H25ClN2O5计)均应为标示量的90.0%~105.0%。
【处方】奥美沙坦酯20g苯磺酸氨氯地平(氨氯地平) 6.944g(5g)制成1000片【性状】本品为薄膜衣片,除去包衣后显白色。
【鉴别】(1)在含量测定项下记录的色谱图中,供试品溶液两个主峰的保留时间应分别与对照品溶液两个主峰的保留时间一致。
(2)取本品1片,置离心管中,加乙腈-水(3︰2)8ml,超声并不时振摇,直至片剂完全崩解。
将该悬浮液离心,取上清液70µl,加乙腈-水(3︰2)10ml。
照紫外-可见分光光度法(中国药典2010年版二部附录ⅣA)在240nm至380nm范围内进行扫描,在256nm(奥美沙坦峰)和360nm(氨氯地平峰)波长处有最大吸收。
【检查】含量均匀度取本品1片,精密称定,置离心管中,加入内标溶液[取四羟基苯甲酸异丁酯0.88g,精密称定,用乙腈-5g/L氯化钠(3︰2)溶解并稀释至1000ml]20ml,超声,不时振摇直至片剂完全崩解,以3500rpm的速度离心该悬浮液10分钟。
精密量取上清液2.0ml,置25ml量瓶中,用流动相稀释至刻度,混匀,作为供试品溶液。
另取苯磺酸氨氯地平对照品35mg,精密称定,置100ml 量瓶中,用乙腈-5g/L氯化钠(3︰2)溶解(超声,不时的振摇),稀释至刻度。
精密量取该液2.0ml,置25ml量瓶中,加内标溶液2.0ml,用流动相稀释至刻度,混匀,作为对照品溶液。
照含量测定项下的方法测定含量,应符合规定(中国药典2010年版二部附录ⅩE)。
有关物质取本品1片,置离心管中,加乙腈-水(3∶2)20ml,超声并不时振摇,直至片剂完全崩解。
奥美沙坦酯(Aomeishatanzhi)原料药生产工艺规程

STP-HCGY-021-00
奥美沙坦酯(Aomeishatanzhi)原 料 药 生 产 工 艺 规 程
6/8
8.2 三废治理 8.2.1 生产中产生的废水进入本厂总废水管道,经处理达标后排放。 8.2.2 生产中产生的药渣,有利用价值的处理后重新利用,其它的经处理 运往垃圾场,废弃包装物应按销毁程序集中销毁。 8.2.3 生产中产生的废气进入废气管道,经处理达标后高空烟囱排放。 9 劳动组织、工时定额、生产周期 9.1 劳动组织 原料药合成车间:加料反应班、脱色过滤干燥班、粉碎筛分总混班、包装班。 9.2 工序工时定额: 计算公式:
按 干 燥 品 计 算 含 C29H30N6O6 不 少 于 98.5%。
7 技术安全及劳动保护 7.1 技术安全 7.1.1 各班组工作岗位严禁吸烟,禁止使用明火。 7.1.2 各种电器下班后须切断电源。 7.1.3 车间内重要岗位须放置灭火器。 7.1.4 操作者必须严格按设备操作规程进行操作,新上岗工人不得单独操作机器,凡接 触滚动设备,必须穿紧袖衣,并不得留长发,也不得用手搅拌物料。 7.1.5 各工序应严格执行岗位责任制,交班制,文明生产制度和清场制度。 7.1.6 真空抽料时应随时观察液面情况,谨防跑料。 7.2 劳动保护 7.2.1 各工序均应配全工作服、鞋、帽、口罩、手套等,特殊岗位的劳保用品要按国家 及吉林省的有关规定配发,并按规定更新。 7.2.2 洁净区生产人员要采取有效的防暑降温措施,以改善工人的劳动条件。 7.3 异常情况的防护措施与注意事项。 7.3.1 人身伤亡的防护措施与注意事项。 7.3.2 设备故障的防护措施与注意事项。 7.3.3 火灾事故的防护措施与注意事项。 7.3.4 其它异常情况的防护措施与注意事项。 8 综合利用与“三废”治理 8.1.综合利用 8.1.1 生产、定额包装所得头子,零头及尾料,按规定处理,可进行再利用 8.1.2 采用蒸馏的方法回收乙醇,经处理转入下批生产使用。 8.1.3 生产余气接至总回气管道,返回锅炉房重新利用,或余热取暖。
奥美沙坦酯杂质A和C的合成

Pharmacy Information 药物资讯, 2016, 5(2), 9-13Published Online May 2016 in Hans. /journal/pi/10.12677/pi.2016.52002Syntheses of Impurity A and C ofOlmesartan MedoxomilWeisi Li, Guoping Chen, Xin Fan, Jingyu TangJiangsu Zhongbang Pharmaceutical Co., Ltd., Nanjing JiangsuReceived: Mar. 30th, 2016; accepted: Apr. 26th, 2016; published: Apr. 29th, 2016Copyright © 2016 by authors and Hans Publishers Inc.This work is licensed under the Creative Commons Attribution International License (CC BY)./licenses/by/4.0/AbstractObjective: A synthetic method towards impurity A and C of olmesartan medoxomil has been pro-vided through optimizing literature reaction conditions. Methods: Impurity A was directly ob-tained by acidic-removal of Trt protecting group of starting material 1 with subsequent recrystal-lization from acetone, whereas impurity C was afforded through dehydration of tertiary alcohol group of starting material 2 followed by acidic-removal of Trt protecting group. Results: Through optimization of literature reaction condition, impurity A and C with chemical purity greater than 95% can be readily obtained. Conclusion: The current method towards impurity A and C is simple and practical with good reproductivity.KeywordsOlmesartan Medoxomil, Impurity A and C, Syntheses奥美沙坦酯杂质A和C的合成李维思,陈国萍,范鑫,唐景玉江苏中邦制药有限公司,江苏南京收稿日期:2016年3月30日;录用日期:2016年4月26日;发布日期:2016年4月29日李维思等摘要目的:优化和改进奥美沙坦酯杂质A和C的合成反应条件,提供了一条简单实用的合成奥美沙坦酯杂质A 和C杂质对照品的路线。
多条溶出曲线评价奥美沙坦酯片的质量

Table 3 Olmesartan medoxomn tablets(20110201 batch) dissolution homogeneity test resuIts
图2
自制样品与参比制剂溶出曲线对比
curve
FigIlre 2 Dissolution
000
研究以及溶出曲线的精确客观绘制,既可初步为 体内生物利用度研究提供参考,也可以揭示各制 剂工艺的差别和内在品质的优劣。本文以国外上
市的制剂为参比制剂,考察自制奥美沙坦酯片在 不同溶出介质中的溶出行为,并采用相似因子法 评价药品的内在质量。
1
mL为溶出
mL,
介质,转速为50 r/min,经30 min,取溶液10
摘要:
以国外上市的奥美沙坦酯片作为参比制剂,考察自研制剂和参比制剂在不同pH溶出
介质中体外溶出行为的相似性。通过测定2种制剂中奥美沙坦酯的溶出曲线,采用f2相似因子对溶 出曲线的相似度进行评价。结果显示,在不同pH的溶出介质中,自研制剂中奥美沙坦酯的溶出曲线 与参比制剂比较,f2相似因子均大于50,自研制剂和参比制剂在不同pH溶出介质中的体外溶出行为 相似。 关键词: 奥美沙坦酯;溶出曲线;相似因子
1
过滤,精密量取续滤液适量,加溶出介质稀释成每
mL中约含奥美沙坦酯10斗g的溶液,按照紫外 一可见分光光度法(中国药典20lo年版二部附录
实验材料与仪器
奥美沙坦酯片参比制剂:批号110010,第一
ⅣA),在258 nm的波长处测定吸光度;另取奥美 沙坦酯对照品约20 mg,精密定量,置100 mL容量 瓶中,加乙腈一水(60:40,体积比)适量,超声使
奥美沙坦酯及其片剂

奥美沙坦酯及其片剂
无
【期刊名称】《中国医药技术与市场》
【年(卷),期】2005(005)004
【摘要】新药3(1)类;薄膜衣层20mg/片,用于高血压。
【总页数】2页(P46-47)
【作者】无
【作者单位】无
【正文语种】中文
【中图分类】R972.4
【相关文献】
1.奥美沙坦酯加氨氯地平与奥美沙坦酯加氢氯噻嗪治疗原发性高血压对比观察 [J], 郭东华;韩清华
2.盐酸安妥沙星片剂与盐酸左氧氟沙星片剂随机、双盲、双模拟治疗急性呼吸道感染的Ⅲ期临床研究 [J], 杨春;袁哲;黄文祥;刘成伟
3.高效液相色谱-紫外分光光度法测定奥美沙坦酯片剂的含量及有关物质 [J], 封宇飞;王志宏;倪明月;孙春华
4.HPLC法同时测定复方片剂中奥美沙坦酯与苯磺酸氨氯地平的含量 [J], 张宁;孙进;
5.二甲双胍普通片剂和缓释片剂治疗社区糖尿病的对比研究 [J], 段文燕;宋爽
因版权原因,仅展示原文概要,查看原文内容请购买。
奥美沙坦酯的研究进展

奥美沙坦酯的研究进展
徐彩丽;袁华;喻宗沅
【期刊名称】《化学与生物工程》
【年(卷),期】2005(022)004
【摘要】奥美沙坦是一种强效和特异性血管紧张素Ⅱ受体拮抗剂,用于治疗高血压,它的前体药物是奥美沙坦酯.介绍了奥美沙坦的药理作用,综述了奥美沙坦酯的合成方法,并对其市场前景作了展望.
【总页数】2页(P7-8)
【作者】徐彩丽;袁华;喻宗沅
【作者单位】湖北省化学研究院,湖北,武汉,430074;湖北省化学研究院,湖北,武汉,430074;湖北省化学研究院,湖北,武汉,430074
【正文语种】中文
【中图分类】R972.4
【相关文献】
1.奥美沙坦酯药理毒理作用研究进展 [J], 樊志萍
2.奥美沙坦酯的临床研究进展 [J], 郭冬华;韩常宝
3.血管紧张素受体拮抗剂——奥美沙坦酯的临床研究进展 [J], 周宇子
4.奥美沙坦酯加氨氯地平与奥美沙坦酯加氢氯噻嗪治疗原发性高血压对比观察 [J], 郭东华;韩清华
5.奥美沙坦酯治疗高血压对血压及Hcy、hs-CRP水平的影响 [J], 张增红;嵇志凤;田培培;孙磊;屈明全
因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
项目报批 纯度高于98%
扬信医药代理各品种杂质对照品:舒更葡糖钠杂质,达托霉素杂质,依维莫司杂质,他克莫司杂质,阿奇霉素杂质,克拉维酸钾杂质, 红霉素杂质,克拉霉素杂质,林可霉素杂质,罗红霉素杂质,克林霉素杂质,恩曲他滨杂质,艾地那非杂质,瑞卢戈利杂质,艾氟康唑 杂质等;并提供COA、NMR、HPLC、MS等结构确证图谱;详情请点 用户名 ,谢谢! 专业<杂质对照品>解决方案,代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGM
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
Olmesartan Impurity 奥美沙坦酯杂质C 3(Olmesartan Medoxomil 879562-26-2
EP Impurity C)
10mg 25mg 50mg 100mg 更大规格请咨询
奥美沙坦酯杂质汇总列表集
中文名称
英文名称
CAS
Olmesartan Impurity 奥美沙坦酯杂质A 1(Olmesartan Medoxomil 144689-24-7
EP Impurity A)
规格
10mg 25mg 50mg 100mg 更大规格请咨询
用途
项目报批 纯度高于98%
结构式
Olmesartan Impurity 2 奥美沙坦酯杂质B (Olmesartan Medoxomil 849206-43-5
项目报批 纯度高于98%
奥美沙坦杂质37 Olmesartan Impurity 37 172875-98-8
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
奥美沙坦杂质43 Olmesartan Impurity 43 138402-33-2
10mg 25mg 50mg 100mg 更大规格请咨询
