有机化学(医学专业)第二章:立体化学
2024版《有机化学》课件立体化学

优化药物分子的立体构型,以提高其与靶标的结合能力和选择性。
药物代谢
考虑药物在体内的代谢过程,避免产生有害的立体异构体。
生物大分子中立体化学问题
蛋白质折叠
蛋白质的空间构象对其功能至关重要,错误的折 叠可能导致疾病。
DNA结构
DNA的双螺旋结构中的碱基对具有特定的空间排 列,影响遗传信息的传递和表达。
周环反应
羰基化合物的反应
如醛酮的亲核加成反应、缩合反应等,涉及 手性传递和立体选择性。
如电环化反应、环加成反应等,探讨其立体 化学过程和产物构型。
02
01
不对称合成
通过手性辅助剂、手性催化剂等实现不对称 合成,获得单一构型产物。
04
03
生物活性物质中立体化学问题
05
探讨
生物活性物质中手性现象及其意义
命名规则及实例解析
命名规则
在立体化学中,化合物的命名需遵循一定的规则,包括确定手性碳原子的构型、指定取代基的位置和编号 等。例如,对于含有手性碳原子的化合物,需在名称中注明其R或S构型。
实例解析
以乳酸为例,其Fischer投影式中,羧基位于上方,羟基位于下方,手性碳原子上的甲基位于右侧。根据 R/S标记法,该化合物为R构型。因此,其系统命名为(R)-2-羟基丙酸。
解析复杂结构
对于复杂分子或难以通过其他手段解析的结构,X射线晶体衍射技术 可以提供精确的结构信息。
核磁共振波谱法在结构鉴定中作用
1 2
确定分子骨架 通过核磁共振波谱法中的一维和二维谱图,可以 解析出分子的骨架结构,包括碳链的长度、支链 的位置等。
识别官能团 核磁共振波谱法可以识别分子中的官能团,如羟 基、羰基、氨基等,从而推断出分子的可能性质。
有机化学基础知识点整理立体化学基础概念

有机化学基础知识点整理立体化学基础概念有机化学基础知识点整理——立体化学基础概念引言:有机化学是研究碳元素化合物的构造、性质和变化的一门学科,而立体化学则是有机化学中重要的基础概念之一。
在有机化学中,分子的立体构型对于反应性、性质和生物活性有着重要影响。
本文将着重整理一些有机化学中的立体化学基础概念,以帮助读者更好地理解有机化学中的立体结构,进而对有机化学进行深入学习。
一、手性与手性中心手性是指分子或物体与其镜像体不可重合的性质。
在有机化学中,手性分子是指拥有手性中心或手性轴的分子。
手性中心是指一个碳原子上连接着四个不同基团的碳原子,它使得分子无法与自身的镜像体重合。
手性分子在光学活性、药物作用和化学性质等方面具有独特的特性。
二、立体异构与构象异构1. 立体异构立体异构是指分子的空间排列方式不同而产生的异构体。
常见的立体异构有以下两种类型:(1) 旋转异构:由于单键的自由旋转,骨架构型可以发生一定程度的旋转,产生旋转异构体。
(2) 互变异构:由于键的旋转受到某些限制,使分子无法通过旋转达到立体异构体之间的互变。
2. 构象异构构象异构是指分子在空间中采取不同的构象,但化学键没有发生断裂或形成新的键。
构象异构分为以下几种类型:(1) 键的旋转构象异构:分子在有某些限制的情况下,通过键的旋转而形成的构象异构。
(2) 环的变形构象异构:分子中含有环系统,通过环的弯曲或平面变形产生的构象异构。
(3) 键的翻转构象异构:分子中存在于键的两个端点之间的三个最佳位置,通过在这三个位置间进行翻转形成的构象异构。
三、立体化学的表示方法1. 常用的立体表示方法(1) 空间结构式:通过笛卡尔坐标系中的三维坐标表示分子的立体构型。
(2) 键切式:通过表示分子和化学键之间关系的切面图形来表示立体构型。
(3) 投影式:通过投影方式来表示立体构型,包括斜投影式、哈维利投影式等。
2. 立体异构体的命名方法(1) IUPAC命名法:使用希腊字母(R和S)来表示手性异构体,其中R表示顺时针方向,S表示逆时针方向。
有机化学02立体化学

CHO H OH CH2OH
OH
H CO2H OH OH CO2H
44
H H OH CO2H
CO2H
H
Fischer 式的特点与应用注意: (1) 不能转动90˚,不能离开平面反转, 只可平移或180˚转动。 (2) 任意两基互换,转变为其对映体。 (3) 任意三基依次轮换,构型不变。
oleic acid
linoleic acid linolenic acid arachidonic acid
11
OH
Vitamin A
12
§2.2 对称性与手性
一、对称性 分子的对称性是由其对称性元素决定的。 1、对称元素 对称面 对称中心 对称轴
13
对称面 m 操作:反映
m
H
H Cl
m
手性分子与其镜像互相对映,但不能完全重叠。
手性是对映异构的必要、充分条件。
27
L-丙氨酸的镜像是 D-丙氨酸,二者不能重叠, 是不同的分子,属于对映异构体。
CO2H H H3C NH2 H H2N
CO2H CH3
L-丙氨酸
D-丙氨酸
28
CO2H H3C H OH H HO
CO2H CH3
29
二、手性因素 手性因素有手性中心、手性轴与手性面。 1、手性中心 常见的是手性碳原子, 也叫不对称碳原子 (asymmetric carbon)。 连接四个不同的原子或基团的碳原子, 是为手性碳原子,常用*Cabcd 标注。
47
5、D/L 指定右旋甘油醛Fischer式中羟基在右侧,规 定为D型, 左旋甘油醛羟基在左侧,为L型。
CHO HO H CH2OH
有机化学课件立体化学ppt课件

基于量子力学原理计算分子的电子结构和性质,可深入揭示有机 物的立体化学本质和反应机理。
人工智能与机器学习
结合大数据和机器学习算法,可加速新有机物的设计和合成,为 立体化学研究提供新的思路和方法。
06
总结与展望:立体化学发展趋势和挑 战
当前存在问题和挑战
01
立体化学合成方法有限
目前立体化学合成方法仍然相对有限,对于复杂分子的合成仍面临较大
05
立体化学分析方法与技术进展
传统分析方法回顾(如:极谱法、色谱法等)
极谱法
利用物质在电解过程中的电极电位与浓度之间的关系进行分析,主要用于无机物和有机物的定性和定量分析。
色谱法
基于物质在固定相和流动相之间的分配平衡,通过流动相的洗脱将不同物质分离,常用于复杂样品的分离和纯化。
现代波谱技术在立体化学中应用(如
立体选择性合成是获得具有特定立体构型药物分子的关键步骤,对于提高药物疗效和降低副 作用具有重要意义。
面临的挑战
立体选择性合成面临着反应条件苛刻、合成步骤繁琐、产物纯度难以控制等挑战。
机遇与发展
随着有机合成化学、计算化学等学科的不断发展,立体选择性合成的方法和技术也在不断改 进和完善,为药物研发提供了更多的机遇和可能性。例如,利用不对称催化、新型手性配体 等策略,可以实现高效、高选择性的立体选择性合成。
对称性与手性判断
对称性判断
通过观察分子是否具有对称轴、对称 面等对称因素来判断。
手性判断
通过判断分子是否具有手性碳原子或其 他不对称因素来判断。具有手性碳原子 的分子一定是手性分子,但手性分子不 一定具有手性碳原子。
立体化学原理ห้องสมุดไป่ตู้应用
立体化学原理
有机化学基础知识点整理立体化学的基本概念与表示方法

有机化学基础知识点整理立体化学的基本概念与表示方法有机化学基础知识点整理——立体化学的基本概念与表示方法立体化学是有机化学中的重要分支,研究有机化合物中分子空间结构和立体异构体的性质与反应规律。
本文将对立体化学的基本概念与表示方法进行整理与介绍。
一、立体化学的基本概念1. 立体异构体:指在化学式相同、分子式相同的情况下,分子结构排列不同而具有不同性质的化合物,称为立体异构体。
立体异构体分为构象异构体和对映异构体两大类。
2. 立体异构体的原因:分子由于碳原子的四个价键都可以自由旋转,导致构象异构体的产生。
对映异构体则由于分子内部存在不对称碳原子或手性中心,使得它们的镜像体不能重合。
3. 立体异构体的性质:立体异构体在物理性质和化学性质上有所区别,例如物理性质如熔点、沸点、密度等差异明显,化学性质如对外界的反应、催化剂的选择等也有较大差异。
二、立体化学的表示方法1. 立体表示法:主要有盘状投影式、锥面式、楔面式和Fischer式等。
a. 盘状投影式:将分子按水平投影在纸面上,使用实线表示平面内的键,棱柱形状表示键在平面之上,圆圈表示键在平面之下。
b. 锥面式:将分子沿轴线向外投影,用三角形表示键在轴线上方,用带状表示键在轴线下方。
c. 楔面式:将分子通过楔形物理模型或立体图形展示,用楔形箭头表示键在垂直于纸面的方向上,用缺口箭头表示键在纸面下方。
d. Fischer式:以垂直于纸面的轴线为支架,将分子垂直展示,左右的羰基或羟基用垂直于轴线的线条表示。
2. 立体描述法:包括立体描述词、R/S命名法、E/Z命名法和Fukui-Liontelli规则等。
a. 立体描述词:用于描述分子中的任意一个手性中心或不对称碳原子的构型,一般为S、R两个字母的组合。
b. R/S命名法:适用于手性中心为单一物种构成的有机分子,根据规定的优先级顺序(按原子序数决定),通过相互对应的方式命名为R(草莓糖)或S(山梨糖)。
c. E/Z命名法:适用于存在双键的有机分子,根据优先级顺序,通过相互对应命名为E(德恩斯烯)或Z(沙通烯)。
有机化学立体化学PPT课件

官能团对分子极性和溶解性的影响
03
官能团的电性和极性会影响分子的极性和溶解性,从而影响分
子在溶液中的行为。
官能团间相互作用和转化规律
官能团间的相互作用
不同官能团之间可能存在相互作用,如共轭效应、诱导效应 等,这些相互作用会影响分子的性质和反应。
官能团的转化规律
在一定条件下,官能团可以发生转化,如醇氧化成醛、醛还 原成醇等,这些转化规律是有机化学中的重要内容。
不对称烷基化反应
通过手性辅剂或催化剂的作用,实现烷基化反应的不对称诱导, 生成具有手性中心的产物。
不对称氧化反应
利用手性氧化剂或催化剂对底物进行不对称氧化,生成具有手性 中心的产物。
立体选择性反应在药物合成中应用
手性药物合成
手性药物具有特定的生理活性和药效,其合成过程中常涉及立体选择性反应。例如,通过 不对称催化氢化合成治疗心血管疾病的L-多巴等手性药物。
异构体间相互转化机理
包括化学键的断裂和形成、原子或基团的迁移等过程。
异构体间相互转化实例
如顺反异构体之间可以通过光照或加热等条件进行相互转 化;对映异构体之间可以通过手性试剂进行拆分或外消旋 化等过程进行相互转化。
05 立体选择性反应 原理及应用
立体选择性反应概念及分类
立体选择性反应定义
指在一定条件下,反应物分子中某一特定立体构型的原子或基团优先发生反应,生成具有特定立体构型的产物的 化学反应。
碳-碳单键旋转自由度受限情况
碳-碳单键 旋转自由度受限,导致有机分子具有特定构象。
环状化合物中碳原子构型判断
环状化合物中碳原子构型判断方法
通过比较环上相邻碳原子的相对构型,可以确定整个环状化合物的立体构型。
环状化合物中碳原子构型与性质关系
有机化学基础知识点整理立体化学的基本概念与应用

有机化学基础知识点整理立体化学的基本概念与应用在有机化学中,立体化学是一个重要的分支领域,它研究的是分子和化合物的三维结构及其对化学性质的影响。
立体化学的概念和应用在有机化学领域具有举足轻重的地位。
本文将对有机化学中的立体化学进行基本概念的整理,并探讨其在化学研究与应用中的重要性。
一、立体化学的基本概念1. 手性:手性是立体化学的一个重要概念,指的是分子或离子的不可重合的镜像异构体。
手性分子无法通过旋转或挪动使其镜像与原分子完全重合,就好像左手和右手无法完全重合一样。
2. 构象异构体:构象异构体指的是同分子式、同结构式但不同空间构型的异构体。
构象异构体的存在是由于分子的键旋转或自由转位所引起的。
典型的构象异构体如反式异构体和顺式异构体等。
3. 立体异构体:立体异构体指的是具有不同立体构型的分子或化合物。
常见的立体异构体有立体异构体、顺反异构体、环异构体等。
立体异构体的存在表明分子或化合物在空间上具有多种不同的构型。
4. 立体中心:立体中心是指一个分子中与不同基团相连的一个原子。
立体中心通常是由于其所连接的基团不对称而导致的。
一个分子可以有一个或多个立体中心。
5. 伪旋光体系:伪旋光体系是一种没有旋光性质的化合物与另一种旋光体系混合而形成的旋光体系。
这种混合体系的旋光性质来源于两个(或多个)异构体存在的旋光性质的合成。
二、立体化学的应用1. 手性药物:手性药物是指那些由手性分子构成的药物。
由于手性药物和其镜像异构体具有不同的生物活性,所以对于手性药物的合成和分离有着重要的意义。
立体化学在药物研发和制备中发挥着重要作用。
2. 光学活性物质:光学活性物质是指那些能够旋转平面偏振光的化合物。
通过立体异构体的性质,光学活性物质可以用于制备偏光镜、偏振片等光学器件,同时也广泛应用于化学分析和手性分离等领域。
3. 反应立体化学:立体化学对于有机反应的研究和理解具有重要意义。
通过研究反应的立体选择性、选择性和环境中对于反应物立体异构体的识别能力,可以更好地设计有机反应和催化剂的设计。
有机化学立体化学课件
(c)和(d)之间是何种关系?
30
将 (d) 在纸平面上旋转180,就和 (c) 完全相同。
CCOOOOHH
COCOOHOH
COOH
HH OOHH HHOO H H
H OH H
HHO OHH
HHO OHH
H OH H
CCOOOOHH
COCOOHOH
COOH
(c)
(d)
象 (c) 这种构型的分子, 虽然有两个手性中心, 但作 为分子整体来说是非手性的。 (c) 称为内消旋化合 物 (meso compound)。
8
问题:下列化合物哪些含手性碳原子?
1. CH3CHCH2CH3
*CH3
2.CH3CHClCH2CH3
**
3. CH3-CH-CH-CH2CH3 OH OH
有对称因素的分
有手性碳就一定有手性吗?
子没有手性
三、对称面和非手性分子
有对称面的分子与它的镜像能重合,因此没有对 映异构现象,称为非手性分子
对称因素
透视式是书写立体结构式常见的方法之一。
应注意它的书写方法,通常实线 “” 代表位 于纸平面上的键;虚线 “ ” (或“ ”) 代表 伸向纸平面后方的键,楔形线 “ ” 代表伸 向纸平面前方的键。
CO2H
CO2H
Cl
Cl
CH HC
I C Br Br C I
H3C OH
HO
CH3
H
H
13
(三) 费歇尔投影式 横前竖后
纯液体为密度 通常还要注明溶剂
比例常数 [α] 称为比旋光度。它是单位长度和单 位浓度下的旋光度。
如:[α]D20 = +98.3o (C, 0.05, CH3OH)
有机化学基础知识点立体化学的基本概念

有机化学基础知识点立体化学的基本概念立体化学是有机化学中非常重要的一个概念,它涉及到分子的空间结构和构象。
在有机化学反应中,分子的立体构型对反应的速率和产物的选择性有着重要的影响。
本文将介绍立体化学的基本概念,包括立体异构、手性分子、构象等知识点。
1. 立体异构立体异构是指化学物质的分子在空间中的排列方式不同,从而导致其化学性质与物理性质的差异。
立体异构可以分为构造异构和空间异构两种类型。
1.1 构造异构构造异构是指分子结构的连接方式不同,分为链式异构、官能团异构和位置异构三种类型。
链式异构:同分子式下,碳骨架的排列方式不同,如正丁烷和异丁烷就是一对链式异构体。
官能团异构:同分子式下,分子中的官能团位置不同,如乙醇和甲醚就是一对官能团异构体。
位置异构:同分子式下,官能团位置相对于主链排列的位置不同,如2-丁醇和3-丁醇就是一对位置异构体。
1.2 空间异构空间异构是指分子在空间中的三维排列方式不同,分为立体异构和对映异构两种类型。
立体异构:分子中存在非自由旋转的键,由于旋转受限,使得分子结构不同,如顺式-反式异构。
对映异构:对称分子具有镜像关系,不能通过旋转重叠,如手性分子。
2. 手性分子手性分子是指与其镜像物不可重叠的化合物,也称为不对称分子。
手性分子通常包含一个或多个手性中心,手性中心是一个碳原子,与四个不同的基团连接。
手性分子的最重要特征是其对映异构体的存在。
对映异构体具有相同的分子式、相同的化学键,但是无法通过旋转或平移重叠。
这种现象称为手性体。
手性分子有很多实际应用,如生物活性物质、药物、拆分光等。
同时,手性分子还涉及到光学活性、旋光度等概念。
3. 构象构象是指分子在空间中的不同取向,由于化学键的旋转、振动等运动而引起的。
构象是立体化学中的重要概念之一,它与立体异构密切相关。
分子的构象由于化学键的自由旋转而产生,通常与键长、键角、键的取代基团等因素有关。
构象的改变可能会导致分子性能的变化。
有机化学第二章立体化学

CH2OH
H
CH2OH
H OHC
CH2OH
CHO
OH
26
第二章 立体化学 费歇尔投影式
严格的Fischer 投影式:
一般将主碳链放在竖直线上,把命名时编号最小的 碳原子放在上端 ( 主链下行) 。
H
CHO
OH
CH2OH
H
OH HOCH2 CHO HO
H OHC
CH2OH
CH2OH
H
√
CHO
OH
费歇尔投影式表示的多个手性碳的直链化合物为 重叠式,并非分子的真实结构。
23
(二) 立体结构式 CO2H
CH
H3C OH
Cl I C Br
H
第二章 立体化学 费歇尔投影式
CO2H
HC
HO
CH3
Cl Br C I
H
24
第二章 立体化学 费歇尔投影式
(三) 费歇尔投影式
CO2 H HO
C
H CH3
书写Fischer投影式的要点:
CO2H HO
H
CH3
(1) 水平线和垂直线交叉点代表手性碳。
手性碳原子(chiral carbon atom)
思考:仔细观察丙酸和乳酸分子,差别在哪里?
丙酸 H
CO2H CH
CH3
CO2H
*C
乳酸 OH
H
CH3
凡是连有4个不同的原子或基团的碳原子称为 手性碳原子,也可称为手性中心(chiral center)。
13
第二章 立体化学 手性分子和对映异构体
问题:下列化合物哪些含手性碳原子?
只含一个手 性碳原子的 分子必定是 手性分子。
有机化学中的立体化学

有机化学中的立体化学有机化学是研究含碳化合物的一门重要学科,其中立体化学是其核心分支之一。
立体化学关注分子在三维空间中的结构及其对物理和化学性质的影响。
理解立体化学的基本原理,对于设计合成新型药物、材料以及其他功能性分子至关重要。
立体异构体从定义上来看,立体异构体是指具有相同的分子式和原子连接方式,但在三维空间中以不同方式排列的化合物。
立体异构体主要分为两类:镜像异构体和几何异构体。
镜像异构体镜像异构体(或称为对映异构体)是指一对结构相同但彼此呈镜像关系的分子。
这类异构体在手性中心存在时形成,手性中心通常是一个连接着四个不同取代基的碳原子。
镜像异构体具有相同的物理性质,但其在生物系统中的活性往往显著不同。
例如,氨基酸是生物中最基本的组成单位,其中L-赖氨酸与D-赖氨酸便是一对重要的手性分子。
虽然它们在分子结构上极为相似,但对生物酶及受体的作用却大相径庭。
这种现象在药物设计中十分重要,因为药物的效果常常依赖于其特定的手性形式。
几何异构体几何异构体是在双键或环结构中由于旋转受限而产生的异构现象。
这类异构体可分为顺式和反式,其中顺式表示相同取代基在双键或环结构同侧,而反式则表示它们位于对侧。
例如,顺-2-丁烯(cis-2-butene)与反-2-丁烯(trans-2-butene)就是一对典型的几何异构体。
在某些情况下,几何异构体还可能展现出截然不同的物理和化学性质,这使得它们在材料科学和药物化学中尤其受到关注。
手性与手性中心手性是立体化学中一个核心概念。
当一个分子的镜像无法与自身重叠时,该分子被称为是手性的。
手性分子的存在一般以手性中心来定义,通常是一个连接着四个不同原子的碳原子。
手性的存在使得药物在对应生物靶点上的活性具有高度选择性。
无论是天然存在还是人工合成,许多生物活性的分子往往具备手性。
例如,部分氨基酸、糖类及许多药理活性的小分子都展现出强烈的手性特征。
在药物开发过程中,科学家需特别关注药物的手性配置,因为不同的对映体可能具有截然不同的药理作用和副作用。
有机化学中的立体化学

有机化学中的立体化学有机化学是研究含碳化合物的化学科学,而立体化学则是有机化学中一个非常重要的分支。
立体化学研究的是有机分子中空间构型的特性,包括手性、立体异构体等。
在有机化学中,立体化学的研究对于理解分子的性质、反应机理以及药物设计等方面都具有重要意义。
本文将介绍有机化学中的立体化学,包括手性、立体异构体、构象等内容。
一、手性手性是立体化学中一个非常重要的概念。
手性分子是指不能与其镜像重合的分子,也就是具有不对称中心的分子。
手性分子的镜像称为对映体,对映体之间是不可重合的。
手性分子的对映体性质有时候会有很大的差异,比如药物的对映体可能会有不同的药效。
因此,研究手性对于药物设计和合成具有重要意义。
手性分子的命名通常使用R和S来表示其立体构型。
R和S的确定是根据卡尔·彼得·克朗的规则来进行的,通过比较不同取代基的优先级来确定手性中心的构型。
手性分子的对映体性质可以通过手性合成来获取纯度较高的对映体。
二、立体异构体立体异构体是指分子结构相同但空间排列不同的异构体。
立体异构体包括构象异构体和对映异构体。
构象异构体是由于键的旋转或双键构型不同而导致的异构体,比如顺反异构体。
对映异构体则是由于分子具有手性中心而导致的异构体,无法通过旋转使其重合。
立体异构体在化学反应中可能会表现出不同的性质,比如活性、稳定性等。
因此,研究立体异构体对于理解反应机理、优化合成路线等具有重要意义。
三、构象构象是有机分子在空间中的特定排列方式。
构象的不同可能会导致分子性质的差异,比如反应活性、稳定性等。
构象的研究对于理解分子的性质和反应机理具有重要意义。
构象的确定通常通过实验方法和计算方法来进行。
实验方法包括X 射线衍射、核磁共振等技术,可以直接观察分子的空间结构。
计算方法则是通过计算机模拟来确定分子的构象,可以预测分子的性质和反应活性。
总结有机化学中的立体化学是一个非常重要的研究领域,涉及手性、立体异构体、构象等多个方面。
有机化学 立体化学PPT课件

对映体是一对相互对映的手性分子,它们都有旋光性, 两者的旋光方向相反,但旋光度(能力)相同.
第15页/共69页
8.2.2 比旋光度
• 由旋光仪测得的旋光度,甚至旋光方向,不仅与物 质结构有关,而且与测定的条件(样品浓度,盛放样 品管的长度,偏正光的波长及测定温度等)有关.
乳酸的分子模型和投影式
菲舍尔投影式:
牢记
两个竖立的键—表示向纸面背后伸去的键;
两个横在两边的键—表示向纸面前方伸出的键.
在纸面上旋转180º—构型不变;旋转90º或270º或翻身—镜象
第21页/共69页
总结: Fischer投影式的转换规则
1. 不能离开纸面翻转。翻转180。,变成其对映体。 2. 在纸面上转动90。, 270 。,变成其对映体。 3. 在纸面上转动180。构型不变。 4. 保持1个基团固定,而把其它三个基团顺时针或
有2重对称轴的分子(C2)
第7页/共69页
σ (2) 对称面(镜面)--
——设想分子中有一平面,它可以把分子分成互 为镜象的两半,这个平面就是对称面.
例:氯乙烷
有对称面的分子
第8页/共69页
(3) 对称中心--i
——设想分子中有一个点,从分子中任何一个原子 出发,向这个点作一直线,再从这个点将直线延长出 去,在与该点前一线段等距离处,可以遇到一个同样 的原子,这个点就是对称中心.
手性分子—既没有对称面,又没有对称中心,也没 有4重交替对称轴的分子,都不能与其镜象叠合,都是 手性分子.
非手性分子—凡具有对称面、对称中心或交替对 称轴的分子.
在有机化学中,绝大多数非手性分子都具有对称面或对称中心,或者同时还具有4重
有机化学中的立体化学基本概念

有机化学中的立体化学基本概念有机化学是研究有机分子结构、性质、变化规律及合成方法的一门化学学科。
而在有机化学中,立体化学是一个非常重要的概念。
立体化学主要研究有机分子或配合物中的不同空间构象以及这些构象对分子性质、反应过程和分子间作用力的影响。
本文将从有机化学中的基本概念入手,详细探讨立体化学在有机化学研究中的重要性。
1. 键的自由旋转和限制在有机分子中,碳碳单键和碳碳双键的自由旋转是一个非常重要的概念。
碳碳单键可以自由旋转,使得分子可以有多种构象。
而碳碳双键的存在将限制了双键两侧的原子或基团的旋转。
这种键的自由旋转和限制影响了分子的空间构象,并直接影响了分子的性质和反应。
2. 手性分子和手性中心在有机化学中,手性分子是指其镜像不能通过旋转重合的分子。
手性分子具有不可重叠的镜像,其镜像之间属于非同一构象。
手性分子中存在手性中心,该手性中心是一个不对称的碳原子,其四个配位基团也不能通过旋转相互重合。
手性中心的存在使得手性分子具有光学活性,可以旋转平面偏振光线的偏振方向。
3. 立体异构体在有机化学中,立体异构体是指分子化学式相同,但空间结构不同的分子。
立体异构体包括构象异构体和对映异构体。
构象异构体是指由键的旋转所引起的不同构象,例如环状化合物的椅式和船式构象。
而对映异构体则是指存在手性中心的分子的镜像构象。
4. 空间构象的确定为了确定分子的空间构象,化学家使用了许多方法和工具,其中最常用的是X射线晶体学、核磁共振和圆二色谱等技术。
这些技术可以帮助科学家确定分子的立体构象,研究分子的性质和反应机理。
5. 立体化学在有机合成中的应用立体化学对于有机合成具有重要的意义。
通过控制合成过程中反应条件和配体的选择,可以合成具有特定立体结构的有机分子。
手性配体在金属有机化学和有机合成领域中有着广泛的应用,它们可以有效地催化不对称合成反应,合成出手性纯度较高的有机产物。
6. 结语在有机化学中,立体化学是一个复杂而重要的领域。
有机化学基础知识点立体化学基础概念

有机化学基础知识点立体化学基础概念有机化学中的立体化学是研究有机分子空间构型和立体化学性质的重要分支。
立体化学关注分子中的空间排列方式,包括分子的手性、立体异构体和立体反应等内容。
本文将介绍有机化学中的一些基础立体化学概念。
1. 手性手性是指分子或物体与其镜像光学异构体不重合的性质。
一个手性分子可以分为左旋体和右旋体两种形式。
在化学中,手性分子的存在对于药物合成和酶催化反应等非常重要。
手性分子的手性来源于其分子结构中的手性中心,即一个碳原子上连接着四个不同取代基团。
2. 立体异构体立体异构体是指分子在空间中构型不同而又无法通过旋转单键使其相互转变的异构体。
立体异构体包括构象异构体和对映异构体两种类型。
2.1 构象异构体构象异构体是由于分子内部化学键的旋转而产生的不同构型的异构体。
构象异构体之间的转换是不需要断裂化学键的,只需要旋转共轭化学键即可。
其中最常见的构象异构体是顺反异构体,即环状化合物中取代基团的位置不同。
2.2 对映异构体对映异构体是指分子在空间中有镜像对称性,但不能通过旋转或挪移使其重合的异构体。
对映异构体分为手性对映异构体和平面对映异构体两种形式。
3. 立体反应立体反应是指在反应中发生分子构型的改变或从一个立体异构体转变为另一个立体异构体的反应。
立体反应可以是顺反异构体之间的互变,也可以是对映异构体之间的互变。
在立体反应中,空间位阻是一个关键的因素。
分子中的取代基团会引起空间位阻,从而影响分子的反应性质和选择性。
例如,在烷基化反应中,取代基团的位置对于反应速率和产物构型具有重要影响。
4. 立体化学表示法为了方便描述分子的立体构型,化学家们提出了多种立体表示法。
常见的立体化学表示法包括:4.1 立体式投影图立体式投影图是将分子在平面上投影成线条的方式,用来表示分子的立体构型。
在立体式投影图中,立体中心用一个交叉表示,取代基团则通过水平或垂直线条连接到立体中心。
4.2 锥式投影图锥式投影图是一种三维表示法,将分子在空间中呈锥形展开。
高等有机化学教案立体化学

立体化学 分子结构
一. 对映异构
(一)分子的对称性 ( ) 对称要素 对称分子 ( ) 非对称分子 不对称分子
(二〕含一个手性中心的分子 ( )
手性中心为碳原子的分子
高等有机化学教案立体化学
手性中心为氮原子的分子 手性中心为其它杂原子的分子
二. 顺反异构 (C高is等-有T机r化a学教n案s立I体s化o学merism)
Part 2: Stereochemistry
原子或原子团在分子中的排列形式
立体化学 与
分子结构
原子在空间的成键形状和顺序
由此引起的物理性质、化学性质 的变化
高等有机化学教案立体化学
分子式相同,原子的成键顺序不同。
分子构造
(三) 含两个(或多个)手性中心的分子 ( ) 赤藓型 苏阿型
非对映异构 体 (Diastereomers) 内消旋体 (meso-) (四〕 环状化合物的对映异构 ( )
(五)不含手性中心的手性分子 ( )
(六) 前手性分子 (Prochiral Molecules) (七 〕不对称合成 (Asymmtric Synthesis)
CH3
C 2H 5 NO Ph
不同取代开链叔胺分子不具有旋光活性:
R
R' N R"
R N R' 两种对映体因快速翻转
R" 相互转化,导致消旋。
手性中心 - 其它杂原子:
CH2Ph S O
H2C CHCH2 P CH3
[α]27D = +92.4°
[α] D = +16.8°
高等有机化学教案立体化学
碳骨架异构 官能团异构 官能团位置异构
有机化学中的立体化学手性分子和立体异构体的概念

有机化学中的立体化学手性分子和立体异构体的概念在有机化学领域,分子的立体化学是一个重要的研究领域。
其中,手性分子和立体异构体是立体化学中的重要概念。
本文将介绍有机化学中的立体化学,以及手性分子和立体异构体的概念。
一、有机化学中的立体化学1. 立体化学的背景立体化学研究的起源可以追溯到19世纪的法尼斯特实验。
通过法尼斯特实验,科学家发现在有机化合物中,存在着多种立体异构体。
这一发现引起了人们对分子结构的兴趣,进一步推动了立体化学的发展。
2. 立体化学的研究对象立体化学主要研究分子的空间构型和空间关系。
研究对象包括分子中的原子、键以及它们之间的排列组合。
3. 立体化学的重要性立体化学的研究对于理解分子的性质和反应机理至关重要。
分子的立体构型会影响其物理性质、化学性质以及与其他分子的相互作用。
因此,研究分子的立体构型有助于预测分子的性质,优化合成方法以及开发新的药物。
二、手性分子的概念手性分子是指不重叠的镜面镶嵌体,也就是说,它们无法通过旋转或平移使其与其镜像重合。
手性分子存在两种形式,一种是左旋性分子(L-型),另一种是右旋性分子(D-型)。
1. 手性分子的特点手性分子具有以下特点:- 不能与其镜像重合- 具有旋光性,即对旋光的天然偏振光产生旋光现象- 在手性催化反应中表现出不对称性2. 手性分子的表示方法手性分子可以通过立体公式进行表示,其中常用的表示方法包括Fisher投影式、锔伦式以及空间轨迹投影式。
三、立体异构体的概念立体异构体是指在化学结构中,分子的立体构型不同而化学式相同的化合物。
在立体异构体中,既包括手性异构体,也包括非手性异构体。
1. 手性异构体手性异构体是指在同一个分子式下,其立体构型与其镜像形式不同。
手性异构体分为两类:对映异构体和非对映异构体。
- 对映异构体:由相同的原子组成,但它们的分子构型与镜像分子构型不完全重合。
对映异构体的名称通常以R和S来表示。
- 非对映异构体:由原子的排列方式不同组成。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
NO2
HO H
H NHCOCHCl2 CH2OH
2
1
H Cl2CHCOHN
OH H CH2OH
1R, 2R- (-)
1S, 2S - (+)
氯霉素 抗菌活性 ( - ) ∶ ( + ) = 100 ∶ 0.4
合霉素 —— 外消旋体 已淘汰
历史教训(1959-1962年 欧洲)
镇静催眠药(沙利度胺 Thalidomide )
两者还有十分重要的不同性质:
对偏振光的作用不同; 生理作用上有着显著的不同
3、判断对映体的方法
1. 最直接的方法是建造一个分子及其镜像的模型。 如果两者能重合,说明分子无手性,没有对映异构现 象;如果两者不能重合,则为手性分子,有对映异构 现象,存在对映体。 2. 考察分子有无对称面。如果分子有对称面,则 该分子与其镜像就能重合,没有对映异构现象。
D-(+)-甘油醛
HgO
COOH H OH CH2OH
L-(-)-甘油醛
COOH H2N H CH3
D-(-)-甘油酸
L-丙氨酸
常用于糖类和氨基酸的构型标记
2. R/S 构型标记法( 1979年被 IUPAC 建议采用) (1) 标记R/S 构型的步骤
按原子序数大小确定与手性碳原子相连的 四个原子或基团的大小顺序。 将手性碳原子的四个原子或基团中最小的
阴离子部位
平面区
阴离子部位 受体
平面区
受体未接触部位
L-(+)-肾上腺素
D-(-)-肾上腺素
血管收缩作用:D型比L型强12~20倍
人体为什么有左旋和右旋(手性)之分?
现代科学从陨石的研究发现,地球的的生命来自太空。
1. 由于星际磁场的原因,使左旋氨基酸的含量占据 了主导地位;
2. 太阳系尘埃和气体在形成之初,某些化学过程导 致了这一现象; 3. 太阳星云辐射的条件下,产生了左旋氨基酸,或 破坏了右旋氨基酸。最初的左旋过量经一种类似 于结晶化的过程而被放大。 ………
2 * 2个C 2 个对映体
n * n个C 2 个对映体
非对映体
HOOC CH CH COOH OH OH
COOH H OH H OH COOH
( Ⅰ)
*
*
2,3-二羟基丁二酸(酒石酸)
COOH H OH HO H COOH
( Ⅳ)
=
COOH HO H HO H COOH
( Ⅲ)
COOH HO H H OH COOH
造成6000多名无头或缺腿缺手的“海豹儿”
还能够显著抑制孕妇的妊娠反应(止 吐等反应),所以叫做反应停。
沙利度胺 Thalidomide
R - (+) —— 有镇静作用,消除孕妇妊娠反应
S - ( - ) —— 对胚胎有很强的致畸作用
(a)
(b)
手性分子与手性生物受体之间的相互作用
(a)一个对映体容易进入手性的受体靶位,发挥 它的生物效应 (b)另一个对映体不能合适地进入相同的受体靶 位 ,因此它没有同样的生物效应
> —CH2CH2CH3 —CH2CH3 > —CH3 > —D > —H >
要点: 按照次序规则排次序,顺时针为R,逆时针为S构型
OH
OH
A
C 2H 5
H
CH3
CH3
H
e D
B
C2H5
R-2-丁醇
S-2-丁醇
想一想 试标记乳酸的构型
COOH H H3 C C OH
COOH C HO H CH3
第二章 立体化学
习题集p30 2. 编号为:
NO2
HO H
H NHCOCHCl2 CH2OH
2 3
1
答案:1R,2R
ChemOffice
如何画化学分子式
球棍模型
填充模型
CHClBrI的立体视图
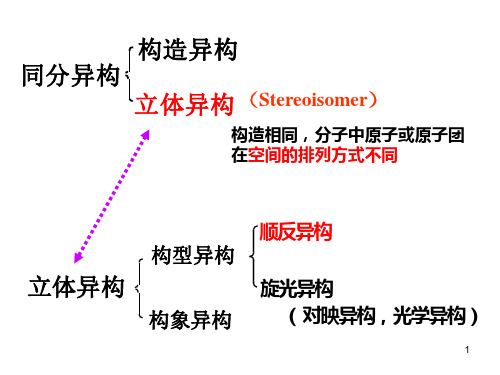
构造异构
(分子中原子间的排 列顺序、结合方式)
碳架异构 位置异构 官能团异构
顺反异构
同分异构 立体异构
C H H
O C H
O C OH
看作
C
N
看作
基团大小的次序:
—I >—Br > —Cl > —SO3H > —SH > —F >—O—C—R > —OR O > —OH > —NO2 > —NR2 > —NHR > —NH2 > —CCl3 > —CO2H > — C —NH2 > —C—H > —CH2OH > —C≡N > O O > —C≡CH > —C(CH3)3 > —CH=CH2 > —CH(CH3)2
(构造相同,原子在 空间排布方式不同)
对映异构 构型异构
构象异构
对映异构又叫光学异构或旋光异构。它 是一类与物质的旋光性质有关的立体异构。
一、手性分子和对映体
二、旋光性
三、费歇尔投影式
四、构型标记法
五、含两个C*的对映异构
六、手性分子的生物作用
手 性 分 子
立 体 化 学 基 础 :
一、手性分子和对映体 1. 基本概念
左手的镜像是右手
右手的镜像是左手
实物
镜象
手性
手性分子
对映异构体(对映体)
左右手互为镜像与实物关系(称 为对映关系),彼此又不能重合 的现象称为手性。
2. 含有一个手性C的对映异构
CH3 CH COOH OH
COOH
*
乳酸
COOH HO
C H
H
C OH
CH3
透视式
CH3
透视式
手性碳原子 C *
手性中心
( Ⅱ)
2R,3S
2S,3R
2R,3R
2S,3S
内消旋体 (立体异构体数< 2n)
想 一 对映体、非对映体、外消旋体、内消旋体、 想 相同化合物
试以酒石酸的立体异构为例说明以下概念:
想一想
用R/S构型命名法指出下面化合物 的构型,并说明其相互关系
(1)
CH3 3 H 2 Br H3C H OH
Br H (2) H3C
t —— 测定时的温度(℃) D —— 钠光波长 589nm α —— 旋光度(°)
l —— 旋光管的长度(dm)
C —— 溶液的浓度(g﹒mL-1)
想一想将胆固醇样品 260mg 溶于5mL 氯仿中, 然后将其装满 5cm 长的旋光管,在室温(20℃) 时通过偏振的钠光,测得旋光度为-2.5°, 计算 胆固醇的比旋光度。 解: [α ]D =
末优基团处在横方向(即左或右)时,用 同样的方法画圆弧,顺时针为S型,反之为R 型。
Cl H
Br
CH3
Br CH3
Cl
H Br
CH3CHCH CH2
R
S
想一想 用Fischer 投影式表示S-3-溴-1-丁烯的结构
CH CH2 Br H CH3
五、含两个手性 的对映异构 4 3 2 C1
CH2 OH
编号小端放上面。
3
乳酸
CH3
* COOH CH
OH
2
1
COOH H3C H C OH
COOH C HO H CH3
(1) Fischer 投影式不能离开纸面翻转,只能在纸 面上旋转180°或其整数倍;若转90°或270°,
COOH CH3 H OH
2. 书写Fischer投影式须注意:
构型发生改变。
1. 旋光度与比旋光度
单一对映体的溶液
尼科尔棱镜
尼科尔棱镜
手性化合物具有旋光性
旋光度α
(+ )右旋(顺时针)
(-)左旋(逆时针)
圆盘旋光仪
自动旋光仪
t
比旋光度 [α ]D =
t —— 比旋光度 [α ]D
α
l ×C
为了使一个化合物的旋 光度成为特征物理常数, 通常用1dm长的旋光管, 待测物质的浓度为 1g/ml , 用 波 长 为 589nm 的 钠 光 (D 线 ) 条 件下,所测得的旋光度, 称为比旋光度。
CH3 OH
手性分子
Br
非手性分子
CHCH3 手性分子
*
二、旋光性
只在一个平面上振动的光称为平面偏振光(planepolarized light),简称偏振光。偏振光的振动平 面习惯称为偏振面。 化合物能使偏振光的偏振面旋转的性能称为旋光 性(optical activity)。手性化合物都具有旋光性。
OH COOH CH3
(3) Fischer 投影式中保持一个基团不变,而把 另外三个基团顺时针或逆时针地调换位置,其 构型不变。
COOH HO H CH3 H COOH OH CH3
想一想 指出互为相同的构型
Br
Br
CH3
CH3
Cl
(1) Cl
H
(2) CH3
Cl H
(3) Cl
H
Br
(4) CH3
10
结论1 含有一个手性碳原子的化合物必 定是手性化合物,有一对对映体 (C连四个不同的基团)
H CH3-CH2-COOH CH3
非手性分子
H
对称面
COOH
结论2 具有对称面的分子是非手性分子
(C连两个以上相同基团或少于四个基团)
一对对映体有相同的物理性质 除了与手性试剂反应外,对映体的化学性质也相同
S - (+) - 乳酸 OH > COOH > CH3
R - (-)-乳酸
(2) R/S 构型标记法在Fischer投影式中的应用 末优基团在竖方向(即上或下)时,只须在 纸平面上沿最优→次优→再次优基团画圆弧, 顺时针为R型,反之为S型。
