电极溶液界面结构与性质介绍
电化学基本原理与应用-第3章

净电荷
α
偶极层
3.2.1 “孤立相”的几种电位
(1)外电位(Ψα)
将试验电荷自无穷远处移至距球面约 10-4~10-5厘米处。在这一过程中可以认为 球体与试验电荷之间的短程力尚未开始作 用。根据电位的定义,此时所做的功为:
W1 = Zie0ψ α
ψ α = W1
Z ie0
球体α的外部电位
试验电荷电量
当试验电荷从相内逸出到相外时,这一过 程所涉及的能量变化(-Wiα)相当于试验电荷从 该相逸出而必须摆脱与该相物质之间的短程 相互作用及越过表面时对表面电势所做的功。 这部分功称为试验电荷在α相的“逸出功”, 显然应满足下列关系式:
−Wiα = μiα + Zi Fχ α
3.2.1 “孤立相”的几种电位
(b)内电位差,又称“伽伐尼(Galvani) 电位差”,定义为φα-φβ。直接接触的两相 间的内电位差,用 αΔβφ 表示。由于表面电 位无法测量,所以该值不能测量。也无法理 论计算。
3.2.2 相间电位差
φα −φ β = (χ α +ψ α ) − (χ β +ψ β ) = (ψ α − ψ β ) + ( χ α − χ β )
(1)相间电位差的种类 两相之间出现“相间电位差”的原因只可
能是界面层中带电粒子或偶极子的非均匀分 布,并形成了界面荷电层。
根据以上关于孤立相电位的讨论不难推 想,所谓α、β两相之间的电位差也因此可 能有各种不同的定义,其中较常用的有下面 三种:
3.2.2 相间电位差
(a) 外电位差,又称“伏打(Volta)电位 差”,定义为ψα-ψβ。直接接触的两相间的 外电位差,用 αΔβψ 表示。两相均为金属 时,为金属接触电位差,可直接测量。
电极过程动力学第2章电极-溶液界面的基本性质

电极表面吸附现象
物理吸附
物理吸附是指物质通过范德华力等物理作用在电极表面吸附的现象。 物理吸附对电极反应的影响较小。
化学吸附
化学吸附是指物质通过化学键合作用在电极表面吸附的现象。化学 吸附对电极反应的影响较大,可以改变电极表面的性质。
电极过程动力学第2章电极-溶 液界面的基本性质
目
CONTENCT
录
• 电极-溶液界面概述 • 电极表面特性 • 溶液性质对界面影响 • 界面电势差与双电层结构 • 界面电荷转移过程 • 界面传质过程与扩散层结构
01
电极-溶液界面概述
界面定义与分类
界面定义
电极与溶液之间的接触区域,发生电 化学反应的场所。
竞争吸附
当多种物质在电极表面发生吸附时,它们之间可能存在竞争关系。竞 争吸附的结果取决于各种物质的吸附能力和电极表面的性质。
03
溶液性质对界面影响
溶液组成与性质
溶质种类与浓度
不同溶质及其浓度会对电极-溶液界面的性质产生显著影响。例如 ,某些溶质可能在界面处发生吸附或反应,从而改变界面的结构 和性质。
电极表面的能量状态与晶体内部 不同,表面能的高低影响了电极 反应的进行。
电极表面粗糙度
表面形貌
电极表面的粗糙度是指表面形貌的不规则程度,它 对电极反应速率和电流分布有重要影响。
真实面积与表观面积
电极表面的真实面积通常比表观面积大,这是由于 表面粗糙度引起的。真实面积对电极反应速率有直 接影响。
粗糙度因子
扩散层结构特点
01
扩散层定义
在电极表面附近,由于浓度梯度引 起的物质扩散区域。
电极溶液界面课件

contents
目录
• 电极溶液界面基础 • 电极溶液界面的电化学性质 • 电极溶液界面的物理化学性质 • 电极溶液界面的应用 • 电极溶液界面的研究方法与技术
01
电极溶液界面基础
电极溶液界面的定义
总结词
电极溶液界面是指电极和与之接触的溶液之间的界面,是电化学反应的重要场 所。
燃料电池
燃料电池利用电极溶液界面将化学能转化为电能。电极溶液界面的性质决定了燃料电池的效率和耐久 性。优化电极溶液界面的结构和组成可以提高燃料电池的性能。
传感器与生物电分析
电化学传感器
电极溶液界面在电化学传感器中发挥着关键作用。通过监测电极溶液界面上的电化学反应,可以实现对气体、离 子、有机物等的快速、灵敏检测。例如,电化学气体传感器利用电极溶液界面检测环境中的有害气体。
形貌
电极表面形貌对溶液在电极表面的润湿和电化学反应过程产 生影响,不同形貌的电极具有不同的电化学性能。
04
电极溶液界面的应用
电化学能源存储与转换
电池技术
电极溶液界面在电池中起着至关重要的作用。它可以影响电池的能量密度、充放电速度和循环寿命。 例如,锂离子电池利用电极溶液界面进行电荷转移和离子传输,从而实现高效的能量存储和释放。
电极反应的步骤和涉及的中间产物。
电极反应动力学方程
描述电极反应速率与反应物浓度、温度等因素关系的方程。
离子传输与迁移
01
02
下的迁移 速率。
离子淌度
离子迁移速率与电场强度 的比值。
离子扩散系数
描述离子在溶液中扩散速 率的参数。
双电层结构与电动现象
双电层结构
电极表面与溶液之间的电荷分布, 包括紧密层和扩散层。
电化学 第2章 双电层(3)
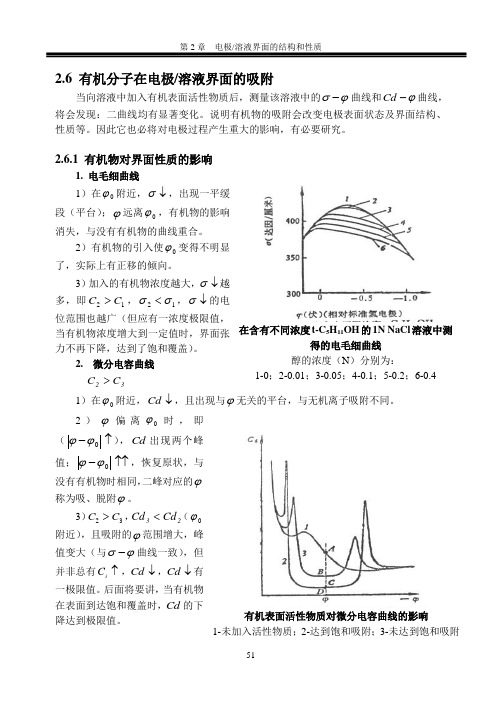
2.6 有机分子在电极/溶液界面的吸附当向溶液中加入有机表面活性物质后,测量该溶液中的ϕσ-曲线和ϕ-Cd 曲线,将会发现:二曲线均有显著变化。
说明有机物的吸附会改变电极表面状态及界面结构、性质等。
因此它也必将对电极过程产生重大的影响,有必要研究。
2.6.1 有机物对界面性质的影响1. 电毛细曲线1)在0ϕ附近,↓σ,出现一平缓段(平台);ϕ远离0ϕ,有机物的影响消失,与没有有机物的曲线重合。
2)有机物的引入使0ϕ变得不明显了,实际上有正移的倾向。
3)加入的有机物浓度越大,↓σ越多,即12C C >,12σσ<,↓σ的电位范围也越广(但应有一浓度极限值,当有机物浓度增大到一定值时,界面张力不再下降,达到了饱和覆盖)。
2. 微分电容曲线32C C >1)在0ϕ附近,↓Cd ,且出现与ϕ无关的平台,与无机离子吸附不同。
2)ϕ偏离0ϕ时,即(↑-0ϕϕ),Cd 出现两个峰值;↑↑-0ϕϕ,恢复原状,与没有有机物时相同,二峰对应的ϕ称为吸、脱附ϕ。
3)23C C >,23Cd Cd <(0ϕ附近),且吸附的ϕ范围增大,峰值变大(与ϕσ-曲线一致),但并非总有↑i C ,↓Cd ,↓Cd 有一极限值。
后面将要讲,当有机物在表面到达饱和覆盖时,Cd 的下降达到极限值。
在含有不同浓度t-C 5H 11OH 的1N NaCl 溶液中测得的电毛细曲线 醇的浓度(N )分别为: 1-0;2-0.01;3-0.05;4-0.1;5-0.2;6-0.4有机表面活性物质对微分电容曲线的影响1-未加入活性物质;2-达到饱和吸附;3-未达到饱和吸附那么,如何解释ϕ-Cd 曲线中出现的平台以及峰值呢?再有,能否利用ϕ-Cd 曲线求有机物在表面的吸附量呢?茀鲁姆金做了这方面的工作,我们来介绍一下。
2.6.2弗鲁姆金的吸附假说所谓假说,就是说该理论没有严格的热力学依据,但可以解释实验现象。
我们就看一看这个假说的内容以及它是如何解释实验现象的。
应用电化学-1-3-双电层

电极溶液界面的紧密 双电层结构
考虑了热运动干扰时的电极溶 液界面双电层结构
在金属相中,自由电子的浓度很大,可达1025 mol/dm3 ,少量 剩余电荷在界面的集中并不会明显破坏自由电子的均匀 分布,因此可以认为金属中全部剩余电荷都是紧密分布 的,金属内部各点的电势均相等。 在溶液相中,当溶液总浓度较高,电极表面电荷密度较 大时,由于离子热运动较困难,对剩余电荷分布的影响 较小,而电极与溶液间的静电作用较强,对剩余电荷的 分布起主导作用,溶液中的剩余电荷也倾向于紧密分布, 形成紧密双电层。
q
1.3.4 双电层的结构
在电极/溶液界面存在着两种相间相互作用:
(1)电极与溶液两相中的剩余电荷所引起的静电长程作用; (2)电极和溶液中各种粒子(离子、溶质分子、溶剂分子等等) 之间的短程作用,如特性吸附、偶极子定向排列等,它只 在几个Å的距离内发生。
电极溶液界面的基本结构
• 静电作用使得符号相反的剩余电荷力图相互靠近,形成紧密 的双电层结构,简称紧密层。 • 热运动处使荷电粒子倾向于均匀分布,从而使剩余电荷不可 能完全紧贴着电极表面分布,而具有一定的分散性,形成分 散层。
1.3.1.1 界面电荷层的形成
自发形成的双电层 M
+ + + + + + + + + + + + + + + + + + + +
S
M
+
S
+
M
+
S
+
(a)离子双电层
(b)吸附双电层
(c)偶极双电层
强制形成的双电层
非法拉第过程讲解

1.3.1.1 界面电荷层的形成
自发形成的双电层
M
S
+ +
+ +
+ +
+ +
M
S
M
S
+
+
+
+
+ +
+
+
+
+
+
+
+
+
+ +
(a)离子双电层 (b)吸附双电层 (c)偶极双电层
强制形成的双电层
KCl ++++++ Hg ------
理想极化电极
2Hg – 2e- = Hg22+ , =0.1 V
K+ + e- = K , = -1.6V
1.3.2 双电层的结构
在电极/溶液界面存在着两种相间相互作用:
(1)电极与溶液两相中的剩余电荷所引起的静电长程作用; (2)电极和溶液中各种粒子(离子、溶质分子、溶剂分子等等) 之间的短程作用,如特性吸附、偶极子定向排列等,它只 在几个Å的距离内发生。
非法拉第过程:在电极-溶液界面间没有电荷转移,但是随 着电势变化,由于吸附和脱附过程发生以及双电层的充放电, 导致电极-溶液界面结构发生变化,并引起电流流动,这种电 流流动过程称为非法拉第过程。不遵循法拉第定律。
1.3.1 界面电荷层
当性质不同的相接触时,在相界面上形成了不 同性质的电势差。 出现电势差的原因是带电粒子或偶极子在界面 层中的非均匀分布。
电化学原理简答题

电化学原理简答题第三章电极/溶液界面的结构与性质1.为什么电毛细曲线是具有极大值的抛物线形状?溶液界面存在双电层,剩余电荷无论带正电还是负电,同性电荷间相互排斥,使界面扩大,而界面张力力图使界面缩小,两者作用效果相反,因此带电界面的张力比不带电时小,且电荷密度越大,界面张力越小,因此电毛细曲线是具有极大值的抛物线形状。
2.标准氢电极的表面剩余电荷是否为零?不一定,标准氢电极电位为0指的是氢标电位,是人为规定的,电极表面剩余电荷密度为0时的电位指的是零电荷电位,其数值并不一定为0;因为形成相间电位差的原因除了离子双电层外,还有吸附双电层\偶极子双电层\金属表面电位。
3.影响双电层结构的主要因素是什么?为什么?静电作用和热运动。
静电作用使符号相反的剩余电荷相互靠近,贴于电极表面排列,热运动使荷电粒子外散,在这两种作用下界面层由紧密层和分散层组成。
4.什么叫Ψ1电位?能否说Ψ1电位的大小只取决于电解质总浓度而与电解质本性无关? Ψ1电位的符号是否总是与双电层总电位的符号一致?为什么?距离电极表面d处的电位叫Ψ1电位。
不能,因为不同的紧密层d的大小不同,而紧密层的厚度显然与电解质本性有关,所以不能说Ψ1电位的大小只取决于电解质总浓度而与电解质本性无关。
当发生超载吸附时Ψ1电位的符号与双电层总电位的符号不一致。
5.简要概括电极/溶液界面发展的四个阶段、优缺点及其主要内容。
①亥姆赫兹紧密双电层模型:主要内容:将双电层比作是平行板电容器优点:a能够解释界面张力随电极电位变化b能够解释微分电容曲线上所出现的平台区域缺点:a解释不了界面电容随电极电位和溶液总浓度的变化规律b解释不了在稀溶液中,零电荷电位下微分电容最小等实验事实②Gouy和Chapman分散层模型:主要内容:溶液中的离子在静电作用和热运动作用下,按位能场中粒子的波尔兹曼分配律分布,完全忽略紧密层,只考虑分散层。
优点:a能较好解释微分电容最小值的出现b能较好解释电容随电极电位的变化规律缺点:a理论计算微分电容值与实验事实相差太大b解释不了微分电容曲线上的“平台区”的出现③Stern模型(双电层静电模型):主要内容:双电层由紧密层和分散层两部分组成。
第三章-电极溶液界面
• 影响:改变电极上双电层的分布,从而影 响反应粒子在电极表面的浓度和活化能, 使反应速率发生变化
一、无机离子的吸附
• 1.大多数无机阴离子是表面活性物质,而无 机阳离子的表面活性很小,只有少数离子 才表面活性。
表面张力变化原因
• 无论双电层是带正电还是带负电,由于同 性电荷的相互排除使界面有扩大的趋势, 与表面张力使界面缩小的趋势相反。因此, 带电界面比不带电界面表面张力下。而剩 余电荷密度与电势有关,故表面张力与电 势有关。
二、电毛细曲线的微分方程
• 根据吉布斯等温吸附方程
d id i
i
电子的表面吸附量 e q / F
• 常用的方法: • 充电曲线法
• 电位扫描法
氢原子的吸附
• 氢的吸附过程伴随有氢分子的分解,分解 生成的氢原子与金属表面相互作用而形成 吸附键。吸附氢原子与吸附自由氢原子是 不同的,吸附过程放出大量吸附热,吸附 氢原子的能量低得多。
氧原子的吸附
• 在常温下,主要是氧原子和含氧粒子的吸 附。这些含氧粒子是在逐步还原或OH-逐步 氧化过程形成并吸附的。
若保持电位恒定,并保持i组分外的化学势不变
i
(
i
) ,ki
负离子可逆,正离子表面剩余电荷量
(
Ina
)
1
正离子离子可逆,负离子表面剩余电荷量
( Ina
)
1
求解表面剩余电荷量的步骤
• 1.测量不同电解质浓度的电毛细曲线 • 2.从各条电毛细曲线下取同一相对电位下的
• 值,做出 ~ Ina 关系曲线。
双电层电位由紧密层电位差和分散层电位差
电极与溶液界面的性质

(3)“紧密层”中的电势分布呈线性,“分散层”中的电势分布为非线 性
27
可解释以下实验现象: (1)、在稀溶液中,Cd有极小值; (2)、电极表面荷正电时,Cd值较大; (3)、电极表面荷较大负电时, Cd值约20; (4)、随电极表面荷电量的加大, Cd急剧上升。
C=ε0 ε/d dH2O=2.8 X10-8cm ε0= 8.85 X10-8μF/cm; εH2O= 6; C= 8.85 X10-8X6/2.8 X10-8 ≈20 μF/cm2
0.2V/20Å
106 V/cm
速率V2= exp(-βFΔV/RT)×速率V1
研究“电极 /溶液”界面的目的:弄清界面性质与电极反应速度的关联
性; 加深对界面电势和电极电势等物化概念的理解
6
“电极溶液”界面对电极反应速度的影响因素: ( 1 )材料因素:电极材料及其表面状态、电解质溶液性质 对电极反应速度有影响
上一章基本概念回顾
电极反应 阳极,阳极反应 阴极,阴极反应 电极过程,阳极过程,阴极过程 电极过程的主要特征
控制步骤
电极电势:绝对电极电势,相对电极电势,氢标电势 极化
超电势
1
本章内容引导
现象:
1、在不同电极上,同一电极反应的进行速度可以相 差10个数量级;
H+ + e
H2( Pt上比Hg上快10个数量级)
(电解质溶液的组成和浓度、电极材料的物理、化学性质及 表面状况)
(2)电场因素:界面电场影响反应的活化能,从而影响电极
反应速度;
7
3、电极/溶液界面附近荷电层的形成、结构 形成机制(金属电极/电解质界面): (1)、离子双电层
由电极表面的剩余电荷与溶液中与之相反的离子组成
3、电极-溶液界面的结构与性质

电毛细曲线微分方程 ( Lippmann方程 )
3、2 电毛细现象
对电毛细曲线微分方程的实验解释 当电极表面存在正的剩余电荷时:
q 0: 0
对应电毛细曲线左半部分(上升分支); 当电极表面存在负的剩余电荷时, q 0: 0 对应电毛细曲线右半部分(下降分支) 。
RT
Page 20
ln
,
3、2 电毛细现象
离子表面剩余量的具体求法 测出不同浓度的
~ 曲线;
从 ~ 曲线上取同一
下的 值,做
,
由 ~ ln 曲线求出某一浓度下的斜率 ~ ln, 即 ,从而得 。
3、2 电毛细现象
电极的极化(polarization) 当电极上无电流通过时,电极处于平衡状态,这时 的电极电势分别称为阳极平衡电势和阴极平衡电 势——理想极化电极。
在有电流通过时,随着电极上电流密度的增加,电
极实际分解电势值对平衡值的偏离也愈来愈大,
这种对平衡电势的偏离称为电极的极化。
Page 9
零电荷 0
左半部 0 电极表面剩余电荷密度 为正值。 右半部 0 电极表面剩余电荷密度 为负值。
Page 28
3、3 双电层的微分电容
溶液越稀微分电容曲线的极小值
点越明显。
微分电容曲线有“平台”出现,
即
不随 Cd
变化。
但正、负离子出现“平台”的数
值不同,表明双电层结构不同。
Rf
通常情况下,通过外电路 流向“电极/溶液”界面的 电荷可能参加两种不同的 过程:
C
电极体系的等效电路
在界面上参加电化学(电极)反应而被消耗,相当 于部分电量通过一个电阻
电化学电极与溶液界面的性质

d
界面荷电层中离子浓度的分布: 遵循Bolizmann分布
j-y y
j
(具体数学表达式见参考书)
j
d
x
10
4、研究电极/溶液界面的实验手段和方法
研究电极溶液界面的基本思路:实验测量反映界面性质的 参数(如界面张力,微分电容,电极表面剩余电荷密度等) 与电极电势的关系,根据结果给出理论模型。
j j-y y
d d
j
x
20
现象: 在离零电势较远的负电势区,界面微分电容值几 乎与电势无关,也与溶液中阳离子的半径及价态基本 无关。且在不同金属的荷负电表面上,微分电容具有 相近的数值(20微法/平方厘米)。
21
1963年,Bockris等人提出BDM双电层模型(BockrisDavanathan-Muller): 紧密层由两个串联的双电层组成。紧靠电极表面的内 层为吸附的水分子偶极层,外层为水化离子层。
“电极/溶液”界面的构造和性质
1
1、何为电极/溶液界面
(静电、特性吸附、水偶极分子定向排布)
电极/溶液界面:当电极与溶液接触时,在各种界面因素 的作用下,电极和溶液相之间形成的一个在结构和性质上 与本体溶液不同的过渡相。 2
E.g. 锌电极插入硫酸锌溶液中
电极/溶液界面的结构:指在这一两相过渡区域中剩余电荷和电势的分布;
电极/溶液界面的性质:指结构随电极电位的变化关系。
3
2、为什么要研究电极/溶液界面?
“电极/溶液”界面是电极反应发生的“客观环境”,其结构和性质对电极 反应速度有重大影响!
实验现象:
(1)在不同电极上,同一电极反应的进行速度可以 相差10个数量级;
H+ + e
大学电化学第二章-2

d1
d2
“ 电极/溶液”界面模型概要
1.由于界面两侧存在剩余电荷 (电子及离子电荷)所引起的界 面双电层包括紧密层和分散层两 个部分。前者是带有剩余电荷的 两相之间的界面层,其厚度不超 过几个埃 Å ,而后者是液相中具 有剩余离子电荷及电势梯度的表 面层。
“ 电极/溶液”界面模型概要
2.分散层是离子电荷的热运动所引起的,其结构(厚 度、电势分布等)只与温度、电解质浓度(包括价型)及 分散层中的剩余电荷密度有关,而与离子的个别特性无关。 它们之间的基本关系可用下式表示。如果存在特性吸附, 则该式中需用 q分散 代替 q 。
0
• 将 x 代入Poisson方程得
2 x xF xF 4c 0 F [exp( ) exp( )] 2 RT RT x
4 x 2 E x x 2
三、双电层模型的数学表达式
2 x xF xF 4c 0 F [exp( ) exp( )] 2 x RT RT
dq Cd d
1 1 dq dq d ( 1 ) d 1
1 d d ( 1 ) d 1 Cd dq dq
1 1 CH CG
紧密层电容
分散层电容
CH CG
影响双电层结构的因素 浓度的影响 温度的影响 电极电位的影响 组分与电极间作用的影响
三、双电层模型的数学表达式
1
1 CH
RTC0 z F z F [exp( i 1 ) exp( i 1 )] 2 2RT 2RT
(3)
RTci 0 | zi | 1F | zi | 1F q [exp( ) exp( )] 2 2RT 2RT
1 1 CH
2009-01-15--第三章+电极-溶液界面结构与性质(3.4-双电层的结构和零电荷电位2学时)
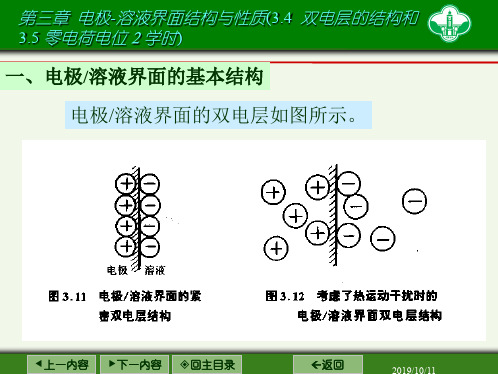
一、电极/溶液界面的基本结构
电极/溶液界面的双电层如图所示。
上一内容 下一内容 回主目录
返回
第三章 电极-溶液界面结构与性质(3.4 双电层的结构和 3.5 零电荷电位2学时)
电极/溶液界面剩余电荷分布和电位分布如图3.14所示。
常数
2RT F
ln a
RT F
ln
c
Ψl<0时
1
常数
2RT F
ln( a)
RT F
ln
c
式中,“常数”为:
2RT ln 1 F C紧
2 RT 0 r
上一内容 下一内容 回主目录
返回
第三章 电极-溶液界面结构与性质(3.4 双电层的结构和 3.5 零电荷电位2学时)
RT
)
返回
第三章 电极-溶液界面结构与性质(3.4 双电层的结构和 3.5 零电荷电位2学时)
当
1和x=时,
x
=0和
x
=0
利用数学关系式
2
x2
1 ( )2
2 x x
从x=d到x=∞积分
(
x
)2 x=d
2cRT
0 r
exp(
1F
上一内容 下一内容 回主目录
返回
第三章 电极-溶液界面结构与性质(3.4 双电层的结构和 3.5 零电荷电位2学时)
双电层电位差由紧密层电位差与分散层电位差两部分 组成,可以利用下列式计算双电层电容:
1 da d (a 1) d1 1 1
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
R,f
Rl
a Cd
b
C
, d
辅助电极上(如Pt)几乎无反应,所以 可以去掉,又由于其面积很大,Cd很大, 相当于辅助电极短路,可以将电路进一 步简化为:
Rf
a Cd
Rl
b
对理想极化电极还可以进一步简化为:
Cd
a
Rl
b
三. 微分电容曲线
1 — 0.0001mol L KCl 2 — 0.001mol L KCl
三.电毛细曲线法的主要应用 判断电极表面带电状况(符号); 求电极表面剩余电荷密度q ;
求离子表面剩余量 i 。
离子表面剩余量
离子表面剩余量 :界面层溶液一侧垂直
于电极表面的单位截面液柱中,有离子 双电层存在时i离子的摩尔数与无离子双 电层存在时i离子的摩尔数之差。
i
i
, ji
实际上,由于下述原因做不到 恒定:
Cd
dq
d
积分电容:从φ0到某一电位φ之间的平均电 容称为积分电容 。
Ci
q
与 的关系:
Ci Cd
∵
q
q
dq
0
0 Cd d
∴
Ci
q
q
o
1
0
0 Cd d
二. 微分电容的测量
交流电桥法:在处于平衡电位平或直流
极化的电极上迭加一个小振幅的正弦波 (扰动<10mV),用交流电桥测量与电 解池阻抗相平衡的串联等效电路的电容 值与电阻值,从而求得 Cd 。
一. 电毛细曲线的测定
体系平衡时:
gh 2 cos
r
∴
gr K h 2 cos
恒定一个电位 ,通
过调节贮汞瓶高度使 弯月面保持不变,从
而求得 。
毛细管静电计示意图
二.电毛细曲线及其微分方程
电毛细曲线微分方程的推导 由Gibbs吸附方程:
d idi
界面张力的 变化
表面吸 附量
化学位变 化
对电毛细曲线微分方程的实验解释
当电极表面存在正的剩余电荷时:
q 0 : 0
对应电毛细曲线左半支; 当电极表面存在负的剩余电荷时,
q 0 : 0
对应电毛细曲线右半支。
当电极表面剩余电荷等于零,即无离子 双电层存在时:
q 0 : 0
定义:表面电荷密度q等于零时的电极电 位,也就是与界面张力最大值相对应的 电极电位称为零电荷电位 (zero charge potential)。
3 — 0.01mol L KCl 4 — 0.1mol L KCl
微分电容曲线的应用
利用 0 判断q正负 ;
研究界面吸附 ; 求q、 Ci :
q Cd d
Ci
q
q
o
1
0
0 Cd d
第四节 双电层结构
一.电极/溶液界面的基本结构 电极/溶液界面的特点: 静电作用:使符号相反的剩余电荷形成 紧密双电层结构; 热运动:使荷电粒子趋向均匀分布,形 成分散层结构。
(+) Hg Hg e 0.1V
(-) K e K Hg 1.6V
在+0.1~-1.2V之间可以认为 该电极是理想极化电极。
第二节 电毛细现象 electrocapillarity
电毛细现象:界面张力б随电极电位变化 的现象。
电毛细曲线:界面张力与电极电位的关 系曲线 。
基本线路
交流讯 号源
交流电桥
直流极 化回路
电极电位测量 回路
交流电桥法测定微分电容的基本线路
电解池的设计及其等效电路分析
Cab
Ra
a
Rf
R
, f
Rl
Rb
b
Cd
C
, d
由于电极本身是金属材料,导电性能好, 可不考虑Ra和Rb;同时由于两电极间距离 大,所以Cab<<Cd,此时,电路简化为:
Rf
Helmholtz模型(紧密层模型)
该模型只考虑电极与溶
液间的静电作用,认为
电极表面和溶液中的剩
余电荷都紧密地排列在
界面两侧,形成类似荷
M
电平板电容器的界面双
电层结构。
Helmholtz模型成功之处:
解释了界面张力随电极电位变化的规律;
可以解释微分电容曲线的平台区。
对电极体系,可将电子看成可在表面移 动积累产生吸附的粒子。 若电极表面剩 余电荷密度为q,则:
q e F
电子的表 面吸附量
其化学位变化为:
de Fd
∴
edi qd
Gibbs方程改为: d idi qd
对理想极化电极: di 0无反应
∴ =-q
或:
q
u
电毛细曲线微分方程 ( Lippmann方程 )
用来改变界面结构。
Rf
C
电极等效电路
理想极化电极
定义:在一定电位 范围内,有电量通 过时不发生电化学 反应的电极体系称 为理想极化电极。
Ideal polarized electrode
C
理想极化电极等效电路
常用的理想极化电极——滴汞电极 dropping mercury electrode (DME)
率
ln
,
,
即
i,从而得 i ~ 。
在0.1mol / L溶液中,正、负离子表面剩余量随电极电位的变化
第三节 双电层的微分电容
一. 微分电容与积分电容
微分电容(differential capacity):引 起电位微小变化时所需引入电极表面的
电量,也表征了界面在电极电位发生微
小变化时所具备的贮存电荷的能力。
第四章 电极/溶液界面的结构 与性质
重点要求
研究双电层结构的主要方法的基本原理、 优缺点和用途;
界面结构的物理图像(模型); 特性吸附对双电层结构、性质的影响; 相关概念
第一节 概述
一. 研究电极/溶液界面性质的意义 界面电场对电极反应速度的影响
电解液性质和电极材料及其表面状态的 影响
两电极体系中,改变组分i的浓度,参比 电极电位将发生变化;
在电解质溶液中不可能单独只改变一种 离子的浓度,往往改变的是电解质MA的 浓度。
为使用方便,常采用下面的公式:
RT
ln
,
具体求法
测出不同浓度的 ~ 曲线;
从 ~ 曲线上取同一 ,下的 值,做
~ ln
由 ~ ln 曲线求出某一浓度下的斜
二. 研究电极/溶液界面的基本方法
研究电极/溶液界面的思路: 通过使用一些可测的界面参数来研究电
极/溶液界面;
根据一定的界面结构模型来推算界面参 数 ,根据实验测量数据来检验模型。
基本方法: 充电曲线法 微分电容曲线法 电毛细曲线法
研究电极/溶液界面对研究电极的要求
通过外电路流向“电 极/溶液”界面的电 荷可能参加两种不同 的过程: 在界面上参加电化学 反应而被消耗 ;
