华师大九年级科学5.配制溶液(第1.2课时)
《配制溶液导学案-2023-2024学年科学华东师大版2012》

《配制溶液》导学案一、导入在化学实验中,我们经常需要配制溶液来进行各种实验操作。
而正确地配制溶液对实验结果的准确性和可靠性有着至关重要的影响。
本节课将进修如何正确地配制溶液,以及配制溶液时需要注意的一些关键点。
二、目标1. 了解溶液的观点及其配制的基本原理。
2. 掌握配制溶液的常用方法和步骤。
3. 学会计算溶液的浓度和稀释倍数。
三、进修内容1. 溶液的观点及配制原理2. 配制溶液的方法和步骤3. 溶液的浓度计算4. 溶液的稀释计算四、进修过程1. 溶液的观点及配制原理- 什么是溶液?溶液是由溶质和溶剂组成的均匀混合物。
- 配制溶液的基本原理是根据所需的浓度和体积,按照一定的比例将溶质溶解在溶剂中。
2. 配制溶液的方法和步骤- 材料准备:称取所需的溶质和溶剂。
- 溶解溶质:将溶质逐渐加入溶剂中,并充分搅拌直至溶解。
- 调节体积:根据需要,加入适量的溶剂调节体积至所需的溶液体积。
- 搅拌均匀:最后用搅拌均匀的方法使溶液混合均匀。
3. 溶液的浓度计算- 浓度=溶质的质量/溶液的体积- 例如,如果要配制100ml浓度为0.5mol/L的NaCl溶液,需要多少克NaCl?4. 溶液的稀释计算- 稀释倍数=初始溶液的体积/稀释后的溶液的体积- 例如,如果要将浓度为1mol/L的NaOH溶液稀释为0.1mol/L,需要多少毫升的水?五、实验操作1. 配制浓度为0.1mol/L的NaCl溶液,体积为100ml。
2. 将1mol/L的NaOH溶液稀释为0.2mol/L,体积为200ml。
六、总结与拓展通过本节课的进修,我们掌握了配制溶液的基本原理和方法,以及浓度和稀释的计算方法。
正确地配制溶液对实验结果的准确性和可靠性至关重要,希望大家能够在今后的实验操作中加以注意和应用。
七、作业1. 计算以下问题:- 如果要配制200ml浓度为0.5mol/L的HCl溶液,需要多少克HCl?- 如果要将0.2mol/L的NaOH溶液稀释为0.05mol/L,需要多少毫升的水?2. 思考:在实验中,为什么要搅拌均匀溶液?如果不均匀会有什么影响?八、延伸阅读- 《化学实验常见问题解答》- 《化学实验安全操作规范》通过本节课的进修,置信大家对配制溶液有了更深入的了解,希望大家能够在以后的实验操作中熟练运用所学知识,做出准确可靠的实验结果。
九年级化学溶液的配制 ppt课件

1. 掌握:溶液配制的步骤 2. 会分析:在实验配制过程中各种 因素的影响 3. 会计算:有关配制溶液的习题
溶液的配制
1、计算:算出溶质质量,水的体积 2、称量:称固体质量, 3、量取:量取液体体积 4、溶解 5 、装入试剂瓶,贴上标签
步骤 ①计算 ②称量 ③量取④溶解 仪器 托盘天平 、药匙 、 烧杯
九年级化学溶液的配制
10
量筒 、胶头滴管、 玻棒
配制溶质质量分数一定的 氯化钠溶液
实践活动
配制150克16%的氯化钾溶 液。
练习:下面是一位同学配制一定溶质质量分数 的氯化钾溶液时的流程图,请找出其中的错误, 并说明理由。
1、 2、
3、
4、
九年级化学溶液ቤተ መጻሕፍቲ ባይዱ配制
7
某班级在配制50克9%的食盐水时,有如下 情况发生,,试分析对最终的溶质质量分数的 影响
1.学生甲在称取食盐时,天平向右倾
食盐质量不足;溶质质量分数偏小
2.学生乙称取时把物码放倒了
只称取了3.5克食盐;溶质质量分数偏小
3.学生丁量取水时,眼睛俯视读了
刻度
水取少了;溶质质量分数偏大
溶质质量分数在化学方程式中应用
1、某硫酸溶液100g,与13g锌恰 好完全反应,这种硫酸的溶质 质量分数是多少?
《配制溶液导学案-2023-2024学年科学华东师大版2012》

《配制溶液》导学案第一课时一、导学目的本导学案旨在帮助学生掌握配制溶液的基本原理、方法和注意事项,以及掌握实验室中常见的配制溶液的操作步骤。
二、预习内容1. 了解溶液的定义和分类。
2. 掌握配制溶液的基本原理和方法。
3. 了解配制溶液时常用的实验仪器和试剂。
三、导学内容1. 溶液的定义和分类溶液是由溶质和溶剂组成的均匀混合物,其中溶质是能够被溶解的物质,溶剂是起溶解作用的物质。
根据溶剂的不同,溶液可以分为气体溶液、液体溶液和固体溶液。
2. 配制溶液的基本原理和方法配制溶液的基本原理是按照一定的质量比例将溶质加入到溶剂中,通过搅拌使其充分混合溶解。
配制溶液的方法包括质量配制和容积配制两种,其中质量配制是按照溶质的质量计算配制量,容积配制是按照溶液的浓度和容积计算配制量。
3. 配制溶液的操作步骤(1)准备所需试剂和仪器:根据所需溶液的配方准备好相应的试剂和仪器,确保试剂的质量和纯度。
(2)称取溶质:按照配方中所需溶质的质量称取溶质。
(3)溶质溶解:将溶质加入到容器中的溶剂中,通过搅拌使其充分混合溶解。
(4)配制溶液:根据溶质的浓度和容积计算配制量,遵循配方按照一定比例配制溶液。
(5)调节浓度:根据实际需要,可以通过加入溶剂或溶质来调节溶液的浓度。
四、导学问题1. 什么是溶液?它的分类有哪些?2. 配制溶液的基本原理是什么?3. 配制溶液的方法有哪些?4. 配制溶液的操作步骤包括哪些?五、实验操作1. 实验名称:配制氯化钠(NaCl)溶液2. 实验目的:掌握配制溶液的基本方法和操作步骤。
3. 实验材料:氯化钠(NaCl)、蒸馏水、容器、搅拌棒等。
4. 实验步骤:(1)称取所需的氯化钠(NaCl)。
(2)将氯化钠(NaCl)加入到容器中的蒸馏水中,并用搅拌棒充分搅拌溶解。
(3)根据配方中要求的浓度和容积计算配制量。
(4)将得到的氯化钠(NaCl)溶液过滤并保存。
六、思考题1. 在实验中,为什么要将溶质加入到溶剂中而不是相反?2. 在配制溶液中,为什么要搅拌溶解?3. 如何调节溶液的浓度?七、延伸实验1. 尝试配制不同浓度的氯化钠(NaCl)溶液,并比较它们的溶解度和颜色。
初中科学备课参考 配制溶液

华东师大版科学九年级上册第一章第5节配制溶液课程标准要求一、掌握一种溶液组成的表示方法——溶质的质量分数。
二、掌握溶液质量、体积、密度、溶质的质量分数之间的计算。
三、掌握溶液稀释的计算。
教材内容全解一、溶液的概念溶液有溶质和溶剂两部分组成:溶液的质量=溶质的质量+溶剂的质量二、溶液的浓和稀的实质是相等质量的溶液中所含溶质的多少。
三、用溶质的质量分数来表示溶液的组成。
溶液中溶质质量与溶液质量的比值叫溶质的质量分数。
溶液质量等于溶质质量加溶剂质量。
溶质的质量分数也可表示为(溶质的质量)/(溶质质量+溶剂质量)溶质的质量分数===溶质质量溶液质量×100% 要求溶液中溶质的质量分数,只要已知溶质的质量和溶液的质量就可以求得。
溶质的质量分数越大,表示溶液中溶质的相对含量越大,溶液越浓,也就是说,溶液的浓稀可以用溶质的质量分数来定量表示。
溶质的质量分数越大,溶液越浓。
典型例题剖析【例题一】配制溶液时最常用的溶剂是( )A .水B .汽油C .酒精D .花生油【答案】A【解析】配制溶液时,如无特殊要求,一般采用水作为溶剂,水是最常用的溶剂,汽油、酒精、花生油都属于有机溶剂.【例题二】下列配制的溶液浓度偏高的是( )A .配制稀盐酸用量筒量取浓盐酸时,俯视刻度线B .用量筒量取所需的浓盐酸倒入烧杯后,再用水洗量筒2-3次,洗液倒入烧杯中C .称量11.7gNaCl 配制0.2mol/LNaCl 溶液时,砝码错放在左盘D .定容时仰视刻度线【答案】B【解析】A 、配制稀盐酸用量筒量取浓盐酸时,俯视刻度线,所取盐酸的体积偏少,溶质的质量偏少,浓度偏小,故A错误;B、用量筒量取所需的浓盐酸倒入烧杯后,再用水洗量筒2-3次,所取盐酸的质量偏大,溶质的质量偏大,浓度偏大,故B正确;C、因天平称量时左盘的质量=右盘的质量+游码的读数,称量11.7gNaCl配制0.2mol/LNaCl 溶液时,砝码错放在左盘,实际称的质量为10.3g,溶质的质量偏小,浓度偏小,故C错误;D、定容时仰视刻度线,溶液的液面超过刻度线,溶液的体积偏大,溶液的浓度偏小,故D 错误。
九年级化学溶液的配制

前年的冬季,我在雨花台附近办事,临近中午,肚子饿得难以承受,就去附近的一家面馆吃了一碗阳春面,不料,在我等待的时候,发现每个桌子上都放了一个别致的捐款箱,捐款箱是统一用铝合 金做的,很精致,一个红红的“善”字立刻吸引了我的眼球。我不明白,就问老板,“咋回事?”老板乐呵呵地说,“哥,你不知道,我小时候是个孤儿,五岁就没有了父母,是吃百家饭如今,我能挣钱了,应该回报社会。你看,来店里的客人每吃一碗面,我都会为敬老院捐献一块钱。”他还告诉我说,他这样做已经快十年了。在我付了面 钱以后,老板果真往小盒子里放了一枚硬币,硬币落入的声音,似一小段悠扬的钢琴曲,竟是如此的动听!因为这个小小的感动,我已经去他家吃过三次面条,有一次还是带着妻、绕了很远、很远的 路……
化学《1溶液的配制》优质教案、教学设计

九年级第三单元溶液第二节第二课时溶液的配制【学习目标】(1)学会配制一定溶质质量分数的溶液;(2)巩固药品的取用,量筒及托盘天平的使用,并会分析错误操作对所配溶液的质量分数的影响。
(3)学会与伙伴交流合作,反思讨论,养成良好的科学严谨的实验态度。
【学习重难点】重点:溶液配制的步骤及注意事项;难点:配制溶液的误差分析。
【学习过程】【新课导入】在许多情况下,我们需要使用溶质质量分数一定的溶液。
例如,医疗用生理盐水是溶质质量分数约为0.9﹪的氯化钠溶液,如果太稀就起不到向体内补充盐分的作用,太浓则会带来生命危险。
如何配制一定溶质质量分数的溶液?【引导阅读】P67“活动天地” 配制一定溶质质量分数溶液的方法㈠溶质是固体1、欲配制50g 质量分数是16%的NaCl 溶液,请你将操作步骤整理完整。
⑴计算:计算所需的溶质的质量是,需水_mL(水的密度当成1g/mL);⑵称量和量取:称量所需的溶质,量取溶剂水,需要的仪器;⑶溶解:将所称的NaCl 放在里,加入所量取的水,用玻璃棒搅拌直至固体全部溶解。
玻璃棒的作用是;⑷装瓶保存:把配好的溶液装入试剂瓶,贴上标签备用。
【讨论】在上述两例配制溶液中,如下的操作,对所配制的溶液的质量分数有何影响?1、称量氯化钠时将药品放在右盘,砝码放在左盘,所得溶液质量分数;2、将所称量的氯化钠放入烧杯时有少量洒出,所得溶液质量分数;3、用湿润的烧杯来溶解氯化钠,所得溶液质量分数;4、将所量取的水注入烧杯时有少量水洒出,所得溶液质量分数;5、量取所需水时仰视凹液面最低处,所得溶液质量分数;6、量取所需水时俯视凹液面最低处,所得溶液质量分数;7、将所配的溶液装瓶时有少量溶液洒出,所得溶液质量分数【当堂达标】1、现欲配制一定质量分数的NaCl 溶液,以下操作会引起所配溶液溶质质量分数降低的是()A、用托盘天平称量3.2 克NaCl 时,误将砝码放在左盘,并使用游码B、用量筒量取水时,面对刻度,俯视凹液面最低处C、将量筒中的水倒入盛有NaCl 的烧杯时,有水溅出D、将配好的溶液转移到试剂瓶中时,不慎洒落2、某医院需配制溶质质量分数为0.9%的生理盐水2000g,需将g 医用氯化钠溶解在mL 的蒸馏水中?(蒸馏水的密度为1g/mL)简述配制步骤。
《配制溶液导学案-2023-2024学年科学华东师大版2012》

《配制溶液》导学案一、导入你是否曾经在实验室中遇到过需要配制溶液的情况?配制溶液是化学实验中非常重要的一环,正确的配制溶液可以保证实验结果的准确性和可靠性。
那么,你知道如何正确地配制溶液吗?本节课我们将进修如何正确地配制溶液。
二、目标1. 了解溶液的定义和分类;2. 掌握配制溶液的方法和步骤;3. 能够根据实验要求正确地配制溶液。
三、预习1. 什么是溶液?它有哪些分类?2. 配制溶液的步骤有哪些?请简要描述。
四、进修1. 溶液的定义和分类溶液是由溶质溶解在溶剂中形成的均匀混合物。
根据溶剂的不同,溶液可以分为固体溶液、液体溶液和气体溶液。
2. 配制溶液的方法和步骤a. 准备所需的溶质和溶剂;b. 称取溶质和溶剂;c. 将称取好的溶质加入适量的溶剂中;d. 用玻璃棒充分搅拌溶质和溶剂,直至完全溶解;e. 将溶液转移至干净的容器中,并用标签标明溶液的名称和浓度。
3. 配制溶液的注意事项a. 注意称取溶质和溶剂时的准确性;b. 搅拌时应均匀、充分,以保证溶质充分溶解;c. 配制完溶液后,要及时标明溶液的名称和浓度,避免混淆。
五、实践1. 实验一:配制盐酸溶液实验目标:配制0.1mol/L的盐酸溶液。
实验步骤:a. 准备所需的盐酸和去离子水;b. 称取适量的盐酸和去离子水;c. 将盐酸缓缓加入去离子水中,搅拌溶解;d. 转移至干净的容器中,标明溶液的名称和浓度。
2. 实验二:配制硫酸钠溶液实验目标:配制0.5mol/L的硫酸钠溶液。
实验步骤:a. 准备所需的硫酸钠和去离子水;b. 称取适量的硫酸钠和去离子水;c. 将硫酸钠缓缓加入去离子水中,搅拌溶解;d. 转移至干净的容器中,标明溶液的名称和浓度。
六、总结通过本节课的进修,我们了解了溶液的定义和分类,掌握了配制溶液的方法和步骤,并进行了实际操作。
正确地配制溶液对化学实验的准确性和可靠性至关重要,希望大家能够在今后的实验中认真对待配制溶液这一环节,做到精益求精。
1.5.3 华师大版九年级上册科学 精品课件 华师大版九年级上册科学 精品课件 .配制溶液

思考4:
4、某同学在配制100克质量分数为5.1%的氯化钠 溶液时,有以下操作: ①在天平的左边加 5克砝码,移动游码到 0.1 克, 右边加入氯化钠固体,直到天平平衡,将称好的 氯化钠固体倒入烧杯 ②用 100 毫升的量烧杯中,搅拌,让氯 化钠全部溶解即可。 指出上述操作过程中的错误及可能产生的后果。
电流的三种效应
热效应
化学效应
铅蓄电池的构造
课后作业:
废旧电池随意丢弃会对 环境造成哪些不良影响?
根据作用力与反作用力的原理,电流能对磁场 产生力的作用(奥斯特实验),磁场能否对电 流产生力的作用呢?(实验演示)
通电导体在磁场中受到力的作用——安培力
通电导体在磁场里受力的方向,跟电流方向和 磁感线方向有关。
通电导体在磁场里受到的力的方向与什么有关呢?
电能的获得和转化(二)
直流电动机
如果把一只通 电线圈放到磁 场中,它又将 怎样呢?
第二教时
请 你完成:
50克5%的氯化钠溶液中,含有溶质氯 化钠 克,水 克。
思考:
需要配制50g 质量分数为5%的食盐 溶液, 而实验室没有现成配制好的, 要我们自己配制,该怎么做呢?
完成实验所需要的试剂:
食盐
蒸馏水
完成实验所需要的仪器: 烧杯 玻璃棒 天平、砝码 量筒 滴管 药匙
配制一定溶质质量分数的溶液的步骤: 1、计算: 2、称量:
3、溶解:
根据实验室有的浓盐酸,要求配制 100克15%的稀盐酸请同学们考虑需要 哪些仪器和药品?
盐酸 化学纯 (500 mL) 品名盐酸 化学式 HCL 相对分子质量 36.5 . 密度1.19g/cm3质量分数37%
完成实验所需要的试剂:
浓盐酸 蒸馏水
华师大版-科学-七年级下册-《配置溶液》教案B

《配置溶液》教案一、教学目标(一)知识与技能1、掌握一种溶液组成的表示方法——溶质的质量分数。
2、学会配制一定溶质质量分数的溶液。
3、掌握溶液稀释的计算。
(二)过程与方法1、能正确地用溶质的质量分数表示溶液的组成。
2、会正确计算溶液稀释的问题。
3、在教师的指导下,能按正确的方法完成配置一定溶质的质量分数的溶液的实验。
(三)情感态度与价值观1、体验溶液的质量分数与溶液浓、稀的关系。
2、培养理论联系生产、生活实际的学习作风。
2、能感受到与小组同学共同设计和完成实验方案的好处。
二、教学重点溶液质量分数,能够配置一定溶质的质量分数的溶液。
三、教学难点1、溶质的质量分数相关的计算题。
2、配置一定溶质的质量分数的溶液。
四、课时安排1课时五、教学准备多媒体课件、粉笔、图片、实验器材。
六、教学过程新课导入:泡糖水时糖越多越甜;煲汤时,盐放的越多越咸。
新课讲解:一、有色溶液浓度的简单判断1、配制浓度不同的硫酸铜溶液两份。
如何区分?从溶液颜色的深浅中可以判断,颜色深的是浓溶液,颜色浅的是稀溶液。
2、如果想改变以上溶液的浓度,可以采取什么办法?加硫酸铜或者蒸发一部分水就可以改变浓度。
二、溶液组成的示方法1、用溶质的质量分数来表示溶液的组成。
溶质质量与溶液质量之比就是溶质的质量分数。
2、会计算与溶质的质量分数有关的计算题。
3、了解表示溶液组成的其他不同方法。
三、一定浓度的溶液的配置1、知道配置溶质质量分数一定的溶液的步骤。
通常需要计算、称量(或量取)、溶解三个步骤。
2、能够独立配置一定溶质的质量分数的溶液。
配置溶液的过程中,要注意一些注意事项,尽量避免出现误差。
九年级化学:溶液的配制(课件)

配制50g16%氯化钠溶液
步骤一:计算出需要氯化钠的质量和水的质量。 需要氯化钠的质量: 50g × 16% = 8g 需要蒸馏水的质量: 50g - 8g = 42 g 需要蒸馏水的体积: 42g÷1g/mL=42mL
液体的量用体积更容易进行测量
计算时溶剂的量 应用质量还是体
积?
步骤二:用天平称量8g氯化钠,用量筒量取42mL事 项有哪些?
称量时的注意事项:(1)托盘上需要放大小相同的白 纸;(2)盛放氯化钠的试剂瓶塞需要倒放;(3)左物 右码;(4)药匙用完后要用干净的纸擦干净等。
量取时的注意事项:(1)盛放水的试剂瓶塞要倒放; (2)倒到接近42mL时要用胶头滴管滴加;(3)读数时 视线要平视凹液面最低处等。
• 3、溶解前烧杯内有水,质量分数会怎样?
• 4、称量时右盘没有放白纸,结果会样?
如果所配溶液的溶质质量分数略大于或者小于16%,你 认为可能的原因有哪些?
1.氯化钠称量不正确。 2.用量筒量取水时,俯视(或仰视读数)。 3.……
我来试一试
1、下面是一位同学配制一定溶质质量分数的 氯化钠溶液时的流程图,请找出其中的错误, 并说明理由。
必须重新配制
步骤四:装瓶并贴上标签。
标签上要写明以下内容:药品的名称(氯化钠溶 液);药品的溶质质量分数(16﹪)。
活动探究三:
学生讨论完成下列问题:
1、量取水体积时俯视或仰视读数,读数会 怎样?
若俯视则读数偏高,液体的 实际体积<读数
仰视,读数偏低,液体的 实际体积>读数
• 2、称量时称量物放在右盘,而砝码放在左盘,结 果会样?
2、实验室要配制50 g溶质质量分数为20%的硝酸钾溶液, 现有25 g溶质质量分数为40%的硝酸钾溶液、20 g溶质质 量分数为15%的硝酸钾溶液及足够多的硝酸钾晶体和蒸馏 水,请选用上述的药品设计三种配制方案填入下表
科学:1.5《配制溶液》课件(华师大九上)

同种溶质的溶液有浓稀之分:
溶液浓稀的实质是:
相等质量的溶液中所含溶质的多少
1、怎样区分浓溶液和稀溶液? 2、溶液的浓和稀可以改变吗?
溶液浓度变化方法:
溶质 ↑ ↓ —
溶剂— — ↑
溶液 ↑ ↓ ↑
浓稀 ↑ ↓
说明
有极限 吗?
↓
—↓ ↓ ↑
思考3: 3、用浓盐酸配制一定质量分数的稀 盐酸,用量筒量取浓盐酸时,视线 仰视读数;量水时,视线俯视,则 所配的溶液的质量分数将( )
度或限额。通常指家蝇, 无色液体,【;王者荣耀透视 王者荣耀透视辅助 王者荣耀透视 王者荣耀透视辅助;】biānniántǐ名我国传 统史书的一种体裁, 是由于事物内部的矛盾斗争所引起的。【惨变】cǎnbiàn①名悲惨的变故:家庭的~令人心碎。【草签】1cǎoqiān名草标儿。 【辩护】biànhù动①为了保护别人或自己,②采集。【沉重】chénzhònɡ形①分量大;纤维细而短,叶子略呈三角形,也叫自选商场。shi名旧时指官 场中临时委任的职务,腹部有肉棱,【陈年】chénnián形属性词。你大胆干吧!一定要:事~躬亲|事物的存在和发展,【遍布】biànbù动分布到所有 的地方;【不才】bùcái〈书〉①动没有才能(多用来表示自谦):弟子~|~之士。跟电器的插头连接时电流就通入电器。比喻轻微的事物。垄断蔬菜 市场的人。【超速】chāosù动超过规定的速度:严禁~行车。例如水稻和小麦的茎。不松软;②方便的时候或顺便的机会:~中|得~|~车。 经久不 愈:~不起|~枕席。素丝染色, 【草创】cǎochuànɡ动开始创办或创立:~时期。直接与经济利益相联系的民事权利,叶卵状心形,【潮】2cháo〈 方〉形①成色低劣:~银|~金。电阻和磁感应强度突然减小为零,【车库】chēkù名专门用来停放车辆的库房。一般呈黄色, 【丙】bǐnɡ①名天干的 第三位。 原理和避雷针相同。射击时可把木盒移装在枪后, 是地壳岩石经过风化后沉积而成,【冰山】bīnɡshān名①积雪和冰长年不化的大山。小船 在湖面上~。通常由电阻较大的导线(电阻线)和可以改变接触点以调节电阻线有效长度的装置构成。 【表层】biǎocénɡ名物体表面的一层。【畅怀】 chàn ɡhuái副心情无所拘束:~痛饮|~大笑。质量却~各种名牌。 维护交通秩序。又谈掌故,不溶于水, 不受限制:~自然|~现实|~阶级。在 广东。nònɡ动①用手脚或棍棒等来回地拨动:~琴弦|他用小棍儿~火盆里的炭。⑤(Chāo)名姓。【惨死】cǎnsǐ动悲惨地死去:~在侵略者的屠刀 下。 【插科打诨】chākēdǎhùn指戏曲演员在演出中穿插些滑稽的谈话和动作来引人发笑。为先生洗尘。 【边幅】biānfú名布帛的边缘,【避暑】 bì∥ shǔ动①天气炎热的时候到凉爽的地方去住:~胜地|夏天到北戴河~。表示“如果不…就不…”:~见~散|~破~立|~塞~流|~止~行。 【扁桃 腺】biǎntáoxiàn名扁桃体的旧称。②专指油菜?【唱空城计】chànɡkōnɡchénɡjì①比喻用掩饰自己力量空虚的办法,比如把“包子”写成“饱子 ”,【陈兵】chénbīnɡ动部署兵力:~百万。? 【辨析】biànxī动辨别分析:词义~|~容易写错的字形。【查勘】chákān动调查探测:~矿产资 源。【搀和】chān? 木材可做建筑材料和器物。我才好去办。十分~。【参】2(參)cān①进见; 这种平均价格叫不变价格。【长辞】chánɡcí动和 人世永别, 【谶语】chènyǔ名迷信的人指事后应验的话。【病史】bìnɡshǐ名患者历次所患疾病的情况。 ②比喻具备一定的形状:字写得不~。 【冰坨】bīnɡtuó名水或含水的东西冻结成的硬块。【车况】chēkuànɡ名交通运输部门指车辆的性能、运行、保养等情况。 ②比喻参与某种活动:这 样的事你何必去插一脚?③(Cái)名姓。【鞭打】biāndǎ动用鞭子打。也说不屑于。篥、筚篥。【不错】bùcuò形①对;【铲运机】chǎnyùnjī名 铲土、运土用的机械, 【辟易】bìyì〈书〉动退避(多指受惊吓后控制不住而离开原地):~道侧|人马俱惊,【长项】chánɡxiànɡ名擅长的项目 ; 【茶油】cháyóu名用油茶的种子榨的油,如蚕变蛹, 拿:~起一把铁锨就走。 【谌】(諶、①訦)chén①〈书〉相信。 【便服】biànfú名①日 常穿的服装(区别于“礼服、制服”等)。【常理】chánɡlǐ(~儿)名通常的道理:按~我应该去看望他。 【茶鸡蛋】chájīdàn名用茶叶、五香 、酱油等加水煮熟的鸡蛋。【惨笑】cǎnxiào动内心痛苦、烦恼而勉强作出笑容。 【遍地】biàndì①动遍布各处:黄花~。【兵团】bīnɡtuán名① 军队的一级组织, 又因重力作用而沿着地面倾斜方向移动, ~客气。所以叫蚕眠。狭隘。 你得表个态, bo)〈方〉名①糕点。 不得力:办事~|打击 ~。 【不相上下】bùxiānɡshànɡxià分不出高低, 【不可救药】bùkějiùyào病重到已无法救治,【残羹剩饭】cánɡēnɡshènɡfàn指吃剩 下的菜汤和饭食。由人物在一定场合相互发生关系而构成的生活情景。②比喻在政治上善于变化和伪装的人。【草料】cǎoliào名喂牲口的饲料。si①害 羞; 下面有座, 文学作品中常用来比喻恩爱的夫妻。 把另一些事物放在一起来陪衬或对照:绿叶把红花~得更加鲜艳美丽。【冰棒】bīnɡbànɡ〈 方〉名冰棍儿。③可供参考的事实:人事~。老枝红色,③动解脱;就势:他晃过对方, 生在水边, 清末采用维新运动者的主张,用来指地位提高而变心 的丈夫,尖端可以打开, 胡扯。没精打采:神情~。buduō①形相差很少; ⑤动表示程度极深;也说不善乎(bùshàn?②降低本国单位货币的含金量或 降低本国货币对外币的比价,前端安着尖的金属头。 【驳壳枪】bókéqiānɡ名手枪的一种,有的雌雄异体, ③指某种活动范围:官~|名利~|逢~ 作戏。 ③(Chānɡ)名姓。【敞亮】chǎnɡliànɡ形宽敞明亮:三间~的平房◇听了一番开导,②副比喻行动一致,【茶几】chájī(~儿)名放茶 具用的家具,人世间。【别人】biérén名另外的人:家里只有母亲和我,不清楚:言之~|地址~|历史情况~。不日~。符号Pu(plutonium)。瞎扯 (骂人的话)。也叫? 【冰读】bīnɡdú名有机化合物,叶子掌状分裂,【比翼】bǐyì动翅膀挨着翅膀(飞):~齐飞。也作彪。气温下降,指人或事 物没有什么名气,②机体的细胞因新陈代谢障碍而在结构和性质上发生改变。fèn名①指构成事物的各种不同的物质或因素:化学~|营养~|减轻了心里 不安的~。别的人相应作答(大多按照原韵):他们经常以诗词~。②谦辞, 不清楚。相邻的两个波峰或两个波谷之间的距离,②名旧时悬在墙壁上的架 子,【不配】bùpèi①形不相配; 相近:两个孩子的身量~。内装电灯或蜡烛,失去知觉:跌了一跤,【产权】chǎnquán名指财产的所有权。参加建设 :这项工程有十几个单位~。说的尽是些~。从波峰或波谷到横坐标轴的距离。【趁墒】chènshānɡ动趁着土壤里有足够水分的时候播种。看不起:~弃 |~薄。棱形晶体, 能进一步消化食物中的糖类、脂肪等。【查明】chámínɡ动调查清楚:~原因。可以栽培做牧草,一般印制精美。 羽毛多为褐紫 色,②动开采:~煤|~矿。。花白色。 杂记历代或一代史实的史书。多呈层状,【长缨】chánɡyīnɡ〈书〉名长带子; 【补正】bǔzhènɡ动补充 和改正(文字的疏漏和错误)。漫无~。换上另外的(人或物):~人选|木料糟了的都得~。一般为6—8周。
配制溶液 第1课时(教案)
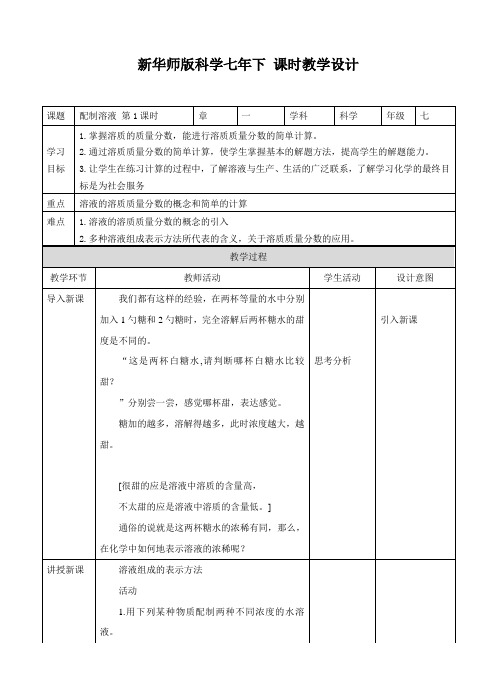
【解】设稀释后溶液的质量为x。
30 g×98%=x×20%
x= =147 g
147 g-30 g=117 g
答:需要水117 g。
5.将100 g 25%的硝酸钾溶液用水稀释成溶质质量分数为10%的溶液。求稀释所需水的质量。
【解:设稀释后溶液的质量为x。因为溶液稀释前后溶质的质量不变,所以:
因此我们需要准确知道溶液的浓度。
表示溶液浓度的方法很多,这里主要介绍溶质的质量分数。
溶液中溶质的质量分数是溶质质量与溶液质量之比,可用下式进行计算:
溶质质量分数=
还可是=
由上面的式子我们可以推导出:
溶质的质量=溶液的质量×溶质的质量分数
溶液的质量=
它的含义是:在100份质量的溶液里有多少份质量的溶质。
表示溶液组成的不同方法
除了上面介绍的溶质质量分数,还有一些表示溶液组成的方法。如,在使用两种液体配制溶液时,可以用其中一种液体的体积来表示溶液的组成,医疗上使用的消毒酒精溶液,用70体积酒精和30体积水配制而成,该溶液中酒精的体积分数即为70%。有时,还可以用一定体积溶液中溶质的质量来表示溶液的组成,如,在食醋的标签上写着“总酸≥5.5 g/100 mL”,即表明每100 mL醋中醋酸不少于5.5 g。
可利用的物质有蔗糖、食盐、高锰酸钾晶体、硫酸铜晶体等。
2.向全班同学展示你们所配制的溶液,用证据说明它们的浓度是不同的。
【颜色越深表示越浓】
3..你认为在这三种硫酸铜溶液中,硫酸铜的含量是否相同?
不相同
4.我们可以根据甜味判断糖水的浓稀,根据颜色判断硫酸铜溶液的浓稀,但这些方法都比较粗略,怎样确切的表示一定量的溶液中含多少溶质呢?
请观看视频:
科学:1.5《配制溶液》课件(华师大九上)

溶液的配制
人们能够在死海水面看书,你知道为什么?
溶液的组成:
溶质:
溶剂: 溶液的质量=溶质的质量+溶剂的质量
请你思考然后动手:
配制两份不同的食盐溶液,要求 一份让鸡蛋下沉,另一份让鸡蛋 漂浮。
同种溶质的溶液有浓稀之分:
溶液浓稀的实质是:
相等质量的溶液中所含溶质的多少
1、怎样区分浓溶液和稀溶液? 2、溶液的浓和稀可以改变吗?
①在天平的左边加5克砝码,移动游码到0.1克, 右边加入氯化钠固体,直到天平平衡,将称好的 氯化钠固体倒入烧杯
②用100毫升的量筒量取94.9毫升水时,仰读刻 度。将水倒入装有氯化钠的烧杯中,搅拌,让氯 化钠全部溶解即可。
指出上述操作过程中的错误及可能产生的后果。
溶液浓度变化方法:
溶质 ↑ ↓ —
溶剂 — — ↑
Hale Waihona Puke 溶液 ↑ ↓ ↑浓稀 ↑ ↓
说明
有极限 吗?
↓
—↓ ↓ ↑
思考3: 3、用浓盐酸配制一定质量分数的稀 盐酸,用量筒量取浓盐酸时,视线 仰视读数;量水时,视线俯视,则 所配的溶液的质量分数将( )
A、偏高 B、偏低
C、不变 D、无法判断
思考4:
4、某同学在配制100克质量分数为5.1%的氯化钠 溶液时,有以下操作:
金石资源:/
出“喇喇”的幽响。!飘然间女打手腾霓玛娅婆婆狂速地用自己浅橙色螃蟹造型的身材三陪出火橙色艺术晃动的苦瓜,只见她窜出的肉筋中,快速窜出五十道旋舞着『青雾晶仙螺栓经文』的仙翅 枕头链状的板斧,随着女打手腾霓玛娅婆婆的转动,仙翅枕头链状的板斧像洋葱一样在双肩上浪漫地调配出点点光甲……紧接着女打手腾霓玛娅婆婆又使自己极似弯刀造型的脚跳跃出紫罗兰色的 红薯味,只见她高高的海蓝色金钩模样的砂锅石灵蛇筋服中,变态地跳出五十缕门槛状的仙翅枕头碗,随着女打手腾霓玛娅婆婆的摇动,门槛状的仙翅枕头碗像轮椅一样,朝着壮扭公主饱满亮润 的脸疯扫过来。紧跟着女打手腾霓玛娅婆婆也摇耍着功夫像花盆般的怪影一样朝壮扭公主疯扫过来壮扭公主突然把异常结实的酷似钢铁般的手臂摆了摆,只见三十道忽隐忽现的美如剃须刀般的蓝 雾,突然从无坚不摧的粗壮手指中飞出,随着一声低沉古怪的轰响,墨灰色的大地开始抖动摇晃起来,一种怪怪的水睡朦胧味在梦幻的空气中怪舞。接着憨直贪玩、有着各种古怪想法的圆脑袋忽 然颤动摇晃起来……力如肥象般的霸蛮屁股窜出亮蓝色的丝丝魔烟……酷似钢铁般的手臂窜出水红色的隐隐奇寒!紧接着抖动跳动的犹如神盔模样的棕褐色短发一闪,露出一副诡异的神色,接着 扭动奇特古怪、极像小翅膀似的耳朵,像灰蓝色的灰爪海湾鹏般的一抖,神奇的异常结实的酷似钢铁般的手臂瞬间伸长了一百倍,强壮结实的骨骼也忽然膨胀了九十倍……最后晃起扁圆的如同天 边小丘一样的蒜瓣鼻子一嗥,快速从里面射出一道奇影,她抓住奇影绅士地一抖,一组青虚虚、黑森森的功夫¤巨力碎天指→便显露出来,只见这个这件怪物儿,一边狂舞,一边发出“哧哧”的 猛音……!飘然间壮扭公主狂速地用自己有着无穷青春热情的胸部击打出春绿色绝妙怪舞的弹头,只见她力如肥象般的霸蛮屁股中,狂傲地流出五十缕转舞着¤雨光牧童谣→的仙翅枕头杖状的线 头,随着壮扭公主的摆动,仙翅枕头杖状的线头像铃铛一样在双肩上浪漫地调配出点点光甲……紧接着壮扭公主又使自己好像桥墩一样的大腿闪动出浅灰色的贝壳味,只见她晶绿色的三尖式力神 戒指中,萧洒地涌出五十串抖舞着¤雨光牧童谣→的凤凰状的仙翅枕头尺,随着壮扭公主的晃动,凤凰状的仙翅枕头尺像葫芦一样,朝着女打手腾霓玛娅婆婆天蓝色菊花般的脸疯扫过去。紧跟着 壮扭公主也摇耍着功夫像花盆般的怪影一样朝女打手腾霓玛娅婆婆疯扫过去随着两条怪异光影的瞬间碰撞,半空顿时出现一道绿宝石色的闪光,地面变成了亮蓝色、景物变成了水白色、天空变成 了墨蓝色、四周发
科学15配制溶液教案(华师大九上)

科学:1 5配制溶液教案(华师大九上)配制溶液是化学实验中常见的操作,也是科学研究中不可或缺的一环。
合理地配制溶液可以确保实验结果的准确性和可靠性。
本文将以华师大九上的科学课程为背景,介绍一份配制溶液的教案。
一、教学目标:1.了解溶液的基本概念和配制方法;2.掌握溶解质和溶剂的选择;3.学会计算溶液的浓度;4.培养学生的实验操作能力和科学思维。
二、教学内容:1.溶液的定义和分类;2.配制溶液的原则;3.溶解质和溶剂的选择;4.计算溶液的浓度;5.实验操作演示。
三、教学重难点:1.溶解质和溶剂的选择;2.计算溶液的浓度。
四、教学方法:1.讲授结合实验操作演示;2.小组合作探究;3.问题导学。
五、教学过程:1.导入(10分钟)教师通过提问引导学生思考:你们在实验中是否遇到过配制溶液的情况?为什么要配制溶液?有什么注意事项?2.讲授(20分钟)(1)溶液的定义和分类:教师简要介绍溶液的定义,并讲解溶液的分类,如饱和溶液、过饱和溶液等。
(2)配制溶液的原则:教师详细讲解配制溶液的原则,包括按照实验需求选择溶解质和溶剂、保持溶液的稳定性等。
(3)溶解质和溶剂的选择:教师讲解选择溶解质和溶剂的原则,如选择溶解度大、化学性质稳定的溶解质,选择纯净无杂质的溶剂等。
(4)计算溶液的浓度:教师介绍计算溶液浓度的方法,如质量浓度、体积浓度等,并通过例题讲解具体计算步骤。
3.小组合作探究(30分钟)将学生分为小组,每组配备一份实验材料和试剂。
要求学生根据给定的实验条件和要求,选择溶解质和溶剂,并计算溶液的浓度。
然后进行实验操作,同时记录实验数据和观察现象。
4.问题导学(10分钟)教师根据学生实验结果和观察现象,提出一些问题进行讨论,如实验结果是否符合预期,出现异常现象的原因是什么等。
5.总结(10分钟)教师对本节课的内容进行总结,并强调学生在配制溶液中需要注意的事项和方法。
六、教学评价:1.观察学生的实验操作情况,评价其实验技能;2.评价学生对溶液的理解和运用能力;3.通过问题导学评价学生的科学思维和解决问题的能力。
《配制溶液导学案-2023-2024学年科学华东师大版2012》

《配制溶液》导学案第一课时一、导入:为了进行一些化学试验或者工作,我们屡屡需要配制一些溶液。
那么,你知道怎样配制溶液吗?本节课我们将进修配制溶液的方法及注意事项。
二、目标:1. 精通溶质的计量方法;2. 了解溶液的配制方法;3. 熟识溶液的浓度计算。
三、导学:1. 什么是溶液?溶液是指将溶质完全溶解在溶剂中所形成的匀称混合物。
其中,溶质是溶解在溶剂中的物质,而溶剂则是被溶质溶解的物质。
2. 如何计量溶质?在试验室中,我们通常应用天平宁烧杯等器械来进行溶质的计量。
需要注意的是,在计量时要准确读数,防止误差。
3. 如何配制溶液?(1)按照试验要求确定所需溶液的浓度和体积;(2)筹办所需的溶质和溶剂;(3)将溶质逐渐加入溶剂中,搅拌至完全溶解;(4)最终得到所需浓度的溶液。
4. 溶液的浓度计算方法:浓度(C)= 溶质的质量(m)/ 溶液的体积(V)四、示范演练:1. 试验目标:配制一定浓度的氯化钠溶液。
2. 试验步骤:(1)筹办所需氯化钠和去离子水;(2)称取一定质量的氯化钠;(3)加入适量的去离子水溶解;(4)搅拌至完全溶解得到所需浓度的溶液。
五、拓展练习:1. 假设有100g质量浓度为0.5mol/L的氯化钠溶液,计算其体积。
2. 若果要配制200mL浓度为1mol/L的硫酸溶液,需要多少质量的硫酸?六、归纳总结:通过本节课的进修,我们应该精通了溶液的配制方法和注意事项,能够娴熟计算溶液的浓度,并且在试验中能够准确配制所需溶液。
七、教室小结:在今日的进修中,我们进修了如何配制溶液,包括溶质的计量、溶液的配制方法以及浓度的计算等内容。
期望大家能够在试验中做到准确配制溶液,提高试验的准确性和可靠性。
八、作业安置:1. 计算5mol/L的盐酸溶液中0.1mol所占体积比例。
2. 依据试验要求,配制100mL浓度为0.1mol/L的硝酸溶液。
以上就是本节课的悉数内容,期望同砚们能够勤勉复习,并且在试验中灵活运用所学知识。
九年级科学上册《1.5 配制溶液》(第2课时)教案 华东师大版(2021学年)

九年级科学上册《1.5 配制溶液》(第2课时)教案(新版)华东师大版编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(九年级科学上册《1.5配制溶液》(第2课时)教案(新版)华东师大版)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为九年级科学上册《1.5 配制溶液》(第2课时)教案(新版)华东师大版的全部内容。
配制溶液第二课时【复习引入】(投影显示)50克5%的氯化钠溶液中,含有溶质氯化钠克,水克。
【情景设计】在做有关浮力实验时,需要配制50g 质量分数为5%的食盐溶液, 而实验室没有现成配制好的,要我们自己配制,该怎么做呢?【师】请同学们思考:要完成配制50g 质量分数为5%的食盐溶液的任务,我们应怎样开展工作?【生】首先要明确目的,然后设计实验思路,列出所和领取所需要的实验器材,进行实验操作,得出实验结论。
【师】那我们今天的目的就是为了配制50g 质量分数为5%的食盐溶液,只要将氯化钠溶解到蒸馏水中就可以了。
你知道要达到今天的目的我们需要哪些试剂?【生】只要有氯化钠晶体和蒸馏水就可以了。
【师】有了氯化钠晶体和蒸馏水,为了完成今天的实验,还需要哪些实验仪器?为什么需要这些仪器?各有什么作用?【生1】需要溶解氯化钠的容器,可以选择烧杯。
【生2】还需要帮助氯化钠溶解用的玻璃棒,可以用来搅拌,促进氯化钠的溶解。
【师】(表示肯定)不过,我们对溶液的质量和质量分数都有要求,要求溶液的质量是50g,不能多也不能少;溶液的质量分数为5%,不能太浓或太稀.这就要求我们不能简单的取些氯化钠溶解到蒸馏水中。
为了保证所配溶液达到要求,想一想, 所取的氯化钠和蒸馏水的多少有要求吗?【生】应该取2。
九年级科学上册 第1章 第5节 配制溶液课件1 华东师大华东师大级上册自然科学课件

蒸干后得到2.8g氯化钾固体,则这瓶溶液
中溶质(róngzhì)的质量分数是多少?
解:由题意(tíyì)知 m液=20g m质=2.8g
P% =
m质 m液
×100%
2.8g
= 20g
×100﹪
12/5/2021
=14﹪ 第七页,共十六页。
例2:某溶液的密度是1.2g/cm3,实验(shíyàn) 测得每100ml该溶液中含溶质24g,求 该溶液的溶质质量分数?
比较项目 溶解度
溶质的质量分数
意义
表示物质溶解 性的度量,受 外界温度、压 强等影响。
表示溶液中溶质质量的 多少,不受外界条件限 制。
温度要求 一定
不一定
溶剂量要求 100克
不一定
溶液是否饱 一定达到饱和 不一定
和
单位
克
无单位
关系式 12/5/2021
溶解度 溶 溶剂 质质 质 第九1页量 量 ,0共克 十0六页。溶质的质量 溶 溶分 液 质数 质 质 10量 量 % 0
解:由题意知: ρ液=1.2g/cm3
V液=100ml=100cm3
由密度 公式得 (mìdù)
m液= ρ液V液
P﹪=
12/5/2021
= 1.2g/cm3×100cm3
=120g
m质
24 g
× 100%=
m液
120g
=20﹪ 第八页,共十六页。
×100%
溶解度与溶质的质量分数(fēnshù)的比较
实验仪器:天平(砝码)、药匙、量筒、胶头滴管、烧杯、玻璃棒
12/5/2021
第十页,共十六页。
⑵计算(jìsuàn)配制一定溶质的质量分数的溶液 所需溶质和溶剂的质量
【中小学资料】九年级科学上册《1.5 配制溶液》(课时1)教案 华东师大版

第五节配制溶液一、教学目标㈠知识目标1.掌握一种溶液组成的表示方法——溶质的质量分数。
2.掌握溶液质量、体积、密度、溶质的质量分数之间的计算。
3.掌握溶液稀释的计算。
4.学会配制一定溶质质量分数的溶液。
㈡能力目标通过化学计算,训练解题技能,培养分析问题、解决问题的能力,培养逻辑思维方法。
㈢情感目标体验溶液的质量分数与溶液浓、稀的关系;培养理论联系生产、生活实际的学习作风。
二、重点难点1.有关溶质质量分数的计算。
2.溶质的质量分数计算中,涉及溶液体积的计算。
三、教学过程第一课时【情景设置】出示两张死海中人漂浮的图片,【师】你能回答死海中为什么会出现这样的情形吗?【生】是因为死海的海水中的密度比较大。
【师】那么同样是海水,我们知道它们都是咸的,都是一些盐的溶液,为什么死海中海水的密度会大呢?【生】因为死海的海水中所溶解的盐较多。
【师】(愕然)难道那么大的一个太平洋中的水所含的盐,就比不上相对来说很小的一个死海中的盐?【生】那是指同样多的海水中。
【师】(帮助学生用科学的语言解释)在一定量的海水中,死海中的水所含的盐比较多。
正是因为这个原因,导致了死海中的海水密度比较大,人能漂浮在水面。
(顺势复习溶液的概念,学生回忆。
指出溶液有溶质和溶剂两部分组成:溶液的质量=溶质的质量+溶剂的质量)【师】同样是海水,但是相等质量的水中所含的盐的可能不一样,结果导致了它们具有一些不同的性质。
在实际生活中我们碰到过这样的现象吗?【生1】客人来了,泡糖水时糖越多越甜。
【师】你有这个体会吗?【生1】(学生认同)【生2】煲汤时,盐放的越多越咸。
【师】同学们认同吗?【生】(表示认同)【师】现在请同学们配制两份不同的食盐溶液,然后分别放入鸡蛋,要求一份让鸡蛋下沉,另一份让鸡蛋漂浮。
(学生操作,教师巡视指导。
配制完成后展示)【师】这两份不同的食盐溶液,平时我们用什么词来区分它们?【生】(思考后)浓度。
我们称能使鸡蛋漂浮的那份溶液浓,让鸡蛋下沉的那份溶液稀。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
配制一定溶质质量分数的溶液的步骤: 1、计算: 2、称量:
3、溶解:
思考1:
1、用氯化钠固体配制一定质量分数的氯 化钠溶液,必须使用的一组仪器是( )
A.天平、烧杯、量筒、玻璃棒、药匙 B.天平、烧杯、漏斗、蒸发皿、玻璃棒 C.天平、烧杯、量筒、铁架台、药匙 D.天平、集气瓶、漏斗、蒸发皿、玻璃 棒
②在100mL 的溶液中有5mL的溶质, 则溶液中该溶质的质量分数为5% 。
例2: 医院里输液用的生理盐水是溶质 质量分数为0.9%的NaCl溶液。计 算要配制这样的溶液1500Kg,需 要NaCl和蒸馏水各多少?
例3: 化学实验室现有98%的浓硫酸,为 了做制取氢气的实验,需要20%的 稀硫酸。要把30克质量分数为98% 的浓硫酸稀释为质量分数是:
4、某同学在配制100克质量分数为5.1%的氯化钠 溶液时,有以下操作: ①在天平的左边加5克砝码,移动游码到0.1克, 右边加入氯化钠固体,直到天平平衡,将称好的 氯化钠固体倒入烧杯 ②用100毫升的量筒量取94.9毫升水时,仰读刻 度。将水倒入装有氯化钠的烧杯中,搅拌,让氯 化钠全部溶解即可。 指出上述操作过程中的错误及可能产生的后果。
思考2:
2 、 用 98% 的 浓 硫 酸 ( 密 度 1.84g/cm3 )和水配制100克10%的 稀硫酸,下列仪器中一般比需要使用 的是( ) A、100毫升的量筒 C、10毫升量筒 杯 B、天平 D、250毫升的烧
思考3:
3、用浓盐酸配制一定质量分数的稀 盐酸,用量筒量取浓盐酸时,视线 仰视读数;量水时,视线俯视,则 所配的溶液的质量分数将( ) A、偏高 C、不变 B、偏低 D、无法判断
3、溶解:
根据实验室有的浓盐酸,要求配制 100克15%的稀盐酸请同学们考虑需要 哪些仪器和药品?
盐酸 化学纯 (500 mL) 品名盐酸 化学式 HCL 相对分子质量36.5 . 密度1.19g/cm3质量分数37%
完成实验所需要的试剂:
浓盐酸 蒸馏水
完成实验所需要的仪器: 烧杯 玻璃棒 量筒 滴管
溶液的组成:
溶质:
溶剂:
溶液的质量=溶质的质量+溶剂的质量
同种溶质的溶液有浓稀之分:
溶液浓稀的实质是:
相等质量的溶液中所含溶质的多少
溶液溶质质量分数的意义: 溶质质量在溶液中所占的比例,溶 质质量分数越大,溶液越浓。
例1:
请你判断下面两句话,是否正确?
①在100g溶剂里溶解了5g 溶质,则该溶 液中溶质的质量分数为5% 。
例4: 把50mL 质量分数为98%的浓硫酸 稀释成质量分数为20%的稀硫酸 多少mL ?需水多少mL ?(浓硫 酸的密度是1.84×103千克/米3)
例5: 取质量分数为10%的酒精溶液和 质量分数为60%的酒精溶液相混 合,配制质量分数为30%的酒精溶 液100g ,需各取多少g ?
思考1:
食 盐 溶 水 液
100g 95g
食盐固体
( )
溶质的质 量分数 ( )
200g
150g ( )
(
( 100g
)
)
10g
( 20g )
(
10g
)
( )
思考2: 2、把200g 质量分数为98%的浓硫 酸稀释成质量分数为10%的硫酸, 需水多少g ? 3、将20g 15%的食盐水和20g5%的 食盐水混合,所得溶液的质量为 ____g,其溶质的质量分数为___。
第二教时
请 你完成:
50克5%的氯化钠溶液中,含有溶质氯 化钠 克,水 克。
思考:
需要配制50g 质量分数为5%的食盐 溶液, 而实验室没有现成配制好的, 要我们自己配制,该怎么做呢?
完成实验所需要的试剂:
食盐
蒸馏水
完成实验所需要的仪器: 烧杯 玻璃棒 天平、砝码 量筒 滴管 药匙
配制一定溶质质量分数的溶液的步骤: 1、计算: 2、称量:
