最新(四)竞赛专项练习题之晶体结构
晶体结构考试(含答案)

晶体结构考试(含答案)高中化学竞赛专题考试——晶体结构 1.008Zr Nb Mo T c Ru Rh Pd Ag Cd In S n S b T e I Hf T a W Re Os Ir Pt Au Hg T l Pb Bi Po At Ac-Lr H Li Be B C N O F Na Mg Al S i P Cl S K Ca S c T i V Cr Mn Fe Co Ni Cu Zn G a G e As S e Br Rb Cs Fr S r Ba Ra Y La Lu -6.9419.01222.9924.3139.1040.0885.4787.62132.9137.3[223][226]44.9647.8850.9452.0054.9455.8558.9363.5558.6965.3910.8126.9869.7212.0128.0972.61114.8204.4118.7207.2112.4200.6107.9197.0106.4195.1102.9192.2101.1190.298.91186.295.94183.992.91180.991.22178.588.9114.0116.0019.0030.9774.92121.8209.032.0778.96127.6[210][210][210]126.979.9035.454.00320.1839.9583.80131.3[222]He Ne Ar Kr Xe Rn 相对原子质量Rf Db Sg Bh Hs Mt一 选择题(每题有一个或者两个正确选项,每题2分,共20分。
)1、下列各组物质汽化或熔化时,所克服的微粒间的作用力,属于同种类型的是( )A .碘和干冰的升华B .二氧化硅和生石灰的熔化C .氯化钠晶体和铁的熔化D .冰的融化和烧碱的熔化 2、在结构中,表示成SiO 4,则该结构式的通式为 ( )A. (Si 2O 5)n 2n-B. (SiO 3)n 2n-C. (Si 6O 17)n 10n-D. (Si 6O 19)n 14n-3、某钾(·)的石墨嵌入化合物沿c 轴的投影图如图,该化合物的化学式为 ( )A.KC 12B. KC 10C. KC 8D. KC 64、下面二维平面晶体所表示的化学式为AX3的是()A BC D5.下面图像是从NaCl或CsCl晶体结构图中分割出来的部分结构图,试判断属于NaCl晶体结构的是①②③④A 图①B 图②C 图③D 图④6 非整数比化合物Fe0.95O具有NaCl型晶体结构,由于n (Fe)∶n(O)<1∶1,所以晶体存在缺陷。
竞赛习题-晶体结构题
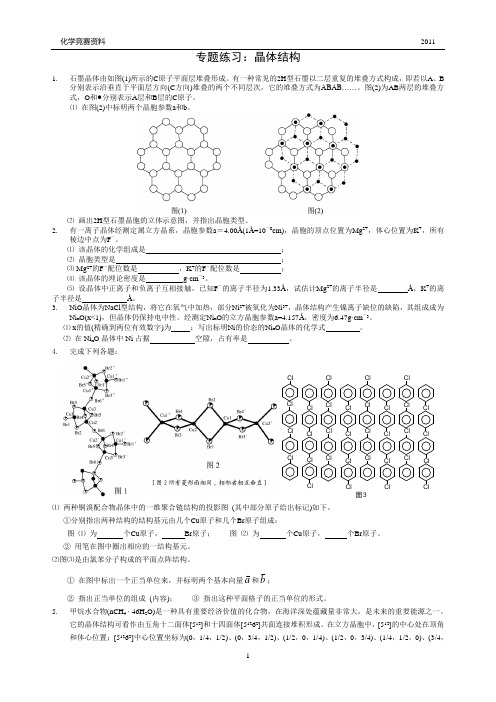
专题练习:晶体结构1. 石墨晶体由如图(1)所示的C 原子平面层堆叠形成。
有一种常见的2H 型石墨以二层重复的堆叠方式构成,即若以A 、B分别表示沿垂直于平面层方向(C 方向)堆叠的两个不同层次,它的堆叠方式为ABAB……。
图(2)为AB 两层的堆叠方式,O 和●分别表示A 层和B 层的C 原子。
⑴ 在图(2)中标明两个晶胞参数a 和b 。
⑵ 画出2H 型石墨晶胞的立体示意图,并指出晶胞类型。
2. 有一离子晶体经测定属立方晶系,晶胞参数a =4.00Å(1Å=10-8cm),晶胞的顶点位置为Mg 2+,体心位置为K +,所有棱边中点为F -。
⑴ 该晶体的化学组成是 ;⑵ 晶胞类型是 ;⑶ Mg 2+的F -配位数是 ,K +的F -配位数是 ;⑷ 该晶体的理论密度是 g·cm -3。
⑸ 设晶体中正离子和负离子互相接触,已知F -的离子半径为1.33Å,试估计Mg2+的离子半径是 Å,K +的离子半径是 Å。
3. NiO 晶体为NaCl 型结构,将它在氧气中加热,部分Ni 2+被氧化为Ni 3+,晶体结构产生镍离子缺位的缺陷,其组成成为Ni x O(x<1),但晶体仍保持电中性。
经测定Ni x O 的立方晶胞参数a=4.157Å,密度为6.47g·cm -3。
⑴ x 的值(精确到两位有效数字)为 ;写出标明Ni 的价态的Ni x O 晶体的化学式 。
⑵ 在Ni x O 晶体中Ni 占据 空隙,占有率是 。
4. 完成下列各题: Cl Cl Cl Cl Cl Cl Cl ClCl Cl Cl Cl Cl Cl Cl ClCl Cl Cl Cl Cl Cl Cl ClCl Cl Cl ClCl Cl Cl Cl 图3⑴ 两种铜溴配合物晶体中的一维聚合链结构的投影图 (其中部分原子给出标记)如下。
①分别指出两种结构的结构基元由几个Cu 原子和几个Br 原子组成:图 ⑴ 为 个Cu 原子, Br 原子; 图 ⑵ 为 个Cu 原子, 个Br 原子。
化学竞赛晶体结构综合例题
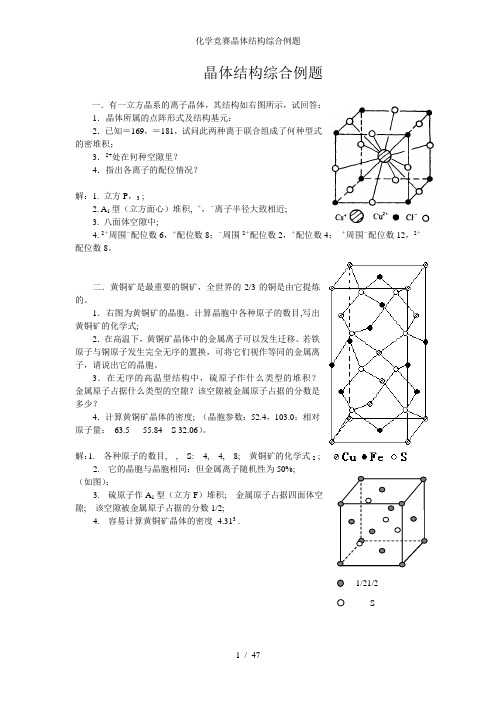
晶体结构综合例题一.有一立方晶系的离子晶体,其结构如右图所示,试回答:1.晶体所属的点阵形式及结构基元;2.已知=169,=181,试问此两种离于联合组成了何种型式的密堆积;3.2+处在何种空隙里?4.指出各离子的配位情况?解:1. 立方P,3 ;2. A1型(立方面心)堆积, +,-离子半径大致相近;3. 八面体空隙中;4. 2+周围-配位数6,+配位数8;-周围2+配位数2,+配位数4;+周围-配位数12,2+配位数8。
二.黄铜矿是最重要的铜矿,全世界的2/3的铜是由它提炼的。
1.右图为黄铜矿的晶胞。
计算晶胞中各种原子的数目,写出黄铜矿的化学式;2.在高温下,黄铜矿晶体中的金属离子可以发生迁移。
若铁原子与铜原子发生完全无序的置换,可将它们视作等同的金属离子,请说出它的晶胞。
3.在无序的高温型结构中,硫原子作什么类型的堆积?金属原子占据什么类型的空隙?该空隙被金属原子占据的分数是多少?4.计算黄铜矿晶体的密度; (晶胞参数:52.4,103.0;相对原子量:63.5 55.84 S 32.06)。
解:1. 各种原子的数目, , S: 4, 4, 8; 黄铜矿的化学式2 ;2.它的晶胞与晶胞相同;但金属离子随机性为50%;(如图);3.硫原子作A1型(立方F)堆积; 金属原子占据四面体空隙; 该空隙被金属原子占据的分数1/2;4.容易计算黄铜矿晶体的密度4.313 .1/21/2S三.冰晶石(36)用作电解法炼铝的助熔剂。
冰晶石晶胞是以大阴离子(63-)构成的面心立方晶格,+可看作是填充在晶格的空隙中,已知冰晶石的密度为2.953,—F 键长181 ,相对原子质量: 23.0; 27.0;F 19.0。
1.指出63-配离子中心离子的杂化轨道类型、配离子空间构型和所属分子点群。
2.指出36的点阵形式;阴离子作何种形式的堆积,阳离子占据何种空隙及占有率;写出它们的分数坐标。
3.计算冰晶石晶体的晶胞参数。
中学化学竞赛《晶体结构》测试题

中学化学竞赛《晶体结构》测试题晶体结构测试题(ⅰ)姓名___________1、建有一ab型晶体,晶胞参数就是a=b=3.98?,c=3.72?,α=β=γ=90°,一个晶胞中存有两个a,其座标就是(0,0,0),(?,?,0),未知晶胞中一个b的座标就是(0,?,?)。
①该晶体属什么晶系?②属什么格子?③一个晶胞中所含几个b?晶胞中另外一些b原子的座标若想确认,写下其座标,若无法确认,表明其理由。
2、铜有一种氧化物,其晶胞结构可描述如下:a原子占据立方体的顶点及体心;而在每间隔一个小立方体的中心处放上一个b原子。
①说明a与b各代表什么原子,并写出该氧化物的分子式。
②该晶体的晶格型式为何?结构基元是什么?一个晶胞中有几个结构基元?③cu原子和氧原子的配位数各是多少?④已知晶胞参数a=4.26?,计数cu原子之间,o原子之间及铜氧原子之间的最短距离。
3、金属钋晶体就是直观立方晶格结构,按密切沉积原理,排序晶体中空隙体积的百分数。
4、在caf2和六方zns晶体中,正离子占有什么空隙?正离子占有空隙的百分率为多少?5、某黄铜中cu和zn的摩尔分数分别是0.75和0.25,该合金的结构跟纯铜相同(立方最紧密堆积),只是zn原子统计地无序取代了cu原子。
在每一原子的位置上,cu和zn的占有率正比于合金的组成,即合金可以看作是由cu0.75zn0.25组成的。
已知合金的密度为8.51g/cm3,计算合金的统计原子半径。
(相对原子质量:cu63.5zn65.4)(第26届icho竞赛试题)6、建有一ab4型晶体,属于立方晶系,每个晶胞中存有一个a和四个b,一个a的座标就是(?,?,?),四个b原子的座标分别就是(0,0,0),(?,?,0),(?,0,?),(0,?,?),此晶体的晶格型式为何?7、每一立方晶系晶体,晶胞的顶点位置全为a占据,面心为b占据,体心为原子c占据。
①写出此晶体的化学组成;②用分数坐标写出诸原子在晶胞中的位置;③给出晶体的晶格型式。
化学竞赛晶体结构综合例题

晶体结构综合例题一.有一立方晶系的离子晶体,其结构如右图所示,试回答:1.晶体所属的点阵形式及结构基元;2.已知r Cs+=169pm,r Cl-=181pm,试问此两种离于联合组成了何种型式的密堆积;3.Cu2+处在何种空隙里?4.指出各离子的配位情况?解:1. 立方P,CaCsCl3 ;2. A1型(立方面心)堆积, Cs+,Cl-离子半径大致相近;3. 八面体空隙中;4. Cu2+周围Cl-配位数6,Cs+配位数8;Cl-周围Cu2+配位数2,Cs+配位数4; Cs+周围Cl-配位数12,Cu2+配位数8。
二.黄铜矿是最重要的铜矿,全世界的2/3的铜是由它提炼的。
1.右图为黄铜矿的晶胞。
计算晶胞中各种原子的数目,写出黄铜矿的化学式;2.在高温下,黄铜矿晶体中的金属离子可以发生迁移。
若铁原子与铜原子发生完全无序的置换,可将它们视作等同的金属离子,请说出它的晶胞。
3.在无序的高温型结构中,硫原子作什么类型的堆积?金属原子占据什么类型的空隙?该空隙被金属原子占据的分数是多少?4.计算黄铜矿晶体的密度; (晶胞参数:a=52.4pm,c=103.0pm;相对原子量:Cu 63.5 Fe 55.84 S 32.06)。
解:1. 各种原子的数目Cu, Fe, S: 4, 4, 8; 黄铜矿的化学式CuFeS2 ;2.它的晶胞与ZnS晶胞相同;但金属离子随机性为50%;(如图);3.硫原子作A1型(立方F)堆积; 金属原子占据四面体空隙; 该空隙被金属原子占据的分数1/2;4.容易计算黄铜矿晶体的密度 4.31g/cm3 .1/2Cu+1/2FeS三.冰晶石(Na 3AlF 6)用作电解法炼铝的助熔剂。
冰晶石晶胞是以大阴离子(AlF 63-)构成的面心立方晶格,Na +可看作是填充在晶格的空隙中,已知冰晶石的密度为2.95g/cm 3,Al —F 键长181 pm ,相对原子质量:Na 23.0;Al 27.0;F 19.0。
竞赛专项练习题之晶体结构

(四)晶体结构一、(2005)(12分)LiCl和KCl同属NaCl型晶体,其熔点分别为614℃和776℃。
Li+、K+和Cl-的半径分别为76pm、133pm和181pm。
在电解熔盐LiCl 以制取金属锂的生产工艺中,加入适量的KCl晶体,可使电解槽温度下降至400℃,从而使生产条件得以改善。
1.说明加入熔点高的KCl反而使电解温度大大下降的原因;2.有人认为,LiCl和KCl可形成固溶体(并画出了“固溶体的晶胞”)。
但实验表明,液相LiCl和KCl能以任意比例混溶而它们的固相完全不混溶(即不能生成固溶体!)。
请解释在固相中完全不混溶的主要原因。
3.写出计算LiCl和KCl两种晶体密度之比的表达式(须包含离子半径的符号);4.在KCl晶体中,K+离子占据由Cl- 离子围成的八面体空隙,计算相距最近的八面体空隙中心之间的距离。
5.实验证明,即使产生了阳离子空位,KCl晶体在室温下也不导电。
请通过计算加以说明。
二、(2005)(12分)为纪念1905年爱因斯坦连续发表6篇论文导致物理学大变革100周年,今年被定为国际物理年。
本题涉及的“热电效应”机理也是爱因斯坦首先阐释的,即他提出的被后人称为“爱因斯坦振荡器”的独立振荡原子与温度关系的模型。
1.左上图是热电效应之一的图解。
给出图中所有英文单词(或词组)及物理学符号的意义,并为此图写一篇不超过200字(包括标点符号等)的说明文。
2.右上图是化学家合成的能实现热电效应的一种晶体的晶胞模型。
图中的大原子是稀土原子,如镧;小原子是周期系第五主族元素,如锑;中等大小的原子是周期系VIII 族元素,如铁。
按如上结构图写出这种热电晶体的化学式。
给出计算过程。
提示:晶胞的6个面的原子数相同。
设晶体中锑的氧化态为-1,镧的氧化态为+3,问:铁的平均氧化态多大?三、(2005B)(10分)固体发光材料是一种能将激发的能量转变为可见光的固体物质。
在基质中掺入杂质,含量可达千分之几或百分之几,可调整发光效率、余辉及发光光谱。
全国高中化学竞赛教练员习题答案晶体结构

五、晶 体 结 构1. 因为立方晶系中,六个面都是等价的,若有底心立方晶胞存在,则必有面心立方晶胞存在,故立方晶系中不存在底心立方晶胞。
不带电荷的分子或原子(金属)之间的相互作用力小,若原子(非金属)以共价键连接,简单立方中的两个原子之间距离又太大,不利于共价键形成,所以不带电荷的分子或原子往往采取六方或立方最紧密堆积或立方体心密堆积结构。
由于六方最紧密堆积结构与立方紧密堆积的空间利用率相同,所以它们具有相同的密度。
在这两种紧密堆积中,原子的配位数为12。
2. Cu 为面心立方晶体,1个晶胞中Cu 原子个数=8×(18) + 6×(12)= 4(1)(2) =1.119 Å 3. ∵Fe 原子半径是相同的,在α型中,Fe3A 2M N a ααρ=g ,在γ型中, Fe γ3A γ4M N a ρ=g 在α型中,43r a α=,∴43a rα=;在γ型中,42r a γ=,∴22a r γ=∴Fe 3A (43)N rαρ=g ,Fe γ3A (22)N r ρ=g∴ 33γ(22)360.918682(43)r r αρρ===4. (1)(2) 原子堆积系数(100)=2222(4141)0.78544(22)r a r ππ⨯+=== 原子堆积系数(110)=22(414212)0.5554242r a π⨯+⨯== 原子堆积系数(111)= 22(316312)30.90696(12)(2)sin60r a ππ⨯+⨯==⨯o 23A 324A 463.548.936,8.97110(3.165)10m N V N ρ-⨯===⨯⨯⨯ 解得=Cu 42,24r a r a =∴=5. (1 ) MgO 与MnO 的d M —O 相差很大,这说明O 2–围成的正八面体空隙小,而Mg 2+、Mn 2+的半径差别大,导致d MnO >d MgO ;而S 2–和Se 2–半径大,围成的正八面体空隙既大于 ,又大于 ,所以d MgS ~d MnS ,d MgSe =d MnSe ,相当于Mg 2+和Mn 2+在S 2–和Se 2–围成的正八面体空隙中“扰动”。
全国高中生化学竞赛试题2 晶体结构(答案)

晶体结构答案第1题(6分)所有原子都是Mg (得3分)所有原子都是O (得3分)画更多原子者仍应有正确几何关系。
第2题(5分)2-1MgB 2(2分)(注:给出最简式才得分)2-2或a =b ≠c ,c 轴向上(3分)(注:任何能准确表达出Mg :B =1:2的晶胞都得满分,但所取晶胞应满足晶胞是晶体微观空间基本平移单位的定义,例如晶胞的顶角应完全相同等。
)第3题(10分)3-1①12②2③钠(各1分,共3分)3-2晶胞体积V =[2×(116pm +167pm)]3=181×106pm 3离子体积v =4×43π(116pm)3+4×43π(167pm)3=104×106pm 3v /V =57.5%(1分)(有效数字错误扣1分,V 和v 的计算结果可取4位,其中最后1位为保留数字,不扣分。
)3-3表面原子为8(顶角)+6(面心)+12(棱中心)=26总原子数为8(顶角)+6(面心)+12(棱中心)+1(体心)=27表面原子占总原子数26/27×100%=96%(1分)注:26和27均为整数值,比值26/27是循环小数0.962,取多少位小数需根据实际应用而定,本题未明确应用场合,无论应试者给出多少位数字都应按正确结果论。
3-4计算分两个步骤:步骤一:计算表面原子数。
可用n =2、3的晶胞聚合体建立模型,得出计算公式,用以计算n =10。
例如,计算公式为:[8]+[(n -1)×12]+[n ×12]+[(n -1)2×6]+[n 2×6]+[(n -1)×n ×2×6]顶角棱上棱交点棱上棱心面上棱交点面上面心面上棱心n =10,表面原子总数为2402(2分)步骤二:计算晶胞聚合体总原子数n 3×8+[8]×7/8+[(n -1)×12]×3/4+[n ×12]×3/4+[(n -1)2×6]/2+[n 2×6]/2+[(n -1)×n ×2×6]/2=8000+7+81+90+243+300+540=9261(2分)表面原子占总原子数的百分数:(2402/9261)×100%=26%(1分)(注:本题计算较复杂(还有更简单的计算方法),若应试者用其他方法估算得出的数值在26%左右2个百分点以内可得3分,3个百分点以内可得2分,其估算公式可不同于标准答案,但其运算应无误。
化学竞赛晶体结构综合例题

晶体结构综合例题一.有一立方晶系的离子晶体,其结构如右图所示,试回答:1.晶体所属的点阵形式及结构基元;2.已知r Cs+=169pm,r Cl-=181pm,试问此两种离于联合组成了何种型式的密堆积;3.Cu2+处在何种空隙里?4.指出各离子的配位情况?解:1. 立方P,CaCsCl3 ;2. A1型(立方面心)堆积, Cs+,Cl-离子半径大致相近;3. 八面体空隙中;4. Cu2+周围Cl-配位数6,Cs+配位数8;Cl-周围Cu2+配位数2,Cs+配位数4;Cs +周围Cl-配位数12,Cu2+配位数8。
二.黄铜矿是最重要的铜矿,全世界的2/3的铜是由它提炼的。
1.右图为黄铜矿的晶胞。
计算晶胞中各种原子的数目,写出黄铜矿的化学式;2.在高温下,黄铜矿晶体中的金属离子可以发生迁移。
若铁原子与铜原子发生完全无序的置换,可将它们视作等同的金属离子,请说出它的晶胞。
3.在无序的高温型结构中,硫原子作什么类型的堆积?金属原子占据什么类型的空隙?该空隙被金属原子占据的分数是多少?4.计算黄铜矿晶体的密度; (晶胞参数:a=52.4pm,c=103.0pm;相对原子量:Cu 63.5 Fe 55.84 S 32.06)。
解:1. 各种原子的数目Cu, Fe, S: 4, 4, 8; 黄铜矿的化学式CuFeS2 ;2.它的晶胞与ZnS晶胞相同;但金属离子随机性为50%;(如图);3.硫原子作A1型(立方F)堆积; 金属原子占据四面体空隙; 该空隙被金属原子占据的分数1/2;4.容易计算黄铜矿晶体的密度4.31g/cm3 .三.冰晶石(Na 3AlF 6)用作电解法炼铝的助熔剂。
冰晶石晶胞是以大阴离子(AlF 63-)构成的面心立方晶格,Na +可看作是填充在晶格的空隙中,已知冰晶石的密度为2.95g/cm 3,Al —F 键长181 pm ,相对原子质量:Na 23.0;Al 27.0;F 19.0。
1.指出AlF 63-配离子中心离子的杂化轨道类型、配离子空间构型和所属分子点群。
竞赛习题-晶体结构题
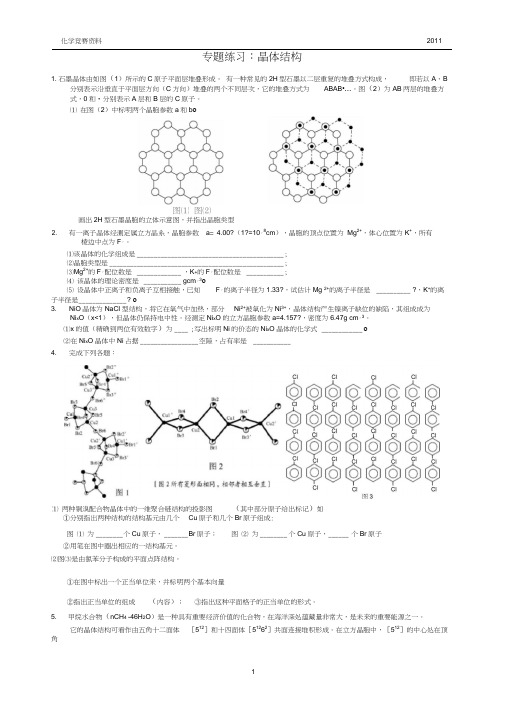
专题练习:晶体结构1. 石墨晶体由如图(1)所示的C原子平面层堆叠形成。
有一种常见的2H型石墨以二层重复的堆叠方式构成,即若以A、B 分别表示沿垂直于平面层方向(C方向)堆叠的两个不同层次,它的堆叠方式为ABAB•…。
图(2)为AB两层的堆叠方式,0和•分别表示A层和B层的C原子。
⑴ 在图(2)中标明两个晶胞参数a和b o图⑵画岀2H型石墨晶胞的立体示意图,并指岀晶胞类型有一离子晶体经测定属立方晶系,晶胞参数a= 4.00?(1?=10「8cm),晶胞的顶点位置为Mg2+,体心位置为K+,所有棱边中点为F「。
⑴该晶体的化学组成是___________________________________________ ;⑵晶胞类型是___________________________________________________ ;⑶Mg2+的F「配位数是_____________ ,K+的F「配位数是___________ ;⑷ 该晶体的理论密度是___________ gcm「3o⑸ 设晶体中正离子和负离子互相接触,已知F「的离子半径为1.33?,试估计Mg 2+的离子半径是__________ ?,K+的离子半径是______________ ?o3. NiO晶体为NaCI型结构,将它在氧气中加热,部分Ni2+被氧化为Ni3+,晶体结构产生镍离子缺位的缺陷,其组成成为Ni x O(x<1),但晶体仍保持电中性。
经测定Ni x O的立方晶胞参数a=4.157?,密度为6.47g cm「3。
⑴x的值(精确到两位有效数字)为____ ;写出标明Ni的价态的Ni x O晶体的化学式____________ o⑵在Ni x O晶体中Ni占据_________________ 空隙,占有率是___________4. 完成下列各题:①分别指出两种结构的结构基元由几个Cu原子和几个Br原子组成:图⑴ 为________ 个Cu原子,_______ B r原子;图⑵ 为________ 个Cu原子,______ 个Br原子②用笔在图中圈出相应的一结构基元。
全国高中学生化学竞赛[省级赛区]试题—晶体结构专题
![全国高中学生化学竞赛[省级赛区]试题—晶体结构专题](https://img.taocdn.com/s3/m/e23c5a3a763231126fdb1121.png)
全国高中学生化学竞赛[省级赛区]试题—晶体结构专题2000年:4.理想的宏观单一晶体呈规则的多面体外形。
多面体的面叫晶面。
今有一枚MgO 单晶如图所示。
它有6个八角形晶面和8个正三角形晶面。
宏观晶体的晶面是与微观晶胞中一定取向的截面对应的。
已知MgO 的晶体结构属NaCl 型。
它的单晶的八角形面对应于它的晶胞的面。
请指出排列在正三角形晶面上的原子(用元素符号表示原子,至少画出6个原子,并用直线把这些原子连起,以显示它们的几何关系)。
(6分)答案如图。
所有原子都是Mg(得3分)所有原子都是O(得3分)画更多原子者仍应有正确几何关系。
5.最近发现一种由钛原子和碳原子构成的气态团簇分子,如附图2所示,顶角和面心的原子是钛原子,棱的中心和体心的原子是碳原子,它的化学式是______。
答案:Ti 14C 13(2分)2001年:第5题(5分)今年3月发现硼化镁在39K 呈超导性,可能是人类对超导认识的新里程碑。
在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,像维夫饼干,一层镁一层硼地相间,图5-1是该晶体微观空间中取出的部分原子沿C 轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。
5-1 由图5-1可确定硼化镁的化学式为: 。
5-2 在图5-l 右边的方框里画出硼化镁的一个晶胞的透视图,标出该晶胞内面、棱、顶角上可能存在的所有硼原子和镁原子(镁原子用大白球,硼原子用小黑球表示)。
图5-1硼化镁的晶体结构示意图第5题:(答案)(5分)5-1 MgB 2 (2分)(注:给出最简式才得分)或a =b ≠c ,c 轴向上(3分)5-2 (注:任何能准确表达出Mg ︰B =1︰2的晶胞都得满分,但所取晶胞应满足晶胞是晶体微观空间基本平移单位的定义,例如晶胞的顶角应完全相同等。
)2002年:第2题(6分)用地壳中某主要元素生产的多种产品在现代高科技中占重要位置,足见化学对现代物质文明的重要作用。
高中化竞-晶体结构专题训练4

高中化学奥林匹克竞赛辅导晶体结构专题训练4班级:_____________________,姓名:________________________。
1.某钛的二元化合物的晶体结构示意图如下所示。
大球为钛原子、小球为氘原子,写出该化合物的化学式;每个氘原子周边有几个最近的钛原子?【答案】TiD24个2.某二元化合物的晶胞如图所示,图中小球为金属原子,大球为非金属原子,所有原子均在晶胞中。
其晶胞参数:a=0.3374 nm,c=0.5187 nm,γ=120°。
2-1 观察该化合物的晶胞,回答下面的问题:2-1-1 写出该化合物的化学式(金属用M表示,非金属用N表示)。
2-1-2 写出该晶体的结构基元的内容。
2-1-3 金属原子占据何种类型的多面体空隙,填隙率是多少?2-2 对该晶胞进行晶胞变换,画出得到的新晶胞。
2-3 若该晶体的密度D=5.910 g·cm-3,则通过计算写出该物质的化学式。
【答案】2-1-1 MN2-1-2 两个MN2-1-3 八面体空隙100%2-22-33.晶体X只含钠、镁、铅三种元素。
在不同的温度和压力下,晶体X呈现不同的晶相。
α-X是一种六方晶系的晶体,而γ-X是立方晶系的晶体。
在α-X中,镁和铅按1:1的比例形成类似于石墨的层状结构,钠填在层间。
在γ-X中,铅做立方最密堆积,其余两种原子填满所有的四面体空隙和八面体空隙。
3-1 给出X的化学式。
3-2 画出一层α-X的结构。
3-3 已知α-X的晶胞参数a=511 pm,c=1017 pm,Z=2,计算α-X的密度。
3-4 在不同的条件下,γ-X也呈现不同的结构。
3-4-1 画出由铅形成的八面体空隙仅被镁占据时,γ-X的立方晶胞。
3-4-2 画出由铅形成的八面体空隙仅被钠占据时,γ-X的立方晶胞。
【答案】3-1 Na2MgPb3-23-3 D=4.01 g·cm-33-44.某化合物X仅含A和B两种元素。
(四)竞赛专项练习题之晶体结构共5页文档

(四)晶体结构一、(2019)(12分)LiCl和KCl同属NaCl型晶体,其熔点分别为614℃和776℃。
Li+、K+和Cl-的半径分别为76pm、133pm和181pm。
在电解熔盐LiCl 以制取金属锂的生产工艺中,加入适量的KCl晶体,可使电解槽温度下降至400℃,从而使生产条件得以改善。
1.说明加入熔点高的KCl反而使电解温度大大下降的原因;2.有人认为,LiCl和KCl可形成固溶体(并画出了“固溶体的晶胞”)。
但实验表明,液相LiCl和KCl能以任意比例混溶而它们的固相完全不混溶(即不能生成固溶体!)。
请解释在固相中完全不混溶的主要原因。
3.写出计算LiCl和KCl两种晶体密度之比的表达式(须包含离子半径的符号);4.在KCl晶体中,K+离子占据由Cl- 离子围成的八面体空隙,计算相距最近的八面体空隙中心之间的距离。
5.实验证明,即使产生了阳离子空位,KCl晶体在室温下也不导电。
请通过计算加以说明。
二、(2019)(12分)为纪念1905年爱因斯坦连续发表6篇论文导致物理学大变革100周年,今年被定为国际物理年。
本题涉及的“热电效应”机理也是爱因斯坦首先阐释的,即他提出的被后人称为“爱因斯坦振荡器”的独立振荡原子与温度关系的模型。
1.左上图是热电效应之一的图解。
给出图中所有英文单词(或词组)及物理学符号的意义,并为此图写一篇不超过200字(包括标点符号等)的说明文。
2.右上图是化学家合成的能实现热电效应的一种晶体的晶胞模型。
图中的大原子是稀土原子,如镧;小原子是周期系第五主族元素,如锑;中等大小的原子是周期系VIII 族元素,如铁。
按如上结构图写出这种热电晶体的化学式。
给出计算过程。
提示:晶胞的6个面的原子数相同。
设晶体中锑的氧化态为-1,镧的氧化态为+3,问:铁的平均氧化态多大?三、(2019B)(10分)固体发光材料是一种能将激发的能量转变为可见光的固体物质。
在基质中掺入杂质,含量可达千分之几或百分之几,可调整发光效率、余辉及发光光谱。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(四)竞赛专项练习题之晶体结构(四)晶体结构一、(2005)(12分) LiCl和KCl同属NaCl型晶体,其熔点分别为614℃和776℃。
Li+、K+和Cl-的半径分别为76pm、133pm和181pm。
在电解熔盐LiCl以制取金属锂的生产工艺中,加入适量的KCl晶体,可使电解槽温度下降至400℃,从而使生产条件得以改善。
1.说明加入熔点高的KCl反而使电解温度大大下降的原因;2.有人认为,LiCl和KCl可形成固溶体(并画出了“固溶体的晶胞”)。
但实验表明,液相LiCl和KCl能以任意比例混溶而它们的固相完全不混溶(即不能生成固溶体!)。
请解释在固相中完全不混溶的主要原因。
3.写出计算LiCl和KCl两种晶体密度之比的表达式(须包含离子半径的符号);4.在KCl晶体中,K+离子占据由Cl- 离子围成的八面体空隙,计算相距最近的八面体空隙中心之间的距离。
5.实验证明,即使产生了阳离子空位,KCl晶体在室温下也不导电。
请通过计算加以说明。
二、(2005)(12分)为纪念1905年爱因斯坦连续发表6篇论文导致物理学大变革100周年,今年被定为国际物理年。
本题涉及的“热电效应”机理也是爱因斯坦首先阐释的,即他提出的被后人称为“爱因斯坦振荡器”的独立振荡原子与温度关系的模型。
1.左上图是热电效应之一的图解。
给出图中所有英文单词(或词组)及物理学符号的意义,并为此图写一篇不超过200字(包括标点符号等)的说明文。
2.右上图是化学家合成的能实现热电效应的一种晶体的晶胞模型。
图中的大原子是稀土原子,如镧;小原子是周期系第五主族元素,如锑;中等大小的原子是周期系VIII 族元素,如铁。
按如上结构图写出这种热电晶体的化学式。
给出计算过程。
提示:晶胞的6个面的原子数相同。
设晶体中锑的氧化态为-1,镧的氧化态为+3,问:铁的平均氧化态多大?三、(2005B)(10分)固体发光材料是一种能将激发的能量转变为可见光的固体物质。
在基质中掺入杂质,含量可达千分之几或百分之几,可调整发光效率、余辉及发光光谱。
如在刚玉Al2O3基质中掺入0.05~1.0%的Cr3+及在Y2O3基质中掺入Eu3+等均可制成固体发光材料。
1.推测Al2O3基质中掺入Cr3+的发光原理。
2.Y2O3属立方晶系,将Y2O3的立方晶胞分为8个小立方体,Y在小立方体的面心和顶点,O位于小立方体内的四面体空隙,画出这样四个小立方体,指出Y和O的配位数。
【答案】1.Al3+和O2-是满壳层电子结构,能隙大,电子不易激发,故无色;(2分)掺入的Cr3+是过渡金属,具有3d电子,在晶体中置换部分Al3+形成较低的激发态能级,两个强吸收带分别吸收黄绿色及蓝色的光,只有红光透过,因而掺Cr3+的刚玉呈绚丽的红色,称为红宝石。
(3分)2.(4分)Y的O的配位数为6,O的Y配位数为4。
(1分)四、(2004)(4分)2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N-N键的键能为160kJ/mol(N2的键能为942kJ/mol),晶体结构如图所示。
在这种晶体中,每个氮原子的配位数为;按键型分类时,属于晶体。
这种固体的可能潜在应用是,这是因为:。
五、(2004)(6分)最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性。
鉴于这三种元素都是常见元素,从而引起广泛关注。
该晶体的结构可看作由镁原子和镍原子在一起进行(面心)立方最密堆积(ccp),它们的排列有序,没有相互代换的现象(即没有平均原子或统计原子),它们构成两种八面体空隙,一种由镍原子构成,另一种由镍原子和镁原子一起构成,两种八面体的数量比是1︰3,碳原子只填充在镍原子构成的八面体空隙中。
1.画出该新型超导材料的一个晶胞(碳原子用小球,镍原子用大○球,镁原子用大球)。
2.写出该新型超导材料的化学式。
六、(2003)(6分)钒是我国丰产元素,储量占全球11%,居第四位。
在光纤通讯系统中,光纤将信息导入离光源1km外的用户就需用5片钒酸钇晶体(钇是第39号元素)。
我国福州是全球钒酸钇晶体主要供应地,每年出口几十万片钒酸钇晶体,年创汇近千万美元(1999年)。
钒酸钇是四方晶体,晶胞参数a=712pm,c=629pm,密度d=4.22g/cm3,含钒25%,求钒酸钇的化学式以及在一个晶胞中有几个原子。
给出计算过程。
钒酸钛的化学式:一个晶胞中的原子数:七、(2002)(6分)用地壳中某主要元素生产的多种产品在现代高科技中占重要位置,足见化学对现代物质文明的重要作用。
例如:1.计算机的芯片的主要成分是;2.光导纤维的主要成分是:3.目前应用最多的太阳能电池的光电转化材料是;4.用作吸附剂、干燥剂、催化剂或催化剂载体的人造分子筛大多是一类称为的化合物;5.有一大类化合物,结构独特,兼备无机材料和有机材料双重性能,有耐温、电绝缘性好、难燃、憎水、耐腐蚀……等特性,广泛用于航空航天、电子电气、建筑、运输等行业,用于密封、粘合、润滑、涂层、表面活性、防水、防潮……,已为现代社会不可替代的新材料。
这类材料在分子结构上的特点是和。
八、(2001)(5分)今年3月发现硼化镁在39K呈超导性,可能是人类对超导认识的新里程碑。
在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,像维夫饼干,一层镁一层硼地相间,图5-1是该晶体微观空间中取出的部分原子沿C轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。
1.由图1可确定硼化镁的化学式为:。
2.在图l右边的方框里画出硼化镁的一个晶胞的透视图,标出该晶胞内面、棱、顶角上可能存在的所有硼原子和镁原子(镁原子用大白球,硼原子用小黑球表示)。
图1硼化镁的晶体结构示意图九、(2001)(10分)研究离子晶体,常考察以一个离子为中心时,其周围不同距离的离子对它的吸引或排斥的静电作用力。
设氯化钠晶体中钠离子跟离它最近的氯离子之间的距离为d,以钠离子为中心,则:1.第二层离子有个,离中心离子的距离为 d,它们是离子。
2.已知在晶体中Na+离子的半径为116pm,Cl-离子的半径为167pm,它们在晶体中是紧密接触的。
求离子占据整个晶体空间的百分数。
3.纳米材料的表面原子占总原子数的比例极大,这是它的许多特殊性质的原因,假设某氯化钠纳米颗粒的大小和形状恰等于氯化钠晶胞的大小和形状,求这种纳米颗粒的表面原子占总原子数的百分比。
第11题(10分)12,d2,钠 (各1分,总3分)11-2 晶胞体积V=[2×(116pm+167pm)]3=181×106pm3离子体积 v=4x (4/3)π(116pm)3+4x (4/3)π(167pm)3=104×106 pm3v/V=57.5% (1分)(有效数字错误扣1分,V和v的计算结果可取4位,其中最后1位为保留数字,不扣分。
)11-3表面原子为8(顶角)+6(面心) +12(棱中心)=26a=b≠c,c轴向上总原子数为 8(顶角)+6(面心)+12(棱中心)+1(体心)=27表面原子占总原子数 26/27×100%=96 %(1分)注:26和27均为整数值,比值26/27是循环小数0.962, 取多少位小数需根据实际应用而定, 本题未明确应用场合,无论应试者给出多少位数字都应按正确结果论。
11-4 计算分两个步骤:步骤一:计算表面原子数。
可用n=2、3的晶胞聚合体建立模型,得出计算公式,用以计算n=10。
例如,计算公式为:[8]+[(n-1)×12]+[n×12]+[(n-1)2×6]+[n2x6]+[(n-1)×n×2×6]顶角棱上棱交点棱上棱心面上棱交点面上面心面上棱心n=10,表面原子总数为2402 (2分)步骤二:计算晶胞聚合体总原子数:n3×8+[8] ×7/8+[(n-1)×12]×3/4+[n×12]×3/4+[(n-1)2×6]/2+[n2×6]/2+[(n-1)×n×2×6]/2=8000+7 + 81 + 90 + 243 + 300 + 540=9261 (2分)表面原子占总原子数的百分数: (2402/9261)×100%=26% (1分)(总5分)(注:本题计算较复杂,若应试者用其他方法估算得出的数值在26% 左右2个百分点以内可得3分,3个百分点以内可得2分,其估算公式可不同于标准答案,但其运算应无误。
本题要求作估算,故标准答案仅取整数,取更多位数不扣分。
)十、(2000)(2分)最近发现一种由钛原子和碳原子构成的气态团簇分子,如右图所示,顶角和面心的原子是钛原子,棱的中心和体心的原子是碳原子,它的化学式是______。
【答案】Ti14C13(2分)说明:凡按晶胞计算原子者得零分。
十一、(2000)(8分)铂系金属是最重要的工业催化剂。
但其储藏已几近枯竭,上小行星去开采还纯属科学幻想。
研究证实,有一类共价化合物可代替铂系金属催化剂。
它们是坚硬的固体,熔点极高,高温下不分解,被称为“千禧催化剂”(millennium catalysts)。
下面3种方法都可以合成它们:①在高温下将烃类气体通过钨或钼的氧化物的表面。
②高温分解钨或钼的有机金属化合物(即:钨或钼与烃或烃的卤代物形成的配合物)。
③在高度分散的碳表面上通过高温气态钨或钼的氧化物。
1.合成的化合物的中文名称是______和__________。
(共4分,各2分)2.为解释这类化合物为什么能代替铂系金属,提出了一种电子理论,认为这些化合物是金属原子与非金属原子结合的原子晶体,金属原子周围的价电子数等于同周期的铂原子或钌原子的价电子数。
这类化合物的化学式(即最简式或实验式)是_______和_______。
(4分,各2分)十二、(1998)(12分)钨酸钠Na2WO4和金属钨在隔绝空气的条件下加热得到一种具有金属光泽的、深色的、有导电性的固体,化学式Na x WO3,用X射线衍射法测得这种固体的立方晶胞的边长a=3.80×10-10m,用比重瓶法测得它的密度为d=7.36g/cm3。
已知相对原子质量:W 183.85,Na 22.99,O 16.00,阿伏加德罗常数L=6.022×1023mol-1。
求这种固体的组成中的x值(2位有效数字),给出计算过程。
