【读片时间】第1483期:特发性家族性脑血管铁钙质沉着症
颅脑常见病变的CT诊断

病例一
中毒
CO中毒脑损伤的发病机理:
CO吸入人体进入血液后,迅速与血红蛋白结合形成碳氧血红 蛋白(HBCO),HBCO不仅不能携带氧,而且还影响氧合血红蛋 白的解离,使血红蛋白失去携氧能力,阻碍氧的释放和传递,导 致机体内形成低氧血症,引起组织缺氧。在人体各种组织中, 脑组织对缺氧最为敏感,往往首先受累,尤以基底节最为明显 。急性CO中毒导致脑缺氧后,脑部血管先发生痉挛,而后扩张, 渗透性增加而诱发脑细胞内水肿。由于缺氧和脑水肿后的脑 血液循环障碍,可造成小血管内血栓形成,缺血性坏死,软化或 广泛的脱髓鞘病变。
颅咽管瘤的发病年龄有两个高峰:8-12岁及40-60岁,无 性别差异。
常因肿瘤压迫邻近器官,产生相应的临床症状后就诊发现,临 床症状依其原发部位、发展方向而定,常表现在颅内压增高、 视觉障碍及内分泌症状。当肿瘤向鞍上生长压迫视交叉时引起 视觉障碍,压迫第三脑室、室问孔时造成脑积水,向下压迫垂 体时产生内分泌症状。
部颅骨内板下间隙增宽,脑室系统扩张。
病例四
男,10岁,外伤1天 左侧颞顶枕叶见不规则脑沟回样钙化,局部脑沟增宽加深,
蛛网膜下腔增宽。 Sturge-Weber综合征
Sturge-Weber综合征
又称颜面部血管瘤--青光眼综合征、皮肤--软脑膜血管瘤病 等,系由于胚胎发育6周时血管系统发育不良,影响到脑、骨 膜、皮肤的血管所致。其主要临床表现有三方面:
头昏,无恶心呕吐,无四肢抽搐。就诊于云阳县人民医院就 诊,行头颅CT提示:左侧额顶部包块伴局部骨折缺损,今
为求进一步治疗,入我院,门诊以“左侧额顶部颅骨病变”
收入。
病例九
患者女,27岁 主诉:G1P0孕35周先兆早产(双胎),嗜睡、失语3h。 主要表现:剖宫产术后1天血压升高,头痛,测血压
Fahr综合征

Fahr综合征又名:Fahr综合征;大脑钙质沉着伴晚发性脑病;大脑钙质沉着;基底节钙化;对称性大脑钙化综合征。
特发性两侧对称性大脑基底节钙化症;特发性家族性脑血管亚铁钙沉着;家族性基底节钙化。
对称性大脑钙化综合征于1930年由Fahr所描述。
国内有少数报道。
【病因】未明。
一般认为是假-假性甲状旁腺机能减退(Albright遗传性骨营养不良症)的一种异常类型,是常染色体隐性遗传,多伴有因甲状旁腺功能缺陷而致之钙-磷代谢改变,钙、磷离子与含大量蛋白质的有机基质相结合。
发病机制:是肾脏对甲状旁腺(PTH)正常下的反应,血清钙磷正常,钙化起始于基底节和齿状核,钙化的过程与生理性钙化相似,随疾病的进展、钙沉着的程度和范围也增加,可能因血管壁钙化所致的血管闭塞而造成脑萎缩,钙质沉着不一定伴神经系统症状。
【临床表现】多数病例有钙质沉着,但无神经系统症状,仅于脑部X线检查时发现,一般可于45~60岁出现症状。
主要为精神衰退、锥体外系统性运动缺陷、小脑性共济失调、震颤症状群及构音障碍、情感迟钝、记忆减退,有的表现焦虑、抑郁伴偏执、妄想、精神病样症状。
颅部X线:双侧基底节对称性钙化,脑CT检查除双侧基底节、小脑齿状核和脑沟处可见钙化外,还可发现大脑轻度萎缩和脑室扩大。
【诊断】自幼开始出现慢性进行性智能衰退和锥体外系受损症状,结合颅部X线的表现以及脑CT的可靠证据确诊。
本病应与下列疾病鉴别:①特发性甲状旁腺机能减退:是由于甲状旁腺激素不足,造成低血钙,高血磷及Ellsworth-Howard试验(甲状旁腺激素磷利尿试验)阳性。
②假性甲状旁腺功能减退:系因骨骼和肾小管对甲状旁腺激素有对抗所致。
有低血钙、高血磷和Ellsworth-Howard试验阴性,血清甲状旁腺素浓度高于正常。
③假-假性甲状旁腺机能减退:血清钙、磷浓度正常,骨骼和肾小管对甲状旁腺激素的反应也正常,即Ellsworth-Howard试验正常。
假性和假-假性甲状旁腺功能减退之患者都具有特征性躯体表现:身材短小,圆脸,掌跖骨短,牙齿异常,白内障和软骨组织钙化等;而Fahr综合征仅有大脑钙质沉着及神经精神症状,并无上述躯体特征,可作区别之条件。
最新全球罕见疾病-PPT文档

哥伦比亚男童患“乌龟背” 成功脱除
哥伦比亚一个村庄的一个6岁大的男孩 Didier Montalvo因为患有先天性色素痣 (congenital melanocytic nevus), 背上硕大的痣让他看起就像长了乌龟壳。 当地迷信的村民诬称,他的大痣是在一次 日食中附体的,会给他们带来不好的影响, 因此排斥Didier和他的家人,也不让 Didier上学。2012年4月,在得知这个情 况后,英国的医师为Didier做了手术,让 他得以像正常人一样生活。
越南一女子过敏后患怪病短时间内衰老50岁
2011年10月,一名越南年轻女子因对海鲜极度过敏引发怪病,短短几个 月内就从23岁的迷人美女变成七旬老妇。这名女子名叫阮莳芳(Nguyen Thi Phuong),现年26岁。从2008年开始,她的脸部开始肿胀,皮肤也开 始松垂,但是由于家庭贫困无力治疗,一直拖延。现在医生正试图搞清楚究 竟是什么导致了这一“闪电”衰老。阮时芳说,自己对海鲜过敏,在2008年 有过一次严重过敏,“当时我全身发痒,开始尝试传统药物,疹子消失了, 也不觉得痒了,但是,我的皮肤开始松弛起褶皱。”阮时芳称,虽然衰老影 响了她的脸及全身的皮肤,但并没有影响头发、牙齿、眼睛以及头脑。有专 家认为,阮时芳的这种情况属于脂肪代谢障碍,这种病症极为罕见,全球大 约只有2000人患有此病。
英国一女孩患怪病一天最多呕吐100次
英国12岁女孩艾丽莎 阿特金森患有一种罕见 怪病,发病时每天要呕吐数十次,最多一天呕吐 100多次。母亲马吉说,阿特金森从6岁时就开始 出现这种怪病的症状,每次发病可能持续数天甚 至数周。阿特金森病情最严重的一次,24小时内 呕吐了100次。医生称阿尔金森换上了周期性呕 吐综合症。
英国女青年杰德·霍尔因患有罕见 遗传疾病普拉德-威利综合征而食量 惊人,每天吃个不停。凡是拿在手上 的东西,她都往嘴里塞,哪怕有时拿 着的是狗粮甚至肥皂。
Fahr’s病

Fahr’s病基底核钙化症即特发性基底核钙化(idiopathic basal ganglia calcification,IBGC)概述:Fahr病甚罕见,1930年由Fahr首次报道。
1930年Fahr报告了此病的尸检资料,其特征为脑血管壁内大量的钙沉积,尤以豆状核和齿状核的血管为甚。
Fahr病又称家族性特发性基底节钙化症、锥体外系铁钙沉着症或特发性家族性脑血管亚铁钙沉着症 .是以双侧基底节对称性钙质沉着为病理学特征的一组疾病,常有家族遗传,临床表现为进行性痴呆、锥体外系症状和癫痫发作[1]。
但有家族性发病的报告诊断标准:后来由Moskowitz等拟定了诊断标准:(1)影像上有对称性双侧基底节钙化;(2)无假性甲状旁腺功能减退现象;(3)血清钙、磷均正常;(4)肾小管对甲状旁腺激素反应功能正常;(5)无感染、中毒代谢等原因。
Fahr病是以基底节钙化为主要病理特征,Fahr为双侧基底节、丘脑、小脑齿状核及大脑皮质下中枢对称性钙质沉着。
病理研究结果表明,在组织学上没有发现病灶周围的毛细血管内有非动脉硬化性的铁质、钙质沉着,说明钙化的原因与血清中的钙无重要联系。
有人认为病灶区小血管外层和中层以及血管周围的组织中,含有粘多糖蛋白、脂类的混合物,这些物质可能与细胞的钙、磷代谢紊乱有关。
其主要病理改变是小血管及其周围有以羟基磷灰石形成的钙盐沉淀,结石的成分除钙、磷外,还有锰、铜、铁、锌、铝、镁、钼及少量的氟元素等;主要病理过程为酸性粘多糖组成的嗜酸性物质在血管周围沉积,钙盐在此基础沉着。
钙化部位常有神经元的丧失和神经胶质细胞增生,少数有脱髓鞘改变,晚期部分脑实质几乎都被钙化和神经胶质替代。
常规尸检发现有40%~70%被检者苍白球、齿状核呈某种程度钙化。
基底节钙化中许多人无神经系统异常表现,且绝大多数在40岁以上,临床意义仅相当于松果体钙化和脉络丛钙化,尤其是钙化仅限于苍白球者,这种生理性钙化的发生率约为6‰。
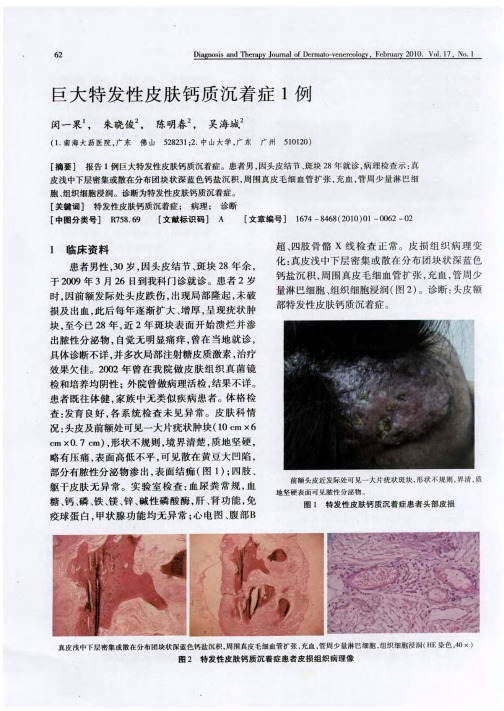
巨大特发性皮肤钙质沉着症1例
[ ] 临床皮肤病 学 [ . 3版. 1 M] 第 南京江 苏科学 技术 出版
社 ,0 193 20 :6
『 ] Sa G, at iG . co l a ioi:si i oa i 2 adA Z a r S Sr a cl ns i t d p t c a t c s i h
2 0 ,9 1 ) 1 2 0 3 2 ( 2 :2 2—1 2 . 2 4
诊 断头皮额部特发性皮肤钙 质沉着症无疑 。应与 本病 鉴别诊 断 的疾病有 : 瘢 痕疙 瘩 : 发 于前 ① 好
[ 收稿 日期 ] 2 0 0 3 09— 8— 1 [ 回 日期 ] 2 1 0 — 4 修 0 0— 1 0
皮肤性病诊疗学杂志 21 2月— 1 00生 鲞笈
2 讨 论 特发性皮肤 钙沉着症 是一种少 见的皮肤 病 , 患者可既无组织损 伤也无 钙 、 磷代 谢紊乱 而有钙 盐沉 积 于 皮 肤 、 下组 织 和肌 肉¨ , 因未 明。 皮 病 Sa G等 认 为特发性钙质沉着症 系上皮囊肿 adA 炎症后 钙化形成 。皮 疹 多为 0 5c ~ m直径 . m 5c
易 复 发 引。
[ 考文献 ] 参
的丘疹 、 结节或斑块 , 质坚如骨 , 常发生于会阴 、 躯
干、 四肢 。而本例特点是青年男性患者 , 病程长达
2 年, 8 开始为头皮丘疹结 节 , 缓慢增 大 , 与皮 肤粘
连 , 成 坚 硬 固定 (0a × 31 0 7a 大 4 / 形 1 m 6(' . m) , ̄ 1× 1 I
1. 1 第二届 国际微创整形外科 和皮肤病学会议 (00 9 1 9 1 , 国首尔 ) 2 1 :.0— .2 韩
1.第二十五届欧洲抗性病协会 (U T ) 2 IS I 年会( 00 9 2 92 , 2 1 :.3~ .5 格鲁吉亚第 比利斯 )
特发性肺含铁血黄素沉着症科普讲座PPT课件

如何诊断特发性肺含铁血黄素沉着症? 临床检查
医生会通过患者的病史、体检和影像学检查来初 步判断。
胸部X光和CT扫描是常用的影像学工具。
如何诊断特发性肺含铁血黄素沉着症? 实验室检查
血液检查和肺功能测试有助于了解患者的整体健 康状况。
特别是铁代谢相关的实验室指标。
如何诊断特发性肺含铁血黄素沉着症? 组织活检
特发性肺含铁血黄素沉着症科普 讲座
演讲人:
目录
1. 什么是特发性肺含铁血黄素沉着症? 2. 特发性肺含铁血黄素沉着症的症状有哪 些? 3. 如何诊断特发性肺含铁血黄素沉着症? 4. 特发性肺含铁血黄素沉着症的治疗方式 是什么? 5. 如何预防特发性肺含铁血黄素沉着症?
什么是特发性肺含铁血黄素沉 着症?
在高风险环境中工作的人应采取适当的防护措施 ,减少铁质粉尘的吸入。
如佩戴口罩和使用通风设备。
如何预防特发性肺含铁血黄素沉着症? 定期健康检查
定期进行肺部健康检查,及时发现潜在问题。
特别是从事相关行业的工作者。
如何预防特发性肺含铁血黄素沉着症? 公众教育
增强公众对该疾病的认识,提高早期识别和干预 的意识。
在某些情况下,可能需要进行肺组织活检以确认 诊断。
活检可以帮助明确沉积物的性质。
特发性肺含铁血黄素沉着症的 治疗方式是什么?
特发性肺含铁血黄素沉着症的治疗方式是什么? 药物治疗
目前尚无特效药物,主要以对症治疗为主。
例如,使用支气管扩张剂缓解呼吸困难。
特发性肺含铁血黄素沉着症的治疗方式是什么? 生活方式调整
发性肺含铁血黄素沉着症是一种肺部疾病,主 要特征是在肺组织中异常积聚含铁血黄素。
这种疾病通常与慢性肺部疾病或长期吸入铁质颗 粒有关。
小儿特发性肺含铁血黄素沉着症科普宣传PPT课件

目前无特效药物治疗,主要以支持性疗法为主, 包括氧疗和营养支持。
在某些情况下,可能需要进行肺部清洗或机械通 气。
如何诊断和治疗?
预后
预后因病情严重程度和治疗的早晚而异,早期治 疗通常预后较好。
长期随访是必要的,以监测肺功能和其他潜在问 题。
如何预防?
如何预防? 孕期管理
确保孕期营养充足,避免环境有害因素,减 少早
目录
1. 什么是小儿特发性肺含铁血黄素沉着症 ? 2. 为什么要关注该疾病? 3. 如何诊断和治疗? 4. 如何预防? 5. 总结与展望
什么是小儿特发性肺含铁血黄 素沉着症?
什么是小儿特发性肺含铁血黄素沉着症?
定义
小儿特发性肺含铁血黄素沉着症是一种罕见的肺 部疾病,主要特征为肺部含铁血黄素的异常沉积 。
临床试验可能为新疗法的开发提供重要数据。
总结与展望
多学科合作
需要儿科医生、呼吸科医生和营养师等多学科团 队共同管理患者。
这种合作可以提高患者的整体护理质量。
总结与展望
家长的角色
家长在疾病管理中扮演重要角色,需关注孩子的 健康变化。
积极参与治疗决策和随访,有助于改善孩子的健 康状况。
谢谢观看
为什么要关注该疾病? 早期干预的重要性
早期诊断和治疗可以显著改善预后,减少长 期并发症的风险。
定期监测和随访也是管理病情的关键。
如何诊断和治疗?
如何诊断和治疗? 诊断方法
通过临床评估、影像学检查(如胸部X光、CT) 和实验室检测(如血液测试)来确诊。
病理检查有助于确认铁血黄素的沉积。
如何诊断和治疗?
在高风险人群中(如早产儿),发病率可能更高 。
为什么要关注该疾病?
Fahr’s病

Fahr’s病基底核钙化症即特发性基底核钙化(idiopathic basal ganglia calcification,IBGC)概述:Fahr病甚罕见,1930年由Fahr首次报道。
1930年Fahr报告了此病的尸检资料,其特征为脑血管壁内大量的钙沉积,尤以豆状核和齿状核的血管为甚。
Fahr病又称家族性特发性基底节钙化症、锥体外系铁钙沉着症或特发性家族性脑血管亚铁钙沉着症 .是以双侧基底节对称性钙质沉着为病理学特征的一组疾病,常有家族遗传,临床表现为进行性痴呆、锥体外系症状和癫痫发作[1]。
本病可发生于任何年龄,无明显的性别差异,病因尚不明确,多为散发,但有家族性发病的报告诊断标准:后来由Moskowitz等拟定了诊断标准:页脚内容1(1)影像上有对称性双侧基底节钙化;(2)无假性甲状旁腺功能减退现象;(3)血清钙、磷均正常;(4)肾小管对甲状旁腺激素反应功能正常;(5)无感染、中毒代谢等原因。
Fahr病是以基底节钙化为主要病理特征,Fahr 为双侧基底节、丘脑、小脑齿状核及大脑皮质下中枢对称性钙质沉着。
病理研究结果表明,在组织学上没有发现病灶周围的毛细血管内有非动脉硬化性的铁质、钙质沉着,说明钙化的原因与血清中的钙无重要联系。
有人认为病灶区小血管外层和中层以及血管周围的组织中,含有粘多糖蛋白、脂类的混合物,这些物质可能与细胞的钙、磷代谢紊乱有关。
其主要病理改变是小血管及其周围有以羟基磷灰石形成的钙盐沉淀,结石的成分除钙、磷外,还有锰、铜、铁、锌、铝、镁、钼及少量的氟元素等;主要病理过程为酸性粘多糖组成的嗜酸性物质在血管周围沉积,钙盐在此基础沉着。
钙化部位常有神经元的丧失和神经胶质细胞增生,少数有脱髓鞘改变,晚期部分脑实质几乎都被钙化和神经胶质替代。
常规尸检发现有40%~70%被检者苍白球、齿状核呈某种程度钙化。
基底节钙化中许多人无神经系统异常表现,且绝大多数在40岁以上,临床意义仅相当于松果体钙化和脉络丛钙化,尤其是钙化仅限于苍白球者,这种生理性钙化的发生率约为6‰。
Fahr综合征

Fahr综合征Fahr综合征又称特发性基底节钙化综合征或对称性大脑钙化综合征。
过去认为它是一种较为罕见的疾病,但随着医学影像学的发展,被发现的病例数有所增加。
但至今国内外对特发性非家族性局限于基底节的钙化报道甚少。
为此,我们收集了近5年在我院诊治的75例该病患者的临床及影像学资料,进行回顾性分析,并进行讨论,旨在提高对本病的认识,现报告如下。
1 临床资料1.1 一般资料根据头部CT结果将75例颅内钙化患者分为两组:I组为钙化局限于双侧苍白球以内者37例(49.3%),男22例,女15例;年龄13— 82岁,平均48.5岁;1I组为钙化范围扩大到苍白球以外部位38例(50.7%),男25例,女13例;年龄1.5~_______67岁,平均30.2岁。
两组均无阳性家族史。
Ⅱ组患者既往13例(34.2%)有CO中毒史,5例(13.2%)服用过抗惊厥药,9例(23.7%)出生时窒息或产伤,3例有肝豆状核变性史,2例有EB病毒性脑炎病史,3例放化疗后。
i.2 症状与体征 I组患者没有任何阳性症状和体征;1I组患者头痛头晕13例,癫痫6例,肢体活动受限7例,眩晕5例(其中位置性眩晕2例),肢体震颤4例,双侧肌张力高5例(其扭转痉挛3例,共济失调2例),痴呆和精神行为障碍3例,言语不清3例。
两组均无甲状腺功能减低与假性甲状旁腺低功体征。
1.3 发病形式癫痫或癫痫样抽搐发病的17例,以头痛头晕发病的19例,以锥体外系症状发病5例,以手足抽搐、麻木发病4例,以痴呆、精神发育迟滞起病2例。
急性起病27例,慢性起病18例。
1.4 影像学表现所有病变于CT平扫上均表现为均匀一致高密度,于MRI T WI上呈低信号,T,WI上呈高信号。
CT:I组患者均有苍白球对称性钙化,呈斑点状,密度不均,边界不清,钙化灶直径为0.5~1.1cm,其中23例合并脉络丛和松果体钙化;Ⅱ组CT特点为不对称钙化,苍白球以外钙化38例,其中,13例一氧化碳中毒均累及两侧苍白球以外区域,其中5例伴有两侧脑室周围白质的低密度脱髓鞘改变,3例伴有小脑点状钙化;5例服用过抗惊厥药,其中3例累及杏仁体,2例累及屏状核,9例出生时窒息或产伤均累及两侧豆状核;3例肝豆状核变性,其中2例累及两侧壳核,1例同时累及两侧壳核及尾状核头部;2例EB病毒性脑炎,其中1例累及两侧壳核,1例同时累及两侧豆状核、尾状核头部及两侧丘脑;3例放疗化疗后均累及两侧豆状核及皮质。
Fahr's病CT表现

• Fahr’s病又称家族性特发性脑血管亚铁钙 沉着症。
• 发病原因迄今仍未明确,主要与家族遗传有 关,大多支持常染色体显性遗传。
• 发病年龄跨度较大,各年龄段均可发生
• 临床表现多种多样:最多见的是帕 金森综合征;其它表现有舞蹈病; 震颤;张力障碍;手足徐动征;口 面部运动障碍;癫痫;语言障碍; 痴呆;记忆力下降;智力低下以及 继发于小脑损害的共济失调等。
• CT表现
• 颅内广泛双侧对称性钙化。
• 钙化最常累及苍白球、皮髓质交界 、丘脑及小脑齿状核
Байду номын сангаас
• Fahr’s病最重要的鉴别诊断:
• 甲状旁腺功能低下性疾病,两者的 影像学改变几乎完全相同,临床症 状也大致相同,结合实验室检查、 家族病史、既往史等基本可作出鉴 别
谢谢!
脑铁沉积诊断标准-概述说明以及解释

脑铁沉积诊断标准-概述说明以及解释1.引言1.1 概述脑铁沉积是一种常见的神经系统疾病,其特征是大量铁元素在脑组织中的异常积聚。
这种异常积聚的铁元素会影响神经细胞的功能,并可能导致一系列严重的神经系统症状和病理变化。
脑铁沉积的临床表现各异,但通常包括运动障碍、认知功能下降和情绪变化等。
随着对脑铁沉积的认识不断深入,对其诊断标准的规范化和完善变得尤为重要。
本文旨在探讨脑铁沉积诊断标准的建立和完善,以提高对该疾病的准确诊断。
首先,文章将详细介绍脑铁沉积的定义和特征,包括形成机制、影响因素以及铁元素在脑组织中的异常分布情况。
其次,文章将阐述脑铁沉积所引起的临床表现,分析其对患者身体和心理健康的影响。
最后,文章将强调脑铁沉积诊断标准的重要性,并探讨现有标准的不足之处。
针对现有标准的不足,本文将提出建立完善脑铁沉积诊断标准的必要性,并介绍一些可能的改进方向。
通过对脑铁沉积诊断标准的研究和改进,我们可以更准确地诊断该疾病,提早干预和治疗,以改善患者的生活质量。
同时,建立完善的诊断标准也有利于促进脑铁沉积疾病的研究和治疗进展,为进一步深入探究其病理机制和寻找新的治疗方法提供科学依据。
本文将进一步探讨脑铁沉积诊断标准的制定和完善的必要性,并对未来的研究方向进行展望。
1.2文章结构文章结构:本文将分为引言、正文和结论三个部分进行阐述。
引言部分主要对脑铁沉积诊断标准这一课题进行概述,介绍脑铁沉积的背景和现状,并提出本文的目的和意义。
正文部分将详细探讨脑铁沉积的定义和特征,包括脑铁沉积的形成机制、分布特点以及与其他相关疾病的关联等内容。
其次,将深入讨论脑铁沉积的临床表现,包括脑功能损害的表现、神经精神症状以及身体症状等方面。
最后,将重点阐述脑铁沉积给个体和社会带来的影响和危害,包括对认知功能、情绪心理及生理健康的影响,以及社会经济负担等方面。
结论部分将强调脑铁沉积诊断标准的重要性,指出目前现有的脑铁沉积诊断标准存在的不足,包括不能全面识别患者的脑铁沉积情况等。
铁质沉着症名词解释

铁质沉着症名词解释
铁质沉着症(Hemochromatosis)是一种遗传性疾病,也被称为
铁过多症。
它是由于体内铁的代谢紊乱导致铁的过量沉积在身体各
个组织和器官中,引起多种病理变化的疾病。
铁质沉着症主要是由于体内铁的吸收过多而导致的。
正常情况下,人体通过肠道吸收的铁能够满足身体的需要,但在铁质沉着症
患者中,肠道对铁的吸收能力异常增强,导致体内铁的储存量逐渐
增加。
铁质沉着症可分为原发性和继发性两种类型。
原发性铁质沉着
症是由HFE基因突变引起的,这是最常见的遗传性疾病形式。
而继
发性铁质沉着症则是由其他疾病(如贫血、酒精性肝病等)或治疗(如长期输血)引起的。
铁质沉着症的症状和表现可以因个体差异而有所不同。
早期症
状可能包括疲劳、关节疼痛、肝脏肿大等,随着疾病的进展,铁的
过量沉积可以引起肝脏损害、心脏病、糖尿病、皮肤色素沉着等。
诊断铁质沉着症通常需要进行一系列的检查,包括血液铁指标、
基因检测、肝功能检查、肝组织活检等。
治疗方面,主要目标是减少体内铁的负荷,通常通过静脉放血(献血)或药物治疗(如螯合剂)来实现。
在一些严重的病例中,可能需要肝移植。
总结来说,铁质沉着症是一种遗传性疾病,由于体内铁的代谢紊乱导致铁的过量沉积在身体各个组织和器官中,引起多种病理变化。
早期诊断和治疗对于预防并发症的发生非常重要。
脑干矿物质沉积

脑干矿物质沉积是指在脑干区域出现异常的矿物质沉积现象。
脑干是连接大脑和脊髓的重要结构,负责控制人体的许多基本功能,如呼吸、心跳、消化等。
当在脑干中出现矿物质沉积时,可能会对脑干功能产生影响,引起一系列症状。
脑干矿物质沉积可以有多种原因和形式。
下面是一些常见的脑干矿物质沉积及其详细介绍:1. 铁质沉积:铁质沉积是指在脑干中积聚异常过多的铁元素。
它可以发生在一些代谢障碍性疾病中,如Wilson病(一种遗传性铜代谢障碍疾病),导致铁沉积在脑干中。
这种沉积可引起脑干结构的改变,干扰神经信号的传递,导致痉挛、肌张力异常、不稳定的姿势和运动障碍等症状。
2. 钙质沉积:钙质沉积是指在脑干中形成异常的钙结晶。
它可以发生在一些病理情况下,如颅内感染、外伤、中枢神经系统炎症等。
钙质沉积可能导致脑干神经细胞激活异常、炎症反应增加,从而影响脑干正常功能,出现疼痛、肌肉僵硬、认知障碍等症状。
3. 锰质沉积:锰质沉积是指在脑干中过度积聚的锰元素。
一些特定的职业接触或长期暴露在锰污染环境中的人可能面临锰沉积的风险。
锰质沉积可以导致锰中毒,引起运动障碍、颤抖、肌肉僵直、认知和行为问题。
脑干矿物质沉积的影响取决于矿物质类型、分布范围和沉积程度等因素。
矿物质沉积的诊断通常依靠影像学检查,如MRI扫描,以评估沉积的位置和程度。
治疗方法根据具体情况而定,可能包括药物治疗、康复训练和针对原发病的治疗。
需要强调的是,脑干矿物质沉积是一种病理状况,严重影响患者的生活质量。
如果遇到相关症状,建议尽快咨询医生进行全面评估和治疗。
本解答仅供参考,具体诊断和治疗需求专业医生进行判断。
特发性家族性脑血管亚铁钙沉着症

MMIBIMONTHLYVol13No.4Aug2004294。
2KingTD,MillsNL.Nonoperativeelosureofartrialseptaldefect.Surgery,1974;75:383—388.3李志中,韩玲,金梅等。
应用Amplatzer封堵器治疗动脉导管未闭。
中华心血管病杂志,2000,5:371。
373。
4张戈军,戴汝平,刘延龄等。
经导管置入CardioSEAL封堵器治疗房问隔缺损及其疗效评价。
中华心血管病杂志,2001,5:327~330。
5戴汝平,刘延龄,张戈军等。
应用Amplatzer封堵器治疗房间隔缺损疗效评价。
中华心血管病杂志,2000,28:87~92。
6张戈军,戴汝平,刘延玲等。
房间隔缺损封堵术后心功能的变化。
中华心血管病杂志,2001,29(3):163~166。
7徐立,戴汝平,刘延龄等。
Amplatzer法房间隔缺损封堵术一经食道超声心动图测量值选择封堵器的可能性。
中华心血管病杂志,2001,29:297—299。
8张玉奇,陈树宝,孙琨等。
双平而食管超声心动图在Am—platzer封堵器经心导管关闭小儿房间隔缺损中的价值。
中华超声影像学杂志,2001,10(11):651—653。
9朱振辉,刘延玲,戴汝平等。
经胸超声心动图监测引导经导管房间隔缺损封堵术的临床研究。
中华超声影像学杂志,2001,10(8):455—458。
特发性家族性脑血管亚铁钙沉着症武警陕西总队医院放射科(西安710054)陈毓秀徐杰牛灵芝特发性家族性脑血管亚铁钙沉着症,又称Fain(法氏病)或称家族性基底节钙化,它是以双侧基底节、丘脑、小脑齿状核及皮质下中枢对称性钙质沉着为主要病理学特征的疾病,临床资料报道较少,笔者在工作中遇到1例,现报道如下:患者男,60岁,以高血压心脏病收住院。
既往有头痴病史,为慢性钝痫。
查体:神清合作,一般状况好,神经系统及各脏器检查未见明显异常。
家族性特发性基底节区钙化的临床特点

家族性特发性基底节区钙化的临床特点葛义俊;宋苏琪;陈贵海【期刊名称】《临床神经病学杂志》【年(卷),期】2018(31)1【摘要】Objective To investigate the clinical features of familial idiopathic basal ganglia calcification (FIBGC).Methods Clinical data of 4 FIBGC patients from 2 families were analyzed retrospectively.Results The average age of 4 patients was(62.7 ±13.4)years old.The first symptom of 2 female patients was depression and schizophrenia, while 2 male patients displayed dementia and Parkinson's syndrome.Patients treated with vitamin D capsules,follow-up period for 3 to 6 months.All patients showed symptomatic improvement.Conclusions Clinical symptoms of FIBGC are complicated,and progressive development.The main symptom of female is mental symptoms, and male patients accompanied with dementia and dyskinesia.There is still no effective therapeutic plan for FIBGC.%目的探讨家族性特发性基底节钙化(FIBGC)患者的临床特征.方法回顾性分析2个家系4例FIBGC患者的临床资料.结果 4例患者平均发病年龄为(62.7 ±13.4)岁,2例女性分别以情绪障碍和精神行为异常为首发症状,2例男性患者则以认知障碍和帕金森综合征为突出表现.予以维生素D软胶囊治疗,并随访3~6个月,患者临床症状均有明显改善.结论 FIBGC患者临床症状复杂多样,呈进行性发展,女性患者以精神症状为主,而男性患者常伴有痴呆和运动障碍.目前尚缺乏有效的治疗方案.【总页数】4页(P57-60)【作者】葛义俊;宋苏琪;陈贵海【作者单位】238000 巢湖,安徽医科大学附属巢湖医院睡眠医学科;238000 巢湖,安徽医科大学附属巢湖医院睡眠医学科;238000 巢湖,安徽医科大学附属巢湖医院睡眠医学科【正文语种】中文【中图分类】R742.8【相关文献】1.中国人家族性特发性基底节钙化病(附一家系报道及文献复习) [J], 高伟;吴立文2.8个家族性特发性基底节钙化家系患者的临床研究 [J], 黄远桃;张伟;邹国英;李萍;周高雅;杨敏慧;向光红;周宏灏3.家族性特发性基底节钙化一家系报告 [J], 张嵘4.家族性特发性基底节钙化1例报告 [J], 郭亚珂;高艺伟;邢燕蒙;薛冰;刘沛东;刘洪波5.家族性特发性基底节钙化病3例 [J], 潘维花;李杰;谢秀娟因版权原因,仅展示原文概要,查看原文内容请购买。
《脑组织铁沉积神经变性病诊治专家共识》要点

《脑组织铁沉积神经变性病诊治专家共识》要点脑组织铁沉积神经变性病(neurodegeneration with brain iron accumulation,NBIA)是一组由基因突变导致的以锥体外系症状为主,伴有其他复杂临床症状,在脑组织特定部位可见异常铁沉积的罕见的神经遗传变性疾病,发病率在(1~3)/1 000 000。
尽管NBIA疾病谱系具有很高的临床和遗传异质性,但此类疾病在影像学尤其是磁共振(MRI)上因铁离子异常沉积而具有特征性的异常征象。
分子遗传学检测致病基因可以确诊。
NBIA疾病谱系中10个亚型已经明确了致病基因。
各亚型的命名推荐采用“突变蛋白相关性神经变性病”的模式来统一命名。
铁属于顺磁性物质,异常沉积在MRI上有特征性的表现。
在常规序列T2加权像及磁敏感系列,铁沉积部位显示低信号,在T1像铁沉积显示等信号。
常见铁沉积部位为苍白球、黑质、红核、丘脑等脑深部灰质核团。
但不是所有的NBIA疾病都会在MRI上显示铁沉积,也不是任何显示铁沉积的病例都属于NBIA疾病谱系。
一、NBIA疾病谱系(一)泛酸激酶相关性神经变性病(PKAN)根据发病年龄,PKAN可分为早发典型PKAN和晚发不典型PKAN。
1. 典型PKAN:10岁以前发病,90%病例在3~6岁发病。
首发症状多为步态障碍及姿势异常,少数病例以精神行为异常或视力障碍为首发症状。
2. 不典型PKAN:发病年龄跨度大,平均13~14岁,但也可成年发病,临床症状不典型。
常见表现为语言障碍、神经精神症状及运动障碍。
3. PKAN影像学特点:PKAN病例T相上可见苍白球部位铁沉积显示低信号,而在苍白球的前内侧由于神经元死亡、胶质增生而显示高信号,这一影像学表现被称为“虎眼征”。
(二)非钙依赖型磷脂酶A2相关性神经变性病(PLAN)PLAN有3个临床亚型1. 婴儿神轴索营养不良(INAD):发生于婴儿和儿童早期,通常在6月龄至3岁发病。
首发症状多为精神运动发育迟滞或倒退,继而出现肌无力、严重的躯干张力低下、小脑性共济失调、减反射减弱或消失、视神经萎缩致视力障碍、斜视、眼球震颤。
铁沉积

第四节铁沉积铁是重要的金属元素,在人体代谢中扮演着重要角色。
人体代谢过程中可能会出现铁沉积过多的问题,铁沉积可以是生理性的,也可能是病理性的。
MRI对铁含量的变化非常敏感,本节将简要介绍人体组织铁沉积的MRI信号特点。
主要介绍三个方面:(1)脑内铁沉积,(2)遗传性血色病,(3)继发性血色病。
一、脑内铁沉积生理性铁沉积常发生于脑内,特别是在脑的神经核团沉积比较明显。
研究表明新生儿脑组织内无明显铁沉积,随着年龄增加,脑组织各部在不同年龄段开始生理性铁沉积。
如苍白球的铁沉积始于6个月的婴儿,黑质始于9~12个月的婴儿,红核始于18~24个月的婴儿,小脑齿状核始于3~7岁。
各部位开始出现铁沉积的年龄不同,发展速度也存在差异,如苍白球的铁沉积开始就比较明显,而壳核开始时铁含量很低,以后随年龄增加逐渐增多,一般直到70岁左右其铁含量才与苍白球接近。
大脑和小脑的灰白质的生理性铁沉积很轻微,相对较高的为颞叶皮层下弓状纤维,其次为额叶脑白质和枕叶脑白质。
在内囊后肢及视放射则几乎没有铁沉积。
脑组织中这种铁选择性沉积的机理目前还不明了。
脑内一些疾病也可出现病理性的铁沉积,如早老性痴呆病人大脑皮层铁沉积增多,帕金森氏病患者的壳核和苍白球铁沉积增多,慢性血肿周围铁沉积增多等。
脑组织中的铁沉积主要在细胞内,细胞内的铁主要造成局部磁场的不均匀,从而加快质子失相位,因此在T2WI或T2*WI上组织信号减低。
在T1WI上往往信号变化不明显,或可呈轻微高信号,严重铁沉积者在T1WI上也可呈现低信号。
另外需要指出的是铁沉积造成的磁敏感效应在高场强MRI仪比较明显,因此比较容易显示,在低场强的MRI仪上较轻微铁沉积不能得以显示。
二、遗传性血色病遗传性血色并也称原发性血色病,为常染色体隐性遗传疾病。
主要问题是小肠粘膜吸收和转运到血中的铁过多。
血中的铁积少成多,并逐渐以铁蛋白的形式沉积于肝细胞、胰腺腺上皮细胞、心肌细胞、关节软骨细胞内等处。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
【读片时间】第1483期:特发性家族性脑血管铁钙质沉着症
特发性家族性脑血管铁钙质沉着症
(一)简要病史
男性,14岁。
发作性意识丧失、四肢僵直反复发作3年。
实验室检查:全段甲状旁腺素升高(iPTH 80.4pg/ml),钙减低(1.40mmol/L )。
(二)影像所见
头颅CT平扫示:双侧大脑半球、基底节区、丘脑及小脑齿状核见多发对称性的高密度钙化灶。
诊断:考虑Fahr病(家族性特发性脑血管亚铁钙沉着症)。
(三)解读思路
1.有无病变:根据CT表现病变明确。
2. 定位诊断:本例病变弥漫对称分布于双侧大脑半球及小脑实质。
3.定性诊断:双侧大脑半球皮髓质交界区、基底节区、丘脑、小脑齿状核及皮质下中枢见多发对称性钙化,结合临床病史,考虑Fahr 病(家族性特发性脑血管亚铁钙沉着症)。
4.鉴别诊断:结合临床表现及血生化检查,行家族调查大多可作出正确的诊断,但需与下列几种疾病鉴别:①甲状旁腺功能低下:其CT表现与本病相似,临床主要症状和体征与低血钙有关,大多发生在甲状腺或甲状旁腺手术后。
②结节性硬化:多表现为室管膜下多发结节状钙化,皮质下亦可结节状钙化。
临床表现多有癫痫、皮脂腺瘤、智力迟钝。
③维生素D中毒、铅中毒及放疗后钙化:根据特殊的检验指标及明确的病史可鉴别。
④科克因综合征:CT表现广泛对称性的脑内钙化,主要位于基底节区,以苍白球和尾状核头部为主,影像学表现相似,但本病是一种罕见的常染色体隐性遗传性疾病。
常于出生后6〜12个月发病,临床表现以光敏性皮炎及智力低下为主,结合发病年龄及典型的临床表现等可以鉴别。
⑤颅内感染性疾病:可出现钙化或痊愈后表现为钙化,以及苍白球和小脑齿状核等生理性钙化,也要作出相应鉴别。
(四)述评
特发性家族性脑血管铁耗质沉着症(idiopathic familial cerebral calcinosis of iron),最早由Fahr于1930年首先报道,故又称Fahr 综合征,发病年龄跨度大,各年龄段均有发生,部分有家族史。
表现及其多样,因脑内钙化的部位和程度而异,一般呈进行性发展。
常有缓慢进行性精神异常、智力减退、记忆力丧失,甚至痴呆;有语言障碍,有不同程度的癫痫发作,出现锥体外系症状,舞蹈症或偏身舞蹈症,空间定位能力差,以及各种神经症状,实验室检查血清钙磷正常,主要影像表现为脑内多发对称性钙化,以双侧基底节区、丘脑、小脑齿状核、大脑灰白质交界处较为常见,有时也见于小脑皮层、脑干及双侧半卵圆区深部。
脑内左右两侧钙化部位大致对称,钙化程度部分病例可表现不一致。
随着病程进展,钙化部位和程度相应增多和提高。
CT是发现颅内钙化的最佳检查方法。
