第七章气体动理论(答案)
第7章气体动理论习题解答

第7章 气体动理论7.1基本要求1.理解平衡态、物态参量、温度等概念,掌握理想气体物态方程的物理意义及应用。
2.了解气体分子热运动的统计规律性,理解理想气体的压强公式和温度公式的统计意义及微观本质,并能熟练应用。
3.理解自由度和内能的概念,掌握能量按自由度均分定理。
掌握理想气体的内能公式并能熟练应用。
4.理解麦克斯韦气体分子速率分布律、速率分布函数及分子速率分布曲线的物理意义,掌握气体分子热运动的平均速率、方均根速率和最概然速率的求法和意义。
5.了解气体分子平均碰撞频率及平均自由程的物理意义和计算公式。
7.2基本概念1 平衡态系统在不受外界的影响下,宏观性质不随时间变化的状态。
2 物态参量描述一定质量的理想气体在平衡态时的宏观性质的物理量,包括压强p 、体积V 和温度T 3 温度宏观上反映物体的冷热程度,微观上反映气体分子无规则热运动的剧烈程度。
4 自由度确定一个物体在空间的位置所需要的独立坐标数目,用字母i 表示。
5 内能理想气体的内能就是气体内所有分子的动能之和,即2iE RT ν= 6 最概然速率速率分布函数取极大值时所对应的速率,用p υ表示,p υ==≈其物理意义为在一定温度下,分布在速率p υ附近的单位速率区间内的分子在总分子数中所占的百分比最大。
7 平均速率各个分子速率的统计平均值,用υ表示,υ==≈8 方均根速率各个分子速率的平方平均值的算术平方根,用rms υ表示,rms υ==≈ 9 平均碰撞频率和平均自由程平均碰撞频率Z 是指单位时间内一个分子和其他分子平均碰撞的次数;平均自由程λ是每两次碰撞之间一个分子自由运动的平均路程,两者的关系式为:Zυλ==或λ=7.3基本规律1 理想气体的物态方程pV RT ν=或'm pV RT M=pV NkT =或p nkT =2 理想气体的压强公式23k p n ε=3 理想气体的温度公式21322k m kT ευ==4 能量按自由度均分定理在温度为T 的平衡态下,气体分子任何一个自由度的平均动能都相等,均为12kT 5 麦克斯韦气体分子速率分布律 (1)速率分布函数()dNf Nd υυ=表示在速率υ附近单位速率区间内的分子数占总分子数的百分比或任一单个分子在速率υ附近单位速率区间内出现的概率,又称为概率密度。
2022大学物理B-第7章气态动理论答案

第7章 气体动理论练习题一、选择题1、若理想气体的体积为V ,压强为p ,温度为T ,一个分子的质量为m ,R 是摩尔气体常量,k 称为玻耳兹曼常量,则该理想气体的分子数为[ B ](A) pV/m. (B) pV/(kT).(C) pV/(RT). (D) pV/(mT).2、下列各式中哪一式表示气体分子的平均平动动能?(式中M 为气体的质量,m 为气体分子质量,N 为气体分子总数目,n 为气体分子数密度,mol M 为摩尔质量,A N 为阿伏加得罗常量)[ A ] (A)pV M m 23. (B) pV M M mol 23. (C) npV 23. (D) pV N MM A 23mol . 3、根据经典的能量按自由度均分原理,每个自由度的平均能量为[ C ](A) kT /4. (B)kT /3.(C) kT /2. (D)kT.4、在20℃时,单原子理想气体的内能为[ D ](A)部分势能和部分动能. (B)全部势能. (C)全部转动动能.(D)全部平动动能. (E)全部振动动能.5、如果氢气和氦气的温度相同,摩尔数也相同,则[ B ](A)这两种气体的平均动能相同. (B)这两种气体的平均平动动能相同.(C)这两种气体的内能相等. (D)这两种气体的势能相等.6、在一密闭容器中,储有A 、B 、C 三种理想气体,处于平衡状态.A 种气体的分子数密度为n 1,它产生的压强为p 1,B 种气体的分子数密度为2n 1,C 种气体的分子数密度为3 n 1,则混合气体的压强p 为[D ](A) 3 p 1. (B) 4 p 1.(C) 5 p 1. (D) 6 p 1.7、在容积V =4×10-3 m 3的容器中,装有压强P =5×102 Pa 的理想气体,则容器中气体分子的平动动能总和为[B ](A) 2 J . (B) 3 J .(C) 5 J . (D) 9 J .8、若室内生起炉子后温度从15℃升高到27℃,而室内气压不变,则此时室内的分子数减少了[B ](A) 0.500. (B) 400.(B) 900. (D) 2100.9、麦克斯韦速率分布曲线如图所示,图中A 、B 两部分面积相等,则该图表示[ D ](A) 0v 为最概然速率.(B) 0v 为平均速率.(C) 0v 为方均根速率.(D) 速率大于和小于0v 的分子数各占一半.0 v二、填空题 1、有一个电子管,其真空度(即电子管内气体压强)为1.0×10-5 mmHg ,则27 ℃ 时管内单位体积的分子数为_________________ .(玻尔兹曼常量k =1.38×10-23 J/K , 1 atm=1.013×105 Pa =76 cmHg )解:nkT p =故3001038.176010013.1100.12355⨯⨯⨯⨯⨯⨯==--kT p n =3.2×1017 /m 32、图示曲线为处于同一温度T 时氦(原子量4)、氖(原子量20)和氩(原子量40)三种气体分子的速率分布曲线。
大学物理学第7章气体动理论(Temperature)

4
研究对象:大量无规则热运动气体分子构成的系统 研究内容:物质与冷热有关的性质及这些性质的变化
对象特点:单个分子 无序性、偶然性、遵循力学规律 整体(大量分子):服从统计规律
mvx
l2
立直角坐标系。
a
O
-mvx
X
(2)选任意一个分子a作为研
究对象,求其对A1面的压力 Z
l1
分子“a” 的速度:
分子“ a”碰撞器壁A1面一次所受的冲量:
由牛顿第三定律可知,器壁A1面受分子碰撞一次所受的冲量:
23
分子“ a”相继碰撞器壁A1面两次所用的时间为: 单位时间内,分子“ a”与器壁A1面碰撞的次数为: 单位时间内,分子“ a”对器壁A1面的冲量即冲力为:
如压强 p、体积 V、温度 T等 .
平衡态:一定量的气体,在不受外界的影响下, 经过一 定的时间, 系统达到一个稳定的, 宏观性质不随时间变 化的状态称为平衡态 .(理想状态)
平衡态的特点
( p,V ,T )
p
*( p,V ,T )
o
V
1)单一性(
处处相等);
2)物态的稳定性---与时间无关;
3)自发过程的终点;
(2)在平衡态下,分子按位置的分布是均匀的 n dN N
则各处分子数密度是相同的。
dV V
(3) 分子速度指向任何方向的机会是一样, 或分子速度按方向的分布是均匀的。
vx2 vy2 vz2
各个方向的速度分量的平均值相等。
vx 2
v1 x 2
07 气体动理论答案(2016)

一.选择题 1、[ A ](基础训练2)下列各式中哪一式表示气体分子的平均平动动能?(式中M 为气体的质量,m 为气体分子质量,N 为气体分子总数目,n 为气体分子数密度,N A 为阿伏加得罗常量)(A)pV M m 23. (B) pV M Mmol23.(C) npV 23. (D) pV N M M A 23mol . 【解】:根据气体分子的平均平动动能:201322k m v kT ε==,==N p nkT kT V ,而=M N m,则333==222k pV mkT pV N Mε= 2、[ B ](基础训练5)一定量某理想气体按pV 2=恒量的规律膨胀,则膨胀后理想气体的温度(A) 将升高. (B) 将降低. (C) 不变. (D)升高还是降低,不能确定. 【解】:由于pV 2=恒量,又=pVC T,则有=VT C ',因此,体积膨胀,温度将降低。
3、[ C ](基础训练8)设某种气体的分子速率分布函数为f (v ),则速率分布在v 1~v 2区间内的分子的平均速率为 (A)⎰21d )(v v v v v f . (B) 21()d v v v vf v v ⎰.(C)⎰21d )(v v v v v f /⎰21d )(v v v v f . (D)⎰21d )(v v v v v f /()d f v v ∞⎰.【解】:速率分布在v 1~v 2区间内的分子的速率总和:⎰21d )(v v v v v f N ,速率分布在v 1~v 2区间内的分子数总和:21()d v v Nf v v ⎰,因此速率分布在v 1~v 2区间内的分子的平均速率:222111222111()()()()v v v v v v v v v v v v vdN vNf v dv vf v dvv dNNf v dvf v dv===⎰⎰⎰⎰⎰⎰4、[ B ](基础训练9)一定量的理想气体,在温度不变的条件下,当体积增大时,分子的平均碰撞频率Z 和平均自由程λ的变化情况是:(A) Z 减小而λ不变. (B)Z 减小而λ增大. (C) Z 增大而λ减小. (D)Z 不变而λ增大.【解】:根据分子的平均碰撞频率:n v d Z22π=,和平均速率公式:v =,在温度不变的条件下,平均速率不变,当体积增大时,分子数密度Nn V=减小,平均碰撞频率Z 减小。
物理学教程(第二版)上册课后答案7

物理学教程(第二版)上册课后答案7第七章 气体动理论7 -1 处于平衡状态的一瓶氦气和一瓶氮气的分子数密度相同,分子的平均平动动能也相同,则它们( )(A) 温度,压强均不相同 (B) 温度相同,但氦气压强大于氮气的压强(C) 温度,压强都相同 (D) 温度相同,但氦气压强小于氮气的压强分析与解 理想气体分子的平均平动动能23k /kT =ε,仅与温度有关.因此当氦气和氮气的平均平动动能相同时,温度也相同.又由物态方程nkT p =,当两者分子数密度n 相同时,它们压强也相同.故选(C).7-2 三个容器A 、B 、C 中装有同种理想气体,其分子数密度n 相同,方均根速率之比()()()4:2:1::2/12C 2/12B 2/12A =v v v ,则其压强之比C B A ::p p p 为( )(A) 1∶2∶4 (B) 1∶4∶8(C) 1∶4∶16 (D) 4∶2∶1 分析与解 分子的方均根速率为M RT /3=2v ,因此对同种理想气体有3212C 2B 2A ::::T T T =v v v ,又由物态方程nkT ρ,当三个容器中分子数密度n 相同时,得16:4:1::::321321==T T T p p p .故选(C).7 -3 在一个体积不变的容器中,储有一定量的某种理想气体,温度为0T 时,气体分子的平均速率为0v ,分子平均碰撞次数为0Z ,平均自由程为0λ ,当气体温度升高为04T 时,气体分子的平均速率v 、平均碰撞频率Z 和平均自由程λ分别为( ) (A)04,4,4λλZ Z ===0v v (B) 0022λλ===,,Z Z 0v v (C) 00422λλ===,,Z Z 0v v (D) 00,2,4λλ===Z Z 0v v 分析与解 理想气体分子的平均速率M RT π/8=v ,温度由0T 升至04T ,则平均速率变为0v 2;又平均碰撞频率v n d Z 2π2=,由于容器体积不变,即分子数密度n 不变,则平均碰撞频率变为0Z 2;而平均自由程n d 2π21=λ,n 不变,则λ也不变.因此正确答案为(B).7 -5 有一个体积为35m 1001⨯.的空气泡由水面下m050.深的湖底处(温度为C 0.4o )升到湖面上来.若湖面的温度为C 017o .,求气泡到达湖面的体积.(取大气压强为Pa 10013150⨯=.p )分析 将气泡看成是一定量的理想气体,它位于湖底和上升至湖面代表两个不同的平衡状态.利用理想气体物态方程即可求解本题.位于湖底时,气泡内的压强可用公式gh pp ρ+=0求出, 其中ρ为水的密度( 常取33m kg 100.1-⋅⨯=ρ).解 设气泡在湖底和湖面的状态参量分别为(p 1 ,V 1 ,T 1 )和(p 2 ,V 2 ,T 2 ).由分析知湖底处压强为gh ρp gh ρp p+=+=021,利用理想气体的物态方程222111T V p T V p =可得空气泡到达湖面的体积为()3510120121212m 1011.6-⨯=+==T p V T gh p T p V T p V ρ 7 -6 一容器内储有氧气,其压强为Pa 100115⨯.,温度为27 ℃,求:(1)气体分子的数密度;(2) 氧气的密度;(3) 分子的平均平动动能;(4) 分子间的平均距离.(设分子间均匀等距排列)分析 在题中压强和温度的条件下,氧气可视为理想气体.因此,可由理想气体的物态方程、密度的定义以及分子的平均平动动能与温度的关系等求解.又因可将分子看成是均匀等距排列的,故每个分子占有的体积为30d V=,由数密度的含意可知n V /10=,d 即可求出.解 (1) 单位体积分子数325m 1044.2⨯==kTp n (2) 氧气的密度3-m kg 30.1/⋅===RTpM V m ρ (3) 氧气分子的平均平动动能J 102162321k -⨯==./kT ε(4) 氧气分子的平均距离m 10453193-⨯==./n d通过对本题的求解,我们可以对通常状态下理想气体的分子数密度、平均平动动能、分子间平均距离等物理量的数量级有所了解.7-7 2.0×10-2 kg 氢气装在4.0×10-3 m 3 的容器内,当容器内的压强为3.90×105Pa 时,氢气分子的平均平动动能为多大?分析 理想气体的温度是由分子的平均平动动能决定的,即23k /kT =ε.因此,根据题中给出的条件,通过物态方程pV =Mm 'RT ,求出容器内氢气的温度即可得kε. 解 由分析知氢气的温度mRMpV T =,则氢气分子的平均平动动能为J 1089.3232322k -⨯='==Rm pVMk kT ε7 -8 某些恒星的温度可达到约1.0 ×108K ,这是发生聚变反应(也称热核反应)所需的温度.通常在此温度下恒星可视为由质子组成.求:(1) 质子的平均动能是多少? (2) 质子的方均根速率为多大?分析 将组成恒星的大量质子视为理想气体,质子可作为质点,其自由度 i =3,因此,质子的平均动能就等于平均平动动能.此外,由平均平动动能与温度的关系2/32/2kT m =v,可得方均根速率2v .解 (1) 由分析可得质子的平均动能为 J 1007.22/32/152k-⨯===kT m v ε (2) 质子的方均根速率为1-62s m 1058.13⋅⨯==mkT v 7 -9 日冕的温度为2.0 ×106K ,所喷出的电子气可视为理想气体.试求其中电子的方均根速率和热运动平均动能.解 方均根速率16e 2s m 105.93-⋅⨯==m kT v 平均动能J 10142317k -⨯==./kT ε7-10 在容积为2.0 ×10-3 m 3 的容器中,有内能为6.75 ×102J 的刚性双原子分子某理想气体.(1)求气体的压强;(2) 设分子总数为5.4×1022个,求分子的平均平动动能及气体的温度.分析 (1) 一定量理想气体的内能RT i M m E 2=,对刚性双原子分子而言,i =5.由上述内能公式和理想气体物态方程pV =νRT 可解出气体的压强.(2)求得压强后,再依据题给数据可求得分子数密度,则由公式p =nkT 可求气体温度.气体分子的平均平动动能可由23k /kT ε=求出.解 (1) 由RT i E 2ν=和pV =νRT 可得气体压强 Pa 1035.125⨯==iVE p (2) 分子数密度n =N/V ,则该气体的温度()()K 1062.3//2⨯===nk pV nk p T 气体分子的平均平动动能为J104972321k -⨯==./kT ε 7 -11 当温度为0C 时,可将气体分子视为刚性分子,求在此温度下:(1)氧分子的平均动能和平均转动动能;(2)kg 100.43-⨯氧气的内能;(3)kg 100.43-⨯氦气的内能.分析 (1)由题意,氧分子为刚性双原子分子,则其共有5个自由度,其中包括3个平动自由度和2个转动自由度.根据能量均分定理,平均平动动能kT 23kt =ε,平均转动动能kT kT ==22kr ε.(2)对一定量理想气体,其内能为RT i M mE 2'=,它是温度的单值函数.其中i 为分子自由度,这里氧气i =5、氦气i =3.而m '为气体质量,M 为气体摩尔质量,其中氧气13mol kg 1032--⋅⨯=M ;氦气13mol kg 100.4--⋅⨯=M .代入数据即可求解它们的内能.解 根据分析当气体温度为T=273 K 时,可得(1)氧分子的平均平动动能为J 107.52321kt -⨯==kT ε 氧分子的平均转动动能为J 108.32221kr -⨯==kT ε (2)氧气的内能为J 10 7.1J 27331.8251032100.42233⨯=⨯⨯⨯⨯⨯='=--RT i M m E (3)氦气的内能为J 10 3.4J 27331.823100.4100.42333⨯=⨯⨯⨯⨯⨯='=--RT i M m E 7 -12 已知质点离开地球引力作用所需的逃逸速率为gr v 2=,其中r 为地球半径.(1) 若使氢气分子和氧气分子的平均速率分别与逃逸速率相等,它们各自应有多高的温度;(2) 说明大气层中为什么氢气比氧气要少.(取r =6.40 ×106 m) 分析 气体分子热运动的平均速率M RTπ8=v ,对于摩尔质量M 不同的气体分子,为使v 等于逃逸速率v ,所需的温度是不同的;如果环境温度相同,则摩尔质量M 较小的就容易达到逃逸速率. 解 (1) 由题意逃逸速率gr 2=v ,而分子热运动的平均速率M RTπ8=v .当v v = 时,有RMrg T 4π= 由于氢气的摩尔质量13H mol kg 10022--⋅⨯=.M,氧气的摩尔质量12O mol kg 10232--⋅⨯=.M ,则它们达到逃逸速率时所需的温度分别为 K10891K,101815O 4H 22⨯=⨯=..T T (2) 根据上述分析,当温度相同时,氢气的平均速率比氧气的要大(约为4倍),因此达到逃逸速率的氢气分子比氧气分子多.按大爆炸理论,宇宙在形成过程中经历了一个极高温过程.在地球形成的初期,虽然温度已大大降低,但温度值还是很高.因而,在气体分子产生过程中就开始有分子逃逸地球,其中氢气分子比氧气分子更易逃逸.另外,虽然目前的大气层温度不可能达到上述计算结果中逃逸速率所需的温度,但由麦克斯韦分子速率分布曲线可知,在任一温度下,总有一些气体分子的运动速率大于逃逸速率.从分布曲线也可知道在相同温度下氢气分子能达到逃逸速率的可能性大于氧气分子.故大气层中氢气比氧气要少.7-13 容积为1 m 3 的容器储有1 mol 氧气,以v =10-1s m ⋅的速度运动,设容器突然停止,其中氧气的80%的机械运动动能转化为气体分子热运动动能.试求气体的温度及压强各升高了多少. 分析 容器作匀速直线运动时,容器内分子除了相对容器作杂乱无章的热运动外,还和容器一起作定向运动.其定向运动动能(即机械能)为221mv .按照题意,当容器突然停止后,80%定向运动动能转为系统的内能.对一定量理想气体内能是温度的单值函数,则有关系式:T R M m v m E Δ25%8021Δ2'=⋅'=成立,从而可求ΔT .再利用理想气体物态方程,可求压强的增量.解 由分析知T R M m m E Δ2528.0Δ2⋅'='=v ,其中m '为容器内氧气质量.又氧气的摩尔质量为12m ol kg 1023--⋅⨯=.M ,解得ΔT =6.16 ×10-2 K当容器体积不变时,由pV =M mRT 得Pa 51.0ΔΔ==T VRM m p7-14 有N 个质量均为m 的同种气体分子,它们的速率分布如图所示.(1) 说明曲线与横坐标所包围的面积的含义;(2) 由N 和0v 求a 值;(3) 求在速率0v /2到30v /2 间隔内的分子数;(4) 求分子的平均平动动能.题 7-14 图分析 处理与气体分子速率分布曲线有关的问题时,关键要理解分布函数()v f 的物理意义.()υd d N Nf =v ,题中纵坐标()v v d /d N Nf =,即处于速率v 附近单位速率区间内的分子数.同时要掌握()v f 的归一化条件,即()1d 0=⎰∞v v f .在此基础上,根据分布函数并运用数学方法(如函数求平均值或极值等),即可求解本题.解 (1) 由于分子所允许的速率在0 到20v 的范围内,由归一化条件可知图中曲线下的面积()N Nf S v ==⎰v v d 020即曲线下面积表示系统分子总数N .(2 ) 从图中可知,在0 到0v 区间内,()0/v v v a Nf =;而在0 到20v 区间,()αNf =v .则利用归一化条件有vv v vv ⎰⎰+=0020d d v v a a N(3) 速率在0v /2到30v /2间隔内的分子数为12/7d d Δ2/3000N a a N =+=⎰⎰v v v v v v v(4) 分子速率平方的平均值按定义为()v v f v v v d /d 0222⎰⎰∞∞==N N故分子的平均平动动能为20220302k 3631d d 212100v v v v v v v v v v m N a N a m m =⎥⎦⎤⎢⎣⎡+==⎰⎰ε 7-15 一飞机在地面时,机舱中的压力计指示为Pa100115⨯.,到高空后压强降为Pa101184⨯..设大气的温度均为27.0℃.问此时飞机距地面的高度为多少?(设空气的摩尔质量为2.89 ×10-2kg·mol -1) 分析 当温度不变时,大气压强随高度的变化主要是因为分子数密度的改变而造成.气体分子在重力场中的分布满足玻耳兹曼分布.利用地球表面附近气压公式()kT mgh p p /ex p 0-=,即可求得飞机的高度h .式中p 0 是地面的大气压强. 解 飞机高度为()()m 1093.1/ln /ln 300⨯===p p MgRT p p mg kT h7 -16 目前实验室获得的极限真空约为1.33×10-11Pa ,这与距地球表面1.0×104km 处的压强大致相等.而电视机显像管的真空度为1.33×10-3Pa ,试求在27 ℃时这两种不同压强下单位体积中的分子数及分子的平均自由程.(设气体分子的有效直径d =3.0×10-8cm)解 理想气体分子数密度和平均自由程分别为n =k T p ;pd kT λ2π2=,压强为1.33×10-11Pa 时,-39m 1021.3/⨯==kT p nm 108.7π282⨯==pd kT λ 从λ的值可见分子几乎不发生碰撞.压强为1.33×10-3Pa 时,3-17m 1021.3⨯==kT p n ,m 8.7π22==pd kT λ此时分子的平均自由程变小,碰撞概率变大.但相对显像管的尺寸而言,碰撞仍很少发生. 7-17 在标准状况下,1 cm 3中有多少个氮分子?氮分子的平均速率为多大?平均碰撞次数为多少?平均自由程为多大?(已知氮分子的有效直径m 1076.310-⨯=d )分析 标准状况即为压强Pa 10013.15⨯=p ,温度K 273=T .则由理想气体物态方程nkT p =可求得气体分子数密度n ,即单位体积中氮分子的个数.而氮气分子的平均速率、平均碰撞次数和平均自由程可分别由公式MRTv π8=,n v d Z 2π2=和nd 2π21=λ直接求出.解 由分析可知,氮分子的分子数密度为325m 1069.2-⨯==kTpn 即3cm 1中约有191069.2⨯个.氮气的摩尔质量为M =28 ×10-3kg·mol -1,其平均速率为MRTv π8==454 1s m -⋅则平均碰撞次数为-192s 107.7π2⨯==n v d Z平均自由程为m 106π2182-⨯==nd λ 讨论 本题主要是对有关数量级有一个具体概念.在通常情况下,气体分子平均以每秒几百米的速率运动着,那么气体中进行的一切实际过程如扩散过程、热传导过程等好像都应在瞬间完成,而实际过程都进行得比较慢,这是因为分子间每秒钟上亿次的碰撞导致分子的自由程只有几十纳米,因此宏观上任何实际过程的完成都需要一段时间.7-18 在一定的压强下,温度为20℃时,氩气和氮气分子的平均自由程分别为9.9×10-8m 和27.5×10-8m.试求:(1) 氩气和氮气分子的有效直径之比;(2) 当温度不变且压强为原值的一半时,氮气分子的平均自由程和平均碰撞频率. 分析 ( 1 ) 气体分子热运动的平均自由程()p d kT nd 22π2/π21==λ,因此,温度、压强一定时,平均自由程2/1d λ∝.(2) 当温度不变时,平均自由程p λ/1∝.解 (1) 由分析可知67.1//r 22r A N N A ==λλd d(2) 由分析可知氮气分子的平均自由程在压强降为原值的一半时,有m 105.527N N22-⨯=='λλ而此时的分子平均碰撞频率22222N N N N N 2π/8λM RT λZ ='=v将T =293K ,M N2 =2.8×10-2kg·mol -1代入,可得-18N s 1056.82⨯=Z。
《大学物理学》(网工)气体的动理论部分练习题(解答)

然 速 率 为 ___________ ; 氧 气 分 子 的 最 概 然 速 率 为
___________。
【 提 示 : P 2RT 。 由 于 温 度 一 样 , 而 P1 P2 , ∴ O
M mol
2000
(m s1)
M1 M 2 ,可判明曲线Ⅰ是氧气、曲线Ⅱ是氢气,氢气的最概然速率为 (P )H2 2000 m / s ;
(A)氧分子的质量比氢分子大,所以氧气的压强一定大于氢气的压强;
(B)氧分子的质量比氢分子大,所以氧气的数密度一定大于氢气的数密度;
(C)氧分子的质量比氢分子大,所以氢分子的速率一定大于氧分子的速率;
(D)氧分子的质量比氢分子大,所以氢分子的方均根速率一定大于氧分子的方均根速率。
【提示:氢气和氧气不同的是其摩尔质量, M O2 M H2 ,由公式 P nkT ,所以 PO2 PH2 ;某一分
M M mol
,m
M mol NA
,有A】
拓展题:若理想气体的体积为V,压强为P,温度为T,一个分子的质量为m,k为玻耳兹曼常
量,R为摩尔气体常量,则该理想气体的分子数为 ( B )
(A) PV / m ; (B) PV /(kT ) ; (C) PV /(RT ) ; (D) PV /(mT ) 。
5 . 一 容 器 内 的 氧 气 的 压 强 为 1.01 105 P a , 温 度 为 37℃ , 则 气 体 分 子 的 数 密 度
,
M mol
RT
1.60
,
M mol
2
3RT
pV RT
M mol
,考虑到
M
M mol
大学物理(科学出版社,熊天信、蒋德琼、冯一兵、李敏惠)第七、八章习题解

第七章 气体动理论7–1 一定量的理想气体,在保持温度T 不变的情况下,使压强由P 1增大到P 2,则单位体积内分子数的增量为_________________。
解:由nkT P =,可得单位体积内分子数的增量为kTP P kT P n 12-=∆=∆ 7–2 一个具有活塞的圆柱形容器中贮有一定量的理想气体,压强为P ,温度为T ,若将活塞压缩并加热气体,使气体的体积减少一半,温度升高到2T ,则气体压强增量为_______,分子平均平动动能增量为_________。
解:设经加热和压缩后气体的压强为P ',则有TV P T PV 22/⨯'=所以P P 4='压强增量为P P P P 3=-'=∆由分子平均平动动能的计算公式kT 23=ε知分子平均平动动能增量为kT 23。
7–3 从分子动理论导出的压强公式来看,气体作用在器壁上的压强,决定于 和 。
解:由理解气体的压强公式k 32εn P =,可知答案应填“单位体积内的分子数n ”,“分子的平均平动动能k ε”。
7–4 气体分子在温度T 时每一个自由度上的平均能量为 ;一个气体分子在温度T 时的平均平动动能为 ;温度T 时,自由度为i 的一个气体分子的平均总动能为 ;温度T 时,m /M 摩尔理想气体的内能为 。
解:kT 21;kT 23;kT i2;RT i M m 27–5 图7-1所示曲线为处于同一温度T 时氦(原子量4)、氖(原子量20)和氩(原子量40)三种气体分子的速率分布曲线,其中曲线(a )是__________气分子的速率分布曲线; 曲线(c )是__________气分子的速率分布曲线。
解:在相同温度下,对不同种类的气体,分子质量大的,速率分布曲线中的最慨然速率p v 向量值减小方向迁移。
可得图7-1中曲线(a )是氩气分子的速率分布曲线,图7-1中曲线(c )是氦气分子的速率分布曲线。
7–6 声波在理想气体中传播的速率正比于气体分子的方均根速率。
气体动理论

1质量为 m 摩尔质量为 M 的理想气体,在平衡态下,压强 p、体积 V 和热力学温度 T 的关系 式是 A、pV=(M/m)RT B、pT=(M/m)RV C、pV=(m/M)RT D、VT=(m/M)Rp 正确答案: C 我的答案:C 得分: 9.1 分2一定量某理想气体按 =恒量的规律膨胀,则膨胀后理想气体的温度 A、将降低 B、将升高 C、保持不变 D、升高还是降低,不能确定正确答案: A 我的答案:A 得分: 9.1 分3在标准状态下,任何理想气体每立方米中含有的分子数都等于 A、 B、 C、 D、 正确答案: C 我的答案:A 得分: 0.0 分 4 有一截面均匀的封闭圆筒,中间被一光滑的活塞分隔成两边,如果其中的一边装有 0.1 kg 某一温度的氢气,为了使活塞停留在圆筒的正中央,则另一边应装入同一温度的氧气的质量 为 A、0.16 kg B、0.8 kg C、1.6 kg D、3.2 kg 正确答案: C 我的答案:C 得分: 9.1 分5若理想气体的体积为 V,压强为 p,温度为 T,一个分子的质量为 m,k 为玻尔兹曼常量, R 为普适气体常量,则该理想气体的分子数为 A、pV / m B、pV / (kT) C、pV / (RT) D、pV / (mT) 正确答案: B 我的答案:C 得分: 0.0 分6一定量的理想气体在平衡态态下,气体压强 p、体积 V 和热力学温度 T 的关系式是 A、 B、 C、 D、 正确答案: C 我的答案:C 得分: 9.1 分 7 某理想气体在温度为 27℃和压强为 1.0×10-2atm 情况下,密度为 11.3g/m3,则这气体的 摩尔质量 Mmol=______g/mol。
正确答案:第一空: 27.8-28我的答案: 得分: 0.0 分第一空: 0.0113批语 8热力学温度 T 和摄氏温度 t 的关系是 T=t+_________(取整数) 正确答案:第一空:273我的答案: 得分: 9.1 分 第一空: 273批语 9质量为 m、摩尔质量为 M 的理想气体,处于平衡态时,状态方程写为这 pV=(m/M)________, 状态方程的另一形式为 p=nkT,其中 n 是理想气体的________,k 称为________常数。
气体动理论习习题解答

欢迎阅读习题8-1 设想太阳是由氢原子组成的理想气体,其密度可当成是均匀的。
若此理想气体的压强为1.35×1014 Pa 。
试估计太阳的温度。
(已知氢原子的质量m = 1.67×10-27 kg ,太阳半径R = 6.96×108 m ,太阳质量M = 1.99×1030 kg ) 解:m R M Vm M m n 3π)3/4(===ρ8-2 目前已可获得1.013×10-10 Pa 的高真空,在此压强下温度为27℃的1cm 3体积内有多少个解:8-3 (1∑t εn p i =∑8-4 气的解:8-5 温度从27 ℃上升到177 ℃,体积减少一半,则气体的压强变化多少?气体分子的平均平动动能变化多少?分子的方均根速率变化多少?解:已知 K 300atm 111==T p 、根据RT pV ν=⇒222111T V p T V p =⇒atm 3312==p p8-6 温度为0 ℃和100 ℃时理想气体分子的平均平动动能各为多少?欲使分子的平均平动动能等于1 eV ,气体的温度需多高?解:(1)J 1065.515.2731038.12323212311--⨯=⨯⨯⨯==kT t ε (2)kT 23J 101.6ev 1t 19-==⨯=ε 8-7 一容积为10 cm 3的电子管,当温度为300 K 时,用真空泵把管内空气抽成压强为5×10-4 mmHg 的高真空,问此时(1)管内有多少空气分子?(2)这些空气分子的平均平动动能的总和是多少?(3)平均转动动能的总和是多少?(4)平均动能的总和是多少?(将空气分子视为刚性解:(1(2(3(48-8 也就是解:8-9 3。
求:(1和转动动能各为多少?(4)容器单位体积内分子的总平动动能是多少?(5)若该气体有0.3 mol ,其内能是多少?解:(1)231v p ρ=⇒m/s 49432≈=ρp v (2)g 28333⇒322≈===ρμμpRT v RTRTv 所以此气体分子为CO 或N 2(3)J 1065.52321-⨯==kT t ε (4)J 1052.123233∑⨯===P kT n t ε (5)J 170125==RT E ν 8-10 一容器内储有氧气,其压强为1.01×105 Pa ,温度为27.0℃,求:(1)分子数密度;(2)氧气的密度;(3)分子的平均平动动能;(4)分子间的平均距离。
2013第七章气体动理论答案 (1)

一. 选择题1. (基础训练2)[ C ]两瓶不同种类的理想气体,它们的温度和压强都相同,但体积不同,则单位体积内的气体分子数n ,单位体积内的气体分子的总平动动能(E K /V ),单位体积内气体的质量?的关系为: (A) n 不同,(E K /V )不同,??不同. (B) n 不同,(E K /V )不同,??相同. (C) n 相同,(E K /V )相同,??不同. (D) n 相同,(E K /V )相同,??相同. 【解】: ∵nkT p =,由题意,T ,p 相同∴n 相同;∵kTn V kTNVE k2323==,而n ,T 均相同∴V E k 相同 由RT M m pV =得m pMV RTρ==,∵不同种类气体M 不同∴ρ不同 2. (基础训练6)[ C ]设v 代表气体分子运动的平均速率,p v 代表气体分子运动的最概然速率,2/12)(v 代表气体分子运动的方均根速率.处于平衡状态下理想气体,三种速率关系为(A) p v v v ==2/12)( (B) 2/12)(v v v <=p(C) 2/12)(v v v <<p(D)2/12)(vvv>>p【解】:最概然速率:pv==算术平均速率:()v vf v dv∞==⎰2()v f v dv∞==⎰3.(基础训练7)[B]设图7-3所示的两条曲线分别表示在相同温度下氧气和氢气分子的速率分布曲线;令()2Opv和()2H p v分别表示氧气和氢气的最概然速率,则(A)图中a表示氧气分子的速率分布曲线;()2Opv/()2H p v=4.(B)图中a表示氧气分子的速率分布曲线;()2Opv/()2H p v=1/4.(C)图中b表示氧气分子的速率分布曲线;()2O p v/()2H p v=1/4.(D)图中b表示氧气分子的速率分布曲线;()2O p v/()2H p v= 4.【解】:理想气体分子的最概然速率pv=pv越小,又由氧气的摩尔质量33210(/)M kg mol-=⨯,氢气的摩尔质量3210(/)M kg mol-=⨯,可得()2Opv/()2H p v=1/4。
第七章 气体动理论(答案)

一、选择题[ C ]1、(基础训练2)两瓶不同种类的理想气体,它们的温度和压强都相同,但体积不同,则单位体积内的气体分子数n ,单位体积内的气体分子的总平动动能(E K /V ),单位体积内气体的质量ρ的关系为:(A) n 不同,(E K /V )不同,ρ 不同.(B) n 不同,(E K /V )不同,ρ 相同. (C) n 相同,(E K /V )相同,ρ 不同.(D) n 相同,(E K /V )相同,ρ 相同. 【提示】① ∵nkT p =,由题意,T ,p 相同,∴n 相同;② ∵kT n V kTNV E k 2323==,而n ,T 均相同,∴V E k 相同;③ RT M MpV mol=→RT pM V M mol ==ρ,T ,p 相同,而mol M 不同,∴ρ不同。
[ B ]2、(基础训练7)设图示的两条曲线分别表示在相同温度下氧气和氢气分子的速率分布曲线;令()2O p v 和()2H p v 分别表示氧气和氢气的最概然速率,则(A) 图中a 表示氧气分子的速率分布曲线;()2O p v /()2H p v = 4.(B) 图中a 表示氧气分子的速率分布曲线;()2O p v /()2H p v =1/4.(C) 图中b表示氧气分子的速率分布曲线;()2O p v /()2H p v =1/4.(D) 图中b表示氧气分子的速率分布曲线;()2O p v /()2H p v = 4.【提示】①最概然速率p v =p v 越小,故图中a 表示氧气分子的速率分布曲线;②23,3210(/)mol O M kg mol -=⨯, 23,210(/)mol H M kg mol -=⨯,得()()22Ov v p p H14=[ C ]3、(基础训练8)设某种气体的分子速率分布函数为f (v ),则速率分布在v 1~v 2区间内的分子的平均速率为(A)⎰21d )(v v v v v f . (B) 21()d v v v vf v v ⎰.(C)⎰21d )(v v v v v f /⎰21d )(v v v v f . (D)⎰21d )(v v v v v f /0()d f v v ∞⎰ .【提示】① f (v )d v ——表示速率分布在v 附近d v 区间内的分子数占总分子数的百分比;② ⎰21)(v v dv v Nf ——表示速率分布在v 1~v 2区间内的分子数总和;③21()v v vNf v dv ⎰表示速率分布在v 1~v 2区间内的分子的速率总和,因此速率分布在v 1~v 2区间内的分子的平均速率为22112211()()()()v v v v v v v v vNf v dv vf v dvNf v dvf v dv=⎰⎰⎰⎰[ B ]4、(基础训练9)一定量的理想气体,在温度不变的条件下,当体积增大时,分子的平均碰撞频率Z 和平均自由程λ的变化情况是:(A) Z 减小而λ不变. (B) Z 减小而λ增大. (C) Z 增大而λ减小. (D) Z 不变而λ增大.【提示】①2Z d n =,其中v =不变;N n V =,当V 增大时,n 减小; ∴Z 减小。
大学物理(气体动理论)习题答案

大学物理(气体动理论)习题答案8-1 目前可获得的极限真空为Pa 1033.111-⨯,,求此真空度下3cm 1体积内有多少个分子?(设温度为27℃)[解] 由理想气体状态方程nkT P =得 kT V NP =,kT PV N =故 323611102133001038110110331⨯=⨯⨯⨯⨯⨯=---...N (个)8-2 使一定质量的理想气体的状态按V p -图中的曲线沿箭头所示的方向发生变化,图线的BC 段是以横轴和纵轴为渐近线的双曲线。
(1)已知气体在状态A 时的温度是K 300=A T ,求气体在B 、C 、D 时的温度。
(2)将上述状态变化过程在 T V -图(T 为横轴)中画出来,并标出状态变化的方向。
[解] (1)由理想气体状态方程PV /T =恒量,可得:由A →B 这一等压过程中BBA A T V T V = 则 6003001020=⋅=⋅=A AB B T V V T (K) 因BC 段为等轴双曲线,所以B →C 为等温过程,则==B C T T 600 (K)C →D 为等压过程,则CCD D T V T V = 3006004020=⋅=⋅=C CD D T V V T (K) (2)8-3 有容积为V 的容器,中间用隔板分成体积相等的两部分,两部分分别装有质量为m 的分子1N 和2N 个, 它们的方均根速率都是0υ,求: (1)两部分的分子数密度和压强各是多少?(2)取出隔板平衡后最终的分子数密度和压强是多少?010203040[解] (1) 分子数密度 VNV N n VN V N n 2222111122====由压强公式:231V nm P =, 可得两部分气体的压强为 VV mN V m n P VV mN V m n P 3231323120220222012011====(2) 取出隔板达到平衡后,气体分子数密度为 VN N V N n 21+==混合后的气体,由于温度和摩尔质量不变,所以方均根速率不变,于是压强为:VV m N N V nm P 3)(31202120+==8-4 在容积为33m 105.2-⨯的容器中,储有15101⨯个氧分子,15104⨯个氮分子,g 103.37-⨯氢分子混合气体,试求混合气体在K 433时的压强。
大学物理试题精选2

⼤学物理试题精选2第七章⽓体动理论⼀、热学基础1. 下列各量是微观量是:A .PB .EC .D .V2.下列各量是宏观量是:A.TB.vC.mD.w3.平衡态就是所有分⼦都静⽌的状态.( × )4.令⾦属棒的⼀端插⼊冰⽔混合的容器,另⼀端与沸⽔接触,待⼀段时间后棒上各处温度不随时间变化,此时⾦属棒处于平衡态。
()答案: 4. ×⼆、理想⽓体的压强和温度1. 理想⽓体的压强公式为A .w n 31; B . w n 32; C . w n ; D . w n 21。
2.⼀定量的理想⽓体,当其体积变为原来的三倍,⽽分⼦的平均平动动能变为原来的6倍时,则压强变为原来的:A .9倍B .2倍C .3倍D .4倍3.容器内贮有1摩尔氢⽓和1摩尔氦⽓,若两种⽓体各⾃对器壁产⽣的压强分别为p 1和p 2,则两者的⼤⼩关系是()A .p 1>p 2B .p 1<p 2C .p 1= p 2D .不确定4.温度的测量是建⽴在哪个定理基础上的:A .热⼒学第⼀定律 B.热⼒学第⼆定律C.热⼒学第三定律D.热⼒学第零定律5.关于温度的意义,下述说法中不正确的是:A .⽓体的温度是分⼦平均平动能的量度B .⽓体的温度表⽰单个⽓体分⼦的冷热强度C .⽓体的温度是⼤量⽓体分⼦热运动的集体表现,具有统计意义D .温度的⾼低反映物质内部分⼦热运动剧烈程度的不同三、能量按⾃由度均分、理想⽓体内能公式:1.在平⾯上运动的质点的⾃由度为()A . 2;B . 5;C . 3;D . 6。
2. 分⼦的平均平动动能⽤温度表⽰的公式是 3/2kT ,设理想⽓体的温度为T ,⾃由度为i 理想⽓体分⼦的平均总动能公式为 i/2kT 。
3. 刚性氧⽓分⼦和氨⽓分⼦的⾃由度分别是 5 , 6 ;对应的分⼦平均平动动能分别是 3/2kT , 3/2kT 。
4.温度为T 时,刚性氧⽓分⼦和氦⽓分⼦的平均平动动能分别为 3/2kT 和 3/2kT 。
气体动理论习题答案及解法(2010.12.15)

气体动理论习题、答案及解法一、 选择题1. 一定量氢气(视为刚性分子的理想气体),若温度每升高1K ,其内能增加20.8J ,则该氢气的质量为 【 B 】 (A )1.0⨯10kg 3- (B)2.0⨯10kg 3-(C)3.0⨯10kg 3- (D)4.0⨯10kg 3-参考答案:T R i M E ∆⎪⎭⎫⎝⎛=∆2μ 5=i 刚性双原子的自由度为 ()kg 100.2131.851028.202233--⨯=⨯⨯⨯⨯⨯=∆⋅∆=T iR E M μ2. 有一瓶质量为m 的氢气(是作刚性双原子分子的理想气体),温度为T ,则氢分子的平均动能 【 B 】 (A )kT 23(B )kT 25 (C ) RT 23 (D )RT 25参考答案:kT i2=ε 5=i 刚性双原子的自由度为 3. 有两瓶气体,一瓶是氦气,另一瓶是氢气(均视为刚性分子理想气体),若它们的压强、体积、温度均相同,则氢气的内能是氦气的 【 C 】 (A )21倍 (B )32倍 (C )35倍 (D )2倍参考答案:T R i M E ⎪⎭⎫ ⎝⎛=2μ RT MpV μ=3522222==⎪⎪⎭⎫⎝⎛⎪⎪⎭⎫⎝⎛=e e eH H H H H H i i T R i M T R i M E E μμ4. A 、B 、C3个容器中皆装有理想气体,它们的分子数密度之比为A n :Bn :C n =4:2:1,而分子的平均平动动能之比为4:2:1::=C B A εεε,则它们的压强之比C B A p p p :::为 【 A 】(A )1:1:1 (B)1:2;2 (C )1:2;3 (D )1:2;4参考答案:εn p 32=1:1:132:32:32:::==C C B B A A C B A n n n p p p εεε 5. 2g 氢气与2g 氦气分别装在两个容器相等的封闭容器内,温度也相同(氢气分子视为刚性双原子分子),氢气与氦气内能之比eH H E E 2为(A )31 (B )35 (C )310 (D)316 【 C 】参考答案:T R i M E ⎪⎭⎫⎝⎛=2μ31010231045223322222=⨯⨯⨯⨯==⎪⎪⎭⎫ ⎝⎛⎪⎪⎭⎫⎝⎛=--H H H H H H H H H H e e e e ei i T R i M T R i M E E μμμμ 6.1mol 的单原子分子理想气体,在1atm 的恒定压强下,从c 0︒加热到c 100︒,则气体的内能改变了 【 D 】(A )0.25J 103⨯ (B )J 105.03⨯ (C )J 100.13⨯ (D )J 1025.13⨯ 参考答案:T R i M E ∆⎪⎭⎫⎝⎛=∆2μ ()()J 1025.127337331.82323⨯=-⨯⨯=∆⎪⎭⎫ ⎝⎛=∆T R i M E μ7. 在容积为3210m -的容器中,装有质量g 100的气体,若气体分子的方均根速率为1200-⋅s m ,则气体的压强为 【B 】 (A )Pa 1067.05⨯ (B )Pa 1033.15⨯ (C )Pa 1066.25⨯ (D )Pa 1099.35⨯参考答案:μRTv 32=RT MpV μ= ()Pa 1033.131522⨯=⎪⎭⎫ ⎝⎛⨯=v V M p8. 如图1所示的两条()v ~v f 曲线分别表示氢气和氧气在同一温度下的麦克斯)(1s m -⋅v韦速率分布曲线。
第七章 气体动理论答案

一.选择题1、(基础训练1)[ C ]温度、压强相同的氦气和氧气,它们分子的平均动能ε和平均平动动能w 有如下关系:(A) ε和w 都相等. (B) ε相等,而w 不相等.(C) w 相等,而ε不相等. (D) ε和w 都不相等. 【解】:分子的平均动能kT i2=ε,与分子的自由度及理想气体的温度有关,由于氦气为单原子分子,自由度为3;氧气为双原子分子,其自由度为5,所以温度、压强相同的氦气和氧气,它们分子的平均动能ε不相等;分子的平均平动动能kT w 23=,仅与温度有关,所以温度、压强相同的氦气和氧气,它们分子的平均平动动能w 相等。
2、(基础训练3)[ C ]三个容器A 、B 、C 中装有同种理想气体,其分子数密度n 相同,而方均根速率之比为()()()2/122/122/12::C B A v v v=1∶2∶4,则其压强之比A p ∶B p ∶C p 为:(A) 1∶2∶4. (B) 1∶4∶8. (C) 1∶4∶16. (D) 4∶2∶1. 【解】:气体分子的方均根速率:MRTv 32=,同种理想气体,摩尔质量相同,因方均根速率之比为1∶2∶4,则温度之比应为:1:4:16,又因为理想气体压强nkT p =,分子数密度n 相同,则其压强之比等于温度之比,即:1:4:16。
3、(基础训练8)[ C ]设某种气体的分子速率分布函数为f (v ),则速率分布在v 1~v 2区间内的分子的平均速率为 (A)⎰21d )(v v v v v f . (B) 21()d v v v vf v v ⎰.(C)⎰21d )(v v v v v f /⎰21d )(v v v v f . (D) ⎰21d )(v v v v v f /0()d f v v ∞⎰ .【解】:因为速率分布函数f (v )表示速率分布在v 附近单位速率间隔内的分子数占总分子数的百分率,所以⎰21d )(v v v v v f N 表示速率分布在v1~v2区间内的分子的速率总和,而21()d v v Nf v v ⎰表示速率分布在v 1~v 2区间内的分子数总和,因此⎰21d )(v v v v v f /⎰21d )(v v v v f 表示速率分布在v 1~v 2区间内的分子的平均速率。
大学物理答案第七章

(3)若沿过程曲线从a到c状态,内能改变为
应用热力学第一定律,系统所作的功为
7-3 2mol的氮气从标准状态加热到373 K,如果加热时(1)体积不变;(2)压强不变,问在这两种情况下气体吸热分别是多少?哪个过程吸热较多?为什么?
分析根据热力学第一定律,系统从外界吸收的热量,一部分用于增加系统的内能,另一部分用于对外作功.理想气体的内能是温度的单值函数,在常温和常压下氮气可视为理想气体,无论经过什么样的准静态过程从标准状态加热到373 K,其内能的变化都相同.在等体过程中气体对外不作功,系统从外界吸收的热量,全部用于系统的内能的增加,而在等压过程中,除增加内能外,还要用于系统对外作功,因此吸热量要多些.
分析气体动理论的能量公式表明,气体的温度是气体分子平均平动动能的量度,而且定义了方均根速率 .只要温度不变,无论经历什么样的过程,方均根速率都不变.本题中,可以通过等温过程中系统所作的功的表达式确定该过程中系统的温度.
解等温过程中系统所作的功为
7-92 m3的气体等温地膨胀,压强从 变到 ,求完成的功.
第七章热力学基础
7-1 假设火箭中的气体为单原子理想气体,温度为2000 K,当气体离开喷口时,温度为1000 K,(1)设气体原子质量为4个原子质量单位,求气体分子原来的方均根速率 .已知一个原子质量单位=1.6605×10-27kg;(2)假设气体离开喷口时的流速(即分子定向运动速度)大小相等,均沿同一方向,求这速度的大小,已知气体总的能量不变.
p
p22
p0等温线
1
p1
OV2V1V
图7-12
分析对于双原子理想气体,热容比 .不论经历什么过程,只要初终态气体的温度相同,就可以应用理想气体状态方程,建立类似于等温过程中初态和终态压强和体积之间的关系.
第七章气体动理论7 –4 能量均分定律理想气体内能一自由度
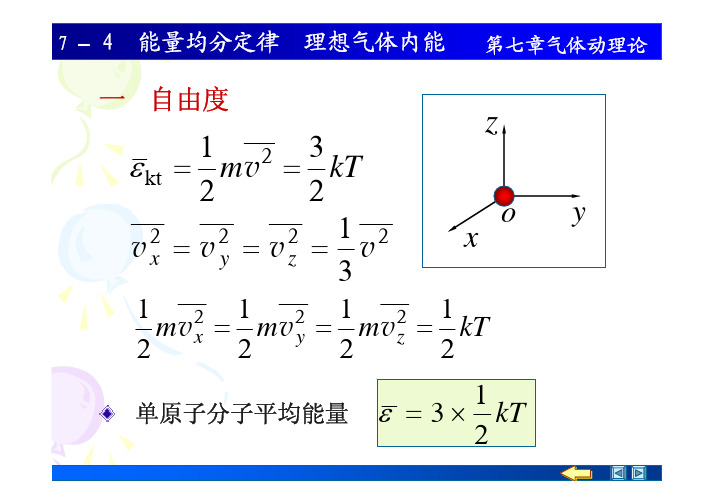
7 – 4能量均分定律 理想气体内能第七章气体动理论一 自由度1 2 3 ε kt = m v = kT 2 2 1 2 2 2 2 vx = v y = vz = v 3zoxy1 2 1 2 1 2 1 m v x = m v y = m v z = kT 2 2 2 21 单原子分子平均能量 ε = 3 × kT 27 – 4能量均分定律 理想气体内能 刚性双原子分子第七章气体动理论分子平均平动动能ε kt1 1 1 2 2 2 = m v Cx + m v Cy + m v Cz 2 2 2分子平均转动动能ε kr1 1 2 2 = Jω y + Jωz 2 27 – 4能量均分定律 理想气体内能 非刚性双原子分子第七章气体动理论分子平均能量ym2* Cε = ε kt + ε kr分子平均振动能量m1xz非刚性分子平均能量1 1 2 2 ε v = µ vCx + kx 2 2ε = ε kt + ε kr + ε v自由度 分子能量中独立的速度和坐标的二次 方项数目叫做分子能量自由度的数目, 简称自由 度,用符号 表示. i7 – 4能量均分定律 理想气体内能 自由度数目第七章气体动理论i=t+r+v平 动 转 动 振 动刚性分子能量自由度分子 自由度t 平动 r3 3 3转动 0 2 3i3 5 6总单原子分子 双原子分子 多原子分子7 – 4能量均分定律 理想气体内能第七章气体动理论二 能量均分定理(玻尔兹曼假设) 气体处于平衡态时,分子任何一个自由度的平均分定理 .1 kT ,这就是能量按自由度 均能量都相等,均为 2分子的平均能量i ε = kT 2三 理想气体的内能和摩尔热容 理想气体的内能 :分子动能和分子内原子间的 势能之和 . 1 mol 理想气体的内能i E = NAε = RT 27 – 4能量均分定律 理想气体内能第七章气体动理论m m i mol 理想气体的内能 E = RT M M 2理想气体内能变化 定体摩尔热容 定压摩尔热容 摩尔热容比m i dE = RdT M 2i CV ,m = R 2i+2 C p,m = R 2 Cp,m i + 2 = γ= CV ,m i。
气体动理论(附答案)

气体动理论一、填空题1.(本题3分)某气体在温度为T = 273 K时,压强为p=1.0×10-2atm,密度ρ = 1.24×10-2 kg/m3,则该气体分子的方均根速率为____________。
(1 atm = 1.013×105 Pa)答案:495m/s2.(本题5分)某容器内分子密度为1026m-3,每个分子的质量为3×10-27kg,设其中1/6分子数以速率v=200m/s垂直向容器的一壁运动,而其余5/6分子或者离开此壁、或者平行此壁方向运动,且分子与容器壁的碰撞为完全弹性的。
则(1)每个分子作用于器壁的冲量ΔP=_____________;(2)每秒碰在器壁单位面积上的分子数n0=___________;(3)作用在器壁上的压强p=_____________;答案:1.2×10-24kgm/s×1028m-2s-14×103Pa3.(本题4分)储有氢气的容器以某速度v作定向运动,假设该容器突然停止,气体的全部定向运动动能都变为气体分子热运动的动能,此时容器中气体的温度上升0.7K,则容器作定向运动的速度v=____________m/s,容器中气体分子的平均动能增加了_____________J。
(普适气体常量R=8.31J·mol-1·K-1,波尔兹曼常k=1.38×10-23J·K-1,氢气分子可视为刚性分子。
)答案::1212.4×10-234.(本题3分)体积和压强都相同的氦气和氢气(均视为刚性分子理想气体),在某一温度T下混合,所有氢分子所具有的热运动动能在系统总热运动动能中所占的百分比为________。
答案:62.5%5.(本题4分)根据能量按自由度均分原理,设气体分子为刚性分子,分子自由度为i,则当温度为T时,(1)一个分子的平均动能为_______。
《大学物理》气体动理论练习题及答案解析

《大学物理》气体动理论练习题及答案解析一、简答题1、你能够从理想气体物态方程出发 ,得出玻意耳定律、查理定律和盖吕萨克定律吗? 答: 方程RT Mm pV '=描述了理想气体在某状态下,p ,V ,T 三个参量所满足的关系式。
对给定量气体(Mm '不变),经历一个过程后,其初态和终态之间有222111T V p T V p =的关系。
当温度不变时,有2211V p V p =,这就是玻意耳定律;当体积不变时,有2211T p T p =,这就是查理定律;当压强不变时,有2211T V T V =,这就是盖吕萨克定律。
由上可知三个定律是理想气体在经历三种特定过程时所表现出来的具体形式。
换句话说,遵从玻意耳定律、查理定律和盖吕萨克定律的气体可作为理想气体。
2、为什么说温度具有统计意义? 讲一个分子具有多少温度,行吗?答:对处于平衡态的理想气体来说,温度是表征大量分子热运动激烈程度的宏观物理量,是对大量气体分子热运动状态的一种统计平均,这一点从公式kT v m 23212=中的2v 计算中就可以看出(∑∑=iii Nv N v22),可见T 本质上是一种统计量,故说温度具有统计意义,说一个分子的T 是毫无意义的。
3、解释下列分子运动论与热力学名词:(1) 状态参量;(2) 微观量;(3) 宏观量。
答:(1)状态参量:在一定的条件下,物质系统都处于一定的状态下,每个状态都需用一组物理量来表征,这些物理量称为状态参量。
(2)微观量:描述个别分子运动状态的物理量。
(3)宏观量:表示大量分子集体特征的物理量。
4、一定量的理想气体处于热动平衡状态时,此热力学系统的不随时间变化的三个宏观量和不随时间变化的微观量分别有哪些?建议:本题“不随时间变化的微观量分别有哪些”不知道通过该设问需要学生掌握什么东西。
其实从微观角度来讲,分子的任何量,如分子速度,动能,动量,严格说来甚至质量也是变化的。
可能会有人回答为平均速度、平均速率、平均自有程等,但那又是一种统计行为,该值对应着某些宏观量,这只能称为统计量,与微观量和宏观量相区别。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、选择题[ C ]1、(基础训练2)两瓶不同种类的理想气体,它们的温度和压强都相同,但体积不同,则单位体积内的气体分子数n ,单位体积内的气体分子的总平动动能(E K /V ),单位体积内气体的质量?的关系为:(A) n 不同,(E K /V )不同,??不同. (B) n 不同,(E K /V )不同,??相同. (C) n 相同,(E K /V )相同,??不同.(D) n 相同,(E K /V )相同,??相同. 【提示】① ∵nkT p =,由题意,T ,p 相同,∴n 相同;② ∵kT n V kTNV E k 2323==,而n ,T 均相同,∴V E k 相同;③ RT M M pV mol =→RTpM V Mmol ==ρ,T ,p 相同,而mol M 不同,∴ρ不同。
[ B ]2、(基础训练7)设图示的两条曲线分别表示在相同温度下氧气和氢气分子的速率分布曲线;令()2O p v 和()2H pv 分别表示氧气和氢气的最概然速率,则(A) 图中a 表示氧气分子的速率分布曲线;()2O p v /()2H p v = 4.(B) 图中a 表示氧气分子的速率分布曲线;()2O p v /()2H p v =1/4.(C) 图中b表示氧气分子的速率分布曲线;()2O p v /()2H p v =1/4.(D) 图中b表示氧气分子的速率分布曲线;()2O p v /()2H p v = 4.【提示】①最概然速率p v =p v 越小,故图中a 表示氧气分子的速率分布曲线;②23,3210(/)mol O M kg mol -=⨯, 23,210(/)mol H M kg mol -=⨯,得()()22Ov v p p H14=[ C ]3、(基础训练8)设某种气体的分子速率分布函数为f (v ),则速率分布在v 1~v 2区间内的分子的平均速率为 (A)⎰21d )(v v v v v f . (B) 21()d v v v vf v v ⎰.(C)⎰21d )(v v v v v f /⎰21d )(v v v v f . (D) ⎰21d )(v v v v v f /0()d f v v ∞⎰ .【提示】① f (v )d v ——表示速率分布在v 附近d v 区间内的分子数占总分子数的百分比;② ⎰21)(v v dv v Nf ——表示速率分布在v 1~v 2区间内的分子数总和;③21()v v vNf v dv ⎰表示速率分布在v 1~v 2区间内的分子的速率总和,因此速率分布在v 1~v 2区间内的分子的平均速率为22112211()()()()v v v v v v v v vNf v dv vf v dvNf v dvf v dv=⎰⎰⎰⎰[ B ]4、(基础训练9)一定量的理想气体,在温度不变的条件下,当体积增大时,分子的平均碰撞频率Z 和平均自由程λ的变化情况是:(A) Z 减小而λ不变. (B) Z 减小而λ增大. (C) Z 增大而λ减小. (D) Z 不变而λ增大.【提示】①2Z d n =,其中v =不变;Nn V =,当V 增大时,n 减小; ∴Z 减小。
②v Z λ==,可见,当n 减小时,λ增大。
[ B ]5、(自测提高3)若室内生起炉子后温度从15℃升高到27℃,而室内气压不变,则此时室内的分子数减少了(A)00. (B) 400. (C) 900. (D) 2100. 【提示】127315288T K =+=,227327300T K =+=;由状态方程1122pV N kT N kT ==,得 121211pV pVN N kT kT pV N kT --==212T T T -=124%300=[ C ](自测提高?7)一容器内盛有1 mol 氢气和1 mol 氦气,经混合后,温度为 127℃,该混合气体分子的平均速率为 (A) πR 10200. (B) πR10400.(C) )210πR . (D) +πR10(400)210πR. 【提示】已知273127400T K =+=,3, 2210(/)mol H M kg mol -=⨯,3, 410(/)mol H e M kg mol -=⨯,根据平均速率的定义,混合气体分子的平均速率为:v =1Nii vN==∑22211()()222H H H H H H AA A vv v v ee v v e N N N +=+=+∑∑∑∑,其中 ππRM RT v H l mo H 10400822,==, H e v ==, v ∴=)210πR二.填空题1、(基础训练?11) A 、B 、C 三个容器中皆装有理想气体,它们的分子数密度之比为n A ∶n B ∶n C =4∶2∶1,而分子的平均平动动能之比为A w ∶B w ∶C w =1∶2∶4,则它们的压强之比A p ∶B p ∶C p = 1:1:1 .【提示】压强公式:t w n p 32= → A p ∶B p ∶C p =n A A w ∶n B B w ∶n C C w =1∶1∶12、(基础训练?14)在平衡状态下,已知理想气体分子的麦克斯韦速率分布函数为f (v )、分子质量为m 、最概然速率为v p ,试说明下列各式的物理意义:(1)()d pf ∞⎰v v v 表示_速率分布在v p~∞区间内的分子数占总分子数的百分率;(2)()201v v d v 2m f ∞⎰ 表示 分子平动动能的平均值__.3、(基础训练?15)用总分子数N 、气体分子速率v 和速率分布函数f(v)表示下列各量:(1) 速率大于v 0的分子数= ⎰∞)(v dv v Nf ;(2) 速率大于v 0的那些分子的平均速率=⎰⎰∞∞0)()(v v dvv f dvv vf ;(3) 多次观察某一分子的速率,发现其速率大于v 0的概率=⎰∞)(v dv v f .【提示】(1)NdNdv v f =)(表示v~v+dv 区间内的分子数dN 占总分子数N 的百分比→速率大于v 0的分子数为: ⎰∞v dN =⎰∞0)(v dv v Nf(2)速率大于v 0的分子的平均速率:0000()()()()v v v v v v vdN vNf v dv vf v dvv dN Nf v dvf v dv∞∞∞∞∞∞===⎰⎰⎰⎰⎰⎰(3)某一分子的速率大于v 0的概率→分子速率处于0v ~∞区间的概率→0v ~∞区间的分子数占总分子数的百分数⎰∞)(v dv v f .4、(基础训练?17)一容器内储有某种气体,若已知气体的压强为 3×105Pa ,温度为27℃,密度为0.24 kg/m 3,则可确定此种气体是 氢 气;并可求出此气体分子热运动的最概然速率为 1578.92 m/s .【提示】① 3, 210/, mol mol M MRT RTpV RT M kg mol M V pp ρ-⎛⎫=∴===⨯ ⎪⎝⎭∴是氢气; ②1578.92/p v m s == 5、(自测提高12)储有氢气的容器以某速度v 作定向运动,假设该容器突然停止,气体的全部定向运动动能都变为气体分子热运动的动能,此时容器中气体的温度上升 K ,则容器作定向运动的速度v =_ 121 _m/s ,容器中气体分子的平均动能增加了232.410 -⨯J .【提示】(1)5i =,()215v 22mol M E R T νν=∆=∆ →v 121/m s ==; (2)52k kT ε=→ 2352.4102k k T J ε-∆=∆=⨯.6、(自测提高16)一容器内盛有密度为 ??的单原子理想气体,其压强为p ,此气体分;单位体积内气体的内能是32p .【提示】①RT M M pV mol =→ρpM pV M RT mol == →∴ρpM RT v mol 332==; ② 单原子分子3i =,故333222RT pV E p V V V ν===三.计算题1、(基础训练?21)水蒸气分解为同温度T 的氢气和氧气H 2O →H 2+21O 2时,1摩尔的水蒸气可分解成1摩尔氢气和21摩尔氧气.当不计振动自由度时,求此过程中内能的增量. 解:内能E 2i RT ν=,水蒸汽:i =6,ν=1,∴6132E RT RT =⨯⨯=水; 分解为氢气和氧气后,i =5,22O 11, 2H νν==,225511512224H O E E E RT RT RT∴=+=⨯⨯+⨯⨯=334RT 25%43RT E E E E E RT-∴-===水水水,,即内能增加了25%2、(基础训练?24)有N 个粒子,其速率分布函数为00()(0)()0()f v C v v f v v v =≤≤=>,,试求其速率分布函数中的常数C 和粒子的平均速率(均通过0v 表示) 解:由归一化条件00()01f v dv Cd d C υυυυυ∞∞=+==⎰⎰⎰, ∴01υ=Cυ= 0()f d υυυ∞⎰=0001d υυυυ⋅⎰=2120υυ⋅=20υ3、(自测提高?21)试由理想气体状态方程及压强公式,推导出气体温度与气体分子热运动的平均平动动能之间的关系式.解:理想气体状态方程 p nkT =,理想气体的压强公式:t n p ε32=, 比较(1),(2)两式得,气体分子的平均平动动能t ε与温度的关系为 kT t 23=ε4、(自测提高?22)许多星球的温度达到108K .在这温度下原子已经不存在了,而氢核(质子)是存在的.若把氢核视为理想气体,求:(1) 氢核的方均根速率是多少 (2) 氢核的平均平动动能是多少电子伏特解:(1) 氢核 M mol =1×10?3 kg ·mol ?1=61.5810(/)m s ==⨯ (2)23815433 1.381010 2.0710 1.291022t kT J eV ε--==⨯⨯⨯=⨯=⨯。
