_中国药典_成方制剂中药材及饮片基源问题
中药质量标准现状及其发展趋势

中药质量标准现状及其发展趋势中药包括中药材、饮片和中成药,是中医治疗疾病的物质基础。
中药的质量直接关系到临床疗效和用药安全性,因此,中药质量标准的建立以及其体系的构建是确保中药安全、有效的关键,也是中药现代化和国际化的关键问题之一。
中药质量标准现状:中药质量标准包括中药材、饮片质量标准和中成药质量标准。
目前中药材、饮片法包括《中国药典》及其补编、《部颁标准》进口药品分册、各省市自治区的药材标准。
中成药法定标准包括《中国药典》、《部颁标准》中药成方制剂(1-20册)、《国家药品标准》、《国家中成药标准汇编》等。
中药材、饮片质量标准包括:名称、来源、形状、鉴别、检查、浸出物、含量测定、炮制、性味与归经、功能与主治、用法与用量、注意、贮藏等。
中成药质量标准内容包括:名称、处方、制法、形性状、鉴别、检查、浸出物、指纹图谱、含量测定、功能与主治、用法与用量、规格、注意、贮藏等。
当前中药质量标准存在的主要问题:1.中药有效成分研究滞后,影响了质量标准的建立2.缺少专属性强的鉴别方法,难以有效地控制中药材品种混乱和中成药的投料问题。
3.对重金属、农药残留量等的研究很少,影响中药材和中成药的出口。
4.中药化学对照品严重缺乏,制约了中药材质量标准的建立。
5.单一指标成分或少数指标成分含量测定不能有效控制中药的质量。
6.中药指纹图谱整体成分控制未能良好的在中药质量标准得到推广应用。
7.中药质量评价系级不完整,影响了中药质量标准的实施,特别是中药材、饮片质量标准如同虚设。
中药质量标准发展趋势:1.加强中药化学成分特别是有效成分研究,为质量标准的建立奠定物质基础。
2.加强重金属、农药残留及内源性有害物质的研究,建立相应是残留物控制标准,确保中药的安全性。
3.加强中药化学对照品的研究和市场化,同时研究推广“一标多测”、“对照提取物”对照等多成分含量方法,多途径解决化学对照品缺乏的问题。
4.研究并建立多成分含量测定方法,提高中药的品质。
《中国药典》成方制剂中药材及饮片基源问题

《中国药典》成方制剂中药材及饮片基源问题
孙宝惠;牛小莲;段吉平;田清存
【期刊名称】《中国药品标准》
【年(卷),期】2006(7)3
【摘要】药材基源准确是确保药品质量的首要条件,为此,《中国药典》2005年版一部(以下简称《药典》)在附录Ⅲ中对成方制剂中本版《药典》未收载的药材及饮片进行了补充说明,这是完全必要的,但这一补充还不够完善,遗漏品种较多;有的药材名称与《药典》正文【处方】中使用的不一致;有些品种并未在制剂【处方】项出现,应予增补、修订或删除。
【总页数】3页(P8-10)
【作者】孙宝惠;牛小莲;段吉平;田清存
【作者单位】河北省药品检验所,石家庄,050011;河北省药品检验所,石家
庄,050011;河北省药品检验所,石家庄,050011;河北以岭医药研究院,石家
庄,050091
【正文语种】中文
【中图分类】F4
【相关文献】
1.《中国药典》2010年版成方制剂处方饮片名称规范的商榷 [J], 张丽丽;孙宝惠;
秦陇;马静;刘丹
2.《中国药典》成方制剂中药材及饮片基源问题讨论 [J], 张丽丽;孙宝惠;马静;秦
陇;刘丹
3.2015年版《中国药典》(一部)中含毒性饮片成方制剂的归纳与分析 [J], 李春晓;王盼盼;李学林;张辉;唐进法
4.《中国药典》成方制剂处方中饮片名称亟待规范 [J], 孙宝惠;段吉平;牛小莲;王璐
5.《中国药典》2005年版部分中药成方制剂含量测定限量高于相应中药材问题的探讨 [J], 刘德军
因版权原因,仅展示原文概要,查看原文内容请购买。
2020年版药典中药材、中药饮片都有哪些新变化

2020年版药典中药材、中药饮片都有哪些新变化{{中国药典}}2020年版收载品种总数计划达到6400个左右,其中:中药增加品种约220个,化学药增加品种约420个,生物制品增加品种收载30个,药用辅料增加品种约100个,药包材品种收载30个,共约800个。
药典已收载品种计划修订1400个,其中:中药500个,化药600个,生物制品150个。
中药材标准的增修订中药材是中医临床和中药产业的根本,是基础中的基础,必须建立严格、科学的标准。
(一)品种的增加与退出(1)增加收载有临床用药需求、基础研究扎实、资源(野生和栽培)丰富的品种。
(2)增加收载现版药典收载或拟收载中成药处方药味中未收入药典的中药材标准。
(3)对于野生资源枯竭、商品匮乏、存在明显安全性、伦理等问题(如化石类、人类胎盘类、动物粪便类等),以及基础研究薄弱的品种从药典中退出或不再增加收入本版药典。
(4)已有中药材品种新增基原,原则上按照“新发现中药材”进行申报注册,获得批准后,可考虑作为新的基原收入药典,但经本草考证证明属于历史误用需要正本清源的品种不在此列。
(二)中药材名称、来源和药用部位的修订与规范根据本草考证,结合中药材生产实际,对部分中药材名称、来源和药用部位进行修订;对原植、动物的科、属、种和拉丁学名、原矿物的类、族和矿石进行进一步的考证,进一步修订和规范中药材的来源。
(三)中药材采收和加工方法及药材性状的修订当前,随着中药农业的快速发展,许多常用中药材已不再依赖野生资源,实现了大规模种植养殖,且采收和加工已相对集中,并逐步实现机械化。
中国药典要顺应中药产业的变革和进步,把好质量关,本版药典须对中药材采收和加工方法及药材性状进行修订。
(1)制定中药材采收加工技术评价方法和指导原则,把中药材采收和产地加工纳入科学化、法制化轨道。
(2)收载和规范中药材趁鲜切片直接干燥的产地加工方式。
其收载品种必须符合上述指导原则的要求,仅限于部分传统采收加工方法落后,药材难以干燥且长时间干燥过程中易霉变或导致成分明显下降的中药材以及对传统采用硫磺熏蒸改用产地无硫加工方法的中药材。
浅论2010年版《中国药典》药材及饮片之变化

完 善安 全性检 查项 目:进 一步 提高对 药材 及饮 片 的
标 准要求 : 进一 步加 强对 重金属 或有 害元素 、 药残 农 留量 、 杂质 、 留溶剂 等 的控 制 ; 中药正 文 标准 中 残 在 增加 或完善 安全 性检查 项 目, 如对 易霉 变 的陈皮 、 僵 蚕 、 大海 、 胖 桃仁 、 酸枣 仁等新 增黄 曲霉毒 素 检测 , 方 法 和限度 与 国际标准 一致 ; 正文 标准 中对 川乌 、 在 草 乌 、马钱 子 等 剧 毒 性 饮 片 ,采 用 高 效 液 相 色 谱 法 f L) HP C 等更先 进 、 精确 的方法 加 以限量 检查 ; 更 在重 金 属及 有害元 素控 制方 面 ,新 版药 典采用 电感 耦合
氧化硫 残 留量 测定 法 、黄 曲霉 毒素 测定 法等 1 . 4种 同时对 2 0 0 5年版 《 国药典》 中 中检测 项 目中的 4 7项 进 行 了修订 , 突破单 一成 分控 制药材 质量 的模 式 。 采 用 多 成分 或 特征 色 谱 峰群 综 合控 制质 量 的方法 : 保 留 了 20 0 0年 《 国药典 》 甘 草 和黄 芪 药材 中的有 中 对
中药 历史悠 久 、 品种繁 多 . 个药 品的来 源存 在 一 多 个科 、 多个 种 属 , 种情 况 给 中 医临床 应 用 、 这 中药 科研 、 实验数 据 的准确性 带来 了很 大难题 , 解决 这 为
一
问题 , 在 1 9 早 9 5年版 《 中国药典 》 以后就 已经开 始
着手解 决 。如漏 芦分化 为漏芦 ( 州漏芦 ) 祁 和禹州 漏
加 .初步 解决 了长期 困扰 中药饮 片产业 发展 缺少 国 家标 准 , 方炮制 规 范不统 一等 问题 , 对 于提 高 中 地 这 药饮 片质量 , 保证 中医临床用 药 的安全有 效 , 推动 中
《中国药典》中药质量标准复核技术要求

附件:《中国药典》中药质量标准复核技术要求国家药典委员会为编制好《中国药典》,保证增修订品种质量标准中检测方法的科学性、重现性和可行性,保证设定的方法与指标基本能控制药品质量,规范标准复核的试验工作,特制定本技术要求。
一、实验室条件的要求1、从事药品标准复核检验的药品检验所,应当按照《药品检验所实验管理规范》和国家计量认证的要求,通过同级技术监督部门的计量认证或国家实验室认可。
2、按国家药品监督管理局颁布的药品检验所基本仪器设备配置要求,具有完善的中药检验仪器设备和必要的设施,符合药品检验的质量保证体系和技术要求。
3、能确保实验消耗品的来源,如各类试剂、试药、对照物质、色谱柱等。
4、如果个别项目不具备复核条件,应向国家药典委员会提出,转交其他省级药检所复核,不得到起草单位或由起草单位提供条件进行复核。
二、标准复核人员要求1、承担标准复核的药检所应指定标准复核负责人专门负责复核工作,应对复核实验过程进行监督,及时处理和解决实验中出现的问题,并对实验结果进行审查和负责。
标准复核负责人应具有高级以上(包括高级)技术职称,具有较丰富的标准研究和起草经验,能指导标准复核承担人员进行实验复核。
2、标准复核承担人员应具有中级以上(包括中级)技术职称,具有一定的标准研究和起草经验。
三、复核的资料和样品要求1、实验复核负责人和承担人员应首先审阅起草单位提供的技术资料(请复核公文、质量标准草案、起草说明、复核用样品检验报告书、复核用样品、复核用对照物质、项目任务书等),确认上述资料完整并基本符合起草技术要求后,安排实验复核工作。
否则,应向起草单位提出补充资料或退回的要求。
2、复核用样品,中药材、中药饮片每个品种至少包括3个不同产地或3个不同饮片生产企业的样品,多来源品种应尽可能包含不同基源的药材;中成药、中药提取物应为正式生产的3个批号样品,多生产企业的品种,应包括至少3个企业的3个批号样品。
样品量应为一次检验用量的三倍,一般,普通药材每份不少于100g,贵重药材不少于15g。
探疏2020年版《中国药典》药材饮片及成方制剂项下影响质量的存疑之处

探疏2020年版《中国药典》药材饮片及成方制剂项下影响质
量的存疑之处
杜萍;卢金福;黄英姿;邵家德;陆兔林
【期刊名称】《中成药》
【年(卷),期】2022(44)10
【摘要】《中国药典》具有严肃性和权威性,但其中一些不足之处同样应值得重视,尤其是在版本更新数次的情况下依然出现者。
本研究对2020年版《中国药典》中鹿角霜、肿节风、葛根、黄柏等药材饮片及其成方制剂在功能主治、用法用量、指标成分、含量测定等项下影响质量的存疑之处进行探疏,以期为后续版本修订提供参考。
【总页数】3页(P3289-3291)
【作者】杜萍;卢金福;黄英姿;邵家德;陆兔林
【作者单位】南京中医药大学附属医院药学部;南京中医药大学;常熟市第二人民医院;南京中医药大学药学院中药炮制学教研室
【正文语种】中文
【中图分类】R921.2
【相关文献】
1.《中国药典》2010年版成方制剂处方饮片名称规范的商榷
2.2015年版《中国药典》(一部)中含毒性饮片成方制剂的归纳与分析
3.《中华人民共和国药典》(2020年版)中药材\r和中药饮片质量标准增修订工作思路
4.《中国药典》1995年
版成方制剂处方中饮片用名规范化的建议5.关于中药饮片质量和质量标准及《中国药典》2020年版饮片标准修订的思考与建议
因版权原因,仅展示原文概要,查看原文内容请购买。
药材及成方制剂显微鉴别法检验通则

目的建立药材及成方制剂显微鉴别法的检验通则,保证检验人员操作的规范化、标准化,确保公司的产品质量。
范围适用于药材及成方制剂显微鉴别的检验责任化验员、中心化验室主任内容1 执行标准:《中华人民共和国药典》2005版一部2 标准内容2.1 定义:显微鉴别系指用显微镜对药材(饮片)切片、粉末、解离组织或表面制片及含药材粉末的制剂中药材的组织、细胞或内含物等特征进行鉴别的一种方法。
2.2 鉴别时选择有代表性的供试品,根据各品种鉴别项的规定制片。
制剂根据不同剂型适当处理后制片。
2.3 药材显微制片2.3.1 横切片或纵切片制片2.3.1.1 仪器:生物显微镜(XSP-2CA型)2.3.1.2 器具:刀片、测量尺2.3.1.3 试药:甘油、醋酸、水合氯醛2.3.1.4 试液配制甘油醋酸试液:见“常用试液配制标准操作规程”水合氯醛试液:见“常用试液配制标准操作规程”2.3.1.5 操作法选取药材适当部位,软化后用徒手或滑走切片法,切成10—20um的薄片,必要时可包埋后切片。
选取平整的薄片置载玻片上,根据观察对象不同,滴加甘油醋酸试液、水合氯醛试液或其他试液1-2滴,盖上盖玻片。
必要时滴加水合氯醛试液后,在酒精灯上加热透化,并滴加甘油乙醇试液或稀甘油,盖上盖玻片。
2.3.2 粉末制片2.3.2.1 仪器:生物显微镜(XSP-2CA型)2.3.2.2 试药:甘油、醋酸、水合氯醛2.3.2.3 试液配制甘油醋酸试液:见“常用试液配制标准操作规程”水合氯醛试液:见“常用试液配制标准操作规程”2.3.2.4 操作法供试品粉末过4号筛,挑取少量置载玻片上,滴加甘油醋酸试液、水合氯醛试液或其他适宜的试液,盖上盖玻片。
必要时,按上法透化。
2.3.3 表面制片2.3.3.1 仪器:生物显微镜(奥林巴斯CHK型)、百分之一天平(DT2200A/0.01g)2.3.3.2 器具:剪刀2.3.3.3 试药:水合氯醛2.3.3.4 试液配制水合氯醛试液:见“常用试液配制标准操作规程”2.3.3.5 操作法将供试品湿润软化后,剪取欲观察部位约4mm2,一正一反置载玻片上,或撕取表皮,加适宜的试液或加热透化后,盖上盖玻片,一部分或撕取其表皮,加水合氯醛试液观察。
中药饮片基源意思

中药饮片基源意思【实用版】目录1.中药饮片的定义和分类2.中药饮片的基源意义3.中药饮片基源的现代研究4.中药饮片基源对中药疗效的影响5.结论正文一、中药饮片的定义和分类中药饮片是指经过加工炮制后的中药材,它是中医临床用药的主要形式。
根据加工方法的不同,中药饮片可分为普通饮片、精致饮片和散剂等。
普通饮片是指经过简单的切制、干燥等工艺制成的,如甘草片、桂枝片等;精致饮片则是在普通饮片的基础上,经过炒制、炙制、煅制等复杂工艺制成的,如六味地黄丸、附子理中丸等;散剂则是指将中药材研磨成粉末,方便患者冲服或调制成丸剂等。
二、中药饮片的基源意义中药饮片的基源意义主要体现在两个方面:一是中药材的来源和品种,二是中药饮片加工炮制的方法。
中药材的来源和品种直接关系到中药饮片的疗效,我国地域辽阔,药材资源丰富,不同产地的中药材品质差异很大,因此,正确选择中药材的品种和来源至关重要。
中药饮片加工炮制的方法则是决定中药饮片药效的关键,不同的加工方法可以使中药材的药效得到不同程度的发挥,甚至可以改变药物的性质和功能。
三、中药饮片基源的现代研究随着科学技术的发展,对中药饮片基源的现代研究也在不断深入。
现代研究已经证实,中药饮片的加工炮制过程可以改变药材的化学成分和药理活性,从而影响药物的疗效和安全性。
例如,甘草经过炙制后,其甘草酸含量增加,抗炎、抗肿瘤作用增强;附子经过炮制后,其乌头碱含量降低,毒性降低,但温经散寒作用增强。
四、中药饮片基源对中药疗效的影响中药饮片基源对中药疗效的影响主要体现在两个方面:一是中药材的品质,二是中药饮片的加工炮制。
高品质的中药材可以保证中药饮片的疗效,而正确的加工炮制方法可以使中药材的药效得到最大限度的发挥。
因此,对中药饮片基源的研究,不仅可以提高中药饮片的疗效,还可以保证中药饮片的安全性。
五、结论中药饮片基源是中药饮片疗效的关键,对中药饮片基源的研究,不仅可以提高中药饮片的疗效,还可以保证中药饮片的安全性。
中华人民共和国药典临床用药须知全三部

《中华人民共和国药典临床用药须知全三部》
作者:国家药典委员会编
出版社:中国医药科技出版社出版时间:2011-7-1
版次:1印刷时间:2011-7-1纸张:胶版纸
I S B N:9787506748643包装:精装
总定价:1980元优惠价:1280元
一:2010版中华人民共和国药典临床用药须知-化学药和生物制品卷I S B N:9787506749060定价:798
二:2010中华人民共和国药典临床用药须知-中药饮片卷
I S B N:9787506748643定价:592元
三:2010中华人民共和国药典临床用药须知-中药成方制剂卷I S B N:9787506748629定价:590元
用“相互参阅”的原则,便于临床医师准确、全面地了解药物的治疗效果。
《临床用药须知》是《中国药典》的重要配套用书,对临床用药和编写药品说明书具有权威指导意义。
本版《临床用药须知》的编撰是由第九届国家药典委员会医学专业委员会、中医专业委员会组织全国200多名医药学权威专家,根据临床用药经验并结合国内外公认的相关资料编写而成。
本版在前几版基础上做了大胆的探索和创新,做到覆盖《国家基本药物目录》、《医保目录》及临床常用药品,达到信息广博、内容丰富、与时俱进、科学合理、经典实用、准确权威的总目标,具有较高的实用性和权威性。
《中国药典》2010年版英文版和《临床用药须知》2010年版的出版发行,必将丰富我国医药知识宝库,有力促进医药卫生事业的健康发展,在深化医药卫生体制改革中将起到重要的作用。
药物分析名词解释及简答题

简答题:1.我国现行药典为2010年出版,其结构分为几部,各部内容分别是什么?答:1)分为一部,二部,三部.2)药典一部:收载(中药材及饮片),(植物油脂和提取物),(成方制剂和单味制剂)等.药典二部:收载(化学药品,抗生素,生化药品,放射性药品)以及(药用辅料).药典三部:收载生物制品。
2.列出我国已颁布实施的药品质量管理规范。
答:1)《药品非临床研究质量管理规范》GLP2) 《药品生产质量管理规范》GMP3)《药品经营质量管理规范》GSP4)《药品临床实验质量管理规范》GCP5)GAP试行3.《中国药典》对铁盐检查的原理是什么?试述在铁盐检查过程中加入盐酸的目的。
答:原理:铁盐在盐酸酸性溶液中与硫氰酸盐作用生成红色可溶性的硫氰酸铁配离子。
与一定量标准铁溶液用同法处理后进行比色。
目的:在盐酸酸性条件下反应,可防止Fe3+的水解。
经实验,以50ml溶液中含稀盐酸4ml为宜。
4.重金属检查方法哪些?各适用什么药物中的重金属检查?答:1)硫代乙酰胺法:适用于溶于水,稀酸和乙醇的药物。
2)炽灼后的硫代乙酰胺法:适用于含芳环杂环及难溶于水,稀酸和乙醇的有机药物。
3)硫代钠法:适用于溶于碱性水溶液而难溶于稀酸或在稀酸中即生成沉淀的药物。
4)微孔膜法:适用于重金属限量低(含重金属杂质2-5ug)的药物。
5.中国药典收载的古蔡氏检查砷盐法的原理是什么?操作中加入碘化钾和酸性氯化亚锡的作用各是什么?答:1)原理:金属锌与酸作用产生新生态的氢与药物中微量的砷盐反应生成具挥发性的砷化氢,遇溴化汞试纸,产生黄色至棕色的砷斑,与一定量标准溶液所生成的砷斑比较,判断供试品中重金属是否符合限量规定。
2)①五价砷在酸性溶液中也能被金属锌还原为砷化氢,但生成的砷化氢的速度较三价砷慢,故反应中加入碘化钾及氯化亚锡将五价砷还原为三价砷,②碘化钾被氢化生成的碘又可被氯化亚锡还原为碘离子,后者与反应中产生的锌离子能形成稳定的配位离子,有利于生成砷化氢的反应进行。
中药药剂学考试试题及答案

中药药剂学考试试题及答案1. 1、根据药物的性质、用药的目的和给药途径,将原料药加工制成适合于医疗或预防医疗应用的形式,称为 [单选题]A、处方药B、非处方药C、剂型(正确答案)D、药剂E、制剂答案解析:【答案解析】2. 2、《中华人民共和国药典》最早的版本是 [单选题]A、1949年B、1960年C、1957年D、1953年(正确答案)E、1955年答案解析:【答案解析】【考点】中国药典的版次★★★★★【解析】新中国成立以来,我国最早颁布的药典是1953年的《中华人民共和国药典》。
3. 3、对药典的论述错误的是 [单选题]A、反映了国家药物生产、医疗和科技的水平B、药典颁布的内容,一般每隔几年修订C、具有法律的约束力D、一般收载疗效确切、不良反应少、质量稳定的药物E、中华人民共和国药典现已有8个版本(正确答案)答案解析:【答案解析】【考点】中国药典的版次★★★★★【解析】①药典由国家组织药典委员会编纂,并由政府颁布施行,具有法律约束力。
⑦药典中收载疗效确切、毒副作用小、质量稳定的常用药物及其制剂,规定其质量标准、制备要求、检验方法等,作为药物生产、检验、供应与使用的依据。
③药典在一定程度上反映了该国家药物生产、医疗和科技的水平,也体现出医药卫生工作的特点和服务方向。
根据我国药典颁布的时间可知,药典颁布的内容,一般每隔几年修订。
其中,1953年的药典为一部,1963年至2000年版的均分为一二两部。
2005年的药典分为三部。
2010年药典分三部。
4. 4、下列说法错误的是 [单选题]A、将原料药加工制成适合于医疗或预防应用的形式,称为制剂(正确答案)B、凡用于治疗、预防及诊断疾病的物质总称为药物C、药物包括原料药和药品D、玉屏风散属于一种制剂E、无需医生处方,消费者可自行判断、购买和使用的药品称为非处方药答案解析:【答案解析】将原料药加工制成适合于医疗或预防应用的形式,称为剂型。
根据药典、部颁标准或其他规定的处方,将原料药物加工制成具有一定规格,可直接用于临床的药品,称为制剂,如玉屏风散、双黄连粉针等。
关于提高中药材、中药饮片及其制剂质量标准的意见

中国医药指南2008年9月第6蓉第17期G u i de of C h i na M edi ci ne,Sept em ber2008,V06,N o.17关于提高中药材、中药饮片及其制剂质量标准的意见黄灿华曾卫阳【摘要】根据多年药品监首检验工作经验,对中药材、中药饮片及其制荆质量标准的提高提出参考意见.【关键词】质量标准;提高中图分类号:R282文献标识码:A文章编号:1671-8194(2008)17-0129-02作为一名从事药品监督检验工作多年的工作人员,有感于不完善的现行药品质量标准给工作带来的诸多不便和不利,根据工作中所遇见的具体问题,通过总结分析,对现行中药材、中药饮片及其制剂质量标准的提高提出一些粗浅的意见和看法,以供商榷.1亟待整理.提高的药品标准亟待整理、提高的药品标准有《卫生部药品标准》(含中药成方制剂标准、藏药标准、蒙药标准、维药标准、中药材标准)、Ⅸ中国药典》中药饮片部分,《国家药品标准地方标准上升国家标准》、《【中药材炮制规范》及地方中药材质量标准等.2急需解决的问题及解决的方法现行中药材、中药饮片及其制剂的部分质量标准存在质量可控性差、重现性差、可操作性差及行文欠科学严谨等弊病,严重制约了中医中药及其监管工作的发展。
2.1《卫生部药品标准》(含中药成方制剂标准、藏药标准、蒙药标准、维药标准和卫生部中药材标准)内容简单粗糙.其质量标准多数没有制定专属性强的定性指标和控制主要成分或活性成分的定量指标,亟需整理提高.如收载于《卫生部药品标准》中药成方制剂第十八册的。
刺五加注射液。
质量标准.其【含量测定l项以芦丁为对照品采用紫外分光光度法、在510d:2nm波长处测定刺五加注射液中总黄酮的含量。
而资料l J显示.刺五加及其制剂中有效成分为紫丁香苷(刺五加苷B),紫丁香树脂酚(刺五加D)异秦皮素及总黄酮等,并不含芦丁。
实验证明,刺五加注射液在510+2r i m波长处并无最大吸收。
中药材、中药饮片鉴定教材

中药材、中药饮片的鉴定中药鉴定的依据和取样中药鉴定工作的进行,主要依据药典和国家颁布的有关药品标准。
《中华人民共和国药典》,简称《中国药典》,是国家药品的法典。
它规定了药品的来源、质量要求和检验方法。
全国的药品生产、供应、使用和检验等单位都必须遵照执行。
各省颁发的中药饮片炮制规范是地方标准,其所载品种和内容上若与国家药典标准有矛盾时,应按国家药典执行,药典没有规定的按省炮制规范执行。
解放以来,国家先后出版了《中国药典》1953年版、1963年版、1977年版和1985年版,1990年版、2000年版七版药典,其中63年版、77年版及85年版90年版、95年版、2000年版药典均分一、二部出版,在一部中收载中药材及中药成方制剂等。
2000年版药典一部共收载992种药品,每个药材品种项下,按顺序一般分别列有中文名称、汉语拼音名与拉丁名、来源、性状、鉴别、检查、含量测定、炮制、性味与归经、功能与主治、用法与用量、注意、贮藏等内容。
其中鉴别项下一般列有显微鉴定和理化鉴定的内容。
在检验方法上除层析法、紫外分光光度法、红外分光光度法、还应用气相色谱法、高效液相色谱法等先进检验技术。
值得指出的,由于我国的中药资源极其丰富,品种繁多,有许多品种在国家药典和药品标准上没有收载,因此在鉴定中药时还可根据有关的参考书籍和资料,进行分析、鉴定。
供鉴定用的药材,在取样前一般应先注意品名、产地、批号、规格、等级及包件式样是否相符,检查包装的完整性、清洁程度以及有无水迹、霉变或其他物质污染等异常情况,详细记录。
如有个别包件严重变质不能供药用的,应另行处理,不作取样范围。
药材的取样,按药材取样法进行操作。
药材取样法是指选取供检定用药材供试品的方法。
取样的代表性直接影响到检定结果的正确性。
因此,必须重视取样的各个环节。
一、取样前,应注意品名、产地、规格等级及包件式样是否一致,检查包装的完整性、清洁程度以及有无水迹、霉变或其他物质污染等情况,详细记录。
生药学各章详细习题并答案剖析

绪论一、名词解释:1.“生药”2.“中药”3.“草药”4.“道地药材”二、单项选择题:1.我国十六世纪以前对药学贡献最大的著作( )A.《本草图经》B.《本草纲目拾遗》C.《本草纲目》D.《证类本草》2.《本草纲目》是明代李时珍所著,其中收载药物( )A.730种B.1082种C.1892种D.12092种答案:一、名词解释:1.“生药”:来源于天然的、未经加工或只经简单加工的植物类、动物类和矿物类药材。
2.“中药”:中医用以治病的药物,是根据中医学的理论和临床经验用于医疗保健的药物。
3.“草药”:局部地区民间草医用以治病或地区性口碑相传的民间药。
4.“道地药材”:来源于特定产区的货真质优的生药。
二、单项选择题:1.C2.C第一章生药的分类与记载第一节生药的分类简答题:生药学多采用按天然属性及药用部分的分类方法进行分类,其优点为何?答案:答:按天然属性及要用部分的分类方法进行分类,便于学习和研究生药的外形和内部构造,掌握各类生药的外形和显微特征及其鉴定方法。
第二节生药的记载填空题:1.基源项包括、、和。
2.生药的拉丁名通常由和两部分组成。
答案:填空题:1.原植(动)物的科名植(动)物名称学名药用部分2.动植物学名药用部分第二章生药的化学成分及其生物合成第一节生物的出生代谢产物与次生代谢产物一、名词解释:1.初生代谢2.次生代谢二、填空题:1.初生代谢产物包括、、、、、。
2.次生代谢产物包括、、、、、、。
答案:一、名词解释:1.初生代谢:合成必需的生命物质的代谢过程。
2.次生代谢:利用初生代谢产物又产生对生物体本身常常无明显作用的化合物的过程。
二、填空题:1.糖类氨基酸蛋白质脂肪酸酯类核酸2.生物碱萜类挥发油酚类醌类内酯类苷类第二节生药的化学成分单项选择题:1.挥发油常用的显色试剂是( )A.醋酐浓硫酸B.α-萘酚浓硫酸C.香草醛浓硫酸D.异羟肟酸铁2.用水合氯醛试液透化装片后,可观察( )A.淀粉粒B.糊粉粒C.脂肪油D.草酸钙结晶答案:单项选择题:1.C2.D第三章生药的鉴定第一节生药鉴定的意义简答题:1.何为生药的鉴定?2.开展生药鉴定的中药意义主要体现在哪些方面?答案:1.答:生药的鉴定是综合利用传统的和现代的检测手段,依据国家药典、有关政策法规及有关专著、资料等对生药进行真实性、纯度及品质优良度的评价,最终达到确保生药的真实性、安全性和有效性。
中药分析我国药典解读

苯
甲苯
中药分析我国药典解读
25/51
二、深入加强有效性质量控制
重视质量控制指标专属性、有效性; 重视中药质量控制整体性和可控性。
增加了符合中药特点专属性判别和含量 测定项,采取指纹图谱和特征图谱技术等,保 证了质量标准有效性和可控性,为更为有效 地控制药品质量提供了技术保障。
中药分析我国药典解读
26/51
中药分析我国药典解读
16/51
一、安全性控制项目大幅提升
(一)二氧化硫残留检测和程度要求 中药材重复熏蒸很轻易造成二氧化硫超标,
而且在性状和颜色会发生显著改变,不符合 中药标准要求。
新版药典锐意加强科学监管,预防中药材 加工过程中滥用或过分使用硫磺熏蒸,从而提 升及发展绿色中药材。
中药分析我国药典解读
(五)药用辅料品种收载数量显著增加,标准水平 显著提升
年版《中国药典》四部新增药用辅料品种139个, 修订95个,收载总数达270个。
注射剂使用辅料:版 2
版 23
极大提升了药用辅料质量水平,填补了当前我国药用 辅料标准短缺问题,保障药用辅料关联审批制度顺 利执行,推进我国药用辅料行业快速健康发展。
中药分析我国药典解读
8/51
版《中国药典》主要改变
(二)药典标准愈加系统化、规范化 经过药典凡例、通则、总论全方面增修订,从整
体上提升了对药品质量控制要求,完善了标准 技术要求,使药典标准愈加系统化、规范化。 (三)健全了药品标准体系
药用辅料品种增加至270个,新增相关指导标准; 标准物质新增相关通则和指导标准;药包材新增相 关指导标准;在归纳、验证和规范基础上实现了《中 国药典》各部共性检测方法协调统一。
中药分析我国药典解读
中药饮片基源意思

中药饮片基源意思
【最新版】
目录
1.中药饮片的概念
2.中药饮片的基源
3.中药饮片的制作过程
4.中药饮片的分类
5.中药饮片的应用
正文
【中药饮片】中药饮片是一种经过特殊加工的中药材,其目的是为了更好地发挥药效。
中药饮片是将中药材经过洗净、干燥、切片、炮制等一系列工艺处理后制成的。
它们可以根据需要进行配伍,制成中药处方,用于治疗疾病。
【基源】中药饮片的基源是中药材。
中药材是指从植物、动物、矿物等天然物质中提取的具有药用活性的成分。
中药饮片的制作过程就是将这些中药材进行加工,使其药效得到提升,更易于人体吸收。
【制作过程】中药饮片的制作过程主要包括洗净、干燥、切片、炮制等步骤。
洗净是将药材中的杂质、污垢等清除干净;干燥是为了保证药材的质量和保存时间;切片是将干燥后的药材切成薄片,以便于后续的炮制;炮制则是为了增强药效或者改变药性,这是一个相当复杂的过程,包括炒、炖、煮、蒸、炙等多种方式。
【分类】中药饮片可以根据其制作工艺、药效、药用部位等进行分类。
根据制作工艺,中药饮片可以分为生片、熟片、炭片等;根据药效,可以分为温性、寒性、平性等;根据药用部位,可以分为根片、叶片、花片等。
【应用】中药饮片是中医药的重要组成部分,被广泛应用于中医临床。
它们可以根据病情需要进行配伍,制成中药处方,用于治疗各种疾病。
同时,中药饮片也被用于制作中成药、保健品等。
_中国药典_成方制剂中药材及饮片基源问题
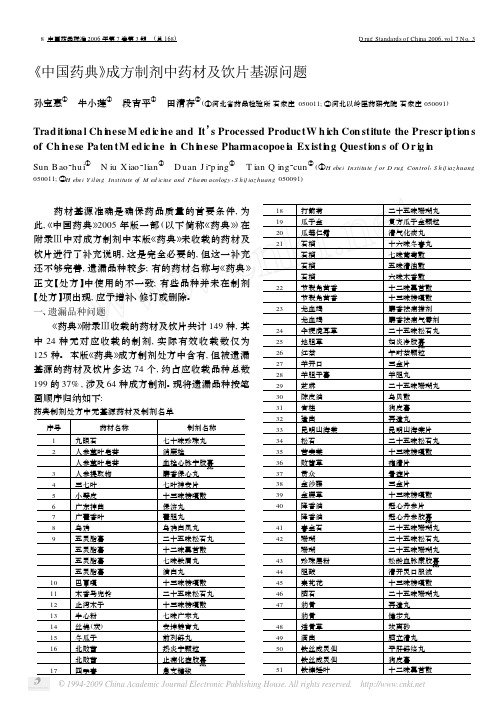
叶、槐枝、鼠妇虫、蔓荆子根 24 种药材在《药典》成方 制剂正文【处方】中均未出现。
二、名称问题
四、讨论
11 中药制剂处方中被遗漏的药材及饮片存在严
11《药典》收载的成方制剂处方中除本版《药典》
重的同名异物问题。例如暑症片中的贯众, 在湖南、四 已收载的药材及饮片外, 未收载品种应在附录 中明
川、贵州等 10 省市中药材标准中均有收载, 其基源分 确规定其来源及炮制方法。例如十五味沉香丸中的紫
8 中国药品标准 2006 年第 7 卷第 3 期 (总 168)
D rug Standards of Ch ina 2006, vo l. 7 N o. 3
《中国药典》成方制剂中药材及饮片基源问题
孙宝惠① 牛小莲① 段吉平① 田清存② (①河北省药品检验所 石家庄 050011; ②河北以岭医药研究院 石家庄 050091)
Trad itiona l Ch inese M ed ic ine and It’s Processed ProductW h ich Con stitute the Prescr iption s of Ch inese Pa ten tM ed ic ine in Ch inese Pharmacopoe ia Ex isting Question s of O r ig in
属蕨类植物 5 科 11 种之多; 坎离砂中的透骨草, 在云 檀香、高山辣根菜、悬钩子茎、木藤蓼、野姜、石灰华;
南、上海、广西等 10 个省市中药材标准中均有收载, 正骨水中的豆豉姜、买麻藤、过江龙、香樟等药材基源
其基源分属 5 科 11 种植物[1]; 狗皮膏中的官桂广西、 都作了明确的规定。《药典》增补版时, 应对本版《药
药材基源准确是确保药品质量的首要条件, 为 此,《中国药典》2005 年版一部 (以下简称《药典》) 在 附录 中对成方制剂中本版《药典》未收载的药材及 饮片进行了补充说明, 这是完全必要的, 但这一补充 还不够完善, 遗漏品种较多; 有的药材名称与《药典》 正文【处方】中使用的不一致; 有些品种并未在制剂 【处方】项出现, 应予增补、修订或删除。 一、遗漏品种问题
常用中药材质量检验中存在的问题及对策分析

常用中药材质量检验中存在的问题及对策分析【摘要】目的研究常用中药材质量检验中存在的问题及对策分析。
方法选择我院2021年1月-2021年12月购进常用中药材的52份质量检验报告进行研究,对质量检验报告进行分析,寻找常见中药材质量检验工作中存在的问题。
结果52种中药材中出现10种(19.23%)检验结果不达标的情况,其中药物描述不准确占比最多7.69%,其次为检验标准不完善5.77%。
结论常用中药材质量检验期间主要是由于检验结果不达标,检验标准不完善、药物成分含量不准确等,因此临床工作仍需要不断完善药材质量检验工作,提升工作质量,保证用药安全。
【关键词】常用中药材;质量检验;问题;对策中医是我国的瑰宝,中药材是我国宝贵的自然资源,包括植物、动物等。
但随着近年来国家及药品监管部门进行各种检查以及工作结果中,中药材存在的问题较为严重[1]。
由于中药的质量会直接影响患者治疗效果以及生命安全,且多种因素均会影响中药材质量检验工作的质量[2]。
因此提高重要中药质量检验成为我国医疗机构重点研究对象,本文通过分析我院质量检验期间存在的问题,报道如下。
1资料与方法1.1一般资料将52份我院2021年1月-2021年12月购进常用中药材的52份质量检验报告作为研究对象。
52份报告中包括:黄芪、当归、茯苓等28种植物类药材,蝎子、地龙等12种动物类药材,石膏、珍珠等12种矿物类药材。
1.2方法对常用中药材送往相关质检单位进行检验,得出检验报告,并对所有检验报告结果实施分析。
1.3观察指标对所有药材进行检验,从质检报告结果中的是否符合国家标准、药品成分、质检环境等几个方面进行汇总分析。
1.4统计学处理本研究采用SPSS 18.0统计软件对本文数据进行分析,计量资料用±s表示,采用t检验,计数资料用百分比表示,采用χ2检验,P<0.05为差异有统计学意义。
2结果52种中药材中出现10种(19.23%)检验结果不达标的情况,其中药物描述不准确占比最多7.69%,其次为检验标准不完善5.77%,见表1。
中药药剂学知到章节答案智慧树2023年湖南中医药大学

中药药剂学知到章节测试答案智慧树2023年最新湖南中医药大学第一章测试1.药品生产、供应、检验和使用的主要依据是()参考答案:中国药典2.《中华人民共和国药典》最早于何年颁布()参考答案:1953年3.将原料药物加工制成具有一定规格的制品,称为( )参考答案:制剂4.中药药剂学研究的主要内容包括中药药剂的( )参考答案:临床应用;生产技术;制剂理论;质量控制5.下列属于药品的是( )参考答案:生脉散;丹参滴丸6.研制新药时,选择药物剂型必须考虑的因素有( )参考答案:药物的理化性质;制剂的生物利用度;制剂的稳定性及其质量控制;生产、服用、携带、运输、贮藏的方便性;诊断、预防和治疗的需要7.下列陈述,正确的有()参考答案:从事中药药剂工作必须遵从各种药品管理法规和规范;《中国药典》一部主要收载中药材和饮片、植物油脂和提取物、成方制剂和单味制剂;自2001年2月28日起我国取消了药品地方标准;《中国药典》二部主要收载化学药品、抗生素、生化药品等8.《唐本草》是我国第一部官方颁布的药典,《太平惠民和剂局方》是我国第一部官方颁布的制剂规范。
()参考答案:对9.药品可分为优质品、合格品和不合格品3个等级。
()参考答案:错10.现行GMP大致分为三种类型:国际组织的GMP、国家性的GMP和制剂行业的GMP。
()参考答案:对第二章测试1.以下中药处方调配程序,正确的是()参考答案:审查处方—计价—调配—复核—发药2.处方中如有乌头、半夏,调剂人员应()参考答案:与医生协商,医生重新签字后再调配3.以下处方调配的操作,错误的是( )参考答案:鲜药与群药同放,写明用法用量4.法定处方是指()参考答案:《局颁药品标准》处方;《中国药典》处方5.中药“斗谱”的编排原则有()参考答案:按处方需要排列;按药物性味功能排列;按入药部位排列;按方剂组成排列;按需特殊保管的药物特殊排列6.中药配方颗粒具有哪些优点()参考答案:与传统饮片具有相同的有效成份、性味归经、主治功效;复合铝箔包装,携带、保存方便;单位药物重量轻,体积小,储存和运输方便;不需要煎煮,临用时温开水配成冲剂;单位质量有效成份比传统饮片高若干倍7.调配处方的注意事项有哪些()参考答案:调配处方时,应精神集中,认真仔细;如有先煎、后下等需特殊处理的饮片,应单包并注明用法;用时需捣碎的饮片,应称取后置专用铜冲内捣碎;分剂量时应按“等量递减”、“逐剂复戥”的原则;体积泡松饮片应先称,以免覆盖他药8.发药时要做到二核对:核对病人姓名、取药凭证。
最新《中国药典》中药质量标准研究制定技术要求

附件:《中国药典》中药质量标准研究制定技术要求国家药典委员会为编制好《中国药典》等国家药品标准,体现中药质量标准的制定符合中药的特点,保证中药质量标准所设定的方法与指标基本能控制中药质量,规范标准起草工作,特制定本技术要求。
本技术要求由总则和各论二部分组成,各论又分为中药材及饮片、植物油脂和提取物、中药成方制剂三部分。
总则一、基本原则1、坚持提高药品质量、维护公众健康的原则药品标准应贯彻落实科学监管理念,支持国家药品监督管理发展的需要,保障药品质量与用药安全,维护人民健康,促进我国医药事业的健康发展。
2、坚持继承、发展、创新的原则坚持继承与发展相结合,鼓励自主创新,加大自主知识产权的标准研究力度,促进科学研究与标准化工作的有效结合,提高我国药品标准中自主创新技术含量,使我国医药领域的自主创新技术通过标准快速转化为生产力,提高我国药品的国际竞争力。
3、坚持科学、实用、规范的原则制定、修订药品标准时,应充分考虑来源、生产、流通及使用等各个环节影响药品质量的因素,设置科学的检测项目、建立可靠的检测方法、规定合理的判断标准;在确保能准确控制质量的前提下,应倡导简单实用;药品标准的体例格式、文字术语、计量单位、数字符号以及通用检测方法等应统一规范。
4、坚持质量可控性原则国家药品标准适用于对合法生产的药品质量进行控制。
所建立的检测方法应专属、准确、精密。
5、坚持标准先进性原则《中国药典》所载药品的质量标准,应充分反映现阶段国内外药品质量控制的先进水平,对于多企业生产的同一品种,其标准的制定应在科学合理的基础上坚持就高不就低的标准先进性原则。
6、坚持标准发展的国际化原则注重新技术和新方法的应用,积极采用国际药品标准的先进方法,加快与国际接轨的步伐。
促进我国药品标准特别是中药标准的国际化。
二、实验室条件及人员的要求承担《中国药典》等国家药品标准起草任务的单位应具有通过计量认证并能满足起草任务要求的实验室,具有相应技术人员,具备中药研究、检验常用仪器和设备,能确保实验用试剂、试药及对照物质符合规定。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
桂 C. m a irei levl[1], 在《卫生部药品标准》中药成方制 东神曲、藏木香膏、五灵脂膏、羊胆干膏等应规定其处
剂所附药典未收载的药材名称及来源中, 官桂来源在 方、工艺等, 以确保其质量。
第 四 册 中 为 樟 科 植 物 肉 桂 C innam om um m a irei
珊瑚丸中的禹粮土,《药典》中的药材及饮片部分收载 的法定名称为“禹余粮”。
31《卫生部药材标准》中药材第一册 (1992 年) 分 别以北寒水石和南寒水石两味药材收载。《药典》2005 年版将十一味能消丸、七味铁屑丸等 6 个制剂处方中 的寒水石明确为北寒水石或南寒水石, 但《药典》附录
中寒水石 (平制)、寒水石 (奶制) 名称却未修订。 41 六神曲作为制剂已收载于《卫生部药品标准》
Trad itiona l Ch inese M ed ic ine and It’s Processed ProductW h ich Con stitute the Prescr iption s of Ch inese Pa ten tM ed ic ine in Ch inese Pharmacopoe ia Ex isting Question s of O r ig in
我 院 在 使 用《药 典》收 载 品 种 乳 酸 钠 溶 液 (1) (030506 河南偃师乳酸有限公司) 配制制剂前, 依法 对 其 进 行 了 含 量 测 定, 结 果 分 别 为 47110%、 49149%、53197% , pH 610~ 7104 (同批不同瓶) ; 除 此以外其它各项指标均符合《药典》有关规定。 但配 制 040114 和 040528 两批乳酸钠林格注射液, 其成 品 中 乳 酸 钠 的 含 量 差 别 很 大, 分 别 为: 01294%、 01499% , 是标示量 0131% 的 94184% 和 160197%。 经查文献(2) , 并对乳酸钠溶液进行处理后, 乳酸钠含 量比较稳定也配制出了质量稳定的合格制剂。因此, 《药典》(1) (3) 收载的乳酸钠溶液的标准不够完善, 现 将其存在的问题及建议报告如下。 一、存在的问题
叶、槐枝、鼠妇虫、蔓荆子根 24 种药材在《药典》成方 制剂正文【处方】中均未出现。
二、名称问题
四、讨论
11 中药制剂处方中被遗漏的药材及饮片存在严
11《药典》收载的成方制剂处方中除本版《药典》
重的同名异物问题。例如暑症片中的贯众, 在湖南、四 已收载的药材及饮片外, 未收载品种应在附录 中明
川、贵州等 10 省市中药材标准中均有收载, 其基源分 确规定其来源及炮制方法。例如十五味沉香丸中的紫
8 中国药品标准 2006 年第 7 卷第 3 期 (总 168)
D rug Standards of Ch ina 2006, vo l. 7 N o. 3
《中国药典》成方制剂中药材及饮片基源问题
孙宝惠① 牛小莲① 段吉平① 田清存② (①河北省药品检验所 石家庄 050011; ②河北以岭医药研究院 石家庄 050091)
贵州、北京等省市中药材标准中, 来源于樟科 4 种植 物, 分别是肉桂 C innam om un ca ssia P resl、川桂 C. w ilson ii Gam b le、少花桂 C. p auciflo rum N ees 和银叶
典》遗漏的药材及饮片基源在附录 给予补充完善, 对不规范的药材名称予以纠正,《药典》【处方】中未出 现的药材, 例如三颗针皮、大麦、大皂角等应予删除。
Sun B ao 2hu i① N iu X iao 2lian① D uan J i2p ing① T ian Q ing2cun② ( ①H ebei Institu te f or D rug Con trol, S h ij iaz huang
050011; ②H ebei Y iling Institu te of M ed icine and P ha rm acology , S h ij iaz huang 050091)
法, 但未规定六神曲的药味组成、用量及加工方法, 给 实际操作带来不便, 市售六神曲多数加工不规范, 偷 工减料现象普遍存在, 故六神曲的质量无法保障。 制 剂中的酒曲、建曲、寒食曲、广东神曲、土木香膏等均 无处方、工艺及质量标准。 三、应予删除品种
68 罂粟壳浸膏
止咳宝片
《药典》附录 收载的三颗针皮、大麦、大皂角、山
《药典》附录 收载的药材及饮片共计 149 种, 其 中 24 种无对应收载的制剂, 实际有效收载数仅为 125 种。 本版《药典》成方制剂处方中含有, 但被遗漏 基源的药材及饮片多达 74 个, 约占应收载品种总数 199 的 37% , 涉及 64 种成方制剂。现将遗漏品种按笔 画顺序归纳如下:
属蕨类植物 5 科 11 种之多; 坎离砂中的透骨草, 在云 檀香、高山辣根菜、悬钩子茎、木藤蓼、野姜、石灰华;
南、上海、广西等 10 个省市中药材标准中均有收载, 正骨水中的豆豉姜、买麻藤、过江龙、香樟等药材基源
其基源分属 5 科 11 种植物[1]; 狗皮膏中的官桂广西、 都作了明确的规定。《药典》增补版时, 应对本版《药
10 中国药品标准 2006 年第 7 卷第 3 期 (总 170) 105
[ 2 ] 国家药品监督管理局. 药品标准. 新药转正标准. 第十六至二十六 册. 中药. 2002 652
[ 3 ] 国家药品监督管理局. 药品标准. 新药转正标准. 第十一册. 1997
D rug Standards of Ch ina 2006, vo l. 7 N o. 3 44
石榴 石榴 石榴 22 节裂角茴香 节裂角茴香 23 龙血竭 龙血竭 24 伞梗虎耳草 25 地胆草 26 红茶 27 羊开口 28 羊胆干膏 29 芝麻 30 陈皮油 31 官桂 32 建曲 33 昆明山海棠 34 松石 35 苦卖菜 36 败酱草 37 贯众 38 金沙藤 39 金腰草 40 降香油 降香油 41 青金石 42 珊瑚 珊瑚 43 珍珠层粉 44 胆酸 45 秦艽花 46 脑石 47 豹骨 豹骨 48 透骨草 49 酒曲 50 铁丝威灵仙 铁丝威灵仙 51 铁棒锤叶
69 蔓荆子茎及叶 70 鲜竹沥 71 橘叶
雅叫哈顿散 复方鲜竹沥液 乳块消片
沉香、牛心、毛巴豆 (根、茎、叶)、羊胆、甘青青兰、多叶 棘豆、角茴香、直立紫堇、苦菜、迭达、细叶白前子、草
72 藏木香
催汤丸
乌芽、胆矾、菱角、铜绿、麻花秦艽花、鹿茸草、黑草乌
藏木香 73 鳖甲胶 74 糯米
七味铁屑丸 化回症回生片 复方鸡血藤膏
省市中药材标准中均有收载, 其基源分属毛茛科乌头 上一支蒿、昆明山海棠、罂粟壳浸膏以及同名异物药
属 6 种植物的块根。 如果这些问题不能尽快解决, 中 药制剂的质量问题就没有保证。
21 制剂处方药材饮片名称有的不够规范, 与本
材, 例如贯众、透骨草、官柱等, 应尽快制定其质量标 准, 确保中药制剂的安全有效。
药典制剂处方中无基源药材及制剂名单
序号 ቤተ መጻሕፍቲ ባይዱ 2
3 4 5 6 7 8 9
10 11 12 13 14 15 16
17
药材名称
九眼石 人参茎叶皂苷 人参茎叶皂苷 人参提取物 三七叶 小檗皮 广东神曲 广藿香叶 乌鸡 五灵脂膏 五灵脂膏 五灵脂膏 五灵脂膏 巴夏嘎 木香马兜铃 止泻木子 牛心粉 丝棉 (炭) 冬瓜子 北败酱 北败酱 四季青
文献(2) 记载乳酸溶液为 60% 乳酸与 30% 乳酸 酐的混合物; 而乳酸酐与 N aO H 在室温下中和反应 极慢, 要在碱性条件下煮沸或 115℃加热后乳酸酐 才能分解成乳酸钠(2)。 因此, 室温下乳酸与 N aO H 中和制备的乳酸钠溶液, 实际上是乳酸钠与乳酸酐 的混合溶液。 为此, 乳酸钠溶液存在如下问题:
中国药品标准 2006 年第 7 卷第 3 期 (总 169) 9
52 鸭嘴花 53 猪去氧胆酸
猪去氧胆酸 54 猪脊髓 55 绿绒蒿 56 船形乌头 57 雪上一支蒿 58 鹿尾 59 鹿茸血 60 寒食曲 61 猴头菌培养物浸膏 62 紫苏叶油
紫苏叶油
二十五味松石丸 清开灵口服液 清开灵注射液 大补阴丸 二十五味松石丸 二十五味松石丸 三七伤药片 安坤赞育丸 参茸固本片 七珍丸 猴头健胃灵胶囊 藿香正气口服液 藿香正气水
31《药典》未收载的药材及饮片, 如果部颁标准有
L evl. 的干燥树皮。而在第五册中为樟科植物肉桂C. 收载, 且无同名异物现象, 可执行部颁或局颁标准, 例
ca ssia P ressl. 的干燥根皮。还有三七伤药片中的毒性 如硼砂[4]、西青果[5]等。 国家标准未收载的常用中药
药“雪上一支蒿”, 在《药典》1977 年版、四川、贵州等 5 材, 例如白花蛇舌草、北败酱、冬瓜子; 毒性药, 例如雪
中药成方制剂第 19 册, 但实际并未按制剂管理。《药 典》附录 收载的六神曲只记述了六神曲的炮制方
紫苏叶油 63 紫菀花 64 雄蚕蛾 (制) 65 黑木耳
黑木耳 66 熊胆粉 67 獐牙菜
獐牙菜
藿香正气软胶囊 二十五味珊瑚丸 蚕蛾公补片 产复康颗粒 妙济丸 万应胶囊 十三味榜嘎散 二十五味珊瑚丸
[ 4 ] 药典委员会. 卫生部药品标准. 藏药. 第一册 1995 1 61 114 [ 5 ] 国家食品药品监督管理局. 进口药材质量标准 2004 8 24
对“乳酸钠溶液”标准的疑议
马忠杰(解放军第 16 医院 新疆 阿勒泰 836501)
D oubt on the D rug Standard of Lactic Ac id Solution M a Zho ng2jie (PL A N o. 16 H osp ita l, A leta i 836501)
