03第三章烯烃-chy
合集下载
有机化学 第三章 烯烃全

KOH
Br
C2H5OH
+ HBr
17
3-4 烯烃的物理性质
物质状态 C2~C4 气体,C5~C18液体 ,C19~固体
沸点、熔点和相对密度 均随相对分子量的增加而上升;直链烯烃的沸 点略高于支链烯烃;末端烯烃(α-烯烃)的沸点 略低于双键位于碳链中间的异构体。
溶解性 不溶于水,易溶于有机溶剂。
HCl CF3CH2CH2 Cl
Cl
CF3CH2CH2
(主)
HCl CF3CHCH3
Cl
Cl
CF3CHCH3
35
烯烃的亲电加成反应
HX反应活性 HI > HBr > HCl > HF
H2C CH2
HBr HAc
CH2 Br
CH2 H
HCl H2C CH2 AlCl3
H2C CH3 Cl
36
与硫酸的加成 ——间接水合
H3C C
H
CH3 C
H
H C
H3C
CH3 C
H
顺式
反式
7
3-2 烯烃的异构和命名
系统命名法
选主链:选择含双键的最长碳链作主链, 称 “某烯”, 若碳原子数大于10, 则称为“某碳 烯”;
编号:从靠近双键的一端开始编号,确定双键 (两双键碳原子中编号小的数字)及其它取代 基的位次;
其它同烷烃的命名。
18
顺 反 异 构 体 的 差 异
极性较大, b.p. 较高 极性较小, b.p. 较低
对称性较差,m.p. 较低
对称性较好,m.p. 较高19
3-5 烯烃的化学性质(重点)
• 反应:加成、氧化、卤代
α HCCC
有机化学第三章烯烃分析

CC
δ+ δ–
-X—
X—
H
碳正离子
X CC
H
25
Markovnikov 规则
1
1
+ H Br 2 2
Br
Br
第三章 烯烃 (Alkene)
一、烯烃的结构 二、烯烃的同分异构和命名 三、烯烃的来源和制备 四、烯烃的物理性质 五、烯烃的化学性质
烯烃概述
烯 烃:分子中含有碳碳双键的不饱和烃 官能团:碳碳双键 通式:CnH2n ,有一个不饱和度。
2
乙烯
乙烯与生长素、赤霉素一 样,是植物的内源激素, 不少植物器官中都含有少 量乙烯,尤其是在成熟的 果实中,有较多的乙烯, 利用人工方法,提高未成 熟青果中的乙烯含量,可 促使果实成熟,是水果的 催熟剂。
OC
CO
CO
-I > -Br > -Cl > -SO3H > -F > -OCOR > -OR >-OH >… … >-CR3 > -C6H5 > - CHR2 > -CH2R > - CH3 > -H
15
顺式不一定是Z构型,反式也不一定是E构型
H3C C
CH3CH2
CH3 C
Cl
(Z)-3-甲基-2-氯-2-戊烯 顺-3-甲基-2-氯-2-戊烯
H3C C
H
CH3 C
H
H C
H3C
CH3 C
H
顺式
反式
7
3-2 烯烃的异构和命名
系统命名法
选主链:选择含双键的最长碳链作主链, 称 “某烯”, 若碳原子数大于10, 则称为“某碳 烯”;
编号:从靠近双键的一端开始编号,确定双键 (两双键碳原子中编号小的数字)及其它取代 基的位次;
有机化学课件——第三章 烯烃

2、与烷烃的差异
由于烯烃中有π键,其物理性质与烷烃 又有差异。例如,端烯烃的沸点比相应的 烷烃略高;烯烃的折射率比相应的烷烃大; 烯烃在水中的溶解度比相应的烷烃略大; 相对密度也比相应的烷烃大,但仍小于1。 这主要是它们的极性大于烷轻。
3、顺反异构体的差异
烯烃的顺、反异构体的物理性质也有差 异。一般说来反式异构体的沸点比顺式异 构体的沸点低,而反式异构体的熔点却比 顺式异构体的高。这是由于反式异构体分 子极性小,对称性好;反式异构体热力学 能低,比较稳定。
命名规则 例子
命名规则
一般在烯烃名称前面加“顺”(cis-) 或“反”(trans-)
例子
顺-2-丁烯
反-2-丁烯
反-3-甲基-2-戊烯
?
(2)Z/E标记法
Z式:双键碳原子上两个较优基团或原子处于双键 同侧。 E式:双键碳原子上两个较优基团或原子处于双键 异侧。
次序规则 命名规则 例子
次序规则
Methylene
CH3CH= 亚乙基
ethylidene -CH2CH2- 1,2- 亚乙基 ethylene (dimethylene)
(CH3)2C= 亚异丙基
isopropylidene -CH2CH2CH2-
1,3- 亚丙基 trimethylene
1、构造异构体的命名
(1)衍生命名法 (2)系统命名法
位次,写在烯烃名称之前。
例子
3-庚烯
5-甲基-3-庚烯
2-乙基(-1-)戊烯
3,4-二丙基-1,3,5-己三烯 2-十八碳烯
2、顺反异构体的命名
(1)顺反标记法 (2)Z/E标记法
(1)顺反标记法
顺式:双键碳原子上两个相同的原子或基团处于 双键同侧。
有机化学第三章 烯烃ppt课件

( 优 ) C H C H C H ( 优 ) 3 2 3 C H C H ( C H ) ( 优 ) 3 3 2 顺序大 C C C C 的基团称 H C H 3 ( 优 ) C H C H 3 2 C H C H C H 较优基团 2 2 3
(Z)- 3-甲基-2-戊烯
(E)- 3-甲基-4-异丙基-3-庚烯
C H C H = C H 3 丙 烯 基
(2) 顺反异构体的命名和 Z、E标记法
C H 3 C H C H 2 3 CC H H 顺 2 戊 烯 H C H C H 2 3 CC C H H 3 反 2 戊 烯
Z式:双键碳原子上两个较优基团或原子处于双键同侧。 E式:双键碳原子上两个较优基团或原子处于双键异侧。
C ( C l 、 H 、 H ) C ( F 、 F 、 H ) C ( C 、 H 、 H 、 ) C ( C 、 C 、 H )
注意:优先顺序由原子序数确定而非由基团体积大小确定
3) 含双键或叁键的基团,则作为连有两个或叁个相同 的原子。。
C C H ( C )( C ) C CH ( C )( C ) C ( C H ) 3 3 C H 3 C C H 3 C H 3 C HC H 2 ( C )( C ) C CH HH
① 物理性质:顺反异构体的物理性质如熔点、沸点和偶 极矩等均有显著的不同。 ② 化学性质:因为官能团相同,化学性质基本相同,但 是与空间排列有关的化学性质则有差异。如丁烯二酸的脱水 反应: H C C H COOH COOH -H2O H H C C C=O C=O
如何命名下列物质?
Br H
C=C H CH3
反-1-溴丙烯
Cl
C=C CH3
Cl
讨
(Z)- 3-甲基-2-戊烯
(E)- 3-甲基-4-异丙基-3-庚烯
C H C H = C H 3 丙 烯 基
(2) 顺反异构体的命名和 Z、E标记法
C H 3 C H C H 2 3 CC H H 顺 2 戊 烯 H C H C H 2 3 CC C H H 3 反 2 戊 烯
Z式:双键碳原子上两个较优基团或原子处于双键同侧。 E式:双键碳原子上两个较优基团或原子处于双键异侧。
C ( C l 、 H 、 H ) C ( F 、 F 、 H ) C ( C 、 H 、 H 、 ) C ( C 、 C 、 H )
注意:优先顺序由原子序数确定而非由基团体积大小确定
3) 含双键或叁键的基团,则作为连有两个或叁个相同 的原子。。
C C H ( C )( C ) C CH ( C )( C ) C ( C H ) 3 3 C H 3 C C H 3 C H 3 C HC H 2 ( C )( C ) C CH HH
① 物理性质:顺反异构体的物理性质如熔点、沸点和偶 极矩等均有显著的不同。 ② 化学性质:因为官能团相同,化学性质基本相同,但 是与空间排列有关的化学性质则有差异。如丁烯二酸的脱水 反应: H C C H COOH COOH -H2O H H C C C=O C=O
如何命名下列物质?
Br H
C=C H CH3
反-1-溴丙烯
Cl
C=C CH3
Cl
讨
第3章-烯烃

构造异构:
是由于原子或基团在分子中排列和结 合的顺序不同而引起的异构称构造异构。 (包括碳链异构和官能团位置异构 )
烯烃的命名
* 烯烃的命名与烷烃相似,用衍生物命名法 命名时,以乙烯为母体,如:CH3CH=CH2(甲 基乙烯)。
* 系统命名:与烷烃相似,不同的是: 1)主链必须是含有双键的最长链 2)编号时必须从靠近双键的一端开始 3)命名时写出双键的位次标在母体名称前, 双键在第一个碳时可省略 “1”。 例如:
* 催化加氢
催化加氢的反应条件和所用的催化剂有关,
用Pt或Pd做催化剂时,反应在常温下就能进行,
用Ni则需较高的温度和压力。近年来工业上常
用雷尼镍,因为它的活性较高,加氢可以在常
温和不高的压力下进行。这种加氢反应是在催 化剂表面进行的,又叫表面催化。反应历程如
下:
* 亲电加成反应 在反应中具 有亲电性能的试剂叫亲电试剂 (electrophile),由亲电试 剂的作用而引起的加成反应叫 亲电加成反应(electrophilic addition)。
Pd 存在下通入氧气)可得到醛和酮。
由臭氧化物水解所得的醛或酮保 持了原来烯烃的部分碳链结构,因 此由醛、酮结构的测定,就可以推 导原来烯烃的结构。
* 聚合反应
烯烃可在引发剂或催化剂作用下, π
键断裂而相互加成,得到长链的高分子化合
物,由低相对分子量的有机化合物相互作用 而生成高分子化合物的反应叫做聚合反应。 如:
* π键的特点:
1.π键键能小,不如σ键稳定,比较容易断 裂。 2.π键电子云分布在原子所在平面的上下方, 具有较大的流动性,容易受到外界电场 的影响。电子云比较容易极化,发生化 学反应。
3.由于π键是两个P轨道“肩并肩”的重叠而 成,所以不能自由旋转,否则π键将被 破坏。
是由于原子或基团在分子中排列和结 合的顺序不同而引起的异构称构造异构。 (包括碳链异构和官能团位置异构 )
烯烃的命名
* 烯烃的命名与烷烃相似,用衍生物命名法 命名时,以乙烯为母体,如:CH3CH=CH2(甲 基乙烯)。
* 系统命名:与烷烃相似,不同的是: 1)主链必须是含有双键的最长链 2)编号时必须从靠近双键的一端开始 3)命名时写出双键的位次标在母体名称前, 双键在第一个碳时可省略 “1”。 例如:
* 催化加氢
催化加氢的反应条件和所用的催化剂有关,
用Pt或Pd做催化剂时,反应在常温下就能进行,
用Ni则需较高的温度和压力。近年来工业上常
用雷尼镍,因为它的活性较高,加氢可以在常
温和不高的压力下进行。这种加氢反应是在催 化剂表面进行的,又叫表面催化。反应历程如
下:
* 亲电加成反应 在反应中具 有亲电性能的试剂叫亲电试剂 (electrophile),由亲电试 剂的作用而引起的加成反应叫 亲电加成反应(electrophilic addition)。
Pd 存在下通入氧气)可得到醛和酮。
由臭氧化物水解所得的醛或酮保 持了原来烯烃的部分碳链结构,因 此由醛、酮结构的测定,就可以推 导原来烯烃的结构。
* 聚合反应
烯烃可在引发剂或催化剂作用下, π
键断裂而相互加成,得到长链的高分子化合
物,由低相对分子量的有机化合物相互作用 而生成高分子化合物的反应叫做聚合反应。 如:
* π键的特点:
1.π键键能小,不如σ键稳定,比较容易断 裂。 2.π键电子云分布在原子所在平面的上下方, 具有较大的流动性,容易受到外界电场 的影响。电子云比较容易极化,发生化 学反应。
3.由于π键是两个P轨道“肩并肩”的重叠而 成,所以不能自由旋转,否则π键将被 破坏。
chem-03烯烃

慢
溴鎓离子
⑵加卤化氢 (HX)
CH2 CH2 + HX CH3CH2X
反应活性: 原因: 反应活性: HI > HBr > HCl(原因:键能、原子半径 原因 键能、原子半径) 用 途:用于制备一卤代烷
反应历程(分两步进行) 反应历程(分两步进行)
碳正离子中间体
碳正离子
是一个活泼的中间体 是一个活泼的中间体 碳原 产生原因 碳碳双键不能自由旋转 当双键两个C各连有不同的原子或基团时, 当双键两个 各连有不同的原子或基团时,就会产 各连有不同的原子或基团时 生顺反异构。 只要双键任一C连有相同的原子或基团 连有相同的原子或基团, 生顺反异构 。 只要双键任一 连有相同的原子或基团 , 都不会产生顺反异构。 都不会产生顺反异构。
CH3CH2CH2CH2Br
95%
在日光或过氧化物存在下,烯烃与 在日光或过氧化物存在下,烯烃与HBr的加成的取向正好 的加成的取向正好 与马尔科夫尼科夫规律相反(反马氏规则) 与马尔科夫尼科夫规律相反(反马氏规则)
※注:仅对HBr有效(HCl,HI均无此反应) 仅对HBr有效(HCl,HI均无此反应) HBr有效 均无此反应
①诱导效应 定义
δ
+
δ
-
方向
C
Y
斥电子诱导、 斥电子诱导、正诱导
+I
C C
H X 吸电子诱导、 吸电子诱导、负诱导 -I
-F>-Cl>-Br>-I>-OR>-C6H5>-CH2=CH2>H> Cl> Br> OR> -CH3>-CH2CH3>-C(CH3)3 见书P 见书P315 ②超共轭效应 电子离域的现象称为共轭 电子离域的现象称为共轭 由σ键参与的共轭称为超共轭 键参与的共轭称为超共轭 共轭称为 CH3 CH2= CH2
溴鎓离子
⑵加卤化氢 (HX)
CH2 CH2 + HX CH3CH2X
反应活性: 原因: 反应活性: HI > HBr > HCl(原因:键能、原子半径 原因 键能、原子半径) 用 途:用于制备一卤代烷
反应历程(分两步进行) 反应历程(分两步进行)
碳正离子中间体
碳正离子
是一个活泼的中间体 是一个活泼的中间体 碳原 产生原因 碳碳双键不能自由旋转 当双键两个C各连有不同的原子或基团时, 当双键两个 各连有不同的原子或基团时,就会产 各连有不同的原子或基团时 生顺反异构。 只要双键任一C连有相同的原子或基团 连有相同的原子或基团, 生顺反异构 。 只要双键任一 连有相同的原子或基团 , 都不会产生顺反异构。 都不会产生顺反异构。
CH3CH2CH2CH2Br
95%
在日光或过氧化物存在下,烯烃与 在日光或过氧化物存在下,烯烃与HBr的加成的取向正好 的加成的取向正好 与马尔科夫尼科夫规律相反(反马氏规则) 与马尔科夫尼科夫规律相反(反马氏规则)
※注:仅对HBr有效(HCl,HI均无此反应) 仅对HBr有效(HCl,HI均无此反应) HBr有效 均无此反应
①诱导效应 定义
δ
+
δ
-
方向
C
Y
斥电子诱导、 斥电子诱导、正诱导
+I
C C
H X 吸电子诱导、 吸电子诱导、负诱导 -I
-F>-Cl>-Br>-I>-OR>-C6H5>-CH2=CH2>H> Cl> Br> OR> -CH3>-CH2CH3>-C(CH3)3 见书P 见书P315 ②超共轭效应 电子离域的现象称为共轭 电子离域的现象称为共轭 由σ键参与的共轭称为超共轭 键参与的共轭称为超共轭 共轭称为 CH3 CH2= CH2
第三章烯烃PPT课件

4-乙基环己烯
环戊烯
1-甲基环己烯
.
3-氯环庚烯
16
顺反异构体的命名
顺反命名法: 系统名称前加一“顺(或cis)”或“反(trans)”字。
顺-2-戊烯 cis-2-pentene
反-2-戊烯 trans-2-pentene
顺反命名法有局限性,即在两个双键碳上所连接的两个基团彼此 应有一个是相同的,彼此无相同基团时,则无法命名其顺反。
这是两种不同的命名法。顺、反异构体 的命名指的是相同原子或基团在双键平面同一 侧时为"顺",在异侧时为"反"。Z、E构型指 的是原子序数大的原子或基团在双键平面同一 侧时为"Z",在异侧时为"E"。
.
19
Cl
H
Br
Cl
反- 1,2-二氯-1-溴乙烯
Trans- 1-bromo-1,2-dichloroethene
几何异构体之间在物理性质和化学性质上都可以 有较大的差别,因而容易分离。
满足条件:每个双键碳上都. 连有不同原子或原子团 9
a
C
b
a
C
b
a
C
b
a
C
d
a
C
b
c
C
d
a
C
a
c
C
d
.
10
己烯雌酚
反式(有生理活性)
顺式 (无)
治疗卵巢功能不全或
垂体功能异常引起的
各种妇科疾病
.
11
三.烯烃的命名
(1)普通命名法
➢补充:苄基和烯丙基碳正离子的相对稳定性:
PhCH2 > 3°> 2°> 1°
第03章烯烃ppt课件

(4) 其它命名原那么同烷烃, 如:
●烯基:烯烃上去掉一个氢原子后剩下的基团。
●几个重要的烯基: CH2 CH
CH3CH CH CH2 CH CH2
乙烯基 1-丙烯基 2-丙烯基(烯丙基)
H3C C
H3C CH Cl
CH2 C CH3
CH2 C10H3 C
CH2 Cl
1-甲基乙烯基(异丙烯基)
普通不用顺反命名法
—当多烯烃主链的编号有两种能够时,规定编号由 Z 型双键一端起始。 例如:
3. 顺、反异构体的命名与〔Z〕、〔E〕构型的命名区别:
●Z/E命名法为IUPAC系统命名(适用于一切构造) ●顺、反异构体的命名指的是一样原子或基团在双键平面同一侧时 为“顺〞,在异侧时为“反〞。 ● Z、E构型指的是原子序数大的原子或基团在双键平面同一侧时 为"Z",在异侧时为"E"。
α C3H C H C2H+
XX
O NB( r 简 称 N B S ) h ν α C2H C H C2H
O
Br
2 α氢原子的氧化 —烯烃的α氢原子易被氧化,在烯烃氧化的讨论中已提到丙烯在一定条 件下可被空气催化氧化为丙烯醛。但在不同条件下,丙烯还可被氧化为 丙烯酸。
3 氨氧化反响 —丙烯在氨存在下的氧化反响叫做氨化氧化反响,简称氨氧化反响。 由此可以得到丙烯腈。 —丙烯中的甲基氧化为氰基(-CN)
a
aa
a
CC
b
b
CC
b
d
a
aa
d
CC
a
b
bCCd
有 顺 反 异 构 的 类 型
无 顺 反 异 构 的 类 型
●烯烃具有双键,其异构景象较烷烃复杂,主要包括: —碳干异构; —双键位置不同引起的官能团位置异构〔position isomerism〕; —双键不能自在旋转产生的立体异构景象--顺反异构。如:
03第三章烯烃-chy

C H2 I
氢加到含氢较多,为主的反应
叫:马克尼克夫(Markovnikov) 法则 — 亲电的正部分要加在使正碳离子稳定的部分上
Markovnikov规则的解释: 理由 1 诱导效应
1)诱导效应:受分子中电负性不同的原子或基团的影响,整个
分子中成键的电子云向着一个方向偏移,分子发生极化的效应。 δ+
2
C H
0.109 (nm)
s
S 成分低(1/4)
s
3
sp
0.110 (nm)
S 成分越多,键越短
C:1S22S22P2
激发 2p 2s 2p 2s sp2杂化
sp2
基态
激发态
每个sp2杂化轨道具有1/3s成分和2/3p成分。
sp2杂化轨道形状:
+
-
H C H
+ _
H C H
烯 烃 富 电 子
3-乙基-2-己烯
3.2 异构和命名 3.2.1烯烃的同分异构现象 构造 异构 碳架异构
烯烃 的异 构
官能团位置异构
立体 异构
顺反 异构
官能团排 布不同
构象与构型涵义的比较
起 因 转化能量 分离情况 绕σ 键轴相 对旋转而得 象 的各种空间 排列 因σ 键轴旋 转受阻而引 型 起
不同构象的 分子一般不 一般较低 能分离,是 可逆的 不同构型的 分子能稳定 存在,可以 分离,是不 可逆的。
反式 μ= 0 bp = 0.9 0C (偶极矩小) mp = -106 0C (对称性高)
3.4 烯烃的化学性质 C
H 3C
官能团
C H = C H2
H
易发生加成、 取代、氧化、 聚合反应
有机化学课件第三章烯烃
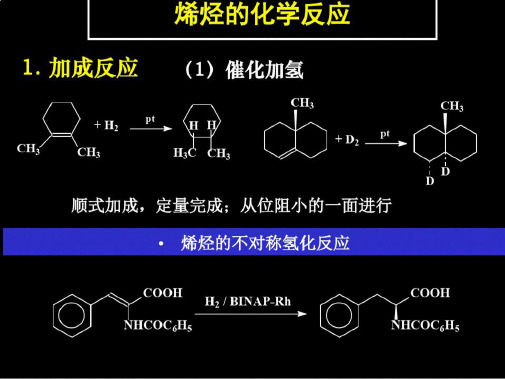
第三十页,编辑于星期一:二十三点 十四分。
第三十一页,编辑于星期一:二十三点 十四分。
第三十二页,编辑于星期一:二十三点 十四分。
第三十三页,编辑于星期一:二十三点 十四分。
第三十四页,编辑于星期一:二十三点 十四分。
第三十五页,编辑于星期一:二十三点 十四分。
第三十六页,编辑于星期一:二十三点 十四分。
第四十四页,编辑于星期一:二十三点 十四分。
第四十五页,编辑于星期一:二十三点 十四分。
第四十六页,编辑于星期一:二十三点 十四分。
第四十七页,编辑于星期一:二十三点 十四分。
第三十七页,编辑于星期一:二十三点 十四分。
第三十八页,编辑于星期一:二十三点 十四分。
第三十九页,编辑于星期一:二十三点 十四分。
第四十页,编辑于星期一:二十三点 十四分。
第四十一页,编辑于星期一:二十三点 十四分。
第四十二页,编辑于星期一:二十三点 十四分。
第四十三页,编辑于星期一:二十三点 十四分。
第十六页,编辑于星期一:二十三点 十四分。
第十七页,编辑于星期一:二十三点 十四分。
第十八页,编辑于星期一:二十三点 十四分。
第十九页,编辑于星期一:二十三点 十四分。
第二十页,编辑于星期一:二十三点 十四分。
第二十一页,编辑于星期一:二十三点 十四分。
第二十二页,编辑于星期一:二十三点 十四分。
第一页,编辑于星期一:二十三点 十四分。
第二页,编辑于星期一:二十三点 十四分。
第三页,编辑于星期一:二十三点 十四分。
第四页,编辑于星期一:二十三点 十四分。
第五页,编辑于星期一:二十三点 十四分。
第六页,编辑于星期一:二十三点 十四分。
有机化学课件——Chapter 03 烯烃

有机化学课件
32
第三章 烯烃、炔烃和二烯烃
(4) 区位选择性 马尔科夫尼科夫规则(Markovnikov’s Rule)(原始陈述): 质子酸和烯烃双键的加成得到的主要产物是酸的质子与 拥有氢原子最多的碳原子相连(Rich get richer). 马尔科夫尼科夫规则(通用规则): 烯烃的亲电加成中,亲 电试剂以产生最稳定中间体的方式加成.
E-Z命名规则
首先将双键每个碳原子上连接的两个原子或基团按“次序规 则”确定出优先次序. 优先基团在同侧命名为Z- (zusammen 德语“在一起”). 优先基团在异侧命名为E-(entgegen 德语“相反”).
有机化学课件
21
第三章 烯烃、炔烃和二烯烃
1 H3C
1 Cl
2 H
Cl 1 CH CH3 H 2
两种亚基:中文名称通过前面的编号来区别, 英文名称通过词尾来区别
有机化学课件
17
第三章 烯烃、炔烃和二烯烃
命名下列化合物
苯乙烯
1,4-二乙烯基苯
甲叉环己烷(亚甲基环己烷)
有机化学课件
18
第三章 烯烃、炔烃和二烯烃
4. 普通命名法
普通命名法通常用于命名简单化合物。
CH3 CH2 CH2 CH2 CH CH3 propylene CH2 C CH3 isobutylene
有机化学课件
5
第三章 烯烃、炔烃和二烯烃
3. π 键比σ键反应活性高。 键离解能(Bond dissociation energies): C=C BDE C-C BDE π bond 146 kcal/mol -83 kcal/mol 63 kcal/mol
有机化学课件
6
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
下面三式有无 顺反异构?
C H 3C H 2 H
H C C H
CH3 C H C
CH3 CH3
CH3 C ( C H 3) 2 C H C
CH3 H
C 5 H 10
C C
C C
C C
C C
C C
官能团位置不同
C C C C C C C C C C
碳架不同 + 官能团位置
C
C C
C
C
C
C
C
C
C
C H3
AlCl3
HX的活泼性: HI >HBr >HCl
醋酸
C H 3C H CH2 + HBr C H 3 C H C H 3 + C H 3 C H 2C H 2 Br Br
主要产物
次要产物
H 3C
CH I
C H2 H
多,主要 2-碘甲烷 少,次要
H 3C
HC = C H2 + H I
H 3C
CH H
• 溶解性:难溶于水,易溶于苯,乙醚,氯仿,四氯化碳等 有机溶剂。
熔点—对称性—大,mp大 沸点—偶极矩—大,bp大
H C C H CH 3 CH 3
H C C CH 3 H
CH 3
顺式:沸点高 反式:沸点低
顺式
μ = 0.33D bp = 3.7 0C (偶极矩大) mp = -139 0C (对称性低)
+
H
H H H C C H
+
H
H
H
C H
9个超共轭
6个超共轭
(4)与水加成
CH 2 =CH
2
+ H
2O
H 3 PO 4 /硅藻土 300 C,7~8MPa
。
CH 3 -CH 2 -OH
OH
CH 2 =CHCH
3
+ H
2O
H 3 PO 4 /硅藻土 195 C,2MPa
。
CH 3 -CH-CH
异丙醇
烯 烃 富 电 子
(-NH2, -OH, -OR, -CN, Fe2+)
α-H的取代反应(P40)
C H 3C H C H 2 + C l2
400~500℃
C H 2C H Cl
CH2
自由基取代反应
α -C:与官能团直接相连的碳。α -H:α -C上的氢。
(3) 与卤化氢的加成
130~150℃
H 2C CH2 + HCl C H 3C H 2 C l
3.4.1 加成反应
通式:
C
C
+
Y--Z
C Y
C Z
1、1个π 键 2个σ键; 2、sp2杂化的碳 sp3杂化的碳;
3、构型的改变:平面 四面体。
是个放热反应
3.4.1.1催化加氢
C C
+
H2
C H
C H
ΔH = 125.4 kJ/mol
常用的催化剂
P t, P d, N i, R h
3-乙基-2-己烯
3.2 异构和命名 3.2.1烯烃的同分异构现象 构造 异构 碳架异构
烯烃 的异 构
官能团位置异构
立体 异构
顺反 异构
官能团排 布不同
构象与构型涵义的比较
起 因 转化能量 分离情况 绕σ 键轴相 对旋转而得 象 的各种空间 排列 因σ 键轴旋 转受阻而引 型 起
不同构象的 分子一般不 一般较低 能分离,是 可逆的 不同构型的 分子能稳定 存在,可以 分离,是不 可逆的。
C Cl
实际上
Br - 背面进攻
Br
Br
C Br C
C Br C
C Br
C
注意:氯翁离子不易形成
亲电加成 (Electrophilic addition) 亲电试剂所起的反应
与给出电子 的物质才 进行反应
H C H + _ H C H
亲电试剂 — 酸性,缺电子 (X2, HX, H2SO4, Fe3+, Hg2+) 亲核试剂 — 碱性,富电子
H 2C = C H 2 + H
2
C H3
C H3
作用:反应定量完成,可用于测定双键数目
ΔE
ΔE
催化使活化能减小 但反应热不变
CH2 =CH2
+ H2
ΔH
CH3—CH3
反应进程
(2)烯烃与卤素的加成
C C l4
C
C
+
X
X
C X
C X
溶剂: CH2Cl2, CHCl3, CCl4
.. H 2O
C H3 H 3C C C H3 O H2
+
C H3 _ H
+
H 3C
C C H3
OH
叔丁醇
醇
高温 低温
烯
这是一个 可逆反应
(5)烯烃与 H-OSO3H(硫酸)的加成
H 2S O 4 C C 0 C H O S O 3H H
o
间接水合法
C C OH
H 2O C C
遵循马氏规则
(乙醇和异丙醇的工业制法)
底物
C
—络合物 不能分离
+
Br Br
C C
富 电 子
Br
Br
C
Br C + C Br
诱导极化 分子极化 亲电试剂 溴翁离子
慢
旧键破 新键成
sp2杂化 正碳离子 p 空
Br C + C Br
快
Br
.. H 2O
Br C C
C Br
C O H2
Br C
+
C
Cl
-
C Br
-
Cl
+
+ H
+
X
-
活泼,易反应
不活泼 不易反应
次氯酸的加成反应 同样是 反式加成
C H3 O H Cl C H3
+
HO C l
(7)与烯烃加成(烯烃的聚合)
C H3 C H2 C H = C H
请记住这些基的名称
3.2.3 烯烃的命名
1.系统命名法 b.编号:使C=C双键的编号最小。 c.写出名称:要标出双键的位置。
CH3 CH3
5
a.主链:选择含C=C双键的最长的碳链为主链,称为“某烯”。
CH
4
CH
3
CH
2
CH3
1
CH3—CH2—C=CH—CH3 4-甲基-2-戊烯 CH2—CH2—CH3 3-乙基-2-己烯
CH 2 CH 2 CH 3 CH CH 3 CH 3
最长链
(Z)-3-甲基-4-异丙基-3-庚烯
如:(2)
CH 3 C CH 3 CH 2 C
CH 2 CH 3 CH 2 CH 2 CH 3
相同基团 , 两侧
大基团,同侧
反-3-甲基-4-乙基-3-庚烯
Z或E式与顺或反式
没有相关性
(Z)-3-甲基-4-乙基-3-庚烯
命名举例:
C (1) C C C C C C
双键为小
4,4-二甲基-2-戊烯
C (2) C C C C C C
3-甲基-2-乙基-1-丁烯
怎样命名以下化合物:
C H3 C C H 3C H 2 C C HC H3 C H3 C H 2C H 2C H 3
顺式还是反式?
E-Z命名法
2 Z,E–命名法
第三章
不饱和烃
不饱和烃:分子中含有不饱和键的碳氢 化合物。包括单烯烃(烯烃)、多烯烃、 环烯烃和炔烃等。
A 烯烃
B 炔烃
C 双烯烃
• 不饱和烃的结构、同分异构现象、命名 • 物理性质、化学性质
I. 烯烃
官能团 — 活泼部分
(分子中)
C
C
Cn H2n
环烷烃
3.1 烯烃的结构
CH2 甲烯 (卡宾)本身不存在
肩碰肩 (侧面交盖) 键能小 263kJ/mol 分布在分子平 面上下;分布 分散,易极化 不能自由旋转
3.2 异构和命名
系统命名法
1.选择包含双键的最长碳链为主链。 2.主链碳原子的编号由距离双键最近的一端开始; 3.命名时必须注明双键的位置,写在母体名称之前。
例: CH3—CH2—C=CH—CH3 CH2—CH2—CH3
3
催化剂:强酸(H2SO4, H3PO4 等) 可用于醇的制备,反应副产物多,缺乏制备价值。 遵循马氏规则 为了减少“三废”,保护环境,可用固体酸,如杂 多酸代替液体酸催化剂。
— 烯烃的直接水合反应
C H3 H 3C C C H2 + H
+
C H3 H 2 S O 4 (60%) H 3C C C H3
(X = C l, B r)
常温下可迅速进行,不需高温、光照、 和催化剂。 卤素活性: F2>>Cl2 >Br2 >I2
I2一般不与烯烃发生反应, F2反应太激烈,易发生碳
链断裂,无实用意义。
应用:鉴别烯烃 例:烯烃 + 5%溴的CCl4溶液(溴水) 红棕色褪去
以乙烯和溴反应为例:
A、实验事实:
反式 μ= 0 bp = 0.9 0C (偶极矩小) mp = -106 0C (对称性高)
3.4 烯烃的化学性质 C
H 3C
官能团
C H = C H2
H
易发生加成、 取代、氧化、 聚合反应
受双键影响很活泼
烯烃是很活泼化合物
