QS记录表
FAMI—QS标准

欧洲饲料添加剂和预混料经营者操作规范目录1前言2范围3术语和定义4管理体系4.1总要求4.2管理原则4.3文件总要求5管理职责5.1管理承诺5.2质量和安全方针5.3职责、权利和沟通5.4管理者代表5.5管理评审6资源管理6.1资源提供6.2人力资源6.2.1能力、意识和培训6.2.2个人卫生6.3基础设施6.3.1基本要求6.3.2设施、生产场所和设备的要求6.3.2.1设施和生产场所6.3.2.2设备6.4监视和测量设备的维护和控制6.5清洁6.6虫害控制6.7废物控制7产品实现7.1产品要求7.1.1与产品有关要求的确定7.1.2产品要求的符合性6.1.3顾客沟通7.2 HACCP计划7.3设计和开发7.3.1新产品和加工过程的开发7.3.2变更控制7.4原辅料管理7.4.1原辅料采购7.4.2原辅料验证7.5成品生产7.5.1生产和质量控制7.5.2生产过程的确认7.5.3标识和可追溯性7.5.4产品防护7.6运输7.6.1总要求7.6.2包装产品的运输7.6.3散装产品的运输8体系评审8.1总要求8.2内部审核9不合格品控制9.1总要求9.2投诉处理程序9.3召回9.4风险控制10统计技术1、前言(略)2、范围欧洲饲料添加剂和预混料操作规范不仅适用于从首次上市起的各个阶段的饲料和预混料经营者,同样适用于从第三国进口上市的饲料添加剂和预混料。
操作规范的目的是建立一个行业标准来减少相关的风险,以免饲料添加剂和预混料中掺杂的杂质进入食物链。
操作规范是以满足饲料卫生法规要求为目的的一个标准,另外,它还提供措施以确保和其它适用法律法规要求相一致。
3、术语和定义下列术语和定义适用于本指南和相关附件。
授权人:具有与岗位说明、工艺说明或管理体系中特别指明的能力、资格以及所预期相一致的人。
校准:是指通过可参照或可追溯的标准的前提下,为确定计量器具示值与对应的计量标准复现量值之间关系的一组操作。
残留物:由于设备上次使用带来原料或产品批与批之间的污染,将会改变物质的质量特性,并且超出已建立的规范要求。
QS手册新版

目录1 质量负责人任命书2 有关质量管理工作旳归口管理规定3 质量方针、质量目旳及实行方案4 质量管理组织机构图5 各部门职责和权限6 不合格品及纠正措施管理制度7 设备维修、清洗、消毒管理制度8 检测设备、计量器具管理制度9 文献管理制度10 采购管理制度11 生产作业指导书12 生产工艺管理考核措施13 生产过程质量管理控制及考核措施14 生产过程关键控制点旳管理规定15 关键控制点生产作业指导书16 产品质量检查管理制度附录1) 不合格品及纠正措施处理单2) 生产设备一览表3) 设备清洗消毒登记表4) 设备维修记录5) 设备检查记录6) 检测设备一览表7) 周期检定计划表8) 文献发放回收记录9) 采购计划10) 选料检查记录11) 腌制监控记录12) 卤制监控记录13) 进货检查记录及台账14) 生产过程质量检查记录15) 产品出厂检查汇报16) 产品销售明细表质量负责人任命书为推进企业质量管理工作有效开展,保证XXXX制品质量持续满足有关法规和顾客规定,现授权XXXXXXXX 为企业质量负责人,并授予如下职责和权限:1) 领导并组织企业建立、实行和保持质量管理制度;2) 向总经理汇报质量工作状况和任何改善旳需求;3) 组织召开企业质量分析会;4) 代表企业与外部各方联络质量工作有关事宜。
有关质量管理工作旳归口管理规定为推进企业平常质量管理工作旳有效开展,现决定在企业质量负责人领导下,XXXXXXXXX 负责企业质量管理工作旳归口管理,组织建立企业质量管理体系,并负责处理企业平常质量管理事务。
总经理质量方针、质量目旳及实行方案一、质量方针:精心选料精心制作精美口味精诚服务二、质量目旳:1、市场抽查质量、卫生指标达标率100%。
2、因质量问题而引起旳客户投诉为零。
3、最终产品一次检查合格率99%三、实行方案1 严格执行食品法规及产品质量、卫生原则规定2 建立、健全质量管理制度,深入持续运行。
JY-1.13-22食品QS食品净含量检验细则含抽样表2018

净含量检验细则净含量是指去除包装容器和其他包装材料后内装物的实际质量或体积,即内容物(可食物)的实际量。
计量检验时,不论产品的包装材料,还是与该产品包装在一起的其他材料,均不计入净含量。
预包装食品的净含量应符合产品标签中的明示值、相应产品标准以及《定量包装商品计量监督管理办法》(国家质监总局第75号令)的有关规定。
1抽样方案1.1产品包装的净含量复秤一般在生产车间中内包装完成后由车间主任或质检员进行,按随机取样方式,抽取当天生产的未检产品(5~10个包装)进行称量,并作记录。
每天一次,具体依据需要而定。
1.2产品出厂检验可按下列抽样方案的确定样本量。
再从成品仓库待检验产品批中按随机取样方式抽取规定的样本量。
1.3.1按照企业执行的产品标准和《产品出厂检验操作规程》的规定进行组批、抽样和检验,必要时按《定量包装商品净含量计量检验规则》(JJF1070-2005)中的规定进行。
1.3.2原辅材料验收检验:如原辅材料采购验收时需作净含量检验的,也可参照此法进行。
2检验方法与记录2.1计量器具选择:根据包装大小选用合适大小的计量器具(磅秤、台秤、天平等秤具或量筒等量具、量器)进行测定,结果记录于检验原始记录表中。
2.2连包装称量法2.2.1分别称取毛重(总重量)与皮重(内包装材料重)或平均皮重,毛重与皮重之差即为净含量。
2.2.2平均皮重测定方法:随机从包装材料库中抽取50只~100只包装袋,按下面两种方法:①分别一只只称量,相加后除以只数得到平均值;②一起称量后除以只数得到平均值,求得的平均值即为平均皮重(值)。
2.3去包装计量法2.3.1固态食品:仔细去掉包装物、直接称取其内容物(可食物)的重量(净含量)。
2.3.2液态食品:直接将内容物倒入量器(如量筒)中进行计量得到体积。
具体测定方法实例可参见附录C。
2.4相对密度值计量法2.4.1液态食品如食用油,净含量一般是以体积计的。
节2.3.2方法虽直接、准确,但食品检验属破坏性检验法,在生产企业中不实用、难以执行。
食品QS果冻加工过程和检验等记录表1
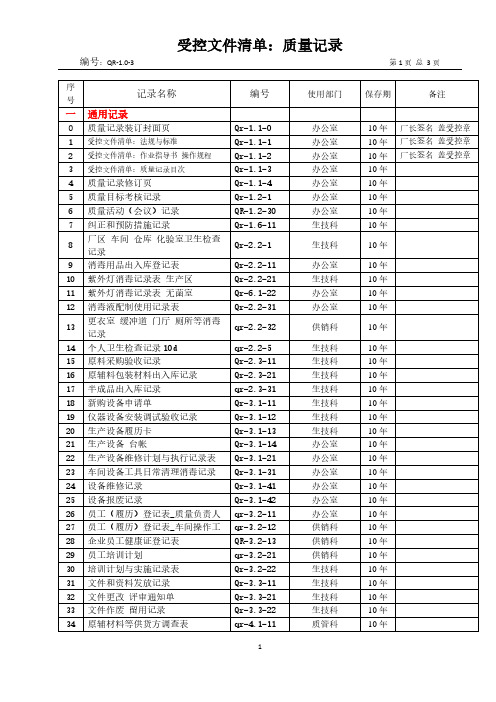
序号记录名称编号使用部门保存期备注一通用记录0 质量记录装订封面页Qr-1.1-0 办公室10年厂长签名盖受控章1 受控文件清单:法规与标准Qr-1.1-1 办公室10年厂长签名盖受控章2 受控文件清单:作业指导书操作规程Qr-1.1-2 办公室10年厂长签名盖受控章3 受控文件清单:质量记录目次Qr-1.1-3 办公室10年4 质量记录修订页Qr-1.1-4 办公室10年5 质量目标考核记录Qr-1.2-1 办公室10年6 质量活动(会议)记录QR-1.2-30 办公室10年7 纠正和预防措施记录Qr-1.6-11 生技科10年8 厂区车间仓库化验室卫生检查记录Qr-2.2-1 生技科10年9 消毒用品出入库登记表Qr-2.2-11 办公室10年10 紫外灯消毒记录表生产区Qr-2.2-21 生技科10年11 紫外灯消毒记录表无菌室Qr-6.1-22 办公室10年12 消毒液配制使用记录表Qr-2.2-31 办公室10年13 更衣室缓冲道门厅厕所等消毒记录qr-2.2-32 供销科10年14 个人卫生检查记录10d qr-2.2-5 生技科10年15 原料采购验收记录Qr-2.3-11 生技科10年16 原辅料包装材料出入库记录Qr-2.3-21 生技科10年17 半成品出入库记录qr-2.3-31 生技科10年18 新购设备申请单Qr-3.1-11 生技科10年19 仪器设备安装调试验收记录Qr-3.1-12 生技科10年20 生产设备履历卡Qr-3.1-13 生技科10年21 生产设备台帐Qr-3.1-14 办公室10年22 生产设备维修计划与执行记录表Qr-3.1-21 办公室10年23 车间设备工具日常清理消毒记录Qr-3.1-31 办公室10年24 设备维修记录Qr-3.1-41 办公室10年25 设备报废记录Qr-3.1-42 办公室10年26 员工(履历)登记表_质量负责人qr-3.2-11 办公室10年27 员工(履历)登记表_车间操作工qr-3.2-12 供销科10年28 企业员工健康证登记表QR-3.2-13 供销科10年29 员工培训计划qr-3.2-21 供销科10年30 培训计划与实施记录表Qr-3.2-22 生技科10年31 文件和资料发放记录Qr-3.3-11 生技科10年32 文件更改评审通知单Qr-3.3-21 生技科10年33 文件作废留用记录Qr-3.3-22 生技科10年34 原辅材料等供货方调查表qr-4.1-11 质管科10年序号记录名称编号使用部门保存期备注35 合格供货方名单汇总qr-4.1-12 质管科10年36 采购计划表qr-4.1-21 质管科10年37 采购合同QR-4.1-22 质管科10年38 生产计划表qr-5.1-41 质管科10年39 领料单qr-5.1-42 质管科10年40 成品发货通知单qr-5.1-51 质管科10年41 成品出入库记录qr-6.3-52 质管科10年42 产品销售明细表qr-6.3-53 质管科10年43 台帐检测设备化验器具qr-6.1-12 质管科10年44 检测设备化验器具履历卡qr-6.1-21 办公室10年45 计量器具计量检定计划与执行记录化验室qr-3.1-31 质管科10年46 计量器具计量检定计划与执行记录车间qr-3.1-3247 化验室试剂出入库记录qr-6.1-4148 无菌室与超净工作台无菌程度测试记录qr-6.1-51 质管科办公室10年49 无菌室与超净工作台消毒灭菌记录qr-6.1-5250 不合格(品)评审处置记录直式qr-6.4-1151 紧急放行申请处置单qr-6.4-2152 顾客投诉受理处置记录qr-6.4-4553 顾客满意度调查表a QR-6.4-4654 食品生产加工企业食品添加物质使用备案表Qr-6.3-4555 产品委托检验计划与执行记录Qr-6.3-456 产品召回处置记录表QR-7.2-157 产品回收通知(函)Qr-7.2-258 不安全食品销毁台帐QR-7.2-359 风险监测及评估信息收集和处置记录bQR-8.4-160 食品安全事故处置记录Qr-7.2-261 食品生产加工企业落实质量安全主体责任情况自查表QR-8.5-162 食品添加剂使用合规性自评表QR-8.6-163 工艺文件汇编目次QR-9.164 检验文件汇编目次QR-9.2序记录名称编号使用部门保存期备注号二专用记录(工艺)CIP清洗记录表QR-3.1-452水纯化监控记录QR-5.1-112化糖监控记录QR-5.1-113煮料操作监控记录QR-5.1-114调味调色料配制记录果冻QR-5.1-105充填封口岗位操作记录QR-5.1-117杀菌岗位生产记录QR-5.1-118二专用记录(检验)过程(工序)检验记录果冻QR-5.1-432产品出厂检验原始记录(合并)果冻QR-6.3-443产品出厂检验报告果冻QR-6.3-451工艺文件汇编目次1 果冻加工作业指导书 (1)2 果冻加工工艺流程图……………………………………3 调味调色料配制作业指导书 ……………………………4 车间加工设备操作规程………………………………5 果冻充填封口机使用规范………………………………6 标签贮运作业指导书 …………………………………化验室(检验)文件汇编目次1 化验室操作规程 (1)2 原辅材料、包装材料采购质量验收操作规程…………3 感官检验实施细则 ……………………………………4 净含量检验实施细则…………………………………5 产品出厂检验操作规程 ………………………………6 化验室仪器操作规程 …………………………………7 过程(工序)检验操作规程 ……………………………8 委托检验计划 …………………………………………9 罐头食品中可溶性固形物含量的测定(GB/T10788)…10 食品微生物学检验总则(GB/T4789.1)………………11 菌落总数的测定方法(GB/T4789.2)……………………12 大肠菌群的测定方法(GB/T4789.2)……………………水处理监控记录表审核/日期:CIP清洗操作记录表审核/日期:原辅材料、包装材料的验收记录编号:QR-6.3-4.2.2 №:材料名称牌号规格进货日期供方名称总数量抽样数量检验内容项目检验结果与评定项目检验结果与评定包装状况净含量标签感官检验形态色泽气味与滋味杂质供方质量资质证明验证:检验员:日期:不合格的处理措施:质检科:质量负责人:日期:[键入文字]产品委托检验计划与执行记录[键入文字] 编号:QR-6.3-43 委托检验机构:****食品质量监督检验中心№:1序号产品名称委托检验项目计划时间执行时间检验结果执行人备注1 果冻一、理化:总砷苯甲酸铅山梨酸铜甜蜜素蛋白质糖精钠二氧化硫残留量安赛蜜着色剂(根据色泽选择测定)二、微生物:霉菌、酵母、致病菌(沙门氏菌、志贺氏菌、金黄色葡萄球菌) 2006-06-15 2006-07-05 合格***2 果冻2006-11-30 审核/日期:食品生产加工企业食品添加物质使用备案表生产者名称(盖章): 注册地址:实际生产地址: 联系电话: 填报日期:食品名称食品类别食品生产许可证号食品执行标准号添加物质名称添加剂类别用途是否进口添加剂生产企业添加剂生产许可证号实际最大使用量添加剂来源添加剂来源详细信息备案机构(盖章):备案日期:调味料配制记录表编号:QR-5.1-105 №:日期批号花生仁食盐白砂糖辣椒粉香兰素工序检验责任人(签名)形态色泽口感编号:QR-6.3-443№:产品名称批号20**060801 抽样基数78箱抽样量13箱规格5kg/箱检验日期20**.06.10 检验依据GB 19883-2005,GB 19299-2003,GB/T 10788-1989,GB/T 4789.2-2003,GB/T 4789.3-2003 检验结果备注感官样品状态形态色泽气味与滋味杂质合格正常,内外包装封装良好,标签标注符合要求符合要求符合要求符合要求无可溶固形物/% 样品温度:℃测定结果(1)(2)(3)净含量/g 序号 1 2 3 4 5 6 7 8 9 10 11 12 13 平均净含量:5.02 k g超出最大允许负偏差件数:无净重 5.01 5.02 4.95 4.98 5.03 5.00 5.03 5.04 5.06 4.97 4.99 5.03 5.18标重60 60 60 60 60 60 60 60 60 60 60 60 60偏差0.01 0.02 -0.05 -0.02 0.03 0.00 0.03 0.04 0.06 -0.03 -0.01 0.03 0.18菌落总数/cfu/g不同稀释度菌落总数-0.1g×2 平均数0.01 g×2 平均数0.001 g×2 平均数空白大肠菌群/MPN/100g不同稀释度发酵管数复发酵阳性管数<30 1g×3 0.1g×3 0.01g×3 1g×3 0.1g×3 0.01g×30 0 0编号:QR-6.3-443№:产品名称批号20**060801 抽样基数78箱抽样量13箱规格5kg/箱检验日期20**.06.10 检验依据GB 19883-2005,GB 19299-2003,GB/T 10788-1989,GB/T 4789.2-2003,GB/T 4789.3-2003 检验结果备注感官样品状态形态色泽气味与滋味杂质合格正常,内外包装封装良好,标签标注符合要求符合要求符合要求符合要求无可溶固形物/% 样品温度:℃测定结果(1)(2)(3)净含量/g 毛重 5.41 5.42 5.35 5.38 5.43 5.39 5.42 5.43 5.45 5.36 5.41 5.45 5.60 平均净含量:5.02 k g超出最大允许负偏差件数:无皮重0.40 0.40 0.40 0.40 0.40 0.39 0.39 0.39 0.39 0.39 0.42 0.42 0.42净重 5.01 5.02 4.95 4.98 5.03 5.00 5.03 5.04 5.06 4.97 4.99 5.03 5.18偏差0.01 0.02 -0.05 -0.02 0.03 0.00 0.03 0.04 0.06 -0.03 -0.01 0.03 0.18菌落总数/cfu/g不同稀释度菌落总数-0.1g×2 平均数0.01 g×2 平均数0.001 g×2 平均数空白大肠菌群/MPN/100g不同稀释度发酵管数复发酵阳性管数<30 1g×3 0.1g×3 0.01g×3 1g×3 0.1g×3 0.01g×30 0 0产品出厂检验报告编号:QR-6.3-451№:产品名称规格60g/个抽样日期20**.10.11 批号20**101101 总数量98瓶抽样数量 2 kg 抽样人*××项目标准要求检验结果评定包装状况要求内、外包装及封装完好,有产品合格证完好合格标签符合GB 7718要求:①品名、②配料表、③净含量及字符高度、④厂名、⑤厂址、⑥生产日期和⑦保质期清晰、⑧产品标准号、⑨符合要求合格规格杯形的杯口内径或杯口内侧最大长度(cm):≥3.5 3.5合格感官检验形态和质地凝胶果冻呈凝胶状,脱离包装容器后,能基本保持原有的形态,组织柔软适中符合要求合格色泽具有该品种应有色泽,着色基本均匀符合要求合格气味与滋味具本品固有的口感风味,味纯正,酸甜适中,无异味。
企业质量管理纪录表格大全样本

质量记录控制清单编号:QR/WKN—424—01编制:批准:质量记录控制清单编号:QR/WKN—424—01编制:批准:质量记录控制清单编号:QR/WKN—424—01编制: 批准:质 量记 录 控 制 清 单编号:QR/WKN —424—01编制:批准:受控文件清单编号:QR/WKN ——423—01编制:审核:批准:日期:外来文献控制清单编号:QR /WKN——423—02 序号:文献发放/收回记录编号:QR/WKN—423—03 序号:001文件更改申请编号:QR/WKN——423—04 序号:文件销毁申请编号:QR/WKN——423—05 序号:管理评审计划编号:QR/WKN——560—01 序号:管理评审通知编号:QR/WKN——560—02 序号:管 理 评审 报 告记录编号:QR/WKN ——560—03 序号:管理评审评价表编号:QR/WKN 560—05评审员签名:评审日期:管理评审评价资料(之)编号:QR/WKN——560—06 资料顺序号:编制:审核:批准:年度培训筹划编号:QR/WKN——620—01培训记录表编号:QR/WKN—620—02 序号:员工培训需求申请单编号:QR/WKN—620—03设施验收单编号:QR/WKN——630—02 序号:设施寻常保养项目表编号:QR/WKN 630—03设施名称:设施编号:使用部门:保养人:月设施检修筹划编号:QR/WKN——630—04执行部门:序号:设施检修单编号:QR/WKN—630—05设施使用部门:序号:设施报废单编号:QR/WKN——630—06使用部门:序号:产品规定评审表编号:QR/WKN—720—01□初次评审□修订(原评审表号:)序号:定单确认表编号:QR/WKN—720—02 序号:顾客反馈解决登记表编号:QR/WKN—720—04 序号:时间:从年月—年月设计开发建议书编号:QR/WKN—730—01 序号:设计和开发筹划书编号:QR/WKN—730—02 序号:设计和开发任务书编号:QR/WKN—730—03 序号主管副总经理签名:年月日设计和开发方案编号:QR/WKN—730—04 序号设计开发验证记录编号:QR/WKN—730—05 序号:设计评审登记表编号:QR/WKN—730—06 序号:设计开发输出清单编号:QR/WKN—730—07 序号:设计实验报告编号:QR/WKN—730—09 序号:客户试用报告编号:QR/WKN—730—10 序号:新产品鉴定报告编号:QR/WKN—730—11 序号:设计和开发信息联系单编号:QR/WKN——730-12 序号:供方评估登记表编号:QR/WKN—740—01 序号:合格供方名单编号:QR/WKN—740—02 序号:供方业绩评价表编号:QR/WKN—740—03 序号:采购申请单编号:QR/WKN—740—04 序号:采购员:日期:主管领导批准:日期:生产计划单编号:QR/WKN—751—01 序号:编制:日期:审核:日期:批准:日期:测量监视设备履历卡编号:QR/WKN—760—02 序号:填表人:审核:批准:计量设备校准计划表编号:QR/WKN—760—03 序号:编制:审核:批准:时间:校准记录表编号:QR/WKN—760—04 序号:顾客满意度调查表编号:QR/WKN—821—02 序号:年度内审计划编号:QR/WKN—822—01 序号:审核实施计划编号:QR/WKN——822—02 序号:审核组组长:成员:年月日第页共页1、审核目:2、审核根据:GB/T 19001- idt ISO 9001:公司质量手册第一版及质量管理体系其她文献3、审核覆盖产品:4、审核时间:年月日到月日初次会议时间:年月日时分末次会议时间:年月日时分5、现场审核期间请被审核方关于人员参加下列活动:首、末次会议:最高管理者和代表及与审核关于管理人员参加。
食品企业QS现场审查应准备的文件和质量记录

食品企业QS现场审查应准备的文件和质量记录一、21个质量安全管理制度1、设立质量管理机构文件;2、质量安全目标;3、岗位责任制度;4、不合格品管理制度;5、从业人员管理制度;6、技术文件管理制度;7、原辅材料及包装材料采购验证管理制度;8、生产过程质量管理制度;9、清洁卫生管理制度;10、生产设备管理制度;11、产品防护管理制度;12、质量检验管理制度;13、贮存管理制度;14、食品标识管理制度;15、食品销售管理制度;16、食品安全信息及投诉管理制度;17、食品安全事故应急处理制度;18、设立质量检验人员文件;19、检验设备管理制度;20、质量管理考核办法;21、食品添加剂专人管理和独立存放制度。
二、标准1、国家、行业、企业标准,包括最新的产品执行标准,原料、食品添加剂、包装材料标准等,其中企业产品标准要合理、备案。
2、检验试验方法最新的标准或书籍。
三、工艺流程图、作业指导书1、食用植物油工艺流程图,关键控制点有:炒籽、压榨、脱酸(去磷)、配比2、酿造酱油工艺流程图,关键控制点有:制曲、发酵、灭菌3、味精分装工艺流程图,关键控制点有:质检,说明:要有味精的检验规定或方案,现场能提供每批次产成品的检验记录,包括对应的原始记录。
四、现场审查必须提供的基本质量记录(表格)、台帐1、不合格品处置记录;2、生产设备一览表(台帐);3、设备清洗消毒记录;4、本年度设备维修保养计划;5、设备维修记录;6、检测设备一览表(台帐);7、检测设备周期检定计划;8、检测设备检定合格证书(记录);9、合格供方名册(台帐)、有效资格证书;10、供方评定记录;11、采购物资清单;12、采购计划;13、生产关键工序控制记录;14、生产、配料、卫生消毒监控记录;15、食品添加剂使用投放记录;16、进货检验记录;17、生产过程质量检验记录;18、成品出厂质量检验报告;19、产品销售明细记录;20、销售合同台帐;21、顾客反馈意见及处理记录;22、纠正和预防措施处理记录;23、质量管理活动考核记录;24、公司文件、外来文件清单;25、文件发放回收一览表;26、员工培训计划;27、培训记录;28、员工健康证明。
IPQC巡检记录表-线束

备注:IPQC需严格按要求进行巡检并填写记录;每次检查的量≧10PCS;若出现异常将不良现象标出,用“X”标示并写上处理方法,跟进记 录,巡查时若无异常用“√”表示。
备注:IPQC需严格按要求进行巡检并填写记录;每次检查的量≧10PCS;ቤተ መጻሕፍቲ ባይዱ出现异常将不良现象标出,用“X”标示并写上处理方法,跟进记 录,巡查时若无异常用“√”表示。
线束IPQC巡检记录表
表单编号:QS-QAD/AHXS-0001 项目 序号 巡检内容 频次 1H 1H 1H 1H 1H 1H 1H 1H 1H 1H 异常处理方法: 8:009:00 9:0010:00 10:0011:00 11:0011:20 13:3014:30 记录日期: 14:30- 15:3015:30 16:30 16:3017:30 加班 所有加工物料是否与图纸相符,不符 01 项是否有ECN或相关文件,生产数量和 型号是否对应生产订单; 端子来料的型号规格以及重点尺寸是 02 否合格 是否在产品生产时进行了首件制作和 03 测试,测试是否已通过。 开线尺寸、剥皮尺寸是否正确,有无 04 伤到线芯;线芯数量是否正确 线 束 05 06 07 08 09 10 品质异常: 端子铆接作业员是否严格按照图纸工 艺要求、作业指导书施工 拉力检测是否合格,并做好《端子拉 力测试表》 检查铆接后的端子有无损伤、变形;重 点尺寸是否在公差范围以内 检查铆接后的线束是否存在飞线、包 胶等现象 PQC是否及时将不良品记录在QC日报表 上,不良信息是否及时反馈和解决 生产现场原材料、半成品、成品是否 严格分区摆放并标识
线束IPQC巡检记录表
表单编号:QS-QAD/AHXS-0001 项目 序号 巡检内容 频次 1H 1H 1H 1H 1H 1H 1H 1H 1H 1H 异常处理方法: 8:009:00 9:0010:00 10:0011:00 11:0011:20 13:3014:30 记录日期: 14:3015:30 15:3016:30 16:3017:30 加班 所有加工物料是否与图纸相符,不符 01 项是否有ECN或相关文件,生产数量和 型号是否对应生产订单; 端子来料的型号规格以及重点尺寸是 02 否合格 是否在产品生产时进行了首件制作和 03 测试,测试是否已通过。 开线尺寸、剥皮尺寸是否正确,有无 04 伤到线芯;线芯数量是否正确 端子铆接作业员是否严格按照图纸工 线 05 艺要求、作业指导书施工 束 拉力检测是否合格,并做好《端子拉 06 力测试表》 检查铆接后的端子有无损伤、变形;重 07 点尺寸是否在公差范围以内 检查铆接后的线束是否存在飞线、包 08 胶等现象 PQC是否及时将不良品记录在QC日报表 09 上,不良信息是否及时反馈和解决 生产现场原材料、半成品、成品是否 10 严格分区摆放并标识 品质异常:
食品QS酱腌菜加工过程质量控制记录表

QR-5.1-105
生产部 10 年
41 HWR 辣椒酱:灌装记录
QR-5.1-106
生产部 10 年
42 HWR 辣椒酱:蒸汽杀菌记录
QR-5.1-107
生产部 10 年
43 HWR 辣椒酱:工序检验记录
QR-5.1-108
质管部 10 年
44 生产计划单
QR-5.1-4.1
生产部 10 年
45
格式 1:工序(生产过程质量)考核 记录(任选一种)
QR-5.1-4.2.4
46
格式 2:工序(生产过程质量)考核 记录(任选一种)
QR-5.1-4.2.4
生产部 10 年 不定期,由质量人巡查性考核 生产部 10 年 不定期,由质量人巡查性考核
47 领料单
QR-5.1-4.2.5.1 生产部 10 年
48 成品发货通知单
QR-5.1-4.2.5.2 生产部 10 年
生产部 10 年
19 设备维护保养计划与执行表
QR-3.1-4.4.2 生产部 10 年
20 设备工具:日常清理消毒登记表
QR-3.1-4.5.1 生产部 10 年
21 设备维修记录
QR-3.1-4.6.0 生产部 10 年
22 设备报废记录
QR-3.1-4.6.1 生产部 10 年
23 员工履历登记表
质管部 10 年
75
76
77
78
End
第3页共4页
杭州经济技术开发区文荣酱菜加工场
编号:HWR/QR-3.3-5.4
审核或批准/日期:
受控文件一览表:质量记录
第4页共4页
编号:QR-5.1-102
腌制 池号
食品进货查验记录表

QS
票据
合格证
食品进货查验记录表
进货
时间
名称
规格
数量/㎏
生产批号
QS
保质期
供货商﹡
采购地点﹡
联系方式
定点
索取证照、采购票据
验收人
手机号码
是
否
生产商许可证
供应商许可证
QS
票据
合格证
食品进货查验记录表
进货
时间
名称
规格
数量/㎏
生产批号
QS
保质期
供货商﹡
采购地点﹡
联系方式
定点
索取证照、采购票据
验收人
手机号码
是
否
生产商许可证
供应商许可证
QS
票据
合格证
食品进货查验记录表
进货
时间
名称
规格
数量/㎏
生产批号
QS
保质期
供货商﹡
采购地点﹡
联系方式定点索取证照源自采购票据验收人手机号码
是
否
生产商许可证
QS审核步骤

序号内容审查项目判定标准制度规定了该人负责质量安全工作的职能,符合;制度对质量安全工作负责人规定不清楚,基本符合;制度未规定质量安全工作负责人,不符合。
申请人有明确的机构或专职人员负责质量管理工作,符合;有机构和兼职人员负责质量管理工作,基本符合;无机构和人员负责企业的质量管理工作,不符合。
有明确的质量安全目标,符合;质量安全目标不明确,基本符合;无质量安全目标,不符合。
制定了管理制度,并规定各有关部门质量职责、权限,且内容合理,符合;规定的内容不全面,基本符合;没制定质量管理制度或制定了部门质量管理制度但内容不合理,不符合。
制定了不符合情况管理办法,符合;制定了不符合情况管理办法,但内容不合理,基本符合;未制定不符合情况管理办法,不符合。
审查日期: 年 月 日使用说明4.“审查记录”一栏应当填写审查发现的基本符合和不符合情况。
1.本审查记录表适用于对设立食品生产企业的申请人规定条件中申请材料的审核和生产场所核查。
2.本审查记录表分为:申请材料审核和生产场所核查两个部分共37个项目。
对每一个审查项目均规定了“符合”、“基本符合”、“不符合”的判定标准。
3.审查组应按照对每一个审查项目的审查情况和判定标准,填写审查结论。
对设立食品生产企业的申请人规定条件审查记录表申请人名称:申证食品品种类别:申请生产食品申证单元:生产场所地址:1.2质量目标申请人应制定明确的质量安全目标。
1.1组织领导1.申请人治理结构中至少有一人全面负责质量安全工作。
2.申请人应设置相应的质量管理机构或人员,负责质量管理体系的建立、实施和保持工作。
1.3管理职责1.申请人制定各有关部门质量安全职责、权限等情况的管理制度。
2.申请人应当制定对不符合情况的管理办法,对企业出现的各种不符合情况及时进行纠正或采取纠正措施。
一、 申请材料审核明确,符合;符合资格规定,责任、权力或者义务规定不明确,基本符合;资格不符合规定,或未明确责任、权力和义务,不符合。
IPQC巡检记录表-线束

备注:IPQC需严格按要求进行巡检并填写记录;每次检查的量≧10PCS;若出现异常将不良现象标出,用“X”标示并写上处理方法,跟进记 录,巡查时若无异常用“√”表示。
重点尺寸是否在公差范围以内pqc是否及时将不良品记录在qc日报表上不良信息是否及时反馈和解决生产现场原材料半成品成品是否严格分区摆放并标识异常处理方法
线束IPQC巡检记录表
表单编号:QS-QAD/AHXS-0001 项目 序号 巡检内容 频次 1H 1H 1H 1H 1H 1H 1H 1H 1H 1H 异常处理方法: 8:009:00 9:0010:00 10:0011:00 11:0011:20 13:3014:30 记录日期: 14:3015:30 15:3016:30 16:3017:30 加班 所有加工物料是否与图纸相符,不符 01 项是否有ECN或相关文件,生产数量和 型号是否对应生产订单; 端子来料的型号规格以及重点尺寸是 02 否合格 是否在产品生产时进行了首件制作和 03 测试,测试是否已通过。 开线尺寸、剥皮尺寸是否正确,有无 04 伤到线芯;线芯数量是否正确 端子铆接作业员是否严格按照图纸工 线 05 艺要求、作业指导书施工 束 拉力检测是否合格,并做好《端子拉 06 力测试表》 检查铆接后的端子有无损伤、变形;重 07 点尺寸是否在公差范围以内 检查铆接后的线束是否存在飞线、包 08 胶等现象 PQC是否及时将不良品记录在QC日产现场原材料、半成品、成品是否 10 严格分区摆放并标识 品质异常:
备注:IPQC需严格按要求进行巡检并填写记录;每次检查的量≧10PCS;若出现异常将不良现象标出,用“X”标示并写上处理方法,跟进记 录,巡查时若无异常用“√”表示。
线束IPQC巡检记录表
表单编号:QS-QAD/AHXS-0001 项目 序号 巡检内容 频次 1H 1H 1H 1H 1H 1H 1H 1H 1H 1H 异常处理方法: 8:009:00 9:0010:00 10:0011:00 11:0011:20 13:3014:30 记录日期: 14:30- 15:3015:30 16:30 16:3017:30 加班 所有加工物料是否与图纸相符,不符 01 项是否有ECN或相关文件,生产数量和 型号是否对应生产订单; 端子来料的型号规格以及重点尺寸是 02 否合格 是否在产品生产时进行了首件制作和 03 测试,测试是否已通过。 开线尺寸、剥皮尺寸是否正确,有无 04 伤到线芯;线芯数量是否正确 线 束 05 06 07 08 09 10 品质异常: 端子铆接作业员是否严格按照图纸工 艺要求、作业指导书施工 拉力检测是否合格,并做好《端子拉 力测试表》 检查铆接后的端子有无损伤、变形;重 点尺寸是否在公差范围以内 检查铆接后的线束是否存在飞线、包 胶等现象 PQC是否及时将不良品记录在QC日报表 上,不良信息是否及时反馈和解决 生产现场原材料、半成品、成品是否 严格分区摆放并标识
BRC记录QS记录-CR011A 月度离子风机日常点检确认表
确认 作成
编号:CR011A 点检项目
1、作业规范静电量是否在100V以下 2、过滤片是否有污质 3、吹出口是否有污质 4、放置位置及风量标识是否在指定位置
担当者 确认者
点检项目 1、作业规范静电量是否在100V以下 2、过滤片是否有污质 3、吹出口是否有污质 4、放置位置及风量标识是否在指定位置
注意事项:1、点检过程中,发现有异常时,需及时向上司报告; 2、发生异常的项目,在该对应栏上打“×”,符合的项目,在该对应栏上打“√”。
担当者 确认者
点检项目 1、作业规范静电量是否在100V以下 2、过滤片是否有污质 3、吹出口是否有污质 4、放置位置及风量标识是否在指定位置
担当者 确认者
பைடு நூலகம்
月度离子风机日常点检确认表
年月 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31
年月 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31
年月 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31
生产用水水质检查记录
生产用水水质检查记录生产车间消毒液有效氯检查记录编号:JS/QS-S008-1-A/O-2005试剂配置记录表微生物培养箱检查记录无菌室环境检查记录表表面样品检测记录编号:: 原料进厂检验记录表: 原(辅)料检验报告单编号: JS/QS-Q015-1-002-A/O-2005 年月审核:检验报告:仪器损坏登记表感官、理化检测原始记录检验通知单编号:检验通知单编号: 知会人:通知人: 年月日成品出厂检验单产品标示单编号:合格证月制表: 审核:编号: JS/QS-Q019-6-001-A/O-2005日产品名称:不合格品单编号:报废单编号:让步接受单编号:不合格品处理记录表审核: 硬化室温湿度记录表彭化加工记录表编班次:JS/QS-Q018-1-003-A/0-2005JS/QS — Q018-1-004-A/0--2005切片加工记录表编班次:计量加工记录表JS/QS— Q018-1-005-A/0--2005班:成品检验报告单编号:JS/QS-Q019-4-002-A/O-2005样品名称:检验日期:审核:检验人:报告日期:原材料检验报告单样品名称:样品来源:采样日期:数量:生产批号:报告日期:审核:二次包装记录表内包装材料以及包装工具的消毒记录编号:JS/QS-S005-2--A/O-2005加工过程中人员出入车间记录编号:JS/QS-S004-2--A/O-2005 日期:记录:审核:储藏库卫生消毒记录编号:JS/QS-S002-2-004-A/0-2005车间空间消毒记录编号:JS/QS-S0022003-A/0-2005消毒液配置记录消毒液配制使用记录编号:JS/QS-S008-2-002-A/O-2005备注:车间地面消毒执行记录编号:JS/QS-S002-2-002-A/0-2005 班次日期:机器清洗消毒记录JS/QS-S002-2-001-A/0-2005编班次:每日卫生控制记录贮藏库卫生、消毒检查记录(注:合格(-0 ,不合格(X))更衣室、厕所设施的卫生与维护检查记录编号:JS/QS-S004-1-A/0-2005(注:合格(^),不合格,检查内容:地面,靴架的清洁;排水,地面的清洁,垃圾的清除;3 ,各系统的正常运行;4,肥皂,纸巾,卫生纸的供应等) 审核:投料加工阶段记录表编班次:JS/QS-Q018-1-002-A/0-2005审核: 有毒有害化学物品购买记录表有毒有害化学物品领用记录表编号:JS/QS-Q030-3-A/O-2005药品试剂台帐编号:JS/QS— Q019-5—002—A/0--2005品名:级别:规格:纠正和预防措施建议书编号:发送单位收到单位发送日期事实描述:类型:口不合格口潜在问题原因分析:改进意见:单位负责人:年月日是否需要实施纠正措施/预防措施:单位负责人:年月日内部质量体系审核检查表编号:审核组长: 审核员:内部质量体系审核不合格报告编号:审核组长要求纠正措施完成时间责任单位不合格事实陈述:不合格类型:严重不合格口轻微不合格口不符合标准/程序:不符合原因分析:纠正措施:单位负责人:年月日纠正措施的验证:审核员:年月日内部质量体系审核纠正措施跟踪表被审核单位:编号:。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
食品厂原辅材料验货记录(包括原料、食品添加剂、包装材料等)序号原料名称规格型号进货数量进货时间执行标准生产厂名及国别验货方式验货日期验货结论处置结果负责人签字、日期遂宁市船山区常兴食品厂产品销售台帐序号产品名称生产批号生产日期执行标准检验结论产量(单位)销量(单位)销售日期销往地区及企业名称单证编号备注遂宁市船山区常兴食品厂原辅材料供方评价登记表(包括原材料、食品添加剂、营养增加剂包装材料等)序号原辅料名称供方名称供方地址营业执照注册号卫生许可证登记号生产许可证登记号质检报告编号质保书合格证标准代号质量问题记载生产日期供货时间食品厂原辅材料投料、使用记录(包括食品添加剂、营养强化剂使用情况)序号产品名称原辅料名称使用量产品产量生产批号生产日期检验结论检验报告编号备注食品厂关键工艺、关键工序质量控制记录工序名称质量控制点质量要求控制措施生产班次责任人质量控制运行情况异常情况记录处置措施处置结果备注食品厂计量器具检定、使用台账序号计量器具名称规格型号精度等级生产厂家生产日期购置日期台件数量使用场所责任人检定周期检定有效截止日期完好状态食品厂生产设备管理台账序号设备名称规格型号生产厂家生产日期购置日期数量使用场所责任人检修周期检修时间完好状态食品厂消毒剂、清洗剂使用记录序号试剂名称生产厂家有效期限配制浓度使用场所使用班次使用量使用时间责任人备注食品厂质量管理考核记录序号考核内容考核依据考核类型考核时间不合格项考核组负责人整改要求整改期限整改措施整改效果验收时间验收责任人食品厂包装材料使用记录序号产品名称包装材料名称生产厂家生产日期、生产批号检验证书编号检验结论使用量备注食品厂主要负责人员、工程技术人员一览表序号姓名性别年龄身份证号职务职称文化程度专业资格证及编号备注食品厂使用食品添加剂备案表填报单位(盖章):填报时间:年月日食品添加剂名称食品添加剂生产企业名称食品添加剂生产企业地址、电话食品添加剂生产许可证号应用于何种食品使用量g/kg或(g/L)月使用量(kg)注:企业首次备案应把食品添加剂购买发票、合格证、使用说明书附后,当企业更换食品添加剂时应重新备案。
填报人:联系电话:食品厂原料记录表计量单位:( ) 田质监食表01-2005日期原料名称进货数量供应单位质检结果堆放点原库存量现库存量验收人员签名注:采购原料时应向供应商索取产品合格证或质检报告,食品添加剂还需要收集使用说明书、采购发票。
食品厂生产记录表日期开停机时间(hh:mm)生产小时数加工成品量( )质检结果原料消耗量( ) 原库存量( )现库存量( )加工人员签名注:原料消耗量栏目必须把食品添加剂的名称与用量填上。
食品厂产品销售记录表计量单位:( ) 田质监食表03-2005日期产品名称销售数量( )售价经销(代销)单位质检结果原库存量现库存量销售人员签名食品厂原料信息记录表填报单位(盖章):填报日期:品名供应商注册地址卫生许可证号原料卫生标准批号规格生产日期有效期至生产厂家出厂合格证检验报告书有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□有□无□填报人:联系方法(手机/固话/传真):注:1、企业应如实全数填写报表;2、上报时应附上相关供应商、生产厂家的资质证书复印件、产品检验报告书复印件(均需加盖公章);3、发生增减品种时应及时上报,以便更新数据库有关内容。
不合格原料通知单产品名称规格数量供货/生产单位责任人质量等级执行标准序号检验指标标准要求实测值检验结论标识隔离备注检验员:复核:检验时间:不合格产品评审处置表购进或生产品名称产品规格产日期检验人检验单号责任部门不合格品描述:原因分析:部门负责人:处置方案:返工○退换○作废○处置结论:厂长:年月日处置实际情况:验证情况:监督员:年月日质量工作会议记录会议名称主持人会议时间会议地点参加人员主要内容技术文件发放及回收记录文件发放文件回收发放日期发文单位(人)文件名称签收人回收日期归还单位(人)文件名称归还人松弛时间醒发温度℃醒发时间生产日期记录时间班次搅拌后面团操作人记录人备注温度℃生产日期记录时间班次烘烤温度℃烘烤时间操作人记录人备注不合格项纠正记录不合格项目:不合格原因:纠正措施:实施人:年月日纠正后的效果:检查人:年月日生产人员伤病调离通知单姓名性别调离时间年月日伤病情况:批准人:年月日返回岗位时间:年月日伤病痊愈情况:批准人:年月日生产人员伤病调离通知单姓名性别调离时间年月日伤病情况:批准人:年月日返回岗位时间:年月日伤病痊愈情况:批准人:年月日培训记录培训主题培训日期授课人课时参加人数培训记录培训目的培训对象培训内容实施情况记录人记录日期备注食品厂设备维修(保养)记录设备名称设备编号型号规格使用部门故障发生的时间和现象(计划内不需填写此栏):申请人:年月日检修情况记录:检修结果备注检修人:日期:(部门负责人)确认:日期:消毒剂入库、领用记录入库数量出库数量领用人保管人库存数量备注药品名称出、入库日期设备、设施及地面卫生清洗消毒记录消毒剂名称:生产日期消毒对象消毒时间消毒数量消毒液浓度(ml/L)配制比例(消毒剂:水)消毒方法操作人员备注消毒方法:浸泡、喷洒、擦洗消毒液配制记录消毒剂名称:生产日期配制消毒对象配制时间配制人备注消毒剂(ml)水(L)比例(消毒剂:水)消毒液浓度(ml/L)工作服消毒记录记录人:审核人:年月日日期数量(件)紫外灯消毒起止时间备注开始时间结束时间抽样单产品名称样品编号生产时间生产班组抽样数量抽样基数抽样日期抽样人抽样单产品名称样品编号生产时间生产班组抽样数量抽样基数抽样日期抽样人抽样单产品名称样品编号生产时间生产班组抽样数量抽样基数抽样日期抽样人生产过程产品感官检验记录生产日期班次品种规格形状色泽滋味与口感组织杂质检验员备注成品卫生检验原始记录样品名称细菌数结果(个/克)大肠菌群结果(MPN/100克)倍数1:10倍数1:100倍数1:1000倍数1:10倍数1:100倍数1:1000判定与处理:检验员:检验日期:年月日净含量及感官检验原始记录编号生产日期及班次检验日期产品名称规格生产数量净含量感观检验员总重(克)皮重(克)净含量(克)标明净含量(克)偏差形态色泽滋味和气味组织杂质+ -配料记录生产日期产品名称配方共配料数配料员备注采购验证记录产品名称型号规格供应/生产单位进货日期进货数量验证数量验收方式验证项目标准要求验证结果合格/不合格验证结论:检验员:日期:年月日不合格处置:退货()让步接收()选用()报废()批准人:日期:年月日采购验证记录产品名称型号规格供应/生产单位进货日期进货数量验证数量验收方式验证项目标准要求验证结果合格/不合格验证结论:检验员:日期:年月日不合格处置:退货()让步接收()选用()报废()批准人:日期:年月日出厂检验报告单产品名称规格检验类别出厂检验抽样数量抽样方式随机抽样基数生产日期抽样地点检验依据检验项目单位技术要求检验结果判定一.感官1.形态2.色泽3.滋味和气味4.组织5.杂质二.净含量g﹪三.干燥失重(水份)四.卫生指标1.细菌总数(个/克)2.大肠菌群(MPN/克)检验结论检验员:审核人:报告日期:年月日干燥失重(水分)检验原始记录生产日期:检测项目检验方法水分含量(%)样品名称及编号器号容器重m3(g)[容器+样品重]m1(g)样品质量m(g)烘后[容器+样品重]m2(g)失水质量(g)测定结果平均值备注:计算公式:m1-m2X1=————×100m1-m3式中:X1-样品中水份的含量,﹪m3-容器的质量,g m1-容器+样品重,g m2-烘后[容器+样品重],g检验员审核人检验日期干燥失重(水分)检验原始记录生产日期:检测项目检验方法水分含量(%)样品名称及编号器号容器重m3(g)[容器+样品重]m1(g)样品质量m(g)烘后[容器+样品重]m2(g)失水质量(g)测定结果平均值备注:计算公式:m1-m2X1=————×100m1-m3式中:X1-样品中水分的含量,﹪m3-容器的质量,g m1-容器+样品重,g m2-烘后[容器+样品重],g检验员审核人检验日期物资采购计划单物资名称数量规格、型号申请部门批准人批准日期执行情况合同号物资采购计划单物资名称数量规格、型号申请部门批准人批准日期执行情况合同号成品入库记录入库时间产品名称产品规格入库数量库存量库房总量交货人收货人备注成品出库记录出库时间产品名称产品规格出库数量库存量库房总量发货人领货人发往地备注细菌总数检测原始记录室温:℃湿度:% 第页共页检测依据接种时间使用主要仪器报告时间样号样品名称36+1 ℃培养24~48h稀释度报告数cfu/ml(g)空白接种量ml皿号计数方式菌落总数(个/皿)皿号计数方式菌落总数(个/皿)备注:1.√表示全皿计数,×表示多不可计数。
2.选取菌落数在30-300之间的平皿作为菌落总数测定标准。
参照GB/T4789.2-7.3.2稀释度的选择报告菌落数。
3.菌落数在100以内时,按其实有数报告,大于100时,采用两位有效数字用10的指数来表示。
检验员:审核人:审核时间:总大肠菌群检测证实试验记录环境温度:℃环境湿度 % 第页共页检测依据接种时间使用主要仪器报告时间样号样品名称培养温度、时间培养基名称结果判定报告数(MPN)/100ml(g) ℃ h乳糖发酵培养基分析号 1 2 3 4 5 6 7 8 9 复发酵产酸、气EMB分离培养革兰氏染色复发酵产酸、气EMB分离培养革兰氏染色备注:乳糖发酵阳性管转种培养实验:1.复发酵:+/+表示产酸、产气为阳性;-/-表示不产酸、不产气为阴性;+/-表示产酸、不产气。
接种量在1ml以上者,用双料发酵管;1ml以下者,用单料发酵管。
2.在鉴别性琼脂平板EMB上36±1℃培养18~24h,观察菌落形态,具有大肠菌群其典型特征“+”表示,不具有大肠菌群其典型特征“-”表示3.做革兰氏染色,“⊕”表示阳性,“⊙”表示阴性检验员:审核人:审核时间:。
