晶体中结构基元的确定
晶体结构

晶体结构和布拉菲格子的区别
晶体结构和布拉菲格子的区别
基矢 原胞 晶胞(单胞)
初基元胞 点阵的基本 平移矢量。
有多种取法。
12面体
14面体
布拉伐格子 晶向 晶面
标志?
互质的整数(h1h2h3)-----晶面指数
若以单胞的棱a,b,c为坐标系对应的指数(h1h2h3)----miller index
33 23
13
32 22 12
31
33 11
21 31 13;32 12 32 0
11
23 21 21 0
同样若沿Z轴作对称操作-转动900
0 1 0 A 1 0 0
0 0 1
A1A
22
0
0
11
0
13
11
0
0
22
13
0
0 31 33
31 0 33
7晶系14种Bravais Lattice介绍
可以证明,由于对称性的要求,共有14种Bravais Lattice, 分为7个晶系(点阵只有7种点群)。 对称操作群{D/t} D--点(宏观)对称操作; t--平移对称操作. 点阵点群-------{D/t=0}7个7个晶系 点阵空间群-------{D/t}14个14 lattices
绪论
������ 固体物理是研究固体的结构和其组成粒子之间的相互作用 及运动规律,以阐明其性能和用途的学科。
固体的分类 晶体(晶态):原子按一定的周期规则排列的固体(长程有序)。 非晶体(非晶态):原子排列没有明确的周期性(短程有序)。
[理学]1-1 第一章 晶体的结构布拉伐格子、原胞_OK
![[理学]1-1 第一章 晶体的结构布拉伐格子、原胞_OK](https://img.taocdn.com/s3/m/494796bb852458fb760b568d.png)
Be2O3晶体内部结构
Be2O3玻璃内部结构
4
多晶体:由两个以上的同种或异种单晶组成的结晶物质。
其中各单晶通过晶界结合在一起的。多晶由成千上万的晶粒构 成,晶粒的尺寸大多在厘米级至微米级范围内变化,多晶没有 单晶所特有的各向异性特征。
液晶:一些晶体当加热至某一温度时转变为介于固体与液体
之间的物质,在一维或二维方向上具有长程有序。当继续加热 至温度时,转变为液体。
5
准晶体:1984年Shechtman等人用快速冷却方法制备的
AlMn准晶体,用XRD测得一种介于晶体和非晶体结构之间的 物质结构。
6
最简单、最常见的晶格结构
原子的正方堆积
17
原胞
• 最小的重复单元,包含一个格点 • 用格矢平移原胞,将填满整个空间,没有遗漏,
也没有重叠 • 选取方法可以不只是一种,但体积相同 • 三维 • 二维 • 一维
18
最小重复单元
19
原胞的多重选择
思考:有没有一种原胞,它的选取是唯一的?
20
Wigner-Seitz原胞
• 以某个格点为中心,作其与邻近格点的中垂面, 这些中垂面所包含最小体积的区域
结点的总和基元点阵晶体结构结构具体用没有大小的几何点来代表基元这种点在空间排列成阵列点阵基元平移没有转动地放在点阵上晶体结构基元将填满所有空间没有重叠也没有遗漏思考
第一章、晶体的结构
1
晶体特征
• 物理:固定熔点,长程有序,解理性 • 几何:凸多面体,晶棱平行,晶面面积、夹角
守恒
2
3
晶体化学基本原理2012

结构投影图:(俯视图)用标高来表示,0-底面;25- 1/4;50-1/2;75 -3/4。(0-100;25- 125;50-150是等效的) 配位数: CN+=CN-=4;极性共价键,配位型共价 晶体。
配位多面体: 〔ZnS4〕四面体,在空间以共顶方式相连接 属于闪锌矿型结构晶体有:β-SiC;GaAs;AlP;InSb等。
阳离子的配位数与阴阳离子半径比 的关系:正离子总是在自己 半径所允许的条件下,具有尽可能高的配位数,使得正负离子 相接触而负离子之间稍有间隔,使体系处于最稳定状态。
(二)第二规则(静电价规则):
在一个稳定的晶体结构中,从所有相邻接的阳离子到达一 个阴离子的静电键的总强度,等于(或近似等于)阴离子的电 荷数。
位移性转变:质点间位移、键长、键角的调整,转变速 度快(高低温型转变)。 重建型转变:旧键的破坏,新键的形成,转变速度慢。
例:SiO2 β-石英 α-石英
573℃
α-石英 α-磷石英
位移性转变,需能量低 重建型转变,转变慢
870℃
2. 根据多晶转变的方向,可分为:
可逆转变: 当温度高于或低于转变点时,两种变体可以反 (双向转变) 复瞬时转变,位移性转变都属于可逆转变。
(四)第四规则:——第三规则的推论 在一个含有不同阳离子的晶体中,电价高而配位数小的 那些阳离子不趋向于相互共有配位多面体的要素。
共顶、共棱和共面
例: 岛状镁橄榄石(Mg2SiO4) Si4+斥力较大,使得[SiO4]间互不相连,以孤立状态存在; 而Si4+与Mg2+间斥力较小,[SiO4]与[MgO6]之间共顶和共棱 相连,形成较稳定的结构。
共价键 4
NaCl型
NaCl型
ZnS型
(四)电负性 各种元素的原子在形成价键时吸引电子的能力。
晶体结构的基本结构单元

晶体结构的基本结构单元
晶体结构的基本结构单元主要有三种:原子、分子和离子。
这些基本结构单元在空间中按照一定的规律排列,形成了具有周期性的三维结构。
1.原子:原子是构成物质的基本粒子,它们按照一定的顺序排列在晶体中,形
成一种重复的模式。
原子的排列方式直接决定了晶体的物理和化学性质。
例如,金属原子按照一种被称为“金属键”的强力键合排列,这使得金属具有良好的导电性和导热性。
2.分子:分子是由两个或更多原子通过共价键结合在一起的。
在晶体中,分子
可以是链状、网状或者层状排列。
分子的排列方式会影响分子的化学性质和物理性质。
例如,在石墨中,碳原子以层状排列,每层之间的相互作用很弱,因此石墨可以轻易地在层之间滑动。
3.离子:离子是带有电荷的原子或分子。
在晶体中,离子通常通过离子键或者
共价键结合在一起。
离子的排列方式会影响晶体的离子导电性和耐压性。
例如,在食盐(NaCl)中,钠离子和氯离子通过离子键结合,这种键合方式使得食盐具有良好的导电性和耐压性。
晶体的结构基元

晶体的结构基元晶体是由原子、离子或分子排列有序形成的固体物质,其结构由基元构成。
基元是指晶体中最小的、可重复排列的结构单元,它决定了晶体的性质和结构。
本文将介绍晶体的结构基元,包括晶格、点阵、Bravais格子、基本晶胞和原胞等。
一、晶格晶格是指在三维空间中无限延伸的点阵,它描述了晶体中原子或离子的排列方式。
每个点代表一个原子或离子,在不同类型的晶体中,这些点按照不同的方式排列。
晶格可以用一个简单单元重复填充整个空间,这个简单单元称为基本晶胞。
二、点阵点阵是指在平面上无限延伸的点阵,它描述了二维物质中原子或离子的排列方式。
每个点代表一个原子或离子,在不同类型的二维物质中,这些点按照不同的方式排列。
与三维空间类似,二维物质也可以用一个简单单元重复填充整个平面。
三、Bravais格子Bravais格子是指在三维空间中无限延伸的点阵,它描述了晶体中原子或离子的排列方式。
Bravais格子包括14种不同类型,每种类型有不同的对称性。
这些对称性可以通过晶体中原子或离子的排列方式来描述。
四、基本晶胞基本晶胞是指最小的、可重复填充整个晶体空间的三维单元,它由一组基元构成。
在一个基本晶胞中,包含了整个晶体结构的所有信息。
不同类型的晶体具有不同形状和大小的基本晶胞。
五、原胞原胞是指在三维空间中无限延伸的点阵中最小的、可重复填充整个空间的三维单元,它由一组基元构成。
原胞可以用来描述Bravais格子和基本晶胞之间的关系。
在一个原胞中,包含了整个Bravais格子结构和所有可能出现的基本晶胞。
六、小结以上介绍了晶体结构中最重要的几个概念:晶格、点阵、Bravais格子、基本晶胞和原胞。
这些概念是理解和描述各种物质结构特征所必需的。
通过深入理解这些概念,可以更好地理解晶体结构和性质,为材料科学和化学研究提供基础。
第一章 晶体结构

19
1.3 对称性和布拉维格子的分类
二 基本对称操作
1 i,Cn,σ (m)
2 n度旋转 ─ 反演轴
绕μ轴旋转
2π后再进行中心反演:
n
1,2,3,,4, i, m 八种独立的对称操作。
宏观上看,晶体是有限的,描述晶体宏观对称性 不包含平移对称操作;但从微观上看,晶体是无 限的,为描述晶体结构的对称性,应加上平移对 称操作。
衍射斑点(峰) ↔ 晶格中的一族晶面 倒格子 ↔ 正格子 点子 ↔ 晶面
斑点分布 ↔ 晶格基矢 → 晶体结构
25
1.4 倒格子/倒易点阵
一 定义
设布拉维格子的基矢为:av1 ,av2 , av3
由
v Rl
=
l1av1
+
l2av2
+
l3av3 决定的格子称为正格子
(direct lattice),
满足
2vπ Gh
4 两点阵位矢的关系
v Rn
•
v Gh
=
2πm
m为整数
利用
aavvii
• •
v bvj bj
= =
2π 0
i= j i≠ j
( ) Rv n •Gvh = (l1av1 + l2av2 + l3av3 )•
v h1b1
+
v h2b2
+
v h3b3
= l1h1 • 2π + l2h2 • 2π + l3h3 • 2π
按坐标系的性质,晶体可划分为七大晶 系,每一晶系有一种或数种特征性的布拉 维原胞,共有14种布拉维原胞:
三斜(简单三斜) 单斜(简单、底心) 正交(简单、底心、体心、面心) 四方(简单、体心) 三角 六角 立方(简单、体心、面心)
晶体结构

§1.1 晶格的周期性
一、布拉菲(Bravais)格子
布喇菲(A. Bravais),法国学者,1850年提出。
定义:
各晶体是由一些基元(或格点)按一定规则, 周期重
复排列而成。任一格点的位矢均可以写成形式
Ra为n3 基 n矢1a1, n。2为Ra其2n 布中n拉3a,3菲、格子、的取n格1整矢n数2,,n或3 称、正、格矢a。1
3、金刚石结构( diamond ):
碳的同素异构体。 经琢磨后的金刚石又称钻石。 无色透明、有光泽、折光力极强,最硬的物质。
金刚石结构是复式晶格结构,基元中有两个碳原子A、B, 布拉菲格子是面心立方。
或可视为两个面心立方子晶格,沿体对角线平移1/4 体对角 线长度套构而成,如图所示.
金刚石晶体的配位数是4, 这4个碳原子构成一个 正四面体,碳-碳键角为109º28´。
基元是化学组成、空间结构、排列取向、周 围环境相同的原子、分子、离子或离子团的集 合。
可以是一个原子(如铜、金、银等),可以是 两个或两个以上原子(如金刚石、氯化钠、磷化 镓等),有些无机物晶体的一个基元可有多达 100个以上的原子,如金属间化合物NaCd2的基 元包含1000 多个原子,而蛋白质晶体的一个基 元包含多达10000 个以上的原子。
具有金刚石结构的晶体有: 金刚石、元素半导体Si、Ge ,灰锡等。
4、闪锌矿(立方ZnS)结构:( cubic zinc sulfide )
与金刚石结构类似,金刚石的基元是化学性质相同的两个 原子A、B ,而闪锌矿结构的基元是两个不相同的原子.
闪锌矿结构也可视为是两个不同原子的面心立方子晶格, 沿体对角线平移1/4 体对角线长度套构而成.
例如,简立方晶格的几个晶列如图所示。
晶体结构基础

左图是晶体
右图是晶体的点阵
左图是晶体
右图是晶体的点阵
在晶体点阵的每个阵点上按 同一种方式安置结构基元,则得
到晶体。
晶体 = 点阵 + 结构基元
结构基元为
一 一 两个粒子
晶体的点阵
粒子的种类相同,且每个粒子均处
于由 3 个粒子构成的正三角形的中心。
但是一类粒子处于一个顶角向上的 三角形的中心 这种粒子相当于右图中的红色粒子
晶系名称
晶格常数特征
独立晶格常数
1 立方晶系 2 四方晶系 3 正交晶系
a=b= c
a a, c a, b, c
= = = 90°
a = b ≠c
= = = 90°
a≠b≠c
= = = 90°
晶系名称
晶格常数特征
独立晶格常数
4 六方晶系
a=b≠c a, c = = 90° =120°
在点阵中可以找到 8 个顶点均为 阵点的平行六面体,如下图的 A
整个空间点阵可以看成是以这个
平行六面体为单位并置而成的
这个平行六面体称为空间点阵的点阵单位
点阵单位并不是唯一的,图中的 A,B 和 C 均属于这样的平行六面体
D 也属于这样的平行六面体
平行六面体上的阵点的位置
可分为 4 种:
c
a 晶格平行六面
体的三个棱长分别
b
三个棱之间的
夹角分别用 ,,
用 a,b,c 表示,
表示。
c
a
b
其中 a 和 b 的夹角为 ,a 和 c 的 夹角为 ,b 和 c 的夹角为 。
c
a
b
晶体结构综合复习讲义

c a
c b a
c b a
六方 Hexagonal a=b≠c, ≠ α=β=90°, β ° γ=120° °
单斜 Monoclinic a≠b≠c ≠ ≠ α=γ=90°, β≠ ° γ ° β≠90°
三斜 Triclinic a≠b≠c ≠ ≠ α=β=γ=90° β γ °
晶胞要素- 晶胞要素-分数坐标
晶胞要素
个原则: (4)划分晶胞要遵循 个原则:一是尽可能反映 )划分晶胞要遵循2个原则 晶体内部结构的对称性;二是尽可能小。 晶体内部结构的对称性;二是尽可能小。 • 对称性 对称性——最高(晶系); 最高(晶系); 最高 • 划分晶胞的不唯一性:正当晶胞和非正当晶胞; 划分晶胞的不唯一性:正当晶胞和非正当晶胞; • 素晶胞和复晶胞。 素晶胞和复晶胞。
金 (gold, Au)
体心立方 e.g., Fe, Na, K, U
简单立方( 简单立方(钋,Po) )
密度与金属固体的结构
(a) 简单立方:d = m/a3 = (M/NA)/(2r)3 = M/(8NAr3) 简单立方: (b) 体心立方: d = m/a3 = (2M/NA)/(4r/31/2)3 = 33/2M/(32NAr3) 体心立方: (c) 面心立方: d = m/a3 = (4M/NA)/(81/2r)3 = 4M/(83/2NAr3) 面心立方: (a):(b):(c) ≅ 1:1.299:1.414 面心结构密度最大, 面心结构密度最大,最稳定 (立方密堆积 立方密堆积) 立方密堆积
配位数: 配位数:8 质点数: 质点数:2
配位数: 配位数:6 质点数: 质点数:1
空间点阵型式要点
• 六方晶系和三方晶系都可按六方晶胞形状表示 空间点阵形式: 空间点阵形式: 六方晶系 简单六方( ) 简单六方(hP) 简单六方( ) 简单六方(hP) 三方晶系 R心六方(hR) 心六方( ) 心六方 (0,0,0; 2/3,1/3,1/3; 1/3, 2/3, 2/3)
固体物理学:晶体结构

l1 、l2 、l3 为一组整数。
➢ 布拉菲点阵的数学定义
R1,0,2 a1 2a3
确定原点和基矢后,晶格中任一格点都可以用矢量: Rn n1a1 n2a2 n3a3
(n1, n2 , n3, 0,1,2,3,)
a3
a2
a (0,0,0) 1
表示。由于格点周期性排列,从任一格点
Na+ Cl-
Na+周期性排列和Cl-周期性排列 正离子和负离子构成
等同点:正离子或负离子
氯化钠晶体结构
2. 晶格平移矢量
基矢:为了描述点阵而引入
在布拉菲点阵中,人为选取的与晶格维数同 样多的一组矢量,使得晶格中任意两个格点 间的位移矢量(即格矢量)可以表达为该矢
第一章 晶体结构
为什么要研究结构
结构决定了相互作用,相互作用又决 定了运动,不同的运动形式具有不同 的性质,也就是结构决定了性质
§1.1 原子的周期性阵列
1、基元(basis)和点阵(lattice)
晶体结构的最显著特点是周期性。理想情况下,晶体可以 看成是由一“基本结构单元”——基元,在空间无限重复排列 构成的,这种性质称为晶体结构的周期性。〔没有边界,所以 所有的基元都是等同的,如果有边界就不同了。理想晶体与实 际晶体的区别〕
2、原胞体积:
v a1 (a2 a3 ) (矢量的混合积)
3、不同原胞中对应点物理性质 V (r)相同,称为平移对称性,用晶格平移矢量表示为:
V (r Rn ) V (r)
4、原胞的选择是多样的,但体积相同。
a2 1
a1
a2
2
a1
a2 3
a1
基元与原胞的区别
概念不同 基元是具体的原子或原子团,是具体的
结构基元的名词解释

结构基元的名词解释一、引言结构基元是指构成物质或事物的最小单位,是实现复杂结构的基础。
无论是自然界中的生物体还是人类社会中的组织体系,都离不开这些基本的构成要素。
在本文中,我们将探讨不同领域中常见的结构基元,并解释其含义和作用。
二、晶格基元在材料科学中,晶格基元是指构成晶体的最小单位。
晶体由原子或分子组成,通过特定的排列形成具有高度有序性的三维结构。
例如,金属结晶体的基元是由相同或不同原子的紧密排列组成的。
晶体结构的特性受基元种类、排列方式以及相互作用力等因素的影响。
三、生物分子基元在生物学中,分子基元是指构成生物体的最基本单位,包括蛋白质、核酸、糖类等生物分子。
这些分子基元相互组合并通过化学键连接,形成各种生物大分子,如DNA、蛋白质和多糖等。
生物分子基元的组合和排列方式决定了生物体的结构和功能。
四、城市空间基元在城市规划和设计领域,空间基元是指构成城市空间的最小单元。
城市可以被分解成各种基本的空间模块,如建筑物、街区和公园等。
这些基元通过不同的组合和排列方式形成了城市的空间结构,并对城市的功能和形象产生重要影响。
五、组织机构基元在组织学中,机构基元是指构成组织机构的最小单位。
无论是政府机构、学校还是企业,都由不同的组织单元构成。
这些基元可以是部门、团队或小组,它们通过相互协调和合作实现组织的整体目标。
机构基元的不同组合和关系形成了各种不同类型的组织机构。
六、信息网络基元在信息科学领域,网络基元是指构成信息网络的最小单位。
信息网络由节点和连接线构成,节点可以是计算机、服务器或其他网络设备。
这些网络基元通过物理或逻辑连接形成了复杂的信息传输和交换系统。
不同组合和布局方式的网络基元决定了信息网络的性能和可靠性。
七、心理认知基元在心理学和认知科学中,认知基元是指构成思维和知觉的最小单元。
例如,字母和数字可以视为语言认知基元,而线段和角度可以视为视觉认知基元。
这些基元通过组合和互动形成了复杂的思维过程和知觉经验。
基元的名词解释固体物理

基元的名词解释固体物理固体物理是研究固态物质的性质和行为的物理学分支。
在固体物理中,我们常常遇到一个重要的概念——基元。
基元是指构成固体物质的最小单位,它可以是原子、分子、晶胞等。
1. 原子基元原子是构成物质的基本单位,是构成一切物质的最小粒子。
原子基元是指由一个或多个原子组成的最小单位。
例如,晶体中的原子基元可以是单个原子,如金属晶体中的铁原子;也可以是多个原子构成的复合基元,如二氧化硅晶体中的硅原子和氧原子组成的硅氧基元。
2. 分子基元分子是由两个或多个原子通过化学键结合而成的基本粒子。
分子基元可以是由相同或不同的原子组成。
例如,水分子(H2O)是由两个氢原子和一个氧原子组成的基元,二氧化碳分子(CO2)是由一个碳原子和两个氧原子组成的基元。
3. 晶胞基元晶体是由大量有序的原子或分子周期性排列而成的结晶体。
晶胞是构成晶体的最小单位,它是由一组原子或分子组成的,并具有特定的几何形状。
晶胞基元是指晶胞中的那些原子或分子,它们通过向各个方向的重复平移堆积而形成整个晶体。
基元在固体物理中具有重要的意义。
通过研究基元的性质和相互作用,我们可以揭示固态物质的结构、电学、磁学、光学等性质。
基元的类型和排列方式对物质的性质产生重要影响。
例如,金属晶体由紧密排列的原子基元组成,导致金属具有良好的导电性;而蓝宝石等非金属晶体由分子基元组成,导致其绝缘性能较好。
同样,晶胞基元的类型和排列方式决定了晶体的晶型(例如立方晶系、六方晶系等)和晶格常数。
除了以上提到的基元类型,固态物理还研究了诸如电子等其他概念。
电子是带有负电荷的基本粒子,也是物质中的一个重要基元。
通过研究电子的行为和相互作用,我们可以解释诸如导电性、半导体效应等现象。
总之,基元在固体物理中扮演着至关重要的角色。
通过将基元的性质与物质性质之间的关系联系起来,我们能够深入理解固态物质的行为,并推动材料科学的发展。
固体物理作为物理学的重要分支,不仅对于基础科学研究具有重要意义,也对于技术应用和工程领域有着广泛的应用前景。
晶体的平移性

2.请画出2种点阵素单位,要求一种顶点无原 子,另一种顶点有原子。
第五题:⑴ 两种铜溴配合物晶体中的一维聚合链结 构的投影图 (其中部分原子给出标记)如下。①分别指 出两种结构的结构基元由几个Cu原子和几个Br原子 组成: 图⑴为 个Cu原子, Br原子; 图⑵为 个Cu原子, 个Br原子。 ② 用笔在图中圈出相应的一结构基元。
一. 晶胞:
晶胞的定义:晶体的重复单元,通过晶胞在空间 平移无隙地堆砌而成晶体。 二.晶格:根据X射线研究晶体的结构表明:组成晶 体的质点(分子、原子、离子)以一定的规则排列 在空间确定的点上,这些质点在空间排列就构成各 种几何形状的空间格子简称晶格,可以看作是三维 空间点阵。 每个质点在晶体所占的位置称为晶格结点。晶体 结点上,可以是原子、分子、或离子。在晶格内可 表示晶格特征的最基本部分称为单位晶格或晶胞。 晶胞在空间重复排列就是晶格。两者既有联系又有 区别。
物质:气态,液态,固态 固态物质:晶体,非晶体 晶体结构:原子规则排列,主要体现是原
子排列具有周期性,或者称长程有序。有 此排列结构的材料为晶体。 晶体中原子、分子规则排列的结果 使晶体具有规则的几何外形,X射线衍射 已证实这一结论。 非晶体结构:不具有长程有序。有此排列 结构的材料为非晶体。
石英晶体
NaCl晶体的二维周期排列的结构及其点阵(黑点代表点阵点)
例题1:点阵素单位是指最小的重复单位,将最小重 复单位的内容用一个点阵表示,最小重复单位中只含 一个点阵点,称为素单位。含2个或2个以上点阵点的 单位称为复单位。画出素单位的关键是能按该单位重 复,与单位预角上是否有圆圈无关。某平面周期性结 构系按右图单位重复堆砌而成。 1.写出该素单位中白圈和黑圈的数目。
⑵图⑶是由氯苯分子构成的平面点阵结构。 ①在图中标出一个正当单位来,并标明两个基本向 量和 ② 指出正当单位的组成 (内容); ③ 指出这种平面格子的正当单位的形式。
结构基元 晶胞

结构基元晶胞什么是结构基元?在固体材料科学中,结构基元是指构成晶体结构的最小重复单元。
它是研究和理解固体材料的基础。
晶体结构是由这些结构基元的周期性排列所组成的。
结构基元可以是原子、分子或离子,它们以一定的方式组合在一起形成晶体。
结构基元的类型和排列方式直接影响着固体材料的性质和行为。
晶胞的定义和特点晶胞是指晶体中最小的对称单元,它是由结构基元组成的。
晶胞具有以下特点:1.周期性:晶胞在空间中以周期性方式重复出现,这是晶体结构的基本特征之一。
晶胞的周期性排列使得晶体具有各向同性和周期性的性质。
2.对称性:晶胞具有一定的对称性,这是由结构基元的排列方式决定的。
晶胞的对称性决定了晶体的点群对称性和空间群对称性。
3.完整性:晶胞是晶体中最小的完整单位,它包含了所有结构基元的信息。
晶胞的完整性保证了晶体结构的一致性和稳定性。
4.体积:晶胞具有一定的体积,它可以通过晶胞参数来描述。
晶胞参数包括晶胞的长度、角度和对称性操作等。
晶胞的类型和分类根据晶胞的对称性和形状,晶胞可以分为以下几种类型:1.立方晶胞:立方晶胞是具有立方对称性的晶胞,它的边长和角度都相等。
立方晶胞常见于立方晶系的晶体,如纯铜和钠氯化物。
2.四方晶胞:四方晶胞是具有四方对称性的晶胞,它的边长相等,但角度不等。
四方晶胞常见于四方晶系的晶体,如硫和镍氧化物。
3.正交晶胞:正交晶胞是具有正交对称性的晶胞,它的边长和角度都不相等。
正交晶胞常见于正交晶系的晶体,如钢和氯化钠。
4.单斜晶胞:单斜晶胞是具有单斜对称性的晶胞,它的边长和角度都不相等。
单斜晶胞常见于单斜晶系的晶体,如硫酸铜和硫酸亚铁。
5.三斜晶胞:三斜晶胞是具有三斜对称性的晶胞,它的边长和角度都不相等。
三斜晶胞常见于三斜晶系的晶体,如铁磁体和石膏。
6.六方晶胞:六方晶胞是具有六方对称性的晶胞,它的边长相等,但角度不等。
六方晶胞常见于六方晶系的晶体,如石墨和石英。
晶胞的表示和描述晶胞可以通过晶胞参数来表示和描述。
晶体结构小结

结构基元在晶体中,原子(离子、原子团或离子团)周期性地重复排列。
上面我们在图形找出了最小的重复单位,类似的,可以在晶体中划出结构基元。
结构基元是指晶体中能够通过平移在空间重复排列的基本结构单位。
【例】一维实例:在直线上等间距排列的原子。
一个原子组成一个结构基元,它同时也是基本的化学组成单位。
结构基元必须满足如下四个条件:化学组成相同;空间结构相同;排列取向相同;周围环境相同。
【例】一维实例:在伸展的聚乙烯链中,-CH₂-CH₂- 组成一个结构基元,而不是-CH₂-。
注意,上图所示的聚乙烯链结构中,红色和蓝色的球虽然均表示-CH₂-, 可它们各自的周围环境并不相同。
上图右侧画出了两种CH₂-CH₂-CH₂片段,其组成和结构相同,但从空间位置关系来看,两者的取向不同,其中一个可由另一个通过旋转180°而得,这表明相邻-CH₂- 的周围环境不同,因而,-CH₂- 只是基本的化学组成,而不是结构基元。
【例】二维实例:层状石墨分子,其结构基元由两个C 原子组成(相邻的2个C 原子的周围环境不同)。
结构基元可以有不同的选法,但其中的原子种类和数目应保持不变。
上图用阴影部分标出了3种选法,但在每种选法中结构基元均含有2个c 原子。
如,在第三个图中,六边形的每个角上只有1/3的C 原子位于六边形之内,所以平均有2个C 原子属于一个六边形。
【例】二维实例:NaCl 晶体内部的一个截面。
一个Na*和一个Cr 组成一个结构基元(四边形内部有1个Na*, 顶角上的每个Cr 只有1/4属于结构基元)。
【例】二维实例:Cu 晶体内部的一个截面。
一个Cu 原子组成一个结构基元。
【例】三维实例:Po 晶体。
结构基元含1个Po 原子。
【例】三维实例:CsC1 晶体。
结构基元含1个Cs*和Cl。
【例】三维实例:金属Na 。
每个Na 原子的周围环境都相同,结构基元应只含有1个Na 原子。
左侧的立方体中含有2个Na 原子(每个顶点提供1/8个Na 原子,中心提供1个Na 原子),它不是结构基元,右侧图中虚线部分包围的平行六面体给出了一种正确的选法。
石墨的结构基元
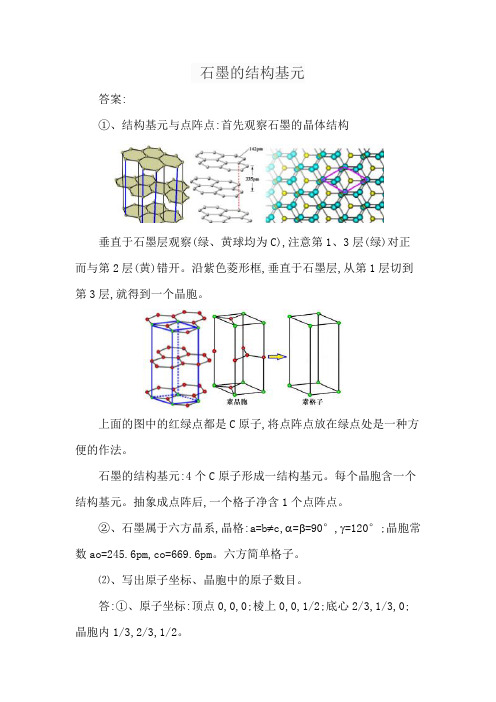
石墨的结构基元答案:①、结构基元与点阵点:首先观察石墨的晶体结构垂直于石墨层观察(绿、黄球均为C),注意第1、3层(绿)对正而与第2层(黄)错开。
沿紫色菱形框,垂直于石墨层,从第1层切到第3层,就得到一个晶胞。
上面的图中的红绿点都是C原子,将点阵点放在绿点处是一种方便的作法。
石墨的结构基元:4个C原子形成一结构基元。
每个晶胞含一个结构基元。
抽象成点阵后,一个格子净含1个点阵点。
②、石墨属于六方晶系,晶格:a=b≠c,α=β=90°,γ=120°;晶胞常数ao=245.6pm,co=669.6pm。
六方简单格子。
⑵、写出原子坐标、晶胞中的原子数目。
答:①、原子坐标:顶点0,0,0;棱上0,0,1/2;底心2/3,1/3,0;晶胞内1/3,2/3,1/2。
上图中展示了理想的石墨晶体结构具有六方晶胞,晶轴和四个不同的C原子的坐标。
②、晶胞中的原子数目晶胞净含4个C原子:8×1/8+4×1/4+2×1/2+1=4。
石墨是一种高温耐火材料,熔点>3500℃,不被熔融金属,炉渣和其它腐蚀介质、润湿(侵蚀),热膨胀系数小,温度升高时尺寸稳定,易加工,而且高温下仍有较高的强度,良好的抗热震性,在还原气氛下是理想的高温材料。
其最主要的用途是作电极及发热体,也可作模具及耐火炉衬,也能作为高温结构材料用于火箭、喷气机等高温部位。
耐火材料中引入C→M-C砖,Al-M-C滑板等。
CN=12。
在石墨结构中,层与层之间距离为言c=334.8pm,而层内碳原子的最短距离为,在两层之间碳原子间距比层内碳原子间距大得多,层状结构的特点很明显。
其中,粗线及实心圆点表示一个晶胞的情况。
层间每个碳原子的3个电子以共价键与周围3个C原子相作用,另一个电子为层中所有C原子共有,以金属键与层中所有C 原子结合,由于这种层状结构特点,使导热系数、热膨胀系数、硬度等,在不同方向有很大差别,如导电率,(层内的电导率为2.5×104~0.2×104Ω1、·cm1、,但垂直于层方向为5~1Ω1、·cm1、。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
晶体中结构基元的确定
一. 结构基元与点阵
晶体的周期性结构使得我们可以把它抽象成“点阵”来研究. 首先确定晶体中重复出
现的最小单元, 作为结构基元. 各个结构基元相互之间不但化学内容完全相同, 而且它们所
处的环境也必须完全相同. 每个结构基元可以用一个数学上的点来代表, 称为点阵点或结点. 于是, 整个晶体就被抽象成了一组点, 称为点阵.
尽管实际晶体的大小有限, 但从微观角度来看, 原子数目仍然极多, 而且处于内部
的原子数目远远多于表面. 所以, 不妨将晶体看作无限重复的周期性结构, 相应地, 点阵也
就包含无穷多的点阵点了.
二. 结构基元与点阵点
(1)一维周期性结构与直线点阵
我们首先以几种简单的一维周期性结构为例, 说明如何从周期性结构中辨认结构基
元(右图中用方框标出), 进而画出点阵. 应当说明, 将结构基元抽象为点阵点以后, 点阵点
放在何处是任意的, 但所有点阵点的放置必须采用同一标准:
由图可见, 并非每个原子或化学单元都能被看作结构基元.
再看两个更实际也稍微复杂的问题——硒的螺旋链和伸展聚乙烯链:
一维周期性结构中的结构基元硒螺旋链
和伸展聚乙烯链的点阵
在此基础上, 再将周期性结构扩展到二维和三维.
(2)二维周期性结构与平面点阵
实例1:Cu晶体的一种密置层(111).
每个原子是一个结构基元,对应一个点阵点(图中平行四边形是一个平面正当格子).
实例2: 石墨层
下图是石墨晶体的一层, 右下图中的小黑点是抽象出的平面点阵(为了比较二者的关系, 暂时将平面点阵放在了石墨层上)
为什么不能将石墨层的每个C原子都抽象成点阵点呢?这就必须从点阵的数学定义来理解了.不难想象, 若将所有结构基元沿某一方向平移到相邻或不相邻的另一个结构基元位置上, 晶体不会有任何变化(当然是假设不考虑表面原子) , 或者说可以复原. 相应地, 若将所有点阵点沿此方向平移到相邻或不相邻的另一个点阵点位置上, 点阵也不应当发生任何变化. 现在, 可以从数学角度给出点阵的定义:
点阵是按连接其中任意两点的矢量将所有的点平移而能复原的一组无限多个点.
石墨层及其点阵
假设石墨层上每个C原子都抽象成点阵点, 得到的是如下的一组无限多个点, 但这并不是点阵! 试选择一个矢量a , 将所有“点阵点”沿此方向平移,请看能够复原吗?
实例:NaCl(100)晶面(左下图). 矩形框中是一个结构基元,包括一对正负离子Na+和Cl-, 可抽象为一个点阵点. 安放点阵点的位置是任意的,但必须保持一致. 这样就得到了点阵(右下图):
石墨层点阵的错误抽取法 NaCl(100)晶面(a)及其点阵(b)
或等价地画成下图. 矩形框中的内容是与上述相同的一个结构基元,也包括一对正负离子Na+和Cl-:
(3)三维周期性结构与空间点阵
下面是一些金属单质的晶体结构,依次叫做立方面心、立方体心和立方简单.其中, 属于立方面心的金属有Ni Pd Pt Cu Ag Au等; 属于立方体心的金属有Li Na K Cr Mo W等; 属于立方简单的金属很少.
如何将这些金属的晶体结构抽象成点阵呢?
立方面心、立方体心和立方简单金属单质(每一个原子对应一个点阵点)
这里的每一个原子就是一个结构基元,从而都可以被抽象成一个点阵点. 所以,点阵看上去与晶体结构一样, 只是概念上有所不同.
CsCl型晶体中A、B是不同的原子,不能都被抽象为点阵点. 否则,得到的将是错误的立方体心点阵. 立方体心点阵虽然不会违反点阵的数学定义,却不是CsCl型晶体的点阵!若把立方体心点阵放回到该晶体中,则如图所示的平移操作将把A与B位置互换,而不能使晶体结构复原.
正确的做法是按统一的取法把每一对离子A-B作为一个结构基元,抽象成为一个点阵点. 点阵点可以放在任意位置,但必须保持一致(例如都放在A处),就得到正确的点阵——立方简单.
同理,NaCl型晶体中,A、B离子不能都被抽象为点阵点,而是每一个离子对A-B按统一的方式构成一个结构基元,抽象为一个点阵点. 于是,点阵成为立方面心:
CsCl型晶体的点阵不是为立方体心的原因将CsCl型晶体抽象成立方体心点阵的做
法
NaCl型晶体及其点阵
如果说CsCl型和NaCl型晶体中都有A、B两种不同的原子, 因而不能都被抽象为点阵点的话,金刚石中的C原子都能被抽象为点阵点吗?
假若可以这样做的话,得到的“点阵点”看上去与晶体中原子的分布相同. 现在, 请你根据点阵的数学定义来检验. 例如, 按图中箭头所示将所有点进行平移,这组点能复原
吗?不能. 说明这组点违反了点阵的定义, 本身就不是点阵! 更别说是金刚石晶体的点阵了.
正确的做法是按统一的取法把每一对原子C-C作为一个结构基元,抽象成为一个点
阵点,就得到正确的点阵——立方面心.
类似地, 六方金属晶体(例如Mg)也不能将每个原子都抽象为点阵点. 否则,得到的
所谓“点阵”也是违反点阵定义的, 本身就不是点阵. 将这种错误的“点阵”作用于晶体并
不能使之复原:
正确的做法是按统一的取法把一对原子Mg-Mg作为一个结构基元,抽象成为一个点
阵点,就得到正确的点阵——六方简单:
金刚石晶体的点阵为立方面心的理由 Mg晶体结构. 右图是一个晶胞
错误的点阵不能使Mg晶体复原从Mg晶体中抽象出六方简单点阵
这些实例表明,将晶体抽象成点阵的关键是正确地辨认结构基元.为了避免出错,当你把一种晶体抽象成一组点以后,应当问自己两个问题:
1. 这一组点符合点阵的定义吗? 将金刚石、Mg晶体中每个原子都抽象成所谓的“点阵点”, 得到的一组点就违反了点阵定义, 所以不是点阵.
2. 它是所研究晶体的点阵吗? 将CsCl型、NaCl型晶体中的每个原子都抽象成点阵点,得到的一组点并不违反点阵定义,但却不是所研究的晶体的点阵.。
