学案24: 卤素单质的相似性和递变性 上海市高一化学 开发海水的化学资源
高一化学开发海水中的卤素资源(20200806100059)

金冠注册
下列变性实质上为组织坏死的是A.细胞水样变性B.玻璃样变性C.纤维素样变性D.黏液变性E.淀粉样变性 [问答题,案例分析题]李军是一位军事家,他带兵打仗的经历极富传奇色彩。甲出版社认为,若出版以李军的战斗经历为主题的传记,能获得较好的社会效益和经济效益,于是向李军约稿。李军所在的部队认为此事对部队建设很有意义,予以大力支持。考虑到李军年事已高且没有子女,还指派文 用语句描述求使1×3×5×7×……×n<1000成立的最大正整数n的算法过程。 血细胞成熟 房间隔缺损,使症状加重的心律失常为A.室早B.房早C.房室传导阻滞D.房颤E.窦性心动过速 男性,35岁。婚后10年不育,检查发现精子运动差。因伴有反复咳黄脓痰和间断咯血,要求进一步检查和确诊。下列哪一项检查最有意义A.免疫学检查B.支气管体层摄片C.痰细菌检查和抗生素敏感性测定D.高分辨计算机体层摄影(HRCT),以了解有无支气管扩张E.纤维支气管镜检查 适用于治疗支原体肺炎的是()A.庆大霉素B.二性霉素BC.氨苄青霉素D.四环素E.氯霉素 铅中毒实验,选用大鼠复制动物模型时,大鼠本身易患进行性肾病,容易与铅中毒所致的肾病相混淆,选用蒙古沙鼠则较好,因为蒙古沙鼠只有铅中毒才会使其出现肾病变。此符合模型评估原则。A、重复性B、相似性C、可靠性D、可控性 患者,男性,60岁,觉右眼视力下降伴眼胀痛半年,曾有眼压升高达30mmHg病史。眼底检查:视乳头颜色变淡,杯凹不明显。视野检查与生理盲点相连的水平偏盲。此患者目前需采用的治疗为()A.降眼压药物治疗B.扩血管治疗,随访眼压,决定进一步的治疗方案C.扩血管治疗D.青光眼手术治 SDH光纤传送网是一个灵活的、兼容的、高可靠性的、可以实行集中智能化管理的网络。SDH的本质是。A、采用标准的光接口B、一种新设备——同步复用设备C、一种新的传输系统——大容量高速光纤传输系统D、一种新的网络技术——同步传输体系 椎间盘由以下几部分组成A.前纵韧带B.后纵韧带C.纤维环D.髓核E.软骨板 水泥砂浆中水泥用量不应小于㎏/M3。A、100B、200C、300D、400 静息状态下心血池显像时正常人心室轴缩短率应该是A.大于>75%B.大于>65%C.大于>45%D.大于>35%E.大于>25% 牙挺的工作原理包括、和。 以下不属于资产配置基本步骤的是。A.明确投资目标和限制因素B.确定有效资产组合的边界C.明确资本市场的方差值D.寻找最佳的资产组合 下列哪项不是晚期产后出血主要原因()A.胎盘、胎膜残留B.蜕膜残留C.剖宫术后子宫伤口裂开D.子宫复旧不全E.凝血功能障碍 不管做什么都应爱岗敬业。A.工种B.职业C.行业D.工作 患者男性,63岁,右耳垂前肿性长大8个月。近期肿物增长较快,痛向耳颞部放散。检查发现肿物约3.5cm、质地硬、有触痛、边界不清。活动度差,右眼睑闭合较对侧迟钝。以下哪项辅助检查对患者来说是不恰当的()A.CT检查B.胸部X线片C.腮腺造影D.细针吸细胞学检查E.切除活组织检查 工程项目按照项目经济特征来划分,其中不包括。A.竞争性项目B.公共项目C.社会事业项目D.其他项目 反映疾病严重程度的指标是A.发病率B.死亡率C.感染率D.病死率E.生存率 疯牛病的病原体是A.卫星病毒B.前病毒C.缺损病毒D.朊粒E.类病毒 我们一般使用以下哪个软件用于编制项目实施计划?A.MS-VISIOB.MS-PROJECTC.EXCELD.WORD 布-加综合征支架置入的适应证有A.肝段下腔静脉膜性或节段性狭窄或闭塞,伴或不伴血栓形成B.PTA疗效不佳或再狭窄病例C.下腔静脉长段完全性闭塞D.下腔静脉癌性狭窄或闭塞E.患者极度衰弱、恶病质者 注册建造师签章文件按照管理程序可分类为。A.报审类B.核准类C.内部管理类D.报告备案类E.对外履行责任类 患者左侧鼻唇沟变浅、口角下垂、额纹变浅或消失、眼裂变大、口角偏向健侧,露齿、吹哨、鼓颊、皱眉、皱额和闭眼等动作不能,同时左眼呈内收位,右侧肢体活动无神经麻痹C.右侧核性面神经麻痹D.中枢性面神经麻痹 如何根据服务对象,如何提高服务质量? 溢流堰法的测量水流量的主要方法,所用的堰顶的形式或堰壁厚度可分为薄壁堰、和。其中薄壁堰使用方法简单,精度较高,广泛使用于明渠测流,并可实现自动测量。 向管网系统送气要强调。 男性,3岁。右腹股沟可复性包块1年余,玩耍后不停哭闹伴呕吐6小时。查体:右侧阴囊肿胀,内可触及肿块,肿块呈蒂状延至腹股沟部,触痛明显,不可还纳。术中见疝内容物系小肠,颜色已成暗紫色,疝环狭小不易回纳,遂切开疝环解除压迫,此时你如何判断肠管是否失去活力A.压迫解除后 ()是规定国家和社会的基本制度,公民的基本权利和义务,国家机关的地位、组织和活动原则等重大社会关系的法律的总称。A.经济法B.民法C.宪法D.商法 角膜A.色白半透明B.无屈光能力C.表面盖有一层球结膜D.富有感觉神经未梢E.富有淋巴管 采集尿液标本时,错误的方法是A.女性患者最好用导尿法收集B.明显的尿路感染患者也应先采集尿液再控制感染C.截瘫患者多采用耻骨上膀胱穿刺法留取尿液D.尿液标本应在12小时内处理,以避免污染和杂菌生长E.一般应留取中段尿液送检 一气团移往某地后,本身温度逐渐升高,这个气团被称为。冬季影响我国的主要气团是、,夏季除此之外还有、。 适用于金瓷冠也适用于铸瓷冠的肩台形式是A.135°肩台B.带斜面90°肩台C.刃状边缘D.90°肩台E.深凹形 在肾静态显像中,为了清楚地显示马蹄肾,应采用的静态显像方式是A.前后位静态显像(ANT)B.后位静态显像(POST)C.左前斜位(LAO)3O度D.右前斜位(RAO)30度E.左后斜位(LPO)45度 较大儿童和成人可在何种局麻下行唇裂修复术()A.上牙槽后神经阻滞麻醉B.眶下神经阻滞麻醉C.腭前神经阻滞麻醉D.鼻腭神经阻滞麻醉E.下颌神经阻滞麻醉 船舶对海洋环境的可能污染源不包括.A、营运产生的废弃物B、海上船舶打捞和拆体C、海损事故造成溢油D、清洁压载水 下列哪些支出不属于政府转移支付:A.社会福利B.军费开支C.贫困救济补助D.社会保险 按储层岩性分的气藏是。A.构造气藏B.砂岩气藏C.岩性气藏D.均质气藏 Wernicke失语患者病变的主要区域是A.额下回后部B.额下回前部C.颞上回后部D.颞上回前部E.额上回后部
学案24卤素单质的相似性和递变性上海市高一化学开发海水的化学资源.docx

------ 卤素单质性质的变化规律及Cl-、Br_. I"一、学习目标(1)掌握卤素原子结构,学会归纳原子结构的相似性和递变性。
(2)认识卤素性质的相似性和递变性,学会归纳卤素性质的相似性和递变性在。
(3)体验结构和性质的相似性和递变性,认识物质结构和性质关系。
(4)通过实验,体验观察、分析、结论的科学的研究方法。
二、知识牵引1、请用化学方程式说明CL、Br2、12的活非金属活泼性强弱方程式: _________________________________2、比较卤素非金属性强弱的方法有: ________ /3用什么化学方法来检验一瓶水是自来水还是蒸憎水?如何排除C03?-的干扰?资料:碳酸银(AgzCOQ白色,不溶于水,但溶于硝酸。
Ag2CO3 +2 HNO3 -* 2AgNO3+H20 + C02 t试剂:______________________________________________现象:盛有自来水的试管:____________________________________盛有蒸憾水的试管: __________________________________化学方程式:___________________________三、问题探究1、卤素原子结构与性质的递变规律卤素元素的原子结构及性质的递变规律卤族元素(VHA)氟9卩氯17CI [臭35Br 碘531 *戒8sAt原子结构原子结构示意图最外层电子数核电荷数、电子层数原了半径原子核对外层电子的引力元素的化合价最低价:-1价,最高价:+7价(氟无负价)阴离子X)半径单质单质的颜色单质的状态(通常状况下)单质的熔、沸点的单质的密度性质单质在水中的溶解度单质的非金属性气态氢化物的生成及稳定性卤化物性质卤化银在水中的溶解度卤化氢(HX)的共性均为无色、有刺激性气味气体,极易溶于水,瓶口有白雾(酸雾,氢卤酸的小液滴分散在空气小形成)气态氢化物水溶液的酸性HF<HCl<HBr<HI (HF是弱酸,其他为强酸)最高价氧化物水化物的酸性HC101>HBr0i>H104 (氟元素没有含氧酸)阴离子(或卤化氢)的还原性大一小(AgF可溶,其他难溶)2、Bi•一、I~离子的检验实验:在盛有漠化钠溶液的试管中滴加硝酸银溶液,再滴加稀硝酸。
最新沪科版高一上第二章《开发海水中的卤素资源》学案

最新沪科版高一上第二章《开发海水中的卤素资源》学案一、学习目标:1、理解粗盐提纯中除去其中难溶性杂质和可溶性杂质的原理,学会溶解、过滤、洗涤、蒸发的操作,提高动手实验的能力2、知道氯碱工业的基本反应和主要产品,认识电解在化学工业中的作用和氯碱工业的重要性,掌握氯化氢(盐酸)和氢氧化钠的性质3、理解实际生产中应适当控制卤水密度的原因二、预习导引(一)独立自主:1、海洋是资源的宝库, 是海洋重要的组成部分,也是化学工业的重要原料。
2、粗盐中氯化钠约占 ,还含有其它一些盐类(如、、、等)和难溶性物质。
依次可用、、、等试剂除去。
(1)先加 ,目的是 ,化学方程式;(2)再加 ,目的是 ,化学方程式;(3)然后加 ,目的是 ,化学方程式;(4)最后加 ,目的是 ,化学方程式;加入试剂的步骤中,Na2CO3溶液必须在 BaCl2溶液之后,这样可以除去过量的 ,离子,而最后加入的必须是。
3、粗盐提纯的基本操作有、、、 ,其中分离难溶性杂质的主要步骤是 ,除去水分的主要步骤是 ,都用到的玻璃仪器是 ,其作用分别是、、、。
4、食盐不但是人类生活中不可缺少的物质,而且是重要的化工原料。
食盐可以用来生产、、、 ,还可以进一步加工成各种含氯和含钠的制品,如、、、、等。
5、氯碱工业中电解饱和食盐水的化学方程式为 ,阳极产物是 ,可以用检验,现象为;阴极产物是、 ,分别可以用、检验,现象分别是、。
(二)小组合作问题探究:1、粗盐提纯中用过几次玻璃棒,每次使用的目的是什么?2、从海水中可以获取哪些资源?3、海水晒盐中要适当控制卤水密度的原因?(三)预习反馈:1、在预习过程中,你认为哪些内容掌握得比较好的?2、在预习过程中,你还有哪些疑问?3、你能进一步提出拓展问题吗?4、小组学习中,存在的共同问题是什么?(组长填写)三、课堂流程:(一)预习反馈:针对预习内容,完成:①知识整理②疑难求助③互助解疑(二)教师精讲:(三)课堂检测:四、课堂总结:(整理知识结构)五、课后练习:1、下列物质有固定的沸点的是A 海水B 食盐水C 液氧D 啤酒2、为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶解于水,然后进行五项操作:①过滤②加过量NaOH溶液③加入适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。
高一化学第一学期 第二章《开发海水中的卤素资源》 沪科版

应用(D)是指以某一学习内容为重点,综合其他内容,
ppt课件
解决比较复杂的自然科学问题,是对知识的较系统的认识。
谢谢大家! 希望各位教师多提宝贵意见!
ppt课件
1、对于离子方程式只要了解其含义,并能理解和 书写课文中出现的几个离子方程式。这方面的内容有待 于以后的学习中再逐步加深。
2、由于学生没有学过电解质,什么时候可用离子 符号表示学生可能会有疑问,可以说明从强酸、强碱及 可溶性的盐这一角度解释。
3、练习部分学生熟悉复分解反应的离子方程式。 4、初步树立电荷守恒的概念。
第二章教材分析
ppt课件
一、教材的地位和作用
1、本单元通过研究开发海水中的化学资源,开始 学习有关元素化合物的知识。
2、充分体现“以学生发展为本”的指导思想,利 于学生综合素质的提高
3、有利于学科素养的养成 4、承前启后的作用
ppt课件
二、教材的内容--本章知识结构
海水 晒盐 食盐电解饱和溶液 (粗盐提纯实验)
ppt课件
阴 极
- +
阳 极
滴加酚 酞的饱 和食盐 水
家用环保型消毒液发生器
1、 氯气和水的反应是可逆 反应,教材P35与P57表示不统 一,学生没有学过可逆反应, 学生可能会有疑问,可以说明 该反应不能进行完全,在同一 体系中反应物与生成物共存。
2、可通过[思考与复习2.2] 中第2小题来巩固学习的氯水的 性质
8. 8.氯、溴、碘的活泼性比较 16. 气体实验室制法
ppt课件
二、教材的内容--课本中实验处理
高中化学鲁科版必修2作业:元素周期表的应用-卤素单质化学性质的相似性和递变性 Word版含解析

卤素单质化学性质的相似性和递变性1.通过分析元素周期表的结构和各元素性质的变化趋势,下列关于砹(原子序数为85)及其化合物的叙述中肯定不正确的是()A.砹与氢气较难发生反应B.相同条件下砹化氢比碘化氢稳定C.相同条件下砹化氢比碘化氢易分解D.砹元素位于第六周期2.砹是原子序数最大的卤族元素,根据卤素性质的递变规律,对砹及其化合物的叙述,正确的是()A.与氢气化合的能力:At2>I2B.砹在常温下为白色固体C.砹原子的最外电子层上有7个电子D.砹能从氯化钠溶液中置换出氯3.若能发现第117号元素X,它的原子结构与卤族元素相似,电子排布有7个电子层,且最外层有7个电子。
下列叙述中正确的是()A.X元素的气态氢化物的化学式为HX,在常温下很稳定B.其单质带有金属光泽,具有强氧化性,可与碘化钾发生置换反应生成单质碘C.其单质的分子式为X2,易溶于有机溶剂D.AgX是一种有色的易溶于水的化合物4.下列说法正确的是()A.氟、氯、溴原子的最外层电子数都是7,次外层电子数都是8B.由HF、HCl、HBr、HI酸性增强,可知氟、氯、溴、碘非金属性增强C.氟、氯、溴、碘的非金属性逐渐减弱是因为它们的电子层数逐渐增大D.砹是原子序数最大的卤族元素,它易溶于水,难溶于四氯化碳5.卤族元素碘的原子半径较大,可能呈现一定的金属性。
下列事实中最能够说明这个结论的是()A.单质碘能与氢氧化钠溶液反应B.已经制得ICl、IBr等卤素互化物C.单质碘易溶于碘化钾等碘化物溶液,形成I离子D.已经制得I (NO3)3、I (ClO4)3·2H2O等含I3+的离子化合物6.下列有关卤族元素的叙述不正确的是()A.卤素单质从F2到I2,颜色加深,熔点沸点升高B.卤素从氯到碘,最高价氧化物对应水化物的酸性减弱C.卤素从氟到碘,卤化氢水溶液酸性增强D.随着核电荷数的增加,卤素单质的氧化性增强7.下列关于卤族元素的叙述中,正确的是()A.随着原子序数的增加,元素的非金属性逐渐增强B.随着原子序数的减小,单质的氧化性逐渐增强C.通常呈黄绿色的也是氧化性最强的D.易升华的也是相对分子质量最大的8.下列说法中,不符合第ⅦA族元素性质特征的是()A.从上到下元素的非金属性增强B.易形成-1价离子C.最高价氧化物的水化物显酸性(氟除外)D.从上到下氢化物的稳定性依次减弱9.卤族元素按氟、氯、溴、碘的顺序,下列叙述正确的是() A.单质的颜色逐渐加深B.气态氢化物的稳定性逐渐增强C.与氢气反应越来越容易D.单质的熔、沸点逐渐降低10.随着卤素原子半径的增大,下列递变规律正确的是() A.单质的熔沸点逐渐降低B.卤素离子的还原性逐渐增强C.气态氢化物稳定性逐渐增强D.与氢气反应越来越容易11.卤族元素随原子核电荷数的增加,下列叙述不正确的是() A.原子半径依次增大B.元素的非金属性依次减弱C.单质的氧化性依次减弱D.氢化物的稳定性依次增强12.下列关于卤族元素的比较中,错误的是()A.气态氢化物的稳定性:HF>HCl>HBr>HIB.单质的氧化性:F2>Cl2>Br2>I2C.离子的还原性:F->Cl->Br->I-D.元素的非金属性:F>Cl>Br>I13.下列关于卤族元素的比较中,不正确的是()A.卤族元素的原子半径:F<Cl<Br<IB.单质的沸点:F2<Cl2<Br2<I2C.单质与氢气化合的难易:F2>Cl2>Br2>I2D.氢卤酸的酸性:HF>HCl>HBr>HI14.下列关于卤化氢的说法中不正确的是()A.卤素原子序数越大,其氢化物越稳定B.卤素原子序数越大,其氢化物越不稳定C.卤化氢稳定性的顺序为HF>HCl>HBr>HID.卤素单质与氢气越难反应,生成的氢化物越不稳定15.关于卤素单质(X2)的下列叙述中正确的是()A.都能与氢气化合发生爆炸B.都能与水剧烈反应C.都能与钠反应生成NaXD.都能与铁反应生成FeX316.关于卤素的下列叙述正确的是()A.卤素只能以化合态存在于自然界中B.卤素单质都能与水剧烈反应,生成氢卤酸和次卤酸C.卤素单质越活泼,其熔点、沸点就越高D.卤素是典型的非金属元素,它们不能与其他非金属元素化合17.下列关于卤素(用X表示)的叙述正确的是()A .卤素单质与水反应的通式为X2+H2O HX+HXOB.卤化氢都易溶于水,其水溶液都是强酸C.卤素单质都有颜色,都有毒D.卤素最高价含氧酸的通式为HXO418.卤素单质能与金属卤化物溶液反应,下列说法中不正确的是()A.该反应为置换反应B.有单质生成C.有卤素单质生成D.可能有氧气生成19.若用X代表氟、氯、溴、碘四种卤素,下列属于它们共性反应的是()A .X2+H2O HX+HXOB .X2+H22HXC .2Fe+3X22FeX3D .X2+2NaOH NaX+NaXO+H2O20.关于卤族元素的下列说法正确的是()A.所有卤族元素的微粒都易得电子B.和氟同一主族的元素都是非金属元素C.化合物中卤族元素都显负价D.卤族元素原子的原子半径从上到下逐渐减小21.氟、氯、溴、碘四种元素,下列有关它们的性质递变规律的说法,不正确的是() A.单质的密度依次增大B.单质的熔点和沸点依次升高C.氯气可从碘化钾溶液中置换出碘D.溴单质可从氯化钠溶液中置换出氯22.往碘化钾溶液中先加入氯水,再加入四氯化碳振荡,静置后出现分层,下层呈() A.橙红色B.紫红色C.无色D.深褐色23.甲、乙、丙三种溶液各含有一种X-(X-为Cl-,Br-,I-),向甲中加淀粉溶液和新制的氯水,则溶液变为橙色,再加丙溶液,颜色无明显变化。
卤素单质的性质比较

卤素单质的性质比较
1.物理性质
(1)相似性:都有颜色和毒性,不易溶于水(除F2外)、易溶于苯、四氯化碳等有机溶剂。
(2)递变性:从氟到碘,颜色依次加深,密度依次增大,熔沸点依次升高。
2.化学性质
(1)相似性:都具有强氧化性,表现在它们均能与金属、非金属、水和碱溶液反应。
(2)递变性:从氟到碘氧化性依次减弱,表现在:
①卤素与金属、非金属和水反应时,剧烈程度及反应的能力均依次减弱。
例如,与铁反应时,氟、氯、溴均将铁氧化为正三价的铁盐,而铁与碘反应生成碘化亚铁(FeI2);与氢气化合愈来愈难;与水反应时,氟与水迅速反应放出氧气,氯与水在光照下缓慢放出氧气,溴跟水反应比氯弱,但比碘强。
②活泼的卤素单质能将不活泼的卤素从其卤化物中置换出来。
注意F2与其他卤化物的水溶液反应,只能从水中置换出氧气,不能置换出其他卤素单质,但可以从熔融态的其他卤化物中置换出卤素单质。
高中化学《2开发海水中的卤素资源2.2海水中的氯氯气性质的研究》300沪科课标教案教学设计

2.2海水中的氯(第一课时)上海市松江二中顾韦平【教学说明】本节内容是高一学生第一次系统学习元素单质及化合物的性质,教学设计时,应该充分激发学生兴趣,利用信息科技提高效率。
氯气有毒,视频教学可以减少污染,保护环境。
这节分三个课时教学,第一课时,氯气的性质研究,第二课时,漂粉精和水的消毒,第三课时,探究气体体积的规律。
根据上海市高中化学学科教学基本要求,氯气的要求有:1、氯气的物理性质(A)2、氯气的化学性质(B)3、氯气的用途(A)4、氯化钠(B)5、氯化氢(B)6次氯酸钙(B),还有涉及物质制备、检验、收集、尾气处理等相关应用。
本节内容是针对我校所有学生,因为是起点年级,学生学习氛围比较好,对化学学习有较强的兴趣。
所以要抓住机会,打好基础,为高二等级考、合格考的学习打好基础。
【教学目标】一、知识目标1、知道氯气的物理性质和化学性质,学会有关的实验技能2、理解氯水和漂粉精的消毒原理3、理解影响气体体积的因素和气体摩尔体积,能进行简单计算二、过程与方法1、用研究的方法学习物质性质2、从理解影响气体体积的因素分析,提高逻辑推理能力。
三、情感态度价值观从消毒原理认识化学与人类健康的关系重点:1、氯气的物理性质和化学性质2、漂粉精的成分和消毒原理3、气体摩尔体积难点:1、氯气与水的反应,氯气与氢氧化钠的反应2、分析氯水的成分中哪种有漂白作用3、漂粉精消毒原理4、阿伏加德罗定律和气体摩尔体积的计算【教学流程】1、复习引入:海水中最多的元素、工业上如何得到氯气?介绍实验室制备氯气的方法PPT2、化学史话,提高阅读分析能力3、氯气性质探究:研究性学习的规律:物理性质化学性质探究方法介绍。
4、课堂实验:以课本实验为主,结合图片、视频和实验操作多角度展示相关性质。
物理性质:实物展示化学性质:1).结构分析2).与金属反应与非金属反应与碱的反应3).氯气与水的反应和漂白作用5、总结氯气的性质P33填表6、回家作业:练习册:课时一【板书设计】2.2海水中的氯一、氯气的来源二、氯气的性质科学研究的一般规律:物理性质:化学性质:归纳:。
卤素单质及其化合物的相似性和递变性 新高考化学专题讲解 考点详细分析深入讲解 化学高考必看 最新版

反应生成NaClO3和NaCl,其离子方程式为
。
2.[2017海南,4改编]在酸性条件下,可发生如下反应: ClO3-+2M3++4H2O
M2O7n-+Cl-+8H+,M2O7n-中M的化合价是
。
3.[2016全国卷Ⅰ,28改编]NaClO2中Cl的化合价为 。利用氯酸钠、硫酸
和SO2制备ClO2,反应中有副产物NaHSO4生成,该反应的化学方程式
“双一流”名校冲刺
A.向苦卤中通入Cl2是为了提取溴 B.粗盐可采用除杂和重结晶等过程提纯 C.工业生产中常选用NaOH作为沉淀剂 D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
“双一流”名校冲刺
解析:苦卤中含有Br-,通入Cl2可将Br-氧化成Br2,A项正确;粗盐中含有 Ca2+、SO42-等杂质离子,故先除杂得NaCl的饱和溶液,而NaCl的溶解度 随温度变化不大,采用重结晶可以得到较纯净的NaCl,B项正确;工业上 沉淀海水中的Mg2+,采用Ca(OH)2,不用NaOH,因为NaOH的价格较贵,C 项错误;Br2易挥发,先用热空气和水蒸气吹出后,再用SO2吸收,生成 H2SO4和HBr,富集后再用Cl2将HBr氧化成Br2,D项正确。
疑难2 从海水中提取氯、溴、碘
1.氯的提取——氯碱工业
“双一流”名校冲刺
2.海水提取溴 (1)流程
注意:溴的富集(④⑤步)还有一种方法:Br2在碱性条件下发生歧化反应 生成Br-和BrO3-,然后在酸性条件下Br-和BrO3-发生归中反应生成Br2。
“双一流”名校冲刺
(2)发生反应的化学方程式
①2NaBr+Cl2
5MnO2↓+12H++2Cl-。
高中化学《2开发海水中的卤素资源2.2海水中的氯氯气性质的研究》313沪科课标教案教学设计

《开发海水中的卤素资源》海水中的氯----氯气与漂粉精1/9上海财经大学附属中学高一化学----王学军学习目标1、掌握氯气的物理性质和化学性质。
2、理解氯水和漂粉精消毒的原理。
3、理解氧化还原反应的本质,树立“对立与统一”等辩证唯物主义观点。
4、理解影响气体体积的因素和气体摩尔体积,并能进行有关的化学计算。
重点难点重点:1、氯气的物理性质和化学性质。
2、漂粉精的成分和消毒作用。
3、氧化还原反应。
4、气体摩尔体积。
难点:1、氯气和水、氢氧化钠的反应。
2、氯水中的成分,及氯水漂白的原因。
3、漂粉精的消毒原理。
4、氧化还原反应中的电子得失。
5、相同温度和压强下,1mol不同气体的体积基本相等。
有关气体摩尔体积的计算。
教学过程引课问题:大家知道我们在家里炒菜时必需要放的是什么?问题:那么我们在生活中所说的盐和我们化学中说的盐含义一样吗?讲述:生活中的盐主要指食盐----氯化钠,化学上的盐指能够电离出金属阳离子和酸根阴离子的化合物。
问题:食盐是有哪两种元素组成的,我们主要通过什么途径来获得食盐?讲述:食盐有钠元素和氯元素组成,通过海水晒盐。
海水中含有大量的氯化钠,氯化镁等盐类,也就必然含有大量的氯元素。
板书海水中的氯氯—氯原子:第周期第族;原子结构示意图:;电子式:。
讲述:氯原子最外层有7个电子,在化学反应过程中极易得到1个电子而形成8电子稳定结构,所以氯元素在自然界中以化合态存在。
问题:在自然界氯以化合态存在,那么有没有游离态的氯,它具有什么样的性质?资料:1、在第一次世界大战期间,一次德军与英、法军战士在比利时的伊普尔《开发海水中的卤素资源》海水中的氯----氯气与漂粉精2/9上海财经大学附属中学高一化学----王学军对峙。
黎明时,英、法军前线战壕的士兵突然看到一股阴森森的黄绿色气体逐渐向前袭来,很快数百名英、法军战士窒息而死,数千名士兵双目失明。
这就是1915年4月22日发生的另人发指的事件。
这种阴森森的黄绿色气体就是氯气。
化学新教材人教版高中化学必修第一册知识解析卤族元素的相似性与递变性
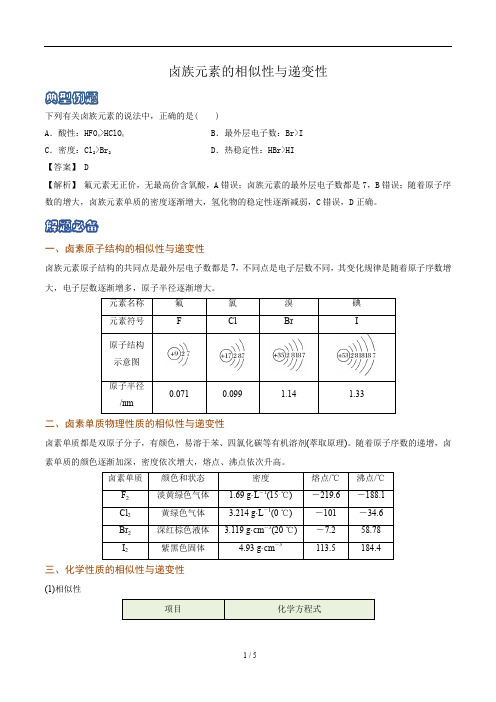
卤族元素的相似性与递变性典型例题下列有关卤族元素的说法中,正确的是( )A.酸性:HFO4>HClO4 B.最外层电子数:Br>IC.密度:Cl2>Br2 D.热稳定性:HBr>HI【答案】 D【解析】氟元素无正价,无最高价含氧酸,A错误;卤族元素的最外层电子数都是7,B错误;随着原子序数的增大,卤族元素单质的密度逐渐增大,氢化物的稳定性逐渐减弱,C错误,D正确。
解题必备一、卤素原子结构的相似性与递变性卤族元素原子结构的共同点是最外层电子数都是7,不同点是电子层数不同,其变化规律是随着原子序数增大,电子层数逐渐增多,原子半径逐渐增大。
元素名称氟氯溴碘元素符号 F Cl Br I原子结构示意图原子半径0.071 0.099 1.14 1.33/nm二、卤素单质物理性质的相似性与递变性卤素单质都是双原子分子,有颜色,易溶于苯、四氯化碳等有机溶剂(萃取原理)。
随着原子序数的递增,卤素单质的颜色逐渐加深,密度依次增大,熔点、沸点依次升高。
卤素单质颜色和状态密度熔点/℃沸点/℃F2淡黄绿色气体 1.69 g·L-1(15 ℃) -219.6 -188.1Cl2黄绿色气体 3.214 g·L-1(0 ℃) -101 -34.6Br2深红棕色液体 3.119 g·cm-3(20 ℃) -7.2 58.78I2紫黑色固体 4.93 g·cm-3113.5 184.4三、化学性质的相似性与递变性(1)相似性项目化学方程式与H2反应X2+H2一定条件2HX与活泼金属反应(如Na) 2Na+X2点燃2NaX与H2O反应X2+H2O HX+HXO (X=Cl、Br、I)(2)递变性①卤素单质与H2的反应:一定条件下均可与氢气反应:H2+X22HX。
从F2→I2反应条件由易到难;反应程度由剧烈变为缓慢;卤化氢的稳定性逐渐减弱。
化学式与氢气的反应化学方程式F2在冷、暗处就能剧烈化合而爆炸,生成的氟化氢很稳定F2+H22HF(氟化氢)Cl2在光照或点燃下发生反应,生成的氯化氢较稳定Cl2+H2光照或点燃2HCl(氯化氢)Br2在加热至一定温度下才能反应,生成的溴化氢不如氯化氢稳定Br2+H2△2HBr (溴化氢)I2持续加热下才能缓慢化合,碘化氢不稳定同时发生分解I2+H2△2HI(碘化氢)②卤素单质间的置换反应:卤素间可以发生置换反应,较活泼的非金属可以将较不活泼的非金属从它们的盐溶液中置换出来。
沪科版化学高一上《开发海水中的卤素资源》教案

第二章沪科版化学高一上《开发海水中的卤素资源》教案卤素资源教学设计教材分析地位:本章是整个高中阶段较为详细、全面地学习和研究一族元素的性质及其变化规律的一章,是一个典型的非金属元素族,本章为元素族概念的形成,同族元素性质递变规律,元素周期律的形成积累感性材料,是学习元素周期律、周期表知识的重要基础。
内容:本章教学内容分为(1)以食盐为原料的化工产品:介绍食盐的提取,工业上电解饱和食盐水,盐酸、氢氧化钠的性质,氯化氢的溶解性及制法。
(2)氯气的性质及重要用途(3)从海水中提取重要元素:学习镁、溴、碘的提取及溴、碘的溶解性、特性。
卤族元素的物理性质及化学性质的相似形和递变性。
(4)进一步学习氧化还原反应,电离方程式,离子方程式,为今后各章节的学习打下重要基础。
教学中可增加氯气的实验室制法,将探究气体体积的规律内容放在物质的量的计算中学习。
教法与学法:重视基础知识的落实和科学方法的培养。
通过对氯气的性质、用途及实验室制法的学习,将其它卤素的性质与氯气的性质进行比较,从个别到一般逐步地、客观地展现这一族元素的性质及变化规律,也为后面学习同族元素的性质提供了方法和研究思路。
教师必须以学生为主体,精心设计问题、创设实验引导学生积极思考,让学生在学习的过程中感受、体验学习的方法,领会知识的内涵及本质。
因此在本章的内容的教学中知识的掌物和方法的形成同等重要。
重视化学实验的教学功能。
俗话说“百闻不如一见,百见不如一练”。
只要能让学生动手的实验,就应该积极地创设条件让学生动手做,不能让学生动手做的实验,教师应该尽量演示。
让学生在实验中观察思考,讨论分析,推理判断,自己去发现问题,解决问题和得出结论。
使学生生动、活泼、主动地发展。
重视联系生产、生活实际。
含卤化合物的介绍,海水资源的开发利用,氯碱工业等应紧密联系生产、生活实际,反映现代科技发展情况,是培养学生学习兴趣,增强学生学习动机的素材。
教师应根据实际情况,有针对性地指导阅读,也可围绕相关问题指导学生收集一些材料,研究一些问题,开展讨论或撰写小论文。
高一化学---海水中的卤素资源知识点及习题汇总

高一化学---海水中的卤素资源知识点及习题汇总考纲要求1.从原子的核外电子排布,了解卤素(单质化合物)的相似性和递变性。
2.了解几种重要的含卤素化合物的性质和用途。
知识准备1. Cl2、Br2、I2的物理性质(1)氯、溴、碘三种元素在元素周期表中排在同一纵列里,都属于___族元素,简称“卤素”。
(2)溴元素主要以______形式存在于海水中,人们把__________称之为“海洋元素”。
Br2是一种________色____体,易挥发;I2是一种______色____体,易升华。
Br2溶解在水中的颜色是________,I2溶解在水中的颜色是____________,Br2溶解在CCl4中的颜色是__________,I2溶解在CCl4中的颜色是__________。
【问题思考】如何保存液溴?______________________________________2. 卤素单质的氧化性和离子的还原性(1)卤素单质氧化性的顺序是:Cl2___Br2___I2;阴离子的还原性顺序是:I-__Br-__Cl-。
(2)请写出Cl2与NaBr、KI溶液反应的离子方程式:_________________________、_______________________________;(3)Br2与KI溶液反应的离子方程式:__________________________________。
3.海水提溴从海水中提取溴一般要经过________、________、________三步。
利用溴的________性,鼓入________或水蒸气,就可将溶解在苦卤中的溴分离出来。
海水提溴方法一①富集:蒸发浓缩得到苦卤,其中Br-的浓度高达6g/L②氧化:向苦卤中通入氯气,使溴离子氧化成溴单质2Br- +Cl2→2Cl- +Br2③吹出:向溴水混合物(Ⅰ)中鼓入热空气,吹出溴得到含溴的空气④吸收:用SO2和H2O吸收吹出的溴Br2 + 2H2O + SO2→H2SO4+ 2HBr⑤氧化:向吸收液中再次通入氯气,氧化出溴单质2HBr +Cl2→2HCl +Br2⑥蒸馏:将溴水混合物(Ⅱ)进行蒸馏,得到高纯度溴。
卤素单质物理性质的相似性和递变性

卤素单质物理性质的相似性和递变性
比起其他元素,卤素元素又叫做“卤族元素”,它们具有极为类似的物理性质,及其重要的递变性,因而在各种化学反应中引起了极大的关注。
卤族元素是波尔是发现的元素之一,紧接着又有密斯,钾,氯,钠等元素被发现,它们都属于共价化合物。
它们都有相似的化学特性,在原子半径上仅比较少,具有低电子层抽取能力,化学反应也比较活跃,它们能互不溶性替换,互补电荷,当所有的卤素都组成时,它们具有向水溶液中阳性离子和氨基引入以及溶剂萃取的能力。
加以考虑,我们可以发现,卤族元素的物理性质具有相似和递变性。
它们之间
的半径仅限于0.98-1.93Å,具有较低的氧化倍数,即1-8;它们还具有很强的可溶性、可解吸和溶机,当组成时,它们具有可以离子聚集和反应的特性。
总的来说,卤素单质的物理性质相似和递变性对于相关的化学反应有着重要的
影响,因此它们在化学领域中体现出极为重要的作用。
此外,卤素元素的相似物理性质使得它们可以在牵引效应和滤柱屏蔽效应等现象中发挥重要的作用,从而使用户获得更加可靠的结果。
【高考推荐】2019-2020高考化学第4章(非金属及其化合物)第2节氯海水资源的利用考点(含解析)

考点二卤素的性质及卤素离子的检验李仕才1.卤素单质的相似性和递变性(1)递变性(2)相似性(用X代表Cl、Br、I)①都能与大多数金属反应:2Fe+3Br2===2FeBr3;I2+Fe===FeI2;②都能与H2反应:H2+X2===2HX;③都能与H2O反应:X2+H2+HXO(F2例外);④都能与碱液(NaOH)反应:X2+2NaOH===NaX+NaXO+H2O(F2例外)。
2.Cl2、Br2、I2的氧化性氯、溴、碘单质的氧化性强弱是Cl2>Br2>I2,阴离子的还原性:Cl-<Br-<I-。
(1)Cl2能从Br-的溶液中置换出Br2,其离子方程式:Cl2+2Br-===2Cl-+Br2;同理,Br2能置换I2,其离子方程式:Br2+2I-===2Br-+I2。
(2)与一些还原性离子反应,如Br2与SO2-3、Fe2+反应的离子方程式分别为SO2-3+Br2+H2O===SO2-4+2Br-+2H+,2Fe2++Br2===2Br-+2Fe3+。
3.特殊性(1)氟①无正价,非金属性最强,F-的还原性最弱。
与H2反应在暗处即爆炸。
②2F2+2H2O===4HF+O2,F2不能在水溶液中置换其他卤素单质。
③氢氟酸是弱酸,能腐蚀玻璃,故应保存在塑料瓶中;有毒。
(2)溴①Br2是深红棕色液体,易挥发。
②Br2易溶于有机溶剂。
在有机溶剂中显橙色或橙红色。
③盛溴的试剂瓶中加水,进行水封,保存液溴不能用橡胶塞。
(3)碘①淀粉遇I2变蓝色。
②I2加热时易升华。
③I2易溶于有机溶剂。
在有机溶液中颜色为紫色或紫红色。
4.卤素离子检验(1)AgNO3溶液——沉淀法判断正误(正确的打“√”,错误的打“×”)1.类比Fe与Cl2的反应判断Fe与I2反应时生成FeI3。
( ×)2.F2通入氯化钠溶液中反应置换出Cl2。
( ×)3.可以用淀粉溶液检验加碘食盐中的KIO3。
卤族元素性质递变规律

1.卤族元素性质的相似性和递变性(1)卤素单质随原子序数的递增,颜色逐渐加深,从F2→Cl2→Br2→I2,颜色由淡黄绿色→黄绿色→深红棕色→紫黑色,状态由气态→气态→液态→固态;卤素单质固态时均为分子晶体,分子量增大,范徳华力增大,熔沸点逐渐升高。
(2)从F→I,电子层数增多,非金属性减弱,表现为:氧化性F2>Cl2>Br2>I2,还原性I->Br->Cl-。
2.卤素氢化物性质的递变规律(1)还原性按HF、HCl、HBr、HI顺序逐渐增强。
例如:①氟单质只能通过电解法才能制取;②浓硫酸可以干燥HCl气体而不能干燥HBr、HI气体;③FeCl3可使淀粉─KI试纸变蓝色。
(2)水溶液的酸性:卤素氢化物都极易溶于水,且其水溶液的酸性依次增强。
(3)热稳定性按HF、HCl、HBr、HI依次降低。
3.卤化银的溶解性、稳定性及卤素离子的检验(1)在AgX中,只有AgF易溶于水,其余均难溶于水,且按AgCl、 AgBr、 A gI顺序溶解度依次减小。
(2)AgX都不稳定,见光或受热易分解为卤素单质和银,且按AgF、AgCl、 A gBr、 AgI的顺序稳定性依次减弱。
(3)AgCl、 AgBr、 AgI都不溶于稀硝酸,且颜色逐渐加深,分别为白色、浅黄色、黄色,所以,可用硝酸酸化的硝酸银来检验Cl-、Br-、I-的存在。
4.卤素单质的制取(1)氯气的制取①工业制氯气:2NaCl + 2H2O ════ 2NaOH + Cl2↑+ H2↑②实验室制取氯气:以含有Cl-的物质为原料,凡能将Cl-氧化成Cl2的物质都可以作为制取氯气的氧化剂。
如:MnO2 + HCl(浓);MnO2+ NaCl + H2SO4(浓);KMnO4 + HCl(浓);KClO3+ HCl(浓);HClO+HCl等。
(2)溴的制取①工业制溴(以海水为原料)Ⅰ、通Cl2气将化合态的溴氧化成单质溴:Cl2+ 2 Br- === 2 Cl- + Br2Ⅱ、以硫酸酸化,NaBr与NaBrO3发生反应,结果化合态的溴转化为溴单质5Br- + BrO3- + 6H+ ═══ 3Br2+ 3H2O②实验室制溴一般用NaBr、浓H2SO4、MnO2共热,即:2NaBr + 2H2SO4(浓) + MnO2═══ Na2SO4 + MnSO4 + Br2 + 2H2O 注意:卤素单质对橡胶制品有强腐蚀性,使用橡胶管时玻璃管要靠紧,使用橡胶塞时,要用铝箔包住。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
学案24: 2.3从海水中提取溴和碘
————卤素单质性质的变化规律及Cl-、Br-、I-一、学习目标
(1)掌握卤素原子结构,学会归纳原子结构的相似性和递变性。
(2)认识卤素性质的相似性和递变性,学会归纳卤素性质的相似性和递变性在。
(3)体验结构和性质的相似性和递变性,认识物质结构和性质关系。
(4)通过实验,体验观察、分析、结论的科学的研究方法。
二、知识牵引
1、请用化学方程式说明Cl
2、Br2、I2的活非金属活泼性强弱
方程式:
2、比较卤素非金属性强弱的方法有: /
3 用什么化学方法来检验一瓶水是自来水还是蒸馏水?如何排除CO32-的干扰?
资料:碳酸银(Ag2CO3)白色,不溶于水,但溶于硝酸。
Ag2CO3 +2 HNO3→2AgNO3+H2O+CO2↑
试剂:
现象:盛有自来水的试管:
盛有蒸馏水的试管:
化学方程式:
三、问题探究
1、卤素原子结构与性质的递变规律
卤素元素的原子结构及性质的递变规律
2、Br-、I-离子的检验
实验:在盛有溴化钠溶液的试管中滴加硝酸银溶液,再滴加稀硝酸。
现象:
化学方程式:
实验:在盛有碘化钾溶液的试管中滴加硝酸银溶液,再滴加稀硝酸
现象:
化学方程式:
思考:还有什么其他方法检验溶液中的Br-、I-?
比较检验Br-、I-离子的几种方法,判断哪种更好?
参考资料:《四氯化碳》
四氯化碳,CCl4,不燃烧,易挥发。
工业上主要用于溶剂和灭火剂等。
四氯化碳具有轻度麻醉及肝脏毒作用。
进入人体可引起急性中毒和慢性中毒。
凡患有器质性神经系统病变或慢性心、肝、肾疾病的患者不宜从事四氯化碳作业。
评价实验方案优劣的一般标准是:、、。
小结:
Cl-、Br-、I-离子的检验方法:在需检验的溶液中加入和;
实验现象:白色沉淀→待测液中含有。
浅黄色沉淀→待测液中含有。
黄色沉淀→待测液中含有。
3.卤化银的性质和用途
1.卤化银(AgX)的性质:A、不溶于水,也不溶于酸和碱(除了氟化银易溶)
B、不稳定性(见光容易分解):
(写方程式)
2.用途:感光纸、胶卷(AgX),变色眼镜(AgBr),人工降雨(AgI)
思考:
如今在中国某些地区,依然私盐猖獗,冒充碘盐贩卖,请你想一个方法来检验真假碘盐?(补充资料:碘盐中碘的存在形态为IO3—,而碘酸根离子的性质IO3—+5I—+6H+→3I2+3H2O)
三、实践感悟
1 、下列物质中,通常状况下呈液态的
A. Cl2 B .N2 C .Br2 D .I2
2、下列物质需密封保存的是
A . 漂白粉
B . 石灰石
C . 溴
D . 纯碱
3、下列微粒半径由大到小顺序排列,正确的是
A . I > Br > Cl > F
B . I- > Br- > Br > Cl
C . I > I- > Cl > Cl-
D . F- > Cl- > Br- > I—
4、下列液体分别与溴水混合,充分振荡后静置,上层液体呈橙色,下层液体呈无色的是
A . 苯
B . 酒精
C . 汽油
D . 四氯化碳
5、下列物质中,不能使湿润的淀粉碘化钾试纸变蓝的是
A.碘水 B.溴水 C.碘化钾溶液 D.氯气
6、在含有NaCl、NaBr、NaI混合溶液中滴加足量的溴水,经充分反应后,将溶液蒸干并灼烧,残渣固体为:
A.NaCl、I2 B.NaBr、NaCl和Br2 C.NaBr、NaCl和I2 D.NaCl、NaBr
7、卤素单质的性质与F2>C12>Br2>I2的变化规律不符合的是
A.与H2反应剧烈程度B.非金属的活泼性C.单质的氧化性D.熔沸点
8、检验溶液中是否含I-,可以加入试剂
A. 只有AgNO3溶液
B. 用AgNO3溶液和稀硝酸
C. 用溴水和CCl4
D. 用溴水和酒精
9、检验氯化氢气体中是否有氯气的方法是
A. 用干燥的蓝色石蕊试纸
B. 用干燥的有色布条
C. 将气体通过硝酸银溶液
D. 用湿润的淀粉碘化钾试纸
10、下列物质中,不能使湿润的淀粉碘化钾试纸变蓝的是
A、碘水
B、溴水
C、碘化钾溶液
D、氯气
11、鉴别NaCl、NaBr、NaI三种溶液可以选用的试剂是:
A、碘水、淀粉溶液
B、溴水、汽油
C、溴水、淀粉溶液
D、氯水、四氯化碳
12、下列关于卤素(用X表示)叙述正确的是
A. 其单质与水反应的通式为:X2+ H2O=HX + HXO
B. HX极易溶于水,其水溶液是强酸
C. 按F、Cl、Br、I的顺序,HX卤化氢热稳定性越来越稳定
D. 按F、Cl、Br、I的顺序,其单质的熔沸点逐渐增大
13.下列物质中,长期露置在空气中,不会变质的是
A.AgI
B.漂白粉
C.食盐
D.次氯酸溶液
14、卤素原子结构的特点:
最外层电子数均为个,卤族元素的稳定价为价。
根据Cl的化合价,Br和 I的化合价有:
15、卤素是活泼的非金属元素的原因:
最外层电子数均为个,所以得电子能力(强、弱)
在相同电子层数的元素中,原子半径最(小、大),吸引电子能力(强、弱),故得电子能力也很(强、弱)
(3)氟在卤素中,原子半径最(小、大),故得电子能力最(强、弱)。
大量事实证明,氟元素是所有非金属元素中活动性最强,故氟(有、无)正价。
16、在分液漏斗中装入溴化钾溶液,加入适量的氯水,振荡后溶液呈色,原因是,反应的方程式。
然后加入苯,振荡后静置,看到上层接近色,下层接近色,这种分离方法称为
17、实验室洗刷仪器时,对做过碘升华实验的烧杯壁上残留的碘,可用_____________洗涤;对制Cl2用的烧瓶底部沾有的MnO2固体,可用_______________________洗涤;对玻璃仪器上沾有的铁锈,应用_________洗涤。
18、一瓶无色溶液中可能含有I-、Cl-、CO32-,在此溶液中加入AgNO3溶液有沉淀生成,再加入稀硝酸,沉淀部分溶解,只剩下黄色沉淀。
由此推断:此溶液中含离子,不含离子。
19、稀溴水和稀碘水都会呈现相同的浅黄色,试用不同的实验方法将它们区别开。
解法一:根据Br2和I2在CCl4中颜色不同,各取的溶液,分别向两试管中加
入,用力,静置片刻,观察CCl4层,呈现色的原来是碘水,呈现色的原来是溴水。
解法二:根据碘单质遇淀粉变蓝的特性,各取少量溶液分别加入少量,
现象的是溴水,的是碘水。
解法三:根据Br2能与KI溶液反应,而I2不能与之反应设计实验。
少量溶液,向其中加入KI溶液,无明显现象的原来是,溶液颜色变深的原来是。
解法四:利用溴水和碘水中分别含有少量的溴离子和碘离子,可用硝酸银溶液检验出来。
