吡啶的化学反应
吡啶 结构

吡啶结构引言:吡啶结构的重要性和应用领域介绍吡啶是一种含氮杂环化合物,由于其稳定性和广泛的化学反应性质,在化学、医学、材料科学等领域中有广泛的应用。
吡啶结构的探究和研究对于人类文明的进步和科学研究的发展有着十分重要的意义。
接下来将从吡啶结构的含义、结构特点、应用领域等几个方面来详细分析。
第一部分:吡啶结构的含义和结构特点吡啶结构是指由一个含氮的芳香环和一个烷基结构组成的化合物。
其分子式为C5H5N,分子量为79.1g/mol。
吡啶结构的特点是其具有一个含有五个碳原子的芳香环和一个相邻的硝基原子组成的烷基结构,因此其结构不仅具有柔韧性和稳定性,还具有强烈的活性基团和反应性能力。
第二部分:吡啶结构的应用领域1. 医学领域吡啶类化合物广泛应用于药物合成中,具有强效抗菌、消炎、抗癌、治疗心血管疾病等功效。
如磺胺类药物、喹诺酮类药物、非类固醇类抗炎药等均含有吡啶结构。
2. 材料科学领域吡啶类化合物作为高分子制备中的功能性单体,其聚合物具有良好的电子传输、半导体特性和荧光性能,在太阳能电池、有机发光二极管等领域有着广泛的应用。
3. 化学领域吡啶结构的化学反应活性可以进行多种官能团的取代,合成出多种求电子性、亲核性、碱性和酸性的有机化合物。
因此,吡啶及其衍生物是制备高效催化剂、高性能涂料、高能指示剂等化学品的重要中间体。
第三部分:吡啶结构中的研究进展1. 吡啶结构的合成方法研究目前,吡啶类化合物的制备方法较多,如使用过渡金属催化剂的环合成、亲核取代反应、氧化反应、还原反应等,部分反应已经得到了大量的研究和发展,如Suzuki偶联反应、Sonogashira偶联反应等。
2. 吡啶结构的功能研究吡啶类化合物的应用领域相对较广,但研究并不充分,很多研究还有待深入进行。
例如针对药物用途的吡啶酮类化合物,在治疗癌症中的具体作用机制、药效等方面还需要更多的研究;利用吡啶结构作为多种官能团的催化剂,其反应机制、催化性能也需要进一步研究。
吡啶和卤代烷反应机理

吡啶和卤代烷反应机理
吡啶和卤代烷的反应机理涉及亲核取代反应。
当卤代烷和吡啶
发生反应时,通常会发生亲核取代反应,其中吡啶的氮原子作为亲
核试剂攻击卤代烷的碳中心,从而形成新的化学键。
这种反应通常
在碱性条件下进行,以促进氮原子的亲核攻击。
具体而言,当吡啶和卤代烷反应时,首先碱性条件下,氢离子
会被吡啶的氮原子中的孤对电子所吸引,形成带负电荷的氮离子。
同时,卤代烷中的卤原子(如氯、溴或碘)会被碱性条件下的氢氧
化物离子(OH-)攻击,生成卤离子。
接下来,带负电荷的氮离子攻
击带正电荷的卤代烷碳中心,形成一个中间体,随后中间体上的卤
离子会被吸引至负电荷的氮离子上,从而形成最终产物。
总的来说,吡啶和卤代烷反应的机理是一个经典的亲核取代反
应过程,在碱性条件下进行。
这种反应机理可以通过实验数据和理
论计算进行验证,从而得到更详细和准确的反应机理描述。
当然,
具体反应条件和反应产物也可能会受到反应物的结构和环境的影响,因此在具体研究和应用中,需要综合考虑多种因素来理解和优化吡
啶和卤代烷的反应过程。
二乙胺和吡啶反应机理

二乙胺和吡啶反应机理
二乙胺和吡啶的反应机理可以描述如下:
1. 反应物准备:
二乙胺(C4H11N)和吡啶(C5H5N)是两种常见的有机胺
化合物,它们可以通过合成化学方法制备得到。
2. 胺和吡啶的亲核取代反应:
在反应中,二乙胺作为亲核试剂攻击吡啶分子的部分正电荷。
反应的机理如下:
1) 初始步骤:二乙胺中的亲核氮原子攻击吡啶中相对较电负
的芳环碳原子上的一个卤素(如溴)。
攻击发生后,形成一个部分负电荷的六元环中间体,并且
一个新的共轭体系开始形成。
2) 第二步:六元环中间体负离子发生质子转移,形成一个较
稳定的产物。
在此步骤中,氮原子上的负电荷通过质子转移得到中性减小,而攻击位置碳原子上的负电荷通过质子转移得到负电荷。
3) 第三步:氟离子进攻氮上的负电荷,还原负离子中的负电荷。
氟离子作为非常好的亲核试剂进攻负离子中的负电荷,造
成氮原子上的负电荷从负离子中脱离。
4) 第四步:最后一个质子转移步骤。
由于氮上减少的负电荷需要被平衡,溴离子进攻位置碳上的负电荷并进行质子转移。
通过上述的反应机理,二乙胺和吡啶可以发生取代反应,从而形成新的有机胺化合物。
这个反应可以用于有机合成中的多种应用,包括药物合成、染料合成和材料科学等领域。
吡啶与碘甲烷反应方程式

吡啶与碘甲烷反应方程式吡啶与碘甲烷反应方程式是一种有机化学实验,在化学实验室中十分常见。
这种反应在有机合成中有很广泛的应用,能够在合成有机化合物时发挥重要的作用。
下面我们来分步骤阐述吡啶与碘甲烷反应的方程式。
1. 实验前准备在进行吡啶与碘甲烷反应前,需要进行一些实验前准备工作。
首先应该准备好实验器材,例如三口瓶、冷凝管、鼓风机、分液漏斗等。
其次需要准备好反应试剂,包括吡啶和碘甲烷。
还需要准备好一定量的有机溶剂,作为反应介质。
可以选择的有机溶剂有丙酮、乙醇、甲醇等。
2. 实验步骤吡啶与碘甲烷反应的具体步骤如下:(1)先将吡啶加入三口瓶中。
(2)向瓶中加入一定量的有机溶剂,用溶剂将吡啶完全溶解。
(3)将碘甲烷滴入分液漏斗中,缓慢地添加到吡啶溶液中。
(4)在添加碘甲烷的过程中,不断搅拌三口瓶,并通过鼓风机将反应产生的气体排出三口瓶。
(5)反应完成后,将反应产物通过冷凝管收集下来。
3. 反应方程式吡啶与碘甲烷反应的方程式如下:C5H5N + CH3I → C6H5IN + CH4化学反应中,吡啶和碘甲烷发生化学反应,生成了C6H5IN和甲烷,其中的甲烷通过鼓风机排出瓶外。
这个反应条件比较温和,并且反应产物的生成是十分明显的。
使用该方法进行合成,得到的产物质量相对较高,产率也较大。
在有机合成中,这种反应被广泛应用于制备具有各种功能团的化合物。
例如可以用该反应制备各种吡啶衍生物,如苯基吡啶、取代基吡啶等等。
总之,吡啶与碘甲烷反应方程是有机合成中非常重要的一种反应,它可以用于制备各种吡啶衍生物,具有较高的产率和较高的产物质量。
因此,在进行有机合成实验时,不可忽略这种重要的化学反应。
磷试剂和吡啶反应

磷试剂和吡啶反应
磷试剂和吡啶反应是一种重要的有机化学反应,常用于合成有机化合物中的C-N键和C-C键。
此反应通常涉及到亲核取代和烷基化反应。
磷试剂是一类常用的有机试剂,包括磷酰氯、三甲基膦、三丁基膦等。
它们可作为亲核试剂参与到吡啶上,形成相应的磷酸酯或膦酸盐。
这些中间体能与其他化合物反应,形成新的C-N键和C-C键。
吡啶是一种广泛用于有机合成中的有机化合物,它有丰富的反应性和化学性质。
在磷试剂和吡啶反应中,吡啶可作为亲电试剂参与到反应中,接受磷试剂中的亲核试剂,形成相应的中间体。
这些中间体可进一步参与到其他反应中,例如亚胺化反应和烷基化反应。
总之,磷试剂和吡啶反应是一种重要的有机化学反应,常用于合成具有重要生物活性的有机化合物,例如药物分子和天然产物。
它们的应用范围广泛,为有机合成化学提供了重要的工具和方法。
- 1 -。
吡啶和氧气完全燃烧的化学方程式

吡啶和氧气完全燃烧的化学方程式是一个涉及到化学反应和能量转化的重要问题。
在化学反应中,吡啶和氧气发生完全燃烧将产生一系列产物,并伴随着释放出能量。
下面将深入讨论吡啶和氧气完全燃烧的化学方程式,并分析其中的化学反应过程和能量变化。
一、吡啶和氧气的化学式1. 吡啶的分子式为C5H5N,是一种含有杂环的有机化合物,其分子结构中包含一个含氮的环状结构和苯环。
它是一种无色液体,在化工和药物领域有着广泛的应用。
2. 氧气的分子式为O2,是地球大气中的重要成分之一,也是支持生命活动的必需气体。
氧气的分子结构中包含两个氧原子,是一种常见的二元分子。
二、吡啶和氧气的完全燃烧反应吡啶和氧气发生完全燃烧的化学方程式如下所示:C5H5N + 7 O2 → 5 CO2 + 5 H2O + N2从上述方程式中可以看出,吡啶和氧气发生完全燃烧的反应产物包括二氧化碳、水和氮气。
在这个化学反应过程中,吡啶和氧气分子发生了氧化和还原的反应,生成了不同的化合物,并释放出了大量的能量。
三、吡啶和氧气完全燃烧的化学反应过程1. 反应启动阶段当吡啶和氧气混合在一起时,需要提供一定的能量来启动化学反应。
这个启动阶段需要克服吡啶和氧气之间的化学键的稳定性,以产生初步的反应物中间体。
2. 氧化还原反应吡啶和氧气发生化学反应时,发生了氧化还原反应。
在这个过程中,吡啶中的碳、氢和氮原子与氧气发生了反应,产生了二氧化碳、水和氮气,并释放出能量。
3. 能量释放吡啶和氧气发生完全燃烧的化学反应是放热反应,释放出大量的能量。
这些能量可以用来加热周围的物体、产生光线或推动机械运动。
四、吡啶和氧气完全燃烧的能量变化1. 化学键的断裂在吡啶和氧气发生完全燃烧的化学反应过程中,吡啶和氧气中的化学键发生了断裂。
这个断裂过程吸收了一定的能量,用来克服化学键的稳定性。
2. 新化学键的形成随着反应的进行,新的化学键在生成的二氧化碳、水和氮气分子中形成。
这个形成化学键的过程释放了大量的能量,使得反应能够向前进行并产生热量。
吡啶硫酸铜鉴别反应

吡啶硫酸铜鉴别反应
吡啶硫酸铜鉴别反应是一种常用的化学反应,用于检测物质中是否存在吡啶。
该反应通过吡啶和硫酸铜之间的化学反应来完成。
首先,将待检测物质溶解在适量的溶剂中,通常选择水或有机溶剂。
接下来,加入硫酸铜溶液到溶液中。
如果溶液中存在吡啶,将会发生特定的反应。
在吡啶存在的情况下,会观察到溶液的颜色发生明显变化。
硫酸铜与吡啶反应生成深蓝色络合物,这是吡啶硫酸铜鉴别反应的关键特征。
相反,如果溶液中不存在吡啶,颜色不发生明显变化,即溶液呈现无色或其他颜色。
这一反应是基于吡啶与硫酸铜之间的络合反应。
吡啶中的氮原子能够与硫酸铜中的铜离子形成络合物,从而导致溶液颜色的变化。
这个反应可以快速、直观地鉴别吡啶的存在。
总结来说,吡啶硫酸铜鉴别反应通过观察溶液颜色的变化来确定物质中是否存在吡啶。
这是一种常用的方法,并且在化学实验室和工业中被广泛应用。
吡啶,硫酸铜氧化羟基

吡啶,硫酸铜氧化羟基
吡啶和硫酸铜氧化羟基的化学反应可以制备一种名为吡啶铜(II)的化合物。
在这一反应中,硫酸铜与吡啶发生氧化反应,将吡啶中的氮原子氧化成氧原子,同时铜离子被氧化为铜(II)离子。
这一反应生成的吡啶铜(II)是一种重要的化工材料,它在水产养殖中被广泛用于防治鱼病、控制有害藻生长和消毒工具和食场,主要通过使病原体内的蛋白质变性、沉淀,导致酶失去活性来实现这些功能。
因此,吡啶和硫酸铜的氧化羟基反应是一种具有重要应用价值的反应。
需要注意的是,在进行该反应时,需要确保硫酸铜的安全浓度范围在允许的范围内,避免金属容器的使用,并根据水质肥瘦、水深和水温等因素调整用药量。
此外,应注意与硫酸亚铁合用,以防止硫酸铜对环境和生态造成破坏。
吡啶和酰氯反应机理

吡啶和酰氯反应机理吡啶和酰氯反应啊,这可有点小复杂但又超级有趣呢。
咱先说说吡啶这小家伙吧。
吡啶就像是一个有点小个性的分子,它的氮原子在那儿就像一个小钩子一样。
这个氮原子可是很关键的哦,它身上带着一对孤对电子呢。
这对孤对电子就像是吡啶的小秘密武器,在和酰氯反应的时候可有大作用啦。
再看看酰氯呢,酰氯就像是一个有点霸道的家伙。
它那个氯原子就特别想离开,为啥呢?因为酰氯整体有点不稳定呀。
酰氯的碳原子就像一个小饿狼,特别渴望得到电子呢。
当吡啶和酰氯碰到一起的时候,就像是一场小闹剧开始了。
吡啶的氮原子看到酰氯的碳原子那么渴望电子,就想着,嘿,我这儿有孤对电子呢,我来帮帮你吧。
于是呀,吡啶的氮原子就把自己的孤对电子拿出来,和酰氯的碳原子分享。
这就像是两个人牵起了小手,形成了一种特殊的相互作用。
在这个过程中呢,酰氯的氯原子就觉得,哎呀,我在这儿好像有点多余了,那我就离开吧。
于是氯原子就开开心心地跑走了,就像一个调皮的小孩子跑出去玩了一样。
然后呢,剩下的部分就组合在一起啦。
吡啶和酰氯反应后的产物就这么诞生了。
这个反应在有机化学里就像是一场小魔术,从两个不同的分子,经过这么一系列有趣的过程,就变成了新的东西。
这个反应在很多地方都超级有用呢。
比如说在合成一些药物的时候,就可能用到这个反应。
就像盖房子一样,这个反应就像是一块重要的小砖头,缺了它可能这个房子就盖不起来了呢。
不过呢,这个反应也不是那么好控制的,有时候就像调皮的小动物一样,需要化学家们很小心地去对待,给它们合适的条件,就像给小动物合适的食物和住所一样,这样它们才能乖乖听话,按照化学家的想法去反应,最后生成人们想要的东西。
吡啶和银络合反应机理

吡啶和银络合反应机理吡啶是一种含氮芳香化合物,具有碱性。
银是一种过渡金属,可以形成络合物。
吡啶与银可以发生络合反应,形成吡啶的银络合物。
本文将介绍吡啶和银络合反应的机理。
吡啶的结构中含有一个五元环,其中氮原子带有孤对电子,具有较强的碱性。
银离子是具有单正电荷的金属离子,具有亲电性。
因此,吡啶和银离子可以通过亲核取代反应形成络合物。
吡啶与银络合反应的机理如下:步骤一:吡啶碱性吸引银离子吡啶中的氮原子带有孤对电子,具有亲电性。
银离子具有正电荷,具有亲电性。
在反应开始时,吡啶的氮原子会吸引银离子,形成吡啶与银离子之间的静电作用。
这个步骤可以看作是吡啶的碱性吸引银离子。
步骤二:氮原子给予银一个电子对在吸引银离子的过程中,吡啶的氮原子会将一个电子对给予银离子,形成吡啶的氮原子与银离子的共价键。
这个步骤是吡啶与银离子之间形成配位键的关键步骤。
步骤三:形成吡啶的银络合物在形成共价键之后,吡啶与银离子会进一步形成络合物。
此时,吡啶的氮原子与银离子之间的共价键结构会发生重新排列,形成吡啶与银离子之间的稳定配位键。
这个步骤是吡啶和银的络合反应的最终产物。
综上所述,吡啶和银络合反应的机理可以简要概括为:吡啶的碱性吸引银离子,吡啶的氮原子给予银离子一个电子对,吡啶与银离子形成共价键,再形成吡啶的银络合物。
吡啶和银络合反应在有机合成和配位化学等领域具有广泛应用。
它可以作为一种重要的催化剂,在许多有机反应中发挥重要的作用。
银络合物也可以作为药物和生物分子的载体,用于药物传递和生物活性分子的探针研究等。
因此,深入理解吡啶和银络合反应的机理对于有机化学和生物化学的研究具有重要意义。
总结起来,吡啶和银络合反应的机理是吡啶的碱性吸引银离子,吡啶的氮原子给予银离子一个电子对,吡啶与银离子形成共价键,再形成吡啶的银络合物。
这个反应在有机合成和配位化学等领域应用广泛。
深入理解吡啶和银络合反应的机理对于有机化学和生物化学的研究具有重要意义。
吡啶的亲电取代反应
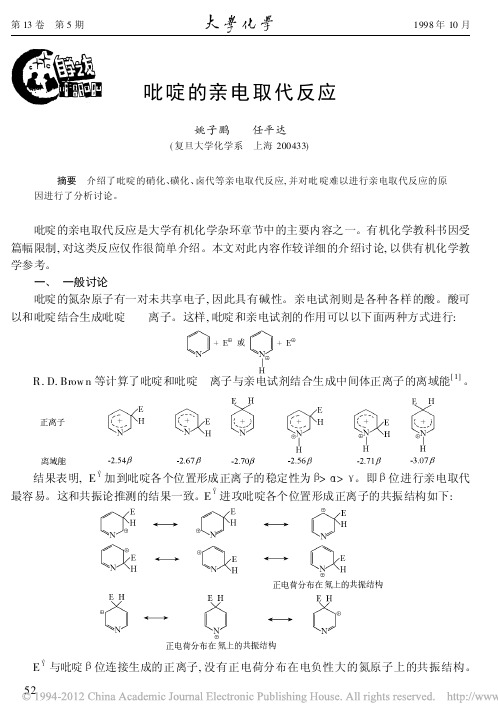
+ A lCl3( 熔融) C l2
1B
2
10%
40%
氯气通入吡啶和三氯化铝的混合物, 却得不到氯代产物。
+ Cl2
AlCl3
这一比较令人奇怪的反应, 其可能的机理如下:
+ A lCl3
和氯代反应不同, 溴代反应已找到了较合适的条件, 并得到较高产率的 3- 溴吡啶[ 6] 。 55
+ Br2
66% 发烟 H2SO4 130 e
+ 浓 HN O 3/ 浓 H2SO 4
300 e 1天
6%
+ NaN O3/ 发烟 H2SO4
300 e 1天
4. 5%
ห้องสมุดไป่ตู้
+ KN O 3/ 发烟 H2SO 4
300 e 1天
15%
+ KN O 3, H NO 3, H 2S O4, Fe
300 e 1天
22%
当吡啶环上有推电子取代基时, 硝化反应产率较好。若取代基是甲基, 则至少要有两个甲
第 13 卷 第 5 期
1998 年 10 月
吡啶的亲电取代反应
姚子鹏 任平达
( 复旦大学化学系 上海 200433)
摘要 介绍了吡啶的硝化、磺化、卤代等亲电取代反应, 并对吡 啶难以进行亲电取代反应的原 因进行了分析讨论。
吡啶的亲电取代反应是大学有机化学杂环章节中的主要内容之一。有机化学教科书因受 篇幅限制, 对这类反应仅作很简单介绍。本文对此内容作较详细的介绍讨论, 以供有机化学教 学参考。
物[ Cp2T i( P- ClC6H4O) 2] 和四丁基氟化铵( T BA F) 的存在下, 将聚甲氢硅氧烷制成了氢硅烷 基衍生物。产 物用 氢氧化钠或 T BAF 处理后得到游离的乳醇。发明者 认为, Cp2T iH 起 催化剂 作用, 内酯先 插入 T i) H 键形 成 一种环中氧与钛配位的烷基氧化物, 然后与 硅烷分 子参与 R- 键复分 解, 生 成钛的 氢化物 和硅烷 基化的 乳醇。
吡啶和醋酸反应方程式及现象

吡啶和醋酸反应方程式及现象
摘要:
一、反应方程式
二、反应现象
三、反应影响因素
四、应用领域
正文:
一、反应方程式
吡啶和醋酸反应的化学方程式为:C6H5Py + CH3COOH →
C6H5PyCOOCH3 + H2O。
其中,C6H5Py 代表吡啶,CH3COOH 代表醋酸,C6H5PyCOOCH3 代表醋酸吡啶酯,H2O 代表水。
二、反应现象
1.反应速度:吡啶和醋酸反应速度较快,在常温下即可迅速发生反应。
2.反应温度变化:反应过程中,体系的温度会略有升高。
3.反应产物外观和性质:反应产物醋酸吡啶酯为无色至微黄色液体,具有特有的气味。
三、反应影响因素
1.反应物浓度:反应物浓度对反应速度有较大影响,浓度越高,反应速度越快。
2.反应温度:反应温度对反应速度和转化率都有影响,适当提高温度可以加快反应速度,但过高的温度会导致副反应的产生。
3.催化剂:催化剂可以降低反应活化能,加快反应速度,常用的催化剂有硫酸、氢氧化钠等。
四、应用领域
1.药物合成:醋酸吡啶酯在药物合成中有着广泛的应用,如合成抗疟疾药物青蒿素等。
2.农业化学:醋酸吡啶酯可以用作农药中的活性成分,具有杀虫、杀菌作用。
3.材料科学:醋酸吡啶酯可用于合成高分子材料,如聚醋酸吡啶等。
三氯化铝和吡啶的反应

三氯化铝和吡啶的反应三氯化铝与吡啶的反应是一种重要的化学过程,反应的遵循的化学方程式为:$Pyridine+AlCl_3\rightarrow[AlCl_2(Pyridine)_2]+HCl$三氯化铝是一种稳定的化合物,在普通温度下具有四面体结构,可以与大多数碱地和氨基酸类物质发生反应。
吡啶是一种宽概的有机化合物,可以通过烷基化反应来合成,具有一系列特殊的物理和化学性质。
吡啶的分子结构包含一个由六面体构成的碳中心,由六个氮原子及其地方性质的电子组成氮桥形成的四个位点附近,具有三个可以与其他分子产生反应的官能团,其中两个是烯烃式保护基,另一个是酰胺基。
由于其具有很强的地方性和介质性,因此吡啶对众多化学反应具有显著的活性,在发生反应时有强烈的吸引力。
三氯化铝与吡啶的反应是一种简单的活性取代反应过程,三氯化铝的三个氯原子可与吡啶的三个反应点发生反应。
在反应的过程中,三氯化铝将取代吡啶的三个反应点,从而产生二价铝离子。
有三种可能的物理机制。
第一种,可能是因为氯离子对吡啶上的电子密度具有猛烈的吸引力,所以在反应开始时,三个氯离子会紧贴在吡啶的三个反应点上,然后交换电子,使形成位置上和官能团上的原子发生转换;第二种可能是,在反应过程中,氯离子中的电子会持续排斥吡啶的电子,从而导致吡啶的电子原子间的左右式变换;第三种可能是,水分子对吡啶的官能团进行攻击,这样就可以形成一个桥接环,然后再由氯离子排斥吡啶上的电子,使得合成物产生取代反应。
无论是什么物理机制,最终结果都是一样的,即三氯化铝可以与吡啶发生活性取代反应,生成相应的二价铝离子产物,同时放出一个氢离子。
三氯化铝与吡啶的反应是一种重要的化学过程,经常用于法医学中的鉴定,检验实验和制药方面的反应,如果两种基础的物质都准备了就可以尝试在实验室中进行这种反应。
反应条件及步骤也非常简单,正确理解这种反应可以为更多的化学实验和分子研究打下基础,它可以为后续反应提供有价值的信息,因此了解这种反应及其机制非常重要。
吡啶作为催化剂的催化机理

吡啶作为催化剂的催化机理
吡啶是一种常用的有机碱,广泛应用于有机合成、医药和材料科学等领域。
吡啶还可以作为催化剂,参与有机反应,促进反应速率和选择性。
吡啶催化机理主要涉及以下几个方面:
1. 物化作用:吡啶可以和反应物形成氢键或范德华力等物化作用,促进反应物之间的接近和反应活性中心的形成。
2. 亲核性:吡啶分子中含有孤对电子,可以作为亲核试剂参与反应,攻击反应物中的电子缺陷,形成新的化学键。
3. 离子化作用:吡啶可以促进反应物中的离子化反应,例如促进烷基化反应中碳氢键的断裂和离子的形成。
4. 氧化还原作用:吡啶可以参与还原和氧化反应,例如参与氧化亚硝酸钠和还原苯酚等反应。
总之,吡啶作为催化剂的催化机理涉及多方面的物化作用和化学反应,具有较高的催化活性和选择性,是有机合成中常用的催化剂之一。
- 1 -。
吡咯和吡啶的亲电取代反应

吡咯和吡啶的亲电取代反应
吡咯和吡啶都是含有杂环氮原子的芳香族化合物,它们可以进行亲电取代反应。
在亲电取代反应中,一个亲电试剂(通常是卤代烃、酰卤、硝基化合物等)攻击芳香环上的π电子,形成一个新的化学键。
这种反应可以在不同位置发生,产生不同的产物。
例如,吡咯的N-1位置和N-2位置都是活泼的亲电位点,可以被许多亲电试剂攻击,如卤代烃、芳香醛、芳香酸等。
而吡啶的C-2、C-4、C-6位置是较活泼的亲电位点,可以被一些强亲电试剂如酰卤、硝基化合物等攻击。
需要注意的是,在取代反应中,通常会出现混合取代产物,并且不同位点的反应速率和产物选择性也可能不同。
因此,在实际应用中需要对反应条件进行优化,以得到高产率和高选择性的产物。
吡啶作为催化剂的催化机理

吡啶作为催化剂的催化机理
吡啶作为催化剂可以分为两种机理,一种是亲核催化机理,另一种是Lewis酸催化机理。
亲核催化机理是指吡啶作为一个亲核试剂,可以与反应物中的电子亲核中心进行反应,形成化合物的中间体,然后这个中间体再被其他反应物攻击,继续进行反应。
这种机理通常被用于羟化反应、烷基化反应和醛基化反应等。
Lewis酸催化机理是指吡啶作为一个Lewis酸,可以形成与反应物中的电子亲核中心之间的络合物,使它们更容易进行反应。
这种机理通常被用于氧化反应和酰化反应等。
总的来说,吡啶作为催化剂的催化机理是通过与反应物中的电子亲核中心或络合物发生反应来加速化学反应的进行。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
吡啶的化学反应
吡啶(pyridine)是一种含有六个碳原子和一个氮原子的杂环化合物,属于芳香族化合物。
由于其碱性和很好的溶解性,吡啶在有机合成中广泛应用于多种化学反应中。
以下是一些常见的吡啶的化学反应:
1. 氧化反应:
-吡啶可以被常见的氧化剂(如高锰酸钾)氧化为对应的吡啶-N-氧化物。
-艾森鲍姆氧化反应可将吡啶氧化成吡啶-N-氧化物,然后进一步氧化为吡啶-N--二氧化物。
2. 反应中的亲电取代:
-吡啶可以进行酰基化反应,以酰氯或酸酐为亲电试剂,生成吡啶酰化物。
-烷基化反应中,吡啶与烷基卤化物或甲酸酯反应,生成吡啶烷基化物。
3. 反应中的亲核取代:
-脱卤反应:吡啶可以与卤代烷烃反应,生成对应的亲核取代产物。
-羟基化反应:吡啶可以与碱式过氧化氢(如叔丁基过氧化氢)反应,生成相应的吡啶-N-氧化物。
4. 缩合反应:
-吡啶可以与醛、酮等进行亲核加成,发生缩合反应,生成亚胺化合物。
5. 重排反应:
-吡啶可以发生烯丙基重排,生成具有烯丙基结构的产物。
这些只是吡啶的一些常见化学反应,吡啶在有机合成中还有许多其他的应用和反应。
需要根据具体的反应条件和所需目标化合物来选择适当的反应方法。
