分子热运动能量和速度的统要点
分子热运动物理笔记

分子热运动物理笔记一、分子动理论的基本内容1. 物质是由大量分子组成的:物质是由无数微小的粒子,即分子所组成的。
这些分子以极小的距离相互间隔开,形成物质的连续体。
2. 分子在永不停息地做无规则运动:无论物质处于固态、液态还是气态,其内部的分子都在不断地、无规则地运动着。
这种运动是随机的,不受外界条件的直接影响。
3. 分子间存在着相互作用的引力和斥力:分子间的引力和斥力同时存在,但它们的大小随分子间距离的变化而变化。
当分子间距离较小时,斥力大于引力,表现为斥力;当分子间距离稍大时,引力大于斥力,表现为引力。
二、分子热运动的特点1. 无规则性:分子热运动的方向和速度大小都是随机的,没有固定的规律。
2. 统计规律性:虽然单个分子的运动是随机的,但大量分子的集体行为却表现出一定的统计规律性。
例如,温度是分子平均动能的宏观表现,温度越高,分子的平均动能越大。
3. 扩散现象:扩散是分子热运动的一个重要表现。
当两种物质相互接触时,由于分子的无规则运动,它们会相互渗入对方,使彼此的边界变得模糊。
扩散现象在日常生活和工业生产中都有广泛的应用。
三、分子热运动的定量描述1. 分子速度:描述分子运动的快慢,用速度v表示。
2. 分子速率:描述分子运动的快慢,用速率v表示,v = |v|。
3. 温度与分子平均动能:温度是分子平均动能的宏观表现,用T表示。
温度越高,分子的平均动能越大。
4. 分子力:描述分子间相互作用的力,用F表示。
分子力的大小与分子间的距离有关,随距离的增大而减小。
四、分子热运动与热力学定律1. 热力学第一定律:热量可以从一个物体传递到另一个物体,也可以与机械能或其他能量互相转换,但是在转换过程中,能量的总值保持不变。
2. 热力学第二定律:热量不可能自发地从低温物体传递到高温物体而不产生其他影响;或者不可能从单一热源取热使之完全转换为有用的功而不产生其他影响;或者不可逆热力过程中熵的微增量总是大于零。
分子热运动和统计规律

商店的百分数
f i (Ni N ) 1,归一化条件
分布函数和平均值
例: 我们以人的身高为例,来引入分布函数的概念。
设 N 为总人数,dN(h)为身高在 h--h+dh 间 的人数。显然
dN (h) N
令 f(h)=dN(h)/Ndh,则
f (h)dh 1
我们把 f(h)称为归一化分布函数。
的统计规律,即统计性。 例如: 在平衡态下,气体分子的空间分布(密度)
是均匀的。(分子运动是永恒的) 可作假设:气体分子向各个方向运动的机
会是均等的,或者说沿各个方向运动的平均分 子数应相等且分子速度在各个方向的分量的统 计平均值也相等。
对大量分子体系的热平衡态,它是成立的。
分子热运动的基本特征
宏观量:表征大量分子的整体特征的量。如温度、 压强、热容等,是实验中能测得的量。
微观量:表征大量分子的整体中个别分子特征的物 理量。如某个分子的质量、速度、能量等, 在现代实验条件下是不能直接测得的量。
(3)统计方法 分子热运动具有无序性与统计性,与机械
运动有本质的区别,故不能简单应用力学定律 来解决分子热运动问题。必须兼顾两种特征, 应用统计方法。
分子热运动的基本特征
统计方法:
1.分子热运动的基本特征
分子热运动的基本特征是永恒的运动与频繁 的相互碰撞。它与机械运动有本质的区别,故不 能简单应用力学定律来解决分子热运动问题。
(1)无序性 某个分子的运动,是杂乱无章的,无序的;
各个分子之间的运动也不相同,即无序性;这正 是热运动与机械运动的本质区别。
分子热运动的基本特征
(2)统计性 但从大量分子的整体的角度看,存在一定
f(h)表征在单位高度内,身高为 h 的人数占总 人数的比率。
初中物理分子热运动知识点整理

初中物理分子热运动知识点整理初中物理分子热运动知识点整理分子是运动的。
而不同的物质互相接触时彼此进入对方的现象叫做扩散。
扩散不仅发生在气体之间,也可以发生在液体和固体之间。
以下是店铺整理的初中物理分子热运动知识点整理,希望对大家有所帮助。
一、分子热运动分子运动论的内容是:(1)物质由分子组成;(2)一切物体的分子都永不停息地做无规则运动。
(3)分子间存在相互作用的引力和斥力。
扩散:不同物质相互接触,彼此进入对方现象。
扩散现象说明:一切物质的分子都在不停地做无规则的运动。
热运动:分子的运动跟温度有关,分子的无规则运动叫热运动。
温度越高,分子的热运动越剧烈。
分子间的作用力:分子间有引力;引力使固体、液体保持一定的体积。
分子间有斥力,分子间的斥力使分子已离得很近的固体、液体很难进一步被压缩。
固体、液体压缩时分子间表现为斥力大于引力。
固体很难拉长是分子间表现为引力大于斥力。
二、内能内能:物体内部所有分子热运动的动能和分子势能的总和叫内能。
物体的内能与温度和质量有关:物体的温度越高,分子运动速度越快,内能就越大。
一切物体在任何情况下都具有内能。
改变物体的内能两种方法:做功和热传递,这两种方法对改变物体的内能是等效的。
1、热传递:温度不同的`物体相互接触,低温的物体温度升高,高温的物体温度降低,这个过程叫热传递。
发生热传递时,高温物体内能减少,低温物体内能增加。
热量:在热传递过程中,传递的内能的多少叫热量(物体含有多少热量的说法是错误的)。
单位:J。
2、做功:(1)对物体做功,物体的内能增加;物体对外做功,本身的内能会减少。
温室效应:太阳把能量辐射到地表,地表受热也会产生辐射,向外传递热量,大气中的二氧化碳阻碍这种辐射,地表的温度会维持在一个相对稳定的水平,这就是温室效应。
大量使用化石燃料、砍伐森林,加剧了温室效应。
所有能量的单位都是:焦耳。
三、比热容比热容(c):单位质量的某种物质温度升高(或降低)1℃,吸收(或放出)的热量叫做这种物质的比热。
精灵般的分子运动认识化学分子的热运动

精灵般的分子运动认识化学分子的热运动精灵般的分子运动——认识化学分子的热运动化学分子是构成物质的最基本单位,它们在空间中不断地热运动,这种热运动正是物质的特性之一。
本文将从分子的热运动速度、分子的碰撞和能量转移等方面,详细介绍精灵般的分子运动,帮助读者更好地理解化学分子的热现象。
一、分子的自由度与热运动速度分子的自由度指的是分子在空间中的运动方式,包括平动、转动和振动三种形式。
这些自由度决定了分子的热运动速度。
1. 平动:分子的平动是指分子整体在空间中的移动,类似于一个人在空旷的地方行走。
平动自由度越大,分子的热运动速度越快。
一般来说,气体分子的平动速度最快,液体次之,固体较慢。
2. 转动:分子的转动是指分子围绕自身的轴心旋转,类似于一个人原地打转。
转动自由度的增加会使分子热运动速度略有增加,但相比于平动速度,转动速度较慢。
3. 振动:分子的振动是指分子内原子之间的相对位置不断变化,类似于一个人做踢腿动作。
振动自由度的增加会使分子的热运动速度稍有增加。
总体来说,分子的热运动速度由分子的质量和分子的自由度共同决定,同时也受到温度的影响。
二、分子间的碰撞与热运动在空间中,分子不断地相互碰撞,这种碰撞是分子热运动的重要表现形式。
分子间的碰撞不仅使分子的运动状态发生变化,还会引发能量的转移。
1. 弹性碰撞:分子间的碰撞通常是弹性碰撞,即碰撞前后分子之间的动能总和守恒。
在碰撞过程中,分子之间会交换动能,速度较快的分子可能会传递动能给速度较慢的分子。
2. 碰撞频率:分子的碰撞频率取决于分子的浓度和速度。
浓度越高、速度越快,分子的碰撞频率就越高。
3. Coulomb力:在分子间的碰撞中,还存在着Coulomb力的影响。
Coulomb力是带电粒子间相互作用的力,它会在分子碰撞过程中产生引力或斥力,影响分子碰撞的后续运动。
通过分子间的碰撞,能量可以从一个分子传递到另一个分子,使物质的温度发生变化。
三、能量转移与分子热运动分子的热运动与能量密切相关,能量的转移是支撑分子热运动的重要基础。
分子热运动

分子热运动引言分子热运动是指分子在物质内部以及物质之间以高速无规则的方式运动的现象。
分子的热运动是所有物质在宏观上呈现出的一些独特的性质和特征的基础。
本文将从分子运动的原理、特性和影响等方面介绍分子热运动的基本概念。
1. 分子运动的原理分子热运动的原理可以从分子动理论的角度来解释。
根据分子动理论,物质是由大量微小的分子组成的,分子又由更小的原子组成。
这些分子具有质量和速度,它们通过碰撞相互作用。
在没有外部作用力的情况下,分子的运动是无规则的和随机的。
分子热运动的速度和方向是由能量的分配和碰撞的影响所决定的。
分子在热运动过程中,会发生弹性碰撞,能量会从一个分子传递给另一个分子,导致速度和方向的变化。
因此,分子的热运动是一个动态平衡的过程。
2. 分子热运动的特性分子热运动具有以下几个特性:2.1 高速运动分子在热运动过程中具有较高的速度,其速度范围从数百米/秒到数千米/秒不等,这取决于物质的性质和温度。
高速运动和碰撞导致了物质的扩散和混合。
2.2 无规则运动分子的运动是无规则、随机的,没有特定的方向。
由于分子之间的碰撞和运动方向的变化,物质在宏观上呈现出的性质是统计平均的,而不是具体的。
2.3 碰撞效应分子之间的碰撞是分子热运动的重要特性之一。
分子之间的碰撞会导致能量的转移和速度的变化。
碰撞效应决定了物质的热传导、扩散和与外界环境的交互等过程。
2.4 热平衡分子热运动是一个动态平衡的过程。
在物质的热平衡状态下,分子的平均能量保持不变,并且处于稳定的温度。
3. 分子热运动的影响分子热运动对物质的性质和现象产生了广泛的影响,主要包括以下几个方面:3.1 温度分子热运动的表现之一是温度。
温度是分子运动速度和能量的度量,与分子的平均动能有关。
分子热运动的速度增加会导致温度的升高,而能量的减少则会导致温度的降低。
3.2 热容量热容量是物质吸收或释放热量的能力的度量。
分子的热运动与物质的热容量密切相关。
在分子热运动过程中,吸收或释放的热量与分子速度和碰撞有关。
热学-统计物理3 第3章 气体分子热运动速率和能量的统计分布律
v v pv v 2
讨论
麦克斯韦速率分布中最概然速率 vp 的概念
下面哪种表述正确?
(A) vp 是气体分子中大部分分子所具有的速率. (B) vp 是速率最大的速度值. (C) vp 是麦克斯韦速率分布函数的最大值.
(D) 速率大小与最概然速率相近的气体分子的比 率最大.
例1 计算在 27 C 时,氢气和氧气分子的方均
M
3.方均根速率 v2
v2
N
0
v2dN N
0
v2Nf N
(v)dv
o
v
v2 v2 f (v)dv 4 ( m )3 2 e mv2 2kT v4dv
0
2 kT
0
v4ev2 dv 3
0
8 5
v2 3kT m
v2 3kT 3RT
2kT
v
麦克斯韦速率分布函数的物理意义: f (v) dNv
Nd v
既反映理想气体在热动平衡条件下,分布在速率 v 附近单
位速率区间内的分子数占总分子数的百分比,又表示任意
一分子的速率出现在 v附近单位速率区间内的概率。
如果以速率为横坐标轴,速率分布函数为纵坐标轴,画 出的一条表示f(v) —v之间关系的曲线,称为气体分子的麦 克斯韦速率分布曲线。 ,它形象地描绘出气体分子按速率 分布的情况。
大量分子的速率的算术平均值叫做分子的平均速率.
v
vNf (v)dv
0
vf (v)dv
v 4 (
m
)3 e2 mv2 2kT v2dv
N
0
0
第三章 气体分子热运动速率和能量的统计分布规律

Ndv
2kT
1.麦克斯韦速率分布函数f()的物理意义
由 dN f (υ)dυ N
f (υ) dN Ndυ
f()表示:在速率附近的单位速率区间内的分子数占总 分子数的百分比。或分子速率出现在附近的单位速率区间内
的概率概率密度。
f (υ)dυ dN
N
—在速率区间 ~ +d 内的分子数占
例 (1) n f()d 的物理意义是什么?(n是分子的数密度)
(2) 写出速率不大于最可几速率p的分子数占总分子数
的百分比。
解 nf (υ)dυ Nf (υ)dυ dN
V
V
n f()d —表示单位体积中,速率在 ~+d 内的分子数。
(2) 写出速率不大于最可几速率p的分子数占总分子数的
dN v y N
g(y )dy
dNvz N
g(z )dz
(2)由独立概率相乘原理,粒子出现在x ~x+dx,y ~y+dy,z ~z+dz的
概率为:
dNv N
g(x )g(y )g(z )dxdydz
F • dxdydz
F就是速度分布函数
(3)由于粒子在任何方向上运动的概率相等,所以F应该与速度的方向 无关,应该是速度的大小的函数。
dNv N
1
3 3
e dv dv dv (vx2 vy2 vz2 ) / 2 xyz
转化成球坐标:
dvxdvydvz v2 sin dddv
vx2
v
2 y
vz2
v2
麦克斯韦速度分布:dNv 1 v2ev2 / 2 sin dddv N 3 3
分子运动与热能

分子运动与热能热能是物体分子运动所具有的能量。
分子运动是指物质微观粒子——分子的热运动。
分子运动的特性和规律对理解热现象和热能转化至关重要。
本文将以分子运动的角度来探讨和解释热能的产生和传递。
一、分子运动的基本特性1. 分子运动的速度:根据气体动理论,分子速度与温度成正比。
在给定温度下,分子的速度服从马克思韦尔分布,即速度分布为高斯分布。
2. 分子运动的路径:分子在运动中呈现随机运动、无规则碰撞的特性。
分子路径的无序性导致能量在物质中的传递和分布。
3. 分子碰撞:分子通过相互碰撞来传递能量。
在碰撞过程中,能量可以从速度更高的分子传递给速度较低的分子,实现能量的平衡。
4. 分子自由度:分子在空间中具有多种运动方式,如平动、转动和振动。
不同自由度的运动会影响分子的能量和热量的传递。
二、分子运动与热能传递1. 热平衡与热传导:当两个物体处于热平衡时,它们之间的热能不再传递。
而热传导是指物体间由于温度差异造成的热能传递。
2. 分子碰撞与热能传递:热能通过分子间的碰撞进行传递。
当两个物体温度不同,分子速度不同,碰撞会使能量从高温物体传递到低温物体。
这种能量传递方式称为热传导。
3. 物质热传导性质:物质的热传导性质与分子运动密切相关。
导热性能好的物质,其分子间的碰撞频率高,能量传递迅速,导热系数较大。
4. 热容与分子运动:物体的热容与其分子的平动能量和振动能量有关。
热容越大,物体吸收或释放的热能越大,热传递能力越强。
三、热力学定律解释1. 热力学第一定律:热力学第一定律给出了能量守恒的原则。
根据这一定律,物体的内能变化等于吸收的热量减去对外界做功的量,即ΔU = Q - W。
2. 热力学第二定律:热力学第二定律阐述了热量自然传递的方向。
根据这一定律,热量不会自动从低温物体传递到高温物体,而是从高温物体传递到低温物体,熵增加。
3. 熵与分子运动:熵是物体无序程度的度量,与分子的运动状态有关。
当物体的熵增加时,分子的运动方式更随机,热能更分散。
热力学-3.气体分子动理论速率与能量

1.59 RT M
一般用于计算分子运动的平均距离;
同理,方均根速率
v2 v2 f (v)dv
3kT
3RT 1.73 RT
0
m
M
M
方均根速率用来计算分子平均动能。
最概然速率
2kT 2RT
RT
vp
m
1.41
M
M
最概然速率用在讨论分子速率分布。
f(v)
O
vp v v2
•在气体动理论方面,他提出气体分子按 速率分布的统计规律。
1。由于分子受到频繁的碰撞,每个分子热运动的速率是变化的, 要某一分子具有多大的运动速率没有意义,所以只能估计在某 个速率间隔内出现的概率;
2。哪怕是相同的速率间隔,但是不同的速率附近,其概率是不 等的。
速率接近为0的可能性很小,速率非常大的可能性也很小, 而居中速率的可能性则较大。
f (v) dN Ndv
速率分布函数
理解分布函数的几个要点: 1.条件:一定温度(平衡态)和确定的气体系统,T和m是一定的;
2.范围:(速率v附近的)单位速率间隔,所以要除以dv; 3.数学形式:(分子数的)比例,局域分子数与总分子数之比。
f (v)dv dN N
N v1 v2
v2
f (v)dv
第三章 气体分子热运动 速率和能量的统计分布律
内容回顾
第一章 平衡态和温度 第二章 压强和温度的微观本质
平均效果
气体分子按速率分布的统计规律最早是由麦克斯韦于
1859年在概率论的基础上导出的,1877年玻耳兹曼由经典统 计力学中导出,1920年斯特恩从实验中证实了麦克斯韦分子 按速率分布的统计规律。
分子热运动物理

分子热运动物理引言:分子热运动是物质微观粒子(分子或原子)在温度作用下的无规则运动。
热运动是物质热力学性质的基础之一,对于理解物质的物理和化学性质具有重要意义。
本文将从分子热运动的原理、分子的运动状态、分子热运动的性质以及分子热运动在物理学中的应用等方面进行阐述。
一、分子热运动的原理分子热运动的原理可以从统计力学的角度来解释。
根据统计力学理论,分子热运动是由于分子间相互作用力的不断碰撞和相互作用所引起的。
分子间的相互作用力包括吸引力和排斥力,这些力使得分子在空间中不断地做无规则的运动。
二、分子的运动状态分子的运动状态可以用速度和能量来描述。
分子的速度大小和方向是随机的,符合统计分布规律。
根据分子平均动能定理,分子的平均动能与温度成正比,即温度越高,分子的平均动能越大。
分子的能量分布服从麦克斯韦速度分布定律,即在给定的温度下,分子速度的分布呈高斯分布。
三、分子热运动的性质1. 分子热运动是无规则的,具有随机性。
分子在热运动中无规律地改变运动方向和速度,呈现出无序的状态。
2. 分子热运动具有碰撞性。
分子之间的相互作用力使得它们在热运动中不断碰撞,碰撞过程中能量的转移和转换也在不断进行。
3. 分子热运动具有统计性。
大量的分子在热运动中呈现出统计规律,可以通过统计方法来研究和描述分子热运动的性质。
四、分子热运动的应用1. 理论物理学中,分子热运动是研究物质性质的基础之一。
通过研究分子热运动的性质,可以揭示物质的热力学性质,如热容、热膨胀等。
2. 物理化学中,分子热运动对于反应速率和化学平衡的研究具有重要意义。
分子的热运动使得分子之间发生碰撞,进而影响化学反应的速率和平衡位置。
3. 材料科学中,分子热运动对于材料的热传导和导电性能起着重要作用。
分子热运动使得热能和电能在材料中传导,影响材料的热导率和电导率。
4. 生物物理学中,分子热运动对于生物大分子的结构和功能具有重要影响。
分子热运动使得生物大分子在空间中不断摆动和旋转,影响其结构的稳定性和功能的发挥。
第3章 气体分子热运动速率和能量的统计分布

v vxi vy j vzk
速度空间体积元
速率分布是速度矢量大小被限制在一定区间
满足此条件的速度矢量其端点位于半径为 v,厚度为dv的球壳内
球壳体积为
17
用球壳体积
代替
并注意 v2 vx2 v2y vz2 得麦克斯韦速率分布
dN 4π(
n n 1 n
•分子数∆n 越大,涨落的百分数就越小,涨落现象越不显著。
• 麦克斯韦速率分布律只对大量分子组成的体系才成立。 9
三、用麦克斯韦速率分布函数求平均值
平均速率(算术平均值)
离散型
v v1N1 v2N2 viNi vnNn i viNi
N
N
连续型
N
v 0 vdN 0 vNf (v)dv
•当R 以一定的角速度转动,铋分子由S3到达G需用一段时间。 • 这段时间内R己转过一角度,铋分子不再沉积在板上P处。 • 不同速率的分子将沉积在不同的地方.速率大的分子由S3到G所需
的时间短,沉积在距P较近的地方,速率小的分子沉积在距P较远 的地方。
34
•设速率为 v的分子沉积在P’处以s 表示弧PP’的长度。 表示R的
N1, N2,…, Ni, …
小球在槽内的分配情况,称为一种分布。
总数足够大,槽内的小球的数目与小球总数之比
..........
.. . .
.......
. . .
. . .
. . .
. . .
. . .
. . .
. . .
. . .
. . .
. .
. . .
.
. . .
.
. . .
气体分子热运动速率和能量的统计分布律

f (v)
dS
o v v dv
物理意义
表示在温度为 T 的平衡
状态下,速率在 v 附近单位
速率区间 的分子数占总数的
v 百分比 .
热学
3
dN f (v)dv dS N
表示速率在 v v dv
区间的分子数占总分子数的 百分比 .
归一化条件
N
0
dN N
0
f
(v)dv
1
f (v)
速率位于 v v dv 内分子数
热学
11
麦克斯韦(James Clerk
Maxwell 1831-1879)
1861年选为伦敦皇家学会会员。1865年春辞去教职回到家乡系统
地总结他的关于电磁学的研究成果,完成了电磁场理论的经典巨著
《论电和磁》,并于1873年出版,1871年受聘为剑桥大学新设立
的卡文迪什试验物理学教授,负责筹建著名的卡文迪什实验室,
麦克斯韦是19世纪伟大的英国物理学家、数 学家。1831年11月13日生于苏格兰的爱丁堡, 自幼聪颖,父亲是个知识渊博的律师,使麦克斯 韦从小受到良好的教育。10岁时进入爱丁堡中学 学习,14岁就在爱丁堡皇家学会会刊上发表了一 篇关于二次曲线作图问题的论文,已显露出出众 的才华。1847年进入爱丁堡大学学习数学和物 理。1850年转入剑桥大学三一学院数学系学习, 1854年以第二名的成绩获史密斯奖学金,毕业 留校任职两年。1856年在苏格兰阿伯丁的马里 沙耳任自然哲学教授。1860年到伦敦国王学院 任自然哲学和天文学教授。
vp
2kT m
2 RT M
v
8kT πm
v2 3kT m
热学
9
f (v)
初三物理分子热运动知识讲解

分子热运动【要点梳理】要点一、物质的构成常见的物质是由极其微小的粒子——分子、原子构成的。
要点诠释:分子、原子的体积很小,用肉眼和光学显微镜都分辨不出它们。
不过,电子显微镜可以观察到分子、原子。
要点二、分子热运动【高清课堂《分子热运动、内能》分子动理论】1、扩散:不同的物质在互相接触时彼此进入对方的现象,叫扩散。
2、影响扩散快慢的主要因素:(1)物质的温度:温度越高,扩散越快。
(2)物质的种类:气体之间的扩散最快,其次是液体,固体之间的扩散最慢。
3、扩散现象说明了:(1)一切物质的分子都在不停地做无规则运动。
(2)分子之间有间隙。
4、分子的热运动:一切物质的分子都在不停地做无规则的运动,这种无规则运动叫做分子的热运动。
要点诠释:1、扩散现象只能发生在不同的物质之间,同种物质间是不能发生扩散现象的。
例如:冷热水混合,虽然冷水分子和热水分子都能彼此进入对方,但不是扩散现象。
2、扩散现象是反映分子的无规则运动的。
而灰尘颗粒、大雾中的微粒及烟尘中的微粒等肉眼能观察到的分子聚合体在外力下的机械运动,都不是扩散现象。
3、扩散是人能够直接观察或感知到的宏观现象;分子的无规则运动是微观现象,人无法直接观察。
因此不能说“观察到分子无规则运动”,或“分子的扩散现象”。
4、一切物质的分子都在不停地做无规则的运动,这种无规则运动叫做分子的热运动。
温度的高低是物体内分子热运动剧烈程度的标志。
温度越高,分子热运动越剧烈,扩散越快。
例如,炒菜时,老远就能闻到菜的香味,当菜冷下来后,香味就逐渐减少了。
要点三、分子间的作用力1、分子之间存在斥力:当固体被压缩时,分子间的距离变小,作用力表现为斥力。
2、分子之间存在引力:当固体被拉伸时,分子间的距离变大,作用力表现为引力。
3、分子动理论的基本观点:(1)常见物质是由大量的分子、原子构成的;(2)物质内的分子在不停地做热运动;(3)分子之间存在引力和斥力。
要点诠释:1、分子之间的引力和斥力同时存在,只是对外表现不同。
分子热运动、内能知识点总结

一、基础知识:分子热运动篇1、物质的组成(1)物质是由分子、原子组成的。
(2)分子非常小,不借助仪器,肉眼是看不见的,如果把分子看成一个个的小圆球(物理模型法),那么一般一个分子的直径大约是10-10m,因此一个物体是由数量巨大的分子组成的。
(3)分子很小,它的直径的数量级是10-10m,1cm3的空气中大约有2.7×1019个分子。
2、扩散现象(1)定义:不同的物质相互接触时,彼此进入对方的现象叫做扩散.(2)扩散现象表明:一切物质的分子都在不停的做无规则运动,间接证明分子之间有间隙。
注意:不同的物质一定要相互接触才能发生扩散,必须是两种物质相互进入彼此。
扩散现象是不同物质的分子运动造成的,要注意和微小颗粒状物体运动的区别。
3、分子热运动(1)定义:一切物质的分子都在不停的做无规则运动,这种无规则的分子运动叫做分子的热运动(2)影响分子热运动的影响因素:分子的热运动与温度有关,温度越高,分子热运动越剧烈,分子扩散的就越快。
4、分子间的作用力(1)固体和液体中的分子之所以不会分散开,而总是聚合在一起,是因为分子间存在引力的作用,从而使固体和液体能保持一定的体积。
由于分子间也存在斥力作用,因此固体与液体很难被压缩。
(2)分子间的引力和斥力总是同时存在的。
它们都随分子间距离的增大而减小,随分子间距离的减小而增大,只是斥力变化的比引力要快。
当分子间距离很小时,作用力表现为斥力;当分子间作用力稍大时,作用力表现为引力。
如果分子间距很远,作用力就变得十分微弱,可以忽略。
内能篇1、内能(1)宏观物体的能表现为机械能,是物体外在的能量;微观物体的能表现为内能,是物体内在的能量。
(2)分子动能:物体是由大量分子组成的,分子在永不停息的做无规则运动,所以分子都具有动能,叫做分子动能。
(3)分子势能:分子之间存在相互作用的引力和斥力,所以分子又具有势能,叫做分子势能。
(4)构成物体的所有分子,其热运动的动能和分子势能的总和叫做物体的内能。
分子的热运动课件

分子热运动的速率分布规律
麦克斯韦速度分布律
在平衡态下,理想气体分子的速度分布遵循麦克斯韦速度分布律 。
速率分布函数
描述分子热运动速率的分布规律,可以通过实验测量得到。
高温与低温极限
在高温时,麦克斯韦速度分布律趋向于正态分布;在低温时,趋向 于泊松分布。
2023
PART 03
分子热运动的影响因素
REPORTING
化学工程
在化学工程中,分子热运动对化学反应过程和产物有重要影响。通过控制分子热运动,可 以提高化学反应效率,优化产物质量和产量。例如,在发酵工程、酶工程等生物工程领域 中,利用分子热运动实现生物反应过程的控制和优化。
2023
REPORTING
THANKS
感谢观看
气体分子的速率分布实验
总结词
通过测量气体分子在不同速率下的分布情况,揭示气体 分子的速度分布规律。
详细描述
气体分子的速率分布实验是通过测量气体分子在不同速 率下的数量或浓度,以揭示气体分子的速度分布规律。 在实验中,通常采用一些特殊设计的仪器来测量气体分 子在不同速率下的分布情况,如速度选择器、分子束装 置等。通过这些实验,可以深入了解气体分子的热运动 特性,为热力学和统计物理等领域的研究提供重要依据 。
温度对分子热运动的影响
总结词
温度越高,分子热运动越剧烈
详细描述
随着温度的升高,分子所获得的能量增大,导致分子间的碰撞频率和碰撞力度 增加,从而使分子热运动变得更加剧烈。
物质种类对分子热运动的影响
总结词
物质种类不同,分子热运动的形式和 强度也不同
详细描述
不同物质分子的质量和电荷分布不同 ,导致分子间的相互作用力和碰撞特 性存在差异,从而影响分子热运动的 形式和强度。
第三章 气体分子热运动速率和分布函数_电子教案白

第 一 节 气体分子的速率分布律
一、 速率分布函数 1.分子速率分布 平衡态下,分布在各速率区间内的分子数占总 分子数的百分率。令 N 为分子数,平衡态下在速率 v : v + dv 内
dN dN = f (v) dv ⇒ f (v) = Ndv N 2、物理意义:在速率 v 附近,单位速率间隔内出现的分子数占总
2
N = 2.6875 ×1019 个 ∆N = 2.484 ×1017
(2) v = vp=
2 kT m0
3
∆v =
− m0 v 2 2 kT
vp 100 4 −1 11 = 4π ( 2 ) 2 e N vp
例:理想气体,求 v = 的分子数的比值。
v 2 ∆v =
解: (1) f (v) =
dN 4πA 2 = v = kv 2 Ndv N
vF
(2)
∫
∞
0
f (v)dv = ∫
∞ 2
0
4π Av 2 vF 3 dv = 1 = 4π A N 3N
vF 2
A=
3N 4π vF 3
(3) v =
2
∫
0
v f (v)dv = ∫
0
2 vF 4π Av2 3 2 3v v dv = ∫ v 3 dv = vF 2 0 N vF 5
2 2 =1:2:4 ,则 p : p : p =? : v 2 2 : vC C B A B
1
解:
pA : pB : pC = nkTA : nkTB : nkTC
∵ (v ) : (v ) : (v ) =
1 2 2 A
1 2 2 B
热学 (3 第三章 气体分子热运动速率和能量的统计分布率)

f ()d dN
N
dN
2
=
f
( )d
N 1
表示速率分布在→+d内的
分子数占总分子数的概率
表示速率分布在1→2内的分
子数占总分子数的概率
N
0
dN N
0
f
d
1
归一化条件
应注意的问题:
分布函数是一个统计结果,以上各种讨论都是建立在众多分子微 观运动基础上的,分子的数目越大,结论越正确。所以:
1、作速率分布曲线。 2、由N和vo求常数C。 3、求粒子的平均速率。 4、求粒子的方均根速率。
f (v)
C ( vo> v > 0) 0 ( v > vo )
f (v)
解:
f (v)dv
0
vo 0
Cdv
Cvo
1
C
C 1 vo
o
vo v
o f ()d o Cd C o2
3. 方均根速率
2
2
f
d
0
3
2
4
m
2 kT
2
e
m 2 2kT
4
d
3kT
3RT
0
mM
2 3kT 3RT
m
M
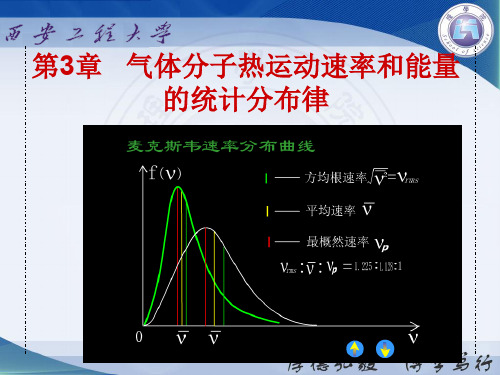
4. 三种速率的比较
最概然速率
p
2kT m
2RT M
平均速率
8kT 8RT m M
方均根速率
一、速率分布函数
气体分子处于无规则的热运动之中,由于碰撞,每个分子的速度都
第三章 气体分子热运动速率和能量的统计分布

气体分子热运动速率 和能量的统计分布
1
第三章 气体分子热运动速率和能量的 统计分布
§1 气体分子的速率分布律 §2 用分子射线实验验证麦克斯韦速度分布律 §3 玻尔兹曼分布律 重力场中微粒按高度的分布 §4 能量按自由度均分定理
2
§1 气体分子的速率分布律
一、速率分布函数
设总分子数N,速率区间v ~ v+dv内分子数 dN占总 分子数的比率为: dN f (v)dv ,其中:
1mol理想气体内能为:
Um
1 2
(r
t
2s)RT
,因此:
CV ,m
1 2
(r
t
2s)R
只与自由度有关
单原子分子气体:
CV ,m
3 2
R
双原子分子气体:
7 CV ,m 2 R
35
五、经典理论的缺陷
CV ,m
根据经典理论:
7R 2
一切双原子分子CV,m相同
5R 2
CV,m与温度无关
3R 2
T/K
理论与实验的不符,根本在于它是建立在经典概念,即能量 连续分布的基础上的。只有用量子理论才能进行较完满的解释。
单位时间内碰到单位面积器壁上速度在vx~vx+dv之间的分子数为:
nvx
f
(vx )dvx
nvx
m
2kT
1/ 2
e dv mvx2 / 2kT x
单位时间内碰到单位面积器壁的总分子数为:
0 nvx f (vx )dvx
n
m
1/ 2
2kT
e v dv mvx2 / 2kT
0
xx
n
kT
气体分子在空间位 置不再呈均匀分布
分子能量的知识点总结

分子能量的知识点总结一、分子能量的概念分子能量是分子内部的能量,是分子振动、旋转和转动等运动形态的能量总和。
分子能量包括热能、势能和动能等形式,是分子内部的能量。
分子能量的大小直接影响着物质的物理和化学性质,可以通过热学性质、热力学性质和动力学性质等方面来研究和表征。
二、分子能量的组成1. 热能:分子内部的振动、转动等运动形态所具有的能量,是分子能量的主要组成部分。
热能是分子内部自由度的能量,随着温度的增加而增加。
2. 势能:分子间的相互作用所具有的能量,包括分子间的引力、斥力、电荷相互作用等形式。
分子的结构、形状、键合等都会影响分子间的势能分布。
3. 动能:分子在运动过程中所具有的能量,包括分子的平移、旋转等运动形态所具有的动能。
分子的速度、质量等因素都会影响分子的动能大小。
三、分子能量与热力学性质1. 内能:分子能量的总和称为内能,是物质所具有的热能和势能的总和。
内能通过温度、压强等热力学性质来表征,可以通过物态方程、内能变化等来研究和描述。
2. 熵:分子运动形态的不确定性的度量,是熵的概念。
分子内部的热运动越剧烈,熵值越大,这是熵增加的基本原因。
3. 热容:物体吸收(释放)热量时,温度升高(下降)的能力,是热容的概念。
热容可以通过分子内部的热运动形态来解释和描述。
四、分子能量与热学性质1. 热膨胀:物体温度升高时,体积扩大的现象,是热膨胀的概念。
分子的热运动形态会导致固体、液体和气体的体积变化。
2. 热传导:物体内部热能的传递过程,是热传导的概念。
分子内部的热运动形态会导致热能的传递。
3. 热辐射:物体发出热能的现象,是热辐射的概念。
分子内部的热运动形态会导致热辐射的产生。
五、分子能量与动力学性质1. 化学反应速率:化学反应进行的速度,是化学反应速率的概念。
分子内部的能量会影响化学反应发生的速度。
2. 反应活化能:化学反应进行所需的能量,是反应活化能的概念。
分子内部的能量会影响反应活化能的高低。
分子热运动特点

分子热运动特点
分子热运动是指分子在空间中的运动状态,它是由分子的热运动引起的。
分子热运动的特点主要有以下几个方面:
1. 无规则性:分子热运动是无规则的,分子在空间中的运动轨迹是随机的,没有规律可循。
这是由于分子之间的相互作用力是复杂的,而且分子的运动速度和方向也是随机的。
2. 高速度:分子热运动的速度非常快,通常在几百米每秒到几千米每秒之间。
这是由于分子在空气中受到的碰撞频率非常高,而且分子之间的相互作用力也非常强。
3. 高能量:分子热运动的能量非常高,通常在几千焦耳到几百万焦耳之间。
这是由于分子在空气中受到的碰撞能量非常大,而且分子之间的相互作用力也非常强。
4. 扩散性:分子热运动具有扩散性,即分子会沿着浓度梯度从高浓度区域向低浓度区域扩散。
这是由于分子在空气中的运动是随机的,而且分子之间的相互作用力也是随机的。
5. 中心扩散:分子热运动的中心扩散是指分子在空气中的运动是以一个中心为基础的扩散。
这是由于分子在空气中的运动是随机的,而且分子之间的相互作用力也是随机的,所以分子的运动会以一个中心为基础扩散。
分子热运动是一种无规则、高速度、高能量、具有扩散性和中心扩散的运动状态。
这种运动状态对于物质的热力学性质和化学反应有着重要的影响,因此在化学、物理、生物等领域都有着广泛的应用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
重力场中微拉按高 度的分布 *沙尘暴 *大气污染的治理 **阿伏伽德罗常量 的测定
*大气标高 *等温大气标高 *等温大气中粒 子的平均高度与平 均重力势能
*均质大气 *均质大气高度 大气粒子总数 44 (N大气 = 1.074010 ) 大气总质量 *大气的总重力势能
*大气的热运动总能量 *世界对初级能源的年 消耗量 **能源问题 **新能源的开发与利 用
1/2 (2kT/m) ,
f(v)dv =
2 exp(x )dx
1/2 2 4 x
=F(x)dx. 但要特别注意: 1/2 2 2 F(x) = 4 x exp(x ) f(v).
麦克斯韦速率 分布曲线出 现极大值的 点的轨迹
1/2 3/2 f(v)=4 [m/(2kT)] 2 2 exp[mv /(2kT)]v .
随机事件 与概率
随机现象:有可 能出现多种结果的 现象。 随机事件:随机 现象的每一表现或 结果。
频率:某事件出 现次数对总次数的 比率。 概率:某事件频 率在总次数趋于无 限大时的极限。
不可能事件 的概率为零。 必然事件的 概率为一。
概率加法定理: 互不相容(互斥) 事件出现的概率的 和等于出现其中任 一事件的概率。
泻流 分子束 *泻流条件 麦克斯韦发射分布 *分子束中分子的平 均速率与方均根速率
麦克斯韦速率分 布律的实验验证 密勒和库士实验 葛正权实验 *葛正权简介
*扩散法分离核素 *电磁法分离核素 *核燃料的生产 *核能的利用 *中国的核科学技术
等温大气 等温气压公式 兰州市区的大气压 *珠穆朗玛峰的大气压 *气压计和高度计
考虑到地面的凹 凸不平时,得干洁 大气粒子总数为 N干 = N N 44 = 1.0696210
大气中水分 子的总数为 41 N水 = 4.3510
考虑到地面的凹 凸不平时,得大气 粒子(含水)总数为 N大气 = N干 + N水 44 = 1.074010
大气粒子总数为
44 1.074010
*大气的温度结构 *大气的均质层 *大气的非均质层 *大气非均质层内 的重力分离现象
*标准大气 *估算大气粒子 总数时忽略了地面 的凹凸不平所造成 的误差
用标准大气 模型估算大 气粒子总数
忽略了地面的凹 凸不平时,得干洁 大气粒子总数为 44 N = 1.10062010
估算干洁大气粒子 总数时,忽略了地面 的凹凸不平所造成的 误差为 42 N = 3.09986610
用麦克斯韦速率分布函数 推导分子的平动能分布函数 *平动能分布曲线的特征 气体分子平动能的平均值 与最概然值 *平动能分布函数的约化 形式
*气体分子的最概然速率 与最概然平动能之间的关 系 *麦克斯韦速度分布曲线 的特征 *麦克斯韦速度分布函数 的约化形式
速度空间 麦克斯韦速度分 布律与麦克斯韦速率分布律 的关系 *麦克斯韦对速度分布律的 推导 用麦克斯韦速度分布函数推 导气体的压强公式和分子通 量公式
地球表面上 干洁大气的 典型数据
v
(当g = 9.80665 p = 101325 Pa, T = 288.150 K = 15.000 C时)
-2 ms ,
分子摩尔质量 -3 = 28.964410 -1 kgmol
气体质量密度 = p/(RT) = 1.2250 -3 kgm
第三章 分子热运动能量 和速度的统 计分布律
分布 分布函数 速率分布函数 速率分布函数的归 一化条件 *速率分布函数的 定义域
麦克斯韦速 率分布函数
f(v) = 2 2 exp[mv /(2kT)]v -1/2 3/2 = 4 [m/(2kT)] 2 2 exp[mv /(2kT)]v .
用麦克斯韦速率分 布函数的约化形式 来求速率分布曲线 出现极大值的点的 轨迹似乎更简便。
x = v/vp, dx/dv = 1/vp. f(v) =F(x)dx/dv =F(x)/vp 1/2 2 2 =4 x exp(x )/vp.
f(vp) = F(1)/vp 1/2 1 = 4 e /vp. 1/2 -1 即vpf(vp) = 4 e =常量. 这是一条双曲线的方 程。
3/2 4[m/(2kT)]
f(v)称为麦克斯 韦速率分布函数, 式中的T为气体的 热力学温度,m为 气体分子质量。
麦克斯韦速率分布 律 麦克斯韦速率分布 律的适用范围 麦克斯韦速率分布 曲线的特征
*路程按时间的分布 函数 *速率恰为某值的分 子数与质点在某时刻 通过的路程 *类比法
气体分子的最概然 速率 *随机事件 *概率 *概率加法定理 *概率乘法定理 *概率分布函数
用麦克斯韦速率分 布函数求平均值 气体分子的平均速 率与方均速率 *平均速率的简捷计 算
平均速率与方均根 速率的关系 速率倒数的平均值 与方均根值 *分子特征速率的 量纲分析
用麦克斯韦速率分布函数求 粒子数 误差函数 *误差函数的计算 *气体分子速率的中值 *线性内插 *速率中值与其他特征速率 之间的关系
将 vp =
1/2 (2kT/m) 代
入f(v)可得:
1/2 3/2 f(vp)=4 [m/(2kT)] 2 2 exp[mvp /(2kT)]vp 1/2 2-2 -3+2 =4 exp[vp ]vp
=
1/2 1 -1 4 e vp .
由此可得: 1/2 1 vpf(vp) = 4 e =常量. 这是一条双曲线 的方程。
概率乘法定理: 互相独立事件同时 出现的概率等于各 事件单独出现时概 率的积。
*麦克斯韦速率分 布函数的约化形式 *麦克斯韦速率分 布曲线出现极大值的 点的轨迹
麦克斯韦速率 分布函数的 1/2 3/2 f(v)dv = 4 [m/(2kT)] 2 2 exp[mv /(2kT)]v dv 1/2 -3 = 4 vp 2 2 2 exp(v /vp )v dv.
