中国药品电子监管网 企业入网流程介绍_医药卫生_专业资料
中国电子药品监管码

药品零售企业入网数据格式与导入说明一、目的为了免除食品药品监管部门繁重的入网审核工作,最大程度确保入网零售企业信息的真实性和准确性,提高零售企业入网效率,零售企业入网方式由企业自主填报调整为省局集中批量二、操作步骤(一)负责核发《药品经营许可证》和《药品经营质量管理规范认证证书》的食品药品监管部门将所发证书数据按照本说明要求认真整理后,上报至省食品药品监管部门。
(二)省食品药品监管部门汇总下级药品监管部门上报的数据,制作本省药品零售企业入网数据。
(需要包括本省所有药品零售企业,不论是否已入网)(三)省食品药品监管部门登录国家药品电子监管平台,在“入网管理-零售企业导入”界面,点击“零售企业导入”按钮,选择本省药品零售企业导入模板,完成导入操作。
三、特别提示(一)为了确保导入零售企业信息按照“属地管理原则”归属到对应的地域(省、地市、区县),方便食品药品监管部门后期管理,导入表中的食品药品监督管理部门名称和地域名称,请参照《药监网入网食药局名称及地域名称字典》(以下简称“地域字典”),该文档(二)导入表中的黑色业务字段不能为空,确因特殊原因导致业务字段数据缺失的,请以“#(三)导入表中的红色字段如果为空,后期还需要零售企业补充完整,使药监网客服中心后(四)平台会检验导入表是否符合格式要求,如果格式错误,请导出失败列表,查看错误原因。
平台支持按照市、县分批导入,也支持一次性全部导入。
(五)零售企业入网后,企业信息发生变更,请企业用户登录零售企业客户端软件,进行相四、导入模板字段格式说明1、行号:不能为空。
数字,格式为阿拉伯数字1、2、3…。
提示:可以使用excel自动填充功能自动编号。
一个行号标识一个企业,如果某个企业的行号为空,则该企业不会被导入。
行号也方便食品药品监管部门核对查询导入数据。
(1)药品经营许可证信息2、证号:不能为空,指药品经营许可证证号。
3、企业名称:不能为空。
指药品经营许可证上的企业名称。
中国药品电子监管网使用手册(I)

主要提供入网企业的明细查询报表,点击“入网企业查询报表”选项卡,打开页面中选择、填写需要统计的起止日期(企业所属省份和城市),点击“查询”按钮,系统自动将符合条件的查询结果输出成报表格式,如下图:
1.5
点击“全国入网企业按月统计”选项卡,打开页面中填写查询条件,点击“查询”按钮,页面将显示符合查询条件的报表,如下图:
1.2.1
“入网企业查询”页面的列表中,点击需要查看企业的记录行,系统将显示企业的基本信息。
1.2.2
“基本信息”页面,点击“药品赋码明细”选项卡,可以查看企业的药品赋码明细列表,再点击列表中的记录行,可以查看药品的已赋码详细信息,如下图:
1.3
点击“入网企业统计”选项卡,打开页面中选择需要统计的起止日期,点击“查询”按钮,系统自动将符合条件的查询结果输出成报表格式,如下图:
《中国药品电子监管网》使用手册
-监管部门分册
国家食品药品监督管理局
信息化工作办公室
二〇〇八年四月
中国药品电子监管网(监管部门)的功能包括:入网管理、药品信息管理、药品流向与追溯、药品召回、统计报表、库存报表、预警管理、帐户管理,页面展现如下图:
页面分为五部分:
1.登录用户信息:页面左上位置
2.功能菜单:页面左中位置
确认通过审核
如确认企业入网登记信息正确无误,点击“审核成功”按钮进行审核确认。
审核不通过
如企业入网登记信息有误或由于其他原因不能通过审核,可点击“审核未成功”按钮,系统将弹出审核未成功原因填写界面,选择、填写不通过的原因,点击“提交”按钮。
如下图:
1.2
点击“入网企业查询”选项卡,选择、填写要查询的条件,点击“查询”按钮,显示所有符合条件的企业列表,如下图:
药品电子监管简易操作流程

药品电子监管简易操作流程
药品电子监管码扫描及进销存入库上传操作流程:
扫描枪的使用:
第一步,登陆—开启扫描枪,提示登陆用户编号:0001,按OK 键;输入用户密码:123456,按OK键;成功进入操作界面。
第二步,扫描—核注入库,选定到核注入库,按OK键;然后是采库入库,继续按OK键;再选择2、普通药品,按OK键;显示“不存在上游企业信息”直接按OK键进入;最后两次输入当天的单据号后,按扫描枪上两个黄色的SCAN(扫描)电子监管码即可成功录入。
扫描—核销出库;按照上面入库的操作流程进行即可。
电子监管码软件上传操作:
第一步,扫描枪数据上传—上传数据,首选扫描枪与电脑用数据线连接;完成后,进入扫描枪,选择6、数据通信,按OK键,选择上传数据,按OK键,再选择上传普药数据,按OK键,然后点击电脑桌面上的“CsharpXML”选择上传文件中的普药,点击确定即可上传成功。
第二步,软件上传数据,双击桌面上“药品监管系统—企业端”,输入用户名:561613536密码:66666666。
点击入出库管理,然后点靠右边的查询,便可出来以下结果:然后在上图显示查询结果单击详细信息如下图所示:
在上图显示选择“发货单位”
输入发货单位拼音的第一字母关键字,如下图所示
选择好以后,如下图
点击上传即可完成整个操作。
中国药品电子监管网操作手册2

附件2:中国药品电子监管网操作手册——监管部门目录1 系统概述 (3)2 监管部门登录方式 (3)2.1 监管部门登录 (3)2.2 收起展开功能菜单 (4)3 系统功能 (6)3.1 入网审核 (6)3.1.1 入网审核 (6)3.1.2 企业信息变更审核 (7)3.2 药品信息管理 (8)3.3 企业信息管理 (13)3.3.1 企业药品目录管理 (13)3.3.2 企业信息查询 (16)3.4 药品召回 (18)3.4.1 发起召回 (18)3.4.2 召回查询 (21)3.5 预警管理 (22)3.5.1 预警定制 (22)3.5.2 预警定制查询 (24)3.5.3 预警处理 (26)3.5.4 预警地图 (27)3.6 统计报表 (30)3.6.1 监管网的实施情况统计 (30)3.6.2 企业生产经营状态统计 (33)3.6.3 预警报表统计 (39)3.6.4 药品召回统计 (40)3.6.5 特殊药品统计报表 (41)3.7 特药计划管理 (48)3.7.1 特药年度计划区间查询 (48)3.7.2 特药计划查询 (49)3.7.3 企业执行进度查询 (52)3.7.4 区域执行进度查询 (53)3.7.5 计划及生产量年度对比 (54)3.8 运输信息管理 (55)3.9 消息中心 (56)3.9.1 消息新增 (56)3.9.2 查询发送消息 (57)3.9.3 接收消息 (59)3.10 药品流向和追溯 (61)3.10.1 码流向查询 (61)3.10.2 药品流向查询 (63)3.10.3 药品追溯查询 (65)3.11 数字证书密码管理 (66)3.11.1 密码修改 (66)1系统概述中国药品电子监管网主要是食品药品监督管理部门对药品从生产、经营进行全程监管的应用平台,通过药品与监管码的一一对应关系可以进行药品的流向追溯和召回。
2监管部门登录方式各级食品药品监管部门申请加入中国药品电子监管网(以下简称监管网),获取数字证书后,直接访问监管网网站(),从“政府登录入口”进入系统内进行操作。
中国电子药监网监管系统使用规程

中国电子药监网监管系统使用规程1.基本操作2.1系统登录2.2界面简介登录界面用户名为企业填写入网申请表时录入的本企业组织机构代码,系统校验用户名是否与用户插入的数字证书信息符合,如果符合,系统弹出数据证书口令输入框,如下图:数字证书密码默认为:88888888,用户可登录客户端后修改密码。
注:在使用数字证书时需要注意,首先要确定已经插入数字证书,并且尽量保证插入的USB接口与上次正确使用时插入的接口是同一个,如需改变接口可能要重新安装数字证书的驱动,数字证书的驱动程序在附带的光盘里;数字证书在登录时插入后,请在退出系统后再拔出,以免影响正常的使用;如果使用时系统没有识别出数字证书,将会弹出未知错误,此时需重新安装数字证书驱动程序。
系统主界面2.参数设置2.3、导入导出目录设置该功能用于设定企业导出药品目录、操作员信息等数据的本地存放目录;以及企业导入的关联关系、入出库数据的本地存放目录。
客户端软件安装时,系统会自动建立并设定默认目录为:导出目录默认设定——D:\SFDA\OutData\。
用于存放导出的往来单位信息、企业药品信息、操作员信息。
关联关系导入目录默认设定——D:\SFDA\InData\Relation\。
从生产线系统导入的关联关系文件,请存放至此目录下。
入出库导入目录默认设定——D:\SFDA\InData\Bussiness\。
从条码扫描终端导入的入出库文件,请存放至此目录下。
用户可自行设定上述目录。
1)双击左侧导航菜单中“参数设置”,点击右侧“导入导出目录设置”选项卡,页面显示当前的目录设置,如下图:2)点击需要设置的目录的按钮,系统会弹出目录设置界面,如下图:3)或者点击按钮,系统会弹出本地目录浏览界面,如下图:4)选择目录点击按钮,此窗口会被关闭,目录更新。
5)然后点击按钮,如果设置成功,系统会提示相应的目录设置成功6)如果失败,系统会提示相应的目录设置失败。
7)如果点击按钮,目录路径会变为原来的路径。
药品监管系统操作步骤

药品监管系统操作步骤(测试训练用)1.在左边菜单中点击参数设置,将接下来所需要的数据通过改变设置放入自己所需要的文件夹中。
2.点击左边菜单中的信息管理,进入药品目录界面(生产企业操作步骤)搜索药品,选中所需药品则进入下一步操作。
如果进入往来单位界面(经营企业操作步骤)输入关键字进行搜索,选定所需单位,点击屏幕中央的向右箭头则可以把选定单位作为往来单位。
如果服务器内没有所搜索的单位则可以自行添加往来单位,点击添加图标,输入相关实际信息即可。
3.点击左边菜单中的导入导出,将先前所选的药品信息或者往来单位信息导入电脑,导入位置为参数设置的文件夹。
4.点击左边菜单的的信息管理(此为生产企业步骤),进入药品信息界面,搜索先前导入的药品信息,确认药品信息是否准确完整。
如不完整则填写相关信息。
5.点击左侧菜单中的监管码管理,进入监管码申请界面,选定所要申请监管码的药品,点击申请。
进入监管码查询界面,查询所申请的监管码是否通过系统审核,如通过则进入监管码下载界面,下载所选药品的监管码,会出现一个压缩文件包,可将其存放在桌面备用,下载成功后,进入监管码解密界面(所下载的监管码需要数字证书解密才可以使用)。
解密完成后,桌面上会出现3个文档分别对应1级包装,2级包装,3级包装的监管码,其中3级包装为外箱包装,2级为中包装,1级为内包装(如果此前在药品信息内所填包装级数不为3级则另算)。
6.点击左侧菜单的信息管理,刷新药品目录,下载药品信息,所下载的信息位置为之前参数设置所选的文件夹。
7.(练习操作步骤,实际生产时则无此步骤)进入Relation(此为生成码文件,需下载)。
生成路径选择第6步中所下载药品信息的文件夹,导入相对应的包装监管码,选中关联关系选项,点击创建,即可生成与药品具有关联关系的监管码文件,将该文件复制到之前参数设置有关关联关系的文件夹。
(如需要生成入出库单,则把关联关系选项改为入库单或者出库单即可)8.点击左侧菜单中的关联关系,进入关联关系查询界面,如之前操作成功,在此界面则可以查询到具有关联关系的药品,进入上传界面点击上传。
药品监管系统-企业端操作规程

药品监管系统-企业端操作规程分发部门1主题内容本标准规定了药品监管系统-企业端的标准操作规程。
2适用范围本标准适用于药品监管系统-企业端的所有操作。
3职责数字证书操作员:负责通过药品监管系统-企业端对维护药品信息、申请并下载解密药监码,上传药品码信息及其他作业信息。
QA :负责对需要维护的信息进行复核4内容4.1 企业客户端及数字证书驱动程序的安装4.1.1企业客户端的安装:通过中国药品电子监管网,网址:。
下载客户端安装包及升级包,先安装客户端,完成后安装升级包,及完成企业客户端的安装操作4.1.2数字证书驱动程序的安装在下载客户端是同时现在数字证书的安装包,在客户端安装完成之后,点击安装驱动程序,选择数字证书种类,进行安装。
安装完成即可登录企业客户端。
4.2 企业客户端的登录当启动系统后,显示如下图:在登录界面填写正确的“用户名”为本企业组织机构代码、“密码”后点击“登录”按钮。
系统校验用户名是否与用户插入的数字证书信息符合,如果符合,系统弹出数据证书口令输入框,如下图:填写数字证书密码,点击登录按钮,系统验证数字证书密码,密码无误,进入系统首页。
4.3消息中心登录系统后最先打开的是消息中心,又来对日常信息和预警信息的处理4.4参数设置双击参数设置,进入参数设置操作界面,在导入导出目录设置中对关联关系、入出库单、导出目录进行设置。
4.5信息管理双击信息管理,进入信息管理操作界面4.5.1 企业信息4.5.1.1 企业信息是在申请数字证书时由中国药品电子监管网进行录入,然后由企业对信息进行维护。
4.5.1.2 企业信息的修改当企业信息发生变更时,需要对企业信息中的相应内容进行修改。
修改方法:1.先点击界面右上角的修改按钮,进入修改界面2.对变更内容进行修改,点击提交,即完成修改。
生产许可证和GMP证书内容修改后需将旧生产许可证和旧GMP证书信息删除。
否则会产生预警。
4.5.3 药品目录药品目录中药品品种的增减需要中国药品电子监管网进行。
药品电子监管系统操作

光液晶显示; (2)扫描终端软件基本功效:
满足药品生产和经营批发企 业入库核注、出库核销和数 据通讯要求。
2. 无线上传条码扫 描终端软硬件要求
(1)硬件要求: 支持GPRS或者802.11局域无
线通讯; (2) 软件要求: a. 扫描终端在监管码采集完
药品电子监管系统操作
第18页
药品电子监管系统操作
Thank You !
Click to edit company slogan .
第19页
(一)药品电子监管网入网、续费操作
1. 申请入网流程
2.数字证书政府代付费操作流程
4. 数字证书注销流程
3. 数字证书续费流程
5. 数字证书退费流程
6. 监管网汇款要求和账户信息
药品电子监管系统操作
第8页
(二)配置条码扫描终端
1.通用条码扫描 终端软硬件要求
(1)扫描终端硬件指标要求: a.激光扫描引擎; b. 满足IP54以上工业等级; c.存放容量尽可能大,断电不丢
❖ 中国药品电子监管网系统支持企业用户在添加往来 单位时,自行为每个往来单位添加自定义编号,并 将往来单位列表导入手持终端,方便在入出库扫码 时可输入自定义编号选择收发货单位,降低单据上 传时录入工作量。
药品电子监管系统操作
第13页
4. 异常业务处理(一)
(1)药品发生退 货时操作流程
(2)药品出现零 头出入库时操作流 程
成后直接生成完整含监管 码单据信息,可经过无线 网络直接上传中国药品电 子监管网。 b. 软件可自动或手动更新, 而无须重新安装。更新后 必须确保业务数据不丢失。
3.选择、配置条码 扫描终端
药品电子监管操作程序

药品电子监管操作程序1.基本要求1.1收货员码放电子监管品种时,必须保证监管码朝外,方便扫码操作。
1.2验收员对采购及销售退回的电子监管产品进行质量验收以及监管码的扫码。
1.2.1对未按规定加印或监管码不符合要求的药品以及非本公司售出的销售退回电子监管产品拒收。
监管码信息与药品包装信息不符的,应当及时向供货单位查询,未得到确认之前不得入库,必要时向当地药品监督管理部门报告。
对验收合格的产品进行扫描,将扫描数据保存在药品监管码采集系统“手持终端”中,保证数据准确无误。
1.2.2扫描原则:整件包装完好的产品,扫描大包装上的监管码。
非整件包装产品,则需扫中(小)包装上监管码。
1.3电子监管产品入库后,在堆码、上架操作过程中,注意勿使包装上印制(粘贴)的监管码损坏、缺失,要保证包装上监管码的完整性。
1.4出库复核人员对出库的电子监管品种进行扫描,并将扫描数据保存在药品监管码采集系统“手持终端”中,保证数据准确无误。
1.5养护员对要销毁的电子监管品种进行扫描,并将扫描数据保存在药品监管码采集系统“手持终端”中,保证数据准确无误。
1.6数字证书操作员次日将前一天采集的电子监管数据上传至药品电子监管网。
1.7数字证书操作员对电子监管网中没有的往来单位,应在监管网中增加。
2.操作流程:2.1电子监管码的采集2.1.1入库采集(采购入库和销售退货入库)在“手持终端”的界面中,输入操作员编号,管理密码,确认进入,时间确认,进入手持终端“条码管理”,选择“1.出入库”进入,选择“1.入库”确认,选择“3.购买入库”,在“单号”处填写相应的“入库单据”号,编号为:日期+顺序编号,再按确定键进入扫描状态,然后用数据采集器逐一对该入库单上所有的入网药品进行扫描,(含独立的大包装、中包装、零散药品),并核对扫描的药品品种及数量和实际入库数量是否相符,核对无误按“确认”键结束。
2.1.2出库采集(销售出库和采购退货出库)在“手持终端”上操作,同采集进入方法进入“条码管理”界面中,选择“1.出入库”进入,选择“2.出库”,选择“1.销售出库/2.退货出库”进入,在“单号”处填写相应的出库单据号,单位编号可为空,确认进入扫描状态,然后用数据采集器逐一对该出库单上所有的入网药品进行扫描,(含独立的大包装、中包装、零散药品),并核对扫描的药品品种及数量和实际出库数量是否相符,核对无误按“确认”键结束。
零售企业入网登记表在线填报步骤及填报说明
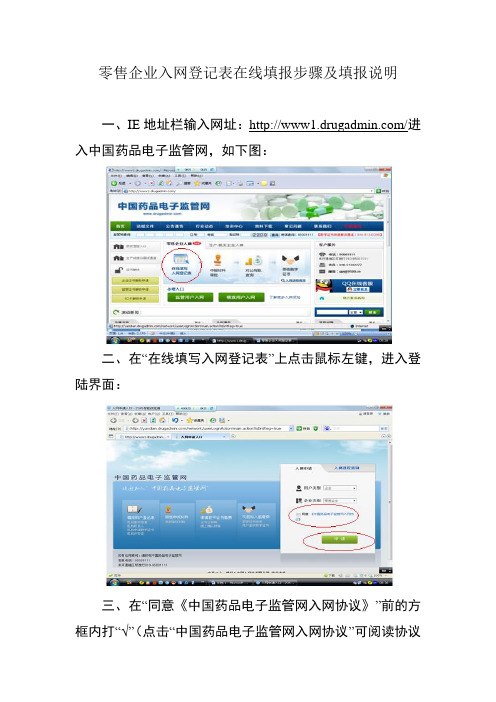
零售企业入网登记表在线填报步骤及填报说明一、IE地址栏输入网址:/进入中国药品电子监管网,如下图:二、在“在线填写入网登记表”上点击鼠标左键,进入登陆界面:三、在“同意《中国药品电子监管网入网协议》”前的方框内打“√”(点击“中国药品电子监管网入网协议”可阅读协议内容),然后点击“申请”进入在线填报界面:四、根据“零售企业入网《入网登记》填写说明”(可在“资料下载”或“常见问题”中下载)在线进行填写,填写完成后,在“本企业已经认真阅读《中国药品电子监管网入网协议》,保证填写信息真实可靠,履行各项入网义务”前的方框内打“√”,然后点击“提交申请”完成填报工作。
零售企业《入网登记表》填表说明《入网登记表》中带“*”号的选项是必填项,其它为选填项。
一、企业信息(一)企业全称:填写内容须与零售企业营业执照上面的名称一致。
(二)法人机构:●选择“否”,需填写“已入网总公司”和“总公司法人代表”。
●选择“是”,在“法人代表”一栏填写零售企业的法人代表姓名即可。
(三)法人代表:填写内容须与零售企业营业执照上的信息一致。
(四)营业执照注册号:填写零售企业营业执照上的注册号(请务必正确填写,认真核对,不要错填、多添或少添数字),在证件的右上角;该证由当地工商行政管理部门颁发。
(五)主要负责人:填写零售企业负责监管网相关事宜的人,该负责人可以是数字证书的持有人,也可以不是。
(六)经济类型:根据零售企业的经济类型进行勾选,勾选项内容为:内资、国有全资、集体全资、股份合作、联营、责任有限公司、股份有限公司、私有、中外投资、中外合资、中外合作、外资、国外投资股份有限公司、其他国外投资、其他等信息。
(七)机构类别:根据零售企业机构类型进行勾选,勾选项内容为:连锁药店总部、直营药店、加盟药店、单体药店、其他。
(八)企业实体店地址:根据零售企业的实际店面地址选填省、市、区县。
(九)归口监管药监局:填写实体店地址后系统会自动带出归口监管药监局。
最新中国药品电子监管网 企业入网流程介绍

❖ 邮件按发送时间降序排列,最新邮件显示在最上方; ❖ 点击其中一封邮件,可查看邮件详细内容。
制作数字证书
入网流程管理回顾
用户入网电子化- 业务示意图 业务进程
注册登记
注册进程 查看
审核
申请
查看
核准
用户交汇 数字证书
服务费
中信21世纪 审核机构
制作数字证书
操作人员
具体操作& 实现方式
工作界面
在线填报或 线下登记
《 用户注册登记表 》
在线查看
现场核对 在线确认
银行汇款或 审核机构缴费 在线查看\ 填报
确认汇款或 收缴费用 数字证书制作
《 用户注册流程 》
《 用户注册登记表 》
相应பைடு நூலகம்质 证明材料
《 汇款信息表》
用户使用
接收
派发数字证书
入网流程管理回顾
派发数字证书
数字证书接收 开通权限 更改登陆 业务使用
邮寄纸质材料
❖ 打印《入网登记表》; ❖ 复印相关资质证明材料,具体材料如下:
➢ 企业法人营业执照复印件 ➢ 组织机构代码证复印件; ➢ 数字证书操作员身份证复印件 ➢ 生产经营许可证复印件; ➢ GMP/GSP证书复印件
注意:以上所有材料必须加盖企业公章邮寄至中国药品电子监管网运 营中心。
入网进程查询
❖ 点击新增,可以新增多个证书信息; ❖ 如果企业有多本证书,请填写完备; ❖ 从申请之日起六个月内维护完整该信息,否则系统自动停
止用户的操作权限;
6)申请其他信息
❖ 记录“登录用户名称”和“登录密码”,登录网站可查询 入网进度;
❖ 点击提交,等待系统审核; ❖ 点击暂存,该表暂存系统内不提交审核,可再次修改。
电子监管码.操作流程-仅供参考
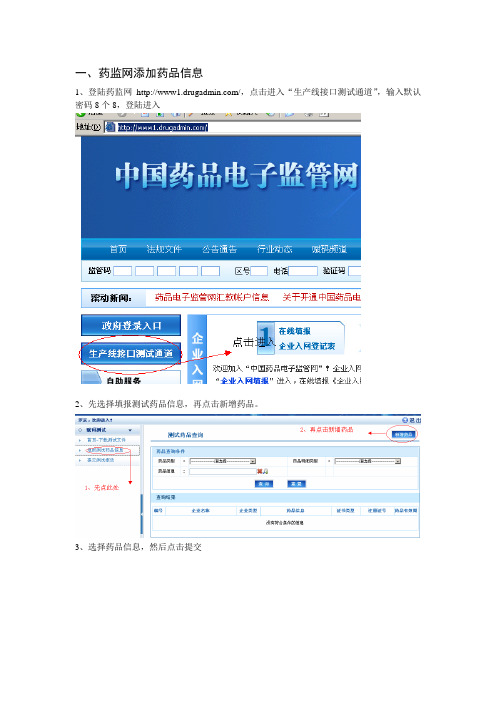
一、药监网添加药品信息1、登陆药监网/,点击进入“生产线接口测试通道”,输入默认密码8个8,登陆进入2、先选择填报测试药品信息,再点击新增药品。
3、选择药品信息,然后点击提交4、再选择填报测试药品信息,刷新页面,查看药品信息是否添加成功。
二、“药品监管系统”下载药品信息及药监码1、登陆“药品监管系统——企业端(培训平台)”,2、点击信息管理,选择药品目录,查询药品信息,点击药品详细信息3、填写所有带*的药品信息,再点新增,然后点击提交4、选择监管码管理,填写带*的基本资料、包装关联资料及所需申请的监管码数量(1级跟2级监管码数量自动关联),然后点击提交。
5、选择监管码下载,点查询,再点下载,选择保存路径,然后点击确认下载。
6、选择监管码解密,选择监管码下载存放路径,点击解密文件7、选择信息管理,点击药品目录,选择药品信息,点击下载药品信息,然后选择下载保存目录,点击保存。
三、药监赋码系统设置1、打开药监赋码,登陆。
2、选择生产维护,选择产品配置管理,点击“导入”,3、浏览选择产品数据文件(也就是2-7保存的药品文件),选择文件,点打开。
4、查看药品信息是否导入成功5、选择监管码管理,选择监管码导入,点击选择文件6、选择药监系统里下载的两个药监码文件,点击打开,点击全部导入来导入监管码。
7、选择监管码打印,点击选择产品,选择要打印产品的监管码8、选择要打印的监管码级别和数量(一级和二级监管码),然后点击打印(如果提示模板错误不能打印,参照8-1)8-1、选择打印模板名称,复制名称,选择系统信息管理-设置管理-打印模板设置,选择1级监管码,点击编辑模板,选择名称,粘贴刚才复制的打印模板名称,然后保存关闭;再选择2级监管码,点击编辑模板,选择名称,粘贴刚才复制的打印模板名称,保存关闭9、选择生产管理-生产维护-赋码生产线管理,然后点击增加车间信息,再添加生产线和工位信息,添加2个以上生产线10、选择生产管理-生产过程管理-订单信息管理,然后点增加下订单,填写订单信息,需要增加2个以上订单11、选择生产管理-生产维护-赋码生产线管理,点击订单绑定的生产线,然后点击右上角的激活12、使用设备扫描一级和二级监管码,分别扫描关联整箱、零箱、拼箱这3个关联信息13、选择赋码关联管理-导出管理-关联关系导出,点击添加订单,选择要导出的产品订单,将不导出的文件打上勾,点击导出,再点击打开导出目录查找导出的关联文件。
中国药品电子监管系统培训材料

G(确认键)
F4(未定义 )
2.如何登陆主菜单?
开机进入
按G键/确认
按G键/确认
初始密码8个1
进入主菜单
3.系统设置(企业性能设定)
(2)企业性能设定
选择5
系统设置 -1功能绑定 2设License 3药品选择 4关联设置 返回5企业设置 选定
录入License
------------------------------------------------------------------
1注销码数据
2建立关联数据
3重建关联数据
4删除关联数据
按上/下翻页
返回
选定
删除选择-1 1删除所有数据
2出入库数据
3盘点数据 4替换码数据 按上/下翻页
返回
选定
按下键
删除选择-3 1关联检验数据
2删产品绑定 3删上有企业名单
按上/下翻页
返回
选定
5.错误处理
(1)强制关机:按住电源键同时按住“ G”键,即可。
返回
选定
系统设置 -1功能绑定 2设License 3药品选择 4关联设置 返回 5企业设置 选定
选择5
设置使用单位
_____________________________
-1生产企业
2运营单位
3使用单位
4设置终端
返回
选定
4.系统操作流程
(1)出入库管理 由于入库和出库的流程相同,下面我们以入库
? 关联关系 ? 监管码激活 ? 全程核注核销
? 核注入库 ? 核销出库
经营企业实施的总体流程
入网登 记
配备手 持终端
企业加入国家药品不良事件监测系统的注册程序

企业加入国家药品不良事件监测系统的注册程序第一篇:企业加入国家药品不良事件监测系统的注册程序企业加入国家药品(医疗器械)不良事件监测系统的注册程序1、登陆网址:114.255.93.2202、点击验证码右侧的“基层注册”3、在“基层单位注册——网页对话框”里填报如下信息:(1)所属应用:企业具备《药品经营(生产)许可证》的,点击“药品”前的方框;具备《医疗器械经营(生产)许可证》的,点击“医疗器械”前的方框;具备双证的企业则同时点击两个方框;医疗机构应同时点击两个方框。
(2)单位名称:填写企业全称。
(3)所属地区:点击右侧的“放大镜”,依此选择“天津市——市辖区——滨海新区”,选择后在所属地区的长方框内出现“滨海新区”字样。
(4)单位类别:如实填报单位类别。
(5)上级单位:依此选择“天津市药品不良反应监测中心——天津市滨海新区食品药品监督管理局——天津市滨海新区食品药品监督管理局XX分局(企业根据坐落地点选择相应所属分局)”(6)联系人:填报企业应据实填报。
联系人应为企业内具备流动性小、负责不良事件职责的管理人员。
(7)联系电话、单位传真、单位邮箱、通信地址、邮政编码:据实填报(8)注册证号、注册时间、注册地址:应填报企业具备的经营(生产)许可证证号、取得时间和地址,医疗机构应填报“组织机构代码证”的证号、取得时间和地址。
(9)法人代表、手机号码:据实填报。
(10)组织简介:对企业情况的基本描述,可不填。
注意:带红色星号标记的填报项目为必填项目。
4、在基层单位注册——网页对话框填报完上述项目后,点击“提交”即可。
5、注册提交后,请及时与所属分局负责工作人员联系,等待所属食品药品监管部门的审核,审核后获得的“用户名”即为今后企业上报不良事件(反应)时登陆网址(114.255.93.220)的用户名,初始密码为“111111”,登陆后企业可更改登陆密码。
6、企业在日常生产、经营和使用药品医疗器械的过程中,涉及到药械不良反应(事件),即可通过该系统进行网上直报。
电子监管系统入网及服务实施内容

电子监管系统入网及服务实施内容1. 引言电子监管系统是一个基于互联网的监管平台,旨在帮助政府及相关部门实施对各类企业和机构的监管工作。
本文将介绍电子监管系统入网及服务实施的相关内容,包括系统入网要求、服务范围以及具体流程等。
2. 系统入网要求电子监管系统入网要求如下:•企业或机构必须具备合法经营资质,符合国家相关法律法规的要求;•企业或机构必须拥有稳定的网络基础设施,并接入互联网;•提供真实、准确的企业或机构信息;•遵守相关的安全保密规定;•安装相关的软件和硬件设备,以便与电子监管系统进行数据交互。
3. 服务范围电子监管系统提供的服务范围主要包括以下几个方面:3.1. 企业或机构在线注册通过电子监管系统,企业或机构可以在线完成注册申请,提供必要的资料并进行身份验证。
系统将自动生成唯一的注册号并分配给每个已注册的企业或机构。
3.2. 信息报送与数据采集企业或机构需要按照监管部门的要求,定期或不定期地向电子监管系统提交相关的信息报表。
系统将按照固定的格式对这些信息进行采集和整理,以便监管部门对企业或机构的经营状况进行监察和评估。
3.3. 安全风险管理电子监管系统将通过网络安全审计、日志监控等手段对注册的企业或机构进行安全风险管理。
系统将自动分析异常行为、风险事件,并及时进行预警和处理。
3.4. 信息查询与共享企业或机构可以通过电子监管系统查询自身的相关信息,如注册资料、经营许可证信息、历史报表等。
同时,监管部门也可以通过系统查询企业或机构的相关信息并进行共享,以实现信息的互通互联。
3.5. 惩罚与纠正措施电子监管系统可以对存在违规行为的企业或机构进行惩罚与纠正措施。
系统将根据违规行为的性质和严重程度,自动生成相应的处罚方案,并下发给相关的企业或机构。
4. 具体流程企业或机构申请入网并使用电子监管系统的具体流程如下:1.在系统网站上进行注册申请,提交必要的企业或机构信息;2.系统会进行身份验证,并为每个注册用户生成唯一的注册号;3.安装相关的软件和硬件设备,以便与电子监管系统进行数据交互;4.根据监管部门的要求,及时报送相关的信息报表;5.对系统的数据进行定期的备份和安全保护;6.定期对系统进行网络安全审计和日志监控,及时处理异常行为和风险事件;7.主动查询和共享企业或机构相关的信息;8.依法对存在违规行为的企业或机构进行惩罚和纠正措施。
