7--第二章毛细管柱色谱法
安捷伦公司毛细管色谱柱

安捷伦公司毛细管色谱柱安捷伦公司的毛细管色谱柱自从Agilent公司合并了JW公司后其品质已达到世界一流水准就连它的价格也和DB系列完全一致。
HP-1-二甲基聚硅氧烷柱说明:这是最常用的非极性键合固定相,HP-1(二甲基聚硅氧烷),具有极好的热稳定性并且在高温下流失很小,具有低的检测限相似的固定相:DB-1,Rtx-1,SPB-1,CP Sil5CB,MDN-1,DB-1h.t.,AT-1007-1恒温/程序升温温度范围:-60至325/350℃,-60至300/320℃0.53内径,-60至260/280℃>2.0mm 液膜应用:胺类、烃类、农药、多氯联苯、酚类、含硫化合物HP-125m,0.20mm,0.33um HP-130m,0.32mm,0.25umHP-115m,0.25mm,0.25um HP-130m,0.32mm,1.0umHP-130m,0.25mm,0.25um HP-160m,0.32mm,0.25umHP-160m,0.25mm,0.25um HP-115m,0.53mm,1.5umHP-130m,0.53mm,2.65umHP-35-二苯基-65%-二甲基硅氧烷共聚物说明:HP-35柱是用苯基取代甲基的聚硅氧烷固定相柱。
EPA(美国环保暑)方法8081和UPS(美国药典)G-42中已经指定用此固定相。
HP-35的中极性使其成为分析杀虫剂、除草剂、药物和胺的良好选择。
相似的固定相:DB-35,Rtx-35,SPB-35,AT-35,Sup-herb等温/程序升温温度范围:-40至300/320℃40至280/300℃应用:芳氯物(Aroclors)、胺类、杀虫剂、药品HP-3515m,0.25mm,0.25um HP-3530m,0.32mm,0.15umHP-3530m,0.25mm,0.25um HP-3530m,0.32mm,0.25umHP-35,60meter,0.25mm,0.25um HP-3530m,0.32mm,0.5umHP-FFAP(键合和改性的交联聚乙二醇)说明:HP-FFAP柱主要特点是能够分析有机酸、游离脂肪酸或用于一些需要定量分析微量酸样品。
第二章色谱基础理论(本)
基础理论
46
基础理论
47
范氏方程说明:
▪ u一定时,A,B,C越小,H越小,柱效越
高,色谱峰越窄;颗粒越小,H越小,柱 效越高。
▪ U很小时,B/U项占主导,CU项可忽略 ▪ U很大时,CU项占主导,B/U项可忽略
基础理论
48
综合考虑: U实际稍高于Uopt 因为: 1.右侧曲线斜率小,U稍变化不会引起
拖尾因子(fs) x = h/20
fs =(B+A)/2A
fs = 0.95-1.05 正常峰
fs <0.95
前延峰
fs >1.05
拖尾峰
即使不进样也会出现的峰
20% - 100% MeOH
60
没有进样
15
30
问题:流动相脏
15
0
3
7
15
17
基础理论
13
二、定 性 参 数
W
(t tR )2
e 2 2
V 2
---呈正态分布 t=tR时,C=Cmax
基础理论
31
Cmax的影响因素:
进样量W愈大,则Cmax愈大,W与Cmax 成正比。 色谱柱内径愈小,填充愈紧密,Cmax/W比值愈
大。即柱愈细填充愈紧密,柱效N越高。 色谱柱愈短,Cmax值愈大。 先出柱的组分k’小,所以Cmax/W大。提高柱温 (GC),增加强洗脱剂的浓度(HPLC),可使
总结
●热力学:保留值的差 别要足够大 Sig
●动力学:色谱峰要
足够窄
Sig
基础理论
time time time 51
第四节 分子间作用力
基础理论
52
一、定向力
色谱法的基本原理

分子扩散项B/u
B = 2Dg
固定相填充在柱内后使气体扩散路径变弯曲的因素.
Dg 组分在气相中的扩散系数(cm2/s)。 填充柱γ= 0.5-0.7 毛细管柱 γ= 1.0 分子量大的组分Dg小,Dg反比于载气密度(分子量)
的平方根, 故采用分子量较大的载气可使B项降低。 保留时间长, 分子扩散项对色谱峰变宽的影响显著.
2021/6/10
3、按分离过程的物理化学原理分类
① 吸附色谱 (L-S,G-S):利用吸附剂对不同组分物理吸附性 能的差异进行分离。
② 分配色谱(L-L,G-L):利用不同组分在两相中分配系数的不 同进行分离。在液-液分配色谱中,根据流动相和固定相相对极性 不同,又分为正相分配色谱和反向分配色谱。
2021/6/10
假定:K = 1 Vs/Vm = 1 k = 1 n = 5 进样量w = 1
w=1μg 1ΔV 2ΔV 3ΔV 4ΔV
2021/6/10
①分布有一最大,两 边逐渐减小 ②最大及整个分布曲 线向后推移 ③流出曲线方程 (塔板理论方程)
在此检测得到位移 随时间变化曲线
被测物流出色谱柱时流动相中被测物浓度随体积(或时间)的变 化曲线:
组分在色谱柱中的保留时间tR包含了组分随流动相通过柱子所需的 时间和组分在固定相中滞留的时间;tR′实际上是组分在固定相中滞 留的时间。单位(s)或(cm)。
2021/6/10
死体积 Vm
不能被固定相滞留的(惰性)组分从进样到出现峰 最大值时所消耗的流动相的体积。死体积可由死时间 与流动相体积流速F0(L/min)计算:
2021/6/10
该理论模型对气相、液相色谱都适用。 Van Deemter方程的数学简化式为:
毛细管气相色谱法测定消毒剂中甲酚位置异构体

毛细管气相色谱法测定消毒剂中甲酚位置异构体赵凌国;尹江伟;付斌;曾双飞;周指明【摘要】建立了毛细管气相色谱法分离和测定消毒剂中3种甲酚位置异构体的方法。
消毒剂中的甲酚用乙醚进行萃取,HP-FFAP 毛细管柱进行分离,氢火焰离子化检测器检测,同时运用外标法和内标法进行定量分析。
乙醚、水杨醛(内标)、对甲酚、间甲酚和邻甲酚完全分离,峰面积和浓度的线性关系良好,3种甲酚位置异构体加标回收率为82%~107%,精密度 RSD 为2.6%~7.2%。
该方法简单、快速,具有良好的准确度和精密度,适用于消毒剂中3种甲酚位置异构体含量的测定。
%The cresol isomers were extracted by diethyl ether. Then they were separated on a HP-FFAP capillary column and analyzed by flame ionization detector. Both the external standard method and internal standard method were used for the quantitative analysis. Diethylether,salicylaldehyde,o-cresol、m-cresol and p-cresol were separated completely. A good linearity was found and the recoveries of cresol i-somers in sterilants ranged from 82% to 107%,and the relative standard deviations (RSDs)ranged from 2.6% to 7.2%. This method is fast,accurate and precise. It is feasible for determination of cresol isomers in sterilants.【期刊名称】《分析仪器》【年(卷),期】2016(000)004【总页数】5页(P32-36)【关键词】甲酚;气相色谱;消毒剂;异构体【作者】赵凌国;尹江伟;付斌;曾双飞;周指明【作者单位】深圳市宝安区疾病预防控制中心,深圳 518100;深圳市宝安区疾病预防控制中心,深圳 518100;深圳市宝安区疾病预防控制中心,深圳 518100;广东医学院,东莞 523808;深圳市宝安区疾病预防控制中心,深圳 518100【正文语种】中文甲酚是重要的精细化工中间体,同时也是环境中较为普遍的有机污染物,研究其分析方法具有重要意义。
第二章 色谱法的原理

按上述分配过程,对于n=5,k=1,m=1的体系,随 着脉动进入柱中板体积载气的增加,组分分布在柱内任一 板上的总量(气液两相中的总质量),由塔板理论可建流 出曲线方程:
C
m n V 2 exp[ (1 ) ] 2 Vr 2 Vr
n
m为组分质量,Vr为保留体积,n为理论塔板数。 当流动相体积V=Vr 时,C值最大,即
分离度和柱效率
理论需要解决的问题:
塔板理论和速率理论都难 以描述难分离物质对的实 际分离程度。即柱效为多 大时,相邻两组份能够被 完全分离。
难分离物质对分离度的大 小受色谱过程中两种因素 的综合影响:
保留值之差──色谱 过程的热力学因素; 区域宽度──色谱过 程的动力学因素。
色谱分离中的四种情况:
① 柱效较高,△K(分配系数)较 大,完全分离; ② △K不是很大,柱效较高,峰 较窄,基本上完全分离; ③ △K较大,柱效较低,但分离的 不好; ④ △K小,柱效低,分离效果更 差。
分离度:相邻两组分色谱峰保留值之差与两组分色谱峰底宽 总和之半的比值,(设W1=W2) 当R<1时,两峰有部分重叠; 当R=1时,分离程度可达98%;
分配系数K与分配比k的关系
cs ms / Vs Vm K k k cm mm / Vm Vs
相比率β:反映各种色谱柱型特点的参数 例如:填充柱,其β值一般为6~35; 毛细管柱,其β值为60~600。
二、 塔板理论(plate
theory)
最早由Martin等人提出塔板理论,把色 谱柱比作一个精馏塔,沿用精馏塔中塔板 的概念来描述组分在两相间的分配行为, 同时引入理论塔板数作为衡量柱效率的指 标。
毛细管气相色谱分析法

适和不脱尾为宜。对复杂的样品应采用程
序升温。
2020/9/29
29
五、 毛细管柱气相色谱系统
(一) 进样系统
进样器(样品导入部件)
进样系统
分流器 分流比阀
针形阀和电磁阀
2020/9/29
30
2020/9/29
31
毛细管柱色谱进样方式分为两类:
分流进样和不分流进样。
根据操作方式,不分流进样又包括柱 上进样和直接进样。
u
2k 3(1 k)2
d
2 f
Ds
u
2020/9/29
5
与填充柱速率理论比较:
(1)毛细管柱中,A=0
(2)在毛细管柱中,因无填料,因此,
阻碍因子γ=0
(3)在毛细管柱中,以柱半径r代替
填料颗粒直径dp,且Cs一般比填充柱小,
气相传质阻抗常为色谱峰展宽的重要 因素。
2020/9/29
6
三、 速率方程讨论
2020/9/29
26
柱温与相对保留值的关系:
lg a b
T
温度范围较窄时,可以写成下式:
a aT b
根据a′数值的大小,曲线的斜率有三种情况: (1) a′为负值,表示降低柱温,会使相对保留
值增大; (2) a′近于0,无论柱温如何变化,相对保留值
保持不变; (3) a′大于0,柱温降低,相对保留值也减小。
2020/9/29
7
(二)最佳适用载气线速度
从速率方程可知,最小板高时的最佳流速:
uopt B (Cm Cs )
对于毛细管柱而言,固定液液膜薄,值较大,Cs Cm,因此,
uopt
B u 4Dm r
3(1 k)2 1 6k 11k 2
气相色谱柱填充柱,毛细管柱

第二章 气相色谱柱第一节气相色谱柱的类型气相色谱法(gas chromatography, 简称GC)亦称气体色谱法,气相层析法。
其核心即为色谱柱。
气相色谱柱有多种类型。
从不同的角度出发,可按色谱柱的材料、形状、柱内径的大小和长度、固定液的化学性能等进行分类。
色谱柱使用的材料通常有玻璃、石英玻璃、不锈钢和聚四氟乙烯等,根据所使用的材质分别称之为玻璃柱、石英玻璃柱、不锈钢柱和聚四氟乙烯管柱等。
在毛细管色谱中目前普遍使用的是玻璃和石英玻璃柱,后者应用范围最广。
对于填充柱色谱, 大多数情况下使用不锈钢柱,其形状有U型的和螺旋型的,使用U型柱时柱效较高。
按照色谱柱内径的大小和长度,又可分为填充柱和毛细管柱。
前者的内径在2~4mm,长度为1~10m左右;后者内径在0.2~0.5mm,长度一般在25~100m。
在满足分离度的情况下,为提高分离速度,现在也有人使用高柱效、薄液膜的10m短柱。
根据固定液的化学性能,色谱柱可分为非极性、极性与手性色谱分离柱等。
固定液的种类繁多,极性各不相同。
色谱柱对混合样品的分离能力,往往取决于固定液的极性。
常用的固定液有烃类、聚硅氧烷类、醇类、醚类、酯类以及腈和腈醚类等。
新近发展的手性色谱柱使用的是手性固定液,主要有手性氨基酸衍生物、手性金属配合物、冠醚、杯芳烃和环糊精衍生物等。
其中以环糊精及其衍生物为色谱固定液的手性色谱柱,用于分离各种对映体十分有效,是近年来发展极为迅速且应用前景相当广阔的一种手性色谱柱。
在进行气相色谱分析时,色谱柱的选择是至关重要的。
不仅要考虑被测组分的性质,实验条件例如柱温、柱压的高低,还应注意和检测器的性能相匹配。
有关内容我们将在以后章节中加以详细讨论。
第二节填充气相色谱柱 填充气相色谱柱通常简称填充柱,在实际分析工作中的应用非常普遍。
据资料统计,日常色谱分析工作大约有80%是采用填充柱完成的。
填充柱在分离效能和分析速度方面比毛细管柱差,但填充柱的制备方法比较简单,定量分析的准确度较高,特别是在某些分析领域(例如气体分析、痕量水分析)具有独特用途。
毛细管柱简单知识

毛细管气相色谱简单知识一、毛细管柱与填充柱的区别与填充柱相比,毛细管柱的特点为:1.分离效能高2.分析速度快3.样品用量少可在几十分钟内分离出包含几百种化合物的汽油馏分,然而样品用量仅有数微克在快速分析方面,可在几秒钟内分离含十几个组份的样品。
其独特的特点在于:渗透性大,分析速度快传质阻力小,可用长柱,并得高的总柱效。
色谱动力学认为:填充柱可看作是一束长毛细管的组合,其内径约等于粒子粒度,因其弯曲,多径扩散严重,故理论板数少。
毛细管柱完全没有这些缺陷,故理论板数可高大106数量级。
用毛细管柱,有利于:提高色谱分离能力,加快色谱分析速度,促进色谱的应用都是十分必要的:二、毛细管色谱法的相关理论在毛细管柱,柱内只有一个流路,故多径项2ldp为0,弯曲因子g=1,且用其液膜厚代替了填充柱中载体的颗粒直径dp。
2.毛细管柱的最小理论板高毛细管柱的H—U图也是一个双曲线,在U值是最佳值时,H值最小。
式中Cg、C1的大小取决于分配系数及柱的几何性(以相比β为代表),但一般毛细管柱液膜薄,β值较大,液相传质阻力C1项不起控制作用。
当被测物质的k﹥10时,如果每米理论板数大于1000/d时,则所用柱子的性能较好表中为K值很大时最好柱效(每米板数)值,其值由H/L = 1000 / d一般认为直径在0.1—0.7mm较好小于0.1mm,入口压力增加,柱负荷减少大于0.7mm,虽柱负荷增大,但柱效下降目前流行0.53mm的大口径管,不必分流。
3.载气线速从速率方程可知,最小板高时的最佳线速为:如果Cl很小,则有:可见,细管径,轻载气更适合于快速分析。
4.样品容量一根色谱柱的最大允许进样量,约为一块理论板的有效体积。
可见最大允许进样量与柱半径、柱长、分配比成正比,与塔板数成反比比较填充柱和毛细管柱的柱容量一根长20米,内径为0.25毫米的毛细管柱,一般可涂上6 mg的固定液,柱内体积而一根长两米,内径3毫米的不锈钢填充柱,柱内体积按12:100的液载比,可涂上800mg固定液。
色谱分析(中国药科大学)第2章色谱法的基本参数及理论
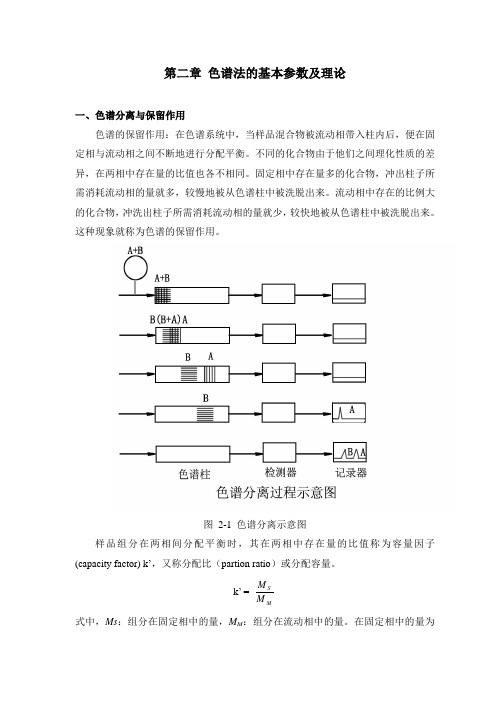
第二章 色谱法的基本参数及理论一、色谱分离与保留作用色谱的保留作用:在色谱系统中,当样品混合物被流动相带入柱内后,便在固定相与流动相之间不断地进行分配平衡。
不同的化合物由于他们之间理化性质的差异,在两相中存在量的比值也各不相同。
固定相中存在量多的化合物,冲出柱子所需消耗流动相的量就多,较慢地被从色谱柱中被洗脱出来。
流动相中存在的比例大的化合物,冲洗出柱子所需消耗流动相的量就少,较快地被从色谱柱中被洗脱出来。
这种现象就称为色谱的保留作用。
图 2-1 色谱分离示意图样品组分在两相间分配平衡时,其在两相中存在量的比值称为容量因子(capacity factor) k ’,又称分配比(partion ratio )或分配容量。
k ’ = MS M M 式中,Ms :组分在固定相中的量,M M :组分在流动相中的量。
在固定相中的量为零的化合物,其k ’=0,这些组分被称为在该色谱条件下的非保留物质。
容量因子(分配比)可通过实验计算:k ’ =MR t t ' 。
即k ’为组分在固定相中消耗的时间与其在流动相中消耗的时间之比。
样品组分在两相中分配平衡时,其在固定相和流动相中的浓度比称为分配系数(partion factor ),分配系数以K 表示。
其公式如下:Ms c c K ==组分在流动相中的浓度组分在固定相中的浓度 K =m m S S V M V M // = k ’· S m V V 式中,Ms/Vs 为样品组分在固定相中的浓度,M m /V m 为样品组分在流动相中的浓度。
分配系数大的组分保留时间长(色谱的保留作用强),分配系数小的组分保留时间短(色谱的保留作用弱)。
K = k ’· Sm V V = k ’· β 式中β = Sm V V 称为相比率,即色谱柱中流动相体积与固定相体积之比。
例在毛细管GC 中壁涂空心柱的相比为:β = 固定相体积(柱中)流动相体积(柱中) = dfrl l r ⋅ππ22 = df r 2式中r为毛细管柱横截面的半径,d f为柱内壁固定液的膜厚。
第二章 色谱法原理

保留时间是色谱法定性的基本依 据,但同一组分的保留时间常受到流
动相流速的影响,因此色谱工作者有
时用保留体积来表示保留值。
6. 保留体积VR 指从进样开始到被测组分在柱后出 现浓度极大点时所通过的流动相的体积。 保留时间与保留体积关系:
VR= tR Fco
7.调整保留体积VR 某组分的保留体积扣除死体积后,称 为该组分的调整保留体积。
以后每当一个新的板体积载气以脉动式进入 色谱柱时,上述过程就重复一次,如下所示:
塔板号r 进样 q p 0 0.5 0.5 0.25 0.25 0.25 0.25 0.125 0.125 1 2 3
进气1△V q p
进气2△V q 0.125 0.125+0.125 p 0.125 0.125+0.125
色谱图(无铅汽油)
农药
碳酸饮料
2、 区域宽度 色谱峰的区域宽度是色谱流出曲线 的重要参数之一,用于衡量柱效率及反 映色谱操作条件的动力学因素。表示色 谱峰区域宽度通常有三种方法。
1.标准偏差---即0.607倍峰高处色谱 峰宽的一半。 2.半峰宽Y1/2---即峰高一半处对应的峰 宽。它与标准偏差的关系为 Y1/2=2.354 3.峰底宽度Y---即色谱峰两侧拐点上的 切线在基线上截距间的距离。它与标 准偏差的关系是 Y = 4
始于马丁(Martin)和辛格(Synge)
提出的塔板模型。
分馏塔:在塔板上多次气液平衡,按沸
点不同而分离。
色谱柱:组分在两相间的多次分配平衡,
按分配系数不同而分离。
板式精馏塔
塔板理论的导出 将色谱分离过程比拟作蒸 馏过程,引用了处理蒸馏过程 的概念、理论和方法来处理色 谱过程。把色谱柱比作一个分 馏塔,色谱柱可由许多假想的 塔板组成(既色谱柱可分成许 多小段),
毛细管柱气相色谱法测定羟丙甲纤维素中甲氧基和羟丙氧基的含量

基金项目:浙江省科技厅大仪协作平台科研课题(2008F70049)作者简介:郑金琪,男,硕士,主管药师 研究方向:药物质量分析 Tel :(0571)86459422 Fax :(0571)86459413 E-mail :jingqizheng@ hotmail. com毛细管柱气相色谱法测定羟丙甲纤维素中甲氧基和羟丙氧基的含量郑金琪1,郑国钢1,李会林1,朱伟2(1. 浙江省食品药品检验所,杭州 310004;2. 浙江大学城市学院医学与生命科学学院,杭州 310015)摘要:目的 建立毛细管柱GC 法测定羟丙甲纤维素中甲氧基和羟丙氧基含量的方法。
方法 通过氢碘酸与羟丙甲纤维素中的甲氧基和羟丙氧基反应生成挥发性的碘甲烷和2-碘丙烷,毛细管柱GC 法测定碘甲烷和2-碘丙烷来计算羟丙甲纤维素中甲氧基和羟丙氧基的含量。
采用DB -624石英毛细管柱(30 m ×0.53 mm ,3.0 μm );检测器: 氢火焰离子化检测器;柱温: 程序升温,100 ℃保持10 min ,然后以50 ℃·min -1升温至230 ℃,保持2 min ;进样口温度200 ℃;检测器温度250 ℃;载气: 氮气;流速:3.0 mL·min -1。
以正辛烷为内标物, 内标法定量。
结果 甲氧基在(2.443~19.57) g·L - 1 内与峰面积呈良好的线性关系(r =0.999 1,n =7),回收率98.8%(RSD=0.64% ,n =9);羟丙氧基在(0.4351~7.494) g·L - 1 内与峰面积呈良好的线性关系(r =0.999 5,n =7),回收率99.1%(RSD=0.45% ,n =9);分析了3批样品,甲氧基的含量为29.0%~29.4%,羟丙氧基的含量为8.48%~8.61%。
结论 本法专属性强,分离度高,操作简便,结果准确,为更好地控制羟丙甲纤维素的质量提供了切实可行的方法。
天然药物化学(中药化学)中药化学第二章2(3)色谱分离技术

浓缩
柱层析操作(跑柱子)
二)、薄层色谱
粒径 5~40 m
1.吸附剂
硅胶
硅胶H 硅胶G 硅胶GF254 硅胶HF254
常用
氧化铝 硅藻土
聚酰胺
微晶纤维素
想一想 H、G、F各代表何种意思?试解释硅胶HF365?
种类
玻璃板 塑料膜
厚度 2mm
规格
5cm×20cm 10cm×10cm 10cm×15cm
紫外分析仪(三用)
6.检视装置
摄像设备
薄层色谱扫描仪(CS9301型)
7、操作技术
分类 自制薄层板
无黏合剂 含黏合剂
10%~15%煅石膏
0.2%~0.5%羧甲基纤维素钠水 溶液
1.薄层板 制备
市售薄层 板
操作方法
普通薄层板(玻璃、聚酰胺薄膜和铝基)
分类
高效薄层板(固定相粒径为5~7 )um
操作方法
临用前一般应在110℃活化30分钟。聚酰胺薄膜不需活 化。铝基片薄层板和聚酰胺薄膜可根据需要剪裁
制板操作方法
• 将1份固定相和3份水(或羧甲基纤维素钠水 溶液)在研钵中沿同一方向研磨混匀,去除 表面的气泡后,置玻璃板上使涂布均匀,或 倒入涂布器(见图8-14)中,在玻板上平稳 地移动涂布器进行涂布(涂层厚度为0.2mm~ 0.3 mm),取涂好的薄层板,置水平台上于室 温下晾干后,在110℃活化30分钟,立即置于 有干燥剂的干燥器中备用 。
薄层色谱(TLC) 纸色谱(PC) 薄膜色谱(TFC)
一、吸附色谱:利用吸附剂对被分离化合物分子 的吸附能力的差别而实现分离的一类色谱。
硅胶
氧化铝 活性炭 聚酰胺
吸附原理
物理吸附
化学吸附——碱 性化合物
仪器分析-气相色谱分析

• 3、保留值:是试样各组分在
色谱柱中保留行为的量度,它 反映组分与固定相间作用力大 小,通常用保留时间和保留体 积表示。 死时间tM:不被固定相吸附或 溶解的组分(如空气、甲烷) 从进样到出现其色谱蜂最大值 所需的时间,图中O'A'所示。 保留时间tR :指某组分通过 色谱柱所需时间,即试样从进 样到出现峰极大值时的时间, 图中O‘B所示。 调整保留时间tR’ 死时间后的 保留时间,它是组分在固定相 中的滞留时间。图中A’B所示, 即 tR’ = tR - tM
通常以有效塔板数neff 和有效塔板高度Heff 表示:
neff H eff
t t 2 5.5 4( ) 1 6( )2 W1 / 2 Wb L neff
' R
' R
2-2-3 速率理论
• 塔板理论存在的假定有缺陷,不能解释塔板高度H
受那些因素影响. 1956年,荷兰化学工程师van Deemter提出了色谱过程动力学速率理论。 • van Deemter方程:H=A+B/u+C*u u 为流动相线速度; A,B,C 为常数. 其中: A — 涡流扩散系数; B — 分子扩散系数; C — 传质阻力系数(包括液相和固相传质阻力系 数)
• 1、气路系统
• 载气:H2,N2,He,Ar等 • 净化器:提高载气纯度 • 稳压恒流装置,气体流速控制和测量。
• 2、进样系统
• 进样器: 微量注射器、六通阀 • 气化室:瞬间气化,死体积尽可能小
• 3、分离系统
• 色谱柱有填充柱和毛细管柱两大类
2-1-3 组成
• • • • •
4、温控系统 色谱柱、气化室、检测室三处温度控制 气化室温度应使试样瞬间气化但又不分解; 检测器除氢火焰外都对温度敏感; 柱温的变化影响柱的选择性和柱效,因此柱室的 温度控制要求精确,温控反复根据需要可以恒温, 也可以程序升温。
毛细管色谱柱简介

毛细管柱简介(仅供参考)Varian(瓦里安)-Chrompack公司毛细管柱简介CP-Sil 2 CB最低极性化学键合柱对环烃具独有的选择性含高分子量烃的交联石英,近似于Squalane柱最低操作温度:25℃最高操作温度:200/200℃The CP-Sil 2 CB柱基本上根据沸点完成分离,世界上许多石化实验室已经由过去使用Squalane柱改成CP-Sil 2 CB柱,这是因为CP-Sil 2 CB柱的:由于化学键合特性,因此具极佳的稳定性更高的最高操作温度对环烃具特有的选择性更大的进样体积应用:农药除草剂抗抑郁药Antidepressants 芳香烃烃 Oxygenates PAHs 溶剂CP-Sil 5 CB 温度极限℃ 330/350组成:100%二甲基聚硅氧烷确保重现性高柱效,高惰性OV-1型柱有融合石英柱和Ultimetal柱0.15mm柱适合于快速分析等同产品:DB-1 HP-1 Rtx-1 SPB-1极性特征CP-Sil 5 CB毛细管柱几乎完全根据沸点分离,因此在该柱的温度范围内具广范围的应用,又由于固定相与色谱柱致密的交联特性,CP-Sil 5 CB能承受大体积进样,确保最大的柱寿命。
应用:醇类醛类胺类芳香烃 EPA方法610 酯类香料游离脂肪酸二醇类卤代烃烃酮 Odours 有机酸 Oxygenates PAHs农药多聚物Polymers 溶剂甾族化合物CP-Sil 5 CB 低流失/MS毛细管柱温度极限℃ 325/350特性:超低流失;100%二甲基聚硅氧烷更高柱效,尤其是用于痕量分析逐个测试,确保超低流失0.15mm微孔柱(micro-bore)专用于快速分析本柱无等同产品应用:醇类、醛类、胺类、芳香烃、EPA方法610 、酯类、香料、游离脂肪酸、二醇类、卤代烃、烃、酮、Odours、有机酸、Oxygenates、PAHs 、农药、多聚物、甾族化合物、溶剂和含硫化合物等CP-Sil 8 CB5%苯基,95%二甲基聚硅氧烷保证无误的重现性,选择性和保留时间高柱效,长寿命SE-54类型柱有熔融石英柱和Ultimetal钢柱0.15mm微孔柱(micro-bore)专用于快速分析极性特征由于加入了5%的苯基基团,CP-Sil 8 CB毛细管柱比CP-Sil 5 CB的极性要高,这就意味着对芳香族化合物具更好的选择性.而且,在建立方法时CP-Sil 8 CB通常是最好的选择,CP-Sil 8 CB柱具优越的柱柱重现性和很高的柱效。
毛细管柱气相色谱法

第六章毛细管柱气相色谱法第一节毛细管气相色谱仪现代的实验室用的气相色谱仪大都既可用作填充柱气相色谱又可用作毛细管色谱仪。
毛细管色谱仪应用范围广,可用于分析复杂有机物,如石油成分,天然产物,环境污染,农药残留等。
图6-1是毛细管气相色谱仪示意图,与填充柱色谱仪比,毛细管色谱仪在柱前多一个分流-不分流进样器,柱后加一个尾吹气路。
由于毛细管柱体积很小,柱容量很小,出峰快,所以死体积一定要小,要求瞬间注入极小量样品,因此柱前要分流。
对进样技术要求高,对操作条件要求严。
尾吹的目的是减小死体积和柱末端效应。
毛细管柱对固定液的要求不苛刻,一般2-3根不同极性的柱子可解决大部分的分析问题。
毛细管柱一般配有响应快,灵敏度高的质量型检测器。
高分辨率毛细管气相色谱仪的三要素是:要选择好的毛细管柱及最佳分析条件;按样品选择合适的毛细管进样系统;选择高性能的毛细管气相色谱仪。
图6-1 毛细管气相色谱仪示意图第二节毛细管色谱柱1957年,美国科学家Golay提出毛细管柱的气相色谱法。
Golay称毛细管色谱柱为开管柱。
因这种色谱柱中心是空的。
毛细管柱是内径为Φ0.1-0.5mm左右、长度为10-300m的毛细柱,虽然每米理论板数约为2000-5000,与填充柱相当,但由于柱子很长,总柱效可高达106。
一、毛细管色谱柱组成通常来说,一根毛细管色谱柱由管身和固定相两部分组成。
管身采用熔融二氧化硅(熔融石英),通常在其表面涂上一层聚酰亚胺保护层。
涂层后的熔融石英毛细管呈褐色:但是涂层后的毛细管之间的颜色却不尽相同。
色谱柱的颜色对于其色谱性能没有什么影响。
经过持续的较高温度处理后.聚酰亚胺涂层管的的温度会变得比以前更深:标准的聚酰亚胺涂层管熔融石英管的温度上限为360℃,高温聚酰亚胺涂层管的温度上限为400℃。
固定相种类很多,大部分的固定相是热稳定性好的聚合物,常用的有聚硅氧烷和聚乙二醇。
另外还有一类是小的多孔粒子组成的聚合物或沸石(例如氧化铝、分子筛等)。
环境仪器分析:第2章 色谱分析法
第二节 气相色谱理论基础
色谱分析的目的是将样品中各组分彼此分离,组 分要达到完全分离,两峰间的距离必须足够远。两峰 间的距离是由组分在两相间的分配系数决定的,即与 色谱过程的热力学性质有关。但是两峰间虽有一定距 离,如果每个峰都很宽,以致彼此重叠,还是不能分 开。这些峰的宽或窄是由组分在色谱柱中传质和扩散 行为决定的,即与色谱过程的动力学性质有关。因此, 要从热力学和动力学两方面来研究色谱行为。
对A、B两组分的选择因子,用下式表示:
α= tR(B)/tR(A)= k(A)/k(B)=K(A)/K(B)
通过选
择因子α把实验测量值k与热力学性质的分配系数K直接联系起来,
α对固定相的选择具有实际意义。如果两组分的K或k值相等,则
α=1,两个组分的色谱峰必将重合,说明分不开。两组分的K或k
值相差越大,则分离得越好。因此两组分具有不同的分配系数是
它不仅随柱温、柱压变化而变化,而且还与流动相及固定相的体 积有关。
k = ms/mm =CsVs/CmVm
式中cs,cm分别为组分在固定相和流动相的浓度;Vm为柱中流 动相的体积,近似等于死体积。Vs为柱中固定相的体积,在各种 不同类型的色谱中有不同的含义。
例如:在分配色谱中,Vs表示固定液的Байду номын сангаас积;在尺寸排阻色谱中, 则表示固定相的孔体积。
➢基线漂移(baseline drift):基线随时间定向的缓慢变化。
➢基线噪声(baseline noise):指各种因素所引起的基线起 伏。
3. 峰高 色谱峰顶点与基线之间的垂直距离,以(h)表示。
4. 保留值 (1) 死时间 tM 不被固定相吸附或溶解的物质(如空气、甲烷)
7色谱分离原理

分配系数
容量因子或分配比 capacity factor
relative retention
ris
?
t'R(i) t'R(s)
?
V'R(i) V'R( s)
distribution coefficient
K ? cs cm
k ? csVs k ? KVs
cmVm
Vm
k ? t'R ? V'R tM VM
色谱法起着关键作用的诺贝尔奖研究工作年代获奖学科获奖研究工作1937化学类胡萝卜素化学维生素a和b1938化学类胡萝卜素化学1939化学1950生理学医学性激素化学及其分离肾皮素化学及其分离1951化学超铀元素的发现1955化学脑下腺激素的研究和第一次合成聚肽激素1958化学胰岛素的结构1961化学光合作用时发生的化学反应的确认1970生理学医学关于神经元触处迁移物质的研究1970化学糖核苷酸的发现及其在生物合成碳水化合物中的作用1972化学核糖核酸化学酶结构的研究1972生理学医学抗体结构的研究72色谱法chromatography以试样组分在固定相和流动相间的溶解吸附分配离子交换或其他亲和作用的差异为依据而建立起来的各种分离分析方法
留值定性的基础
液相色谱保留规律
液相色谱保留值方程 :
1. 二元溶剂反相色谱:
ln k ? A? CcB
cB为流动相中有机相 浓度,C<0, 即容量 因子随cB增加而减少
但蛋白质和多肽空间结构随溶剂疏水性而改变,其保留值呈 非线性变化
? 2. 多元溶剂反相色谱: ln k ? A?
CicBi 近似式
相(即气相色谱)。 发明了 纸色谱 。 氧化铝中加淀粉黏合剂制作薄层板使薄层色谱进入实用阶段。 从理论和实践方面完善了 气-液分配色谱 法。 提出色谱 速率理论,并应用于气相色谱。 基于离子交换色谱的氨基酸分析专用仪器问世。 发明毛细管柱气相色谱 。 发表凝胶过滤色谱的报告。 发明凝胶渗透色谱 。 发展了色谱理论,为色谱学的发展奠定了理论基础。 发明了以离子交换剂为固定相、强电解质为流动相,采用抑制型
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、毛细管色谱柱
毛细管柱可由不锈钢,玻璃等制成。 不锈钢毛细管柱由于惰性差,有一定的催化活性。加上不 透明,不易涂渍固定液,已很少使用。
玻璃毛细管柱表面惰性较好,表面易观察,因此长期在使用, 但易折断,安装较困难。 用熔融石英作柱子,这种色谱柱具有化学惰性,热稳定性及 机械强度好,并具有弹性,占有主导地位。
第八节 毛细管柱气相色谱
毛细管柱气相色谱法是用毛细管柱作为气相色谱柱的一 种高效、快速、高灵敏的分离分析法。 用内壁涂渍一层极薄而均匀的固定液膜的毛细管代替填 充柱,解决组分在填充柱中由于受到大小不均匀载体颗 粒的阻碍而造成的色谱峰扩展,柱效降低的问题。 这种色谱柱的固定液涂在内壁上,中心是空的,故称开 管柱,可惯称毛细管柱。 由于毛细管柱具有相比大,渗透性好,分析速度快,总 柱效高等优点,因此可以解决原来填充柱色谱法不能解 决或很难解决的问题。
三、毛细管柱的色谱系统
分流进样:是将液体试样注入进样器使其气化并与载气均匀混合, 然后让少量试样进入色谱柱,大量试样放空。 放空的试样量与进入毛细管柱试样的比称为流比,通常控制在 50:1,500:1。 尚未能很好适用于痕量组分的定量分析以及定量求高的分析。
目前发展了多种进样技术,冷柱头进样等。
习题讲解
(3)流动相流速增加:不会引起分配系数改变
(4)相比减少:不会引起分配系数改变
4.当下列参数改变时: (1)柱长增加,(2)固定相量增加,(3)流动 相流速减小,(4)相比增大,是否会引起分配比的变化?为什么? 答: k=K/ β ,而β =VM/VS ,分配比k除了与组分、两相的性质、 柱温、柱压有关外,还与相比β 有关,而与流动相流速,柱长无关。 故:
二、毛细色谱柱的特点
1、渗透性好,即载气流动阻力小。
柱渗透性一般用比渗透率B0表示 ,毛细管柱的比渗透率约 为开管柱的100倍,这样就可以在同样柱压降的情况下使用 100米以上的柱子而载气速度维持不变。 2、相比(β )大,有利于实现快速分析。 3、柱容量小,允许进样量少。 4、总柱效高,分离复杂混合物的能力大为提高。
解:定性依据为根据组分在色谱柱中保留值的不同进行定性。 主要的定性方法主要有以下几种: (1)直接根据色谱保留值进行定性; (2)利用相对保留值r21进行定性; (3)混合进样; (4)多柱法; (5)保留指数法; (6)联用技术; (7)利用选择性检测器。
20.在一根2 m长的色谱柱上,分析一个混合物,得到以下数 据:苯、甲苯、及乙苯的保留时间分别为1’20”, 2’2” 及3’1”;半峰宽为0.211cm, 0.291cm, 0.409cm,已知记 录纸速为1200mm/h, 求色谱柱对每种组分的理论塔板数及 塔板高度。 解:三种组分保留值用记录纸上的距离表示时为: 苯: (1+20/60)×[(1200/10)/60]=2.67cm 甲苯:(2+2/60) ×2=4.07cm 乙苯: (3+1/60) ×2=6.03cm
毛细管柱按其固定液的涂渍方法可分为:
1.壁涂开管柱(WCOT):将固定液直接涂在毛细管 内壁上,它是戈雷最早提出的毛细管柱。 由于管壁的表面光滑,润湿性差,对表面接触角大 的固定液,直接涂渍制柱,重现性差,柱寿命短。 现在的WCOT柱,减小表面接触角,再涂固定液。 2.多孔层开管柱(PLOT):在管壁上涂一层多孔性 吸附剂固体颗粒,不再涂固定液,实际上是使用开 管柱的气固色谱。
3.载体涂渍开管柱(SCOT) 为了增大开管柱内固定液的涂渍量,先在毛细管内壁上涂一层 很细的(<2mm)多孔颗粒,然后再在多孔层上涂渍固定液, 这种毛细管柱,液膜较厚,因此柱容量较壁涂开管柱(WCOT) 柱高。 4.化学键合相毛细管柱 将固定相用化学键合方法键合到硅胶涂敷的柱表面或经表面处 理的毛细管内壁上。经过化学键合,大大提高了柱的热稳定性。 5.交联毛细管柱。由交联剂将固定相交联到毛细管管壁上。这 类柱子具有耐高温,抗溶剂抽提,液膜稳定,柱效高,柱寿命 长等特点。发展很快。
(1)柱长增加,分配比不变化;
(2)固定相量增加,分配比增加; (3)流动相流速减小,分配比不改变; 1)增大分配比,(2) 流动相速度增加, (3)减小相比, (4) 提高柱温,是否会使色谱峰变窄?为什么? 答:(1)保留时间延长,峰形变宽;
3.当下列参数改变时:(1)柱长缩短,(2)固定相改变,(3)流动相流 速增加,(4)相比减少,是否会引起分配系数的改变?为什么? 答:固定相改变会引起分配系数的改变,因为分配系数只与组 分的性质及固定相与流动相的性质有关。所以 (1)柱长缩短:不会引起分配系数改变 (2)固定相改变:会引起分配系数改变
(2)保留时间缩短,峰形变窄;
(3)保留时间延长,峰形变宽; (4)保留时间缩短,峰形变窄。
9.能否根据理论塔板数来判断分离的可能性?为什么?
答: 不能,有效塔板数仅表示柱效能的高低,柱分离能力发 挥程度的标志,而分离的可能性取决于组分在固定相和流动 相之间分配系数的差异。
16.色谱定性的依据是什么?主要有那些定性方法?
故理论塔板数及塔板高度分别为:
n苯 tR 2 =5.54( ) =887.09 Y1/2 H苯=L/ n苯 =0.23cm
甲苯和乙苯分别为:1083.7,0.18cm; 1204.2,0.17cm
