ACYW135群脑膜炎球菌多糖疫苗接种知情同意书(2019年版)可编辑
一类疫苗知情同意书

一类疫苗知情同意书篇一:一类疫苗接种知情同意书A群C群脑膜炎球菌多糖疫苗接种知情同意书流行性脑脊髓膜炎,简称流脑,是由脑膜炎奈瑟氏菌(双球菌)引起的急性化脓性脑膜炎。
病原菌有13个亚群,90%以上为A、B、C三个亚群,主要通过咳嗽、打喷嚏借飞沫由呼吸道直接传播。
在5岁以下尤其是6个月至2岁的婴幼儿的发病率最高。
其主要临床表现为突然高热、剧烈头痛、频繁呕吐、皮肤黏膜瘀点、瘀斑及脑膜刺激征,严重者可有败血症休克和脑实质损害,常可危及生命。
接种A群C群脑膜炎球菌多糖疫苗是预防A 群和C群脑膜炎奈瑟球菌引起流行性脑脊髓膜炎的有效手段。
【接种对象和免疫程序】2 周岁以上儿童及成人。
国家免疫程序规定在3周岁和6周岁时各接种一次,两剂次间隔≥3年;第1剂次与A群流脑疫苗第2剂次间隔≥12个月。
于上臂外侧三角肌皮下注射0.5ml。
【禁忌症】⑴ 已知对该疫苗的任何成分过敏者。
⑵ 患急性疾病、严重慢性疾病、慢性疾病的急性发作期和发热者。
⑶ 患脑病、未控制的癫痫和其他进行性神经系统疾病者。
【注意事项】⑴ 以下情况者慎用:家族和个人有惊厥史者、患慢性疾病者、有癫痫史者、过敏体质者、哺乳期妇女。
⑵ 对适龄儿童免费接种。
⑶ 接种后需在接种单位的留观区域观察30分钟,无不良反应方可离开。
⑷ 任何疫苗的保护效果还不能达到100%。
少数人接种后未产生保护力,或者仍然发病,与疫苗本身特性和受种者个人体质有关。
⑸ 家长(监护人)应如实提供儿童健康状况、有无过敏史、患病史和家族病史等。
【不良反应】少数人接种后24小时内可出现注射部位疼痛和触痛,注射局部有红肿、浸润等轻、中度反应,多数情况下2~3天内自行缓解。
也可能出现一过性发热反应。
其中大多数为轻度发热反应,一般持续1~2天后可自行缓解,不需处理;对于中度发热反应或发热时间超过48小时者,可给予对症处理。
如出现其它严重不良反应,应及时诊治并与接种单位联系。
A群脑膜炎球菌多糖疫苗接种知情同意书流行性脑脊髓膜炎,简称流脑,是由脑膜炎奈瑟氏菌(双球菌)引起的急性化脓性脑膜炎。
ACYW135群四价流脑多糖疫苗接种告知书
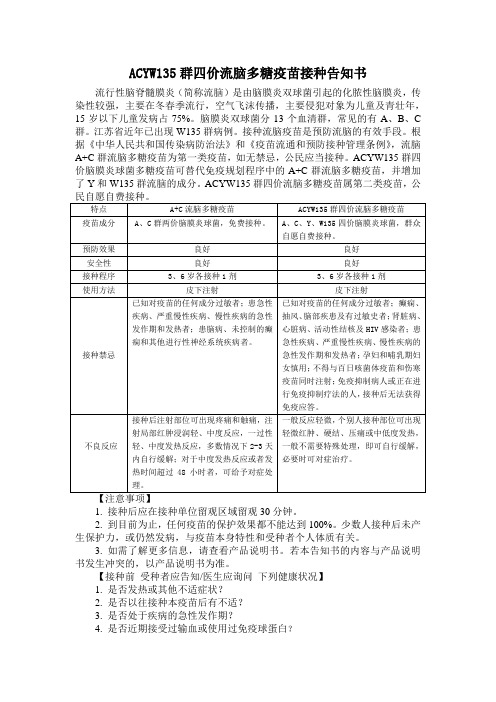
ACYW135群四价流脑多糖疫苗接种告知书
流行性脑脊髓膜炎(简称流脑)是由脑膜炎双球菌引起的化脓性脑膜炎,传染性较强,主要在冬春季流行,空气飞沫传播,主要侵犯对象为儿童及青壮年,15岁以下儿童发病占75%。
脑膜炎双球菌分13个血清群,常见的有A、B、C 群。
江苏省近年已出现W135群病例。
接种流脑疫苗是预防流脑的有效手段。
根据《中华人民共和国传染病防治法》和《疫苗流通和预防接种管理条例》,流脑A+C群流脑多糖疫苗为第一类疫苗,如无禁忌,公民应当接种。
ACYW135群四价脑膜炎球菌多糖疫苗可替代免疫规划程序中的A+C群流脑多糖疫苗,并增加了Y和W135群流脑的成分。
ACYW135群四价流脑多糖疫苗属第二类疫苗,公
1. 接种后应在接种单位留观区域留观30分钟。
2. 到目前为止,任何疫苗的保护效果都不能达到100%。
少数人接种后未产生保护力,或仍然发病,与疫苗本身特性和受种者个人体质有关。
3. 如需了解更多信息,请查看产品说明书。
若本告知书的内容与产品说明书发生冲突的,以产品说明书为准。
【接种前受种者应告知/医生应询问下列健康状况】
1. 是否发热或其他不适症状?
2. 是否以往接种本疫苗后有不适?
3. 是否处于疾病的急性发作期?
4. 是否近期接受过输血或使用过免疫球蛋白?。
A、C、Y、W135群脑膜炎球菌多糖疫苗知情告知书

A、C、Y、W135群脑膜炎球菌多糖疫苗接种通知单
编号
村名
家长姓名
儿童姓名
性别
年龄岁
家长接种意见:我已阅过右联的内容,同意为我的孩子接种A、C、Y、W135流脑多糖疫苗。
家长签名
A、C、Y、W135群脑膜炎球菌多糖疫苗知情告知书
流行性脑脊髓膜炎(流脑)是一种冬春季节常见的急性呼吸道传染病,通过空气传播,多发生于婴幼儿及儿童,发病急,表现为突发高热、头痛、呕吐、乏力、颈项强直等脑膜刺激症,严重者可导致残疾或死亡,病死率高达10%左右,存活者会留下痴呆、肢体障碍等神经系统后遗症。
目前我国已出现由Y、W135脑膜炎球菌菌群引起的流脑。
对2岁以上儿童、青少年及成人接种A、C、Y、W135群流脑疫苗是预防流脑最经济、有效的方法,可以同时预防由A、C、Y、W135群脑膜炎球菌菌群引起的流脑。
为了您或您孩子的健康,家庭的幸福,如您或您的孩子无癫痫、抽风、脑部疾患、肾脏病、心脏病、活动性结核及对疫苗的成分过敏,请及时接种疫苗。
四价疫苗属于二类疫苗,请遵照“知情、自愿、自费”原则;接种A、C、Y、W135流脑多糖疫苗;如孩子正在发热、患病,请暂缓接种。
接种费用每人85 元。
接种A、C、Y、W135流脑多糖疫苗是非常安全的,仅有个别人可能在接种局部会出现疼痛、硬结,也可能会出现低热,但几天就会自行恢复;极个别人可能会出现过敏等异常反应,但经治疗后很快就会痊愈,也不会留下后遗症。
我已阅读过以上内容,同意为我的孩子接种A、C、Y、W135群脑膜炎球菌流脑多糖疫苗。
A群C群脑膜炎球菌多糖疫苗

儿童预防接释告知书A群C群脑膜炎球菌多糖疫苗本疫苗属于国家免疫规划疫苗,由政府统一采购,并实行免费接种。
疫苗安全有效,敬请放心接种。
【疾病简介】行性脑脊髓膜炎(简称流脑)主要是由A群或c群以及W135群和Y群脑膜炎球菌感染脑膜或脑脊髓膜引起的呼吸道传染病。
人与人之间主要通过打喷嚏、咳嗽等形式相互传染。
学校、幼儿园儿童生活接触密切,环境拥挤、卫生习惯不良,易发生流脑的爆发流行。
流脑患者临床主要表现为高烧、头痛、喷射状呕吐、脖子发硬等症状。
病死率达5%-10%,即使治愈,也常会听力下降或耳聋、智力低下等后遗症。
该病的病死率高、后遗症重,是严重危害儿童健康的传染病。
【二类疫苗替代】本剂次政府免费提供的疫苗为国产A群e群流脑多糖疫苗,家长还可根据自愿、自费、知情同意的原则,选择A+C+Y+W135群流脑多糖疫苗或进口A+C群流脑多糖疫苗。
【接种对象】按照现行国家免疫规划疫苗免疫程序,3岁以上儿童接种2剂A+C群流脑多糖疫苗,两剂间隔至少3年,与上一剂A群流脑间隔至少1年。
家长还可根据自愿、自费、知情同意的原则,选择A+C+Y+W135群流脑多糖疫苗或进口A+C群流脑多糖疫苗。
【接种效果】对2岁以上儿童和成人有85%-100%的短期效果,接种l剂A+C群流脑疫苗可提供至少3年的保护作用。
【接种反应】反应轻微,偶有短暂低热,局部稍有压痛感,可自行缓解。
如有严重反应及时诊治。
【接种禁忌】癫痫、惊厥、脑部疾患及有过敏史者;肾脏病、心脏病及活动性肺结核或其他严重疾患者;急性传染病及发热者。
注意:1.本疫苗具体不良反应和接种禁忌症等信息请参考药品使用说明书。
2.接种时请带上儿童预防接种证和家长签字后的告知书,否则不予接种。
3.《疫苗流通和预防接种管理条例》规定,疫苗分为第一类、第二类疫苗,第一类疫苗由政府免费向公民提供接种,第二类疫苗是公民自费并且自愿受种的疫苗。
预防接种知情同意书亲爱的家长:您好!欢迎您带孩子前来进行预防接种,接种A群c群脑膜炎球菌多糖疫苗可以有效预防A群及c群脑膜炎球菌引起的流行性脑脊髓膜炎。
四价流脑疫苗接种通知及知情同意书

四价流脑疫苗接种通知及知情同意书四价流脑(A、C、Y、W135群脑膜炎球菌多糖疫苗)接种通知及知情同意书_____________________(家长姓名):村(居)您好!根据《中华人民共和国传染病防治法》第十一条规定,国家实行有计划的预防接种制度。
国家免疫规划疫苗是适龄儿童必须接种的疫苗,其它疫苗家长可为自己的孩子选择性接种。
国家免疫规划疫苗种类请咨询当地疾病预防控制机构。
根据卫生部《儿童免疫规划程序》要求,请于_______年_____月_____日(上午/下午)带您的孩子___________(儿童姓名)到(单位)接种四价流脑疫苗1. 四价流脑疫苗2。
根据《疫苗流通和预防接种管理条例》,本产品属于第二类疫苗,由公民自费并且自愿受种;因接种第二类疫苗引起预防接种异常反应需要对受种者予以补偿的,补偿费用由相关的疫苗生产企业承担。
【疫苗作用与用途】本品仅用于预防A、C、Y、W135群脑膜炎球菌引起的流行性脑脊髓膜炎。
【不良反应】常见不良反应:1.接种后24小时内,在注射部位可出现疼痛和触痛,注射局部红肿浸润轻、中度反应,多数情况2-3天内自行消失。
2.接种疫苗后可出现一过性发热反应。
其中大多数为轻度发热反应,持续1-2天后可自行缓解,一般不需处理;对于中度发热反应或发热时间超过48小时者,可对症处理。
罕见不良反应:1.严重发热反应,应给予对症处理,以防高热惊厥。
2.注射局部重度红肿或其他并发症,可对症处理。
极罕见不良反应:1.过敏性皮疹:接种疫苗后72小时内可出现皮疹,应及时就诊,给予抗过敏治疗。
2.过敏性休克:一般在注射疫苗后1小时内发生,应及时抢救,注射肾上腺素进行治疗。
3.过敏性紫癜:出现过敏性紫癜反应时应及时就诊,应用皮质固醇类药物给予抗过敏治疗,治疗不当或不及时有可能并发紫癜性肾炎。
4.血管神经性水肿、变态反应性神经炎。
【禁忌】1.已知对该疫苗的任何成分过敏者。
2.患急性疾病、严重慢性疾病、慢性疾病的急性发作期和发热者。
ACYW135群流脑多糖疫苗

ACYW135群流脑多糖疫苗
一、接种方法、剂量及途径、疫苗免疫程序
接种时启开疫苗瓶,按标示量加入所附注射用水(0.5ml),摇匀后吸入注射器,立即于应种对象上臂外侧三角肌附着处消毒后皮下注射,每人剂量为0.5ml。
2周岁开始接种,3年加强接种。
二、不良反应、禁忌症和接种注意事项
(一)不良反应
不良反应轻微,主要为接种部位1~2的红肿、硬结和疼痛,可自行缓解。
偶有短暂低热。
(二)禁忌症
癫痫、抽风、脑部疾患、肾脏病、活动性肺结核、急性传染病、发热及有过敏史者均不得使用本疫苗。
(三)注意事项
1.为预防注射后发生罕见的不良反应,注射本品时需要必要的监护和治疗措施,如备有肾上腺素等,以备偶有过敏反应发生时急救用。
2.使用前应检查安瓿,如瓶有裂纹,瓶塞松动或内有异物者,不得使用。
3.每一瓶(安瓿)制品溶解后,应按规定剂量一次用完,不得分多次使用。
4.严格执行一人一针一管一消毒,杜绝接种事故发生。
5.本疫苗使用后,偶有短暂低热、局部稍有压痛感,一般自行缓解,如有严重反应及时诊治。
6.本疫苗应于2-8°C避光保存和运输,在盒签(或瓶签)标明的有效期内使用。
7.如果本疫苗接种给免疫缺陷者或正在进行免疫抑制剂治疗的患者,则无法获得免疫应答。
国家扩大免疫规划疫苗A群C群脑膜炎球菌多糖疫苗预防接种知情同意书

A群C群脑膜炎球菌多糖疫苗
预防接种知情同意书
【疾病简介】流行性脑脊髄膜炎(以下简称"流脑")是由脑膜炎奈瑟菌引起的急性呼吸道传染病,起病急、病情重,有发热、头痛、呕吐、皮肤出血点及脑膜剌激征,严重者可有败血症休克和脑实质损害,危及生命。
引起流脑的脑膜炎奈瑟球菌有A、B、C等12个血清群。
【疫苗作用】预防A、C群流脑。
【接种禁忌】
1.已知对该疫苗所含任何成分过敏者。
2.患急性疾病、严重慢性疾病、慢性疾病的急性发作期和发热者。
3.患脑病、未控制的癫痫和其他进行性神经系统疾病者。
【不良反应】
常见不良反应:疼痛、触痛、局部红肿、一过性发热。
罕见不良反应:严重发热、注射局部重度红肿或出现其他并发症。
极罕见不良反应:过敏性皮疹、过敏性休克、过敏性紫癜、血管神经性水肿及变态反应性神经炎、变态反应剥脱性皮炎。
【注意事项】
以下情况慎用:家族和个人有惊厥史者、患慢性疾病者、有癫痫史者、过敏体质者、哺乳期妇女。
【郑重提示】请您认真阅读以上内容,如实提供受种者的健康状况。
有不明事项请咨询接种医生。
因疫苗特性或受种者个体差异等因素,疫苗保护率并非100%。
接种后请在现场留观30分钟.接种后如有不适,请及时告知接种医生,严重者请及时就医。
接种该疫苗免费。
受种者姓名:性别:出生日期:年月日Array
省卫生健康委员会监制。
脑膜炎疫苗知情同意书(打印版)

脑膜炎疫苗知情同意书(打印版)
本同意书是为了确保您在接种脑膜炎疫苗前了解相关信息并自愿参与接种,以确保您的权益和安全。
在接种疫苗之前,请您仔细阅读以下内容:
1. 目的:脑膜炎疫苗是一种预防脑膜炎感染的疫苗。
接种疫苗可以减少脑膜炎的风险以及相关并发症。
2. 接种对象:本疫苗适用于年龄在2个月到55周岁之间的人群。
3. 疫苗副作用:接种疫苗可能会引起一些副作用,如注射部位疼痛、发红或肿胀,以及一般性的不适感等。
一般来说,这些副作用都是暂时的,并不会对您的健康造成长期影响。
4. 疫苗禁忌症:某些特殊情况下,可能不适合您接种脑膜炎疫苗。
请告知医生您的过敏史、疾病史、药物使用情况等重要信息,以便医生能够综合考虑您的健康状况来决定是否接种疫苗。
5. 疫苗使用:根据医生的建议和相关法规,疫苗应在合适的医疗机构或接种点进行接种,以确保接种程序的安全和有效。
6. 效果评估:接种疫苗后,短期内可能会有保护效果,但长期有效性尚需进一步研究。
7. 后续注意事项:接种后,您可能需要观察自己的身体反应,并及时就医咨询医生,以应对任何意外情况。
8. 其他风险:除了常见的副作用,接种疫苗可能存在其他未知的风险。
目前尚无疫苗能够提供完全的保护,所以在接种疫苗后,仍然需要采取其他预防措施,如保持良好的个人卫生惯等。
9. 同意规定:我已经阅读并理解了上述信息,我自愿接受接种脑膜炎疫苗,并知晓其可能的副作用和不适应症。
我明白该疫苗可能无法完全预防脑膜炎,我将继续采取其他的预防措施。
签字:________________________
日期:________________________。
ACYW135群脑膜炎球菌多糖疫苗应用指南

ACYW135群脑膜炎球菌多糖疫苗应用指南流行性脑脊髓膜炎(流腑)足脑膜炎奈瑟菌(Veisseria meningitidis,Nm)感染引起以腑膜炎和败血症为主要临床表现的呼吸道传染病。
全球每年流脑发病人数约为 50 万,死亡 5 万,病死率和致残率较高,是大多数国家的重要公共卫生问题。
Nm 已发现 12 个血清群,几乎所有侵袭性腑膜炎球菌病部是由 A、B、C、Y 和 W135 群感染引起。
自 20 世纪以来,不同国家和地区均存在流行菌群变迁现象。
我国目前流脑发病控制在较低流行水平,发病以A 群和C 群为主,2006 年以后出现 W135 群散发病例报告。
我国部分地区 Nm 带菌调查显示,健康人群Y、W135 群血清杀菌抗体水平较低,提示存在发生相关菌群流行的风险。
预防接种是控制流脑最经济、有效的措施。
我国从1980 年代开始广泛使用 A 群流脑多糖疫苗,2007 年将 A 群和 A+C 群流脑多糖疫苗纳入扩大国家免疫规划,2008 年 ACYW135 群流脑多糖疫苗作为第二类疫苗在我国批准使用。
为进一步预防控制流脑,指导ACYW135 群流脑多糖疫苗的使用,中华预防医学会组织国内有关专家,在综合考虑流脑疾病负担、流行特征、疫苗应用效果、我国的儿童免疫程序、WHO 和其他国家关于流脑疫苗接种建议的摹础上,根据循证医学原则,制订了《ACYW135 群脑膜炎球菌多糖疫苗应用指南》(简称《指南》),旨在为疾病预防控制专业人员和基层接种人员应用流脑疫苗提供参考及指导。
今后将根据我国流脑流行特征、疫苗的应用评价等,适时对《指南》进行修订。
一、脑膜炎球菌病病原体及感染临床特征Nm 为需氧性革兰阴性双球菌,有荚膜,一般成对(双球菌)出现,细菌细胞壁的脂寡糖成分(LOS)和荚膜是重要的毒力因子。
Nm 依据荚膜多糖结构,至少可分为A、B、C、29E、H、I、K、L、W135、X、Y、Z12 个血清群,其中致病性最强的为A、B、C、W135 和 Y 群。
预防接种知情同意书(A群C群脑膜炎球菌多糖疫苗资料

关于充分发挥《魅力700》栏目作用构架教育对外良好沟通宣传渠道的通知各县(市)区教育局,江北教育处,市直学校、民办学校:为全面贯彻宣传党的教育方针,充分展示我市素质教育的丰硕成果,大力讴歌教育工作者的辛勤付出,努力构架教育对外良好沟通渠道,更大程度地促进社会群众对教育的了解和理解,共同打造广大青少年健康成长的高位平台,在市领导的高度重视下,经市教育局、市广电局研究决定,由吉林市教育电视台与吉林市电视台教育节目部联合开办大型教育栏目《魅力700》。
为切实发挥好栏目的宣传作用,现就有关事项通知如下:一、栏目内容《魅力700》是一档以学校为平台,以学生、家长、教育工作者为目标收视群体,立足吉林市教育实际、全方位展示教育工作的综合性电视杂志型节目。
《魅力700》的涵义为:教育是最有魅力的事业,师生是最有魅力的群体,节目制作者是具有魅力的电视人,700为节目首播时间。
《魅力700》设有“教育时讯”、“大帆直通车”、“我说你说”、“风采校园”、“激情PK”、“今天我上镜”、“招考时线”等子栏目。
除此之外还策划并承办学校各类校园活动。
二、播出时间《魅力700》栏目时长30分钟。
《魅力700》于2007年1月1日正式开播。
开播后于吉林市电视台《生活频道》每天18时57分首播,次日《新闻综合频道》6时20分重播(播出时差为±3分钟)。
三、有关要求吉林市电视台为一个行业(系统)开办日播节目尚属首次。
此次合作,体现了市委、市政府对教育的高度重视,体现了市广电部门、市电视台对教育的深厚情感。
为此,各县市区教育行政部门、市直各个学校要组织广大师生认真收看节目,并充分利用好《魅力700》栏目这个窗口,宣传、展示好教育工作成果。
为使《魅力700》栏目充分发挥出应有的作用,请各县市区教育行政部门、各级各类学校在利用栏目宣传自己的同时,结合教育发展、学校发展的实际需要,对栏目建设提出意见和建议,合力办好栏目,更好地为教育发展服务,更好地为江城百姓服务。
AC群流脑多糖结合疫苗和ACYW135接种注意事项

AC群流脑多糖结合疫苗和ACYW135
群流脑疫苗接种注意事项
一、接种对象
3月龄——24月龄儿童接种AC群流脑多糖结合疫苗;2周岁以上儿童及成人接种四价流脑疫苗,重点是托幼儿童、中小学校学生。
二、接种原则
实行“知情、同意、自愿、自费”的原则。
三、接种程序
AC群流脑多糖结合疫苗、四价流脑疫苗的接种程序根据疫苗使用说明接种,与国家免疫规划内的A群流脑多糖疫苗、AC群流脑多糖疫苗的接种间隔等联合使用严格按照市疾控中心《关于印发全市流行性脑脊髓膜炎球菌相关疫苗接种指导意见的通知》要求执行。
四、技术要求
1.接种方法:
(1)接种部位:上臂外侧三角肌附着处,皮肤用75%酒精消毒后皮下注射0.5ml,严禁静脉注射。
(2)接种剂量:每人次接种剂量均为0.5ml (即200ug/支)。
(3)疫苗供应:本次流脑疫苗由县疾控中心统一采购,统一供应。
2、禁忌症:
(1)癫痫、抽风、脑部疾患及有过敏史者;
(2)肾脏病、心脏病及活动性结核者;
(3)发热、急性传染病患者;
(4)体质衰弱、先天性免疫缺陷者。
3.不良反应监测:
常见不良反应:可出现短暂低热,局部稍有压疼感,一般可自行缓解,无需特殊处理。
极罕见不良反应:过敏性皮疹,一般接种后72小时出现,应及时就诊。
各预防接种点应备有肾上腺素等药物,以备偶有发生严重过敏反应时急救用。
接受注射者在注射后应在现场观察至少30分钟。
脊髓灰质炎灭活疫苗接种知情同意书(2019年版)可编辑

附件16 2019版XX省非免疫规划疫苗接种知情同意书脊髓灰质炎灭活疫苗受种者姓名:性别:出生日期:年月日根据《中华人民共和国疫苗管理法》第九十七条:非免疫规划疫苗,是指由居民自愿接种的其他疫苗。
国家免疫规划程序以外的脊髓灰质炎灭活疫苗为非免疫规划疫苗。
【疾病简介】脊髓灰质炎(俗称“小儿麻痹症”),是由脊髓灰质炎病毒引起的急性肠道传染病,可引起肢体不对称弛缓性麻痹,部分患者会留下瘫痪后遗症,个别重症者可危及生命。
【疫苗作用】预防脊髓灰质炎。
【接种禁忌】1.对该疫苗所含任何成分过敏者。
2.以前接种本疫苗后出现严重过敏反应者。
3.正处在发热、急性疾病期间者。
4.患严重慢性疾病者。
5.过敏体质者。
【不良反应】1.常见不良反应:发热;注射部位疼痛、发红、肿胀、硬结,嗜睡,烦躁,呕吐,腹泻,皮疹等。
2.极罕见不良反应:注射部位淋巴结肿大,荨麻疹、血管性水肿、过敏性休克,中度、一过性关节痛和肌痛,惊厥(伴或不伴发热),头痛、中度和一过性的感觉异常(主要位于下肢),兴奋、嗜睡和易激惹,广泛分布的皮疹,≤28周早产儿可能出现呼吸暂停。
如接种疫苗后诊断为异常反应,已购买基础保险的由保险公司补偿,未购买基础保险的由疫苗企业补偿。
【注意事项】1.血小板减少症或者出血性疾病者慎用。
2.正在接受免疫抑制剂治疗的患者或患有免疫缺陷者建议在治疗结束后进行接种。
3.未控制的癫痫患者或其他进行性神经系统疾病患者慎用。
4.接种后请留在接种门诊观察30分钟,无异常后方可离开。
请您认真阅读以上内容,如实提供受种者的健康状况和是否有接种禁忌等情况。
如有疑问请咨询医疗卫生人员。
因疫苗特性或受种者个体差异等因素,疫苗保护率并非100%。
国家免疫规划程序以外的脊髓灰质炎灭活疫苗自愿自费接种。
ACYW135群四价流脑多糖疫苗接种告知书

ACYW135群四价流脑多糖疫苗接种告知书流行性脑脊髓炎(简称流脑)是由脑膜炎双球菌引起的化脓性脑膜炎症,是一种急性呼吸道传染病,主要通过空气飞沫传播,冬春季常见,主要临床表现为高热、头痛、呕吐、颈项强直、皮肤黏膜出现瘀点瘀斑等。
具有起病急、病情发展快和病后易留下后遗症及病死率高等特点,是严重危害群众,尤其是危害儿童、青少年身体健康的疾病,给家庭和社会带来沉重的负担。
近年来,流脑的流行菌群已由原来的A群向C群、Y群、W135群变迁,且这些菌群具有易传播、隐性感染比例高、起病急、病程进展快、病死率高等特点,包括山东、湖北、江西、安徽、四川、广东等多个省份已相继发生上述菌群所致疫情。
接种ACYW135流脑疫苗是预防流脑最经济、最简便、最有效的方法。
接种1针ACYW135流脑疫苗可同时预防由A群、C群、Y群、W135群引起的脑膜炎。
本疫苗属第二类疫苗,在群众知情自愿的前提下,自费选择接种,不强制您接种。
1、接种对象:2周岁以上的儿童及成人均可接种,重点对2周岁以上15岁以下,3年内未接种A+C群流脑疫苗的儿童补种1针次。
⑴ 2岁~5岁儿童:仅对未接种A+C群流脑疫苗者补种1针次ACYW135群四价流脑多糖疫苗。
⑵ 6岁~15岁儿童:对从未接种过A+C群流脑疫苗者应补种2针次(2针次间隔不少于3年),对已接种1针A+C群流脑疫苗者且已间隔达3年及以上者补种1针。
2、接种副反应:本疫苗使用后,少数接种者可有轻微红肿、硬结和疼痛,偶有短暂低热,一般不超过72小时可自行缓解。
3、禁忌症:1、患有癫痫、抽风、脑部疾患及有过敏史者;2、心脏病、肾脏病及活动性肺结核患者;3、急性传染病及发热者。
4、由于个体因素,疫苗对90%以上的受种者产生足够保护力而不发病,未产生足够保护力的受种者有可能会感染发病,但其症状轻病程短,严重并发症发生率低。
以上为接种疫苗相关的内容,请受种者或受种儿童的家长/监护人认真仔细阅读,如同意接种,请签名认可并在接种时交付疫苗费用。
类疫苗接种知情同意书模板

流行性腮腺炎(以下称流腮)是由腮腺炎病毒引起的以腮腺肿大、疼痛、发热为主要症状的急性呼吸道传染病,好发于儿童和青少年。
由于其临床症状较轻常被人们忽视,但实际上,流腮的危害远非局限于腮腺,其病毒可侵犯中枢神经系统和多种腺体,临床上可引起脑膜炎、脑炎等严重并发症,严重者还可导致男性不育和耳聋,给社会和家庭造成严重负担。
我国流腮发病逐年上升,尤其常在幼儿园、学校出现爆发,患儿不能上幼儿园或上学,严重影响了学校的公共卫生安全和学习进度。
,接种疫苗是预防流腮的唯一有效手段。
【接种对象】1岁~15周岁儿童。
【接种程序】18月龄儿童:接种一剂次。
4~7岁儿童:加强注射一次。
【常见不良反应】个别人接种疫苗后48小时内出现注射部位轻微红肿和疼痛,有一过性发热、不适等轻微反应,不需特殊处理,一般1~2天内可自行消失。
【禁忌】患严重疾病、急性或慢性感染、发热者。
对鸡蛋有过敏史者。
妊娠期妇女。
【注意事项】开启疫苗安瓿和注射剂,切勿使用消毒剂接触疫苗。
疫苗加入灭菌注射用水后,轻轻振摇应能立即溶解。
疫苗复溶后出现异常浑浊、疫苗安瓿有裂纹、标签不清或过期失效者,均不得使用。
–––––––––––––––- –––––––––––––––––––––腮腺炎疫苗接种服务单(接种单位留存)以下内容由儿童家长或监护人填写:儿童姓名:;性别:男出生日期:年月日;联系电话:详细住址:本人已阅读该疫苗接种告知书,该儿童(有□、无√□)接种禁忌症;儿童家长或监护人(签名:)同意接种该疫苗。
以下内容由接种人员填写:疫苗厂家:;疫苗批号:;接种日期:年月日;接种人员签名:\b型流感嗜血杆菌(Hib)侵袭性疾病有多种临床表现形式,如脑炎、会厌炎、败血症、蜂窝组织炎、关节炎、肺炎、心包炎、脊髓炎等。
Hib侵袭性疾病主要发生在5岁以下的儿童中,通过鼻咽部形成的飞沫传播。
在发展中国家,Hib侵袭性疾病是引起婴幼儿死亡的重要原因。
接种Hib疫苗是预防b型流感嗜血杆菌(Hib)侵袭性疾病的有效手段。
疫苗接种知情同意书

卡介苗接种知情同意书【疾病简介】结核病是由结核杆菌引起的严重危害人类健康的传染病,通过呼吸道传播,肺部是常见感染部位,可累及全身多器官系统,传播到脑部可引起结核性脑膜炎。
【疫苗作用】预防儿童结核病,特别是对婴幼儿结核性脑膜炎和粟粒型肺结核有预防作用。
【接种禁忌】1.对该疫苗所含任何成分过敏者。
2.患急性疾病、严重慢性疾病、慢性疾病的急性发作期和发热者。
3.免疫缺陷、免疫功能低下或正在接受免疫抑制治疗者。
4.患脑病、未控制的癫痫和其他进行性神经系统疾病者。
5.妊娠期妇女。
6.患湿疹或其他皮肤病患者。
【不良反应】1.常见不良反应:一过性发热、红肿、化脓、溃疡、淋巴结肿大。
2.罕见不良反应:严重淋巴结反应。
3.极罕见不良反应:骨髓炎、过敏性皮疹、过敏性紫瘢、播散性卡介苗感染。
【注意事项】1.家族和个人有惊厥史者、患慢性疾病者、有癫痫史者、过敏体质者、哺乳期妇女慎用。
2.注射免疫球蛋白者至少间隔1个月以上接种本疫苗。
3.未接种卡介苗的小于3月龄儿童可直接补种,3月龄〜3岁儿童对PPD试验阴性者补种,4岁及以上儿童不予补种。
4.因疫苗特性或受种者个体差异等因素,疫苗保护率并非100%。
5.接种后请在现场留观30分钟。
6.接种后如有不适,请及时告知接种医生,严重者请及时就医。
请您认真阅读以上容,如实提供受种者的健康状况。
有不明事项请咨询接种医生。
接种此疫苗由政府承担全部费用。
接种者/医生(签名):日期:年月日预防乙型病毒性肝炎疫苗接种知情同意书【疾病简介】乙型病毒性肝炎(以下简称“乙肝”)是由乙肝病毒引起的传染病,主要经血传播(如不安全注射等)、母婴传播和性传播。
感染乙肝病毒后可成为乙肝病毒携带者,感染年龄越小,成为慢性携带者可能性越大,部分人可转化为慢性乙肝患者,甚至发展为肝硬化或肝癌。
【疫苗作用】全程接种3剂可有效预防乙肝。
相同剂量的各类含乙肝成分疫苗预防乙肝效果相近。
因疫苗特性或受种者个体差异等因素,疫苗保护率并非100%。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
附件22 2019版XX省非免疫规划疫苗接种知情同意书
ACYW135群脑膜炎球菌多糖疫苗
受种者姓名:性别:出生日期:年月日根据《中华人民共和国疫苗管理法》第九十七条:非免疫规划疫苗,是指由居民自愿接种的其他疫苗。
ACYW135群脑膜炎球菌多糖疫苗为非免疫规划疫苗。
【疾病简介】流行性脑脊髓膜炎是由脑膜炎奈瑟菌引起的急性呼吸道传染病,起病急、病情重,有发热、头痛、呕吐、皮肤出血点及脑膜刺激征,严重者可有败血症休克和脑实质损害,危及生命。
引起流行性脑脊髓膜炎的脑膜炎奈瑟球菌有12个血清群。
【疫苗作用】预防A、C、Y、W135群流行性脑脊髓膜炎。
【接种禁忌】
1.对该疫苗所含任何成分过敏者。
2.患急性疾病、严重慢性疾病、慢性疾病的急性发作期和发热者。
3.患脑部疾病、癫痫及有过敏史。
4.肾脏病、心脏病、活动性结核患者。
【不良反应】
1.常见不良反应:接种部位1-2天的红肿、硬结、疼痛,发热。
2.罕见不良反应:过敏反应等。
如接种疫苗后诊断为异常反应,已购买基础保险的由保险公司补偿,未购买基础保险的由疫苗企业补偿。
【注意事项】
1.家族和个人有惊厥史者、患慢性疾病者、有癲痫史者、过敏体质者、孕妇、哺乳期妇女慎用。
2.接种后请留在接种门诊观察30分钟,无异常后方可离开。
请您认真阅读以上内容,如实提供受种者的健康状况和是否有接种禁忌等情况。
如有疑问请咨询医疗卫生人员。
因疫苗特性或受种者个体差异等因素,疫苗保护率并非100%。
本疫苗自愿自费接种。
