科粤版(2012)初中化学九下 8.3 酸和碱的反应 课件 _3优秀课件
合集下载
粤科版九年级化学(下册)第八章8.3 酸与碱的反应(共21张PPT)

拓展探究二:
1问题:其他的酸和碱也能发生类似的反应吗?
1、观察实验并描述现象(写出化学方程式) Fe(OH)3固体和稀HCl— 红褐色沉淀溶解 Cu(OH)2固体和稀H2SO4— 蓝色固体溶解 2、得出结论:一般酸和碱都能发生类似的反应; 当酸碱反应时,若无明显现象,要借助指示剂来判断 是否发生反应;而对于难溶性碱与酸反应或生成沉淀 的反应则可以直接观察,不需借助指示剂来判断。
2、分析:有三种可能: 1)恰好完全中和。 2)稀盐酸加多了 3)稀盐酸加少了,氢氧化钠溶液剩余了。
3、设计实验
猜想 猜想一 (中性) 探究方案(写出操作方法、现象、结论)
取少量反应后的溶液于试管,滴入几滴紫 色石蕊试液振荡,若溶液 则猜想正确
取少量反应后的溶液于试管,滴入几滴紫色石蕊试 液振荡,若溶液变 则猜想正确
• 方案2:取少量NaOH溶液于试管中,滴加几滴无色酚酞
试液,再滴加稀HCl ,看溶液颜色的变化?
实验与事实
操作步骤 1 2 取约3ml的NaOH溶液于锥形瓶,滴入1、 2滴酚酞溶液。 逐渐向NaOH溶液,滴稀HCl溶液、 振荡。
现象
变红
红变
无色
完成实验、得出结论: NaOH和稀HCl发生反应
NaOH和稀HCl之间究竟是怎样发生反应的?
学完本节课你收获了什么?
1.酸和碱能发生中和反应,生成盐和水。
+ 其实质是H 与OH 结合生成H 2O
2.酸碱中和反应在生活和生产中有广泛 的应用。
3 .知道了并不是所有的化学反应都有明显 的实验现象,有些反应需要借助指示剂 才能判断反应的发生。
4 .学会了通过科学探究的方法设计实验。
你知道它 的作用吗 ?
胃乐胶囊的主要成分
科粤版(2012)初中化学九下 8.3 酸和碱的反应 课件 _3
酸碱
NaCl + H2O
盐水
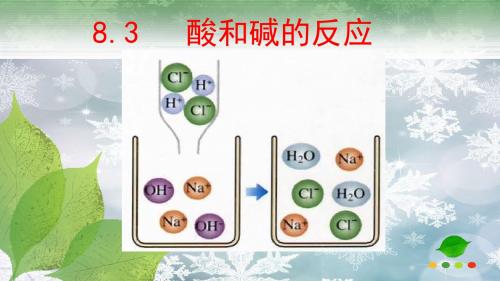
反应前后溶液中离子发生了怎样的变化?
NaOH = Na+ + OHHCl = H+ + Cl-
NaOH + HCl = NaCl +H2O
酸碱反应的实质: 酸溶液中的 H+ 和碱溶液中的 OH- 结合生 成H2O的过程
对比酸、碱的性P239
项目
酸的主要化学性质 碱的主要化学性质
b.先在稀盐酸中滴加酚酞溶液,再滴加 1-2滴氢氧化钠溶液。
实验探究
实
验 现
a . 氢氧化钠溶液中滴加酚酞溶液后, 溶液变红,逐渐滴加稀盐酸,红色消失。
象
b. 稀盐酸中滴加酚酞溶液后不变色,再 加少量氢氧化钠溶液仍不变色。
实验探究
实 验 酸与碱之间会发生反应 结 论
试写出其化学方程式
HCl + NaOH
2 、天空,经常刮风经常下雨经常没太阳;季节,天渐转凉秋意渐浓记得加衣裳!生活,吃得要香睡得要甜身体要健康,祝福工作顺心,事业有 成! 12 、怕吃苦的人苦一辈子,不怕吃苦的人苦一阵子。 7 、一个获得成功的人,从他的同胞那里所取得的,总是无可比拟地超过他对他们所做的贡献。 4 、昔之得一者:天得一以清;地得一以宁;神得一以灵;谷得一以生;侯得一以为天下正。 6 、经过奋斗,终于拨开了云雾,见到了日出,走上了阳光大道。面对取得的成绩,不要骄傲,再接再励,继续向前行。 8 、那些在困难面前能够坚持到底、努力奋进的人最终能够战胜一切困难,取得最后的成功。
与指 紫色石蕊 使紫色石蕊溶液_变__红_ 使紫色石蕊溶液变___蓝_
示剂
作用 无色酚酞 无色酚酞溶液不___变_ 色 使无色酚酞溶液_变___红
NaCl + H2O
盐水
反应前后溶液中离子发生了怎样的变化?
NaOH = Na+ + OHHCl = H+ + Cl-
NaOH + HCl = NaCl +H2O
酸碱反应的实质: 酸溶液中的 H+ 和碱溶液中的 OH- 结合生 成H2O的过程
对比酸、碱的性P239
项目
酸的主要化学性质 碱的主要化学性质
b.先在稀盐酸中滴加酚酞溶液,再滴加 1-2滴氢氧化钠溶液。
实验探究
实
验 现
a . 氢氧化钠溶液中滴加酚酞溶液后, 溶液变红,逐渐滴加稀盐酸,红色消失。
象
b. 稀盐酸中滴加酚酞溶液后不变色,再 加少量氢氧化钠溶液仍不变色。
实验探究
实 验 酸与碱之间会发生反应 结 论
试写出其化学方程式
HCl + NaOH
2 、天空,经常刮风经常下雨经常没太阳;季节,天渐转凉秋意渐浓记得加衣裳!生活,吃得要香睡得要甜身体要健康,祝福工作顺心,事业有 成! 12 、怕吃苦的人苦一辈子,不怕吃苦的人苦一阵子。 7 、一个获得成功的人,从他的同胞那里所取得的,总是无可比拟地超过他对他们所做的贡献。 4 、昔之得一者:天得一以清;地得一以宁;神得一以灵;谷得一以生;侯得一以为天下正。 6 、经过奋斗,终于拨开了云雾,见到了日出,走上了阳光大道。面对取得的成绩,不要骄傲,再接再励,继续向前行。 8 、那些在困难面前能够坚持到底、努力奋进的人最终能够战胜一切困难,取得最后的成功。
与指 紫色石蕊 使紫色石蕊溶液_变__红_ 使紫色石蕊溶液变___蓝_
示剂
作用 无色酚酞 无色酚酞溶液不___变_ 色 使无色酚酞溶液_变___红
酸和碱的反应 课件(共24张内嵌视频) 科粤版化学九年级下册
4.了解中和反应在生产生活中的某些应用。
新知学习
一、酸、碱溶液的导电性
【实验8-13】酸与碱能否产生化学反应
提出问题:在6只小烧杯中分别装有下表列出的溶液各100mL,再按下图的
装置进行实验,当闭合开关接通电源后,视察灯泡是否发亮。
溶
液
蒸 酒 稀 稀 稀烧 澄清
馏 精 盐 硫 碱溶 石灰
水
酸 酸 液
调节溶液的酸碱性
复分解反应
AB + CD == AD + CB
阳离子都是金属离子
当酸遇到碱会有什么现象产生呢?
OH-
氢氧根
阴离子都是____离子
新知学习
二、中和反应
1.酸碱产生的反应
新知学习
实验:
先向氢氧化钠溶液中滴加酚酞溶液
再滴加稀盐酸,视察现象。
现象:
在氢氧化钠溶液中滴加酚酞后溶液显红色,随着滴加盐酸,颜色逐渐消失至无色。
新知学习
思考:1.用玻璃棒沾上述氢氧化钠溶液与稀盐酸刚好反应生成的溶液,在酒
能是( C )
A.氧化铜
B.盐酸
C.氢氧化钠
D.碳酸钠
4.下列实际应用中,利用中和反应原理的是( A )
①用氢氧化钠溶液洗去石油产品中的残余硫酸;②用稀硫酸除铁锈;③用熟
石灰改进酸性土壤;④用碳酸氢钠治疗胃酸过多。
A.①③
B.③④
C.①②④
D.①③④
当堂检测
5.将下列使用过的仪器浸泡于稀盐酸中,然后用水冲洗,不能将仪器处理干净
成盐。酸与碱作用生成盐和水的反应,叫作中和反应。
酸 + 碱 → 盐+水
实质:中和反应的实质是H+和OH-结合生成H2O
H+ + OH- == H2O
粤科版九年级化学(下册)第八章8.3 酸和碱的反应(共25张PPT)
三、中和反应在实际中的应用 1.改良土壤的酸碱性
盐碱地
碱性土壤
加入酸
性物质
中性土壤
酸性土壤
熟石灰 Ca(OH)2
中性土壤
2. 处理工厂的废水
⑴ 如何处理硫酸厂生产中形成的含硫酸的污水?
请写出有关反应的化学方程式:
H2SO4+ Ca(OH)2 = CaSO4 + 2H2O ⑵用CaO来中和污水行不行?
NaOH+HCl == NaCl + H2O 2KOH + H2SO4== K2SO4 + 2H2O
【回顾旧知】
盐
酸根离子
二、中和反应:
1.定义:酸与碱作用生成盐和水的反应。
+
+
酸
HCl + NaOH
碱
盐
NaCl + H2O
水
H2SO4 + 2KOH==K2SO4 + 2H2O
2、中和反应的实质:
你能说说反应现象背后的原因吗?你能评价一下 四个方案的优劣吗?
你能还能借助现有的仪器和药品设计其他的验证酸碱反 应的方案吗?
方案4:往盛有NaOH 溶液的试管加入几滴稀HCl,然后
再加入锌粒,观察有无气泡冒出。 方案5:先测稀HCl的pH,滴入一定量的NaOH 后,再测一 下溶液的pH。
方案6:往盛有稀HCl溶液的试管滴入NaOH溶液后,加 入一定量的碳酸钙或者碳酸钠溶液,看有无气泡冒出
聪明的你们还能想出有其它 方案吗?
继续探究: 酸和碱反应吗
编号 1 操作步骤
P236
观察到的现象 解释
2 3
取3MLNaOH溶液于 溶液 试管中,滴1、2滴酚 变红 酞溶液 逐渐NaOH溶液中的 红色变浅然 稀盐酸、振荡
科粤版化学九年级下册第八章8.3酸和碱的反应(共19张PPT)

阴离子都是 酸根 离子
阴离子都是 氢氧根 离子
Na OH 阳离子都 K OH 是金属 离子 Ca (OH) 2
一.酸和碱的组成
• 酸和碱溶于水生产的产物中都各自有其相 氢离子 ,在 同的一种离子,在酸中是 碱溶液中是 氢氧根离子 。这是它们具 有相似化学性质的原因。
【实验8-14】: 酸和碱会发生反应吗?
课题2 酸和碱的中和反应
(5)氢氧化钠溶液和氢氧化钙溶液具有 相似的化学性质,其本质原因是( B ) A.都能与指示剂作用 B.都能解离出氢氧根离子 C.都能解离出金属阳离子 D.都含有氢元素和氧元素
课题2 酸和碱的பைடு நூலகம்和反应
选做题:将X溶液滴入Y溶液中,在滴加过 程中,Y溶液的PH值变化情况如图所示。
H2SO4 +2 KOH = K2SO4+2H2O
二、中和反应: 1.定义:酸与碱作用生成盐和水的反应。
酸+ 碱
2. 实质:
盐
+
水
酸中的H+和碱中的OH-反应生成水。
H++OHHCl NaOH H2O H+ + ClNa+ + OH-
H2O
小结: 1.酸是由 氢 离子和 酸根 离子 组成; 2.碱是由 氢氧根 离子和 金属 离 子组成。 3.通过实验认识了中和反应;
【实验8-13】 在六只小烧杯中分别装有下 表列出的溶液各100mL,再按图 8-12的装置进行实验,当闭合 开关接通电源后,观察灯泡是 否发亮。
溶液
NaOH
蒸馏水 酒精 稀盐酸 稀硫酸 稀烧碱 澄清石 溶液 灰水
灯泡 亮否
否
否
亮
亮
亮
粤教版九年级化学下册《酸和碱的反应》常见的酸、碱、盐PPT教学课件

酸、碱各自为什么有相似的化学性质?
酸和碱的组成
HCl
H+ 酸
溶于水电离
HNO3
H++酸根离子
会不会发生反应呢?
H2SO4
NaOH
OH- 溶于水电离
碱 KOH
OH-+金属离 子
Ca(OH)2
探究新知
学生实验
设计实验进行操作,记录现象,并写出发生反应的化学方程式(填写在导学案上)
编号 ① ② ③ ④
中和反应是属于复分解反应中的一种
中和反应
酸+碱→盐 +水 实质:酸中的H+和碱中的 OH-发生反应生成H2O
中和反应的应用
达标检测
1.下列必须通过指示剂才能判断反应是否发生的是( C )
A.锌粒和稀硫酸 B.铁锈和稀盐酸 C.烧碱和稀盐酸 D.大理石和稀盐酸
2.胃酸过多的病人常内服含Al(OH)3的药物,反应的化学方程式
碱+_非金属_氧化物 →___盐__+__水___
酸+盐→___新_ 酸___+__新_ 盐____
碱+盐→_新___碱____+__新___盐____
酸+较活泼金属
→__盐__+_氢___气___
酸 + 碱 → ___盐_ ___+___水____
HCl + NaOH
NaCl + H2O
还
有
2HCl + Ba(OH)2
x=15.8g,y=9.85g,z=4.35g,剩余高锰酸钾的质量:
18g-15.8g=2.2g,故固体剩余物是:KMnO4 MnO2 K2MnO4
答案:C.
上一页 下一页
4. 某金属单质X与非金属单质Y可发生反应:2X+Y═X2Y.某实 验探究小组进行了两次实验,测得数据如表: 实验序号 X的用量/g Y的用量/g 生成X2Y的质量/g
科粤版化学九年级下册第八章8.3酸和碱的反应 (共28张PPT)

1、中和反应;酸与碱作用生成盐和水的反应。 2、中和反应的实质是H+和OH- 结合生成水。 3、酸与碱反应时,酸溶液中的氢离子和碱溶液中的
氢氧根离子互相结合生成了中性的水,当二者恰好完全
反应时溶液呈中性。
【课堂练习】 3.下列反应,属于中和反应的是( C )
A. Ca(OH)2+ CO2==== CaCO3↓+H2O B. CuO + 2HCl ==== CuCl 2 + H2 O C. Cu(OH)2 + H2SO4 ==== CuSO4 + 2H2O D. AgNO3 + HCl ==== AgCl↓+ HNO3
新课引入
人的胃内有什么酸?在生活中,当胃酸 过多的病人看医生时,医生让病人口服胃舒 平(主要成分氢氧化铝),为什么胃舒平能治疗 这种胃病?
8.3 酸和碱的反应
1.认识酸和碱的组成,知道酸和碱在溶液中生成了氢离子 和氢氧根离子。 2.通过对酸和碱的反应探究,提高发现和提出问题的能力。 3.认识中和反应的实质,初步学会借助指示剂判断物质是
看玻璃棒上是否有固体。
进行实验
在试管中加入氢氧化钠溶液,滴入几滴无色酚酞溶液。再 用滴管慢慢滴入稀盐酸,并不断用振荡溶液,至溶液颜色刚好 变成无色为止。
实验现象: 溶液由红色变为无色 实验结论: 酸和碱能反应
反应的化学方程式为: HCl+NaOH====NaCl+H2O
对于无明显现象的酸和碱反应,通常要借助指示剂无色 酚酞溶液来帮助判断反应的发生。
-
2.碱溶液中共同存在导电的带电粒子 OH , 故碱有相似的性质。
碱 金属离子 + OH
-
【课堂练习】1.生活中常见的柠檬汁、番茄汁、柑橘汁、 酸奶等物质的水溶液都有一定的酸性,这 是由于它们( D ) A. 溶于水时生成了盐酸 B. 水溶液中含有酸分子 C. 组成中含有氢元素 D. 溶于水时,在水中解离产生了氢离子
粤教版化学九下8.3《酸和碱的反应》ppt-课件

历史课件:/kejian/lish i/
两种__化__合__物_________的反应,叫作复分解反应。复分解反
应与化合反应、分解反应、置换反应通称为基本反应类型。 2.通式:AB+CD―→___A_D____+__C_B____。
3.特点:双交换,价不变。
[注意] 中和反应属于复分解反应,中和反应不是基本反
3.防治 (1)减少含硫煤燃烧。 (2)提倡使用新能源。 (3)对工厂排放的废气净化处理等。
互动探究
探究点一 证明中和反应确实发生 [情景展示]一、观察实验:把氢氧化钠溶液和稀盐酸进行混合。
二、
[问题探究]氢氧化钠溶液和稀盐酸反应时没有明显现象, 如何设计实验证明酸和碱之间确实发生了反应?我们又如 何判断一个反应是不是中和反应?
五 酸雨 1.形成:_煤___和_石__油____燃烧后所产生的烟气中,含有
二氧化硫和氮氧化物,排放到空气中被云层吸收,并经过化 学作用形成酸雾,随同雨水下降便成为显酸性的雨水,若其 pH小于5.6,称为酸雨。
2.危害 (1)腐蚀金属。 (2)侵蚀雕像和建筑。 (3)破坏森林。 (4)使水中生物死亡。
科学课件:/kejian/kexue/ 物理课件:/kejian/wul i/
化学课件:/kejian/huaxue/ 生物课件:/kejian/she ngwu/
地理课件:/kejian/dili/
4.实质:酸溶液中的__氢__离__子__(_H_+__)与碱溶液中的 __氢__氧__根__离__子__(_O_H_-__)______结合生成__水__分__子____的过程。
5.应用:①改良酸性或碱性土壤;②废水处理;③医药 应用;④调节溶液的酸碱性。
三 复分解反应
【科粤版九年级化学下册】第8章8-3酸和碱的反应课件

第八章 常见的酸、碱、盐
科粤版九年级化学下册
第八章 常见的酸、碱、盐
讨论: 1. 酚酞在实验中起什么作用? 答:起指示作用。因为NaOH与HCl反应无明显的
现象发生,根据酚酞溶液由红色变为无色来判断NaOH 和HCl是否反应完全。
2. 为什么在操作中必须逐滴滴入稀盐酸? 答:防止稀盐酸滴加过量。
注意: 滴加盐酸至红色恰好变成无色时即止。 否则盐酸过量。
H2 SO4
Ca2(HO2HO)2
科粤版九年级化学下册
第八章 常见的酸、碱、盐
3. 用于医药
⑴ 中和胃酸过多
用含有氢氧化铝的胃药中和胃酸中过多的盐酸。
化学方程式:
Al(OH)3 + 3HCl=AlCl3 + 3H2O
⑵ 中和蚁酸
可涂抹一些含有碱性物质(如氨水NH3·H2O)的药水。 思考:可不可以用NaOH来中和胃酸、蚁酸?为什么? 答:不可以。因为NaOH的碱性太强,具有强的腐蚀性。
1.改良土壤的酸碱性
盐碱 地
熟石灰
酸性土壤
中性土壤
Ca(OH)2
碱性土 壤
加入酸 性物质 中性土壤
科粤版九年级化学下册
第八章 常见的酸、碱、盐
讨论: ⑴ 为什么向酸性土壤中加入熟石灰,而不可以加入
氢氧化钠粉末? 答:因为氢氧化钠的腐蚀性太强。
⑵ 导致土壤显酸性的主要原因是什么?
答:是酸第八章 常见的酸、碱、盐
2. 处理工厂的废水 ⑴ 如何处理硫酸厂生产中形成的含硫酸的污水? ⑵ 请写出有关反应的化学方程式: ⑶H用2SCOa4+OC来a中(O和H污)2 =水行Ca不S行O4?+ 2 H2O
CaO + H2O =Ca(OH)2 H2SO4+ Ca(OH)2 = CaSO4 + 2 H2O
粤科版九年级化学(下册)第八章8.3 酸和碱的反应(共24张PPT)

请你设计实验来验证氢氧化钠 Cu(OH)溶液由红色逐渐变 +H SO =CuSO +2H O 为无色 与盐酸确实发生了反应。 Cu(OH) +2HCl=CuCl +2H O
2 2 4 4 2 2 2 2
酸
碱
观察到的现象
化学方程式
NaOH+HCl=NaCl+H2O 2NaOH +H2SO4=Na2SO4+2H2O
不能,因为氢氧化钠固体溶 于水也伴随的放热现象。
中和反应的实质是什么呢?
中和反应的实质:酸溶液里的氢离子和碱溶 液里的氢氧根离子结合生成了水分子。
中和反应的实质:酸溶液里的氢离子和碱溶 液里的氢氧根离子结合生成了水分子。
现有三瓶无色溶液:稀盐酸、水、 氢氧化钠溶液,现提供紫色石蕊 溶液和无色酚酞溶液,能否分别 用它们将三者区分开来?如果能, 怎么做?
蜜蜂与马蜂
蜜蜂
被蜜蜂蛰后,用肥皂水或氨水清洗
马蜂
被马蜂蛰后,用食醋止痛止痒
某种消化药片的有效成分氢氧化镁,能减缓因 胃酸过多引起的疼痛,在氢氧化镁与胃酸作用 的过程中,胃液pH变化的情况是 (B)
Na OH + H Cl == NaCl +H O 2 Na OH + H Cl == NaCl +H2O
判断下列反应是否属于中和反应? Ca(OH)2+CO2=CaCO3↓+H2O CuO+ H2SO4 = CuSO4 +H2O H2SO4 + 2NaOH = Na2SO4 + 2H2O AgNO3+HCl=AgCl↓+HNO3
3.下表为家庭中一些常见物质的pH
物质 PH值
粤教初中化学九下《8.3 酸和碱的反应》PPT课件 (5篇供参考)

例题解析
【设计实验】
实验操作
实验现象
实验结论
取反应后的溶液
于试管中,加入 __石__蕊__试__液____
_____溶_液__变__红______ __
猜想三成立
_
【拓展应用】我国土壤的酸碱性有“南酸北碱”之说 碱性物质
法,你认为需向酸性土壤中加入_____________进行
改良。
例题解析
【解析】实验一:氢氧化钠溶液呈碱性,能使酚酞试 液变红,能与盐酸反应生成氯化钠和水; 实验二:由于氢氧化钠呈碱性,能使酚酞试液变红, 而此时溶液是无色的,故一定不会有氢氧化钠剩余; 设计实验:猜想三中含有盐酸,要证明盐酸的存在, 可以加入石蕊试液,盐酸能使石蕊试液变红; 拓展应用:酸和碱能发生中和反应,需向酸性土壤中 加入碱性物质进行改良。
液颜色恰好变成无色为止。 实验现象: 溶液由红色变为无色
得出结论: 酸和碱能反应 这个结论是我们需要的吗?
反应前后溶液中离子发生了怎样的变化?
NaOH = Na+ + OHHCl = H+ + Cl-
NaOH + HCl = NaCl +H2O
氢氧化钠与盐酸反应的本质: 酸溶液中的氢离子和碱溶液中 的氢氧根离子反应生成水的过
③取样,滴加碳酸钠溶液
有气泡产生
④取样,滴加碳酸钠溶液
无气泡产生
⑤取样,加入锌粒等活泼金属 有气泡产生
⑥取样,加入锌粒等活泼金属 无气泡产生
恰好中和 盐酸过量 恰好中和 盐酸过量 恰好中和
化学与健康
人体酸碱性决定健康
血液是人体最重要、量最多的体液,健康血液的pH值呈弱碱 性,如果血液的pH值低于7.30,人体就处在亚健康状态,极有可 能得各种严重疾病――心脑血管病、骨质疏松、肾结石、关节炎、 痛风、高血压、癌症、高脂血症等等――人体的酸化是百病之源。
【设计实验】
实验操作
实验现象
实验结论
取反应后的溶液
于试管中,加入 __石__蕊__试__液____
_____溶_液__变__红______ __
猜想三成立
_
【拓展应用】我国土壤的酸碱性有“南酸北碱”之说 碱性物质
法,你认为需向酸性土壤中加入_____________进行
改良。
例题解析
【解析】实验一:氢氧化钠溶液呈碱性,能使酚酞试 液变红,能与盐酸反应生成氯化钠和水; 实验二:由于氢氧化钠呈碱性,能使酚酞试液变红, 而此时溶液是无色的,故一定不会有氢氧化钠剩余; 设计实验:猜想三中含有盐酸,要证明盐酸的存在, 可以加入石蕊试液,盐酸能使石蕊试液变红; 拓展应用:酸和碱能发生中和反应,需向酸性土壤中 加入碱性物质进行改良。
液颜色恰好变成无色为止。 实验现象: 溶液由红色变为无色
得出结论: 酸和碱能反应 这个结论是我们需要的吗?
反应前后溶液中离子发生了怎样的变化?
NaOH = Na+ + OHHCl = H+ + Cl-
NaOH + HCl = NaCl +H2O
氢氧化钠与盐酸反应的本质: 酸溶液中的氢离子和碱溶液中 的氢氧根离子反应生成水的过
③取样,滴加碳酸钠溶液
有气泡产生
④取样,滴加碳酸钠溶液
无气泡产生
⑤取样,加入锌粒等活泼金属 有气泡产生
⑥取样,加入锌粒等活泼金属 无气泡产生
恰好中和 盐酸过量 恰好中和 盐酸过量 恰好中和
化学与健康
人体酸碱性决定健康
血液是人体最重要、量最多的体液,健康血液的pH值呈弱碱 性,如果血液的pH值低于7.30,人体就处在亚健康状态,极有可 能得各种严重疾病――心脑血管病、骨质疏松、肾结石、关节炎、 痛风、高血压、癌症、高脂血症等等――人体的酸化是百病之源。
科粤版化学九年级下册 酸和碱的反应 课件

知1-讲
(1) 酸溶于水后,能解离出自由移动的H+ 和酸根离子,不
同的酸溶液中都含有相同的H+,故酸具有一些类似的
化学性质。
(2) 碱溶于水后,能解离出自由移动的金属离子和OH-,不
同的碱溶液中都含有相同的OH-,故碱具有一些类似的
化学性质。
感悟新知
知1-讲
特别提醒: 有带电粒子的物质不一定能导电,如氢氧化钠固体
C. Na+ 和Cl- 在该反应过程中没有被消耗
D. 恰好完全反应时,溶液呈中性
感悟新知
知2-练
解析:盐酸中存在的微粒有水分子、氢离子、氯离 子,A 错误;由氢氧化钠溶液与稀盐酸恰好完全反应的微 观示意图知,该反应的微观实质是H+ 和OH- 结合生成水 分子,B 正确;由氢氧化钠溶液和稀盐酸反应的微观示意 图知,Na+ 和Cl- 在该反应过程中没有被消耗,C 正确;恰 好完全反应时,溶质是氯化钠,溶液呈中性,D 正确。
感悟新知
4. 四大基本反应类型的比较
基本反应类型
概念
表达式
化合反应
由两种或两种以上的 物质生成另一种物质 的反应
A+B+… →C
分解反应
由一种物质生成两种
或两种以上其他物质 A →
的反应
B+C+…
知3-讲
特点 多变一
一变多
感悟新知
知3-讲
基本反应类型
概念
表达式
置换反应
由一种单质跟一种化 合物反应生成另一种 单质和另一种化合物 的反应
第八章 常见的酸、碱、盐
8.3 酸和碱的反应
农业和工业上常用熟石灰来改进酸性土壤和处 理酸性废水,你知道其中的原理吗?
粤教版九年级化学下册《 酸和碱的反应》PPT高效课堂 获奖课件 (3)(vip免费)

AB + CD == AD + CB 写出硫酸铜与氢氧化钠反应的化学方程式: ____H__2_S_O_4_+__2_N_a_O__H__=_=_=__N_a_2_S_O__4 _+_2_H__2O_______, 此反应复分解反应吗?_____是________。
知识回顾
知识点2 中和反应的应用 1.改良酸性或碱性土壤 (1)向鱼塘撒石灰,中和鱼塘底泥中过多的有机酸, 使鱼塘水达到适合鱼苗生长的pH。 (2)利用熟石灰中和土壤和某些水源的过多酸性,以 减轻酸雨的危害。
心之所向,行之所至。 只要从心底里非常想做某件事,就一定 会调动 身体里 的所有 潜能, 积极配 合。
2 你 的 恒 心 ,与 你的节 奏有关 当我们立下FLAG的时候,可能一开始都 会忍不 住下狠 劲儿。 之前一步都不想跑,决定健身了,就2公 里开跑 ,冲刺 5公里 。 之前一页书也不想看,决定勤奋了,就 焚膏油 以继晷 ,好像 不熬夜 都不好 意思说 自己看 书。 之前从没拉过筋,决定瑜伽了,就恨不 得立刻 把那支 僵硬了 几十年 的老腿 想掰哪 儿就掰 哪儿。 这种激情维持不了多久,很快就会被打 回原形 。 坚持从来就不是持续消耗,所以太用力 的人一 般都跑 不远。 作家村上春树的生活里有两件非常重要 的事情 :写作 和跑步 。 他全职写作没多久,发现身体变差,便 开始跑 步。 在普通人眼中,职业小说家应该是不舍 昼夜地 伏案工 作,资 深跑者 的锻炼 强度更 难以想 象。可 村上春 树的生 活却有 张有弛 ,十分 规律。 每天早 起后的 三四个 小时集 中精力 写作, 午休后 跑步, 日暮时 读书、 听音乐 。 在与写作和跑步相伴的几十年里,他既 勤勉耐 劳、不 惜体力 ,又谨 小慎微 地呵护 自己的 热情, 既怕惰 性来袭 ,又怕 用力过 猛。 他说:要让惯性的轮子以一定的速度准 确无误 地旋转 到最后 。 坚持,从长远看,要循序渐进,就每一 天来说 ,要量 力而为 。 既要摸清自己的节奏,也要管住自己按 这样的 节奏坚 持下去 。不盲 从,也 不随性 ,不蛮 干,也 不懒散 。 只有不乱节奏,才能持之以恒。
知识回顾
知识点2 中和反应的应用 1.改良酸性或碱性土壤 (1)向鱼塘撒石灰,中和鱼塘底泥中过多的有机酸, 使鱼塘水达到适合鱼苗生长的pH。 (2)利用熟石灰中和土壤和某些水源的过多酸性,以 减轻酸雨的危害。
心之所向,行之所至。 只要从心底里非常想做某件事,就一定 会调动 身体里 的所有 潜能, 积极配 合。
2 你 的 恒 心 ,与 你的节 奏有关 当我们立下FLAG的时候,可能一开始都 会忍不 住下狠 劲儿。 之前一步都不想跑,决定健身了,就2公 里开跑 ,冲刺 5公里 。 之前一页书也不想看,决定勤奋了,就 焚膏油 以继晷 ,好像 不熬夜 都不好 意思说 自己看 书。 之前从没拉过筋,决定瑜伽了,就恨不 得立刻 把那支 僵硬了 几十年 的老腿 想掰哪 儿就掰 哪儿。 这种激情维持不了多久,很快就会被打 回原形 。 坚持从来就不是持续消耗,所以太用力 的人一 般都跑 不远。 作家村上春树的生活里有两件非常重要 的事情 :写作 和跑步 。 他全职写作没多久,发现身体变差,便 开始跑 步。 在普通人眼中,职业小说家应该是不舍 昼夜地 伏案工 作,资 深跑者 的锻炼 强度更 难以想 象。可 村上春 树的生 活却有 张有弛 ,十分 规律。 每天早 起后的 三四个 小时集 中精力 写作, 午休后 跑步, 日暮时 读书、 听音乐 。 在与写作和跑步相伴的几十年里,他既 勤勉耐 劳、不 惜体力 ,又谨 小慎微 地呵护 自己的 热情, 既怕惰 性来袭 ,又怕 用力过 猛。 他说:要让惯性的轮子以一定的速度准 确无误 地旋转 到最后 。 坚持,从长远看,要循序渐进,就每一 天来说 ,要量 力而为 。 既要摸清自己的节奏,也要管住自己按 这样的 节奏坚 持下去 。不盲 从,也 不随性 ,不蛮 干,也 不懒散 。 只有不乱节奏,才能持之以恒。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
A
B
C
D
5.室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,
利用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸
的质量而变化如图所示。
①由图示可知,稀盐酸与氢氧化钠溶液发生的中和反应是 放热 (填
“吸热”、“放热”或“无热量变化”)的反应。
②反应的化学方程式N为aOH+HCl=NaCl+H,2OB点表示的含义是盐化酸钠和溶氢液氧恰。
20 、为目标,晚卧夜半,梦别星辰,脚踏实地,凌云舍我其谁! 17 、美丽的空想比不上踏实地做事,只要开始行动,就算再晚也不迟。 7 、只有你的未来,才能挥霍我的现在;只有我的最爱,给我最致命的伤害。 1 、用心工作,成功根本;用心思考,力量根本;用心读书,智慧根本;用心结缘,交友根本;用心慈悲,做人根本;用心祝福,快乐根本。愿你用 心,幸福一生! 1 、人生,就要闯出一条路来!为了事业,为了奋斗的人生,尽管失去许多,但有失必有得!而得到的往往会比失去的更重要,它是人生的价值 与意义。
(利用给出的药品讨论、设计实验方案)
步骤
药品
现象
结论
结论:酸和碱发生了反应
探究活动二:NaOH溶液和稀盐酸反应后混合物检验
步骤
1.取3mLNaOH溶液于试管 中,滴1、2滴酚酞溶液
现象
溶液变红
结论
溶液呈碱性
2.逐渐往NaOH溶液中滴稀 溶液颜色逐渐变浅, 恰好完全反应,
盐酸、振荡直至恰好褪色 直到恰好无色
A、Zn + 2HCl = ZnCl2 + H2↑ B、CuO + 2HCl = CuCl2+ H2O C、Ba(OH)2 + H2SO4 = BaSO4 ↓+ 2H2O D、AgNO3 + HCl = AgCl↓ + HNO3
1.下列实际应用中,利用中和反应原理的是(A)
①用氢氧化钠溶液洗去石油产品中的残余硫酸; ②用稀硫酸除铁锈; ③用熟石灰改良酸性土壤; ④用碳酸氢钠治疗胃酸过多 A.①③ B.③④ C.①②④ D.①③④
③从A到B过程中,烧杯中溶液的pH逐渐 减小 。
好完全反应
④减小C处溶液中溶质是 NaCl、HC。l
14 、不管你干什么,都会有两种结果: 一种是笑话,一种是神话。如果你半途而废,只能成为别人眼中的笑话;但如果你成功了,你就变成她 们眼中的神话。社会就是现实!要么不做,要么做好。 15 、机遇是难求的,失去了就不会再来,把握好现有的机会,努力进取,那么你将会得到不菲的收获。 17 、只有满怀勇气,不畏艰辛,才能获得更大的成功。 13 、不断进取,勇于面对一切困难,努力克服它,战胜它,这是生存的法则。相反,逃避是懦夫的作为,最终只能带来更多的危机。 3 、善者,吾善之;不善者,吾亦善之;德善。信者,吾信之;不信者,吾亦信之;德信。 8 、我们的安全感,来自于充分体验不安全感。 18 、成功就是在不断地克服困难,在困难中创造自己的价值。有心人会在困境中找出路,而无心的人只会在众多的机会中找借口。 7 、只有你的未来,才能挥霍我的现在;只有我的最爱,给我最致命的伤害。 3 、太上,不知有之;其次,亲而誉之;其次,畏之;其次,侮之。信不足焉,有不信焉。 19 、拥有的时候,多加珍惜,无论是亲情,友情还是爱情,平安就是福。且行且惜,且走且悟,人生之中唯有自强不息,勇敢向前,方可走 出一条阳光大道。
2.下列物质中,属于盐类的是( B )
A.Fe(OH)2 B.AgCl C.CO2 D.H2SO4
3.下列要借助酸碱指示剂才能判断发生的反应是( B )
A.大理石和稀盐酸
B.石灰水和稀盐酸
C.铁锈与稀盐酸
D.镁和稀硫酸
4.往稀盐酸中滴加氢氧化钠溶液至完全中和时为止,
溶液的pH变化的图象正确的是( D)
8.3 酸和碱的反应
蜜蜂
用肥皂水或氨水清洗
马蜂
用食醋止痛止痒
一、中和反应
实验:取3 mL氢氧化钠溶液于试管中,逐 滴加入稀盐酸,观察到什么现象?
a.没有现象,则没有反应
稀盐酸
b.发生反应,但无明显现象
氢氧化钠 溶液
探究活动一:NaOH溶液和稀盐酸能反应么?
提供药品:NaOH 溶液 、 稀盐酸 紫色石蕊试液、无色酚酞试液
酸+ 碱 = 盐 + 水
金属离子 酸根离子
中和反应
2、中和反应的微观实质
HCl + NaOH == NaCl + H2O 2HCl + Cu(OH)2 == CuCl2 + 2H2O H2SO4+ Ca(OH)2 == CaSO4 + 2H2O
H+ + OH- = H2O
1、下列反应中属于 再滴两滴NaOH溶液,振荡
溶液变红
NaOH过量, 溶液呈碱性
4.再次滴入微量稀盐酸, 溶液由红色变为无色 HCl过量或恰好反应,
振荡
溶液呈酸性或中性
讨论
如何用实验证明稀盐酸和氢氧化钠反应后, 酸过量还是恰好完全反应呢?
1、中和反应的定义
HCl + NaOH == NaCl + H2O 2 HCl + Cu(OH)2 == CuCl2 + 2H2O
