紫外可见光谱及其应用(结合文献)
现代分析仪器在药品检测中的应用

现代分析仪器在药品检测中的应用摘要:现代分析仪器在药品检测中的应用越来越广泛,为保证药品质量和安全性起到了重要作用。
本论文主要探讨了几种常见的现代分析仪器及其在药品检测中的应用,包括高效液相色谱仪(HPLC)、气相色谱质谱联用技术(GC-MS)、红外光谱仪(FT-IR)和紫外可见光谱仪(UV-Vis)等。
关键词:现代分析仪器;药品检测;应用引言随着药品的广泛应用和市场需求的增长,对药品质量和安全性的要求也越来越高。
传统的药品检测方法往往面临着复杂样本分析、低灵敏度和时间消耗等问题。
而现代分析仪器的出现和发展为药品检测带来了革命性的变化。
本论文将重点讨论几种常见的现代分析仪器及其在药品检测中的应用,以期为进一步提高药品质量和安全性提供技术支持。
1.现代分析仪器在药品检测中优势1.1高效准确现代分析仪器具备高分辨率和精度的特点,能够准确地分析和定量各种化合物成分。
例如,高效液相色谱仪(HPLC)和气相色谱仪(GC)能够对复杂样品进行快速和准确的分离和定量。
现代分析仪器能够检测非常微量的目标化合物,使得在药品制造过程中不合格的成分被及时发现和排除。
许多现代分析仪器具备快速分析的能力,可以实现高通量的样品处理和分析。
这使得药品制造商能够更快地获得检测结果,提高生产效率。
现代分析仪器可以适应不同类型的药品和检测需求。
无论是检测药物活性成分、污染物残留物还是药品稳定性,不同的分析仪器都可以应用于这些不同的领域。
1.2多功能性和多样性现代分析仪器具备多种功能,可以满足不同类型的药品检测需求。
例如,质谱仪(MS)可以用于鉴定和定量药物活性成分、分析药物代谢产物以及检测其他杂质或污染物等。
存在许多不同类型的分析仪器,涵盖了各种不同的技术和原理。
这使得药品制造商能够选择适合其特定需求的仪器。
例如,使用高效液相色谱仪(HPLC)可以对药物中的溶解度、纯度和活性成分进行分析;而红外光谱仪(IR)则可以对药品中的分子结构进行鉴定。
紫外和可见光吸收光谱

紫外和可见光吸收光谱1.紫外光谱及其产生⑴紫外光的波长范围紫外光的波长范围为4-400nm。
200-400为近紫外区,4-200nm为远紫外区。
由于波长很短的紫外光会被空气中氧和二氧化碳吸收,研究远紫外区的吸收光谱很困难,一般的紫外光谱仅仅是用来研究近紫外区的吸收。
⑵紫外光谱当把一束光通过有机化合物时,某一波长的光可能吸收很强,而对其他波长的光可能吸收很弱,或者根本不吸收。
当化合物吸收一定波长的紫外光时,电子发生跃迁,所产生的吸收光谱叫做紫外吸收光谱,简称紫外光谱。
⑶电子跃迁的种类在有机化合物分子中,由于化合物的价电子有三种类型,即σ键电子、π键电子和未成键的 n 电子,在电子吸收光谱中,电子跃迁主要是经下三种。
①σ-σ*跃迁σ电子是结合得最牢固的价电子,在基态下,电子在成键轨道中,能级最低,而σ*态是最高能级。
σ-σ*跃迁需要相当高的辐射能量。
在一般情况下,仅在200nm以下约~150nm才能观察到,即在一般紫外光谱仪工作范围之外,只能用真空紫外光谱仪才可观察出来(在无氧和二氧化碳的情况下)。
所以测紫外光谱时,常常用烷烃作溶剂。
② n电子的跃迁n 电子是指象N,S,O,X 等原子上未共用的电子。
它的跃迁有两种方式。
第一种方式:n-π* 跃迁未共用电子激发跃入π*轨道,产生吸收带,称为R带(基团型的,Radikalartig德文),由n-π*引起的,在200 nm以上。
如:醛酮分子中羰基在275-295nm处有吸收带,为C=O中n-π*跃迁吸收带。
第二种方式是n→σ*跃迁,这种跃迁所需的能量大于n-π*,故醇醚均在远紫外区才出现吸收带。
~ 200nm。
如甲醇λmax183nm。
③π→π*跃迁乙烯分子中π电子吸收光能量,跃迁到π*轨道。
吸收带在远紫外区。
当双键上氢逐个被烯基取代后,由于共轭作用,π→π*能级减小。
吸收带向长波递增。
由共轭双键产生的吸收带称为K带,其特征是摩尔消光系数大于104。
在近紫外区吸收,CH2=CH2 λmax162nm,CH2=CH-CH=CH2 λmax217nm。
紫外—可见光谱水质cod检测的原理、仪器及方法技术研究

中文摘要 I摘 要随着我国社会经济的高速发展,水污染事件频发,造成水的使用价值降低或丧失,进而影响人民生活和工农业生产。
为此,开展水环境检测监测乃是确保水质安全的重要措施之一。
目前,常见的水质检测技术有化学分析法,光谱法和生物传感法。
紫外-可见光谱法作为光谱法之一,因无二次污染、仪器操作简单、成本低和易于实现在线、实时检测监测等优点,在水质检测监测中,日益为人们所亲睐。
特别是,化学需氧量(Chemical Oxygen Demand ,COD )又往往作为衡量水中有机物质含量多少的指标。
化学需氧量(COD )越大,说明水体受有机物的污染越严重。
有鉴于此,本文以四川省科技支撑技术项目(编号:2012SZ011)和四川碧朗科技有限公司横向合作科研项目“光谱多参数水质在线自动监测仪研制”(合同编号:1042012920140453)及重庆市研究生科研应用型科研创新项目(编号:CYS14039)为依托,以紫外-可见光谱法水质COD 检测技术为背景,开展了紫外-可见光谱法水质COD 检测基本原理、仪器及方法技术研究和开发工作,研究内容主要包括:① 研究并阐述了基于紫外-可见光谱法水质COD 检测的基本原理。
通过对紫外-可见光谱法水质COD 检测原理的分析研究,明确了水质COD 仪器系统研制的实现方案。
② 研究与分析了水质COD 仪器系统研制的功能要求和性能指标。
基此,构建了相关的仪器系统及其应用软件。
借助于光谱仪等光谱测量单元,实现了水样的COD 等参数的测量。
测试了水质COD 仪器系统的性能指标。
与此同时,基于LabVIEW 开发平台,进行了系统软件设计并进行调试。
③ 研究并建立了基于极限学习机(ELM )的水质COD 检测预测模型。
水质COD 是水环境中还原性物质的体现,在河流污染和工业废水性质的研究以及废水处理厂的运行管理中,它是一个重要的而且能较快测定的有机物污染参数。
光谱法检测水质COD ,建立检测预测模型,乃是进行水质COD 检测不可或缺的环节。
紫外原理及其在有机化学中的应用

紫外光谱在有机化学中的应用名字*(某某大学化学系,学校所在城市,邮编)摘要: 本文简要介绍了紫外光谱的基本原理并通过一些实例叙述了其在有机化学中的一些应用,通过这些实例可以理解紫外吸收光谱在有机化学中应用的重要性。
关键词:紫外光谱;有机化学;应用Application of Ultraviolet Spectrum in Organic Chemistry# # *(Department of Chemistry, ##University, ##, P.R. China)Abstract:This paper briefly introduced the basic principle of Ultraviolet Spectrum (UV) and described parts of its application in organic chemistry through some examples which make it evident that significantly important is UV.Key Words: Ultraviolet spectrum; Organic chemistry; Application1.2电子跃迁的类型有机化合物紫外吸收光谱(电子光谱)是由分子外层电子或价电子跃迁所产生的。
按分子轨道理论,有机化合物分子中有:成键σ轨道,反键σ*轨道;成键π轨道,反键π*轨道(不饱和烃);另外还有非键轨道(杂原子存在)。
各种轨道的能级不同,如图1所示。
图1各种电子跃迁的相对能量Fig.1 Relative energy of various electron transition相应的外层电子和价电子有三种:σ电子、π电子和n 电子。
通常情况下,电子处于低的能级(成键轨道和非键轨道)。
当用合适能量的紫外光照射分子时,分子可能吸收光的能量,而从低能级跃迁到反键轨道。
紫外可见吸收光谱、漫反射光谱和荧光光谱及其应用

Tanabe—Sugano图
4.光谱化学系列和电子云扩胀
配合物的能级主要和配位场分裂 能Dg及d电子间的互斥参数B有关,在 分析一系列配合物的电子光谱中,发 现了跟这二个参数(Dg和B)有关的 变化规律,这就是所谓的“光谱化学 系列”和“电子云扩胀系列”,用此 可推出一些化学上有用的信息。
1)姜─泰勒效应
[Ti(H2O)6]3+的吸收光谱
1927年,H.A.John and E.Teller指出,若d壳 层电子云分布呈不对称,则配合物的构型将会 发生形变,产生长、短M-L键。这一现象称为 姜-泰勒效应。
姜-泰勒效应的本质:是体系消除基态简并态 ,电子填入较低的能级中,从而获得额外的 LFSE。
光谱化学系列中的△(或Dg)的大小不仅受到 静电效应的影响,而且还受到共价性的影响。
对同一配位体,Dg也因中心金属离子
的不同而有差别,变化规律大体有: Mn2+ <Co2+ = Ni2+ <V2+ <Fe3+ <Cr3+ <
V3+ <Co3+ <Mn4+ <Mo3+ <Rh3+<Ir3+ < Pt4+ ……
4) 振动偶合
配位场强度与金属──配体距离有关,振动偶合会使状态数 增多,增加了谱带的宽度。
5) 海森堡测不准关系
涉及能量和时间的测不准关系式为:
△Eτ≥1/2 h
式中 △E是寿命为τ的某个状态的能量不确定性。这个关系式 表明,具有有限寿命的状态并不具有准确的恒定的能量,其能 量有一分布或不确定性。此不确定性随寿命的减少而增加。除 基态外,所有的状态都表现出自发发射,所以激发态并无尖锐 的确定能量。而激发态的有限寿命及由此带来的能量不确定性 就使谱峰产生了一定的宽度,测不准加宽属于正常自然宽度, 许多因素对线宽的贡献大大超过了测不准关系。
紫外-可见(UV-Vis)光谱法在中药质量控制中的应用

紫外-可见(UV-Vis)光谱法在中药质量控制中的应用李文龙【摘要】紫外-可见(UV-Vis)光谱法作为一种传统的光谱分析方法,在中药质量控制领域得到广泛应用,本文对该技术的应用现状进行文献综述,对该技术在大类物质含量测定、作为色谱检测器、及其与化学计量学的结合使用情况进行详细论述,并对其应用前景进行展望,可为该技术更为深入、全面的应用提供参考.【期刊名称】《中国民族民间医药》【年(卷),期】2018(027)022【总页数】4页(P47-50)【关键词】紫外-可见光谱;中药质量控制;比色法;检测器;化学计量学【作者】李文龙【作者单位】天津中医药大学中药制药工程学院, 天津 300193;浙江大学药物信息学研究所, 浙江杭州 310058【正文语种】中文【中图分类】R282紫外可见光谱(Ultraviolet-visible spectroscopy, UV-Vis)是指波长范围在200~760 nm之间的波段,该波段属于电子光谱,是由于价电子的跃迁而产生的吸收光谱。
利用物质的分子或离子对紫外和可见光的吸收所产生的UV-Vis光谱及吸收程度可以对物质的组成、含量及结构进行分析、测定和推断。
UV-Vis光谱用于具有紫外、可见光吸收物质的检测,灵敏度高,特征性好,在中药质量控制得到了广泛的应用。
本文对UV-Vis光谱法在中药质量控制中的应用进行综述,并对其应用前景进行展望,以期为相关领域的研究提供参考。
1 比色法测定多种大类物质的含量比色法(colorimetry)是通过比较或测量有色物质溶液颜色深度,并根据朗伯比尔定律确定待测组分浓度或含量的方法。
常用的检测波段是UV-Vis波段,虽然该方法是一种历史悠久的传统分析方法,但目前在中药质量控制领域仍被广泛应用。
苏玉顺等[1]对UV-Vis光谱法测定植物多糖含量过程中的显色剂选取、测定条件的优化以及具体应用进行了分析,具有较好的参考价值。
古炳明等[2]采用UV-Vis 分光光度法建立了巴豆中可溶性蛋白含量的测定方法,检测波长为593 nm,巴豆中可溶性蛋白在0.010 3~0.103 0 mg/ml范围内线性关系良好,平均回收率为98.37%,RSD为1.01%,该方法简单、方便、专属性强,可为其质量评价提供理论依据。
有机波谱分析 期中论文

紫外光谱在化学中的应用姓名:苏超俊应用化学(精细化工)学号:20091811338中文摘要:紫外光谱涉及电子在分子轨道上的跃迁以及各种跃迁对应的吸收带对结构的依赖关系。
虽然紫外吸收带的数目少,峰宽且平,对结构的敏感性差,但作为辅助方法,在结构测定中仍很有用途。
紫外光谱中总结的一些经验规律可用于推断共轭系统及发色团的存在,或用于验证其它方法推演的结构。
紫外分光光度计应用广泛,是常规测试仪器之一,操作简单,方便易行。
ABSTRACT: UltraViolet Absorption Spectrometry involves molecular orbitals during electron transfer processes and various transition corresponding to the absorption band of structural dependencies. Although the amount of UV absorption is very small, peak width is smooth, the sensitivity is bad to the structure. As an auxiliary method, it’s still useful in the structure determination.In the Ultraviolet spectroscopy to summarize some experience rule,in order to inference the existence of the Conjugated system and chromophores,or verficicate the structure in the other methods .Ultraviolet spectrophotometer is used widely, is one of the conventional testing apparatus, simple operation, convenient and easy to operate.关键词:紫外光谱、跃迁、共轭KEY WQRDS:UltraViolet Absorption Spectrometry /Transition/Conjugate一、紫外光谱的基本原理1、紫外吸收的产生这种分子吸收光谱产生于价电子和分子轨道上的电子在电子能级间的跃迁,因此又称电子光谱。
紫外可见光光谱

波长: 400 — 800 nm,1.5 — 3 eV
一般的电子跃迁能量变化在1 – 20 eV。
10
能级 跃迁
电子能级间跃迁 的同时,总伴随 有振动和转动能 级间的跃迁。即 电子光谱中总包 含有振动能级和 转动能级间跃迁 产生的若干谱线 而呈现宽谱带。
11
物质对光的选择性吸收
物质吸收光之后
Bisdisulizole disodium: UVA 苯基二苯并咪唑四 磺酸酯二钠
7
化学防晒霜成分特点
苯环 不饱和键多 杂原子化合物 不饱和键越多,吸收往UVA移
为什么?
8
防晒霜的使用
该涂抹多少?或 是防晒霜的浓度 多高才有效?
9
紫外线为什么会伤害?---- 能 量
紫外光
近紫外: 200 — 400 nm, 3 — 6 eV 真空紫外:100 — 200 nm, 6 — 12 eV
光谱的来源主要是在这些有机分子中s、 p和n轨道上的电子的跃迁。(The observed transitions involve electrons engaged in s or p or nonbonding n electron orbitals.
43
分子轨道(molecular orbitals)
41
Electronic Transitions of organic compounds etc.
紫外可见光谱和分子轨道的跃迁
42
概要
紫外可见光谱研究的主要对象是有机分 子 (Organic compounds represent the majority of the studies made in UV/Vis.)
Ce(IV)离子的吸收光谱 A:使用玻璃比色皿 B:使用石英比色皿 虚假峰的出现(虚假吸收)
实验报告紫外可见光谱实验

实验报告紫外可见光谱实验实验报告紫外可见光谱实验一、引言紫外可见光谱实验是一种常用的分析技术,能够通过测量样品在紫外可见光区的吸收光谱来分析其化学结构和浓度。
本实验旨在通过测量苯酚和水溶液的紫外可见光谱,探究其吸收峰的特征以及相关参数的计算。
二、实验步骤1. 准备工作a. 预先准备苯酚和水溶液。
b. 标定紫外可见光谱仪。
2. 测量吸收光谱a. 将空白试剂(纯溶剂)放入光谱仪的比色皿中,设置空白。
b. 用吸管将苯酚溶液分别取出一定体积放入比色皿中,测量吸收光谱。
3. 数据处理与分析a. 绘制紫外可见光谱图。
b. 记录吸收峰的波长。
c. 根据比色皿中苯酚的浓度,计算吸光度值。
d. 使用Beer-Lambert定律计算苯酚的摩尔吸光系数。
三、实验结果实验结果如下:| 波长 (nm) | 吸光度 ||----------|------------|| 200 | 0.1 || 210 | 0.15 || 220 | 0.2 || 230 | 0.25 || 240 | 0.3 |四、讨论与分析1. 吸收光谱图分析由上述实验结果可知,在紫外可见光区,苯酚溶液对特定波长的光有吸收作用。
从吸光度随波长的变化可以看出,苯酚溶液在200 nm 至240 nm的波长范围内吸收能力逐渐增强。
2. 吸收峰波长计算根据吸收光谱图,吸收峰波长为230 nm。
此波长处的吸光度最大,说明苯酚对该波长的光吸收最强。
3. 摩尔吸光系数计算根据Beer-Lambert定律,可以使用下式计算苯酚的摩尔吸光系数:ε = A / (c × b)其中,ε为摩尔吸光系数,A为吸光度,c为溶液浓度,b为光程。
假设苯酚溶液浓度为1 mol/L,光程为1 cm,则根据实验结果计算得到摩尔吸光系数为0.25 L/mol·cm。
五、结论通过紫外可见光谱实验,我们成功测量苯酚溶液在紫外可见光区的吸收光谱。
根据实验结果,确定了苯酚的吸收峰波长为230 nm,并计算得到其摩尔吸光系数为0.25 L/mol·cm。
紫外可见吸收光谱在Li-S电池中的应用
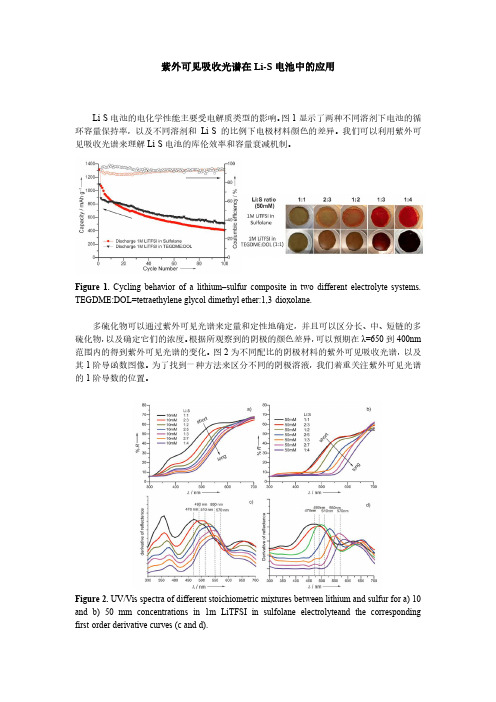
紫外可见吸收光谱在Li-S电池中的应用Li-S电池的电化学性能主要受电解质类型的影响。
图1显示了两种不同溶剂下电池的循环容量保持率,以及不同溶剂和Li-S 的比例下电极材料颜色的差异。
我们可以利用紫外可见吸收光谱来理解Li-S电池的库伦效率和容量衰减机制。
Figure 1.Cycling behavior of a lithium–sulfur composite in two different electrolyte systems. TEGDME:DOL=tetraethylene glycol dimethyl ether:1,3-dioxolane.多硫化物可以通过紫外可见光谱来定量和定性地确定,并且可以区分长、中、短链的多硫化物,以及确定它们的浓度。
根据所观察到的阴极的颜色差异,可以预期在λ=650到400nm 范围内的得到紫外可见光谱的变化。
图2为不同配比的阴极材料的紫外可见吸收光谱,以及其1阶导函数图像。
为了找到一种方法来区分不同的阴极溶液,我们着重关注紫外可见光谱的1阶导数的位置。
Figure 2. UV/Vis spectra of different stoichiometric mixtures between lithium and sulfur for a) 10 and b) 50 mm concentrations in 1m LiTFSI in sulfolane electrolyteand the corresponding first-order derivative curves (c and d).从1阶导数图像中可以看出,在Sulfolane电解液中λ=570 nm是长链的多硫化物。
λ=550和510nm处归因于中链多硫化物,而在λ=490和470 nm处可以归因于短链多硫化物。
同理,在TEGDME:DOI电解液中也观察到类似的趋势: 特征吸收峰为λ=620nm,580nm/550nm,520nm/450nm。
紫外-可见全光谱分析仪在水质监测领域的研究进展与应用

紫外-可见全光谱分析仪在水质监测领域的研究进展与应用作者:刘国肖来源:《价值工程》2019年第31期摘要:随着水环境问题的日益严重,水环境监测以及管理越来越重要,水质监测技术的应用也越加广泛。
直接的紫外-可见全光谱分析仪因其无需化学试剂、成本较低、分析速度较快、无二次污染及可实现多参数测量等很多优点,被广泛应用在工业废水、生活污水及地表水的检测中,本文就紫外-可见全光谱分析仪在水质监测领域的研究进展与应用进行了叙述。
Abstract: With the increasing environmental problems of water environment, water environment monitoring and management are becoming more and more important, and the application of water quality monitoring technology is becoming more widespread. The direct UV-visible full-spectrum analyzer is widely used in industrial wastewater, domestic sewage and surface water because it has many advantages such as no chemical reagents, low cost, fast analysis speed, no secondary pollution and multi-parameter measurement. In the detection, this paper describes the research progress and application of UV-visible full spectrum analyzer in the field of water quality monitoring.关键词:紫外-可见全光谱;水质监测;应用Key words: UV-visible full spectrum;water quality monitoring;application中图分类号:X832;O657.3; ; ; ; ; ; ; ; ; ; ; ; ; ; ;文献标识码:A; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; 文章编号:1006-4311(2019)31-0166-020; 引言近年来,随着国家和政策的发展,对水质监测的实时性和监测频率要求越来越高,使得在线监测技术得到了广泛关注和快速发展,越来越多的水质在线监测设备被广泛应用[1]。
化学中的光谱学及其应用

化学中的光谱学及其应用光谱学是一门研究物质对光的吸收、散射、发射行为的学科。
在化学中,光谱学是一种非常重要的分析手段,在许多领域都有着广泛的应用。
本文将介绍化学中的光谱学及其应用。
一、紫外可见光谱紫外可见光谱是一种测量物质分子电子跃迁的光谱学方法。
其原理是将待测物质溶解于适当的溶剂中,通过吸收可见光和紫外光,使分子内的电子发生跃迁,并产生一些特定的吸收谱带。
通常我们用紫外可见光谱来分析一些具有共轭结构的分子,如吲哚、苯、酚等,这些分子的分子轨道能级结构与跃迁等都较为复杂。
同时,紫外可见光谱也被广泛应用于药物分析的研究中,如草酸钙、盐酸麦角碱、磺胺嘧啶等。
此外,其还可以用于测定水样中的氯离子、硝酸盐离子和铵盐离子等。
二、红外光谱红外光谱是一种研究物质分子振动和转动状态的光谱学方法。
我们经常使用红外光谱去分析能与红外线发生相互作用的物种,如淀粉、蛋白质和有机物。
在药物合成过程中,利用红外光谱的拉曼散射谱和离子化透射谱参数,可以确定药物的结构,并能对比研究药物的不同种类及其制品。
此外,红外光谱还可以对环境污染领域进行分析,如大气中二氧化硫、硝酸盐和颗粒物等。
三、核磁共振光谱核磁共振光谱是一种分析分子结构和杂质的非破坏性光谱学方法。
在化学领域中,核磁共振光谱被广泛用于分析有机化合物的结构和成分。
此外,它还可以用于表征生物大分子,如核酸和蛋白质的三维结构。
在药物过程中,核磁共振光谱可以提供非常明确和准确的信息,帮助确定药物的稳定性、溶解度以及血浆蛋白结合程度等。
四、质谱质谱是一种通过分析分子的离子质量和相对量来确定其组成的光谱学方法。
在化学中,质谱被广泛用于分析分子的结构和组成。
在药物研究中,质谱是一种非常重要的分析手段,可用于药物分子的生产和质量控制。
其在质谱成像和药物代谢研究中的应用也越来越广泛。
总的来说,光谱学是化学分析中一种非常重要的手段,对于药物合成、环境分析等领域都有着广泛的应用。
随着分析技术和分析方法的不断发展,相信光谱学在未来会有更广阔的应用前景。
紫外——可见光谱法在卟啉类化合物结构分析中的应用

紫外-可见光谱法在卟啉类化合物结构表征中的应用摘要:简述了紫外-可见光谱分析的基本原理,及其在有机化化学中的应用;结合卟啉、金属卟啉的吸收特点,对紫外-可见光谱在其结构表征中的应用作了归纳性的总结。
关键词:紫外-可见光谱法;应用;卟啉;金属卟啉;结构表征1 紫外-可见吸收光谱分析基本原理紫外光谱(UV)是指波长在200~400nm;可见光谱则是波长在400~800nm的电磁波吸收光谱。
相应于上述波长的能量范围约在670~314kJ/mol和314~155kJ/mol。
因此,它们是属于π电子(成键的或孤对的电子)跃迁。
所以,不是所有的有机化合物,都能给出它们的吸收光谱,而主要是对具有共轭双键结构的化合物和芳香族化合物才能给出光谱。
如果用紫外和可见光照射含有共轭的不饱和化合物溶液,可以看到一部分光线被吸收了,吸收光线的多少,取决于入射光的波长和化合物的结构。
如果以波长为横坐标,以紫外、可见光线的吸收强度(有时也称消光系数或摩尔吸收度)为纵坐标作图,就得到紫外或可见光谱图。
同一种物质对不同波长的光吸收不同;不同浓度的同一种物质,其吸收曲线形状相似、λmax不变,只是吸光度大小不同;而对于不同物质,它们的吸收曲线形状和λmax均不同。
当外层电子吸收紫外或可见辐射后,就从基态向激发态(反键轨道)跃迁。
主要有四种跃迁形式,如图1。
所需能量ΔΕ大小顺序为:n→π*< π→π*< n→σ*< σ→σ*。
吸收带是指吸收峰在光谱中的波带位置,根据电子及分子轨道理论,有机化合物紫外-可见光区的吸收带有四种类型:R吸收带——由化合物中的n→π*跃迁产生的吸收带。
其强度小,ε<100;λmax位于较长波长处,>270nm;K吸收带——由共轭体系中π→π*跃迁产生的吸收带。
其强度大,ε>104;λmax比R带的短,一般>200nm;B 吸收带——由苯环本身振动及闭合环状共轭双键π→π*跃迁产生的吸收带。
紫外光谱在有机化合物结构分析中的应用

紫外光谱在化合物结构分析中的应用【摘要】紫外-可见光谱(ultraviolet一Visiblespeetroseopy,UV-Vis),也简称为紫外光谱(UV),属于吸收光谱的一种。
由于紫外光谱本身有许多特点:测量灵敏和准确度高,应用范围广,对很多金属元素和非金属元素及其化合物都能进行测定,也能定性或定量的测定大部分有机化合物;此外,仪器的价格比较便宜,操作简便、快速,易于普及推广,至今仍是有机化合物结构鉴定的重要工具。
因此,本文首先介绍紫外光谱用于定性分析的依据和一般规律,然后归纳了影响紫外-可见光谱的一些因素,最后举例说明紫外光谱在化合物结构分析中的应用。
【关键词】紫外-可见光谱定性分析影响因素结构分析光谱数据前言紫外吸收光谱是分子中最外层价电子在不同能级轨道上跃迁而产生的,它反映了分子中价电子跃迁时的能量变化与化合物所含发色基团之间的关系。
UV谱图的特征首先取决于分子中含有的双键数目、共轭情况和几何排列,其次取决于分子中的双键与未成键电子的共轭情况和其周围存在的饱和取代基的种类和数目,它主要提供了分子内共轭体系的结构信息[1]。
通常UV谱图组成比较简单,特征性不是很强,但用它来鉴定共轭发色基团却有独到之处。
UV吸收谱带的位置和摩尔消光系数的数值,一般无法判断官能团的存在,但它能提供化合物的结构骨架及构型、构象情况,因此至今仍为一项重要的测试分子结构的有用手段。
紫外-可见吸收光谱是化学分析中常用的一种快速、简便的分析方法,广泛用于有机[2-3]、无机[4]、生化[5]、涂料[6]、药物[7]等领域和国民经济部门[8]。
紫外光谱用于定性分析的依据和一般规律利用紫外光谱定性分析应同时考虑吸收谱带的个数、位置、强度以及形状。
从吸收谱带位置可以估计被测物结构中共轭体系的大小;结合吸收强度可以判断吸收带的类型,以便推测生色团的种类。
注意所谓吸收带的形状主要是指其可反映精细结构,因为精细结构是芳香族化合物的谱带特征。
药品检测中的光谱分析技术研究

药品检测中的光谱分析技术研究137400摘要:光谱分析技术是药品检测领域的重要工具,它通过分析物质吸收或发射的光谱来鉴定和测定药物成分。
近年来,随着分析技术的不断进步和仪器性能的显著提高,光谱分析技术在药品质量控制、成分分析以及新药研发等方面扮演着越来越重要的角色。
本文综述了光谱分析技术在药品检测中的应用,包括紫外/可见光谱、红外光谱、核磁共振光谱、质谱分析等方法,旨在为相关人员提供参考。
关键词:药品检测;光谱分析;技术研究引言:在药品研发与生产的各个阶段,保证药品的质量安全是至关重要的。
传统的化学与生物学方法往往耗时且破坏性强,而光谱分析技术以其非破坏性、高灵敏度和快速的特点,在药品检测领域中占据了独特的地位。
光谱分析可以提供关于分子结构、组成及浓度等的丰富信息,对于复杂样品的快速鉴定与定量分析具有不可替代的优势。
1.光谱分析的原理及类型光谱分析是指利用物质与电磁辐射之间的相互作用来进行定性或定量分析的一类方法,当物质受到激发时,会吸收或发射特定波长的光,这些光的集合即形成了光谱。
光谱分析根据电磁辐射的不同波段,可以细分为紫外/可见光谱分析(UV/Vis)、红外光谱分析(IR)、核磁共振光谱分析(NMR)和质谱分析(MS)等,每种分析技术都有其独特的优点和适应的样品类型。
例如,UV/Vis 光谱常用于分析药品中的有机化合物,而NMR和MS则在确定复杂有机分子的结构中发挥重要作用。
光谱分析技术在药品检测中的应用不仅提升了检测效率,还可能对药物的研发周期形成积极的推动作用。
随着光源和检测器技术的发展,结合先进的计算机算法和大数据分析,光谱分析技术正向更高的灵敏度、分辨率及快速性发展,为药品检测提供了强有力的技术支持[1]。
2.药品检测中的光谱分析技术分析2.1 紫外可见光谱技术紫外可见光谱(UV/Vis)技术是基于分子吸收紫外或可见光区域的电磁辐射的原理进行的。
该技术主要应用于具有共轭双键系统的有机分子,因为这些结构可以在紫外或可见光区域产生特定的吸收峰。
紫外可见光谱鉴定有机物结构

在具体实践是,可用标准物质测定后经行光谱比较,也可采用与标准的有机化合物光谱图 像对照,常用的标准图谱和电子光谱数据表如下:
Sadtler Standard Spectra (Ultraviolet),Heyden,London,1978 萨特勒标准图谱共收集了 4600 中化合物的紫外光谱;
这就确定了维生素 K 的骨架结构是为:
R.A.Friendel and M.Orhin, Ultraviolet Spectra of Aromatic Compounds,Wiley, New York, 1951 共收集了 579 种芳香化合物的紫外光谱;
③ Kenzo Hirayama, Handbook of Ultraviolet and Visible Abosorption Spectra of Organic Compounds, New York, Plenum.
紫外可见光谱在有机化合物结构鉴定中的应用
1. 定性分析
利用紫外光谱定性分析一般要考虑吸收带的个数、位置、强度以及形状。从吸收带的位置 可以估计被测物质结构中共轭体系的大小;结合强度可以判断吸收带的类型,以便推测生色团 的种类。吸收带的形状主要指其反应的精细结构,这是芳香族化合物谱代的特征。其中,吸收 带的位置(λmax)和吸收强度(εmax)是定性的主要依据。根据紫外光谱原理和和吸收带波长经 验计算方法,可以归纳出有机物紫外吸收与结构关系的一般规律:
4 根据生色团判断化合物的骨架
具有相同生色团及助色团的化合物,其紫外光谱图大致相同。据此,可用来推测未知化合 物的骨架。例如:维生素 K 经测定有 249nm、260nm、325nm 吸收带,研究发现它与 1,4-苯醌 的吸收带(250nm、330nm)相似。因此,将其与几个已知不同取代基的 1,4-苯醌化合物的紫 外光谱进行比较,最终发现维生素 K 的吸收带接近 2,3-二烷基-1,4-萘醌
2.3_紫外-可见吸收光谱法

吸收光谱图所测量的是光通过样品后,光强随 频率(或波长)变化的曲线。 吸光和透光的强度的表示方法: (1)透光率T(%)
I T (%) 100 I0
(2)吸光度 A
I0 A lg( ) I
(3)吸光系数ε
A e Cb
(4)对数吸光系数
lg e
(5)吸光率A(%)
A(%) 1 T (%)
本章学习后应掌握的要点
1、物质对光的选择性吸收可以用吸收曲线来描述。 2、光的吸收定律的数学表达式是A=εcb。吸收系数 ε表示物质对某一特定波长光的吸收能力。 3、光的吸收定律有一定的适用范围。光的吸收定律 产生偏差现象的原因主要是单色光不纯和显色溶 液中发生水解、缔合、沉淀等化学反应。
4、紫外吸收光谱和可见吸收光谱同属电子光谱, 都是由于价电子跃迁而产生的。
ÆÆ Æ ×ÆÆ
ÆÆ×ÆÆ ¨Æ
ÆÆÆÆ
100nm
200nm
400nm
800nm
真空紫外区——波长范围在200nm以下的区域。
普通紫外区——波长范围在200nm-400nm之间的区域。 可见光区——波长范围在400nm-800nm之间的区域。 可见光区与普通紫外区基本上没有太大的差别,只是光源不同,普 通紫外区用氢灯,可见光区用钨丝灯。
同样可以用紫外光谱判别顺反异构。 例 肉桂酸有下面两种构型: H C=C COOH H C=C H COOH
H
由于顺式空间位阻大,苯环与侧链双键共平面性 差,不易产生共轭;反式空间位阻小,双键与苯环在 同一平面上容易产生共轭。因此,反式: lmax=295nm emax=13500, 顺式: lmax=280nm ,emax=7000。反式的 波长和强度比顺式的大。
紫外光谱在中药鉴别和含量测定中的应用

231紫外光谱从本质上讲是一种光谱分析法,其理论基础是最外层价的分子电子会在多个能级轨道上发生跃迁现象,具有操作便利、敏感性高和适用范围广等优势。
现阶段,其对于中药定性分析的应用效果较佳,若中药材的外形相似,该技术能够快速鉴别药材真伪;若中药材的产地不同,该技术能够快速鉴别药材产地。
同时,紫外光谱可严格把控中药材质量,可精准测定药材中的成分含量。
此次研究将全面分析紫外光谱对于中药分析的价值,以充分发挥其鉴别与测定优势。
1 概念界定1.1 中药鉴别我国医学发展史上所提及或使用的药材,即为中药,是指基于中医药学理论,发挥医疗保健作用的药品。
我国富有中药资源,其是传统医学的发展根基,可推动医疗事业发展。
由于中药材的种类繁多,来源渠道广,且贵重中药较为稀有,因此在市场上普遍存在假冒伪劣中药,导致中药混淆。
如天麻是头痛眩晕的常用中药,但其形态结构类似于紫茉莉根,因此不法商家直接将紫茉莉根作为天麻出售。
这就需要准确鉴别中药材,以保证药效。
1.2 中药含量测定鉴别中药原料和成分的真实性,可以判断药材真伪。
中药含量准确测定可以判断特定成分的实际含量,再与相关规定进行比较,最终评价药物质量。
其是中药质量的把控环节之一,通常检测毒性和有效成分或是某个指标性成分的具体含量,从而评估制取工艺的合格率和稳定性,提升中药使用的安全性。
1.3 紫外光谱紫外光谱主要用于检测有机化合物等物质的分子结构,使相关人员可掌握物质的分子特征,进而推动有机化学的长远发展。
采用现代仪器和特定的分析方法,可使检测流程简单,结果精准度高。
2 中药鉴别方法2.1 紫外光谱单一法该方法是指将中药材或制剂浸泡在溶剂中,滤处理后,直接获取滤液,使用紫外分光光度计进行扫描,可获得紫外吸收光谱曲线,根据峰位值与谱线峰数量判断中药或制剂的真伪。
有学者在中药质检期间发现茉莉花替代槐花的情况,使用紫外光进行200~400 nm 扫描,发现槐花醇提液于204 nm 和360 nm 等处呈现出特征吸收情况,茉莉花在202 nm 处出现特征吸收情况,证实伪充想法。
浅谈朗伯比尔定律紫外-可见分光光度计分析的运用——以结焦抑制剂硝酸根的测定为例

丙酮
4.73
4.84
9
化合物名称
2-甲基-异丙醇
癸酸乙酯
3-甲基丁酸
丁二酸二乙酯
戊酸
1.27
0.32
1.08
0.42
2.76
0.41
0.81
0.29
0.29
97
序号
24
25
26
27
28
29
保留时间 / min
20.49
21.95
28.78
32.5
33.21
35.64
表 1( 续)
化合物名称
己酸
苯乙醇
气成分的影响研究[ J] .化学试剂,2018,40(8) :784-788.
[8] 吕长鑫,刘苏苏,李萌萌,等.响应面复合酶法澄清南果梨汁
及其饮料技术[ J] .食品与发酵工业,2016,42(5) :159-166.
[9] 卜庆状,纪淑娟,李江阔,等.冷藏后南果梨常温后熟期香气
成分变化[ J] .食品科学,2013,34(2) :273-276.
不仅可以测量被测溶液的可见光谱,也可以测量紫外光谱。
本文主要以结焦抑制剂硝酸根分光光度法的测定为例,来
分析一下朗伯比尔定律的运用。
1 标准溶液的配制和测定
(1) 硝酸钾标准系列的配制:分别吸取 100 mg / L 的硝酸钾
标准使用液 0,1,2,3,4,5,6,10 mL 于 8 个 50 mL 容量瓶中,各
液,加 3 g / L 盐酸溶液 1 mL,定容于 50 mL 容量瓶中。 在波长为
220 nm 处用石英比色皿测定其吸光度。
此方法,硝酸根的测定范围在 0.2 ~ 20 mg / L。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
紫外-可见吸收光谱法UV-Vis SpectrophotometerUV-Vis Spectrophotometer主要内容紫外-可见吸收光谱法的原理紫外-可见吸收光谱法紫外-可见分光光度计构造紫外-可见分光光度计的应用UV-Vis Spectrophotometer基本原理:光的选择性吸收紫外-可见吸收光谱法分子中的某些基团吸收了紫外可见辐射光后,发生了电子能级跃迁,而产生了相应的吸收光谱。
属分子吸收光谱。
分子吸收光谱的分析方法。
紫外-可见吸收光谱分析是研究物质在紫外-可见光波下的紫外-可见区可细分为:(1)10-200nm;远紫外光区(2)200-400nm;近紫外光区(3)400-800nm;可见光区UV-Vis Spectrophotometer光的吸收定律1.朗伯比尔定律:A=kbc。
紫外-可见吸收光谱法表明:一定温度下,一定波长的单色光通过均匀的、非散射的溶液时,溶液的吸光度与溶液的浓度和液层厚度的乘积成正比。
入射光 I0 透射光 ItA=kbc 式中: A:吸光度;描述溶液对光的吸收程度; k:摩尔吸光系数,单位 L mol-1 cm-1; b:液层厚度(光程长度),通常以cm为单位; c:溶液的摩尔浓度,单位 mol L-1;UV-Vis Spectrophotometer紫外-可见吸收光谱法紫外-可见吸收光谱与分子结构(一)电子跃迁类型(1)电子类型形成单键的σ电子形成双键的π电子未成对的孤对电子n电子C-H C-C C=C C=O C=OsHC HOpnUV-Vis Spectrophotometer紫外-可见吸收光谱法π*、n 能量高低σ<π<n<π*<σ*分子轨道有σ、σ*、π、σ* π*n →σ* π→π*n→π*跃迁n π能量σ→σ*其中σ-σ* 跃迁所需能量最大,n-π*及配位场跃迁所需能量最小,因此,它们的吸收带分别落在远紫外和可见光区。
从图中纵坐标可知π-π*及电荷迁移跃迁产生的谱带强度最大,π-π*、nσ*跃迁产生的谱带强度次之,配位跃迁的谱带强度最小。
σUV-Vis Spectrophotometer紫外-可见吸收光谱法1、生色团从广义来说,所谓生色团,是指分子中可以吸收光子而产生电子跃迁的原子基团。
UV-Vis Spectrophotometer紫外-可见吸收光谱法助色团助色团是指带有非键电子对的基团,如一OH、OR、NHR、一SH、一Cl、一Br、一I等,它们本身不能吸收大于200nm的光,但是当它们与生色团相连时,会使生色团的吸收峰向长波方向移动,并且增加其吸收强度。
红移和紫移在有机化合物中,常常因取代基的变更或溶剂的改变,使其吸收带的最大吸收波长入max发生移动。
向长波方向移动称为红移,向短波方向移动称为蓝移(紫移)。
UV-Vis Spectrophotometer共轭体系的存在----红移紫外-可见吸收光谱法如CH2=CH2的π -π *跃迁,λ max=165~200nm;而1,3-丁二烯,λ max=217nm异构现象:使异构物光谱出现差异。
如CH3CHO含水化合物有两种可能的结构:CH3CHO-H2O 及CH3CH(OH)2; 已烷中,λ max=290nm,表明有醛基存在,结构为前者;而在水溶液中,此峰消失,结构为后者。
空间异构效应---红移如CH3I(258nm), CH2I2(289nm), CHI3(349nm)取代基:红移或蓝移。
取代基为含孤对电子,如-NH2、-OH、-Cl,可使分子红移;取代基为斥电子基,如-R,-OCOR,则使分子蓝移。
苯环或烯烃上的H被各种取代基取代,多产生红移。
UV-Vis Spectrophotometer紫外-可见吸收光谱法pH值:红移或蓝移苯酚在酸性或中性水溶液中,有210.5nm及270nm两个吸收带;而在碱性溶液中,则分别红移到235nm和287nm(p- π共轭)。
溶剂效应:红移或蓝移由n-π*跃迁产生的吸收峰,随溶剂极性增加,形成 H 键的能力增加,发生蓝移;由π-π*跃迁产生的吸收峰,随溶剂极性增加,激发态比基态能量有更多的下降,发生红移。
随溶剂极性增加,吸收光谱变得平滑,精细结构消失。
UV-Vis Spectrophotometer紫外-可见吸收光谱法紫外-可见分光光度计的基本构造基本构造主要由光源、单色器、吸收池、检测器和显示器五大部分组成。
光源单色器样品池检测器显示器UV-Vis Spectrophotometer紫外-可见吸收光谱法Food Chemistry 108 (2008) 310315IF:3.66(2011)UV-Vis Spectrophotometer紫外-可见吸收光谱法一般方法:分光光度法:仪器不太精确,由于光谱重叠,无法测定低浓度的咖啡因浓度。
HPLC:设备昂贵,操作复杂。
一般需要专业人员操作。
傅立叶变换红外光谱近红外反射光谱法拉曼光谱法毛细管电泳法一般实验室不具备,不常用。
紫外可见吸收光谱法:简单,快速,便宜。
可操作性很强。
UV-Vis Spectrophotometer实验思路紫外分光光度计紫外-可见吸收光谱法实验方法咖啡因的表征:5.03 ×10-4 g咖啡因溶解23.07cm3去离子水中3.05×10-4 g咖啡因溶解于15.19cm3二氯甲烷中,磁力搅拌机搅拌1h,室温下分别用紫外可见分光光度计测定其紫外吸收光谱。
咖啡样品的准备:研磨并通过一250μm的筛得到均匀的咖啡,精确称取50mg溶解于25ml的去离子水中,用磁力搅拌器搅拌1h,过滤去杂质。
萃取提取咖啡因:取上述咖啡溶液与二氯甲烷用分液漏斗萃取咖啡因(25:25mL,4次),每次的二氯甲烷提取液分别保存。
分别在200-500nm范围测提取液的紫外吸收光谱摩尔吸收系数、跃迁偶极矩咖啡豆中咖啡因含量高斯拟合:除去3.08-3.10nm咖啡单宁酸的干扰峰Food Chemistry 108 (2008)310315UV-Vis Spectrophotometer结果与讨论紫外-可见吸收光谱法由图一可看出:咖啡因在水溶液中的紫外吸收光谱峰出现在243-302nm范围内。
243处的一个峰是由于溶剂造成的。
最高吸收峰出现在λmax=272nm处, A=1.224。
纯咖啡因水溶液的紫外吸收光谱图Food Chemistry 108 (2008) 310315UV-Vis Spectrophotometer紫外-可见吸收光谱法使用BeerLambert’s方程可有光学吸收强度得到摩尔吸收系数εmax=1115m2mol-1。
跃迁偶极矩由摩尔吸收系数通过:S = 2.9352 ×1060 C-2 mol-1. 从ν1=33000cm-1到ν2=41000cm-1 曲线的积分面积:105.92m2mol-1,得到咖啡因水溶液的过渡偶极矩为μfi=10.40 ×10-30Cm Food Chemistry 108 (2008) 310315UV-Vis Spectrophotometer紫外-可见吸收光谱法纯咖啡因二氯甲烷溶液的紫外吸收光谱 243-301nm λmax=274.7nm,A=1.043,εmax=1115m2mol-1ν1=33000cm-1到ν2=41000cm1 IA=114.16m2mol-1,μfi=10.40 ×10-30Cm时间Food Chemistry 108 (2008) 310315UV-Vis Spectrophotometer紫外-可见吸收光谱法二氯乙烷萃取咖啡因效果最好,萃取率达98%-99% Food Chemistry 108 (2008) 310315UV-Vis Spectrophotometer紫外-可见吸收光谱法仪器无法排除一些干扰因素,如在308nm处存在咖啡单宁酸的吸收峰。
所以需要用高斯方程来拟合。
Food Chemistry 108 (2008) 310315UV-Vis Spectrophotometer紫外-可见吸收光谱法经高斯拟合后的咖啡因二氯甲烷溶液的紫外吸收光谱 Food Chemistry 108 (2008) 310315UV-Vis Spectrophotometer紫外-可见吸收光谱法Food Chemistry 108 (2008) 310315UV-Vis Spectrophotometer紫外-可见吸收光谱法Dalton Trans., 2012, 41, 57895793IF:3.838(2011)UV-Vis Spectrophotometer实验思路紫外-可见吸收光谱法G4是一种特殊DNA,一种端粒结构,基本单元是鸟嘌呤碱基的四联体。
端粒相当于为染色体末端提供了一个帽子,防止染色体互相融合。
重组及一些外切酶、连接酶的作用,防止 DNA的损伤。
形成G4后端粒 2+室温下其水溶液本身没有荧光,而 [Ru(bpy)2(dppzi)] 酶的活性收到抑制。
因此,当主配体dppzi 与G4发生作用时,受到了DNA疏水环能稳定G4的药物可能就是有境的保护,延长了激发态的寿命,显示出非常强的荧效的化疗药物。
光实现“开”。
加入[Fe(CN)6]4后,荧光猝灭,实现 Dalton Trans., 2012, 41, 57895793 “关”。
UV-Vis Spectrophotometer紫外-可见吸收光谱法紫外光谱是研究小分子配合物与DNA相互作用的一种最简便、最常用的技术。
许多小分子配合物本身在紫外可见光区有特征吸收峰,当小分子配合物与DNA作用时,通常会出现相应的特征变化,表现为吸收谱带变宽、吸收峰红移(或蓝移)及减色效应。
这种现象的产生往往来源于小分子配合物发色团与DNA碱基电子云的强烈的相互作用。
因此,紫外可见吸收光谱可以用来研究小分子配合物与G-四联体DNA的相互作用,进而根据其产生的相应特征变化推测其作用模式。
产生过渡金属配合物电子光谱的电子跃迁形式可分为(1)金属离子中心到配体的电荷跃迁(MLCT); (2)配体到金属离子中心的电荷跃迁(LMCT): (3)配体到配体之间的电荷跃迁(LLCT); (4)以金属离子为中心的配位场跃迁(d-d跃迁或f-f跃迁);(5)以同一配体为中心的电子跃迁(LC)。
Dalton Trans., 2012, 41, 57895793UV-Vis SpectrophotometerNA+ K+ 缓冲溶液配合物与作用的紫外滴定曲线 G4 缓冲溶液配合物与 G4 作用的紫外滴定曲线紫外-可见吸收光谱法287nm处的吸收峰是由于(bpy) π→π*; 430nm处的吸收峰是由于Ru(dπ) → bpy (π*) 和Ru(dπ) → dppzi (π*)(MLCM);386nm处的吸收峰是由于以同一配体为中心的电子跃迁(LC)。
