2020年CLSI变化中文版
clsi更新中文

Negative (N=19) 3
24
11
74
7
4
-
-
2
1、已明确 2、用厄他培南纸片法 3、AmpC过表达或ESBL+/-膜不通透 4、NDM-1(7/14产NDM-1菌MHT阴性)
MHT:敏感性:77.4%; 特异性 38.9% MHT对KPC和OXA检出能力好;对NDM-1检出能力低。
Girrlich et al. 2012. J Clin Microbiol. 50:477.
降低亚胺培南、美罗培南的折点;增加多尼培南的 折点
葡萄球菌属
增加青霉素纸片抑菌圈边缘法检测β内酰胺酶。
修订折点必须切记!
CLSI和FDA设定的折点都是针对美国的。 CLSI和FDA建立的折点二者有少许不同 商业化药敏系统必须使用FDA折点 临床实验室即可使用CLSI也可使用FDA
折点
Adapted from Queenan & Bush. 2007. Clin Microbiol Rev. 20:440.
MHT对碳青霉烯酶的检出价值
MHT2
Positive Negative Not interpretable Not Done
Carbapenemase1
Positive (N=35)
针对MDR的报告制度
Section I.D. Selective Reporting ……
Ipnroa另tdodc外oitlio,tno,a每edad个crhes实lasbi验soorala室ttoer必sy tsh须haotu建ladr立ede针vel对op a 对co所nf有irm常ed规as药res敏ist测ant试to均all为ag耐en药ts o的n t制he度ir 。 这rino种cultui制ndee度toeps应ttiopn包asnf括eolsr.增teTsh加tiisn实gprao验dtodc室itoiol 内nshalo部augld可ent完s 成in测-ho试us的e o药r s物end种ing类th或e i必sol须ate送to至a r参efe考re实nce 验la室bo的rato菌ry.株。
临床分离多重耐药菌的分布及变化趋势

临床分离多重耐药菌的分布及变化趋势漆坚【摘要】Objective To analyze types distribution and developing trends of multi-drug resistant organism (MDROs) infection from 2013 to 2015,so as to provide reference for preventing and controlling MDRO healthcare-associated infection(HAI). Methods A retrospective review of MDRO records has been conducted throughout the period from January 2013 to December 2015. Organ-isms identified and tested by an automated identification and susceptibility system were analyzed with WHONET5.6. Results A total of 2232 bacteria strains were isolated,896 (40.1%) of which were MDROs. Of all MDROs,ESBL-ECO (30.1%),CRAB(20.0%),MRSCNS(13.2%),ESBL-KPN(10.5%),MDRPA(7.9%),MRSA(4.7%) was isolated respectively,and mainly distributed in intensive care unit,geriatrics Dept,neurosurgery Dept,urology Dept,neurology Dept,respectively. The MDRO strains mainly isolat-ed from:sputum specimens (42.3%),and was followed by the middle of urine (19.6%),blood (19.2%),discharge (10.7%). ESBL-E-CO in 3 years detection rate is relatively stable;ESBL-KPN in 2015 detection rate (37.0%),significantly lower than in 2013(52. 8%),2014(56.7%). MRSCNS in 2015 detection rate (78.0%),significantly lower than in2014(96.6%),2013(83.0%). 2015 MDRPA detection rate (14.1%) less than 2013(26.4%),2014(33.7%). CRAB in 2015 detection rate (68.7%),lower than in 2013(77.4%), 2014(83.7%);2015 MRSA detection rate(37.5%),compared with 2013(31.2%),2014(27.0%) increased;As special resistant strains, CRKPNdetection rate in 3 years remained stable (4.0%,4.5%,4.1%),2015 CRPA detection rate (12.5%) was significantly lower than in 2014 (28.9%),2015 CRECO detection rate (2.5%) than in 2013 (0%),2014 (0.8%). Conclusion Multiple drug-resistant bacteria has gradually become the main pathogenic bacteria in nosocomial infection,CRAB detection rate is higherin our hospital, MRSA,CRECO increase year by year,comprehensive measures should be taken to carry on the positive and effective prevention and control.%目的:了解2013年至2015年多重耐药菌(MDROs)的分布及变化趋势,为临床有效控制多重耐药菌(MDROs)感染提供依据。
CLSI临床质谱新标准解读

CLSI 临床质谱标准C62-A新内容解读CLSI 临床质谱标准C62-A主题内容架构由基础内容部分包括(1)范围、(2)标准预防措施、(3)术语、(4)仪器;方法内容包括(5)预考察事项、(6)方法建立、(7)方法验证;质控内容包括(8)液质检验方法的质量保证与质量控制、(9)后续监督构成。
其中方法和质控内容是与应用过程直接相关的。
下面进行具体介绍。
5.预考察事项(preexamination considerations)5.1目标分析物内容包括5.1.1 外源性物质、5.1.2内源性物质、5.1.3 外源性和内源性物质的相关因素、5.1.4 样本采集。
要充分了解目标分析物的性质,包含(1)目标分析物的临床意义如生理意义、临床价值、常用检测方法等;(2)理化性质如结构式、分子量、沸点、极性大小、酸碱性等;(3)存在形式如游离型、结合型;(4)干扰因素如类似物、同分异构体、其他代谢产物等;(5)预期浓度如常量级、微量级、参考区间浓度、切点浓度、病理浓度等;(6)样本类型如血清、血浆、全血、尿样、唾液、胆汁、组织等;(7)采集和处理方式如静脉血、足底血、指尖血、离心处理或静置、何种采血管等;(8)储存和运输方式如避光、冷藏、冷冻等。
5.2 内标内标可以校正基质效应或者样本萃取、色谱分离、离子化过程中产生的偏差,有利于提高定量分析的准确性和精密度及方法稳定性。
5.3 试剂和耗材的质量5.3.1 试剂盒耗材的质量:由于MS灵敏度高,因此试剂和耗材要求也高。
在使用前应对试剂、耗材进行验证,避免其中杂质对MS的影响。
使用过程中应按照SOP进行保存、操作,避免污染。
按照ISO 17025:2017进行批间次管控。
5.3.2 实验室设备:配置校准品和内标时,实验室应使用A级的容量瓶和移液器。
6.方法建立(assay development)6.1离子转变(ion transition)在建立和优化质谱采集参数的过程中,要先配制标准物质溶液直接导入质谱检测器进行质谱扫描,获取目标化合物的相关信息。
2020年新版ISO体系清单换版情况说明

2020年之后各个ISO体系更新情况:1、ISO:英文International Organization for Standardization ,中文“国际标准化组织”,一个全球性的非政府组织,主要功能是为人们制定国际化标准。
中国是ISO成员。
2、GB/T:国家、标准、推荐三个词语的首字母,有T代表是推荐性的标准,如果没有T即表示为强制执行的标准。
3、OHSAS:英文Occupational Health and Safety Assessment,中文“职业健康及安全管理体系”,2020年后全面取消这个说法,新版都用ISO开头。
4、双标:在ISO国际组织制定出国际标准后,我国会根据国际标准,翻译转化和修改为我国适用的标准,所以目前说到体系都是双标形式,一般要这样说:如GB/T19001-2016/ISO9001:2015,表示中国根据国外发布的ISO9001:2015标准版本,修订为适用于我国的GB/T19 001-2016版本。
5、各体系更新情况:(1)ISO22000体系(即:食品安全管理体系)现参考标准为国外最新发布的版本ISO22000:2018。
(2)ISO9001体系(即:质量管理体系)现最新版为GB/T19001-2016/ISO9001:2015,中文为《质量管理体系-要求》。
解释:首先ISO9000,不是一个标准的代号,是ISO颁布的关于质量管理方面的一系列标准,其中有关质量方面的共3个:a、ISO9001:是设计、开发、生产、安装和服务的质量保证模式;b、ISO9002:是生产、安装和服务的质量保证模式;c、ISO9003:是最终检验和试验的质量保证模式。
(3)ISO14001体系(即:环境管理体系)总体概括是一套环境管理体系,旨在让企业节约能源,增强环保意识,减少环境污染。
现最新版为:GB/T24001-2016/ISO14001:2015,中文:《环境管理体系-要求及使用指南》。
2020年CTPAT及SCAN反恐安全标准新版变化和标准要求培训教材

CONTENTS主要内容
1 CTPAT背景介绍 2 CTPAT最低安全要求的框架结构变化 3 各章节主要变化和要点解析 4 CTPAT 审核服务介绍
最新安全要求(MSC)框架结构变 化
关注区域
Corporate Security
Transportation Security
People and Physical Security
美国海关的真实案 例
在这个伪装的墙面后面是6939磅大麻
真实案例
2019年3月19日, CBP在来自菲律 宾的集装箱中查获的1185磅可卡因 。
用黑色胶带捆绑的现金藏在卡车 车厢后挡板的夹层里
C-TPAT是什麽
C-TPAT(反恐)是美国国土安全部海关边境保护局(即US Customs and Border Protection,简称“CBP”)在9·11事件发生后所倡议成立的自愿性 计划。 C-TPAT全名为“Customs-Trade Partnership Against Terrorism” ,即“海关-商贸反恐怖联盟”。透过C-TPAT(反恐)的安全建议,CBP希望 能与相关业界合作建立供应链安全管理系统,以确保供应链从起点到终点的 运输安全、安全讯息及货况的流通,从而阻止恐怖份子的渗入。
1更.S新ec的uri最ty 低Vis安ion全a要nd求Responsibility (NEW)
2.Risk Assessment (REVISED)
3.Business Partners
4.Cybersecurity (NEW + REVISED)
5.Conveyance and Instruments of International Traffic (ITT) Security
clsi-m100-s20_2010抗菌药物敏感性试验解释标准(中文)

内部交流资料
Vol . 30 No .1 M1 0 0 - S 20
抗微生物药物敏感性试验的执行标准; 第二十版信息增刊 Performance Standards for Antimicrobial Susceptibility Testing; Twentieth Informational Supplement
抗微生物药物敏感性试验执行标准; 第二十版信息增刊
Volume 30 Number 1
Franklin R. Cockerill, III, MD Karen Bush, PhD Michael N. Dudley, PharmD,FIDSA George M. Eliopoulos, MD Dwight J. Hardy, PhD David W. Hecht, MD Janet F. Hindler, MCLS, MT(ASCP) Janet A. Hindler. MCLS, MT(ASCP) Jean B. Patel, PhD, D(ABMM) Mair Powell, MD, FRCP, FRCPath, MHRA Richard B. Thomson, Jr., PhD John D. Turnidge, MD Melvin P. Weinstein, MD Barbara L. Zimmer, PhD Mary Jane Ferraro, PhD, MPH Jana M. Swenson, MMSc
2015-2019年我院肺炎克雷伯菌的感染特征与耐药机制

文章编号:1001-8689(2021)05-0468-06收稿日期:2020-10-29作者简介:黄晓琳,生于1922年,女,在读硕士研究生,主要研究方向临床微生物检验和耐药机制,E-mail:********************通讯作者:E-mail:*****************2015—2019年我院肺炎克雷伯菌的感染特征与耐药机制黄晓琳1 李明2 范晓怡1 刘菊珍1 黄云祖1 李小丽1 邹海珠1*(1 暨南大学附属第一医院临床检验中心 广州 510630; 2 东莞市滨海湾中心医院 东莞 523000)摘要:目的 分析2015—2019年广州暨南大学附属第一医院肺炎克雷伯菌的感染情况和耐药性变迁,并进一步探讨其耐药机制,为临床防治肺炎克雷伯菌感染用药提供实验室依据。
方法 采用回顾性分析方法,对我院2015—2019年分离的1514株肺炎克雷伯菌进行标本来源、科室分布、耐药性变化等分析,并对其中123株耐碳青霉烯类肺炎克雷伯菌(CRKP)采用改良碳青霉烯类失活法(mCIM)和EDTA 碳青霉烯类失活法(eCIM)进行碳青霉烯酶表型筛选试验,并通过PCR 方法检测bla KPC 、bla VIM 、bla IMP 和bla NDM 4种最常见的碳青霉烯酶耐药基因。
结果 2015—2019年期间我院肺炎克雷伯菌每年的平均分离率为9.44%,从临床标本分布来看,主要分离自痰液(47.36%)、尿液(23.51%)和血液(16.51%);从临床科室分布来看,分离率最高的依次是ICU 病区(17.83%)、呼吸病房(17.83%)和神外病房(9.11%)。
肺炎克雷伯菌对碳青霉烯类药物的耐药率相对较低(10%~30%),但在2019年明显上升;对喹诺酮类、头孢类、单环类、四环素类、磺胺类药物耐药率较高(30%~50%);除头孢哌酮/舒巴坦和复方磺胺甲噁唑外,对其他抗菌药物的耐药率均呈上升趋势。
《2020年国际贸易术语解释通则》的新变化及应用解析

《2020年国际贸易术语解释通则》的新变化及应用解析王庆颖(常州开放大学人文与经济学院,江苏常州213001)摘要:贸易术语是进出口商品价格的重要组成部分,不同的贸易术语下买卖双方承担的责任、义务以及风险大相径庭,《国际贸易术语解释通则》是世界上影响力最大的解释贸易术语的国际惯例,最新版本《2020年国际贸易术语解释通则》于2020年1月1日正式实施,将给世界商品进出口贸易带来重大影响。
与2010年版本相比,2020年版本对贸易术语的解释更加清晰,对交易双方承担的费用和责任更加明确具体,增加了安保分配规则,对某些贸易术语的具体内容及实施进行调整。
文章结合中国进出口业务实践,分析《2020年国际贸易术语解释通则》的实施可能对中国外贸带来的影响,并从外贸企业、高等院校的角度分析了应用《2020年国际贸易术语解释通则》时应关注的问题。
关键词:《国际贸易术语解释通则》;贸易术语;国际商会;新变化;应用解析中图分类号:F752文献标识码:A DOI:10.3969/j.issn.1673-8578.2021.01.008New Changes and Application Analysis of Incoterms2020//WANG QingyingAbstract:Incoterms is the most influential international practice in interpreting trade terms in the world.The latest edition of Incoterms2020which was officially implemented on January1,2020,will have a significant impact on world commodity import and export trade.This paper analyzes the new changes of the2020edition on the basis of comparing the2020edition with the2010edition. Combining with China's import and export business practice,we analyze the possible impact of the implementation of Incoterms2020 on China's foreign trade,and discuss general principles which should be concerned from the perspectives of foreign trade enterprises, colleges and universities.Keywords:Incoterms;trade terms;ICC;new changes;application analysis1国际贸易术语解释通则概述国际贸易术语是表示国际贸易交易商品价格的专门用语,因此也称为“国际价格术语”,由于世界各国对国际贸易术语的认知、习惯做法、法律法规差异很大,为了减少运用国际贸易术语时的争议和纠纷,一些国际组织和商业团体先后制定了解释国际贸易术语的国际惯例,其中在当今世界上使用范围最广、影响力最大的解释贸易术语的国际惯例是《国际贸易术语解释通则》(Incoterms),由国际性的民间组织———国际商会于1936年初次制定,该惯例历经1953年、1967年、1976年、1980年、1990年、2000年、2010年、2020年八次修订,并于2010年取得注册商标Incoterms®,1980年以后每十年修订一次。
新指南CLSIEP9–A3在方法学比对及偏移评估中的应用(最全版)

新指南CLSIEP9–A3在方法学比对及偏移评估中的应用(最全版)新指南CLSI EP9–A3在方法学比对及偏移评估中的应用(最全版)XXX(CLSI)一直致力于制定系列评价临床检验方法的文件,其在制定相关标准和指南时采用特有的协商一致过程,包括方案的建立、认可和公开,对有关文件进行广泛、细致、全面的评论,根据使用者的意见进行文件修订,以保证其适应性等[1]。
CLSI在1986年1月首先推出EP9–P(proposed guideline)版本,1993年4月推出EP9–T(tentative guideline)版本,再经过修订,1995年12月推出批准指南EP9–A(approved guideline)版本[2]。
随后,又经过3次修订,即2002年9月的EP9–A2[3]、2010年7月的EP9–A2–IR(n)和2013年8月的最新版本EP9–A3文件[4],即《用患者样本进行方法比对及偏移评估:批准指南––第三版》,EP9–A3为生产厂家和临床实验室提供了最新的方法学比对和偏移评估指南。
笔者将简要介绍其基本结构、主要用途、比对要求、实验方案、统计方法等内容,供同行参考。
一、EP9–A3概述EP9–A3主要有3个方面用途:(1)临床实验室新引进测量方法与参比方法比对;(2)厂家新建立的测量方法与参比方法相关性研究;(3)厂家对新建立的测量方法比对声明标准确认;3种用途的具体要求见表1.EP9–A3也可进行方法内比对,对于已建立或确认的方法,厂家或实验室可利用40个系列浓度标本对该方法不同条件进行比对分析,如同一方法不同样本类型、不同批号试剂等。
表1EP9–A3对厂家和实验室比对研究具体要求三、比对要求1.标本要求:比对时应使用未经过处理的患者标本,分析物浓度应尽可能在测量范围内均匀分布,各标本基本信息如临床诊断或状态(是否溶血、黄疸、脂血、浑浊)均应记录。
如需使用处理过的标本(如添加纯的高浓度物质),应<比对标本总数的20%。
C-IASI-2020版结构耐撞性与维修经济性评价方案-

中国保险汽车安全指数2020版规程耐撞性与维修经济性指数评价方案研究(内部征求意见版)中国保险汽车安全指数体系技术研究工作组2020.03结构耐撞性与维修经济性评价维度二、可维修性三、维修经济性一、结构耐撞性四、碰撞兼容性总体评价方案约束系统否决项对车辆结构主体安全性进行评价,引导重视车辆结构设计、确保事故车维修后整车相关性能不降低对车辆可更换零部件碰撞损坏和可维修性进行评价,引导社会关注配件可维修性,引导汽车产业向低碳环保方向发展通过相同碰撞工况车辆标准维修成本,对车辆维修经济性进行评价,鼓励汽车生产企业持续降低消费者汽车使用成本对道路交通中车与车的碰撞承力结构进行评价,鼓励汽车生产企业汽车设计中着眼自身安全的同时也确保对方安全在低速碰撞中约束系统启动,气囊展开,整体等级直接评为较差结构耐撞性与维修经济性整体评方方案优秀良好一般较差结构耐撞性02816可维修性01510维修经济性021020碰撞兼容性0124整体评价级别≤2≤11≤25其他注: 碰撞中约束系统作用则整体评价直接降为较差示例:A车结构耐撞性为优秀为0个缺陷,可维修性良好为1个缺陷,维修经济性一般为10个缺陷,碰撞兼容性优秀为0个缺陷,则总体为11个缺陷值,碰撞中气囊也未起爆,最终评价结果为良好。
01一、结构耐撞性评价评价内容前纵梁变形评测前纵梁维修评测后纵梁变形评测后纵梁及地板维修评测后围板维修评测后翼子板维修评测结构碰撞工况缺陷值0-60-60-30-20-20-2备注最高6个缺陷值校准2更换4吊装发动机6最高3个缺陷值校准1更换2校准1更换2校准1更换2保险杠碰撞工况缺陷值0-60-60-30-20-20-2备注最高6个缺陷值校准2更换4吊装发动机6最高3个缺陷值校准1更换2校准1更换2校准1更换2优秀良好一般较差缺陷值≤2≤6≤12其他1、测评为优秀车型,结构件不能更换。
若更换,直接降级为良好。
一、结构耐撞性测评方案一、结构耐撞性纵梁变形缺陷值评测纵梁X向变形量正碰缺陷值追尾缺陷值≤3mm003<X≤6mm10.56<X≤9mm219<X≤12mm3 1.512<X≤15mm4215<X≤18mm5 2.518<X631、根据车辆正面碰撞工况中(结构碰撞、保险杠碰撞),底盘结构变形测量结果,当所有测量点(标记位置的底盘结构变形)的最大变形量≤3mm 时,则缺陷值为0;当每存在1 个测量点的变形量>3mm 时,则增加1项缺陷值,缺陷值即为1,依次累计,当单个测量点的变形量每增加3mm,则增加1项缺陷值,本项最高缺陷值为6。
CLSI 折点更新进展(08-30)

沙门菌属和氟喹诺酮类的耐药性
基因型 gyrA (单位点突变) 1 染色体
奈啶酸 常耐药
表型 环丙 MIC (µg/ml)
0.12 - 1.0
gyrA, gyrB (多位点突变) 1 染色体 qnr +/-; aac(6’)-lb-cr 2 质粒 (新的耐药机制) 没有耐药基因
的大肠埃希菌感染的患者治疗是有效的。 有些商业化药敏系统中厄他培南的最低浓度是0.5μg/ml
厄他培南 – 不同MIC下的累积抑菌百分率
(N= 356 产KPC的肠杆菌科菌) 旧 (2011) <0.25/0.5/>1.0 新 (2012) <0.5/1.0/>2.0
Cumulative % Inhibited
89.3
100
S
I
R
80
S
I
R
60
40
20
0
0.3
0.8
2.2
0
<=0.25 0.5
1
2
MIC (mcg/ml)
7.3
4
>=8.0
12
新折点和碳青霉烯酶的的关系
肠杆菌科菌 不同MIC下的碳青霉烯酶检出率 (µg/ml)
抗菌药物 亚胺培南 美罗培南 厄他培南 多利培南
敏感 ≤1
0%* ≤1
1.2% ≤0.25
•两种折点结果示上述两种菌对头孢他啶的耐药率差异具统计学意义 •新折点获得的药敏结果更符合临床实际,更有利于临床合理选用抗生素 ?!
大肠埃希菌的敏感性变化
年份 株数
2005 3938 2006 5403 2007 6445 2008 6659 2009 7801 2010 9084 2011 11076
中文版clsi更新PPT课件

ECVs和临床折点
临床折点建立根据: 抗菌药物的MIC分布 相关细菌 PK/PD 临床疗效
ECVs建立根据: and 仅仅是MIC的分布
临床微生物室如何使用ECVs
Ø万古霉素可用于治疗痤疮丙酸杆菌感染,但目前尚无临 床相关折点。
抗生素 万古霉素
痤疮丙酸杆菌
ECV(ug/ml)
野生型
非野生型
≤2
≥4
Table1A-1C抗菌药物的分组 Table2A-2J 纸片法及MIC法的解释标准 Table3A-3I筛选实验及确证实验的解释 Table4A-5G质量控制 Table6A-8B制备方案 AppendixA-Glossary3补充说明及术语表
变化的概要
M100-S25 第 13-15页.
重大的变化2015(1)
Ø环丙沙星体外虽然“S”,但临床疗效不是很好
Crump et al. 2008. Antimicrob Agents Chemother. 52:1278.
氟喹诺酮类非敏感——怎么办?
—— P49
沙门氏菌属ቤተ መጻሕፍቲ ባይዱ—氟喹诺酮类折点
抗生素
纸片 含量
环丙沙星 5ug
左氧氟沙星 -
氧氟沙星
-
培氟沙星 5ug
阳性菌株,不需要更改碳青霉烯类敏感性试验结果的解释。
目前不推荐作为临床常规使用。
—— P120
(使用M100-S20 (January 2010))解释标准 在实验室实施修订的碳青霉烯类抗生素的MIC标准之前,如 果肠杆菌科亚胺培南,美罗培南的MIC值为2-4ug/ml或厄他 培南MIC值为2ug/ml,则可能产碳青霉烯酶,需做此试验。
最大变化
Ø引入 Carba NP试验 Ø引入流行病学cutoff值(ECVs)的概念
药敏试验CLSI2008中文版[1]
![药敏试验CLSI2008中文版[1]](https://img.taocdn.com/s3/m/eb5464be960590c69ec37678.png)
达成共识的过程 CLSI 自愿达成共识的过程是确定以下内容的标准草案的过程: ·标准草案的认可 ·文件的形成与公开评议 ·针对实验室使用者的评论意见对文件进行修订 ·文件被接受为临床实验室标准或指南 CLSI 的绝大多数文件要经历两个水平的一致评议----“建议性的”与“批准的”,根据需要,文件 也可以在中间水平接受一致评议。 建议性的:作为建议的标准和指南,CLSI 的文件要接受临床试验的第一阶段评议。文件要接受广泛 的、彻底的技术评估,包括对范围、方法、实用性的整体评估和对技术内容、评论内容的详细评估。 批准的:已批准的标准或指南在医疗保健界已获得共识。进行评议的目的是确定最终文件的实用性, 保证已达成的共识(即充分考虑对早期版本的评论意见),并且确定是否需要其他达成共识的文件。 CLSI 的标准和指南代表了优秀实验室实践的一致意见,也反映了在使用既定的 CLSI 步骤时,那些 深受其影响的、有法定资格且对此感兴趣的参与者之间取得了广泛一致。CLSI 的标准和指南的规定 可能比实用规则更严格或更宽松。因此,遵循这些自愿标准或指南的使用者仍然有义务遵循实用规 则。
2021年CLSI三代头孢菌素折点改变及其临床意义

敏感 ≤1 ≤1 ≤1 ≤1 ≤4 ≤4
M100-S20 中介 2 2 2 2 8 8
对肠杆菌科细菌的头孢菌素MIC的折点降低了 Fresno 11/00zhu_
耐药 ≥4 ≥4 ≥4 ≥4 ≥16 ≥16
肠杆菌科修订…折点( MIC µg/ml )
抗生素
头孢唑啉 头孢噻肟 头孢唑肟 头孢曲松 头孢他啶 氨曲南
mecA阴性的MRSA该怎么办呢?
– 按上述MRS菌种的结果报告原则
Fresno 11/00zhu_
葡萄球菌属 增加… -利奈唑胺 “R” 折点
MIC (µg/ml)
抑菌环直径 (mm)
CLSI M100-S19 (2009) 敏感 中介 耐药
≤4
-
-
≥21
-
-
CLSI M100-S20 (2010) 敏感 中介 耐药
Fresno 11/00zhu_
现在我们对检测ESBLs理解
ESBL表型试验不是最佳的 – 在确证试验中,多重耐药机制的存在可能会掩饰ESBL • ESBL + AmpC • ESBL + 孔蛋白突变 – 除大肠杆菌,克雷伯菌和奇异变形杆菌外,肠杆菌科 其它细菌中也存在ESBLs ,这使确证实验更加不可靠 – 在有些实验室不能实施
2021年CLSI三代头孢菌 素折点改变及其临床意
义
2020/9/13
CLSI的简单介绍
CLSI :The Clinical and Laboratory Standards Institute ,简称CLSI,其前身是NCCLS
CLSI是一个国际性的、跨学科的、非盈利性的、致力 于发展操作标准的教育组织
The following dosage comments were added:
CLSI临床微生物实验室标准解读

CLSI临床微生物实验室标准解读CLSI折点变更的官方说明Janet Hindler, MCLS MT(ASCP) UCLA Medical Center Los Angeles, California CLSI M100-S20编者本文由Hindler教授提供,并允许梅里埃公司翻译及印发Janet Hindler教授现任美国加利福尼亚州洛杉矶医学中心(UCLA)资深专家,华盛顿D.C.公共健康实验室协会顾问等职。
自1994年开始在CLSI细菌抗生素药敏试验委员会的工作,参加制定每年细菌药敏标准,现任CLSI“不常见细菌和苛养菌药敏指南“学组主席,CLSI“累积抗生素药敏试验数据指南(M39-A3)”学组主席等多个CLSI分委会任职。
术语/流程A. 似乎CLSI和其他一些机构在使用术语“折点”和“判读标准”时候可交替使用。
在这两个词之间有区别吗?无区别,折点和判读标准所指的都是同一个数值。
B. 在哪里我可以找到关于CLSI如何建立药敏折点的标准?在CLSI M100-S20的第17页有关于药敏折点建立的简要说明。
关于药敏折点建立的详细指南参见CLSI 文件M23- 体外敏感性试验标准和质控参数的发展C-15682C-1562C. CLSI修订药敏折点的流程和程序是什么?简而言之,修订药敏折点包括系统性的回顾来自微生物学,药物学和临床的数据。
知名专家,赞助商(来自制药工业)和管理者参与药敏制定流程包括在每年2次的CLSI 药敏试验小组委员会会议的公开讨论。
在制定新上市药物的初始药敏折点时候,需要有对照临床试验数据。
尽管在修订药敏折点时最好能够提供对照临床试验数据,这些数据在应对快速变化的细菌耐药机制和“老药”时多数情况下是不可行的。
因此,委员会必须要依赖发表的文献,专家意见和共同商议的流程。
在药敏折点修订时必须要考虑到流行病,临床治疗和监管意见。
CLSI 分委会的会议纪要在下面的链接可以获取。
/Content/NavigationMenu/Committees/Microbiology/AS T/AST.htm在美国FDA和CLSI都建立自己的药敏折点,某些时候这两个机构所设立的药敏折点会有不同。
2020 年版 clsi 药敏结果判定标准

2020 年版 CLSI 药敏结果判定标准随着医学技术的不断进步,药敏测试在临床诊断和治疗中扮演着越来越重要的角色。
CLSI(Clinical and Laboratory Standards Institute)是一个致力于推动医疗实验室标准化的国际组织,他们发布的药敏结果判定标准对于准确判断微生物对抗生素的敏感性至关重要。
今年发布的 2020 年版 CLSI 药敏结果判定标准给我们带来了哪些新的认识和看法呢?本文将从浅入深,全面评估并撰写这一主题。
1. 药敏结果判定标准的基础概念在深入讨论 2020 年版 CLSI 药敏结果判定标准之前,我们有必要对药敏测试的基础概念进行一定的介绍。
药敏测试是指通过实验室测试,确定细菌或真菌对抗生素等药物的敏感性。
而药敏结果判定标准则是根据测试结果来判断微生物对药物的反应。
在这个过程中,很多因素都需要考虑,包括抗生素的类型、浓度、微生物的种类等等。
2. 2020 年版 CLSI 药敏结果判定标准的重大变化2020 年版 CLSI 药敏结果判定标准相较于之前的版本有哪些重大变化呢?可以看到这一版标准对一些传统认知进行了修正和更新。
例如对某些药物的最小抑菌浓度(MIC)判定标准进行了修改,对某些细菌的抗药性评价标准进行了重新界定。
这些变化是基于对临床数据和相关研究的深入分析和总结,为临床治疗提供了更准确的药敏结果判定。
3. 基于 2020 年版 CLSI 药敏结果判定标准的临床应用对于临床医生来说,掌握最新版的药敏结果判定标准以及了解其实际应用非常重要。
通过临床案例的共享和病例分析,我们可以清晰地看到 2020 年版 CLSI 药敏结果判定标准对于临床诊断和治疗的实际影响。
在某些疑难病例中,新版标准的应用能够帮助医生更准确地选择合适的抗生素,有效地控制感染的进展。
4. 个人观点和理解作为一名文章写手,我对 2020 年版 CLSI 药敏结果判定标准持有积极的态度。
EP17-A2 (中)检出限和定量限的建立与验证

版权©2012 临床和实验室标准研究所。除了下面所述,这两者都不是出版物及其任何部分均 不得以任何方式改编,复制或以其他方式复制(电子,机械,影印,录制或其他),未经事 先书面许可临床和实验室标准研究所(“CLSI”)。
CLSI 特此授权每个会员或购买者单独复制本出版物可用于其实验室程序手册中的单一地点。 要求使用权限本出版物以任何其他方式联系执行副总裁,临床和实验室标准研究所,950 西 谷路,2500 室,韦恩,宾夕法尼亚 19087 年,美国。 建议引用 CLSI。临床实验室测量程序的检测能力评估;批准指南 - 第二版。 CLSI 文件 EP17-A2。韦 恩,PA:临床和实验室标准 研究所; 2012。 建议指南 2004 年 3 月 批准指南 2004 年 10 月 批准指南 - 第二版 2012 年 6 月 ISBN 1-56238-795-2(打印) ISBN 1-56238-796-0(电子版) ISSN 1558-6502(平面) ISSN 2162-2914(电子)
摘要 临床和实验室标准研究所文件 EP17-A2-临床实验室检测能力评估测量程序;批准准则 - 第 二版提供评估检测能力的指导临床实验室测量程序(即空白限度,检测和定量)检测能力要 求,以及正确使用和解释不同的检测能力估计。打算使用 EP17 供体外诊断测试,监管机构 和临床实验室的制造商使用。
临床和实验室标准研究所(CLSI)。临床实验室测量的检测能力评估 程 序 ; 批 准 指 南 - 第 二 版 。 CLSI 文 件 EP17-A2 ( ISBN 1-56238-795-2 [ 打 印 ]; ISBN 1-56238-796-0 [电子])。临床和实验室标准研究所,950 West Valley Road,Suite 2500,Wayne, 19087 年美国,2012 年。 临床和实验室标准协会共识流程,这是通过文件移动的机制 医疗保健社区进行两级或更多级别的审查是一个持续的过程。用户应该期望任何修订版本 给定的文件。因为技术的快速变化可能会影响标准或程序中的程序,方法和协议 指南中,用户应该用当前版本的 CLSI 文档替换过时的版本。当前版本已列入 CLSI 目录并在我们的网站 上发布。如果你的组织不是会员,并希望成为 请联系我们:电话:610.688.0100;传真:610.688.0700;电子邮件: customerservice@;网站:
NCL(11-2020)版中文版和区分表修改内容-2020 国家商标局
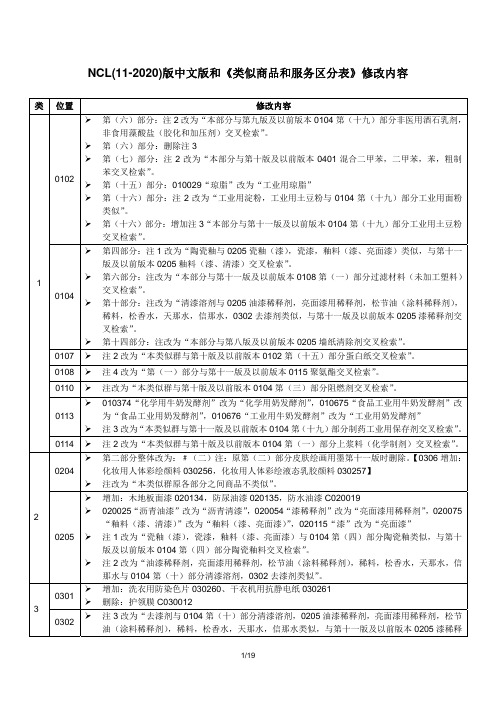
NCL(11-2020)版中文版和《类似商品和服务区分表》修改内容类位置修改内容1 0102第(六)部分:注2改为“本部分与第九版及以前版本0104第(十九)部分非医用酒石乳剂,非食用藻酸盐(胶化和加压剂)交叉检索”。
第(六)部分:删除注3第(七)部分:注2改为“本部分与第十版及以前版本0401混合二甲苯,二甲苯,苯,粗制苯交叉检索”。
第(十五)部分:010029“琼脂”改为“工业用琼脂”第(十六)部分:注2改为“工业用淀粉,工业用土豆粉与0104第(十九)部分工业用面粉类似”。
第(十六)部分:增加注3“本部分与第十一版及以前版本0104第(十九)部分工业用土豆粉交叉检索”。
0104第四部分:注1改为“陶瓷釉与0205瓷釉(漆),瓷漆,釉料(漆、亮面漆)类似,与第十一版及以前版本0205釉料(漆、清漆)交叉检索”。
第六部分:注改为“本部分与第十一版及以前版本0108第(一)部分过滤材料(未加工塑料)交叉检索”。
第十部分:注改为“清漆溶剂与0205油漆稀释剂,亮面漆用稀释剂,松节油(涂料稀释剂),稀料,松香水,天那水,信那水,0302去漆剂类似,与第十一版及以前版本0205漆稀释剂交叉检索”。
第十四部分:注改为“本部分与第八版及以前版本0205墙纸清除剂交叉检索”。
0107 注2改为“本类似群与第十版及以前版本0102第(十五)部分蛋白纸交叉检索”。
0108 注4改为“第(一)部分与第十一版及以前版本0115聚氨酯交叉检索”。
0110 注改为“本类似群与第十版及以前版本0104第(三)部分阻燃剂交叉检索”。
0113010374“化学用牛奶发酵剂”改为“化学用奶发酵剂”,010675“食品工业用牛奶发酵剂”改为“食品工业用奶发酵剂”,010676“工业用牛奶发酵剂”改为“工业用奶发酵剂”注3改为“本类似群与第十一版及以前版本0104第(十九)部分制药工业用保存剂交叉检索”。
0114 注2改为“本类似群与第十版及以前版本0104第(一)部分上浆料(化学制剂)交叉检索”。
