有机化学_第7章_自由基反应汇总
了解有机化学中的自由基聚合反应反应机制和应用

了解有机化学中的自由基聚合反应反应机制和应用自由基聚合反应是有机化学中非常重要的一种反应类型,它在合成高分子材料、制备聚合物以及药物研发等领域都具有广泛的应用。
本文将深入探讨自由基聚合反应的机理和应用。
一、自由基聚合反应的机制自由基聚合反应是一种通过自由基的自由基反应形成聚合物链的过程。
该反应包括三个关键步骤:起始、传递和终止。
1. 起始自由基聚合反应的起始是通过引入一种起始剂,使之发生自由基解离,生成两个自由基。
常用的起始剂有过氧化物、硝酸酯和过氧硫酸铵等。
起始剂的解离会产生两个自由基,从而引发聚合链的生成。
2. 传递传递是自由基聚合反应的核心步骤,主要是自由基与单体分子之间的反应。
在传递过程中,自由基会与单体发生加成反应,生成一个新的自由基和一个共价键。
新生成的自由基会继续参与到传递反应中,进一步延长聚合链。
3. 终止自由基聚合反应的终止过程会导致聚合链的停止,从而形成聚合物。
终止反应可以分为两种类型:链传递终止和自由基自身的消失。
链传递终止是指两个自由基之间的反应,例如两个聚合链相遇并发生反应。
自由基自身的消失则是指自由基与其他物质发生反应或自由基的自发消失。
二、自由基聚合反应的应用自由基聚合反应的机理和特点使其在许多领域中得到广泛应用。
1. 聚合物合成自由基聚合反应是合成聚合物的主要方法之一。
通过选择不同的单体和起始剂,可以合成出具有不同结构和性能的聚合物。
聚合物的种类包括聚乙烯、聚苯乙烯、聚丙烯等广泛应用的工程塑料。
2. 化学药品合成自由基聚合反应在药物合成过程中也起到重要作用。
许多药物合成的关键步骤利用了自由基聚合反应的特点,通过选择不同的单体和反应条件,实现对目标化合物的构建。
3. 材料科学自由基聚合反应在材料科学领域有丰富的应用。
通过控制反应条件和单体的选择,可以制备出具有特定结构和性能的高分子材料,如塑料、橡胶和纤维。
4. 生物医学工程自由基聚合反应在生物医学工程领域中也得到广泛应用。
有机化学基础知识点整理有机分子的自由基反应与机制

有机化学基础知识点整理有机分子的自由基反应与机制有机化学基础知识点整理—有机分子的自由基反应与机制自由基反应是有机化学中一类重要的反应类型,它涉及到自由基的产生、转化以及参与反应。
自由基反应对于有机合成、药物合成等领域具有重要的意义。
本文将整理和探讨一些有机分子的自由基反应与机制的基础知识点。
一、自由基的生成自由基是指电子个数不满足八个原子或离子,具有自由不稳定电子的中间体。
有机分子中的自由基通常是通过化学反应或者一些物理条件来生成的。
1. 光照作用在光照作用下,许多有机分子可以发生光解反应,生成自由基。
例如,溴化物可以在紫外光照射下发生光解反应,产生溴自由基。
2. 热解反应一些有机化合物在高温下也能发生热解反应,产生自由基。
例如,过氧化氢在高温下分解为氧气和氢自由基。
3. 氧化反应有些有机分子在氧化反应中会产生自由基。
例如,过氧化苯甲酸通过氧化过程生成苯甲酸自由基。
二、自由基的反应类型自由基反应可以分为三个主要类型:取代反应、消除反应和加成反应。
1. 取代反应取代反应是指一个原子或者一个基团替换掉有机分子中的一个原子或者一个基团的反应。
常见的取代反应包括氢原子的取代、卤原子的取代等。
2. 消除反应消除反应是指在有机分子中两个相邻的原子或者两个相邻的基团发生脱离的反应。
通常会生成一个双键和一个小分子(如水、氨等)。
3. 加成反应加成反应是指两个分子中的原子或者基团结合成为一个分子的反应。
例如,烯烃与自由基结合形成新的化合物。
三、自由基反应的机制自由基反应的机制可以分为三个步骤:自由基的生成、反应过程和产物生成。
1. 自由基的生成自由基的生成通常通过断裂化学键或者电子转移来实现。
在断裂化学键的反应中,一个化学键被打断,生成两个自由基;而在电子转移的反应中,一个原子或者一个基团上的一个电子被转移到另一个原子或者另一个基团上。
2. 反应过程自由基反应的反应过程一般包括自由基的引发、传递和终止三个阶段。
自由基反应机理

自由基反应机理引言自由基反应是有机化学中一种重要的反应类型,自由基可以通过化学键的断裂来生成,并且具有高度的活性。
自由基反应机理复杂多样,涉及多种反应类型和步骤。
本文将对自由基反应机理进行全面深入的探讨。
自由基的生成自由基是有一个未成对电子的化学物质,具有独立的存在能力。
自由基可以通过多种途径生成,包括光解反应、热解反应、电离反应等。
其中,光解反应是最常见的一种方法。
在光解反应中,有机物分子受到光的激发,键断裂形成自由基。
自由基反应的特点自由基反应具有以下特点:1.高反应活性:自由基具有未成对电子,具有较高的反应活性,可以与其他分子迅速发生反应。
2.反应选择性:自由基反应在分子的特定位置发生,可以选择性地引发特定的反应。
3.自由基链反应:自由基反应通常是自由基链反应,包括起始步骤、传递步骤和终止步骤三个阶段。
4.反应速度受控:自由基反应的速率受到反应物的浓度、温度和反应物排列的影响。
自由基反应的机理自由基反应的机理可以分为以下几个步骤:1.起始步骤:自由基反应的起始步骤通常涉及光解反应或热解反应,生成自由基。
例如,在溴乙烷中,可以通过热解反应生成溴自由基。
2.传递步骤:自由基与其他分子发生反应,将自由基的反应活性传递给其他分子。
这个步骤会反复进行,形成自由基链反应。
例如,溴自由基可以与甲烷反应生成甲基自由基和溴化氢。
3.终止步骤:自由基反应的终止步骤是指自由基链反应中的自由基被消耗完的过程。
通常是两个自由基相遇并结合形成稳定的产物。
自由基反应的应用自由基反应在有机化学合成中有广泛的应用。
以下是几个典型的例子:1.自由基取代反应:通过引入自由基取代剂,可以使有机物中的氢原子被取代为其他基团,从而实现有机合成的目的。
2.氧化反应:自由基反应可以用于氧化反应,例如将醇氧化为酮或醛的反应。
3.重排反应:自由基重排反应是一种重要的有机反应类型,可以产生不同的结构异构体。
4.光化学反应:自由基反应在光化学反应中起着重要的作用,例如光合作用中的光解反应。
有机合成中常见的自由基反应
有机合成中常见的自由基反应
旧文重发,温故知新
具有未成对电子的原子或分子被称为自由基,大多数自由基是活泼的反应中间体,不能稳定存在,但也存在着某些稳定的自由基,如O2分子。
自由基反应机理包括三步:引发、传递和终止。
自由基反应的速率取决于自由基浓度,而自由基浓度主要取决于引发剂的浓度,在动力学上为一级半反应。
大多数有机化合物在高温下可以均裂产生自由基,自由基产生难易取决于其离解能,而离解能的大小与分子结构有关:
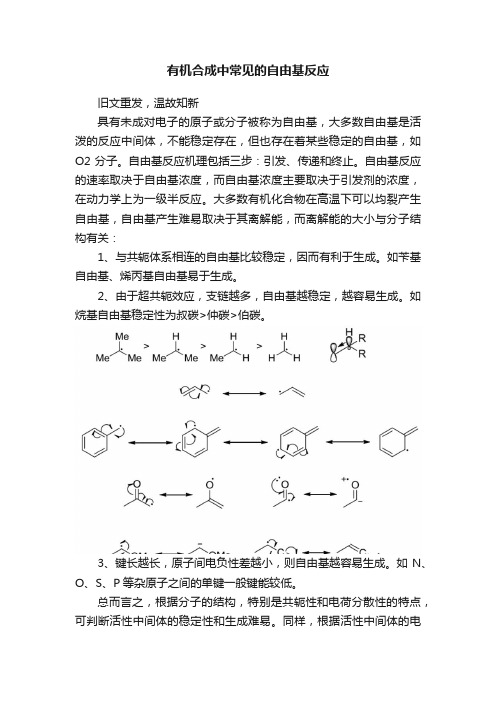
1、与共轭体系相连的自由基比较稳定,因而有利于生成。
如苄基自由基、烯丙基自由基易于生成。
2、由于超共轭效应,支链越多,自由基越稳定,越容易生成。
如烷基自由基稳定性为叔碳>仲碳>伯碳。
3、键长越长,原子间电负性差越小,则自由基越容易生成。
如N、O、S、P等杂原子之间的单键一般键能较低。
总而言之,根据分子的结构,特别是共轭性和电荷分散性的特点,可判断活性中间体的稳定性和生成难易。
同样,根据活性中间体的电
荷分布状态可判断其不同机理的化学反应活性。
第七章自由基与光化学反应总结

共价键异裂时,一对电子保留给其中的一个原子 分别形成一个正离子和一个负离子,这种断裂方 式称为异裂(Heterolytic Cleavage)。
自由基的发现: 实验一、
自由基的产生举例:
1、热均裂反应(热解)
热诱导共价键发生均裂 1)二烷基过氧化物
CH3
H3C C CH3 O O CH3 C CH3 CH3 CH3 2 H3C
S0,放热,系内转化(IC),或发出荧光; T1,系间窜跃(ISC); S0,或发生化学反应,或在反应前发出磷光。
T1相对较稳定,多数光化学反应通过三线态进行。
能量的转移
激发态分子能量失活可以在分子内,也可以在分子间。
hv D (S0)
D (T1)
D (T1) + A (S0)
D (S0)
+ A (T1)
对于给定的烯,多卤代烷活性次序:
CBr4 > CBrCl3 > CCl4>CH2Cl2>CH3Cl
3)醛醇等对烯烃的加成
醛羰基上的氢在自由基进攻下被夺去形成酰基自由基, 与烯烃加成生成酮。
醇的α -H易被自由基夺取形成RCHOH自由基,反应得 到链增长的的醇。
3、分子内自由基反应
1)分子内取代
0
ψ1S1ψ2
(S0
S1)
电子状态多重性M=2[(+1/2)+(-1/2)]+1=1
三线态激发态:ψ1ψ2 对乙烯,ψ1 对苯,ψ3
(1) S1 (2) S1 (3) T1
ψ1ψ2 (S1
T1)
电子状态多重性M=2[(+1/2)+(+1/2)]+1=3
ψ2 ,吸收200nm光,π π* ψ4 ,吸收250-280nm光,π π*
有机化学中的自由基反应反应机制和应用

有机化学中的自由基反应反应机制和应用自由基反应是有机化学中一类重要而特殊的反应类型。
自由基反应的反应机制与传统的架构力学反应机制不同,其具有独特的特点和应用价值。
本文将就有机化学中的自由基反应的基本概念、反应机制以及应用进行探讨。
一、自由基的概念在有机化学中,自由基是指具有不成对电子的分子或离子。
自由基由于电子不成对的存在,其具有较高的化学活性。
自由基的形成有多种途径,比如热解、辐射和化学反应等。
二、自由基反应的基本特点自由基反应具有以下几个基本特点:1. 引发链反应:自由基反应往往会引发连锁反应,其中自由基的生成与消耗是连续进行的。
这种链反应能够加速反应速率,使得反应能在较低的温度和压力条件下进行。
2. 对副反应选择性低:自由基对反应物的选择性较低,容易与不同的反应物发生反应。
这种选择性低的特点使得自由基反应具有较高的官能团多样性,为有机合成提供了更多的可能性。
3. 环境影响:自由基反应对环境的影响较大,容易出现副反应及生成有毒废物。
因此,在实际应用中,需要注意对自由基反应的控制和选择合适的条件。
三、自由基反应的反应机制自由基反应的反应机制可以分为以下几个步骤:1. 自由基的生成:一般情况下,自由基的生成是通过光解、热解或者化学反应等途径实现的。
这些过程会打断键合,使得电子成为自由态,形成具有不成对电子的自由基。
2. 传递和扩散:自由基会通过传递和扩散的方式影响周围的分子,从而引发连锁反应。
传递和扩散是自由基反应中的关键步骤,直接影响着反应速率和产物生成情况。
3. 反应的链终止:自由基链反应在一定的条件下会终止,这可能是由于两个自由基的结合或者由于其他反应的竞争导致。
终止步骤的选择性影响着反应的效果和产物的选择。
四、自由基反应的应用自由基反应在有机合成领域具有广泛的应用价值,主要体现在以下几个方面:1. 引发反应的起始剂:自由基可以作为引发剂来引发一系列的有机反应,如聚合反应、氧化反应和取代反应等。
高等有机化学 第7章_分子重排反应

CH2 N(CH3)2 H CH2
CH3 CH2N(CH3)2
CH2 S CH3 CH3
+
NaOH H2O
CH2 S+CH3 CH2
CH2 H CH2 SCH3
CH2 CH2 SCH3
(4)魏悌息(Wittig)重排
PhCH2 O
CH3
PhLi PhCH CH 3 + H O
H+ O PhCH CH3 OH
C2H5 ONH3
CH3
-卤代酮在碱 作用下加热的 重排反应
=O
C NH2
=O
C
重排机理
=O
C2H5O(CH3)2C Br
从哪一侧打开环,取决于开环 后所生成的负碳离子的稳定性
=O
CH3 C CH2
-
(CH3 )2C Br
C
CH3 CH3
=O
RO-
SN2 O- RO CH3 CH3 CH3 CH3 CH3 C CH3 C CH2CH3
CH3 C6H5
酮肟
C N
OH
反式迁移
H+ CH3 C C6H5 N O+H2 -H2O C6H5 CH3 C NH C6H5 CH3 C N +
CH3 C + N
C6H5
CH3 H2O C OH N
C6H5
◆ 重排范围:酮肟 ◆ 催化剂:浓硫酸、五氯化磷(脱去水,形成正N中心) ◆ 重排立体化学:和羟基处于反式的基团进行迁移 ◆合成上应用:合成取代酰胺。例合成已内酰胺(尼龙-66 中间体)。
3. 频哪醇重排
CH3 CH3 CH3 C OH CH-CH3 OH
H +
有机化学_第7章_自由基反应

2015-6-1
9
2015-6-1
10
CH2 > CH2
苯甲基自由基
CHCH2 > (CH3)3C > (CH3)2CH
三级丁基自由基 异丙基自由基
烯丙基自由基
> CH3CH2 > CH3
乙基自由基
2015-6-1
>
苯基自由基
11
甲基自由基
Question: List in order of decreasing stability all of radicals that can be obtained by abstraction of a hydrogen atom from 2-methylbutane.
2015-6-1
29
Chain Initiation
R O O R 2R O
△
2R O R OH Br
CH3CHCH2 Br CH3CHCH2 ① ②
HBr
Br Chain Propagation:
CH2=CH CH3
Br CH3CHCH2 Br HBr CH3CH2CH2Br Br
Chain Termination:
2015-6-1
20
5.4.2 甲烷的卤化
X
+ CH3-H 439.3
CH3 + H-X H /(kJmol-1) 568.2 -128.9
Ea/(kJmol-1)
F
+4.2
Cl
Br I
431.8
366.1 298.3
+7.5
+73.2 +141
+16.7
+75.3 > +141
有机化学第7章课后习题答案

第7章习题答案章习题答案(1)(3)(5)(7)(9)(11)OH CH 3CH 2CH 2CH 2CH 3CH 2CH 2CH 2CH 3CH 2CH 2CH 2CH 3CH 2CH 2CH 2Mg BrI O C 2H 5CH 3CH 2C H CH 2D NHCH 3CN CH 3CH 3CH 2CH 2CH 2CCCH 3(2)(4)(6)(8)(10)(12)CH 3CH 2CH 2CH 2CH 3CH 2CH 2CH 2CH 3CH 2CH 2CH 2CH 3CH 2CH 2CH 2+ AgBrCH 3(CH 2)3ONO 2+ AgBrCH 3(CH 2)3OOCCH 31.2. 两组化合物的排列顺序为:两组化合物的排列顺序为:(a )按亲核取代反应的难易次序排列:(1)C >B >A (2)B >C >A (b )按与AgNO 3(醇溶液中)反应的活性顺序排列:(1)C >B >A (2)B >C >A (c )按亲电加成难易次序排列(1)B >C > A, 亲电取代的难易次序排列:(2)C >B > A 3. (1) CH 3Br 和C 2H 5Br 是伯卤代烷,进行碱性水解按S N 2机理进行。
增加水的含量,可使溶剂的极性增大,不利于S N 2;(CH 3)3CCl 是叔卤代烷,水解按S N 1机理进行。
增加水的含量,使溶剂的极性增大,有利于S N 1。
(2)(CH 3)3CCH 2X 在进行S N 1反应时,C-X 键断裂得到不稳定的1º1ºC C +,所以S N 1反应速度很慢;(CH 3)3CCH 2X 在进行S N 2反应时,α-C 上有空间障碍特别大的叔丁基,不利于亲核试剂从背面进攻α-C ,所以S N 2速度也很慢。
度也很慢。
(3) 在浓的乙醇钠的乙醇溶液中,反应均按S N 2机理进行,无C +,无重排;,无重排; 在乙醇溶液中加热,反应是按照S N 1机理进行的,有C +,有重排:,有重排:CH 3CHCH=CH 2ClCH 3CHCH=CH 2CH 3CH=CHCH 2- Cl -(4) 亲核性:(B )>)>(C) > (A) 原因:三种亲核试剂的中心原子均是氧,故其亲核性顺序与碱性一致。
自由基反应

O C6H5 + O NBr
CCl4
O NC6H5 + Br O
光引发
O NBr CCl 4
O N O
HBr + C6H5CH2 CH2 CHCH2
+ Br
链传递
Br +
O
C6H5CH3 CH2 CHCH3
O HBr + O NBr Br2 +
O NH O
Br2 +
C6H5CH2 CH2 CHCH2
Br +
C6H5CH2Br CH2 CHCH2Br
例
O O
CH3CH2CH2CH
C6H5COOCC6H5 CH2 NBS/CCl4
CH3CH2CHCH CH2 + CH3CH2CH CHCH2Br
HBr Br
Br
Br Br2
δ⋅ δ⋅
CH3CH2CHCH CH2
CH3CH2CH CH CH2
二、芳环上的自由基取代反应 例1: Sandmeyer反应 反应
Br HBr
C2H5
CH3 *C CH2 Br Br
CH3 * C C2H5
Br CH2
Br
Br2 Br
DBr
同位素标记 C2H5 构型保持产物
CH3 *C CH2 Br D
4.反应举例 4.反应举例 (1)烷烃卤化 反应试剂:X2,CCl4,NBS, (1)烷烃卤化 反应试剂: , BrOOC(CH3)3,RNHX, R2NX, SO2Cl2, , , Cl3CSO2Cl等。除X2外,其它试剂需用引发剂或 等 紫外光照。试剂不同,反应机理不完全相同。 紫外光照。试剂不同,反应机理不完全相同。 例如: 例如: 链引发 链传递
高等有机化学课件自由基反应

目 录
• 自由基反应概述 • 自由基的生成与性质 • 自由基反应机理 • 自由基反应的应用 • 自由基反应的挑战与展望
01
自由基反应概述
定义与特性
定义
自由基反应是指涉及自由基参与的反 应过程,自由基是一种具有未配对电 子的原子或分子片段。
特性
自由基具有高度的反应活性,通常倾 向于与其他分子或自由基发生反应, 从而导致分子结构的改变。
进行。
链终止是自由基反应的结束步骤,通过自由基 活性种的消除或结合,使反应停止进行。
自由基的结合是两个自由基活性种相互结合,形 成稳定的分子结构,从而使自由基消失。
04
自由基反应的应用
在合成中的应用
01
自由基反应在有机合成中具有重要作用,可以用于 合成多种有机化合物,如烯烃、醇、羧酸等。
02
自由基反应可以通过选择适当的反应条件和催化剂 ,实现选择性合成,提高合成效率。
THANK YOU
提高自由基反应效率的方法包括:使 用高活性的自由基源、优化反应条件 、以及使用催化剂。
新技术的应用与展望
随着科技的发展,新的工具和技术不 断涌现,为解决自由基反应的选择性 和效率问题提供了新的可能性。例如 ,使用计算机辅助的分子设计可以预 测和优化反应条件和底物结构。
VS
展望未来,随着计算化学和人工智能 的发展,自由基反应有望在更短的时 间内实现更高的选择性和效率。同时 ,随着绿色化学的发展,自由基反应 也将在实现可持续化学合成方面发挥 重要作用。
在链增长过程中,自由基可以与不同的反应物分子发生加成、取代等反应 ,形成更复杂的分子结构。
链增长过程中,自由基的活性很高,容易发生连锁反应,导致反应迅速进 行。
有机化学基础知识点整理自由基反应和自由基取代反应

有机化学基础知识点整理自由基反应和自由基取代反应有机化学基础知识点整理自由基反应和自由基取代反应在有机化学领域中,自由基反应和自由基取代反应是两个重要且广泛应用的知识点。
了解这些反应类型的基本原理和机理,对于理解有机化学的本质和应用具有重要意义。
本文将对自由基反应和自由基取代反应进行整理和阐述。
一、自由基反应自由基反应是指通过自由基中间体参与的化学反应。
自由基是具有不成对电子的中性分子或离子,通常由光解或热解引发。
自由基反应常见的几种类型包括自由基链反应、自由基偶联反应和自由基置换反应等。
1.自由基链反应自由基链反应是由一个自由基引发,然后通过一系列连锁反应形成产物的反应。
其中最重要的链反应类型包括自由基聚合反应和自由基引发的自由基聚合反应。
自由基聚合反应是一类通过自由基引发、自由基传递和自由基链终止来形成高分子的反应。
例如,聚合氯乙烯的反应过程中,氯自由基首先引发反应,然后不断传递氯自由基,最终形成聚合物。
自由基引发的自由基聚合反应是有机合成中的重要反应类型。
以自由基溴化反应为例,当溴代烷类物质受到光照或热解时,生成溴自由基。
这个自由基可以引发其他有机物质的链反应。
2.自由基偶联反应自由基偶联反应是指两个自由基分子发生反应生成一个新分子的反应。
其中,最常见的自由基偶联反应类型为自由基与烯烃的加成反应。
举例来说,自由基溴反应产生的溴自由基可以与乙烯发生加成反应,生成溴乙烷。
3.自由基取代反应自由基取代反应是一种通过自由基取代反应产生新化合物的反应。
常见的自由基取代反应包括氟自由基取代反应和氯自由基取代反应等。
亲核取代反应通常由亲核试剂攻击亲电中心而发生。
当自由基试剂被引发后,会攻击一段电子密度相对较高的化学键,从而发生取代反应。
例如,自由基氟反应常用于药物合成中,产生氟取代的化合物。
二、自由基反应的应用自由基反应在有机合成和药物研发中有着广泛的应用。
它们能够产生复杂的分子结构并引发多样性选择性反应。
自由基反应 反应相

自由基反应反应相
自由基反应又称游离基反应,是自由基参与的各种化学反应。
自由基电子壳层的外层有一个不成对的电子,对增加第二个电子有很强的亲和力,故能起强氧化剂的作用。
自由基反应一般经历三个阶段:
- 链引发阶段:产生自由基的阶段。
由于键的均裂需要能量,所以链引发阶段需要加热或光照。
有些化合物十分活泼,极易产生活性质点自由基,这些化合物称之为引发剂(initiator)。
有时也可以通过单电子转移的氧化还原反应来产生自由基。
- 链转移阶段:由一个自由基转变成另一个自由基的阶段,自由基不断传递下去,像一环接一环的链,所以称之为链反应。
- 链终止阶段:消失自由基的阶段。
自由基两两结合成键,所有的自由基都消失了,自由基反应也就终止了。
自由基反应在大气化学、光化学烟雾形成等领域中起重要作用。
自由基种类繁多,如过氧化氢自由基(HO2-)、烷氧基自由基(RO-)、过氧烷基自由基(RO2-)、酰基自由基(RCO-)等,在反应中可能扮演中间产物的角色。
有机化学中的自由基反应

有机化学中的自由基反应有机化学是研究碳基化合物的行为和结构的学科,自由基反应是有机化学中一个重要的分支。
自由基是指氧化态电子不满足八个电子的孤立原子或分子离子,自由基反应是它们不配对电子的自然趋势所产生的反应。
一、自由基反应的基本概念自由基反应中最重要的反应是质子自由基反应。
在这种反应中,烷烃和另一个原料(如卤代烃或醇)反应形成自由基。
例如,当氯甲烷和氰化钠一起反应时,产生的自由基是氯和氰根离子(Cl原子和-CN原子)。
这些自由基会在反应中作为反应物或产物的中间体参与反应。
二、自由基反应的特点自由基反应的主要特点是由于自由基没有电荷,因此它们可以通过共价键连接。
自由基反应的过程包括单独自由基生成、自由基反应、金属源(环压剂)消耗等。
自由基反应是一种热力学不稳定的反应,因为它们的反应过程是由新自由基的生成和低次的链反应决定的。
此外,由于自由基没有电荷,因此它们可以参与多种反应类型,包括加成、抽取氢原子、烷基化、取代等。
三、自由基反应的实际应用自由基反应的实际应用非常广泛。
例如,它们可以用于生产化学纤维,合成核桃香精等。
此外,使用自由基反应进行光化学修饰化学键具有很高的选择性和可控性,也可以用于将光转换成热、电信号、荧光等。
而在医药方面,自由基反应在控制细胞增殖、修复DNA、制造新药物等方面起着至关重要的作用。
据研究表明,对于某些药物,如维生素C、辅酶Q10等,它们可以起到自由基清除的作用,从而起到预防疾病、减缓衰老等作用。
四、自由基反应的意义与挑战自由基反应在环保方面也起着至关重要的作用,因为它们可以用于控制废水的处理、脱氧、氧化等。
此外,自由基反应也为化学工业的可持续发展提供了更加灵活的选择。
然而,自由基反应也存在挑战。
因为自由基反应是一种不稳定的反应,它们常常需要顺序化处理,这对实验环境、对参与者本身的安全也提出了更高的要求。
五、结语自由基反应是有机化学中很重要的分支,具有广泛的应用前景,尤其是在医药和环保领域。
自由基取代反应举例

自由基取代反应举例自由基取代反应是一种有机化学中常见的反应类型,它涉及到自由基的生成和利用。
自由基是一种具有未成对电子的分子或离子,具有很高的反应活性。
下面是关于自由基取代反应的十个具体例子。
1. 氯代烷的氯代反应:在氯代烷中,氯原子可以被自由基取代,生成另一个氯代烷。
例如,甲烷和氯气反应生成氯代甲烷:CH4 + Cl2 → CH3Cl + HCl。
2. 烯烃的氢代反应:烯烃中的双键可以被氢原子取代,生成烷烃。
例如,乙烯和氢气反应生成乙烷:C2H4 + H2 → C2H6。
3. 烷基自由基的取代反应:烷基自由基可以取代其他有机分子中的氢原子,生成新的有机分子。
例如,甲基自由基可以与甲烷反应生成乙烷:CH3 + CH4 → CH3CH3。
4. 烯烃的卤代反应:烯烃中的双键可以被卤素原子取代,生成卤代烃。
例如,乙烯和溴气反应生成溴代乙烷:C2H4 + Br2 → C2H4Br2。
5. 自由基链反应:自由基链反应是一种连续的反应过程,其中一个自由基反应生成另一个自由基,从而形成一个反应链。
例如,溴气与甲烷反应生成甲基自由基,然后甲基自由基继续反应生成甲烷和溴气,形成一个自由基链反应。
6. 自由基聚合反应:自由基聚合反应是一种将单体分子通过自由基反应连接成高分子的方法。
例如,乙烯单体可以通过自由基聚合反应生成聚乙烯。
7. 自由基取代反应的选择性:自由基取代反应中,取代位置的选择性是一个重要的问题。
例如,在溴代乙烷的氢代反应中,氢原子的取代位置可以是甲基或乙基,取决于反应条件和反应物的结构。
8. 自由基取代反应的副反应:自由基取代反应中,可能会发生一些副反应,例如链传递反应和分子重排反应。
这些副反应会影响反应的产物分布和反应速率。
9. 自由基取代反应的应用:自由基取代反应在有机合成和药物制造中有广泛的应用。
例如,自由基取代反应被用于合成复杂有机分子和制备药物中的特定官能团。
10. 自由基取代反应的机理研究:自由基取代反应的机理研究对于理解反应过程和优化反应条件非常重要。
高等有机化学课件自由基反应

过氧化物在热或光的作用下裂解, 产生自由基,例如通过过氧化叔 丁酮制备自由基。
引发剂的光解、裂解或加热可产 生自由基,常用于合成聚合物。
X射线辐照
通过X射线辐照可产生大量自由 基,通常用于辐照杀菌和医学辐 照。
自由基氧化反应
1 自由基与氧气反应
自由基和氧气可以发生氧 化反应,产生自由基的α羟基或酮基。
自由基与链转移剂的反应
有机金属化合物的转移剂
通过转移活性烷基自由基,使链 反应发生中止。
碳酸酯的转移剂
碳酸酯自由基具有较高的反应活 性,具有可逆性和特定选择性。
酚的转移剂
酚可以与自由基加成,形成稳定 的自由基,从而阻止链反应的进 行。
自由基在有机生物学中的应用
1
活性氧物质
自由基是活性氧物质的一种,描述生物
高等有机化学课件自由基 反应
本课件将为您带来深入浅出的自由基反应知识。您将学习到自由基的概念及 特点、反应类型、产生方式、分类及特点,并了解自由基反应在有机合成和 制药工业中的应用。
自由基产生方式
紫外线照射
通过紫外线照射可引发自由基反 应,如合成自由基的溴化,产生 卤代烷的反应。
过氧化物裂解
引发剂作用
体内氧化应激的调节与损伤防治
2
与外界环境发生作用的过程中产生的一 类反应性分子。
体内产生的氧自由基和其他自由基通过
各种方式造成胞内的氧化损伤,可通过
引入自由基清除剂来调节和防止氧化应
3
生理过程的网络调控
激的发生。
完整的生理过程往往由多个互相作用、
网络调控的生化元件所组成。
2 自由基链反应氧化
自由基链反应可以在某些 条件下氧化有机物,例如 过氧化氢酸性环境下可以 氧化乙烯。
高等有机化学 重排反应

H2O
CH3
CH3 CO
+
-H2O
CH3
C3H O C O2H -+ H
C3H
CH3 CO CH3
OH+ 3CCOH3C
基团迁移能力顺序 Ph > CH3 3C > (CH3)2CH > H > CH3CH2 > CH3
26
(2) Baeyer-Villiger重排(拜耶尔-维利格 重 排):醛酮被过氧化物氧化为酯,
从碳原子到氮原子 (C
N)
从氮原子到碳原子 (N C)
从碳原子到氧原子 (C O)
从氧原子到碳原子 (O C)
其它杂原子与碳原子间重排
6
4. 按迁移的相对位置分类
1,2 迁移重排 [1,3]迁移重排 [1,5]迁移重排 [1,7]迁移重排 [3,3]迁移重排 [3,5]迁移重排
16
②芳基比烷基易迁移
Ph
Ph H2SO 4 Ph
Ph- H 2O Ph
H3C OH OH CH 3
H3C OH 2OH CH 3
H3C
Ph OH CH 3
Ph Ph
CH 3 - H+
H3C
OH
Ph Ph
CH 3
H3C
O
17
③迁移反应的立体化学-反式迁移 快 慢
18
④氨基醇和卤代醇也可以发生类似重排, 氨基可以经过重氮化反应生成碳正离子。
C H 2N H 2
HNO2 N2
CH2
C H 2O H
H 2O H
CH2
NH2
HNO2 N2
H
OH
H 2O H
H
13
大学有机化学各章重点

大学有机化学各章重点第一章绪论教学目的:了解有机化合物的定义、特性和研究程序,有机化学发展简史,有机化学的任务和作用。
在无机化学的基础上进一步熟悉价键理论、杂化轨道理论、分子轨道理论、共价键的键参数和分子间作用力。
掌握分子间作用力与有机化合物熔点、沸点、相对密度、溶解度等物理性质之间的关系。
熟悉有机化合物的分类,有机反应试剂的种类、有机反应及反应历程的类型。
掌握有机化合物的结构与性质之间的内在联系。
教学重点、难点:本章重点是有机化学的研究对象与任务;共价键理论;共价键断裂方式和有机反应类型。
难点是共价键理论。
教学内容:一、有机化学的发生和发展及研究对象二、有机化合物中的化学键与分子结构1、共价键理论:价键理论、分子轨道理论、杂化轨道理论、σ键和π键的电子结构及其反应性能。
2、共价键的参数:键长、键角、键能、元素的电负性和键的极性。
3、分子间力及有机化合物的一般特点4、共价键断裂方式和有机反应类型三、研究有机化合物的一般方法:分离提纯、分子式的确定、构造式的确定。
四、有机化合物的分类:按碳胳分类;按官能团分类。
第二章饱和烃(烷烃)教学目的:掌握烷烃的命名、结构及其表示方法、构象、化学性质。
了解烷烃的同系列和同分异构,物理性质等。
教学重点、难点:本章重点是烷烃的结构、构象及化学性质。
难点是烷烃的构象及构象分析。
教学内容:一、有机化合物的几种命名方法。
二、烷烃的命名:系统命名法、普通命名法。
三、烷烃的结构和性质:1、烷烃的结构特点及同分异构:碳原子的正四面体概念、烷烃结构的表示方法。
2、烷烃的构象:乙烷、正丁烷的构象;透视式、楔线式及投影式的变换。
3、物理性质4、化学性质:氧化、卤代,自由基反应机理(链反应,游离基及其稳定性)。
四、自然界的烷烃第三章不饱和烃教学目的:掌握烯烃、炔烃的结构、异构及命名,化学性质,马氏规则,共轭二烯烃的分子结构、化学性质。
了解烯烃、炔烃的物理性质、亲电加成反应历程(溴钅翁离子、碳正离子及其稳定性)、异戊二烯和橡胶。
有机合成 第七章 自由基反应

BPO
AIBN
引发剂的作用:自身不稳定首先产生引发自由
基,引发自由基夺取底物原子生成底物自由基。
王鹏
7.2 自由基的产生
加热下能产生自由基的化合物:
分子中含有弱化学键的,如碳-杂原子键
过氧化物,氯代烃或溴代烃等
分子存在强张力的键或碎裂后可得到强化学键
产物的
BPO和AIBN都属于此类化合物
自由基的链式反应对甲烷卤代反应的解释:链
引发、链增长和链终止
王鹏
7.2 自由基的产生
通过氧化还原的化学方法可以使得共价键
因得失电子而异裂,方式分别为氧化方式 和还原方式:
氧化:自由基正离子为代表,二氯二氰基苯醌
(DDQ)和硝酸铈铵(CAN)最为常用: O
NC NC O Cl Cl
二氯二氰 基苯醌
加入引发剂后反应温度可以降低至60到110
度,常使用CCl4为溶剂。
王鹏
7.2 Байду номын сангаас由基的产生
光照法:
光照是产生自由基独特的反应,光照引发的反
应只有自由基反应、D-A反应和电环化反应 分子中存在生色团(吸光基团,如π键)时可 以吸收光子促进键的均裂。
光照下π键化合物可变为自由基,π键越弱,越易激 发,反应就越容易
酯还原偶联得到α-羟基酮(酰偶姻)的反应 醛酮在低价钛诱导下还原偶联得到烯烃
酰偶姻缩合: ※
McMurry烯烃化:
王鹏
7.3 自由基的反应
Pinacol偶联:
羰基化合物在金属作用下发生偶联生成邻二醇化合 物的反应称为嚬哪醇反应
• •
反应通常也可以描述成还原-偶联过程,通常使用 碱土金属或Zn等过渡金属 反应不能使用钠等碱金属,因为在醇中反应只能发 生还原得到产物醇。Mg、Zn等则由于配位作用的 稳定性而优先发生分子内偶联 SmI2等也是常用的反应试剂,生成Sm3+。
有机化学_第7章_自由基反应汇总

烷烃氯化反应的选择性
2020/8/5
22
烷烃溴化反应的选择性
CH3CH2CH3 + Br2
127oC 光照
CH3CH2CH2Br + CH3CHBrCH3
3%
97 %
(CH3)3CH + Br2
127oC 光照
(CH3)2CHCH2Br + (CH3)3CBr
H3CCl
2020/8/5
17
势能 /(kJ mol-1)
Cl
H
CH3
H3C
Cl
Cl
+16.7
Ea1
Ea2
+8.3
CH4 + Cl
CH3 + HCl
Cl2
+7.5
112.9 105.4
CH3Cl + Cl
O 2020/8/5
反应进程
18
甲烷氯化反应势能图的分析
1 第一步反应的活化能比较大,是速控步骤。 2 第二步反应利于平衡的移动。 3 反应 1 吸热,反应 2 放热,总反应放热,所以反应只需开始时供热。 4 过渡态的结构与中间体(中间体是自由基)相似,所以过渡态的稳定 性顺序与自由基稳定性顺序一致。
1%
99 %
溴化 ν 1oH: ν 2:oHν =3oH1 : 82 : 1600
氯化反应和溴化反应都有选择性,但溴化反应的选择性比氯化反应高 得多。
2020/8/5
23
2020/8/5
24
5.4.4 a-H的卤代( Halogenation of a-H)
2020/8/5
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
自由基反应 Radical Reactions
2020/8/5
1
5.1 碳自由基的定义和结构
定义:带有孤电子的原子或原子团称为自由基。 碳自由基:含有孤电子碳的体系称为碳自由基。
CH3CH2
一级碳自由基
CH3CHCH3
二级碳自由基
CH3CCH3 CH3
三级碳自由基
2020/8/5
2
自由基的结构特点:有三种可能的结构; (1)刚性角锥体,(2)迅速翻转的角锥体, (3)平面型。如下图:
2020/8/5
12
两点说明
影响自由基稳 定性的因素是很多 的,如: 电子离 域,空间阻碍,螯 合作用和邻位原子 的性质等;
碳自由基的最
外层为七个电子, 反应时总要寻找另 外的电子来达到八 隅体结构,所以是 亲电的。
2020/8/5
13
5.3 自由基反应的共性
定义:由化学键均裂引起的反应称为自由基反应。
共 (1)反应机理包括链引发、链增长、链终止三个阶段。
(2)反应必须在光、热或自由基引发剂的作用下发生。 (3)溶剂的极性、酸或碱催化剂对反应无影响。
性 (4)氧气是游离基反应的抑制剂。
单自由基比双自由基稳定
CH3 + O O
CH3 O O
2020/8/5
双自由基
单自由基
14
5.4 烷烃的卤化
5.4.1 甲烷的氯化 5.4.2 甲烷的卤化 5.4.3 高级烷烃的卤化
3 无取代基的环烷烃的一氯化反应也可以用相应方法制备, C(CH3)4的一氯化反应也能用此方法制备。
2020/8/5
20
5.4.2 甲烷的卤化
•X + CH3-H F 439.3
• CH3 + H-X H /(kJmol-1) 568.2 -128.9
Ea/(kJmol-1)
+4.2
Cl
431.8 +7.5
C
C
C
刚性角锥体
迅速翻转的角锥体
平面型
2020/8/5
3
2020/8/5
4
2020/8/5
5
2020/8/5
6
5.2 键解离能和碳自由基的稳定性 自由基的产生
热均裂产生
O CH3CO
辐射均裂产生
Br
O OCCH3
55 - 85oC
C6H6
O CH3CO
Br
光
25oC
2Br
单电子转移的氧化还原反应产生
2020/8/5
15
5.4.1 甲烷的氯化
取代反应
分子中的原子或基团被 其它原子或基团取代的 反应称为取代反应。
卤代反应
分子中的原子或基团被 卤原子取代的反应称为 卤代反应。
2020/8/5
16
甲烷的氯化
反应式 CH4 + Cl2
hv
CH3Cl + HCl
反应机理(反应过程的详细描述)
链引发 链增长
2020/8/5
9
2020/8/5
10
CH2 > CH2 CHCH2 > (CH3)3C > (CH3)2CH
苯甲基自由基
烯丙基自由基 三级丁基自由基 异丙基自由基
> CH3CH2 > CH3 >
乙基自由基 甲基自由基 苯基自由基
2020/8/5
11
Question: List in order of decreasing stability all of radicals that can be obtained by abstraction of a hydrogen atom from 2-methylbutane.
2020/8/5
H2O2 + Fe2+ RCOO-
-e-
电解
HO• + HO- + Fe3+ RCOO •
7
2020/8/5
8
自由基的稳定性
CH2 CHCH2
H
CH2 CHCH2 H
均裂 H=359.8kJmol-1(87kcalmol-1)
共价键均裂时所需的能量称为键解离能。 键解离能越小,形成的自由基越稳定。
不变
hv Cl2
CH4 + Cl
2Cl
生成
CH3 + HCl
H = 7.5 kJmol-1 Ea= 16.7 kJmol-1
CH3 + Cl2
CH3Cl + Cl
H = -112.9 kJmol-1 Ea= 8.3 kJmol-1
链终止 Cl + Cl
Cl2
消失
CH3 + CH3
Cl + CH3
H3CCH3
氯化 ν : 1oH ν :2oνH = 13oH : 4 : 5.3
烷烃氯化反应的选择性
2020/8/5
22
烷烃溴化反应的选择性
CH3CH2CH3 + Br2
127oC 光照
CH3CH2CH2Br + CH3CHBrCH3
2020/8/5
21
5.4.3 高级烷烃的卤化
CH3CH2CH2CH3 + Cl2
35oC 光照
(CH3)3CH + Cl2
35oC 光照
CH3CH2CH2CH2Cl + CH3CH2CHClCH3
28 %
72 %
(CH3)2CHCH2Cl + (CH3)3CCl
63 %
37 %
ν 1oH : ν 2oH = 28/6 : 72/4 = 1 : 4 ν 1oH: ν =3oH63/9 : 37/1 = 1 : 5.3
+16.7
Br
366.1 +73.2
+75.3
I
298.3 +141
> +141
总反应热/(kJmol-1): F(-426.8) Cl(-104.6) Br(-30.96) I(53.97)
1. 氟化反应难以控制。 2. 碘化反应一般不用。碘自由基是不活泼的自由基。 3. 氯化和溴化反应常用,氯化比溴化反应快5万倍。
推论:3oH最易被取代,2oH次之,1oH最难被取代。
2020/8/5
19
甲烷氯化反应的适用范围CH4ຫໍສະໝຸດ Cl2 300-400OC
or光照
CH3Cl +
HCl
Cl2 光照
CH2Cl2 +
HCl
Cl2 光照
CHCl3
+ HCl
Cl2 光照
CCl4 +
HCl
1 该反应只适宜工业生产而不适宜实验室制备。
2 该反应可以用来制备一氯甲烷或四氯化碳,不适宜制备二氯甲烷 和三氯甲烷。
H3CCl
2020/8/5
17
势能 /(kJ mol-1)
Cl
H
CH3
H3C
Cl
Cl
+16.7
Ea1
Ea2
+8.3
CH4 + Cl
CH3 + HCl
Cl2
+7.5
112.9 105.4
CH3Cl + Cl
O 2020/8/5
反应进程
18
甲烷氯化反应势能图的分析
1 第一步反应的活化能比较大,是速控步骤。 2 第二步反应利于平衡的移动。 3 反应 1 吸热,反应 2 放热,总反应放热,所以反应只需开始时供热。 4 过渡态的结构与中间体(中间体是自由基)相似,所以过渡态的稳定 性顺序与自由基稳定性顺序一致。
