含氮有机化合物理解练习及答案解析
高考化学氮及其化合物推断题综合练习题及答案解析

高考化学氮及其化合物推断题综合练习题及答案解析一、氮及其化合物练习题(含详细答案解析)1.氮及其化合物在生产生活中有广泛的应用:(1)甲、乙两瓶氨水的浓度分别为1mol/L和0.1mol/L,则甲、乙两瓶氨水中c(OH-)之比____10(填“大于”“等于”或“小于”),并说明理由_____________________________________。
(2)常温下向含0.5mol溶质的稀盐酸中缓慢通入0.5molNH3(溶液体积变化忽略不计),反应结束后溶液中离子浓度由大到小的顺序是______________________;在通入氨气的过程中溶液的导电能力___________(选填“变大”、“变小”或“几乎不变”)。
请设计实验检验铵盐中的NH4+:___________。
【答案】小于加水稀释,弱电解质的电离程度增大 c(Cl-)>c(NH4+)>c(H+)>c(OH-)几乎不变取样,加水溶解,加入氢氧化钠浓溶液,加热,若产生的气体能使湿润的红色石蕊试纸变蓝,则证明有NH4+【解析】【分析】【详解】(1)浓溶液加水稀释,越稀越电离,故0.1mol/L的氨水中电离程度更大,故甲、乙两瓶氨水中c(OH-)之比小于10;答案为:小于;加水稀释,弱电解质的电离程度增大;(2)二者恰好反应生成氯化铵,铵根水解溶液呈酸性,即c(H+)>c(OH−),依据溶液呈电中性有:c(H+)+c(NH4+)=c(OH−)+c(Cl−),因为c(H+)>c(OH−),所以c(NH4+)<c(Cl−),故离子浓度大小关系为:c(Cl−)>c(NH4+)>c(H+)>c(OH−);溶液中离子浓度几乎不变,所以导电能力几乎不变;铵盐能与强碱反应放出氨气,则检验铵根离子的实验方案:取样,加水溶解,加入氢氧化钠浓溶液,加热,若产生的气体能使湿润的红色石蕊试纸变蓝,则证明有NH4+。
【点睛】浓溶液加水稀释,越稀越电离;溶液的导电能力主要取决于溶液中离子的浓度及离子所带的电荷数:离子的浓度越大,导电能力越强;离子所带的电荷数越大,导电能力越强。
药用有机化学试题(第九章:含氮化合物(胺类)附答案 )

第九章:含氮化合物(胺类)223.下列化合物中,低温下能生成稳定重氮盐的是?[1分]A苄胺B苯胺CN-甲基苯胺DN-甲基苄胺参考答案:B224.下列化合物中,沸点最高的是?[1分]A乙酸B乙胺C二乙胺D乙醇参考答案:A225.下列化合物中碱性最强的是?[1分]A NH3B CH3NH2C C 6H5CH2NH2D CH3NHCH3参考答案:D226.的正确名称为?[1分] A苯乙胺B乙苯胺CN-苯基乙胺DN-乙基苯胺参考答案:D227.下列化合物属于芳香胺的是?[1分]ABCD参考答案:B228.能与乙酰氯发生酰化反应的胺是?[1分]A异丙胺B二乙丙胺CN,N-二甲基苯胺D甲乙丙胺参考答案:A229.下列化合物中,沸点最高的是?[1分]A CH3NH2B CH3CH2CH2NH2 C(CH3)3N D CH3NHCH2CH3参考答案:B230.关于苯胺性质的叙述错误的是?[1分]A易被空气中氧气氧化B能与盐酸所用生成季铵盐C能与羧酸反应生成酰胺D 能与溴水反应生成白色沉淀参考答案:B231.与亚硝酸反应可放出氮气的是?[1分]ACH3NH2BCH3NHCH3C(CH3)3NDCH3NHCH2CH3参考答案:A232.与NaNO2和盐酸反应,能生成黄色油状物的是?[1分]AC6H5NH2BCH3CH2NH2CCH3NHCH2CH3D(CH3)3N参考答案:C233.芳香胺的碱性一般较脂肪胺弱。
[1分]参考答案:T234.在实验室合成乙酰苯胺时,可采用苯胺和乙酸进行制备。
[1分]参考答案:T235.所有的胺及其衍生物均呈碱性。
[1分]参考答案:F236.胺的碱性取决于氮原子上电子云密度,电子云密度越大,碱性越强。
[1分]参考答案:T237.胺的盐类属于离子型化合物,具有强酸性。
[1分]参考答案:T238.利用伯、仲、叔胺与HNO2的不同反应性能,可以鉴别伯、仲、叔胺。
[1分]参考答案:T239.胺可与不溶于水的中性或酸性物质分离,是由于胺具有碱性。
第15章 有机含氮化合物习题参考答案
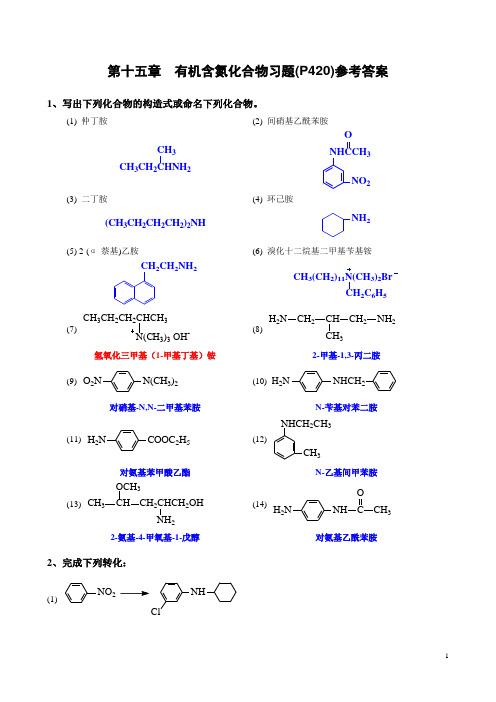
第十五章 有机含氮化合物习题(P420)参考答案1、写出下列化合物的构造式或命名下列化合物。
(1) 仲丁胺(2) 间硝基乙酰苯胺CH 3CH 2CHNH 2CH 3NHCCH 3NO 2O(3) 二丁胺(4) 环己胺(CH 3CH 2CH 2CH 2)2NHNH 2(5) 2-(α-萘基)乙胺(6) 溴化十二烷基二甲基苄基铵CH 2CH 2NH 2CH 3(CH 2)11N(CH 3)2BrCH 2C 6H 5(7)CH 3CH 2CH 2CHCH 3N(CH 3)3 OH-(8)H 2N CH 2CH CH 2NH 2CH 3氢氧化三甲基(1-甲基丁基)铵2-甲基-1,3-丙二胺(9) O 2NN(CH 3)2(10) H 2NNHCH 2对硝基-N,N-二甲基苯胺N-苄基对苯二胺(11) H 2NCOOC 2H 5(12) NHCH 2CH 3CH 3对氨基苯甲酸乙酯N-乙基间甲苯胺(13) CH 3CH CH 2CHCH 2OH 2OCH 3(14)H 2N NH C OCH 32-氨基-4-甲氧基-1-戊醇对氨基乙酰苯胺2、完成下列转化:(1)NO 2NHCl解:NO 2NHCl2Fe, HClNH2Cl(2) CH 2=CH CH=CH 2H 2N(CH 2)6NH 2解:CH 2=CH CH=CH 2H 2N(CH 2)6NH 22Cl CH 2CH=CHCH 2Cl2 Ni(3) 正丁醇正丁胺、正丙胺、正戊胺解:CH 3CH 2CH 2CH 22N - K +O ON OOCH 2CH 2CH 2CH 3CH 3CH 2CH 2CH 2NH 2H OCH 3CH 2CH 2CH 2OHCH 3CH 2CH 2NH 2(1) NH _(1) [O]2CH 3CH 2CH 2CH 2OHCH 3CH 2CH 2CH 2CH 2NH 2(1) SOCl (2) NaCNCH 3CH 2CH 2CH 2CN 2Ni(4) C 2H 5OH 、C 6H6C 6H 5CHCH 3NHC 2H 5解:C 2H 5OHHClNH 3C 2H 5NH 2或PCl 32C 2H 5CH3COOH P O (CH 3CO)2OCCH 3OCHCH 3NHC 2H 5[O]3、排序:(1) 将下列化合物按沸点由高到低顺序排列:(A) 丙胺 (B) 丙醇 (C) 甲乙醚 (D) 甲乙胺 (E) 三甲胺 解:(B )>(A)>(D)>(C)>(E)(2) 将下列化合物按亲核取代反应活性由高到低顺序排列:(A) 氯苯 (B) 对甲氧基氯苯 (C) 对硝基氯苯 (D) 2,4-二硝基氯苯 解:(D)>(C)>(A)>(B)(3) 将下列化合物按碱性由强到弱顺序排列:(A) (CH3)4NOH(B) C6H5NH2(C) C2H5NH2(D) C6H5NHCH3(E) CH3CONH2解:(A)>(C)>(D)>(B)>(E)(4) 将下列化合物按碱性由强到弱顺序排列:(A) CH3CH2CH2NH2(B) CH3CHCH2NH2OH(C)CH3CH2CH2NH2OH(D)CH3CH2CHNH2CH3解:(D)>(A)>(B)>(C)(5) 将下列化合物按碱性由强到弱顺序排列:(A) NHCOCH3(B) NHSO2CH3(C) NHCH3(D) N CH3(E) NH2解:(E)>(D)>(C)>(A)>(B)(6) 将下列化合物按碱性由强到弱顺序排列:(A) 对甲苯胺(B) 苄胺(C) 2,4-二硝基苯胺(D) 对硝基苯胺(E) 对氯苯胺解:(B)>(A)>(E)>(D)>(C)4、用简单的化学方法区别下列化合物:(1) (A) 硝基苯(B) 硝基环己烷(C) 间甲苯胺(D) N-甲基苯胺(E) N,N-二甲基苯胺解:ABCDE溶解不溶解溶解不溶解不溶解不溶解溶解硝基苯硝基环己烷清亮溶液油状物间甲苯胺N-甲基苯胺N,N-二甲基苯胺(2) (A) OH(B) NH2(C) N H(D) N CH3解:ABCD 溶解不溶解不溶解不溶解清亮溶液油状物苯胺环戊胺N-甲基环戊胺苯酚5、用简单的化学方法分离、提纯下列各组混合物:(1) (A) 苄胺(B) N-甲基环己胺(C) 苯甲醇(D) 对甲苯酚解:水层ABCD -油层水层有机层水层H+p-CH3-C6H4-OH (D) C6H5CH2OH (C)(2) 分液p-CH-C H-SO ClNaOH清亮溶液固体沉淀过滤C6H5CH2NH2NHCH3(1) H O/OH-, ∆干燥、蒸馏(1) HO/OH-, ∆干燥、蒸馏(A)(B)(2) N-甲基苯胺中混有少量N,N-二甲基苯胺,请设计实验方案提纯N-甲基苯胺。
氮及其化合物 经典习题(含详解)

氮及其化合物经典习题1.下列关于自然界中氮循环(如下图)的说法不正确的是()A.人工固氮可以得到硝酸盐B.雷电作用可将氮气直接转化为铵盐C.细菌对氮元素的循环有重要作用D.亚硝酸盐转化为硝酸盐的过程中,氮元素被氧化答案 B解析A项,人工固氮是把氮气合成氨,氨和硝酸反应得到硝酸盐,人工固氮可以得到硝酸盐,正确;B项,放电条件下氮气和氧气反应生成一氧化氮,一氧化氮和氧气反应生成二氧化氮,二氧化氮和水反应生成硝酸,不能直接得到铵盐,错误;C项,豆科类植物的根瘤菌能将空气中氮气转化为植物需要的铵盐,实现生物固氮,细菌对氮元素的循环有重要作用,正确;D项,亚硝酸盐中氮元素化合价为+3价,生成硝酸盐中氮元素化合价为+5价,氮元素化合价升高,发生氧化反应,正确。
2.起固氮作用的化学反应是()A.N2和H2在一定条件下反应生成NH3B.NO遇O2转化为NO2C.硝酸工厂用NH3氧化制NOD.用NH3制碳酸氢铵和硫酸铵答案 A解析氮的固定是指游离态的氮转化成化合态的氮。
3.关于氨的下列叙述中,错误的是()A.液氨易汽化,因此可用来做制冷剂B.氨溶于水显弱碱性,因此可使酚酞溶液变为红色C.氨极易溶解于水,因此氨水比较稳定(不容易)分解D.氨可被氯气氧化生成N2,同时还可能产生白烟现象答案 C4.下列关于氨水的说法中,不正确的是()A.氨水和液氨不同,氨水是混合物,液氨是纯净物B.氨水中物质的量浓度最大的粒子是NH3·H2O(水除外)C.氨水显弱碱性,是弱电解质D.在1 mol·L-1氨水中,NH3·H2O、NH+4、NH3的物质的量浓度之和为1 mol·L-1答案 C解析氨极易溶于水,发生如下反应:NH3+H2O NH3·H2O NH+4+OH-;生成的氨水是混合物,其中的NH3·H2O是弱电解质,电离程度小,且NH3分子极易与H2O结合,故其中浓度最大的粒子是NH3·H2O(H2O除外)。
有机化学含氮有机化合物、 杂环化合物和生物碱练习题

有机化学含氮有机化合物、杂环化合物和生物碱练习题一、单选题1、下列化合物中的碱性最大的是()A、二甲胺B、甲胺C、氨D、苯胺正确答案:A2、下列化合物不能和苯磺酰氯发生反应生成白色沉淀的是()A、三乙胺B、叔丁胺C、苄胺D、二乙胺正确答案:A3、能与亚硝酸作用生成难溶于水的黄色油状物的化合物是()A、甲胺B、N-甲基苯胺C、苯胺D、三乙胺正确答案:B解析:仲胺会发生这样的反应4、与亚硝酸作用能放出N2的化合物是()。
A、伯胺B、仲胺C、叔胺D、以上都不能正确答案:A5、下列化合物可以和重氮盐酸盐在低温条件下发生反应生成偶氮化合物的是()A、苯酚B、苯甲酸C、甲苯D、氯苯正确答案:A6、芳香族重氮盐酸盐在下列条件下不会放出氮气的是()A、水溶液,加热B、Cu2Cl2/HCl,加热C、Cu2CN2/KCN,加热D、苯胺(中性或弱酸性),低温正确答案:D7、下列化合物中的碱性顺序从大到小的排列正确的是()a 、乙酰胺b 、邻苯二甲酰亚胺c 、尿素d 、氢氧化四甲铵A、a>b>c>dB、d>c>b>aC、c>d>a>bD、d>c>a>b正确答案:D8、下列化合物能发生缩二脲反应的是()A、尿素B、乙酰胺C、CH 3CH(NH 2)COOHD、H 2NCONHCONH 2正确答案:D9、下列碱性最大的是A、吡咯B、吡啶C、氢氧化四甲铵D、苯胺正确答案:C10、下列亲电取代活性最小的是A、吡啶B、吡咯C、苯D、苯胺正确答案:A二、填空题组成杂环化合物环状结构的原子除碳原子外,常见的有_______、_______和______。
这些非碳原子被称为_______。
根据环的大小杂环化合物可分为_______杂环和_______杂环;根据稠合的环数目杂环化合物可分为_______杂环_______杂环。
正确答案:第1空:氧第2空:硫第3空:氮第4空:杂原子第5空:五元第6空:六元第7空:单第8空:稠。
有机化学课件(李景宁主编)第14章_含氮有机化合物习题

浓 NaOH CHO + CHO + CH 3 KMnO 4 KOH N K COOH COOH N COOH COOH KMnO 4 N O CH 2OH 稀 OH
-
+ O COOH
CH 3COCH 3
O
CH=CH COCH 3
碳水化合物
一、三个单糖和过量苯肼作用后,得到同样晶形的脎,其中一个
CHO
3、化合物A(C8H17N)其NMR中无双峰,A与2molCH3I反应后再与 湿的Ag2O作用,并加热生成B(C10H21N),再重复以上反应则生成 三甲胺及1,4—辛二烯和1,5—辛二烯,给出A、B 的结构并写出有 关反应方程式。
4、化合物A(C6H13O2N)有旋光性,A与HNO2作用放出N2,与 NaHCO3作用放出CO2,A与HNO2的水溶液作用生成B(C6H12O3), B仍有旋光性,B与浓H2SO4作用于脱水生成C(C6H10O2),C能使 KMnO4溶液褪色,与酸性KMnO4作用并加热则生成草酸和2—甲基丙 酸,写出A、B各对映异构体的Fisher投影式,并用R/S命名法命名, 写出C的结构式。
A 伯胺
B 仲胺
C 叔胺
D 都可以
)
7、下列化合物能溶于稀盐酸的是( A 苯胺 B 苯酚 C 苯甲酸
D 乙酰苯胺
8、下列化合物碱性最强的是( ) A CH 3COO-+NH4 C CH3CONH2 A 5%盐酸水溶液 B CH3(CH2)3NH2 D H2NCH2COOH ) D银氨溶液 B 苯磺酰氯和NaOH C 乙酸酐
9、能区分苯胺和N-甲基苯胺的是(
10、反应C6H5NH2 + H2SO4(1mol) A
SO3H NH2
高考化学培优(含解析)之氮及其化合物含答案解析

高考化学培优(含解析)之氮及其化合物含答案解析一、氮及其化合物练习题(含详细答案解析)1.氮的氧化物既是可导致酸雨的物质,也是造成空气污染的重要物质,加大对氮的氧化物的治理是环境保护重要举措。
(1)在一定条件下氨气可用来将氮氧化物转化为无污染的物质。
写出氨气和二氧化氮在一定条件下反应的化学方程式: _____________________________,该反应中氧化剂是_________,还原剂是________________________________________。
(2)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应生成对大气无污染的气体,该反应的化学方程式为___________________________________。
(3)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:NO2+NO+2NaOH===2NaNO2+H2O2NO2+2NaOH===NaNO2+NaNO3+H2O现有V L某NaOH溶液能完全吸收n mol NO2和m mol NO组成的大气污染物。
①所用烧碱溶液的物质的量浓度至少为_________ mol·L-1。
②若所得溶液中c(NO3-)∶c(NO2-)=1∶9,则原混合气体中NO2和NO的物质的量之比n∶m =_________。
③用含n和m的代数式表示所得溶液中NO3-和NO2-浓度的比值c(NO3-)∶c(NO2-)=_________。
【答案】6NO2+8NH37N2+12H2O NO2 NH3 2NO+2CO N2+2CO2 (m+n)/V 3∶2 (n-m)/(3m+n)【解析】【分析】(1)氨气和二氧化氮在一定条件下反应生成氮气和水,反应中元素化合价降低的做氧化剂,元素化合价升高的物质做还原剂;(3)①根据气体和氢氧化钠的关系式计算;②根据二氧化氮、一氧化氮和氢氧化钠反应的方程式中各个物理量之间的关系式计算;③同一溶液中,c(NO3-):c(NO2-)等于其物质的量之比。
华东理工大学有机化学课后答案含氮化合物

(3) .
N(CH2CH3)2 CH3CHCH2CH3
思考题12-15. 如何完成下列转变。
NH2
NHCOCH2CH2CH3 CH3CH2CH2CH2CHO H2 / Ni
答案: (1).
TM
C2H5
HCN CN SN2
C2H5 H CH3 NH2H2C
C2H5 H CH3
(2).
H CH3
Br
思考题 12-16 如保用 Gabriel 合成法来制备苯甲胺。
O C CH2Br NH C O KOH O C N CH2 C O
1. OH 2. H3O
CH2NH2
答案:
此反应为 SN2 历程,适用于位阻小的卤代烃参与的取代反应。
思考题12-17 当(R)-2-甲基丁酰胺在氢氧化钠的水溶液中与溴发生反应,预测产物的结构及它的立体化学。
答案:产物为(R)2-甲基丙胺,构型不变。
答案: (1)a>b>c>d 苯环上取代基硝基是强吸电子基,其通过共轭效应和诱导效应降低了酚氧原子上的电 子云密度,从而使质子容易离去,分子的酸性增强。 (2)a>b>c (3)b>a>c (4)A . b>c>a>d N 上供电子基团越多,N 原子上电子密度高,捕获质子能力就强。但在水中,
含氢少的胺溶剂化效应小,叔胺上没有氢,溶剂化效应极小,碱性反而比伯胺还弱。 B.a>b>c>d 仅有分子中 N 上取代基的电子效应作用。
NH2
(3).
OCH3
NO2
思考题 12-8. 请设计一个分离对甲基苯酚、环己基甲酸和对甲基苯胺混合物的方法。 答案:第一步往混合液中加入碳酸氢钠溶液 ,能溶解羧酸,分液后,(有机层留作第二步用) 往无机层中加 稀酸,羧酸即游离出。 第二步 向分离出的有机层中加入稀盐酸 ,胺能溶于盐酸溶液.分液,无机层中 加入氢氧化钠溶液即胺析出.
有机化学习题(含氮化合物含答案)
COOH
NH2
NH2
NHCOCH3
e.
(CH3CO)2O
f.
NO2 Fe + HCl
NH2
Br2 , Fe
NO2 Fe
+
HCl
Br
NH2NaNO2+ HCl
0-5 0C
N2+Cl-
NH2
弱 H+
NN
Br
Br
Br
NH2
CH3
g.
HNO3
CH3 Fe + HCl
CH3 NaNO2+ HCl
O2N
H2N
O H
b. 中只有Ⅰ 一种氢键
H3C
H3C H3C
H3C N H N H N
H H3C H3C
Ⅰ
3.解释下列事实? a. 苄胺(C6H5CH2NH2)的碱性与烷基胺基本相同,而与芳胺不同。 b. 下列化合物的 pKa 为
O2N
NH2
NH2
H3C
NH2
pKb=13.0
答案:
pKb=9.37
pKb=8.70
0-5 0C
H3C
OH
HO
N2+Cl-
H3C
N- N
OH-
2.化方法鉴别下列各组化合物: a. 邻甲苯胺 N-甲基苯胺
答案:
苯甲酸和邻羟基苯甲酸
CH3
a.
NH2 (A)
NHCH3 (B)
COOH (C)
COOH (D)
OH
NaOH
不溶
A H3C
SO2Cl
B
NaOH
不溶 B 可溶
A
可溶 C D
FeCl3
高考化学推断题综合题专题复习【氮及其化合物】专题解析附答案

高考化学推断题综合题专题复习【氮及其化合物】专题解析附答案一、氮及其化合物练习题(含详细答案解析)1.A 、B 、C 、D 、E 、F 为中学化学中的常见物质,且物质A 由1~2种短周期元素组成,在一定条件下有如图转化关系,请完成下列问题:(1)若常温下A 为有色气体。
①当F 是一种金属单质时,请写出一定浓度的B 溶液和适量F 反应生成C 与气体E 的离子方程式:_________________。
②当C 为直线形分子时,E 具有漂白性,物质F 焰色反应呈黄色,则C 的电子式为________________;D 中所含化学键的类型为____________________。
(2)若A 为淡黄色固体,D 为白色难溶于水的物质,且A 和D 的相对分子质量相等,请用离子方程式表示F 的水溶液呈酸性的原因:_________________。
(3)若A 中一种元素原子的最外层电子数为内层电子总数的15,将B 和D 分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A 与H 2O 反应的化学方程式:____________;B 转化为C 的化学方程式为______________。
【答案】Fe +4H ++NO 3-=Fe 3++NO↑+2H 2O离子键、极性共价键 Al 3++3H 2OAl (OH )3+3H + Mg 3N 2+6H 2O=3Mg (OH )2+2NH 3↑ 4NH 3+5O 2催化剂4NO +6H 2O 【解析】【详解】(1)①若F 是一种金属单质,由转化关系可知,F 为变价金属,F 为铁,B 与铁反应生成Fe 3+;由于A 为有色气体,与水反应生成B 和E ,则A 为NO 2,B 为HNO 3,E 为NO ,C 为Fe(NO 3)3,D 为Fe(NO 3)2;B 与适量F 反应生成C 和气体E 的离子方程式为:Fe +4H ++NO 3-=Fe 3++NO↑+2H 2O ;②A 为有色气体,与水反应生成B 和E ,E 具有漂白性,则A 为Cl 2,B 为HCl ,E 为HClO ,物质F 的焰色反应为黄色,说明含有钠元素,C 为直线型分子,结合转化关系可知,F 为Na 2CO 3,C 为二氧化碳,D 为碳酸氢钠;二氧化碳的电子式为:;D 为碳酸氢钠,其中含有离子键、极性共价键。
高考化学氮及其化合物 (讲义及答案)含答案解析

高考化学氮及其化合物 (讲义及答案)含答案解析一、选择题1.某混合气体可能有CO 、2CO 、3NH 、HCl 、2H 和水蒸气中的一种或几种,当依次通过澄清石灰水(无浑浊现象)、氢氧化钡溶液(有浑浊现象)、浓硫酸、灼热的氧化铜(变红)和无水硫酸铜(变蓝)时,可判断该混合气体中一定有( )A .HCl 、2CO 、2HB .CO 、2H 、2H OC .CO 、2H 、3NHD .HCl 、CO 、2H O【答案】A 【详解】由于混合气体通过氢氧化钡溶液(有浑浊现象),而通过澄清石灰水(无浑浊现象),证明混合气体中一定存在氯化氢和二氧化碳气体;经过浓硫酸干燥后,灼热的氧化铜(变红)说明氧化铜被还原成铜,无水硫酸铜(变蓝)说明反应后有水生成,证明混合气体中一定存在氢气,综上所述,该混合气体中一定有HCl 、CO 2、H 2,故答案为A 。
【点睛】考查常见气体的检验与除杂方法,此题为混合物组成的推断题,完成此题,要根据题干叙述的内容,根据物质的有关性质,抓住解题的关键,根据“通过澄清石灰水(无浑浊现象)、氢氧化钡溶液(有浑浊现象)”可知混合气体中一定存在二氧化碳和氯化氢,一定不存在氨气;根据混合气体通过浓硫酸浓硫酸干燥后通过“灼热的氧化铜(变红)和无水硫酸铜(变蓝)”证明一定存在氢气,可能存在一氧化碳。
2.用右图所示装置进行下列实验,实验结果与预测的现象不一致的是①中的物质 ②中的物质 预测①中现象 A 淀粉碘化钾溶液 浓硝酸 无明显现象 B 酚酞溶液 浓盐酸 无明显现象 C 氯化铝溶液 浓氨水 有白色沉淀 D湿润红纸条饱和氯水红纸条褪色A .AB .BC .CD .D【答案】A【详解】A.硝酸具有挥发性,挥发出的硝酸进入淀粉KI溶液,硝酸具有强氧化性,可以将KI氧化为I2,I2遇淀粉变蓝色,故A错误;B.浓盐酸具有挥发性,挥发出的HCl进入酚酞溶液,酚酞溶液在酸性条件下不变色,故B 正确;C.浓氨水具有挥发性,挥发出的氨气溶于氯化铝溶液,一水合氨与氯化铝反应生成氢氧化铝白色沉淀,故C正确;D.饱和氯水挥发出氯气,氯气与湿润红纸条接触,氯气水反应生成HClO,HClO具有漂白性,使湿润红纸条褪色,故D正确;故答案为A。
含氮有机化合物》练习题

含氮有机化合物》练习题1.下列物质中能发生缩二脲反应的是()。
A.CH3CONHCH2CH3B.C6H5NHCOCH3C.H2NCONH2D.H2NCONHCONH22.不能与亚硝酸作用放出氮气的化合物是( )。
A.乙酰胺B.甲乙胺C.丙氨酸D.尿素3.下列不能发生酰化反应的化合物是()。
A.CH3CH2CH2NH2B.C.CH3CH2N(CH3)2D. 叔丁胺4.下列化合物碱性最强的是()。
A. 尿素B. 氢氧化四甲铵C. 乙胺D.苯胺5.下列化合物属于季铵盐的是()。
6.在碱的溶液中加热,放出的气体可以使湿润的红色石蕊试纸变蓝的是()。
A.苯胺B.苯甲酰胺C.苄胺D.三丙胺7.下列反应属于偶联反应的是()。
A.B.C.8.重氮盐在低温条件下与酚类化合物的偶联反应属于()。
A.亲电取代反应B.亲核取代反应C.亲电加成反应D.亲核加成反应9.反应式的产物是()。
(多选). C. CH3CH2COOH D.CH3COOH10.给下列化合物命名,错误的一组是()。
11.给化合物命名,正确的一组是()。
A.S-1-甲基-1-氨基丙烷B.R-1-甲基-1-氨基丙烷C.S-2-氨基丁烷D.R-2-氨基丁烷12.临床上常用的消毒剂新洁尔灭,从结构式[Ph-CH2-N+(CH3)2C12H25]Br-判断,它是( )。
A.仲胺盐B.叔胺盐C.季铵盐D.季铵碱13.下列胺中,碱性最强的是()。
A.对甲基苯胺B.甲胺C.苯胺D.对硝基苯胺14.溶液中下列化合物碱性最强的是( )。
A.甲胺B.三甲胺C.乙酰胺D.苯胺15.下列化合物中不能发生酰化反应的是()。
16.下列化合物中,与亚硝酸反应产生黄色中性不溶于水的化合物是( )。
17.下列化合物碱性顺序从大到小的顺序正确的是()。
a、b、c、A.a> b> cB.b> a >cC.c> a> bD.a> c > b18.下列化合物的碱性从大到小的顺序正确的是()。
高考化学培优(含解析)之氮及其化合物及答案解析

高考化学培优(含解析)之氮及其化合物及答案解析一、氮及其化合物练习题(含详细答案解析)1.氮氧化合物和二氧化硫是引起雾霾的重要物质,工业用多种方法来治理。
某种综合处理含 NH4+废水和工业废气(主要含 NO、CO、CO2、SO2、N2)的流程如图:已知:NO+NO2+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO3+NaNO2+H2O(1)固体 1 的主要成分有 Ca(OH)2、___________________、__________________(填化学式)。
(2)若实验室需要配制100mL 3.00mol·L-1NaOH溶液进行模拟测试,需用托盘天平称取 NaOH 固体质量为______g。
(3)用 NaNO2溶液处理含NH4+废水反应的离子方程式为_______________________。
(4)捕获剂从气体 3 中捕获的气体主要是__________________ (填化学式)。
(5)流程中生成的 NaNO2 因外观和食盐相似,又有咸味,容易使人误食中毒。
已知 NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O;I2可以使淀粉变蓝。
根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别 NaNO2和 NaCl。
需选用的物质是_____________________(填序号)。
①水②淀粉碘化钾试纸③淀粉④白酒⑤白醋A.①③⑤ B.①②④ C.①②⑤ D.①②③⑤【答案】CaCO3 CaSO3 12 NO2-+ NH4+= N2↑+2H2O CO C【解析】【分析】工业废气通过过量的石灰乳,除去CO2和SO2,生成CaCO3和CaSO3,气体1是NO 、CO 、N2,通入适量的空气,把NO转化为NO2,通过氢氧化钠溶液只得到NaNO2溶液,说明气体2是NO、NO2、N2,气体3是CO和N2,捕获产物是CO,得到的NaNO2溶液和含NH4+废水发生氧化还原反应,得到无污染的气体是氮气。
氮及其化合物知识点及练习题及答案

氮及其化合物知识点及练习题及答案一、选择题1.为了检验某固体物质中是否含有NH;,你认为下列试纸和试剂可用到的是①蒸懈水②NaOH溶液③红色石蕊试纸④蓝色石烷试纸⑤稀硫酸A. ®®④B.②®C.①②③D.①③⑤【答案】C【详解】检验固体物质中的NH;时,为便于反应,通常将固体先溶于水,然后加入强碱溶液、加热,逸出的NH3用湿润的红色石烷试纸检验,所以应选择①②®,故选C。
2.自然界的氮循环如下图所示,下列说法不正确的是()大气中的Y丄城中的微生物------ »A.①中2与。
2反应生成NOB.②中合成氨属于人工固氮C.③中氮元素只被氧化D.氧元素参与了氮循环【答案】C【详解】A.N2和02在放电作用下化合,生成NO, NO被氧化生成NO2, N02溶于水生成硝酸,故A 正确:B.氮的固泄是指氮元素由游离态变为化合态的过程,大气中氮气转化成氮肥属于人工固氮,故B正确;C.③中细菌还原硝酸根中正五价的氮,生成无污染的0价的氮气,所以③中氮元素被还原,而不是被氧化,故C错误:D.如2在放电条件下与02直接化合生成无色且不溶于水的一氧化氮气体,氧元素参与,二氧化氮易与水反应生成硝酸(HNOs)和一氧化氮,3NO2+H2O = 2HNO3+NO,氧元素参加,故D正确:题目要求选不正确的,故选C。
【点睛】本题主要考査了氮以及化合物的性质,理解还原反应、人工固氮等知识点是解答的关键,选项D是解答的易错点。
3.从某些性质来看,地和HO NH「和肛NH「和0H\曾和(T两两类似。
据此判断,下列反应中正确的是()①NH4Cl + NaNH2: NaCl + 2NH. T②CaO + 2NH.CI 1 CaCl2 + 2NH. T +H2O③3Mg(NH4 :Mgs"? +4NH、TA.仅①正确B.②③正确C.①③正确D.全部正确【答案】D【详解】①OH-和NH2-相当,NH3和出0相当,依据NH4CI+NaOH=NaCI+NH3+H2O;类推得到:NH4Cl+NaNH2= NaCI+2NH3.故正确;②NHf和出0+相当,依据CaO+2HCI=CaCl2+H2O,类推得到反应:CaO+2NMCI= CaCl2+2NH3l'+H2O,故正确;③0H-和NH2-相当,N3•和CP-两两相当,依据Mg (OH)2=MgO+H2O,类推得到:3Mg(NH4 二陷心+4NH、T,故正确:因此上述三个反应都能够发生;正确答案D。
备战高考化学易错题精选-氮及其化合物练习题及答案解析

备战高考化学易错题精选-氮及其化合物练习题及答案解析一、氮及其化合物练习题(含详细答案解析)1.氮元素是地球大气中含量最多的元素,请完成下列有关问题:(1)写出氮元素的原子结构示意图:_____________。
(2)通常情况下,氮气性质不活泼,其原因是__________。
A.氮分子是双原子分子 B.氮元素的非金属性很强C.氮原子的半径较小 D.破坏氮分子中的化学键很难(3)N2的电子式:__________,将空气中的氮气转化为氮的化合物的过程称为固氮。
下列能实现人工固氮的是_______A.N2和H2在一定条件下反应生成NH3B.雷雨闪电时空气中的N2和O2化合生成NOC.NH3经过催化氧化生成NOD.NH3和HNO3反应生成NH4NO3(4)氨气的电子式:__________________。
(5)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。
写出此反应的化学方程式______________。
(6)下面是实验室制取氨气的装置和选用的试剂,其中错误的是________。
(7)用圆底烧瓶收集干燥的氨气,用图1装置进行喷泉实验,挤压滴管的胶头时,可以得到红色喷泉,原因(用方程式表示) _________________________。
(8)如果只提供如图2的装置,请说明引发喷泉的方法__________________________。
(9)NH4NO3是常用的铵态氮肥,在施用时若受热会释放出________而降低肥效。
检验NH4+的方法是______。
【答案】 D A Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2OAC NH 3∙H2O NH4++OH−打开止水夹,用手(或热毛巾等)将烧瓶捂热,氨气受热膨胀,赶出玻璃导管内的空气,再将热源移开,水进入烧瓶内,氨气溶解于水中产生压强差,即发生喷泉氨气加入强碱反应,加热能够产生使湿润的红色石蕊试液变蓝的刺激性气体【解析】【分析】(1)氮原子的核电荷数是7;(2)氮气分子为两个氮原子通过共用3对电子形成共价键,该N≡N非常稳定,破坏需要吸收很高的能量,据此解答;(3)N2分子中存在氮氮叁键,将空气中的氮气转化为氮的化合物的过程称为固氮,结合氨元素的形态变化判断即可;(4)氨气是共价化合物,存在3个N-H键;(5)加热消石灰与氯化铵固体得氨气、氯化钙和水;(6)A.NH4Cl固体受热分解生成NH3和HCl,而当温度降低时,NH3和HCl又重新化合成固体NH4Cl;B.CaO遇水生成Ca(OH)2,同时放出大量热量,有利于氨气的生成;C.固体加热制气体时,试管口应略向下倾斜;D.根据浓氨水易挥发分析;(7)氨气极易溶解于水生成NH3•H2O,使烧瓶内压强迅速减小,形成喷泉;(8)喷泉实验需形成明显的压力差;(9)碳酸氢铵不稳定,易分解生成氨气;氨气能使湿润的红色石蕊试纸变蓝色。
《有机化学第四版》习题答案和课件 第15章__有机含氮化合物

15.2.1 胺的分类和命名
命名: ① 习惯命名法:适用于简单胺。
CH3NH2
¬« ¡©
(CH3CH2)2NH
¡¡© « ¡« ª©
NH2
(HOCH2CH2)3N
¡¡¡© «
② 系统命名法:适用于复杂胺。
CH3 NH2 CH3-CH-CH2-CH-CH2-CH3
2-¡¡-4-©¡¡¡ ¬ù ªù é
Zn+NaOH
NH2
¡¡ª ¡ Zn+NaOH
NH-NH
¡¡¡¡ª ¡
第十五章 有机含氮化合物 ③ 选择性还原
or NH4HS ¡ 4)2S2 (NH
Na ¡ 2S2 ¡
NH2 NH2
O2N NO2
OH NO2 NO2
Fe+HCl
NO2 NO2
(NH4)2S
NH2 NO2
OH
OH NO2
Na2S C2H5OH,
第十五章 有机含氮化合物 15.1.4 芳香族硝基化合物的化学性质 (1) 还原 硝基化合物被还原的最终产物是胺。还原剂、介质不同时,还原产物不同。
NO2
[H]
NO
[H]
NHOH
[H]
NH2
硝基苯
亚硝基苯
[H]
N-羟基苯胺
苯胺
[H] :LiAlH4 , H2/Cu , H2/Pt , Fe+HCl , SnCl2+HCl
第十五章 有机含氮化合物 15.1 芳香族硝基化合物 芳环上的一个或多个氢原子被硝基取代后的化合物为芳香族硝基 化合物。例如:
CH3 NO2 CH(CH3)2 2-硝基-4-异丙基甲苯 O 2N NO2 2,4,6-三硝基甲苯 (TNT) 2-硝基萘 CH3 NO2 NO2
含氮有机化合物练习及答案

第十四章含氮有机化合物1. 给出下列化合物名称或写出结构式。
对硝基氯化苄苦味酸 1 ,4,6- 三硝基萘答案:3 -氨基戊烷异丙胺二甲乙胺N -乙基苯胺3 —甲基一N-甲基苯胺2 —氰一4—硝基氯化重氮苯2. 按其碱性的强弱排列下列各组化合物,并说明理由。
(1)(2)答案:(1)吸电子基使碱性降低,供电子基使碱性增强,所以有: b > a > c(2)吸电子基使碱性降低,供电子基使碱性增强,所以有: b > c > a3. 比较正丙醇、正丙胺、甲乙胺、三甲胺和正丁烷的沸点高低并说明理由。
答案:五种化合物中,按形成氢键的可能、能力可推知其沸点从高到低的次序是:正丙醇> 正丙胺> 甲乙胺> 三甲胺> 正丁烷分子间形成分子间氢键沸点高,醇分子中的羟基极性强于胺的官能团,胺三级大于二级又大于一级。
4. 如何完成下列的转变:(1)(2)(3)(4)答案:(1)(2)(3)(4)5. 完成下列各步反应,并指出最后产物的构型是(只)或(S)。
答案:反应的前两步都不涉及到手性碳,反应的第三步为Hofmann重排,转移基团在分子内转移, 其构型保持不变。
由于分子组成而变了,旋光性可能改变,也可能不变,此处测定结果为左旋。
6. 完成下列反应:(1)(3)(4)(5)(6)(7)(8)(9)(10)答案:(1)(注:书中有误,改为)(2)(3)(4)(5)利用Hofmann 重排反应(降级反应)来完成缩碳。
(6)利用卤代烃的氰解来增加一个碳原子。
(7)(8)芳环上的亲核取代反应,先加成后消去。
(9)不对称酮形成烯胺后,再进行烃基化时,烃基化主要发生在取代基较少的a位。
与普通碱催化反应正好相反。
(10)含B-H的氧化叔胺在加热时发生顺式消除反应(协同反应)生成烯烃和R2NOH7. 指出下列重排反应的产物:(1 )( 2 )(4)(5)(6)(7)(8)答案:(1)碳正离子的形成及其重排:(2)碳正离子的形成及其重排:(3)碳正离子的形成及其重排:片呐醇重排反应(4)碳正离子的形成及其重排:片呐醇重排反应(5)碳正离子的形成及其重排:片呐醇重排反应(6)Wolff 重排:(7)Beckmann重排:(8)Baeyer-Villiger 重排:8. 解释下述实验现象:(1)对溴甲苯与氢氧化钠在高温下反应,生成几乎等量的对和间甲苯酚。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十四章 含氮有机化合物1. 给出下列化合物名称或写出结构式。
(CH 3)2CH NH 2(CH 3)2NCH 2CH 3NH CH 2CH 3CH 3NH CH 3O 2NNCN +NCl -O 2NNNOHOHH 3C NH 2HH对硝基氯化苄 苦味酸 1,4,6-三硝基萘 答案:3-氨基戊烷 异丙胺 二甲乙胺 N -乙基苯胺 3-甲基-N -甲基苯胺 2-氰-4-硝基氯化重氮苯O 2NCH 2CLNO 2O 2NNO 2OH NO 2NO 2NO 22. 按其碱性的强弱排列下列各组化合物,并说明理由。
(1)ab c NH 2NH 2NH 2NO 23(2)CH 3CONH 2CH 3NH 2NH 3abc答案:(1)吸电子基使碱性降低,供电子基使碱性增强,所以有:b > a > c(2)吸电子基使碱性降低,供电子基使碱性增强,所以有:b > c > a3.比较正丙醇、正丙胺、甲乙胺、三甲胺和正丁烷的沸点高低并说明理由。
答案:五种化合物中,按形成氢键的可能、能力可推知其沸点从高到低的次序是:正丙醇 > 正丙胺 > 甲乙胺> 三甲胺 > 正丁烷分子间形成分子间氢键沸点高,醇分子中的羟基极性强于胺的官能团,胺三级大于二级又大于一级。
4. 如何完成下列的转变: (1)CH 2CHCH 2Br CH 2CHCH 2NH 2(2)NHCH 3O(3)(CH 3)3CC OHOOC (CH 3)3CCH 2Cl(4)CH 3CH 2CH 2CH 2BrCH 3CH 2CHCH 3NH 2答案: (1)CHCH 2BrCH 2NaCNCH 3CH 2OHCH 2CHCH 2CN LiAlH 4CHCH 2NH 2CH 2(2)ONH 3+(H)NH 2CH 3BrNHCH 3(3)(4)CH 3CH 2CH 2CH 2Br KOH,CH 3CH 2OHCH 3CH 2CH CH 2HBrCH 3CH 2CHCH 3Br 3CH 3CH 2CHCH 3NH 25. 完成下列各步反应,并指出最后产物的构型是(R )或(S )。
C 6H 5CH 2CHCOOHCH 3(1)SOCl (2)NH 3(3)Br 2,OH -C 6H 5CH 2CHNH 2CH 3S-(+)(-)答案:反应的前两步都不涉及到手性碳,反应的第三步为Hofmann 重排,转移基团在分子内转移,其构型保持不变。
由于分子组成而变了,旋光性可能改变,也可能不变,此处测定结果为左旋。
6. 完成下列反应: (1)CH 3N H(1)CH I(过量)(2)Ag 2O,H 2O??(1)CH I (3)加热Ag 2O,H 2O ?(2)CH 32CH 3?(CH 3CO)2O?混酸?H +,H O???NaNO 2(3)CH 3O NH 2CH 3O(4) CH 3CH 2N(CH 3)3Cl+_(5)CH 3O 2NNH 2O 2N(6) CH 3CH 2CH 2NH 2(7)BrNHCO33AcOH?(8)NO 2O 2N F+ H 3CNHH 2NO ?(9)HN +H 3C OH +???CH 2CHCOOEtH +(10)CH3NO-H3CCH3答案:(1)(注:书中有误,改为) (2)(3)(4)(5) 利用Hofmann重排反应(降级反应)来完成缩碳。
(6) 利用卤代烃的氰解来增加一个碳原子。
(7)BrNH NO2C CH3 O(8)芳环上的亲核取代反应,先加成后消去。
(9)不对称酮形成烯胺后,再进行烃基化时,烃基化主要发生在取代基较少的α位。
与普通碱催化反应正好相反。
(10) 含β-H的氧化叔胺在加热时发生顺式消除反应(协同反应)生成烯烃和R2NOH。
CH37. 指出下列重排反应的产物:(1)CH2OH HBr(2)H2C OTOSHOAc(3)C CCH3CH3OHOHH+(4)OHCH3OHCH3H+(5)CH3OHOHCH3H+(6)COOHSOCl2?CH2N22?Ag2OH2O,50-60?(7)OC(CH3)32?HCl?(8) C6H5COCH3CH3CO3H答案:(1)碳正离子的形成及其重排:(2)碳正离子的形成及其重排:(3)碳正离子的形成及其重排:片呐醇重排反应(4)碳正离子的形成及其重排:片呐醇重排反应(5)碳正离子的形成及其重排:片呐醇重排反应(6)Wolff重排:COCl COCHN2l CH2COOH(7)Beckmann重排:C(CH3)3N OH C ONHC(CH3)3(8)Baeyer-Villiger重排:C6H5COCH3O8. 解释下述实验现象:(1)对溴甲苯与氢氧化钠在高温下反应,生成几乎等量的对和间甲苯酚。
(2)2,4-二硝基氯苯可以由氯苯硝化得到,但如果反应产物用碳酸氢钠水溶液洗涤除酸,则得不到产品。
答案:(1)溴苯一般不易发生亲核取代反应,该反应是经过苯炔中间体历程进行的,表示如下:(2) 氯苯可以直接硝化生成2,4-二硝基氯苯,但2,4-二硝基氯苯因两个硝基的吸电子作用,使昨其很易水解,生成2,4-二硝基苯酚,所以得不到2,4-二硝基氯苯的产物。
9. 请判断下述霍夫曼重排反应能否实现,为什么?RCONHCH32-RNHCH3答案:该反应不能实现,因为仲胺分子中N原子上没有两个可被消去的基团,无法形成氮烯中间体,霍夫曼重排反应只能发生在氮原子上无取代的酰胺。
10、从指定原料合成。
(1)从环戊酮和HCN制备环己酮;(2)从1,3-丁二烯合成尼龙-66的两个单体-己二酸和己二胺;(3)由乙醇、甲苯及其他无机试剂合成普鲁卡因(H2N COOCH2CH2NEt2);(4)由简单的开链化合物合成NO2 CH3答案:(1)oHCNOHCN HOCH 2NH 22O(2)2H 2O 2BrBr 2NaCNCN CN Na C 2H 5OHCH 2NH 2CH 2NH 2HOHC OH COHOCOOHCOOH(3)(4)11、选择适当的原料经偶联反应合成:(1)2,2ˊ-二甲基-4-硝基-4ˊ-氨基偶氮苯;(H 3C)2NN NSO 3Na(2)甲基橙(3) 4-叔丁基-4`-羟基偶氮苯答案:(1) 2,2ˊ-二甲基-4-硝基-4ˊ-氨基偶氮苯;(2) 甲基橙(3) 4-叔丁基-4`-羟基偶氮苯12、从甲苯或苯开始合成下列化合物:(1)间氨基苯乙酮(2)邻硝基苯胺(3)间硝基苯甲酸(4)间溴甲苯(5)HOOCOHNO2(6)OHNO2答案:(1)(2)(3)(4)(5)(6)13、试分离PhNH2、PhNHCH3和PH(NH3)2答案:14、某化合物C8H9NO2(A)在氢氧化钠中被Zn还原产生B,在强酸性下B重排生成芳香胺C,C用HNO3处理,再与H3PO2反应生成3,3ˊ-二乙基联苯(D)。
试写出A、B、C和D的结构式。
答案:15、某化合物A,分子式为C8H17N,其核磁共振谱无双重峰,它与2mol碘甲烷反应,然后与Ag2O (湿)作用,接着加热,则生成一个中间体B,其分子式为C10H21N。
B进一步甲基化后与湿的Ag2O 作用,转变为氢氧化物,加热则生成三甲胺,5-辛二烯和1,4-辛二烯混合物。
写出A和B的结构式。
答案:能与两摩尔碘甲烷反应,说明为一个仲胺。
根据产物烯的位置可推知:NMR无双重峰,说明其旁没有单个H。
这句话排除了如下结构式的可能。
16、化合物A分子式为C15H17N用苯磺酰氯和KOH溶液处它没有作用,酸化该化合物得到一清晰的溶液,化合物A的核磁共振谱如下图所示,是推导出化合物A的结构式。
答案:(注:原图可能有误,①在δ值1.2处应为3H,②下边横坐标应为δ/ppm不是τ值)。
化合物分子式为,C15H17N,不饱和度为8,分子中可能含2个苯环。
结合NMR谱图可得化合物A的结构式是:。
