(优选)常见晶胞类型
(完整版)常见晶胞模型

氯化钠晶体离子晶体(1)NaCI晶胞中每个Na+等距离且最近的Cl-(即Na+配位数)为6个(2)(3)NaCI晶胞中每个CI-等距离且最近的Na+(即CI-配位数)一个晶胞内由均摊法计算出一个晶胞内占有的Na+4个; 占有的CI-4个。
在该晶体中每个Na+周围与之最接近且距离相等的Na+ 与每个Na+等距离且最近的CI-所围成的空间几何构型为CsCI晶体(注意:右侧小立方体为CsCI晶胞;左侧为8个晶胞)(1)CsCI晶胞中每个Cs+等距离且最近的C「(即Cs+配位数)为8个CsCI晶胞中每个CI-等距离且最近的Cs+(即CI-配位数)为8个,这几个Cs+在空间构成的几何构型为正方体。
(2)在每个Cs+周围与它最近的且距离相等的Cs+有6个这几个Cs+在空间构成的几何构型为正八面体。
• Cs* OCI- (3)一个晶胞内由均摊法计算出一个晶胞内占有的Cs+ 1个;占有的CI- 1个CaF2晶体(1))Ca2+立方最密堆积,F-填充在全部四面体空隙中。
(2)CaF2晶胞中每个Ca2+等距离且最近的F-(即Ca2+配位数)为8个CaF2晶胞中每个F-等距离且最近的Ca2+(即F-配位数)为4个(3)一个晶胞内由均摊法计算出一个晶胞内占有的Ca2+4个;占有的F-8个。
ZnS晶体:(1)1个ZnS晶胞中,有4 个S2「,有4个Zn2+(2)Zn2+的配位数为4个, S2_的配位数为4个O£n?,•原子晶体(1) 金刚石晶体a 每个金刚石晶胞中含有 8个碳原子,最小的碳环为 6元环,并且不在同一平面(实际为椅 式结构),碳原子为sp 3杂化,每个C 以共价键跟相邻的_4_个 C 结合,形成正四面体。
键角109° 28'b 、 每个碳原子被12个六元环共用,每个共价键被6个六元环共用c 、 12g 金刚石中有2mol 共价键,碳原子与共价键之比为 (2) Si 晶体由于Si 与碳同主族,晶体Si 的结构同金刚石的结构。
常见晶胞类型

4个Ca2+和8个F-
5、决定离子晶体结构的因素
(1)几何因素
晶体中正负离子的半径比. 一般决定配位数的多少:正负离子的半 径比越大,配位数越多.
(2)电荷因素
晶体中正负离子的电荷比. 正负离子电荷比=正负离子的配位数比
金属晶体的堆积方式──钾型
2、体心立方堆积 钾型
配位数:8 空间占有率: 68.02%
由
简非
单 立
密 置 层
方一
堆层
积一
钾型 体心
层 堆 积
立方
而
成
思考:密置层的堆积方式有哪些?
第二层对第一层来讲最紧密的堆积方式是将球对准 1,3,5 位。 ( 或对准 2,4,6 位,其情形是一样的 )
12
6
每个CO2分子周围有多 少个与之最近且等距离
的CO2分子?距离为多 少?(设晶胞边长为a)
12个
a
AD=CD=a/2
AC=AB
=
2a 2
1987年2月,朱经武(Paul Chu)教授等发现钇钡铜氧 化合物在90K温度下即具有 超导性,若该化合物的结构 如右图所示,则该化合物的 化学式可能是( C )
---Cs+ ---Cl-
Cs+的配位数为:8 Cl-的配位数为:8
离子 阴离子的 阳离子的 阴阳离子配 晶体 配位数 配位数 位数的比值
NaCl 6
6
1:1
CsCl 8
8
1:1
CaF2 (萤石)型晶胞(1)立方晶系,面
心立方晶胞。
常见纯金属的晶格类型

常见纯金属的晶格类型
常见金属晶体的晶格类型有:(1)正方晶系;(2)单斜晶系,包括等轴晶系和面心立方晶系;
(3)四方晶系,即一组四个角为120°的平行四边形晶胞。
纯金属中,按照晶胞的大小分为大、中、小三种晶粒尺寸;按照晶体结构可以分为等轴晶系、面心立方晶系、六方晶系、四方晶系、八面体晶系等几种晶格类型。
在单斜晶系中,因为每条棱都是相互垂直的,所以一个晶胞中只能出现两个晶面。
而六方晶系里,由于每条棱都垂直,所以同样一个晶胞中会有6个晶面。
正方晶系中最主要的晶体结构是立方晶胞。
晶胞结构
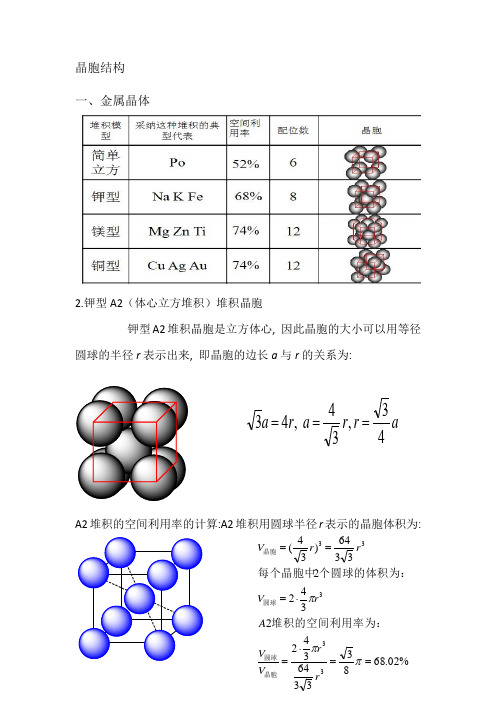
晶胞结构一、金属晶体2.钾型A2(体心立方堆积)堆积晶胞钾型A2堆积晶胞是立方体心, 因此晶胞的大小可以用等径圆球的半径r 表示出来, 即晶胞的边长a 与r 的关系为:A2堆积的空间利用率的计算:A2堆积用圆球半径r 表示的晶胞体积为:ar r a r a 43,34 ,43===%02.68833364342234223364)34(33333==⋅=⋅===πππr r V V A rV rr V 晶胞圆球圆球晶胞堆积的空间利用率为:个圆球的体积为:每个晶胞中3.六方最密堆积(4)A1(面心立方最密堆积)A1是ABCABCABC······型式的堆积,从这种堆积中可以抽出一个立方面心点阵,因此这种堆积型式的最小单位是一个立方面心晶胞。
A1堆积晶胞是立方面心, 因此晶胞的大小可以用等径圆球的半径r 表示出来, 即晶胞的边长a 与r 的关系为:A1堆积空间利用率的计算:A1堆积用圆球半径r 表示的晶胞体积为:(5)A4堆积形成晶胞A4堆积晶胞是立方面心点阵结构, 因此晶胞的大小可以用等径圆球的半径r 表示出来, 即晶胞的边长a 与r 的关系为:A4堆积的空间利用率的计算:A4堆积用圆球半径r 表示的晶胞体积为: ra r a 22 ,42==%05.742312163441344 4216)22(33333==⋅=⋅===πππr r V V A r V r r V 晶胞圆球圆球晶胞堆积的空间利用率为:个圆球的体积为:每个晶胞中ar r a r r a 83,38 ,8243===⨯=%01.34163335123484348 833512)38(33333==⋅=⋅===πππr r V V A r V r r V 晶胞圆球圆球晶胞堆积的空间利用率为:个圆球的体积为:每个晶胞中二、原子晶体1.金刚石立体网状结构,每个碳原子形成4个共价键,任意抽出2个共价键,每两个单键归两个六元环所有,而不是只归一个六元环所有(如图所示,红色的两个碳碳单键,可以构成蓝色和紫红色的两个六元环)。
14种晶体结构

14种晶体结构晶体是由原子、分子或福隔离子按照一定的空间规则排列而成的有序固体。
晶体结构是指晶体中原子、离子或分子排列的规则和顺序。
在固体物质中,晶体结构的种类有很多种,其中比较常见的有以下14种:1. 立方晶体结构:最简单的晶体结构之一,具有三个等长的边和六个等角,包括简单立方、体心立方和面心立方三种类型。
2. 六方晶体结构:其晶胞的基本结构是六方密堆,其中最典型的就是六方晶体和螺旋晶体。
3. 正交晶体结构:晶胞具有三个不相互垂直的晶轴,分别被称为a、b 和c 轴,是最常见的晶体结构之一。
4. 单斜晶体结构:晶胞具有两个不相互垂直的晶轴,是晶体结构中的一种。
5. 三方晶体结构:具有三个相等的轴,夹角为60度,最常见的晶体结构之一是石英。
6. 菱晶体结构:晶胞内部有四面体结构,是一种简单的晶体结构。
7. 钙钛矿晶体结构:一种具有钙钛矿结构的晶体,包括钙钛矿结构和螺旋钙钛矿结构。
8. 蜗牛晶体结构:晶胞的形状像一只蜗牛的壳,是晶体结构中的一种。
9. 立方密排晶体结构:晶胞的结构是立方密排,是晶体结构中的一种。
10. 体心立方晶体结构:晶体结构的晶胞中有一个原子位于晶体的中心,是晶体结构中的一种。
11. 面心立方晶体结构:晶体结构的晶胞的各个面的中心有一个原子,是晶体结构中的一种。
12. 钻石晶体结构:晶体结构的晶胞构成了一种钻石结构,是晶体结构中的一种。
13. 银晶体结构:晶体结构的晶胞构成了一种银结构,是晶体结构中的一种。
14. 锶钛矿晶体结构:晶体结构的晶胞构成了一种锶钛矿结构,是晶体结构中的一种。
晶体结构的种类繁多,每种晶体结构都有其独特的结构特点和性质,对晶体的物理和化学性质有着重要的影响。
研究晶体结构不仅可以帮助我们更好地了解晶体的构成和性质,还有助于我们在材料科学、物理化学等领域的应用和研究。
因此,对晶体结构的研究具有重要的科学意义和应用价值。
晶胞结构类型范文

晶胞结构类型范文晶胞结构是指固体晶体中原子、离子或分子的排列方式和对称性。
根据结构的不同,晶胞结构可分为离子晶体、共价晶体、分子晶体、金属晶体和非晶态材料等几种类型。
1.离子晶体:离子晶体是由正、负电离子通过静电力相互结合形成的晶体。
例如氯化钠(NaCl)晶体,其中钠、氯离子通过离子键相互结合。
离子晶体的晶胞结构一般为六方密堆积结构、立方密堆积结构或钠氯结构。
离子晶体具有高熔点、可导电性等特点。
2.共价晶体:共价晶体是由共价键相互连接的原子构成的晶体。
共价晶体的晶胞结构多种多样,例如钻石(C)晶体由碳原子通过共价键形成的长方体晶胞结构。
共价晶体具有高硬度、高熔点和热稳定性较好等特点。
3.分子晶体:分子晶体是由分子相互结合而构成的晶体。
在分子晶体中,分子之间通过分子间力相互结合,例如氯化铭(NH4Cl)晶体,其中氨气分子和氯化氢分子通过氢键相互结合。
分子晶体的晶胞结构多样,如六方密堆积、正交晶系等。
分子晶体具有低熔点、不导电等特点。
4.金属晶体:金属晶体是由金属原子通过金属键相互连接而成的晶体。
金属晶体的晶胞结构主要有面心立方晶体、体心立方晶体和简单立方晶体。
例如铜(Cu)晶体为面心立方晶体结构。
金属晶体具有高热导率、良好的延展性和塑性等特点。
5.非晶态材料:非晶态材料是一种没有长程有序排列的晶体形态。
在非晶态材料中,原子、离子或分子的排列方式呈无规则的非周期性分布。
非晶态材料的晶胞结构不规则且无序。
非晶态材料具有无定型、不规则等特点,如玻璃材料。
总之,晶胞结构类型多种多样,每种类型都具有自己独特的结构特点和性质。
研究和理解晶胞结构对于材料科学和物理化学的发展具有重要意义。
《常见晶胞类型》PPT课件

12
6
3
54
12
6354,源自AB关键是第三层,对第一、二层来说,第三层可以有两种最紧
密的堆积方式。
.
17
第一种是将球对准第一层的球。 下图是此种六方 紧密堆积的前视图
12
A
6
3
54
B
A
于是每两层形成一个周期,
B
即 AB AB 堆积方式,形成六
A
方紧密堆积。
配位数 12 。 ( 同层 6,上下层. 各 3 )
Cu 8×(1/8) + 8×(1/4) = 3
.
Y1
1/8
Cu铜 Ba钡 Y钇 O氧
38
CsCl晶体
在氯化铯晶体中,每个Cl-(或Cs+)周围与之最接近
且距离相等的Cs+(或Cl-)共有 8个 ;这几个Cs+(或 Cl-)在空间构成的几何构型为 立方体 ;在每个Cs+
周围距离相等且最近的Cs+共有 6 个 ;这几个
Cs+(或Cl-)在空间构成的几. 何构型为
正八面体; 39
每个CO2分子周围有多 少个与之最近且等距离
C
B
12
6
3
54
配位数 12 。 ( 同层 6, 上下层各 3 )
A C B A
此. 种立方紧密堆积的前视图 22
A B A
镁型
C B A
铜型
金属晶体的两种最密堆积方式
.
23
金属晶体的原子空间堆积模型4
• 面心立方 (铜型)
.
24
简 单 立 方
(
六
方 密 堆
镁 型
积
)
高三化学课件常见的晶胞模型

(4)设金属原子的摩尔质量为M g/mol,
则晶胞密度ρ为
体心六方晶胞
g/cm3
/
n
m
ρ=
=
−7 3 =
−
(×10 )
(×10 7)3
Hale Waihona Puke 2×10213=
g/cm
3
二、金属晶体
3、面心立方最密堆积(A 1 型或铜型)
典型代表 Ca Al Cu Ag Au Pd Pt
(4)金属镁形成的晶体中,每个镁原子周围与其距离最近的原子有6个。(×)
三、分子晶体
1、干冰(CO 2 )
2、冰(H 2 O)
3、碘晶体
(1)每个水分子最多与相邻的4个水分子,以氢键相连接
(2)含1 mol H2O的冰中,最多可形成2 mol“氢键”
碘晶体晶胞(长方体)
(3)1 mol液态水中氢键数小于2NA
四、离子晶体
1、氯化钠(型)
(1)每个晶胞中含4个Na+和4个Cl-
(2)每个Na+(Cl-)周围等距且紧邻的Cl-(Na+)有6个
每个Na+周围等距且紧邻的Na+有12个
ClNa+
在氯化钠晶胞中,
与每个Na+等距离且最近的几个Cl-所围成的空间几何构型为 正八面体
四、离子晶体
2、氯化铯(型)
则a=2r
简单六方晶胞
V球=
4
3
πr3 V晶胞=a3
空间利用率=V球/V晶胞×100%=52%
二、金属晶体
2、体心六方堆积(A 2 型或钾型)
典型代表 Li Na K Ba W Fe
(1)晶胞内含原子个数为 2
(2)配位数为 8
常见晶胞类型4

每个CO2分子周围有多少 个与之最近且等距离的
CO2分子?距离为多少? (设晶胞边长为a)
12个
a
AD=CD=a/2
AC=AB
=
2a 2
实用文档
1987年2月,朱经武 (Paul Chu)教授等发现 钇钡铜氧化合物在90K温度 下即具有超导性,若该化合 物的结构如右图所示,则该 化合物的化学式可C能是 ()
B
即 AB AB 堆积方式,形成六
A
方紧密堆积。
配位数 12 。 ( 同层 6,上实下用文层档各 3 )
金属晶体的原子空间堆积模型 3
• 六方密堆积(镁型)
实用文档
六方密堆积
实用文档
பைடு நூலகம்
第三层的另一种排列 方式,是将球对准第一层 的 2,4,6 位,不同于 AB 两层的位置,这是 C 层。
12
6
3
常见晶胞类型
实用文档
1、一个干冰晶胞中平均有几个CO2分子? 2、与一个CO2分子距离最近且相等的CO2分子共 有多少个?
实用文档
分子的密堆积
每个二氧化碳分子周围实用文有档 12个二氧化碳分子。
分子的密堆积
氧(O2)的晶体结构
碳60的晶胞
(与每个分子距离最近的相同分子共有12个 )
实用文档
冰晶体
54
12
6
3
54
实用文档
12
6
3
54
第四层再排 A,于是形
A
成 ABC ABC 三层一个周
《常见晶胞类型》课件

晶胞与晶体结构的关系
01
晶胞的形状和内部结构决定了晶 体结构的对称性和空间排列规律 。
02
通过研究晶胞的结构特点,可以 了解晶体的物理性质和化学性质 ,如熔点、导电性、光学性质等 。
常见晶胞类型的特性
01
02
03
简单立方
具有八个顶点,每个顶点 上都有一个原子或分子。
面心立方
具有六个面,每个面上都 有一个原子或分子。
个稳定的四面体结构。
每个原子的配位数为4,即每个 原子与四个相邻原子形成共价键
。
原子间的距离和键角是固定的, 保证了晶胞的稳定性和对称性。
闪锌矿型晶胞的几何特征
闪锌矿型晶胞具有立方晶系结构,其 晶格常数为a=b=c,α=β=γ=90°。
原子间的距离和键角是固定的,保证 了晶胞的稳定性和对称性。
每个面心有一个原子,每个顶点被四 个原子所共享。
是晶胞的角度。
空间群
密排六方晶胞属于P63/mmc空间 群,具有高度的对称性。
原子间距
在密排六方晶胞中,原子间距相等 ,且与晶胞的边长成比例。
05
CATALOGUE
氯化钠型晶胞
定义与特性
定义
氯化钠型晶胞是一种离子晶体结构,由阳离子和阴离子按一定的规律排列而成,具有较高的离子电导 率和热稳定性。
特性
闪锌矿型晶胞是一种立方晶系 结构,其特点是每个顶点被四 个原子所共享,每个面心有一 个原子。
闪锌矿型晶胞具有较高的对称 性,其晶格常数为a=b=c, α=β=γ=90°。
闪锌矿型晶胞的原子排列紧密 ,具有较高的密度和稳定性。
原子排列与配位数
在闪锌矿型晶胞中,每个原子被 其他四个原子所包围,形成了一
《常见晶胞类型》 ppt课件
晶胞结构知识点总结

晶胞结构知识点总结晶体是一种具有高度有序内部结构的固体材料,其结构可以通过晶胞结构来描述。
晶胞结构是描述晶体内部原子或分子排列方式的一种方法,它可以直观地展示晶体的周期性结构。
掌握晶胞结构对于理解材料的性质、制备和应用具有重要意义。
本文将就晶胞结构的相关知识点进行总结,包括晶体的定义、晶格、晶胞的种类、晶胞的参数和晶体的分类等内容。
一、晶体的定义晶体是由原子、离子或分子按照一定规则组成的固体结构。
晶体的最显著特征是其内部结构具有高度的有序性,这种有序性可以在三维空间中进行周期性重复。
晶体的结构稳定,且具有独特的电学、光学、机械以及热学性质。
由于晶体的周期性结构,它在X射线、电子衍射等技术下会出现特征性的衍射花样,从而可以用于晶体结构分析和确定。
二、晶格晶格是描述晶体内部结构的基本概念,它是指在三维空间中由重复排列的点所构成的结构。
这些点代表着原子、离子或分子的位置,具有固定的空间关系。
晶格具有周期性,在晶体内部重复出现,形成了晶体的内部结构。
晶格中最小的重复单元被称为晶胞。
晶格和晶胞是密不可分的概念,通过晶格可以确定晶胞的形状和尺寸,通过晶胞可以推导出整个晶格的结构。
晶格和晶胞的概念为我们理解晶体的结构和性质提供了基础。
三、晶胞的种类根据晶体内部原子或分子的排列方式,晶胞可以分为立方晶胞、四方晶胞、单斜晶胞、正交晶胞、六角晶胞和三角晶胞六种类型。
1. 立方晶胞:所有边长相等,所有角均为90度,包括简单立方、体心立方和面心立方三种类型。
2. 四方晶胞:其中两个边长相等,与第三个边垂直,所有角均为90度,只有一种类型。
3. 单斜晶胞:所有边长不相等,夹角不为90度,只有一种类型。
4. 正交晶胞:其中两个边长相等,夹角为90度,只有一种类型。
5. 六角晶胞:所有边长相等,两个内角为60度,第三个内角为120度,只有一种类型。
6. 三角晶胞:所有边长相等,三个内角均为60度,只有一种类型。
不同类型的晶胞代表了不同的晶格结构,通过对晶胞的特性进行分析,可以了解晶体的空间排列规律,从而推导出晶体的一些性质。
高中化学常见晶胞类型

高中化学常见晶胞类型
1. 立方晶胞:具有三个相等的边长和90度的角度,分为简单立方晶胞、面心立方晶胞和体心立方晶胞。
2. 正交晶胞:具有三个不相等的边长和90度的角度,分为基本正交晶胞和体心正交晶胞。
3. 单斜晶胞:具有两个相等的边长和90度的角度,一个不等的边长和不等的角度,分为基本单斜晶胞和简单单斜晶胞。
4. 正交二斜晶胞:具有三个不相等的边长和不等的角度,分为基本正交二斜晶胞和简单正交二斜晶胞。
5. 六方晶胞:具有三个相等的边长和120度的角度,一共有四种晶胞形式。
6. 四方晶胞:具有两个相等的边长和90度的角度,一个不等的边长和不等的角度,常见的晶胞形式有两种。
7. 三斜晶胞:具有三个不相等的边长和不等的角度,其中一种形式被称为"菱房晶胞"。
(完整版)常见晶胞模型

氯化钠晶体(1)NaCl晶胞中每个Na+等距离且最近的Cl-(即Na+配位数)为6个NaCl晶胞中每个Cl-等距离且最近的Na+(即Cl-配位数)为6个(2)一个晶胞内由均摊法计算出一个晶胞内占有的Na+4_个;占有的Cl-4个。
(3)在该晶体中每个Na+周围与之最接近且距离相等的Na+共有12个;与每个Na+等距离且最近的Cl-所围成的空间几何构型为正八面体CsCl晶体(注意:右侧小立方体为CsCl晶胞;左侧为8个晶胞)(1)CsCl晶胞中每个Cs+等距离且最近的Cl-(即Cs+配位数)为8个CsCl晶胞中每个Cl-等距离且最近的Cs+(即Cl-配位数)为8个,这几个Cs+在空间构成的几何构型为正方体。
(2)在每个Cs+周围与它最近的且距离相等的Cs+有6个这几个Cs+在空间构成的几何构型为正八面体。
(3)一个晶胞内由均摊法计算出一个晶胞内占有的Cs+ 1个;占有的Cl- 1个。
CaF2晶体(1))Ca2+立方最密堆积,F-填充在全部四面体空隙中。
(2)CaF2晶胞中每个Ca2+等距离且最近的F-(即Ca2+配位数)为8个CaF2晶胞中每个F-等距离且最近的Ca2+(即F-配位数)为4个(3)一个晶胞内由均摊法计算出一个晶胞内占有的Ca2+4个;占有的F-8个。
ZnS晶体:(1)1个ZnS晶胞中,有4个S2-,有4个Zn2+。
(2)Zn2+的配位数为4个,S2-的配位数为 4个。
Si O金刚石 金刚石晶胞 金刚石晶胞分位置注释(1)金刚石晶体a 、每个金刚石晶胞中含有8个碳原子,最小的碳环为6元环,并且不在同一平面(实际为椅 式结构),碳原子为sp 3杂化,每个C 以共价键跟相邻的_4_个C 结合,形成正四面体。
键角109°28’b 、每个碳原子被12个六元环共用,每个共价键被6个六元环共用c 、12g 金刚石中有2mol 共价键,碳原子与共价键之比为 1:2 (2)Si 晶体由于Si 与碳同主族,晶体Si 的结构同金刚石的结构。
大学化学 常见晶胞模型

大学化学常见晶胞模型介绍晶胞模型是研究固体结构和晶体性质的基础。
本文将介绍几种常见的晶胞模型,帮助大学化学研究者更好地理解晶体结构和性质。
简单立方模型简单立方模型是一种简化的晶胞模型,用于描述一些简单的晶体结构。
它由八个立方角共享的原子构成。
每个原子都与六个相邻原子相连,形成一个立方结构。
这种简单的晶体结构适用于一些金属元素,如铁、钠等。
面心立方模型面心立方模型是一种常见的晶胞模型,常用于描述许多金属和化合物的结构。
它由八个立方角共享的原子和每个面上一个原子构成。
每个原子都与十二个相邻原子相连,形成一个紧密堆积的结构。
这种晶体结构具有较高的密度和机械强度。
体心立方模型体心立方模型也是一种常见的晶胞模型,常用于描述一些金属元素和化合物的结构。
它由八个立方角共享的原子和一个位于晶胞中心的原子构成。
每个原子都与八个相邻原子相连,形成一个更紧密的结构。
这种晶体结构同样具有较高的密度和机械强度。
面心体心立方模型面心体心立方模型是一种较复杂的晶胞模型,常用于描述一些化合物的结构。
它由八个立方角共享的原子、每个面上一个原子和一个位于晶胞中心的原子构成。
每个原子都与十四个相邻原子相连,形成一个更加紧密的结构。
这种晶体结构具有更高的密度和较好的热力学性质。
总结通过了解这几种常见的晶胞模型,我们可以更好地理解不同结构的晶体的特点和性质。
化学研究者可以通过进一步研究这些模型,扩展对晶胞结构和晶体性质的认识。
以上即为大学化学常见晶胞模型的介绍。
---注意:以上内容为简化表述,不涉及具体晶胞参数和具体晶体结构的分析。
十四种晶格类型

十四种晶格类型晶格是指晶体中原子、离子或分子的排列方式。
根据晶体中原子的排列方式和对称性,晶体可以分为不同的晶格类型。
下面将介绍十四种常见的晶格类型。
1. 简单立方晶格:原子在三个坐标轴上等间距排列,如钠、铜等金属。
2. 面心立方晶格:除了在立方体的顶点上有原子外,每个面的中心也有一个原子,如铝、铜、银等金属。
3. 体心立方晶格:除了在立方体的顶点上有原子外,立方体的中心也有一个原子,如铁、钨等金属。
4. 六方晶格:原子在六个等间距的平面上排列,如硫、石英等。
5. 斜方晶格:原子在三个坐标轴上等间距排列,但其中两个轴之间的夹角不为90度,如二硫化钼。
6. 正交晶格:原子在三个坐标轴上等间距排列,且三个轴之间的夹角均为90度,如钙钛矿。
7. 三方晶格:原子在三个坐标轴上等间距排列,其中两个轴之间的夹角为90度,而第三个轴的夹角为120度,如石墨。
8. 单斜晶格:原子在三个坐标轴上等间距排列,其中两个轴之间的夹角为90度,而第三个轴的夹角不为90度,如硫酸铜。
9. 三斜晶格:原子在三个坐标轴上等间距排列,其中三个轴之间的夹角均不为90度,如石膏。
10. 钻石晶格:原子在三个坐标轴上等间距排列,其中两个轴之间的夹角为90度,而第三个轴的夹角为120度,如金刚石。
11. 锗晶格:原子在三个坐标轴上等间距排列,其中两个轴之间的夹角为90度,而第三个轴的夹角为109.5度,如锗。
12. 铁素体晶格:原子在三个坐标轴上等间距排列,其中两个轴之间的夹角为90度,而第三个轴的夹角为120度,如铁素体。
13. 铁磁晶格:原子在三个坐标轴上等间距排列,其中两个轴之间的夹角为90度,而第三个轴的夹角为120度,如铁磁体。
14. 铁电晶格:原子在三个坐标轴上等间距排列,其中两个轴之间的夹角为90度,而第三个轴的夹角为120度,如铁电体。
这些晶格类型在材料科学、物理学和化学等领域中具有重要的应用价值。
通过研究晶格类型,可以深入了解晶体的结构和性质,为材料的设计和制备提供指导。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
思考:金属原子在形成晶体时有几种堆积方式? 比较不同方式堆积时金属晶体的配位数、原子的 空间利用率、晶胞的区别。
金属晶体的原子空间堆积模型1
• 简单立方堆积(Po)
晶胞的形状是什么? 含几个原子?
1、简单立方堆积 钋型
金属晶体的原子空间堆积模型2
• 体心立方堆积( IA,VB,VIB)
(优选)常见晶胞类型
1、一个干冰晶胞中平均有几个CO2分子? 2、与一个CO2分子距离最近且相等的CO2分子 共有多少个?
分子的密堆积
每个二氧化碳分子周围有12个二氧化碳分子。
分子的密堆积
氧(O2)的晶体结构
碳60的晶胞
(与每个分子距离最近的相同分子共有12个 )
冰晶体
分子的非密堆积
冰中1个水分子周围有4个水分子
②F-的配位数: 4 CaF2晶体中Ca2+ 和F-的位置关系如何?一 个CaF2晶胞中含Ca2+ 、F-个数是多少?
4个Ca2+和8个F-
5、决定离子晶体结构的因素
(1)几何因素
晶体中正负离子的半径比. 一般决定配位数的多少:正负离子的半 径比越大,配位数越多.
(2)电荷因素
晶体中正负离子的电荷比. 正负离子电荷比=正负离子的配位数比
NaCl晶胞
图3—27
CsCl晶胞
① 在NaCl晶体中,与Na+(Cl-)等距离且最 近的Cl-(Na+)有几个?
② 在CsCl晶体中,与Cs+(Cl-)等距离且最 近的Cl-(Cs+)有几个?
NaCl晶体中阴、阳离子的配位数
Na+的配位数为:6 Cl-的配位数为:6
CsCl的晶体结构示意 图
=正负离子的数目反比
(3)键性因素
离子键的纯粹因素
晶体中微粒的排列、个数及密度的计算
在氯化钠晶体中, 每个Na+周围与 之最接近且距离 相等的Cl-共有 个;6 这几个Cl-在 空间构成的几何 构型 为 正八面体 。
CsCl晶体
在氯化铯晶体中,每个Cl-(或Cs+)周围与之最接近 且距离相等的Cs+(或Cl-)共有 8个 ;这几个Cs+(或 Cl-)在空间构成的几何构型为 立方体 ;在每个Cs+ 周围距离相等且最近的Cs+共有 6 个 ;这几个 Cs+(或Cl-)在空间构成的几何构型为 正八面体;
A C B A
此种立方紧密堆积的前视图
A B A
镁型
C B A
铜型
金属晶体的两种最密堆积方式
金属晶体的原子空间堆积模型4
• 面心立方 (铜型)
简 单 立 方
(
六
方 密 堆
镁 型
积
)
( 体 心 立钾 方型 堆 积 ) ( 面 心 立 方铜 最型 密 堆 积 )
金属晶体的四种堆积模型对比
4、几种常见的离子晶体的晶胞结构:
冰的结构
晶体结构 晶胞示意图
Si
O
180º
109º28´
共价键
• 二氧化硅晶体中 • 每个硅原子周围结合4个氧原子;同时
每个氧原子跟2个硅原子相结合, • 晶体中硅氧原子个数比为1:2。 • 1mol二氧化硅中含有Si-O共价键————
五、金属晶体的原子堆积模型
金属原子在平面上有几种排列方式?
82
4
(2)CsCl晶胞
Cl-
铯离子和氯离子的位置? Cs+ 铯离子:体心
氯离子:顶点 或者反之
每个晶胞含铯离子、氯离 子的个数? 铯离子:1个; 氯离子:1个。
NaCl晶胞
图3—27
CsCl晶胞
重点研究晶体中的配位数: 【在离子晶体中离子的配位数(缩写为 C.N.)是指一个离子周围最邻近的异电性 离子的数目】。
每个CO2分子周围有多 少个与之最近且等距离
的CO2分子?距离为多 少?(设晶胞边长为a)
12个
a
AD=CD=a/2
AC=AB
=
2a 2
1987年2月,朱经武(Paul Chu)教授等发现钇钡铜氧 化合物在90K温度下即具有 超导性,若该化合物的结构 如右图所示,则该化合物的 化学式可能是( C )
金属晶体的堆积方式──钾型
2、体心立方堆积 钾型
配位数:8 空间占有率: 68.02%
由
简非
单 立
密 置 层
方一
堆层
积一
钾型 体心
层 堆 积
立方
而
成
思考:密置层的堆积方式有哪些?
第二层对第一层来讲最紧密的堆积方式是将球对准 1,3,5 位。 ( 或对准 2,4,6 位,其情形是一样的 )
12
6
A. YBa2CuO7-X B. YBa2Cu2O7-X C. YBa2Cu3O7-X D. YBa2Cu4O7-X
Cu 8×(1/8) + 8×(1/4) = 3
Y1
1/8
Cu铜 Ba钡 Y钇 O氧
Ba 2
金刚石和石墨最小的环为 几元环?碳碳键的键角为多 少?
每个环上的碳为三个环共有,故每个环占有2个碳
(1)氯化钠型晶胞
Na+ Cl-
钠离子和氯离子在晶胞中的位置:
氯离子:体心和棱中点; 钠离子:面心和顶点.
或者反之;交错排列
每个NaCl晶胞含Na+、Cl-的个数?
Na+ Cl-
计算方法:均摊法
顶点占1/8;棱占1/4;面心占1/2;体心占1
Na+:8 1 6 1 4 Cl-:12 1 1 4
每个碳连有三个键,每个键为两个碳共有,故每个 碳占有3/2个键
Wg石墨中碳原子数为 (W/12) × NA_碳环数为 _(W/12) ×1/2 × NA ;;碳碳单键数为_ _(W/12) ×3/2 × N;A 三者之比为_2:1:3_。
3
54
12
6
3
54
,
AB
关键是第三层,对第一、二层来说,第三层可以有两种最紧 密的堆积方式。
第一种是将球对准第一层的球。 下图是此种六方 紧密堆积的前视图
12
A
6
3
54
B
A
于是每两层形成一个周期,
B
即 AB AB 堆积方式,形成六
A
方紧密堆积。
配位数 12 。 ( 同层 6,上下层各 3 )
金属晶体的原子空间堆积模型3
---Cs+ ---Cl-
Cs+的配位数为:8 Cl-的配位数为:8
离子 阴离子的 阳离子的 阴阳离子配 晶体 配位数 配位数 位数的比值
NaCl 6
6
1:1
CsCl 8
8
1:1
CaF2 (萤石)型晶胞(1)立方晶系,面
心立方晶胞。
(2) Ca2+立方最密 堆积,F-填充在全部 四面体空隙中。
(3)配位数 ①Ca2+的配位数: 8
• 六方密堆积(镁型)
六方密堆积
第三层的另一种排列 方式,是将球对准第一层 的 2,4,6 位,不同于 AB 两层的位置,这是 C 层。
12
6
3
54
12
6
3
54
12
6
3
54
第四层再排 A,于是形
A
成 ABC ABC 三层一个周
期。 得到面心立方堆积。
C
B
12
6
3
54
配位数 12 。 ( 同层 6, 上下层各 3 )
