物理化学第二章热力学第二定律练习题及答案
物理化学 第二章 热力学第二定律 练习题

热力学第二定律
解决的问题
物理变化和化学变化
过程中方向和限度问题
基本要求及主要公式 自发过程的共同特征—不可逆性,由此 引出第二定律的经验表述 一.第二定律的经验表述 1.克劳修斯说法:不能把热从低温物体传到 高温物体而不引起任何变化。 2.开尔文说法:不能从单一热源取热使之全 部变为功而不引起任何变化。或第二类永 动机是根本造不成的。
4.为了计算绝热不可逆过程的熵变,可在始
末态间设计一条绝热可逆途径来计算。 (×) 5.平衡态熵最大。 (× )
6.冰在0℃,101.325kPa下,转化为液态水, 其熵变△S=△H/T>0,所以该过程为自发 过程。 (× )
7.在等温等压下,吉布斯函数的改变量大于
零化学变化都不能进行。 (× )
p1 p2
若理想气体上式为△G=nRT㏑p2/p1
四、热力学函数的数学表达式 封闭体系,非体积功为零,可逆过程 dU=TdS-pdV
dH=TdS+Vdp
dA=-SdT-pdV dG=-SdT+Vdp
练 习 题
一、判断题 以下说法对吗? 1.自发过程一定是不可逆过程 (√)
2.熵增加过程一定是自发过程。 (×) 3.绝热可逆过程的△S=0,绝热不可逆过程 的△S>0。 (√)
(3)熵 (4)吉布斯函数 (3)
4.1mol理想气体经一等温可逆压缩过程,则 (1)△G>△A (2)△G<△A (3)△G=△A (4)无法比较 (3)
A U T S等Biblioteka 过程: G H T S
U 0
H 0
在相同的始终态之间:△S相等
G A
5.熵变的计算 (1)封闭体系简单状态变化 a、等温可逆 △S=QR/T b、等容过程 c、等压过程
物理化学习题2-热力学第二定律

物理化学测验(二)2003-04-12一、填空题。
在题中“____”处填上答案。
1、(本小题1分)公式的适用条件是 , 。
2、(本小题1分)理想气体节流膨胀时, 0。
(选填 >,=,<) 3、(本小题2分)按系统与环境之间物质及能量的传递情况,系统可分为 系统、 系统、 系统。
4、(本小题2分)已知∆f H (FeO , s , 298 K) =-226.5 kJ ·mol -1; ∆f H (CO 2 , g , 298 K) =-393.51 kJ ·mol -1; ∆f H (Fe 2O 3 , s , 298 K) =-821.32 kJ ·mol -1; ∆f H (CO , g , 298 K) =-110.54 kJ ·mol -1;则 Fe 2O 3(s) + CO(g) == 2FeO(s) + CO 2(g)反应的∆r H (298 K) = 。
5、(本小题2分)某气体的C p ,m = 29.16 J ·K -1·mol -1,1 mol 该气体在等压下,温度由20℃变为10℃,则其熵变∆S = 。
6、(本小题2分)绝热不可逆膨胀过程系统的∆S 0,绝热不可逆压缩过程系统的∆S 0。
(选填 >,< 或 = )7、(本小题5分)5 mol 某理想气体由27℃,10 kPa 恒温可逆压缩到100 kPa ,则该过程的∆U = ,∆H = ,Q = ,∆S = 。
8、(本小题2分)公式∆A=W’的适用条件是 , 。
9、(本小题2分)1 mol 理想气体在绝热条件下向真空膨胀至体积变为原体积的10倍,则此过程的∆S = 。
10、(本小题2分)一绝热气缸带有一无磨擦无质量的活塞,内装理想气体,气缸内壁绕有电阻为R 的电阻丝,以电流I 通电加热,气体慢慢膨胀,这是一个 过程,当通电时间t 后,∆H = 。
热力学第二定律习题

(2) 此过程的始、终态与(1)过程相同,所以 ΔUm、ΔHm、ΔFm、ΔGm、ΔSm 皆与(1)相同。 ∆U = 0, ∆H = 0, ∆Gm = 4443J, ∆S m = −14.90J ⋅ K −1 ∆Fm = −4443J, ∆Sm = 0 nRT nRT Q = W = p ⋅ ∆V = p − = −12.40kJ p1 p2 12400 ∆S = ∆S体 + ∆S环 = −14.90 + = 26.68J ⋅ K −1 298.2 7. 在中等的压力下,气体的物态方程可以写作pV(1一βp)=nRT,式中系数β与气体的 本性和温度有关。 今若在273 K 时,将 0.5 mol O2由1013.25 kPa 的压力减到101.325 kPa,试求ΔG。己知氧的β=-9.277×10-9 Pa-1 (原题β=-0.00094,压力单位为atm)。 解: ∆G = ∫ Vdp = ∫
物理化学习题解答
p1 p2
1− r
T = 2 , r = 1.4, 解之T2 = 497.5K T
T2
r
∆U m = ∫ CV ,m dT = CV .m (T2 − T1 ) = 4142J ⋅ mol−1
T1
∆H m = ∫ C p ,m dT = C p, m ∆T = 5799J ⋅ mol−1
−1
代入数据得: 2.
∆S = −86.67J ⋅ K
0.10 kg 283.2 K 的水与 0.20 kg 313.2 K 的水混合,求 ΔS。设水的平均比热为 4.184
kJ ⋅ K-l ⋅ kg-1。 解: 设混合后水的温度为 T,则 C p (T − T1 ) = −C ' p (T − T2 ) 代入数据求得 T=303.2K 水的熵变为: ∆S1 = ∫
物理化学热二律练习题

热力学第二定律练习题1.关于热力学第二定律,下列说法不正确的是:A. 第二类永动机是不可能制造出来的B. 把热从低温物体传到高温物体,不引起其它变化 是不可能的C. 一切实际过程都是热力学不可逆过程D. 功可以全部转化为热,但热一定不能全部转化为功2.应用克劳修斯不等式 Q dS T δ≥环判断,下列不正确的是: A.QdS T δ=环必为可逆过程或处于平衡状态 B.Q dS T δ>环必为不可逆过程 C.Q dS T δ>环必为自发过程 D.QdS T δ<环违反卡诺定理和第二定律,过程不可能发生3.下列计算熵变公式中,错误的是:A. 水在25℃、p ө下蒸发为水蒸气:T G H S Δ−Δ=Δ B. 任意可逆过程: RT Q δdS ⎟⎠⎞⎜⎝⎛= C. 环境的熵变:环体系环境T Q S −=ΔD. 在等温等压下,可逆电池反应:T H S Δ=Δ4.一理想气体与温度为T 的热源接触,分别做 等温可逆膨胀和等温不可逆膨胀到达同一终态, 已知 ,下列式子中不正确的是:Ir R 2W W =A.B .Ir R S S Δ>ΔIr R S S Δ=ΔC. T Q S Ir R 2=Δ D. (等温可逆)总S Δ0=Δ+Δ=环体S S 总S Δ(等温不可逆)0>Δ+Δ=环体S S5.在一定速度下发生变化的孤立体系,其总熵的变化:A .不变 B. 可能增大或减小C .总是增大 D. 总是减小6.某系统经历一个不可逆循环后,下列正确的是A. ΔS体>0,ΔS环>0B. ΔS体=0,ΔS环=0C. ΔS体>0,ΔS环=0D. ΔS体=0,ΔS环>07.一定量理想气体经绝热恒外压压缩至终态,这时系统和环境的熵变应为A. ΔS体>0,ΔS环>0B. ΔS体<0,ΔS环<0C. ΔS体>0,ΔS环=0D. ΔS体<0,ΔS环=08.实际气体CO2经节流膨胀后温度下降,则:A. ∆S(体) > 0,∆S(环) > 0B. ∆S(体) < 0,∆S(环) > 0C. ∆S(体) > 0,∆S(环) = 0D. ∆S(体) < 0,∆S(环) = 09.实际气体进行绝热自由膨胀,ΔU和ΔS的变化为A. ΔU=0,ΔS>0B. ΔU<0,ΔS<0C. ΔU=0,ΔS=0D. ΔU>0,ΔS>010.1mol理想气体从p1、V1、T1分别经:(a) 绝热可逆膨胀到p2、V2、T2;(b) 绝热恒外压膨胀到p3、V3、T3,若p2 = p3,则A. T3=T2,V3=V2,S3=S2B. T3>T2,V3<V2,S3<S2C. T3>T2,V3>V2,S3>S2D. T3<T2,V3>V2,S3<S211.n mol某气体的恒容下由T1加热到T2,其熵变为ΔS1,相同量的气体在恒压下由T1加热到T2,其熵变为ΔS2,则ΔS1与ΔS2的关系为A. ΔS1 >ΔS2B. ΔS1 =ΔS2C. ΔS1 <ΔS2D. ΔS1 =ΔS2 = 012.当理想气体在等温(500K)下进行膨胀时,求得体系的熵变∆S = l0 J·K-1,若该变化中所做的功仅为相同终态最大功的1/10,该变化中从热源吸热:A. 5000JB. 500JC. 50JD. 100J13.由1mol理想气体A[C V,m(A)=2.5R]与1mol理想气体B[C V,m(B)=3.5R]组成理想气体混合物。
热力学第二定律练习题与答案

热力学第二定律练习题一、是非题,下列各题的叙述是否正确,对的画√错的画×1、热力学第二定律的克劳修斯说法是:热从低温物体传给高温物体是不可能的 ( )2、组成可变的均相系统的热力学基本方程 d G =-S d T +V d p +d n B ,既适用于封闭系统也适用于敞开系统。
( )3、热力学第三定律的普朗克说法是:纯物质完美晶体在0 K 时的熵值为零。
( )4、隔离系统的熵是守恒的。
( )5、一定量理想气体的熵只是温度的函数。
( )6、一个系统从始态到终态,只有进行可逆过程才有熵变。
( )7、定温定压且无非体积功条件下,一切吸热且熵减少的反应,均不能自发发生。
( )8、系统由状态1经定温、定压过程变化到状态2,非体积功W ’<0,且有W ’>∆G 和∆G <0,则此状态变化一定能发生。
( )9、绝热不可逆膨胀过程中∆S >0,则其相反的过程即绝热不可逆压缩过程中∆S <0。
( ) 10、克-克方程适用于纯物质的任何两相平衡。
( )11、如果一个化学反应的∆r H 不随温度变化,则其∆r S 也不随温度变化, ( )12、在多相系统中于一定的T ,p 下物质有从化学势较高的相自发向化学势较低的相转移的趋势。
( ) 13、在-10℃,101.325 kPa 下过冷的H 2O ( l )凝结为冰是一个不可逆过程,故此过程的熵变大于零。
( ) 14、理想气体的熵变公式只适用于可逆过程。
( )15、系统经绝热不可逆循环过程中∆S = 0,。
( )二、选择题1 、对于只做膨胀功的封闭系统的(∂A /∂T )V 值是:( ) (1)大于零 (2) 小于零 (3)等于零 (4)不确定 2、 从热力学四个基本过程可导出VU S ∂⎛⎫⎪∂⎝⎭=( ) (1) (2) (3) (4) T p S pA H U G V S V T ∂∂∂∂⎛⎫⎛⎫⎛⎫⎛⎫ ⎪ ⎪ ⎪ ⎪∂∂∂∂⎝⎭⎝⎭⎝⎭⎝⎭3、1mol 理想气体(1)经定温自由膨胀使体积增加1倍;(2)经定温可逆膨胀使体积增加1倍;(3)经绝热自由膨胀使体积增加1倍;(4)经绝热可逆膨胀使体积增加1倍。
大学物理化学 第二章 热力学第二定律学习指导及习题解答

3.熵可以合理地指定
Sm$
(0K)
0
,热力学能是否也可以指定
U
$ m
(0K)
0
呢?
答:按能斯特热定理,当温度趋于0K,即绝对零度时,凝聚系统中等温变化过
程的熵变趋于零,即
, 只要满足此式,我们就可以任意
选取物质在0K时的任意摩尔熵值作为参考值,显然 Sm$ (0K) 0 是一种最方便的
选择。但0K时反应的热力学能变化并不等于零,
(2)变温过程
A.等压变温过程 始态 A(p1,V1,T1) 终态 B(p 1,V2,T2)
S
T2
δQ R
T T1
T2 Cp d T T T1
Cp
ln
T2 T1
B.等容变温过程 始态 A(p1,V1,T1) 终态 B(p2,V1,T2)
S
T2
δQ R
T T1
C.绝热过程
T2 CV d T T T1
,所以不
能指定
U
$ m
(0K)
0
。
4.孤立系统从始态不可逆进行至终态S>0,若从同一始态可逆进行至同
一终态时,则S=0。这一说法是否正确?
答:不正确。熵是状态函数与变化的途径无关,故只要始态与终态一定S
必有定值,孤立系统中的不可逆过程S>0,而可逆过程S=0 是毋庸置疑的,
问题是孤立系统的可逆过程与不可逆过程若从同一始态出发是不可能达到相同
4.熵 (1)熵的定义式
dS δ QR T
或
S SB SA
B δ QR AT
注意,上述过程的热不是任意过程发生时,系统与环境交换的热量,而必须是在
可逆过程中系统与环境交换的热。
物理化学第二章热力学第二定律练习题及答案

物理化学第二章热力学第二定律练习题及答案第二章 热力学第二定律练习题一、判断题(说法正确否):1.自然界发生的过程一定是不可逆过程。
2.不可逆过程一定是自发过程。
3.熵增加的过程一定是自发过程。
4.绝热可逆过程的∆S = 0,绝热不可逆膨胀过程的∆S > 0,绝热不可逆压缩过程的∆S < 0。
5.为了计算绝热不可逆过程的熵变,可以在始末态之间设计一条绝热可逆途径来计算。
6.由于系统经循环过程后回到始态,∆S = 0,所以一定是一个可逆循环过程。
7.平衡态熵最大。
8.在任意一可逆过程中∆S = 0,不可逆过程中∆S > 0。
9.理想气体经等温膨胀后,由于∆U = 0,所以吸的热全部转化为功,这与热力学第二定律矛盾吗?10.自发过程的熵变∆S > 0。
11.相变过程的熵变可由T H S ∆=∆计算。
12.当系统向环境传热时(Q < 0),系统的熵一定减少。
13.一切物质蒸发时,摩尔熵都增大。
14.冰在0℃,p 下转变为液态水,其熵变TH S ∆=∆>0,所以该过程为自发过程。
15.自发过程的方向就是系统混乱度增加的方向。
16.吉布斯函数减小的过程一定是自发过程。
17.在等温、等压下,吉布斯函数变化大于零的化学变化都不能进行。
18.系统由V 1膨胀到V 2,其中经过可逆途径时做的功最多。
19.过冷水结冰的过程是在恒温、恒压、不做其他功的条件下进行的,由基本方程可得∆G = 0。
20.理想气体等温自由膨胀时,对环境没有做功,所以 -p d V = 0,此过程温度不变,∆U = 0,代入热力学基本方程d U = T d S - p d V ,因而可得d S = 0,为恒熵过程。
21.是非题:⑴“某体系处于不同的状态,可以具有相同的熵值”,此话对否?⑵“体系状态变化了,所有的状态函数都要变化”,此话对否?⑶ 绝热可逆线与绝热不可逆线能否有两个交点?⑷ 自然界可否存在温度降低,熵值增加的过程?举一例。
(完整版)第二章习题解答
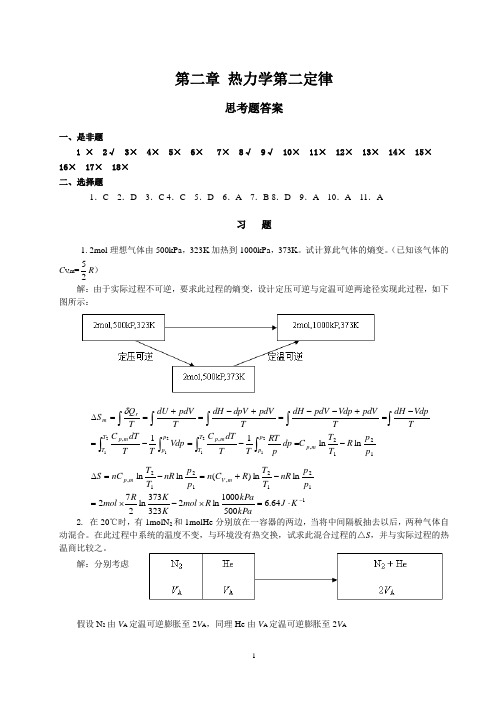
第二章 热力学第二定律思考题答案一、是非题1 × 2√ 3× 4× 5× 6× 7× 8√ 9√ 10× 11× 12× 13× 14× 15× 16× 17× 18× 二、选择题1.C 2.D 3.C 4.C 5.D 6.A 7.B 8.D 9.A 10.A 11.A习 题1. 2mol 理想气体由500kPa ,323K 加热到1000kPa ,373K 。
试计算此气体的熵变。
(已知该气体的C V ,m =25R ) 解:由于实际过程不可逆,要求此过程的熵变,设计定压可逆与定温可逆两途径实现此过程,如下图所示:1212,,,ln ln 1121212121p pR T T C dp p RT T T dT C Vdp TTdT C TVdpdH T pdV Vdp pdV dH T pdV dpV dH TpdVdU T Q S m p p p T T m p p p T T m p rm -=-=-=-=+--=+-=+==∆⎰⎰⎰⎰⎰⎰⎰⎰⎰δ11212,1212,64.65001000ln 2323373ln 272ln ln )(ln ln -⋅=⨯-⨯=-+=-=∆K J kPakPa R mol K K R mol p pnR T T R C n p p nR T T nC S m V m p2. 在20℃时,有1molN 2和1molHe 分别放在一容器的两边,当将中间隔板抽去以后,两种气体自动混合。
在此过程中系统的温度不变,与环境没有热交换,试求此混合过程的△S ,并与实际过程的热温商比较之。
解:分别考虑假设N 2由V A 定温可逆膨胀至2V A ,同理He 由V A 定温可逆膨胀至2V A△S 1 = n (N 2)R ln2 △S 2 = n (He)R ln2所以系统的 △S = △S 1+△S 2 = n (N 2) R ln2 + n (He) R ln2= 2×1mol×8.314 J ·mol -1·K -1×ln2 = 11.52J.K -1而实际过程系统没有与环境交换热和功,则 TQ= 0 即 △S >TQ 3. 1 mol 双原子理想气体,温度为298.15 K ,压强为p θ,分别进行:(1)绝热可逆膨胀至体积增加1倍;(2)绝热自由膨胀至体积增加1倍。
大学物理化学2-热力学第二定律课后习题及答案

热力学第二定律课后习题答案习题1在300 K ,100 kPa 压力下,2 mol A 和2 mol B 的理想气体定温、定压混合后,再定容加热到600 K 。
求整个过程的∆S 为若干?已知C V ,m ,A = 1.5 R ,C V ,m ,B = 2.5 R[题解]⎪⎩⎪⎨⎧B(g)2mol A(g)2mol ,,纯态 3001001K kPa,()−→−−−−混合态,,2mol A 2mol B100kPa 300K 1+==⎧⎨⎪⎪⎩⎪⎪p T 定容()−→−−2混合态,,2mol A 2mol B 600K 2+=⎧⎨⎪⎩⎪T ∆S = ∆S 1 + ∆S 2,n = 2 mol∆S 1 = 2nR ln ( 2V / V ) = 2nR ln2 ∆S 2 = ( 1.5nR + 2.5nR ) ln (T 2 / T 1)= 4nR ln2 所以∆S = 6nR ln2= ( 6 ⨯ 2 mol ⨯ 8.314 J ·K -1·mol -1 ) ln2 = 69.15 J ·K -1 [导引]本题第一步为理想气体定温定压下的混合熵,相当于发生混合的气体分别在定温条件下的降压过程,第二步可视为两种理想气体分别进行定容降温过程,计算本题的关键是掌握理想气体各种变化过程熵变的计算公式。
习题22 mol 某理想气体,其定容摩尔热容C v ,m =1.5R ,由500 K ,405.2 kPa 的始态,依次经历下列过程:(1)恒外压202.6 kPa 下,绝热膨胀至平衡态; (2)再可逆绝热膨胀至101.3 kPa ; (3)最后定容加热至500 K 的终态。
试求整个过程的Q ,W ,∆U ,∆H 及∆S 。
[题解] (1)Q 1 = 0,∆U 1 = W 1, nC V ,m (T 2-T 1))(1122su p nRT p nRT p --=, K400546.2022.405)(5.11221211212====-=-T T kPa p kPa p T p T p T T ,得,代入,(2)Q 2 = 0,T T p p 3223111535325=-=-=--()γγγγ,, T T 320.42303==-()K(3)∆V = 0,W 3 = 0,Q U nC T T V 3343232831450030314491==-=⨯⨯⨯-=∆,()[.(.)].m J kJp p T T 434350030310131671==⨯=(.).kPa kPa 整个过程:Q = Q 1 + Q 2+ Q 3 =4.91kJ ,∆U = 0,∆H = 0,Q + W = ∆U ,故W =-Q =-4.91 kJ∆S nR p p ==⨯=--ln (.ln ..).141128314405616711475J K J K ··[导引]本题的变化过程为单纯pVT 变化,其中U 、H 和S 是状态函数,而理想气体的U 和H 都只是温度的函数,始终态温度未变,故∆U = 0,∆H = 0。
南京大学《物理化学》考试 第二章 热力学第二定律

第二章热力学第二定律物化试卷(一)1.理想气体绝热向真空膨胀,则:(A) ΔS = 0 , W = 0 (B) ΔH = 0,ΔU = 0(C) ΔG = 0,ΔH = 0 (D) ΔU = 0,ΔG =02.熵变ΔS是: (1) 不可逆过程热温商之和 (2) 可逆过程热温商之和 (3) 与过程无关的状态函数 (4) 与过程有关的状态函数 以上说法正确的是:(A) 1,2 (B) 2,3 (C) 2 (D) 43. 理想气体经可逆与不可逆两种绝热过程:(A) 可以从同一始态出发达到同一终态(B) 从同一始态出发,不可能达到同一终态(C) 不能断定 (A)、(B) 中哪一种正确(D) 可以达到同一终态,视绝热膨胀还是绝热压缩而定4. 在标准压力,273.15 K下水凝结为冰,判断体系的下列热力学量中何者一定为零?(A) ΔU (B) ΔH (C) ΔS (D) ΔG5. 水在 100℃,标准压力下沸腾时,下列各量何者增加?(A) 熵 (B) 汽化热 (C) 吉布斯自由能 (D) 蒸气压6. 在 N2和 O2混合气体的绝热可逆压缩过程中,体系的热力学函数变化值在下列结论中正确的是:(A) ΔU = 0 (B) ΔF = 0(C) ΔS = 0 (D) ΔG = 07. 在 270 K,101.325 kPa 下,1 mol过冷水经等温等压过程凝结为同样条件下的冰,则体系及环境的熵变应为:(A) ΔS(体系)< 0 , ΔS(环境)< 0 (B) ΔS(体系)< 0 , ΔS(环境)> 0(C) ΔS(体系)> 0 , ΔS(环境)< 0 (D) ΔS(体系)> 0 , ΔS(环境)> 08. 理想气体在等温条件下,经恒外压压缩至稳定, 此变化中的体系熵变ΔS(体)及环境熵变ΔS(环)应为:(A) ΔS(体)> 0 , ΔS(环)< 0 (B)ΔS(体)< 0 , ΔS(环)> 0(C) ΔS(体)> 0 , ΔS(环)= 0 (D)ΔS(体)< 0 , ΔS(环)= 09.一个由气相变为凝聚相的化学反应,在恒温恒容下自发进行,问下列各组答案中,哪一个是正确的?(A) ΔS(体)>0, ΔS(环)<0 (B) ΔS(体)<0, ΔS(环)>0(C) ΔS(体)<0, ΔS(环)=0 (D) ΔS(体)>0, ΔS(环)=010. 在一简单的(单组分,单相,各向同性)封闭体系中,恒压只做膨胀功的条件下,吉布斯自由能值随温度升高如何变化?(A) (TG/TT)p> 0 (B) (TG/TT)p< 0(/(C) (TG/TT)p= 0 (D) 视具体体系而定11. 某气体的状态方程为p V(m) = RT +αp,其中α为大于零的常数,该气体经恒温膨胀,其热力学能:(A) 不变 (B) 增大 (C) 减少 (D) 不能确定12. 下列四个关系式中,哪一个不是麦克斯韦关系式?(A) (TT/TV)s=(TV/TS)p (B) (TT/Tp)s=(TV/TS)p(C) (TS/TV)T=(Tp/TT)v (D) (TS/Tp)T= -(TV/TT)p13. 下列各式中哪个是化学势?(A) (?T H/?T n(B))T,S, (B) (?T F/?T n(B))T,p,(C) (?T G/?T n(B))T,V, (D) (?T U/?T n(B))S,V,14. 298 K,标准压力下,有两瓶萘的苯溶液,第一瓶为 2 dm3(溶有 0.5 mol 萘), 第二瓶为 1 dm3(溶有 0.25 mol 萘),若以μ1,μ2分别表示两瓶中萘的化学势,则:(A)μ1 = 10μ2 (B)μ2= 2μ2(C) μ1 = μ2(D) μ1= 0.5μ215. 重结晶制取纯盐的过程中,析出的 NaCl 固体的化学势与母液中 NaCl 的化学势比较,高低如何?(A) 高 (B) 低 (C) 相等 (D) 不可比较16. 热力学第三定律可以表示为:(A) 在0 K 时,任何晶体的熵等于零 (B) 在0 K 时,任何完整晶体的熵等于零(C) 在0 ℃时,任何晶体的熵等于零(D) 在0 ℃时,任何完整晶体的熵等于零17.下列四种表述: (1) 等温等压下的可逆相变过程中,体系的熵变ΔS =ΔH 相变/T 相变(2) 体系经历一自发过程总有 ΔS > 0(3) 自发过程的方向就是混乱度增加的方向 (4) 在绝热可逆过程中,体系的熵变为零 两者都不正确者为:(A) (1),(2) (B) (3),(4)(C) (2),(3)(D) (1),(4)18. 在绝热条件下,用大于气筒内的压力迅速推动活塞压缩气体,此过程的熵变为:(A) 大于零 (B) 等于零 (C) 小于零 (D) 不能确定19. 在263 K的过冷水凝结成263 K的冰,则:(A) ΔS<0 (B) ΔS>0 (C) ΔS=0 (D) 无法确定20. 在标准压力和268.15 K下,冰变为水,体系的熵变ΔS体应:(A) 大于零 (B) 小于零 (C) 等于零 (D) 无法确定第二章热力学第二定律物化试卷(二)1. 2 mol H2和 2 mol Cl2在绝热钢筒内反应生成 HCl 气体,起始时为常温常压。
大学《物理化学》第二定律练习题

《物理化学》热力学第二定律练习题1.在两个不同温度的热源之间工作的热机以卡诺热机的效率最大。
判断正确和错误:________。
(√)2.卡诺热机的效率只与两个热源的温度有关而与工作物质无关。
判断正确和错误:________。
(√)3.卡诺热机在T 1=600K 的高温热源和T 2=300K 的低温热源间工作,其热机效率________。
(η=0.5)30011600L R H T T η=-=-卡诺定律:R ηη≤4.改正下列错误(1)在一可逆过程中熵值不变; (2)在一过程中熵变是QS Tδ∆=⎰;(3)亥姆赫兹函数是系统能做非体积功的能量; (4)吉布斯函数是系统能做非体积功的能量; (5)焓是系统以热的方式交换的能量。
答:(1)在绝热可逆过程中熵值不变。
(绝热可逆过程即为等熵过程)(2)在一过程中熵变是rQ S Tδ∆=⎰;(QS Tδ∆≥⎰)(3)在恒温恒容条件下,亥姆赫兹函数是系统能做非体积功的能量;,T V A W '∆≤(=:可逆;>:不可逆) ; ,T V A W '∆≥(=:可逆;>:不可逆)在恒温条件下,亥姆赫兹函数是系统能做功的能量T A W ∆≤(=:可逆;<:不可逆) ; T A W ∆≥(=:可逆;>:不可逆)(4)在恒温恒压条件下,吉布斯函数是系统能做非体积功的能量;,T p G W '∆≤(=:可逆;<:不可逆) ,T p G W '∆≥(=:可逆;>:不可逆)(5)焓没有明确的物理意义。
在封闭系统、恒压且不做非体积功的情况下,焓的增量等于恒压热,即∆H =Qp 。
5指出下列过程中△U ,△H , △S , △A , △G 何者为零。
⑴ 理想气体不可逆恒温压缩; ⑵ 理想气体节流膨胀;⑶ 实际流体节流膨胀; ⑷ 实际气体可逆绝热膨胀; ⑸ 实际气体不可逆循环过程; ⑹ 饱和液体变为饱和蒸气; ⑺ 绝热恒容没有非体积功时发生化学变化; ⑻ 绝热恒压没有非体积功时发生化学反应。
全版热力学第二定律习题

第二章 热力学第二定律习题1. 1L 理想气体在3000 K 时压力为1519.9 kPa ,经等温膨胀最后体积变到10 dm 3,计算该过程的W max 、ΔH 、ΔU 及ΔS 。
解:22max 1111210lnln 1519.91ln103499.73499.7ln1.167/3000H U V V W nRT p V V V J V S nR J K V ∆∆=-=-=-⨯=-∆===等温膨胀,==当等温可逆膨胀时,体系对环境做功最大:2. 1mol H 2在300K 从体积为1dm 3向真空膨胀至体积为10 dm 3,求体系的熵变。
假设使该H 2在300K 从1dm 3经恒温可逆膨胀至10 dm 3其熵变又是多少?由此得到怎样的结论?解:真空膨胀为不可逆过程,要计算熵变,必须先设计可逆过程,即等温可逆膨胀过程,ΔS = nR ln(V 2/V 1)=1×8.314×ln10 = 19.14J/K对于等温可逆膨胀,不需设计可逆过程,直接计算,由于两步的始态和终态一样,所以等温可逆膨胀的熵变也等于19.14J/K 。
结论:只要体系的始态和终态一样,不管是可逆过程还是不可逆过程,体系熵变一样。
3. 0.5 dm 3 343K 水与0.1 dm 3 303K 水混合,求熵变。
解:水的混合过程为等压变化过程,用ΔS = n C p,m ln(T 2/T 1)计算,同时熵是广度性质的状态函数,具加和性,熵变ΔS 等于高温水的熵变ΔS h 加上低温水的熵变ΔS c 。
先计算水终态温度,根据高温水放出的热量等于低温水吸收的热量来计算,设终态水温为T 终。
Q = n C p,m (T 2 - T 1) = (0.1ρ/M ) C p,m (T 终-303) = (0.5ρ/M ) C p,m (343-T 终) T 终 = 336.3KΔS = ΔS h +ΔS c = (0.5ρ/M ) C p,m ln(336.3/343) + (0.1ρ/M ) C p,m ln(336.3/303) = (0.5×103/18)×75.31 ln(336.3/343) + (0.1×103/18)×75.31 ln(336.3/303) = 2.35J/K4. 有473K 的锡0.25kg,落在283K1kg 的水中,略去水的蒸发,求到达平衡时此过程的熵变。
物理化学答案——第二章-热力学第二定律

第二章 热力学第二定律 一、基本公式和基本概念 基本公式1. 热力学第二定律的数学表达式----克劳修斯不等式 ()0A B A B QS Tδ→→∆-≥∑2. 熵函数的定义 ()R QdS Tδ=, ln S k =Ω3. 熵变的计算理想气体单纯,,p V T 变化22,1122,1122,,11ln ln ln ln lnln V m p m p m V m T V S C R T V T p S C R T p V p S C C V p ∆=+∆=-∆=+理想气体定温定压混合过程ln i i iS R n x ∆=-∑封闭系统的定压过程21,d T p m T C S n T T∆=⎰封闭系统定容过程 21,d T V m T C S n T T∆=⎰可逆相变 m n H S T∆∆=标准状态下的化学反应 ,()r m Bm B BS S T θθν∆=∑定压下由1T 温度下的化学反应熵变求2T 温度下的熵变 21,21()()d T p m r m r m T C S T S T T T∆∆=∆+⎰4. 亥姆霍兹函数 A U TS ≡-5. 吉布斯函数 G H TS ≡-6. G ∆和A ∆的计算(A ∆的计算原则与G ∆相同,做相应的变换即可)定温过程G H T S ∆=∆-∆组成不变的均相封闭系统的定温过程 21d p p G V p ∆=⎰理想气体定温过程 21ln p G nRT p ∆= 7. 热力学判据熵判据:,()0U V dS ≥亥姆霍兹函数判据:,,'0(d )0T V W A =≤ 吉布斯函数判据:,,'0(d )0T p W G =≤8. 热力学函数之间的关系组成不变,不做非体积功的封闭系统的基本方程d d d d d d d d d d d d U T S p V H T S V pA S T p V G S T V p=-=+=--=-+麦克斯韦关系S VpS T Vp TT p V S T V p S S p V T S V p T ∂∂⎛⎫⎛⎫=- ⎪ ⎪∂∂⎝⎭⎝⎭⎛⎫∂∂⎛⎫= ⎪ ⎪∂∂⎝⎭⎝⎭∂∂⎛⎫⎛⎫= ⎪ ⎪∂∂⎝⎭⎝⎭⎛⎫∂∂⎛⎫=- ⎪ ⎪∂∂⎝⎭⎝⎭9. 吉布斯-亥姆霍兹方程2()pG HT T T ∆⎡⎤∂⎢⎥∆=-⎢⎥∂⎢⎥⎣⎦ 基本概念1. 热力学第二定律在研究化学或物理变化驱动力来源的过程中,人们注意到了热功交换的规律,抓住了事物的共性,提出了具有普遍意义的熵函数。
物理化学课件-第二定律练习题答案

U W 12.471 (228.2 573.15) 4.302kJ
or
W p2V2 p1V1 nR(T2 T1)
1
1
C p,m 20.785J.mol.K 1
H nCp,m (T2 T1) 20.785 (228.2 573.15) 7.170kJ
S 0
S环=0
Siso S S环 0
胀,(b)恒外压 p外=0.1Mpa等温膨胀,(c) 恒温可逆膨
胀。
可逆恒温膨胀
n1=2 mol, T1=300K, P1=1MPa
恒外压膨胀
n2=2mol, T2=300K, P2=0.1MPa
真空膨胀
4、1 mol单原子分子理想气体始态为273 K,
pθ下,计算经过下列变化后的各个Gm值。设该
条件下气体的摩尔熵为100 J·K-1·mol-1。 (1) 恒压下体积加倍; (2) 恒容下压力加倍; (3) 恒温下压力加倍。
恒压膨胀
n=1mol,
T1=273K, p1=100kPa V1
恒容升温
恒温压缩
V2=2V1 T2=?K, p2=p1=100kPa
V3=V1, T3=? K, P3=2p1=200kPa
1mol H2O, 373K Pө, 气体
可逆相变
1mol H2O, Pө, 373K, 液体
真空膨胀汽化
H Qp 40668.5kJ U H ( pV ) H pV H p[V (g) V (l)] U H pV (g) 406685 ng RT U 406685 8.314 373 37.567kJ
CV ,m CV ,m 1.5R
1
T2
T1
p2 p1
573.15 (
南京大学《物理化学》练习 第二章 热力学第二定律

第二章热力学第二定律返回上一页1. 5 mol He(g)从273.15 K和标准压力变到298.15K和压力p=10×, 求过程的ΔS。
(已知C(V,m)=3/2 R)2. 0.10 kg 283.2 K的水与0.20 kg 313.2 K 的水混合,求ΔS。
设水的平均比热为4.184kJ/(K·kg)。
3. 实验室中有一大恒温槽(例如是油浴)的温度为400 K,室温为300 K。
因恒温槽绝热不良而有4000 J的热传给空气,用计算说明这一过程是否为可逆?4. 在298.15K的等温情况下,两个瓶子中间有旋塞连通。
开始时,一放0.2 mol O2,压力为0.2×101.325kPa,另一放0.8 mol N2,压力为0.8×101.325 kPa,打开旋塞后,两气体互相混合。
计算:(1)终了时瓶中的压力。
(2)混合过程中的Q,W,ΔU,ΔS,ΔG;(3)如果等温下可逆地使气体回到原状,计算过程中的Q和W。
5.(1)在298.2 K时,将1mol O2从101.325 kPa 等温可逆压缩到6×101.325 kPa,求Q,W,ΔU m,ΔH m,ΔF m,ΔG m,ΔS m,ΔS iso(2)若自始至终用6×101.325 kPa的外压等温压缩到终态,求上述各热力学量的变化值。
6. 在中等的压力下,气体的物态方程可以写作p V(1-βp)=nRT。
式中系数β与气体的本性和温度有关。
今若在273K时,将0.5 mol O2由1013.25kPa的压力减到101.325 kPa,试求ΔG。
已知氧的β=-0.00094。
7. 在298K及下,一摩尔过冷水蒸汽变为同温同压下的水,求此过程的ΔG m。
已知298.15K时水的蒸汽压为3167Pa。
8. 将298.15K 1 mol O2从绝热可逆压缩到6×,试求Q,W,ΔU m, ΔH m, ΔF m, ΔG m, ΔS m和ΔS iso(C(p,m)=7/2 R)。
物化练习(热力学第二定律) 厦门大学 物化试题

物理化学练习(热力学第二定律2006.4)一、选择题( 共18题)1. 公式d G = -S d T + V d p可适用下述哪一过程:( )(A) 298K、101325Pa 下的水蒸发过程(B) 理想气体真空膨胀(C) 电解水制取氢(D) N2(g) + 3H2(g)=2NH3(g) 未达平衡2. 理想气体在等温条件下,经恒外压压缩至稳定, 此变化中的体系熵变∆S体及环境熵变∆S 环应为:( )(A) ∆S体> 0 , ∆S环< 0 (B) ∆S体< 0 , ∆S环> 0(C) ∆S体> 0 , ∆S环= 0 (D) ∆S体< 0 , ∆S环= 03. 在101.3 kPa下,110℃的水变为110℃水蒸气,吸热Q p,在该相变过程中下列哪个关系式不成立?( )(A) ∆S体> 0(B) ∆S环不确定(C) ∆S体+∆S环> 0(D) ∆S环< 04. 某体系分A,B两部分,这两部分的热力学概率分别为ΩA和ΩB,则整个体系的微观状态数Ω与ΩA,ΩB的关系为:()(A)Ω=ΩAΩB(B)Ω=ΩB /ΩA(C)Ω=ΩA +ΩB(D)Ω=ΩB–ΩA5. 下列对物质临界点性质的描述哪一个是错误的? ( )(A) 液相摩尔体积与气相摩尔体积相等(B) 液相与气相的临界面消失(C) 汽化热为零(D) 固、液、气三相共存6.2 mol液态苯在其正常沸点(353.2 K)和101.325 kPa下蒸发为苯蒸气,该过程的Δvap F 等于( )(A) 23.48 kJ (B) 5.87 kJ(C) 2.94 kJ (D) 1.47 kJ7. 下列四种表述:(1) 等温等压下的可逆相变过程中,体系的熵变ΔS =ΔH相变/T相变(2) 体系经历一自发过程总有d S > 0(3) 自发过程的方向就是混乱度增加的方向(4) 在绝热可逆过程中,体系的熵变为零两者都不正确者为:( )(A) (1),(2) (B) (3),(4)(C) (2),(3) (D) (1),(4)8.将氧气分装在同一气缸的两个气室内,其中左气室内氧气状态为p1=101.3 kPa ,V1=2 dm3,T1=273.2 K;右气室内状态为p2=101.3 kPa,V2=1 dm3,T2=273.2 K;现将气室中间的隔板抽掉,使两部分气体充分混合。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第二章热力学第二定律练习题一、判断题(说法正确否):1.自然界发生的过程一定是不可逆过程。
2.不可逆过程一定是自发过程。
3.熵增加的过程一定是自发过程。
4.绝热可逆过程的∆S= 0,绝热不可逆膨胀过程的∆S> 0,绝热不可逆压缩过程的∆S< 0。
5.为了计算绝热不可逆过程的熵变,可以在始末态之间设计一条绝热可逆途径来计算。
6.由于系统经循环过程后回到始态,∆S = 0,所以一定是一个可逆循环过程。
7.平衡态熵最大。
8.在任意一可逆过程中∆S = 0,不可逆过程中∆S > 0。
9.理想气体经等温膨胀后,由于∆U = 0,所以吸的热全部转化为功,这与热力学第二定律矛盾吗10.自发过程的熵变∆S > 0。
11.相变过程的熵变可由计算。
12.当系统向环境传热时(Q < 0),系统的熵一定减少。
13.一切物质蒸发时,摩尔熵都增大。
14.冰在0℃,p下转变为液态水,其熵变>0,所以该过程为自发过程。
15.自发过程的方向就是系统混乱度增加的方向。
16.吉布斯函数减小的过程一定是自发过程。
17.在等温、等压下,吉布斯函数变化大于零的化学变化都不能进行。
18.系统由V1膨胀到V2,其中经过可逆途径时做的功最多。
19.过冷水结冰的过程是在恒温、恒压、不做其他功的条件下进行的,由基本方程可得∆G = 0。
20.理想气体等温自由膨胀时,对环境没有做功,所以 -p d V= 0,此过程温度不变,∆U= 0,代入热力学基本方程d U = T d S - p d V,因而可得d S = 0,为恒熵过程。
21.是非题:⑴“某体系处于不同的状态,可以具有相同的熵值”,此话对否⑵“体系状态变化了,所有的状态函数都要变化”,此话对否⑶绝热可逆线与绝热不可逆线能否有两个交点⑷自然界可否存在温度降低,熵值增加的过程举一例。
⑸ 1mol理想气体进行绝热自由膨胀,体积由V1变到V2,能否用公式:计算该过程的熵变22.在100℃、p时,1mol水与100℃的大热源接触,使其向真空容器中蒸发成100℃、p的水蒸气,试计算此过程的∆S、∆S(环)。
23.的适用条件是什么24.指出下列各过程中,物系的∆U、∆H、∆S、∆A、∆G中何者为零⑴理想气体自由膨胀过程;⑵实际气体节流膨胀过程;⑶理想气体由(p1,T1)状态绝热可逆变化到(p2,T2)状态;⑷ H2和Cl2在刚性绝热的容器中反应生成HCl;⑸ 0℃、p时,水结成冰的相变过程;⑹理想气体卡诺循环。
25.a mol A与b mol B的理想气体,分别处于(T,V,p A)与(T,V,p B)的状态,等温等容混合为(T,V,p)状态,那么∆U、∆H、∆S、∆A、∆G何者大于零,小于零,等于零26.一个刚性密闭绝热箱中,装有H2与Cl2混合气体,温度为298K,今用光引发,使其化合为HCl(g),光能忽略,气体为理想气体,巳知(HCl) = ·mol-1,试判断该过程中∆U、∆H、∆S、∆A、∆G是大于零,小于零,还是等于零27.在一绝热恒容箱内,有一绝热板将其分成两部分,隔板两边各有1mol N2,其状态分别为298K、p0与298K、10p0,若以全部气体为体系,抽去隔板后,则Q、W、∆U、∆H、∆S中,哪些为零二、单选题:1.适合于下列过程中的哪一个(A) 恒压过程;(B) 绝热过程;(C) 恒温过程; (D) 可逆相变过程。
2.可逆热机的效率最高,因此由可逆热机带动的火车:(A) 跑的最快; (B) 跑的最慢;(C) 夏天跑的快;(D) 冬天跑的快。
3.在一定速度下发生变化的孤立体系,其总熵的变化是什么(A) 不变;(B) 可能增大或减小;(C) 总是增大;(D) 总是减小。
4.对于克劳修斯不等式,判断不正确的是:(A) 必为可逆过程或处于平衡状态;(B) 必为不可逆过程;(C) 必为自发过程;(D) 违反卡诺定理和第二定律,过程不可能自发发生。
5.下列计算熵变公式中,哪个是错误的:(A) 水在25℃、p0下蒸发为水蒸气:;(B) 任意可逆过程:;(C) 环境的熵变:;(D) 在等温等压下,可逆电池反应:。
6.当理想气体在等温(500K)下进行膨胀时,求得体系的熵变∆S= l0 J·K-1,若该变化中所做的功仅为相同终态最大功的,该变化中从热源吸热多少(A) 5000 J ;(B) 500 J ;(C) 50 J ;(D) 100 J 。
7.1mol双原子理想气体的是:(A) ;(B) ;(C) ;(D) 2R。
8.理想气体在绝热条件下,在恒外压下被压缩到终态,则体系与环境的熵变:(A) ∆S(体) > 0,∆S(环) > 0 ;(B) ∆S(体) < 0,∆S(环) < 0 ;(C) ∆S(体) > 0,∆S(环) = 0 ;(D) ∆S(体) > 0,∆S(环) < 0 。
9.一理想气体与温度为T的热源接触,分别做等温可逆膨胀和等温不可逆膨胀到达同一终态,已知,下列式子中不正确的是:(A) ;(B) ;(C) ;(D) (等温可逆),(不等温可逆)。
10.计算熵变的公式适用于下列:(A) 理想气体的简单状态变化;(B) 无体积功的封闭体系的简单状态变化过程;(C) 理想气体的任意变化过程;(D) 封闭体系的任意变化过程;11.实际气体CO2经节流膨胀后,温度下降,那么:(A) ∆S(体) > 0,∆S(环) > 0 ;(B) ∆S(体) < 0,∆S(环) > 0 ;(C) ∆S(体) > 0,∆S(环) = 0 ;(D) ∆S(体) < 0,∆S(环) = 0 。
12.2mol理想气体B,在300K时等温膨胀,W = 0时体积增加一倍,则其∆S(J·K-1)为:(A) ;(B) 331 ;(C) ;(D) 。
13.如图,可表示理想气体卡诺循环的示意图是:(A) 图⑴;(B) 图⑵;(C) 图⑶;(D) 图⑷。
14.某体系等压过程A→B的焓变∆H与温度T无关,则该过程的:(A) ∆U与温度无关;(B) ∆S与温度无关;(C) ∆F与温度无关;(D) ∆G与温度无关。
15.等温下,一个反应a A + b B = d D + e E的∆r C p = 0,那么:(A) ∆H与T无关,∆S与T无关,∆G与T无关;(B) ∆H与T无关,∆S与T无关,∆G与T有关;(C) ∆H与T无关,∆S与T有关,∆G与T有关;(D) ∆H与T无关,∆S与T有关,∆G与T无关。
16.下列过程中∆S为负值的是哪一个:(A) 液态溴蒸发成气态溴;(B) SnO2(s) + 2H2(g) = Sn(s) + 2H2O(l) ;(C) 电解水生成H2和O2;(D) 公路上撤盐使冰融化。
17.熵是混乱度(热力学微观状态数或热力学几率)的量度,下列结论中不正确的是:(A) 同一种物质的;(B) 同种物质温度越高熵值越大;(C) 分子内含原子数越多熵值越大;(D) 0K时任何纯物质的熵值都等于零。
18.25℃时,将升O2与升N2混合成升的混合气体,该过程:(A) ∆S > 0,∆G < 0 ;(B) ∆S < 0,∆G < 0 ;(C) ∆S = 0,∆G = 0 ;(D) ∆S = 0,∆G < 0 。
19.有一个化学反应,在低温下可自发进行,随温度的升高,自发倾向降低,这反应是:(A) ∆S > 0,∆H > 0 ;(B) ∆S > 0,∆H < 0 ;(C) ∆S< 0,∆H> 0 ;(D)∆S < 0,∆H < 0 。
20.∆G = ∆A的过程是:(A) H2O(l,373K,p0)H2O(g,373K,p0) ;(B) N2(g,400K,1000kPa)N2(g,400K,100kPa) ;(C) 等温等压下,N2(g) + 3H2(g)NH3(g) ;(D) Ar(g,T,p0)Ar(g,T+100,p0) 。
21.等温等压下进行的化学反应,其方向由∆r H m和∆r S m共同决定,自发进行的反应应满足下列哪个关系式:(A) ∆r S m = ∆r H m/T;(B) ∆r S m> ∆r H m/T ;(C) ∆r S m≥∆r H m/T;(D) ∆r S m≤∆r H m/T。
22.等容等熵条件下,过程自发进行时,下列关系肯定成立的是:(A) ∆G < 0 ;(B) ∆F < 0 ;(C) ∆H < 0 ;(D) ∆U < 0 。
23.实际气体节流膨胀后,其熵变为:(A);(B);(C);(D)。
24.一个已充电的蓄电池以 V输出电压放电后,用 V电压充电使其回复原状,则总的过程热力学量变化:(A) Q < 0,W > 0,∆S > 0,∆G < 0 ;(B) Q < 0,W < 0,∆S < 0,∆G < 0 ;(C) Q > 0,W > 0,∆S = 0,∆G = 0 ;(D) Q < 0,W > 0,∆S = 0,∆G = 0 。
25.下列过程满足的是:(A) 恒温恒压(273 K,101325 Pa)下,1mol 的冰在空气升华为水蒸气;(B) 氮气与氧气的混合气体可逆绝热膨胀;(C)理想气体自由膨胀;(D) 绝热条件下化学反应。
26.吉布斯自由能的含义应该是:(A) 是体系能对外做非体积功的能量;(B) 是在可逆条件下体系能对外做非体积功的能量;(C) 是恒温恒压可逆条件下体系能对外做非体积功的能量;(D) 按定义理解G = H - TS 。
27.在 -10℃、下,1mol水凝结成冰的过程中,下列哪个公式可以适用:(A) ∆U = T∆S; (B) ; (C) ∆H = T∆S + V∆p; (D) ∆G T,p = 0。
28.对于封闭体系的热力学,下列各组状态函数之间的关系中正确的是:(A) A > U;(B) A < U;(C) G < U;(D)H < A。
29.、101325Pa的水,使其与大热源接触,向真空蒸发成为、101325Pa下的水气,对这一个过程,应选用哪一个作为过程方向的判据:(A) ∆U;(B) ∆A;(C) ∆H;(D) ∆G。
30.热力学基本方程 d G = -S d T + V d p,可适应用下列哪个过程:(A) 298K、标准压力下,水气化成蒸汽;(B) 理想气体向真空膨胀;(C) 电解水制取氢气;(D) N2 + 3H22NH3未达到平衡。
31.下列过程可用计算的是:(A) 恒温恒压下无非体积功的化学反应;(B) 恒温恒压下可逆原电池反应;(C) 恒温恒压下任意相变;(D) 恒温恒压下任意可逆相变。
