高一化学推断题和离子共存问题分析及习题(含答案)
高一化学离子共存试题答案及解析

高一化学离子共存试题答案及解析1.下列溶液中,一定能大量共存的离子组是A.能使氢氧化铝迅速溶解的溶液: Na+、Fe2+、NO3—、SO42—B.能使酚酞试液变红的溶液: Na+、NH4+、 CO32—、SO42—C.含有大量SO42—的透明溶液: K+、Cu2+、Cl—、NO3—D.含有大量ClO—的溶液: H+、 Mg2+、I—、SO42—【答案】C【解析】A.能使氢氧化铝迅速溶解的溶液可能呈酸性,也可能呈碱性,若呈酸性,则H+、Fe2+、NO3—、会发生氧化还原反应而不能大量共存;在碱性溶液中,Fe2+、OH-会发生沉淀反应液不能大量共存,错误;B.能使酚酞试液变红的溶液呈碱性,此时OH-、NH4+会发生离子反应而不能大量共存,错误;C.含有大量SO42—的透明溶液中,K+、Cu2+、Cl—、NO3—不会发生任何反应,因此可以大量存在,正确;D.含有大量ClO—的溶液有强氧化性,会与H+、I—发生氧化还原反应而不能大量共存,错误。
【考点】考查离子大量共存的知识。
2.某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。
取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。
由此可知原溶液中A.至少存在5种离子B.Cl-一定存在,且c(Cl-)≥0.4mol/LC.SO42-、NH4+、一定存在,Cl-可能不存在D.CO32-、Al3+一定不存在,K+可能存在【答案】B【解析】加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀,说明溶液中一定含有NH4+、Fe3+,其物质的量分别为0.02mol、0.01mol,则溶液中一定不存在CO32-,向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀,说明溶液中存在SO42-,其物质的量为0.02mol,根据电荷守恒规律,阳离子所带电荷总数为0.02+0.03=0.05mol,阴离子所带电荷总数为0.02×2=0.04mol,所以溶液中一定存在Cl-,c(Cl-)≥0.4mol/L,Al3+和K+不能确定。
高中离子共存试题及答案

高中离子共存试题及答案一、选择题1. 在下列离子中,哪些离子在酸性溶液中不能大量共存?A. Na^+、Cl^-、HCO_3^-B. K^+、SO_4^2-、OH^-C. Mg^2+、NH_4^+、Cl^-D. Ca^2+、NO_3^-、HSO_3^-答案:A2. 以下哪种离子组合在碱性溶液中可以大量共存?A. Al^3+、SO_4^2-、OH^-B. NH_4^+、Cl^-、OH^-C. K^+、NO_3^-、HCO_3^-D. Mg^2+、Cl^-、OH^-答案:C二、填空题1. 在含有大量Fe^3+的溶液中,以下哪些离子不能大量共存?______ 答案:Fe^3+与SCN^-、CO_3^2-、PO_4^3-等不能大量共存。
2. 写出在pH=4的溶液中,以下离子可以大量共存的组合:______答案:H^+、Cl^-、SO_4^2-、K^+三、简答题1. 为什么在酸性溶液中,HCO_3^-离子不能大量共存?答案:在酸性溶液中,HCO_3^-会与H^+发生反应生成CO_2和H_2O,因此不能大量共存。
2. 为什么在碱性溶液中,Al^3+离子不能大量共存?答案:在碱性溶液中,Al^3+会与OH^-发生反应生成Al(OH)_3沉淀,因此不能大量共存。
四、实验题1. 通过实验验证,在含有大量Cu^2+的溶液中,哪些离子不能大量共存,并说明原因。
答案:在含有大量Cu^2+的溶液中,Cl^-、SO_4^2-、OH^-等离子不能大量共存。
因为Cu^2+与Cl^-可以形成CuCl_2沉淀,与SO_4^2-可以形成CuSO_4沉淀,与OH^-可以形成Cu(OH)_2沉淀。
2. 设计一个实验来证明在中性溶液中,Ca^2+离子与CO_3^2-离子不能大量共存。
答案:在中性溶液中,加入Ca^2+溶液和CO_3^2-溶液,观察到生成白色沉淀CaCO_3,说明Ca^2+与CO_3^2-不能大量共存。
高中离子共存试题及答案

高中离子共存试题及答案一、选择题1. 下列各组离子中,能大量共存的是()A. Ag+、Cl-、NO3-、Na+B. H+、OH-、Cl-、Na+C. Fe3+、SCN-、Cl-、Na+D. AlO2-、H+、Cl-、Na+答案:A解析:A组离子中,Ag+和Cl-会生成AgCl沉淀,但AgCl在溶液中不溶,因此可以共存。
B组离子中,H+和OH-会生成水,不能共存。
C组离子中,Fe3+和SCN-会生成Fe(SCN)3络合物,不能共存。
D组离子中,AlO2-和H+会生成Al(OH)3沉淀,不能共存。
2. 在碱性溶液中,下列各组离子能大量共存的是()A. Fe2+、NO3-、OH-B. Al3+、Cl-、OH-C. NH4+、Cl-、OH-D. Na+、K+、NO3-、OH-答案:D解析:A组离子中,Fe2+和OH-会生成Fe(OH)2沉淀,不能共存。
B组离子中,Al3+和OH-会生成Al(OH)3沉淀,不能共存。
C 组离子中,NH4+和OH-会生成NH3和水,不能共存。
D组离子中,各离子之间不会发生反应,可以共存。
3. 在酸性溶液中,下列各组离子能大量共存的是()A. AlO2-、H+、Cl-、Na+B. HCO3-、H+、Cl-、Na+C. S2-、Cl-、H+、NO3-D. ClO-、Cl-、H+、Na+答案:D解析:A组离子中,AlO2-和H+会生成Al(OH)3沉淀,不能共存。
B组离子中,HCO3-和H+会生成CO2和水,不能共存。
C组离子中,S2-和H+会生成H2S气体,不能共存。
D组离子中,各离子之间不会发生反应,可以共存。
二、填空题4. 在酸性溶液中,下列离子中不能大量共存的是:Fe3+、Cl-、HCO3-、SO42-、K+。
其中,HCO3-与H+反应生成CO2和水,不能共存。
5. 在碱性溶液中,下列离子中不能大量共存的是:Cu2+、Cl-、OH-、NO3-。
其中,Cu2+与OH-反应生成Cu(OH)2沉淀,不能共存。
高考化学复习离子共存离子检验和推断习题含解析

高考化学复习离子共存、离子检验和推断1.在强酸性溶液中能大量共存的无色透明离子组是( )A.K+、Na+、NO-3、MnO-4B.Mg2+、Na+、Cl-、SO2-4C.K+、Na+、Br-、Cu2+D.Na+、Ba2+、OH-、SO2-4解析:A选项中的MnO-4在水溶液中显紫色;C选项中的Cu2+在水溶液中显蓝色;D选项中会发生离子反应Ba2++SO2-4===BaSO4↓和H++OH-===H2O。
答案:B2.下列离子或分子在溶液中能大量共存,通入CO2后仍能大量共存的一组是( ) A.K+、Ca2+、Cl-、NO-3B.K+、Na+、Br-、SiO2-3C.H+、Fe2+、SO2-4、Cl2D.K+、Ag+、NH3·H2O、NO-3解析:A项中离子能大量共存,通入CO2后,溶液呈酸性,不会生成CaCO3沉淀,各离子仍能大量共存,A项正确;B项中通入CO2后SiO2-3因转化为H2SiO3沉淀而不能大量存在;C 项中Fe2+与Cl2发生氧化还原反应不能大量共存;D项中Ag+与NH3·H2O因能生成银氨配离子而不能大量共存。
答案:A3.常温下,下列各组离子一定能在指定溶液中大量共存的是( )A.使酚酞变红色的溶液中:Na+、Al3+、SO2-4、Cl-B.K wc(H+)=1×10-13mol·L-1的溶液中:NH+4、Ca2+、Cl-、NO-3C.与Al反应能放出H2的溶液中:Fe2+、K+、NO-3、SO2-4D.水电离的c(H+)=1×10-13mol·L-1的溶液中:K+、Na+、AlO-2、CO2-3解析:使酚酞变红色的溶液呈碱性,Al3+不能大量存在,A不符合题意;K wc(H+)=1×10-13mol·L-1的溶液呈强酸性,四种离子能大量共存,B符合题意;与Al反应能放出H2的溶液可能呈强酸性也可能呈强碱性,酸性条件下NO-3氧化Fe2+生成Fe3+,碱性条件下,Fe2+不能存在,C项不符合题意;水电离的c(H+)=1×10-13mol·L-1的溶液可能呈强酸性也可能呈强碱性,酸性条件下,AlO-2、CO2-3都不能大量存在,D项不符合题意。
高一化学推断题和离子共存问题分析及习题(含答案)
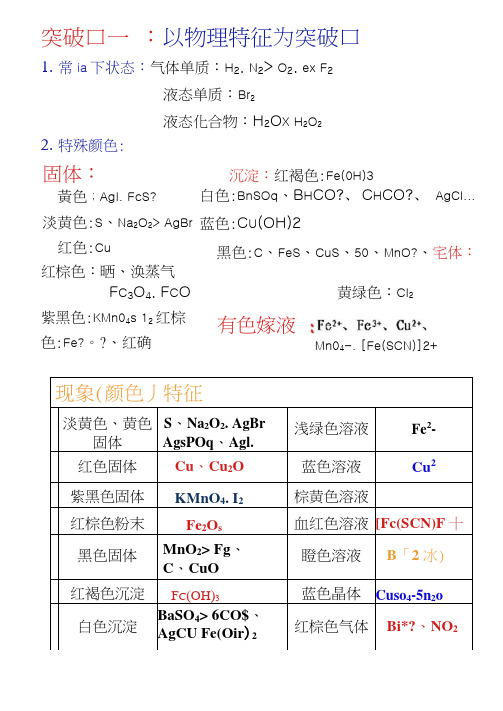
突破口一:以物理特征为突破口1.常ia下状态:气体单质:H2. N2> O2. ex F2液态单质:Br2液态化合物:H2O X H2O22.特殊颜色:沉淀:红褐色:Fe(0H)3白色:BnSOq、B H CO?、C H CO?、AgCl...蓝色:C U(OH)2黑色:C、FeS、CuS、50、MnO?、宅体:红棕色:晒、涣蒸气F C3O4.F C O黄绿色:Cl2紫黑色:KMn04s 12 红棕色:Fe?。
?、红确现象(颜色丿特征淡黄色、黄色固体S、Na2O2. AgBrAgsPOq、Agl.浅绿色溶液Fe2-红色固体Cu、Cu2O蓝色溶液Cu2紫黑色固体KMnO4. I2棕黄色溶液红棕色粉末Fe2O s血红色溶液[Fc(SCN)F 十黑色固体MnO2> Fg、C、CuO瞪色溶液B「2 冰)红褐色沉淀F C(OH)3蓝色晶体Cuso4-5n2o白色沉淀BaSO4> 6CO$、AgCU Fe(Oir)2红棕色气体Bi*?、NO2固体:黃色;AgI. FcS?淡黄色:S、Na2O2> AgBr红色:Cu有色嫁液Mn04-. [Fe(SCN)]2+符合下列情况的离子在溶液屮不能大量共存:(1)生成难溶物或微溶物的离子。
和助甘、Ag+、Ca^cOH■和Mg軒、Zi>2+、Ag+、AP+、F尹、F尹、Cu2+s Ca2+ CO32和Ca»、Mg?十、Ba2 . Ag\ Cu2\Ag+和Cl-等。
〜(2)生成气体或挥发性物质的离子。
如11+和C(V-、R和SO32、出和HCCV、川和HSO3、0H 和NHj等。
(3)生成难电离的物质的离子。
如川和CH3COO、小和0H等。
(4)酸式弱酸根离子(HCO<. llS03-> IIS、11卩0厂、H2PO4)既不能与印大量共存,又不能与0H大量共存。
(5)HSOq不能与0H大量共存°(6)发生氣化还原反应的离子。
高一化学离子反应测试题及答案解析

化学离子反应【1】一.选择题1.已知某酸性溶液中含有Ba2+、Mg2+,则下述离子组中能与上述离子共存的是()A.CO32-、Cl- B.NO3-、Cl- C.NO3-、SO42- D.OH-、NO3-2.在强碱性溶液中,下列各组离子能大量共存的是()A.Na+、 K+、CO32-、Cl-B.Cu2+、 Na+、NO3-、SO42-C.Na+、 K+、HCO3-、Cl-D.Mg2+、 Na+、NO3-、Cl-3.一种无色溶液中加入BaCl2溶液,生成不溶于硝酸的白色沉淀,则该溶液中()A.一定含有 SO42- B.一定含有 CO32-C.一定含Ag+D.可能含有 SO42-,也可能含有Ag+ 4.下列可以大量共存且溶液是无色的离子组是()A.H+,Na+,NO3-,MnO4-B.Fe2+,Mg2+,Cl-,SO42-C.H+,K+,OH-,NO3-D.NO3-,SO42-,K+,Mg2+5.巳知某溶液中存在较多的H+、SO42-、NO3-,则该溶液中还可能大量存在的离子组是()A.Al3+、CH3COO-、Cl-B.Mg2+、Ba2+、Br-C.Mg2+、Cl-、I- D.Na+、NH4+、Cl-6.下列电离方程式中,错误的是()A.NaHCO3 == Na++HCO3- B.H2SO4 == 2H++SO42-C.NaHS==Na++H++S2-D.NaHSO4==Na++H++SO42-7.下列物质的水溶液能导电,但属于非电解质的是()A.HClOB. Cl2C. NaHCO3D. CO28.能用H++OH-= H2O表示的是()A.NaOH溶液和CO2的反应B.Ba(OH)2溶液和稀H2SO4的反应C.NaOH溶液和盐酸反应D.氨水和稀H2SO4的反应9. 不能用离子方程式:CO32-+2H+=H2O+CO2↑来表示的反应是()A.BaCO3+HCl B.K2CO3+H2SO4 C.Na2CO3+HNO3 D.(NH4)2CO3+HCl 10.下列反应完成后没有沉淀的是()A.BaCl2溶液与Na2CO3溶液加足量稀CH3COOHB.Ba(OH)2溶液与KNO3溶液加足量稀H2SO4C.AgNO3溶液与Na2CO3溶液加足量稀HClD.AgNO3溶液与FeCl3溶液加足量稀HNO311.下列离子方程式书写正确的是()A.碳酸钙与盐酸反应:CO32-+2H+==CO2↑+H2OB.硫酸和氯化钡溶液反应:Ba2++SO42-==BaSO4↓C.氢氧化钠和硫酸反应:2OH-+H2SO4==SO42—+2H2OD.铁钉放入硫酸铜溶液中:Fe+3Cu2+==2Fe3++3Cu二.填空题(写出下列反应的离子方程式)12.铜片溶于稀硝酸:13.氯气被氢氧化钠溶液吸收:14.亚硫酸钠溶液加入溴水中:15.FeCl3溶液中加入铜片_____________________________________________16.Cl2通入水中__________________________________________________17.漂白粉投入水中,再通入CO2气体_________________________________________________18.电解饱和食盐水_________________________________________________三.推断题19.某溶液可能含下列阴离子:Cl-、SO42-、SO32-、S2-、CO32-的溶液:(1)若溶液中显强酸性,不能大量共存的离子是_______________。
高一化学离子共存试题答案及解析

高一化学离子共存试题答案及解析1.能在无色溶液中大量共存的一组离子是A.Cu2+、SO42—、OH—、K+B.Fe3+、Cl—、NO3—、H+C.K+、CO32—、Cl—、H+D.H+、Na+、Cl—、SO42—【答案】D【解析】A.Cu2+有色,且Cu2+与OH—反应;B.Fe3+有色;C.CO32—与H+反应;D.H+、Na+、Cl—、SO42—共存。
【考点】无色离子组大量共存的判断。
2.在酸性溶液中,下列各组离子能大量共存且溶液为无色透明的是【答案】C【解析】A、酸性溶液中H+与CO32-不能大量共存,错误;B、Cu2+是蓝色离子,同时酸性溶液中SO32-与NO3-发生氧化还原反应,不能大量共存,错误;C、酸性溶液中各离子都不反应,可以大量共存,正确;D、Fe2+有颜色,且在酸性条件下与NO3-发生氧化还原反应,不能大量共存,错误,答案选C。
【考点】考查给定条件的离子的共存判断3.某溶液能与锌片作用产生H2,则该溶液中可以大量共存的离子组是()A.Na+、NO3-、K+、Fe2+B.Fe2+、Na+、SO42-、K+C.K+、I-、NO3-、H+D.NH4+、NO3-、Na+、HCO3-【答案】B【解析】某溶液能与锌片作用产生H2,则该溶液显酸性。
A.在酸性条件下发生反应:NO3-+4H++3Fe2+= 3Fe3++NO↑+2H2O.故不能大量共存。
错误。
B.在酸性条件下Fe2+、Na+、SO42-、K+不会发生任何反应,可以大量共存。
正确。
C.在酸性条件下发生反应8H++6I-+2NO3-=3I2+2NO↑+4H2O故不能大量共存。
错误。
D.在酸性条件下发生反应:HCO3-+H+= CO2↑+H2O。
不断大量共存。
错误。
【考点】考查离子共存的知识。
4.已知SO32-的还原性大于I-的还原性,某无色溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是①肯定不含I-;②肯定不含Cu2+;③肯定含有SO32-;④可能含有I-A.①③B.①②③C.③④D.②③④【答案】D【解析】Cu2+的水溶液为蓝色,由于该溶液为无色,所以一定不含有Cu2+;因为SO32-的还原性大于I-的还原性,所以向该溶液中加入少量溴水,则首先发生反应: Br2+H2O+SO32-= SO42-+2H++2Br-.溶液仍呈无色。
高一化学离子共存试题答案及解析

高一化学离子共存试题答案及解析1.某无色溶液中只含有下列8种离子中的某几种:Mg2+、H+、Ag+、Na+、Cl-、HC、OH-、N,已知该溶液能与铝反应放出氢气。
试回答下列问题:(1)若反应后生成Al3+,则溶液中可能存在的离子有,一定存在的离子有,一定不存在的离子有,反应的离子方程式为。
(2)若反应后生成Al,则溶液中可能存在的离子有,一定存在的离子有,一定不存在的离子有,反应的离子方程式为。
【答案】(1)Mg2+、Na+H+、Cl-Ag+、HC、N、OH-2Al+6H+====2Al3++3H2↑(2)N、Cl-OH-、Na+H+、Mg2+、Ag+、HC2Al+2OH-+2H2O====2Al+3H2↑【解析】(1)若反应后生成Al3+,则说明该溶液显酸性,则HC、OH-不存在,若有HNO3则不能生成H2,所以也不存在N,则酸只能为HCl,故也不存在Ag+;一定存在H+、Cl-,Mg2+、Na+可能存在。
(2)反应后生成Al,说明溶液呈碱性,则H+、Mg2+、Ag+、HC一定不存在,一定存在OH-、Na+,N、Cl-可能存在。
【考点】铝及铝合金2.水溶液中能大量共存的一组离子是A.Na+、Ca2+、Cl-、SO42-B.Fe2+、H+、SO32-、ClO-C.Mg2+、NH4+、Cl-、SO42-D.K+、Fe3+、NO3-、SCN-【答案】C【解析】A、水溶液中发生反应:Ca2++SO42- CaSO4↓,不能大量共存,错误;B、酸性条件下ClO-与Fe2+、SO32-发生氧化还原反应,不能大量共存,错误;C、水溶液中,组内离子间不反应,能大量共存,正确;D、水溶液中发生络合反应:Fe3++3SCN- Fe(SCN)3,不能大量共存,错误。
【考点】考查离子共存问题。
3.下列各组离子中,在强碱性溶液中能大量共存是A.Na+、HCO3-、CO32-、K+B.K+、Ba2+、Cl-、NO3-C.Na+、NO3-、K+、S2-D.K+、NH4+、SO42-、Cl-【答案】BC【解析】审题“强碱性溶液”说明溶液中有大量的OH-,所以,A. HCO3-与OH-不能共存,错误;B.可以共存,正确;C.可以共存,正确;D. OH-与NH4+不能共存,错误。
第03讲 离子共存、离子的检验与推断(练习)(教师版) 2025年高考化学一轮复习讲练测新教材新高考

第03讲离子共存、离子的检验与推断题型一离子共存1.(2024·浙江·二模)常温下,在水溶液中能大量共存的离子组是A .+Na 、3NO -、23SiO -、I -B .2Fe +、H +、24SO -、3NO -C .4[Al(OH)]-、3HCO -、+Na 、Br -D .K +、32CH CH COO -、Cl -、H +【答案】A【解析】A .+Na 、3NO -、23SiO -、I -可以大量共存,A 正确;B .H +与3NO -可以氧化2Fe +,不可以大量共存,B 错误;C .4[Al(OH)]-与3HCO -反应生成氢氧化铝和碳酸根离子,不可以大量共存,C 错误;D .32CH CH COO -与H +生成弱电解质丙酸,不可以大量共存,D 错误;故选A 。
2.(2024·浙江·三模)在溶液中能大量共存的离子组是A .4Ti +、HCOO -、Cl -、K +B .24CrO -、Ag +、3NO -、2Zn +C .2Ba +、O H -、Na +、23SO -D .I -、SCN -、K +、4NH +【答案】D【解析】A .4Ti +与HCOO -会发生双水解而不能大量共存,A 项错误;B .24CrO -与Ag +会形成24Ag CrO 沉淀不能共存,B 项错误;C .2Ba +与23SO -会生成3BaSO 沉淀而不能大量共存,C 项错误;D .选项中所给离子相互都不反应,可以大量共存,D 项正确;本题选D 。
3.(2024·江西·一模)下列各组离子中,在给定的环境中一定能大量共存的是A .能使甲基橙变红的溶液:S 2-、2-4SO 、-3NO 、Na +B .常温下,由水电离的c(H +)=10-12的溶液中:Be 2+、-3NO 、K +、Cl -C .在水溶液中:-2AlO 、-3HCO 、Ba 2+、F -D .在漂白液中:OH -、Rb +、2-3CO 、2-4SO 【答案】D【解析】A .能使甲基橙变红的溶液含大量H +与S 2-不共存,酸性条件下,-3NO 有强氧化性,与S 2-会发生氧化还原反应不共存,A 错误;B .常温下,由水电离的c(H +)=10-12的溶液中,水的电离受到抑制,可能是酸性溶液,也可以是碱性溶液,OH -与Be 2+不共存,B 错误;C .-3HCO 与-2AlO 不共存,-3HCO +-2AlO +H 2O=()233CO Al OH -+↓,C 错误;D .在漂白液中:OH -、Rb +、2-3CO 、2-4SO 可大量共存,D 正确;故选D 。
高中化学离子共存、离子的检验与推断练习题(20201126211417)

高中化学离子共存、 离子的检验与推断练习题1.某混合溶液中所含离子的浓度如下表,则 M 离子可能为 ( )A.ClB . Ba 2++ 2+C .Na +D . Mg 2+解析:选 D 根据电荷守恒可知 M 带 2 个正电荷,由于 Ba 2+与 SO 42-不能大量共存,所以 M 是Mg 2+。
2.下列各组离子,能在溶液中大量共存的是 ( ) 3 + + - - + 2+ + -A .Al 3+、Na +、HCO 3-、OH -B . Na +、 Fe 2+、 H +、 NO 3-C .K +、 Fe 3+、SCN -、SO 23-D . Na +、 Ag +、H +、NO-3解析:选 D Al 3+、 HCO 3-、OH -相互之间会反应,不能大量共存, A 错误; Fe 2+、H +、 NO 3-能够发生氧化还原反应,不能大量共存, B 错误; Fe 3+、SCN -能够结合生成络合物, Fe 3 +、 SO 23-会发生氧化还原反应,不能大量共存, C 错误;该组离子之间不反应,能够大量共存,故 D 正确。
3.(2018·惠州三模 )下列有关 NaClO 和 NaCl 混合溶液的叙述正确的是 ( ) A .该溶液中, H +、NH 4+、SO 24-、I -可以大量共存 B .该溶液中, Ag +、K +、 NO 3-、NH 4+可以大量共存 C .该溶液中, Fe 2+、Fe 3+、Cl -、NO 3-可以大量共存D .向该溶液中加入浓盐酸,每产生 1 mol Cl 2,转移电子约为 6.02 ×10 23个解析:选 D A 项, ClO -和 H +结合成的 HClO 具有强氧化性,能把 I -氧化成 I 2,不能大 量共存; B 项, Ag +和 Cl -不能大量共存; C 项, ClO -具有强氧化性,能把 Fe 2+氧化成 Fe 3+, 不能大量共存; D 项,加入浓盐酸发生反应 ClO -+Cl -+2H +===Cl 2↑+H 2O ,因此每产生 1 mol Cl 2 ,转移 1 mol 电子。
高一化学离子共存试题答案及解析

高一化学离子共存试题答案及解析1.在能使酚酞变红的无色溶液中,可以大量共存的离子组是()A.Na+、Cu2+、Cl-、B.Na+、、K+、C.K+、、、Cl-D.Ca2+、、Na+、Cl-【答案】B【解析】因为显示紫红色,Cu2+显示蓝色,而溶液是无色透明的,所以可以排除A、D选项;能使酚酞变红的溶液中含有OH-,可以和OH-反应,其反应的离子方程式为+OH-====H2O+ ,排除C选项。
【考点】离子反应2.下列各组离子中,能大量共存且形成无色透明溶液的是A.Mg2+、H+、C1-、OH-B.Na+、Ba2+、C1-、NO3-C.Na+、H+、Cl-、CO32-D.K+、Cu2+、NO3-、SO42-【答案】B【解析】据题意无色溶液,可先排除D选项,因为铜离子是蓝色的。
A选项氢离子与氢氧根离子不能大量共存,C选项氢离子与碳酸根离子不能大量共存。
因此答案选B【考点】考查离子共存问题的相关知识点3.某溶液中存在大量的H+、Clˉ、Fe3+,该溶液中还可能大量存在的离子是A.OHˉB.Ag+C.CO D.SO【答案】D【解析】OHˉ与H+、Fe3+不能大量共存;Ag+与Clˉ不能大量共存;CO与H+、Fe3+不能大量共存。
【考点】考查离子的共存。
4.下列各组离子在指定的溶液中能大量共存的是A.在pH=1的溶液中:Fe2+、NO3-、SO42-、Na+B.能溶解Al(OH)3的溶液中:NH4+、SO42-、Cl-、HCO3-C.酚酞呈红色的溶液中:K+、Na+、AlO2-、NO3-D.含有大量Fe2+的溶液中:H+、K+、ClO-、SO42-【答案】C【解析】离子间如果发生化学反应,则不能大量共存,反之是可以的,A、在pH=1的溶液显酸性,则Fe2+与NO3-在酸性条件下发生氧化还原反应,A不正确;B、能溶解Al(OH)3的溶液可能显酸性,也可能显碱性,如果显酸性则HCO3-不能大量共存;如果显碱性则NH4+、HCO3-均不能大量共存,B不正确;C、酚酞呈红色的溶液显碱性,四种离子均大量共存,C正确;D、H+与ClO-不能大量共存,另外ClO-与Fe2+之间发生氧化还原反应,D不正确,答案选C。
高一离子共存试题及答案

高一离子共存试题及答案一、选择题1. 下列各组离子中,能大量共存的一组是()A. H+、OH-、Cl-B. Ca2+、CO32-、Na+C. Fe3+、OH-、H+D. Ag+、Cl-、K+答案:D解析:A选项中,H+和OH-会结合生成水,不能共存;B选项中,Ca2+和CO32-会结合生成碳酸钙沉淀,不能共存;C选项中,Fe3+和OH-会结合生成氢氧化铁沉淀,不能共存;D选项中,Ag+、Cl-和K+之间不会发生反应,可以大量共存。
2. 在碱性溶液中,能大量共存的离子组是()A. Al3+、AlO2-、HCO3-B. NH4+、AlO2-、HCO3-C. OH-、AlO2-、HCO3-D. Al3+、NH4+、HCO3-答案:C解析:在碱性溶液中,OH-浓度较高。
A选项中,Al3+和AlO2-会结合生成氢氧化铝沉淀,不能共存;B选项中,NH4+和OH-会结合生成氨水,不能共存;C选项中,OH-、AlO2-和HCO3-之间不会发生反应,可以大量共存;D选项中,Al3+和HCO3-会结合生成氢氧化铝沉淀,不能共存。
3. 在加入铝粉能产生氢气的溶液中,能大量共存的离子组是()A. K+、AlO2-、HCO3-B. Al3+、AlO2-、HCO3-C. OH-、AlO2-、HCO3-D. Al3+、NH4+、HCO3-答案:A解析:在加入铝粉能产生氢气的溶液中,溶液可能呈酸性或碱性。
A选项中,K+、AlO2-和HCO3-之间不会发生反应,可以大量共存;B选项中,Al3+和AlO2-会结合生成氢氧化铝沉淀,不能共存;C选项中,HCO3-和OH-会结合生成碳酸根离子和水,不能共存;D选项中,Al3+和HCO3-会结合生成氢氧化铝沉淀,不能共存。
二、填空题4. 在酸性溶液中,下列离子能大量共存的是()。
A. Na+、Cl-、HCO3-B. Na+、Cl-、SO32-C. Na+、Cl-、NO3-D. Na+、Cl-、AlO2-答案:C解析:在酸性溶液中,H+浓度较高。
2020年高考化学一轮总复习文档:第二章第6讲离子共存与离子推断含答案

第6讲 离子共存与离子推断一、离子共存1.离子共存问题是离子反应条件和本质的最直接应用。
所谓几种离子在同一溶液中能大量共存,就是指离子之间□01不发生反应;若离子之间能□02发生反应,则不能大量共存。
2.离子共存判断判断多种离子能否大量共存于同一溶液中,归纳起来就是:一色、二性、三特殊、四反应。
(1)一色——溶液颜色 几种常见离子的颜色:(2)二性——溶液的酸碱性①在强酸性溶液中,□06OH -及弱酸根离子(如□07CO 2-3、□08SO 2-3、S 2-、CH 3COO -等)均不能大量存在。
②在强碱性溶液中,□09H +及弱碱阳离子(如□10NH +4、Al 3+、□11Fe 3+等)均不能大量存在。
③酸式弱酸根离子(如□12HCO -3、HSO -3、□13HS -等)在强酸性或强碱性溶液中均不能大量存在。
(3)三特殊——三种特殊情况①AlO -2与HCO -3不能大量共存,反应的离子方程式为:□14AlO -2+HCO -3+H 2O===Al(OH)3↓+CO 2-3。
②“NO -3+H +”组合具有强氧化性,能与□15S 2-、□16Fe 2+、I -、SO 2-3等还原性的离子因发生氧化还原反应而不能大量共存。
③NH +4与CH 3COO -、CO 2-3,Mg 2+与HCO -3等组合中,虽然两种离子都能水解且水解相互促进,但总的水解程度仍很小,它们在溶液中能大量共存。
(4)四反应——四种反应类型指离子间通常能发生的四种类型的反应,能相互反应的离子显然不能大量共存。
①复分解反应,如Ba 2+与□17SO 2-4,NH +4与□18OH -,H +与CH 3COO -等。
②氧化还原反应,如Fe 3+与□19I -、S 2-,NO -3(H +)与Fe 2+,MnO -4(H +)与Cl -等。
③相互促进的水解反应,如Al 3+与HCO -3,Al 3+与AlO -2等。
④络合反应,如Fe 3+与□20SCN -等。
高一化学离子共存试题答案及解析

高一化学离子共存试题答案及解析1.下列是某无色水样成分的检验,已知该水样中只可能含K+、Mg2+、Fe3+、Cu2+、Ag+、Ca2+、C、S、Cl-中的若干种离子,该小组同学取100 mL水样进行实验:向样品中先滴加硝酸钡溶液,再滴加1 mol·L-1硝酸,实验过程中沉淀质量的变化如下图所示:(1)水样中一定含有的阴离子是,其物质的量浓度之比为。
(2)写出BC段曲线所表示反应的离子方程式:。
(3)由B点到C点变化过程中消耗硝酸的体积为。
(4)试根据实验结果推测K+是否存在?(填“是”或“否”);若存在,K+的物质的量浓度c(K+)的范围是(若K+不存在,则不必回答)。
(5)设计简单实验验证原水样中可能存在的离子:(写出实验步骤、现象和结论)。
【答案】(1)S、C1∶2(2)BaCO3+2H+====Ba2++CO2↑+H2O(3)40 mL(4)是c(K+)≥0.6 mol·L-1(5)取少量水样于试管中,向其中加入过量的硝酸钡溶液和稀硝酸,待沉淀完全后,向上层清液中滴加硝酸银溶液,若产生白色沉淀,则原水样中含Cl-,若不产生白色沉淀,则原水样中不含Cl-【解析】(1)该水样为无色溶液,Fe3+、Cu2+不存在,依据图像分析加入硝酸钡溶液生成沉淀,加入稀硝酸,沉淀部分溶解证明水样中一定含有S、C,又因为C与Ag+、Ca2+、Mg2+发生反应生成沉淀不能大量存在,所以Ag+、Ca2+、Mg2+不存在;n(S)==0.01mol,m(BaCO3)=6.27 g-2.33 g=3.94 g,n(C)=n(BaCO3)==0.02 mol;c(S)∶c(C)=1∶2;(2)BC段所表示反应是碳酸钡溶于稀硝酸的反应,反应的离子方程式为BaCO3+2H+====Ba2++CO2↑+H2O;(3)由B点到C点变化过程中依据图像分析溶解的碳酸钡的物质的量n(BaCO3)=0.02 mol;消耗稀硝酸物质的量为0.04 mol,消耗硝酸的体积==0.04 L="40" mL;(4)依据电解质溶液呈电中性,阳离子K+一定存在;根据电荷守恒得到:0.01 mol×2+0.02 mol×2+n(Cl-)=n(K+)推知n(K+)≥0.06 mol,则c(K+)≥0.6 mol·L-1;(5)可能存在的离子是Cl-,实验设计为:取少量水样于试管中,向试管中加入过量的硝酸钡溶液和稀硝酸,待沉淀完全和无气体生成后,向上层清液中滴加适量的硝酸银溶液,若生成白色沉淀,则原水样中含有Cl-,若无白色沉淀生成,证明无Cl-存在。
高一化学离子共存试题答案及解析

高一化学离子共存试题答案及解析1.某无色透明的酸性溶液中能大量共存的一组离子是A.、、Al3+、Cl-B.Na+、、K+、C.、K+、、Na+D.Mg2+、Na+、、【答案】D【解析】因为显示紫红色,而溶液是无色透明的,所以可以排除C选项;弱酸的酸根离子在酸性溶液中可以和H+反应生成相应的弱酸,所以和H不能在此溶液中大量共存,其反应的离子方程式分别为+2H+====H2O+CO2↑、+H+====H2O+CO2↑,排除A和B选项。
【考点】离子反应2.在能使酚酞变红的无色溶液中,可以大量共存的离子组是()A.Na+、Cu2+、Cl-、B.Na+、、K+、C.K+、、、Cl-D.Ca2+、、Na+、Cl-【答案】B【解析】因为显示紫红色,Cu2+显示蓝色,而溶液是无色透明的,所以可以排除A、D选项;能使酚酞变红的溶液中含有OH-,可以和OH-反应,其反应的离子方程式为+OH-====H2O+ ,排除C选项。
【考点】离子反应3.下列各组离子在指定的溶液中能大量共存的是A.在pH=1的溶液中:Fe2+、NO3-、SO42-、Na+B.能溶解Al(OH)3的溶液中:NH4+、SO42-、Cl-、HCO3-C.酚酞呈红色的溶液中:K+、Na+、AlO2-、NO3-D.含有大量Fe2+的溶液中:H+、K+、ClO-、SO42-【答案】C【解析】离子间如果发生化学反应,则不能大量共存,反之是可以的,A、在pH=1的溶液显酸性,则Fe2+与NO3-在酸性条件下发生氧化还原反应,A不正确;B、能溶解Al(OH)3的溶液可能显酸性,也可能显碱性,如果显酸性则HCO3-不能大量共存;如果显碱性则NH4+、HCO3-均不能大量共存,B不正确;C、酚酞呈红色的溶液显碱性,四种离子均大量共存,C正确;D、H+与ClO-不能大量共存,另外ClO-与Fe2+之间发生氧化还原反应,D不正确,答案选C。
【考点】考查离子共存的正误判断4.在酸性溶液中,下列各组离子能大量共存且溶液为无色透明的是【答案】C【解析】A、酸性溶液中H+与CO32-不能大量共存,错误;B、Cu2+是蓝色离子,同时酸性溶液中SO32-与NO3-发生氧化还原反应,不能大量共存,错误;C、酸性溶液中各离子都不反应,可以大量共存,正确;D、Fe2+有颜色,且在酸性条件下与NO3-发生氧化还原反应,不能大量共存,错误,答案选C。
离子共存、离子的检验和推断(有答案)

离子共存、离子的检验和推断题组一无限制条件的离子大量共存的判断1.能在水溶液中大量共存的离子组是()A.H+、Fe3+、SO、I-B.H+、NH、HCO、NOC.Ag+、K+、Cl-、SOD.K+、AlO、Cl-、OH-答案 D解析A2A.Al3+B.H+、C.Na+、D.K+、答案解析B题组二3A.K+、B.NH、C.Ca2+D.Na+、答案 A解析B反应生成CO和H2O4A.K+、B.H+、NH、Al3+、SOC.Na+、Cl-、MnO、SOD.Na+、CO、CH3COO-、HCO答案 B解析A中SiO能与SO2反应生成沉淀,NO(H+)能氧化SO2;C中MnO能与SO2发生氧化还原反应;D中CO、CH3COO -、HCO均能与SO2反应。
题组三有限制条件的离子大量共存的判断5.下列各组离子在指定的溶液中,能大量共存的划“√”,不能大量共存的划“×”(1)含有大量Fe3+的溶液:Na+、SCN-、Cl-、I-()(2)含有大量NO的溶液:H+、Fe2+、Cl-、SO()(3)常温下,pH=12的溶液:K+、Cl-、SO()(4)c(H+)=0.1mol·L-1的溶液:Na+、NH、SO、S2O()(5)使pH试纸显蓝色的溶液:Cu2+、NO、Fe3+、SO()(6)与铝粉反应放出H2的无色溶液:NO、Al3+、Na+、SO()(7)使红色石蕊试纸变蓝的溶液:SO、CO、Na+、K+()(8)常温下=1×10-12的溶液:K+、AlO、CO、Na+()(9)中性溶液:Fe3+、Al3+、NO、SO()(10)2++(11)c(H+(12)答案(7)√(13)×1(1))(2)(3)2NH,该答案3.答案题组一1A.加入B.通入Cl2后,溶液变为深黄色,加入淀粉溶液后溶液变蓝,可确定有I-存在C.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸后沉淀不溶解时,可确定有SO存在D.加入稀盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO存在答案 B解析Cl-、SO均能与Ag+形成不溶于稀盐酸的白色沉淀,A错;I2遇淀粉变蓝,通入Cl2后,溶液变为深黄色,加入淀粉溶液后溶液变蓝,则溶液中有I-存在,B对;SO与Ba(NO3)2反应形成BaSO3沉淀,加入稀盐酸后在H+、NO的作用下可转化为BaSO4沉淀,C错;能使澄清石灰水变浑浊的气体是CO2或SO2,原溶液中可能存在的离子是CO、HCO、SO或HSO,D错。
高中化学离子共存物质分类离子方程式无机推断练习题(附答案)

高中化学离子共存物质分类离子方程式无机推断练习题一、单选题1.下列有关NaClO 和NaCl 混合溶液的叙述正确的是( )A .该溶液中,H +、+4NH 、2-4SO 、Br-可以大量共存B .该溶液中,Ag +、K +、-3NO 、CH 3CHO 可以大量共存C .向该溶液中滴入少量FeSO 4溶液,反应的离子方程式为: 2Fe 2++ClO -+2H +=== Cl -+2Fe 3++H 2OD .向该溶液中加入浓盐酸,每产生1mol Cl 2,转移电子约为6.02×1023个 2.下列说法正确的是( ) A.酸性氧化物都是非金属氧化物B.2O 和3O 互为同素异形体,二者相互转化属于氧化还原反应C.22Na O 和2O 分别属于电解质、非电解质D.由二种元素的阴离子与另一种元素的阳离子构成的物质一定是纯净物 3.下列法正确的是( )A.碱都是强电解质,酸都是弱电解质B.NH 3的水溶液能导电,所以NH 3比为电解质C.强电解质溶液的导电能力很强D.CaCO 3在水中的溶解度小,但溶解的部分完全电离,故CaCO 3是强电解质 4.下列指定反应的离子方程式正确的是( ) A .氯气溶于水:Cl 2+H 2O=2H ++Cl -+ClO -B .Na 2CO 3溶液中2-3CO 的水解:2-3CO +H 2O=-3HCO +OH -C .酸性溶液中KIO 3与KI 反应生成I 2:-3IO +I -+6H +=I 2+3H 2OD .NaHCO 3溶液中加足量Ba(OH)2溶液:-3HCO +Ba 2++OH -=BaCO 3↓+H 2O5.给定条件下,下列选项中所示的物质间转化均能一步实现的是( )A.粗硅4SiCl SiB. ()2Mg OH ()2MgCl aq MgC. 23Fe O ()3FeCl aq 无水3FeClD. ()3AgNO aq ()()32Ag NH OH aq ⎡⎤⎣⎦Ag6.称取424()NH SO 和44NH HSO 混合物样品7.24g,加入含0.1mol NaOH 的溶液,完全反应,生成3NH 1792mL(标准状况),则424()NH SO 和44NH HSO 的物质的量比为( )A.1:1B.1:2C.1.87:1D.3.65:17.酸性条件下,22H O 可氧化CuS :+2+222CuS+H 2H =Cu +S+2H O O +。
高一化学离子共存试题答案及解析

高一化学离子共存试题答案及解析1.某无色溶液中含有K+、Cl-、OH-、SO32-、SO42-,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞试液。
检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
请回答下列问题:(1)白色沉淀A与试剂②反应的离子方程式是__________________________________。
(2)无色溶液C中加入试剂③的主要目的是____________________________________。
(3)试验中若只加试剂③而不加试剂②,对实验的影响是_______________________。
(4)气体E通入试剂④发生反应的离子方程式是__________________________________。
【答案】(1) BaSO3 + 2H+ Ba2+ + SO2↑ + H2O (2分)(2)中和OH-,防止对Cl-的检验产生干扰(2分)(3)会使SO32-对SO42-的检验产生干扰,不能确定SO42-和SO32-是否存在(2分)(4) SO2 + Br2+ 2H2O 4H+ + SO42- + 2Br-(2分)【解析】亚硫酸根离子和硫酸根离子都可以与钡离子反应生成白色沉淀,而亚硫酸钡沉淀不溶于水但能溶解在酸中,但硫酸钡沉淀既不溶解在水中,也不溶解在酸中。
亚硫酸根离子在硝酸溶液中会被氧化为硫酸根离子,因此要检验硫酸根离子的存在时要先排除掉亚硫酸根离子对其的干扰,因此加的试剂1应为盐酸,【考点】2.下列各组离子在给定条件下能大量共存的是A.强酸性溶液中:NH4+、K+、ClO-、Cl-B.有SO42—存在的溶液中:Na+、Mg2+、Ba2+、I-C.加入铝粉能放出氢气的溶液中:K+、Ba2+、Cl-、Br-D.在含有大量[Al(OH)4]-的溶液中:NH4+、Na+、Cl-、H+【答案】C【解析】A、强酸性溶液中:NH4+与OH-不能大量共存,错误;B、有SO42—存在的溶液中Ba2+与SO42—生成硫酸钡沉淀,不能大量共存,错误;C、加入铝粉能放出氢气的溶液为酸性或碱性,4种离子彼此都不反应,能大量共存,正确;D、在含有大量[Al(OH)4]-的溶液中NH4+、H+都不能大量共存,错误,答案选C。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.在碱性溶液中能大量共存且溶液为无色透明的离子组是( B )
A.K+、Na+、MnO4-、Cl-
B.K+、NO3-、Na+、CO32-
C.H+、Na+、SO42-、NO3-
D.Na+、Fe3+ SO42-、Cl-
2.下列溶液中,因氧化—还原反应而不能大量共存的离子组是( D )
A.K+、Ag+、NO3-、Cl-
B.Ba2+、Na+、SO42-、NO3-
C.K+、H+、CO32-、Cl-
D.Mg2+、Na+、ClO-、I-
3.下列离子在溶液中能大量共存,加入OH-能产生白色沉淀的是( C )
A. Na+、Ca2+、SO42-、Cl-
B. H+、Mg2+、CO32-、Cl-
C. K+、Mg2+、SO42-、NO3-
D. K+、Na+、NO3-、CO32-
4. 已知某溶液中存大较多的H+、SO42-、NO3-,则该溶液中还能大量存在的离子组是( D )
A. Al3+、CH3COO-、Cl-
B. Mg2+、Ba2+、Br-
C. Cu2+、Cl-、I-
D. Na+、NH4+、Cl-
5.A、B、C和D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种,现利用另一种溶液X,用如下图所示的方法,即可将它们一一确定。
试确定A、B、C、D、X各代表何种溶液。
A:_________B:_________C:__________D:__________X:__________
6.短周期元素A、B、C、D中,0.5mol A元素的离子得到6.02×1023个电子被还原为中性原子,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,A原子核内质子数目与中子数目相等,B元素原子核外M层电子数目比K层多1个,C―比A元素的离子多1个电子层,D元素的原子核外L层比K层多2个电子。
(1)A、B、C、D四种元素的名称分别是、、、。
(2)画出C―和D原子的结构示意图
(3)向B、C两种元素形成的化合物的水溶液里逐滴滴入苛性钠溶液,现象为______________________,写出有关离子方程式_________________________________________________________。
参考答案
1.B
2.D
3.C
4.D
5.A:NaOH B:NaNO3C:Ba(NO3)2D:HNO3X:MgSO4
6.(1)镁、铝、氯、碳;
(2) 、;
(3)Al3++3OH-===Al(OH)3↓;Al(OH)3+OH-==AlO2-+2H2O。
