五年高考试题汇编化学平衡.docx
2012年高考化学分类汇编---化学平衡

1 2012年高考化学分类汇编---化学平衡电离平衡 水解平衡 溶解平衡 化学平衡13.(重庆)在一个不导热的密闭反应器中,只发生两个反应: a(g)+b(g)2c(g);△H 1<0,x(g)+3y(g)2z(g);△H 2>0进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是(A) A.等压时,通入惰性气体,c 的物质的量不变 B.等压时,通入z 气体,反应器中温度升高 C.等容时,通入惰性气体,各反应速率不变 D.等容时,通入z 气体,y 的物质的量浓度增大答案:首先要通入惰性气体又要保持压强不变,那么只能增大容积了,那么对于参加反应的气体来说实际上就是减压,此时第二个可逆反应左移,放出热量,而压强对第一个反应没有影响;但是由于压强变化导致的温度变化却能影响第一个可逆反应(题目有绝热字样),温度升高因而第一个可逆反应也要左移,故而c 的物质的量应该是减少的。
选A 。
29.(重庆)尿素[]22()CO NH 是首个由无机物人工合成的有机物。
(1)工业上尿素CO 2和NH 3,在一定条件下合成,其反应方程式为 。
(2)当氨碳比的转化率随时间的变化关系如题29图1所示.①A 点的逆反应速率2)v CO 速( B 点的正反应速率为2)v CO 正((填“大于”、“小于”或“等于”)②NH 3的平衡转化率为 。
答案:8 、(大纲)合成氨所需的氢气可用煤和水作原料经多步反映值得,其中的一步反应为(B )CO (g )+ H 2O(g) −−−→←−−−催化剂CO 2(g) + H 2(g) △H <0反应达到平衡后,为提高CO 的转化率,下列措施中正确的是A 增加压强B 降低温度C 增大CO 的浓度D 更换催化剂12 (福建)一定条件下,溶液的酸碱性对TiO 2光催化染料R降322()4,()n NH CO n CO =C O 2 转化率/%解反应的影响如右图所示。
下列判断正确的是A.在0-50min之间,pH =2 和PH= 7 时R 的降解百分率相等B.溶液酸性越强,R 的降解速率越小C.R的起始浓度越小,降解速率越大D.在20-25min之间,pH = 10 时R 的平均降解速率为0.04mol·L-1·min-1答案:A解析:A项:在0-50min内,PH=2时,20min时,R已经降解完了,因此R平均降解速率计算按0-20min,而PH=7时,40min时,R已经降解完了,因此R平均降解速率计算按0-40min,通过计算,正确;B项:,PH=2时大约在20min降解完,PH=7大约在40min降解完,但是起始浓度不相同,所以溶液的酸性与R降解速率没有直接联系,错误。
2024年高考化学真题模拟题专项汇编__10水溶液中的离子平衡含解析

专题10 水溶液中的离子平衡2024年高考真题1.【2024年7月浙江选考】下列物质在熔融状态下不导电...的是( )A .B .C .D .【答案】C【解析】A.NaOH属于离子化合物,其在熔融状态下能电离成自由移动的Na+和OH-,故其在熔融状态下能导电,A不符合题意;B.CaCl2属于离子化合物,其在熔融状态下能电离成自由移动的Ca2+和Cl-,故其在熔融状态下能导电,B不符合题意;C.HCl是共价化合物,其在熔融状态下不能电离成离子,故其在熔融状态下不导电,C符合题意;D.K2SO4属于离子化合物,其在熔融状态下能电离成自由移动的K+和SO,故其在熔融状态下能导电,D不符合题意。
综上所述,本题答案为C。
2.【2024年7月浙江选考】水溶液呈酸性的是( )A .B .C .D .【答案】B【解析】A.NaCl是强酸强碱盐,其不能水解,故其水溶液呈中性,A不符合题意;B.NaHSO4是强酸的酸式盐,其属于强电解质,其在水溶液中的电离方程式为NaHSO4=Na++H++SO,故其水溶液呈酸性,B符合题意;C.HCOONa属于强碱弱酸盐,其在水溶液中可以完全电离,其电离产生的HCOO-可以发生水解,其水解的离子方程式为HCOO-+H2O⇌HCOOH+OH-,故其水溶液呈碱性,C不符合题意;D.NaHCO3是强碱弱酸盐,既能发生电离又能发生水解,但其水解程度大于电离程度,故其水溶液呈碱性,D不符合题意。
综上所述,本题答案为B。
3.【2024年新课标】以酚酞为指示剂,用0.1000 mol·L−1的NaOH溶液滴定20.00 mL未知浓度的二元酸H2A溶液。
溶液中,pH 、分布系数随滴加NaOH溶液体积V NaOH的改变关系如图所示。
[比如A2−的分布系数:]下列叙述正确的是A.曲线①代表,曲线②代表B.H2A溶液的浓度为0.2000 mol·L−1C.HA−的电离常数K a=1.0×10−2D.滴定终点时,溶液中【答案】C【解析】【分析】依据图像,曲线①代表的粒子的分布系数随着NaOH的滴入渐渐减小,曲线②代表的粒子的分布系数随着NaOH的滴入渐渐增大,粒子的分布系数只有1个交点;当加入40mLNaOH溶液时,溶液的pH在中性发生突变,且曲线②代表的粒子达到最大值接近1;没有加入NaOH时,pH约为1,说明H2A第一步完全电离,其次步部分电离,曲线①代表δ(HA-),曲线②代表δ(A2-),依据反应2NaOH+H2A=Na2A+2H2O,c(H2A)==0.1000mol/L,据此分析作答。
2009-2013年高考化学试题分类汇编:化学反应速率和化学平衡
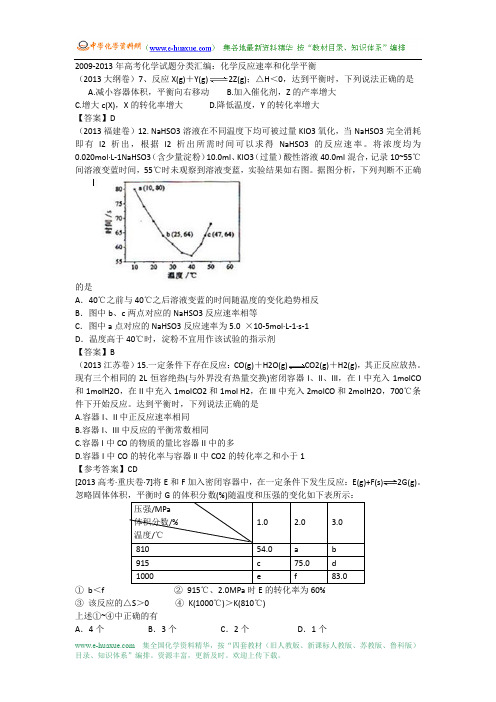
2009-2013年高考化学试题分类汇编:化学反应速率和化学平衡(2013大纲卷)7、反应X(g)+Y(g)2Z(g);△H<0,达到平衡时,下列说法正确的是A.减小容器体积,平衡向右移动B.加入催化剂,Z的产率增大C.增大c(X),X的转化率增大D.降低温度,Y的转化率增大【答案】D(2013福建卷)12. NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3的反应速率。
将浓度均为0.020mol·L-1NaHSO3(含少量淀粉)10.0ml、KIO3(过量)酸性溶液40.0ml混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如右图。
据图分析,下列判断不正确的是A.40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反B.图中b、c两点对应的NaHSO3反应速率相等C.图中a点对应的NaHSO3反应速率为5.0 ×10-5mol·L-1·s-1D.温度高于40℃时,淀粉不宜用作该试验的指示剂【答案】B(2013江苏卷)15.一定条件下存在反应:CO(g)+H2O(g)CO2(g)+H2(g),其正反应放热。
现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO 和1molH2O,在II中充入1molCO2和1mol H2,在III中充入2molCO和2molH2O,700℃条件下开始反应。
达到平衡时,下列说法正确的是A.容器I、II中正反应速率相同B.容器I、III中反应的平衡常数相同C.容器I中CO的物质的量比容器II中的多D.容器I中CO的转化率与容器II中CO2的转化率之和小于1【参考答案】CD。
[2013高考∙重庆卷∙7]将E和F加入密闭容器中,在一定条件下发生反应:忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:①b<f③该反应的△S>0 ④K(1000℃)>K(810℃)上述①~④中正确的有A.4个B.3个C.2个D.1个答案:A【解析】同温下,增大压强,平衡逆向进行,平衡时G的体积分数变小,故可知c>75.0>54.0>a>b,利用c>75.0>54.0可知同压下,升温平衡正向移动,即正反应为吸热反应,从而可知f>75.0,所以①正确;在915℃、2M Pa下,设E的起始量为amol,转化率为x,则平衡时G的量为2ax,由题意得2ax/(a-ax+2ax)=75%,解得x=0.6,②正确;该题是气体体积增大的反应,因此为熵增反应,③正确;结合前面分析知升温平衡正向移动,则平衡常数增大,④正确,故正确答案为:A。
专题41 化学平衡常数及计算(学生版)十年(2013-2022)高考化学真题分项汇编(全国通用)

专题41化学平衡常数及计算1.【2022年辽宁卷】某温度下,在1L 恒容密闭容器中2.0mol X 发生反应2X(s)Y(g)+2Z(g) ,有关数据如下:时间段/min 产物Z 的平均生成速率/-1-1mol L min⋅⋅0~20.200~40.150~60.10下列说法错误的是A .1min 时,Z 的浓度大于-10.20mol L ⋅B .2min 时,加入0.20mol Z ,此时正逆v (Z)<v (Z)C .3min 时,Y 的体积分数约为33.3%D .5min 时,X 的物质的量为1.4mol2.【2022年江苏卷】用尿素水解生成的3NH 催化还原NO ,是柴油机车辆尾气净化的主要方法。
反应为32224NH (g)+O (g)+4NO(g)4N (g)+6H O(g) ,下列说法正确的是A .上述反应ΔS<0B .上述反应平衡常数()()()()46224432c N c H O K=c NH c O c (NO)⋅⋅⋅C .上述反应中消耗31mol NH ,转移电子的数目为232 6.0210⨯⨯D .实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小3.(2021·湖南真题)已知:()()()A g 2B g 3C g + 0H ∆<,向一恒温恒容的密闭容器中充入1molA 和3molB 发生反应,1t 时达到平衡状态I ,在2t 时改变某一条件,3t 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
下列说法正确的是A .容器内压强不变,表明反应达到平衡B .2t 时改变的条件:向容器中加入C C .平衡时A 的体积分数ϕ:(II)(I)ϕϕ>D .平衡常数K :(II)(I)<K K 4.(2020·浙江高考真题)5 mL 0.1mol ⋅L −1KI 溶液与1 mL 0.1mol ⋅L −1FeCl 3溶液发生反应:2Fe 3+(aq )+2I −(aq )⇌2Fe 2+(aq )+I 2(aq ),达到平衡。
2005年全国各省市高考化学试题汇编2

2005年全国各省市高考化学试题汇编--------基本概念、基本理论(05广东)19、关于小苏打水溶液的表述正确的是A 、c (Na +)=c (HCO 3-) + c (CO 32-) + c (H 2CO 3)B 、c (Na +) + c (H +) = c (HCO 3-) + c (CO 32-) +c (OH -)C 、HCO 3- 的电离程度大于HCO 3-的水解程度D 、存在的电离有:NaHCO 3 = Na + + HCO 3-, HCO 3-H + + CO 32- H 2O H ++OH -(05广东)17、对可逆反应4NH 3(g ) + 5O 2 (g4NO (g ) + 6H 2O (g ),下列叙述正确的是A 、达到化学平稳时,4υ正(O 2)= 5υ逆(NO )B 、若单位时间内生成x mol NO 的同时,消耗x mol NH 3 ,则反应达到平稳状态C 、达到化学平稳时,若增加容器体积,则正反应速率减少,逆反应速率增大D 、化学反应速率关系是:2υ正(NH 3)= 3υ正(H 2O )(05广东)16、下列各组离子一定能大量共存的是A 、含有大量Fe 3+的溶液中:NH 4+、Na +、CI -、SCN -B 、在强碱溶液中:Na +、K +、AlO 2-、CO 32-C 、在c(H +)=10-13mol ·L -1的溶液中:NH 4+、Al 3+、SO 42-、NO 3-D 、在pH=1的溶液中:K +、Fe 2+、Cl -、NO 3-(05广东)15、一种新燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y 2O 3)的氧化锆(Z r O 2)晶体,在熔融状态下能传导O 2-。
下列对该燃料说法正确的是A 、在熔融电解质中,O 2-由负极移向正极B 、电池的总反应是:2C 4H 10 + 13O 2 → 8CO 2 + 10H 2O C 、通入空气的一极是正极,电极反应为:O 2 + 4e - = 2O 2-D 、通入丁烷的一极是正极,电极反应为:C 4H 10 + 26e - + 13O 2 = 4CO 2 + 5H 2O(05广东)14、在一定条件下,固定容积的密闭容器中反应:2NO 2(gO 2(g ) + 2NO (g );ΔH >0, 达到平稳。
山东省高考化学真题分类汇编专题07:化学平衡

山东省高考化学真题分类汇编专题07:化学平衡姓名:________ 班级:________ 成绩:________一、单选题 (共1题;共6分)1. (6分)在一定条件下,NO能跟H2发生如下反应:2NO+2H2═N2+2H2O.经研究,上述反应是按以下三步反应依次进行的总反应(括号中是该条件下反应的相对速率):(Ⅰ)2NO+H2═N2O+H2O(慢);(Ⅱ)2N2O═2N2+O2(快);(Ⅲ)2H2+O2═2H2O(更快).以上总反应的速率主要取决于三步反应中的()A . (Ⅰ)B . (Ⅱ)C . (Ⅲ)D . (Ⅱ)和(Ⅲ)二、多选题 (共1题;共4分)2. (4分)下列做法的目的与反应速率有关的是()A . 用冰箱冷藏食物B . 在糖果制作过程中添加着色剂C . 向食盐中添加碘酸钾D . 在化学反应中加入合适的催化剂三、实验探究题 (共2题;共30分)3. (15.0分) (2018高二上·广安期末) 某探究性学习实验小组做了如下实验:实验一:利用H2C2O4 溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:A29320.0250.13t1B T120.0230.1V18C31320.02V20.15t1(1)通过实验A、B,可探究出________ (填外部因素)的改变对反应速率的影响,其中V1=________,T1=________;通过实验________可探究出温度变化对化学反应速率的影响。
(2)若t1<8,则由此实验可以得出的结论是________;利用实验B 中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)= ________。
(3)实验二:探究酸的强弱对酸与镁条反应速率的影响。
实验步骤:(a)检查装置的气密性后,添加药品;(b)反应开始后,每隔1min 记录一次生成H2的体积;(c)将所记录的数据转化为曲线图(上图乙)。
高考化学选择题专项练习汇编-水溶液中的离子平衡

高考化学选择题专项练习汇编-水溶液中的离子平衡考试范围:水溶液中的离子平衡;命题人:韦东寒一、单选题1.(3分)常温下,下列关于pH=3的CH3COOH溶液的叙述正确的是()A.该溶液中由H2O电离出的c(OH−)=1.0×10−3mol⋅L−1B.与等体积pH=11的NaOH溶液混合,所得溶液呈中性C.该溶液中离子浓度大小关系:c(H+)>c(CH3COO−)>c(OH−)D.滴加0.1mol⋅L−1 CH3COONa溶液至c(CH3COO−)=c(Na+)时,溶液pH>72.(3分)H2C2O4(草酸)为二元弱酸,在水溶液中H2C2O4、HC2O4-和C2O42-物质的量分数与pH关系如图所示,下列说法不正确的是A.由图可知,草酸的K a=10-1.2B.0.1 mol·L—1NaHC2O4溶液中c(Na+)>c(HC2O4-)>c(H+)>c(OH-)C.向草酸溶液中滴加氢氧化钠溶液至pH为4.2时c(Na+)+c(H+)=3c(C2 O42-)+c(OH-) D.根据图中数据计算可得C点溶液pH为2.83.(3分)20℃时,用NaOH调节0.10mol/LH2C2O4溶液的pH,假设不同pH下均有c(H2C2O4)+c(HC2O4—)+c(C2O42-)=0.10mol/L。
使用数字传感器测得溶液中各含碳微粒的物质的量浓度随pH的变化曲线如下图。
下列有关分析正确的是A.曲线a代表H2C2O4浓度随pH的变化B.pH从4到6时主要发生的反应离子方程式为2OH-+H2C2O4====2H2O+C2O42-C.在曲线a、c交界点有:c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-)D.当溶液pH=7时:c(Na+)>c(C2O42-)>c(HC2O4-)>c(H2C2O4)4.(3分)25℃时,向20mL0.2mol·L-1NaCN溶液中加入0.2mol·L-1的盐酸,溶液pH 随所加盐酸体积的变化如图所示(M>7)。
2020-2021高考化学化学反应速率与化学平衡综合题汇编及详细答案

2020-2021高考化学化学反应速率与化学平衡综合题汇编及详细答案一、化学反应速率与化学平衡1.影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol/L、2 mol/L、18.4 mol/L)。
设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如下表实验步骤现象结论①分别取等体积的2mol/L的硫酸于试管中②反应速率Mg>Fe,Cu不反应金属的性质越活泼,反应速率越快(1)甲同学表中实验步骤②为____________________(2)甲同学的实验目的是:在相同的温度下,__________________________________。
实验二:乙同学为了更精确的研究浓度对反应速率的影响,利用下图所示装置进行定量实验。
(3)乙同学在实验中应该测定的数据是______________。
(4)乙同学完成该实验应选用的实验药品是______________________;该实验中不选用某浓度的硫酸,理由是_________________________。
【答案】分别投入大小、形状相同的Cu、Fe、Mg 研究金属(或反应物)本身的性质与反应速率的关系一定时间内产生气体的体积(或产生一定体积的气体所需时间) Mg(或Fe)和0.5 mol/L硫酸和2 mol/L硫酸常温下Mg与18.4 mol/L硫酸反应生成SO2,Fe在18.4 mol/L硫酸中钝化【解析】【分析】(1)要比较金属和稀硫酸的反应快慢,则应该使金属的形状和大小都是相同的,即分别投入形状、大小相同的Cu、Fe、Mg;(2)根据步骤和现象,目的是探究金属(反应物)本身的性质与反应速率的关系;(3)要定量研究,需要测定一定时间内产生气体的体积(或产生一定体积的气体所需要的时间);(4)浓硫酸和金属反应不能生成氢气,而铜与稀硫酸又不反应,所以选择的药品是Mg (或Fe)、0.5ol/L硫酸和2mol/L硫酸。
[高中化学历年高考题分类汇编7、溶液中平衡选择题练习
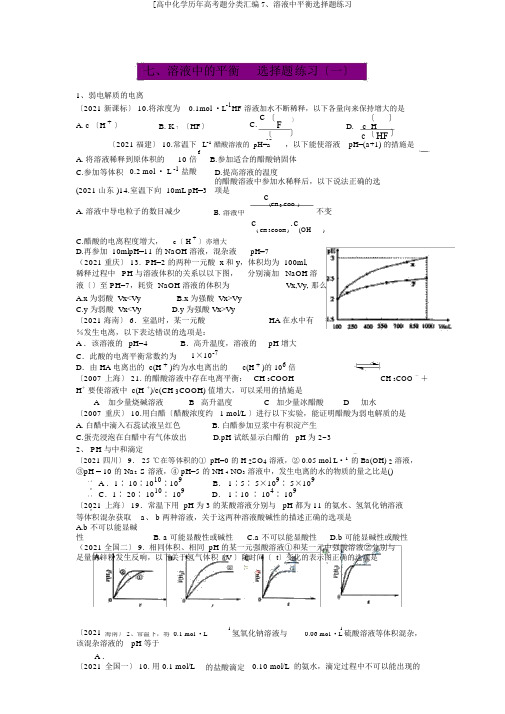
七、溶液中的平衡选择题 练习〔一〕1、弱电解质的电离〔2021 新课标〕 10.将浓度为 0.1mol ·L -1HF 溶液加水不断稀释,以下各量向来保持增大的是 A. c 〔H +〕B. K ? 〔HF 〕C.c 〔F-〕D.〔 〕〕c H〕〔c 〔 HFc H〔2021 福建〕 10.常温下 L -1醋酸溶液的 pH=a,以下能使溶液 pH=(a+1) 的措施是gA. 将溶液稀释到原体积的 10 倍B.参加适合的醋酸钠固体C.参加等体积 0.2 mol · L -1盐酸D.提高溶液的温度 (2021 山东 )14.室温下向 10mL pH=3 的醋酸溶液中参加水稀释后,以下说法正确的选项是A. 溶液中导电粒子的数目减少c(CH 3 COO )不变B. 溶液中c( CH 3COOH ).c(OH)C.醋酸的电离程度增大, c 〔 H + 〕亦增大D.再参加 10mlpH=11 的 NaOH 溶液,混杂液 pH=7 ( 2021 重庆〕 13. PH=2 的两种一元酸 x 和 y ,体积均为 100ml, 稀释过程中 PH 与溶液体积的关系以以下图, 分别滴加 NaOH 溶 液〔〕至 PH=7,耗资 NaOH 溶液的体积为 Vx,Vy, 那么 A.x 为弱酸 Vx<Vy B.x 为强酸 Vx>Vy C.y 为弱酸 Vx<Vy D.y 为强酸 Vx>Vy 〔2021 海南〕 6.室温时,某一元酸HA 在水中有 %发生电离,以下表达错误的选项是: A .该溶液的 pH=4 B .高升温度,溶液的pH 增大C .此酸的电离平衡常数约为 1×10-7D .由 HA 电离出的 c(H + )约为水电离出的 c(H + )的 106 倍CH 3COO -+〔2007 上海〕 21. 的醋酸溶液中存在电离平衡: CH 3COOHH +要使溶液中 c(H +)/c(CH 3COOH) 值增大,可以采用的措施是A 加少量烧碱溶液B 高升温度C 加少量冰醋酸D 加水〔2007 重庆〕 10.用白醋〔醋酸浓度约 1 mol/L 〕进行以下实验,能证明醋酸为弱电解质的是 A. 白醋中滴入石蕊试液呈红色 B. 白醋参加豆浆中有积淀产生 C.蛋壳浸泡在白醋中有气体放出 D.pH 试纸显示白醋的 pH 为 2~3 2、 PH 与中和滴定 -〔2021 四川〕 9. 25 ℃在等体积的① pH=0 的 H 2SO 4 溶液,② 0.05 mol L ·1 的 Ba(OH) 2 溶液, ③pH = 10 的 Na 2 S 溶液,④ pH=5 的 NH 4 NO 3 溶液中,发生电离的水的物质的量之比是()A .1∶ 10∶1010∶109B . 1∶5∶ 5×109∶ 5×109C .1∶ 20∶ 1010∶ 109D . 1∶10 ∶ 104∶ 109〔2021 上海〕 19.常温下用 pH 为 3 的某酸溶液分别与 pH 都为 11 的氨水、氢氧化钠溶液等体积混杂获取 a 、 b 两种溶液,关于这两种溶液酸碱性的描述正确的选项是 A.b 不可以能显碱性 B. a 可能显酸性或碱性 C.a 不可以能显酸性 D.b 可能显碱性或酸性( 2021 全国二〕 9. 相同体积、相同 pH 的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反响,以下关于氢气体积〔V 〕随时间〔 t 〕变化的表示图正确的选项是〔2021 -1氢氧化钠溶液与-1硫酸溶液等体积混杂,海南〕 2、常温下,将 0.1 mol ·L 0.06 mol ·L 该混杂溶液的 pH 等于A .〔2021 全国一〕 10. 用 0.1 mol/L的盐酸滴定 0.10 mol/L 的氨水,滴定过程中不可以能出现的结果是A. c( NH 4 ) > c(Cl ) , c(OH ) > c(H )B. c(NH 4 ) = c(Cl ) , c(OH ) = c(H )C. c(Cl ) > c(NH 4 ) , c(OH ) > c( H )D. c(Cl ) > c(NH 4 ) , c(H) > c(OH )〔2021 上海〕 20.关于常温下 pH 为 1 的硝酸溶液,以下表达正确的选项是 A .该溶液 lmL 稀释至 100mL 后, pH 等于 3B .向该溶液中参加等体积、 pH 为 13 的氢氧化钡溶液恰好完好中和C .该溶液中硝酸电离出的c( H ) 与水电离出的 c(H + ) 之比值为 10 -12 。
五年2018-2022高考化学真题按知识点分类汇编30-温度对化学平衡移动的影响(含解析)

五年2018-2022高考化学真题按知识点分类汇编30-温度对化学平衡移动的影响(含解析)一、单选题1.(2022·广东·高考真题)恒容密闭容器中,()()()()422BaSO s 4H g BaS s 4H O g ++ˆˆ†‡ˆˆ在不同温度下达平衡时,各组分的物质的量(n)如图所示。
下列说法正确的是A .该反应的Δ0H <B .a 为()2H O n 随温度的变化曲线C .向平衡体系中充入惰性气体,平衡不移动D .向平衡体系中加入4BaSO ,H 2的平衡转化率增大2.(2022·江苏·高考真题)乙醇-水催化重整可获得2H 。
其主要反应为-125222C H OH(g)+3H O(g)=2CO (g)+6H (g) ΔH=173.3kJ mol ⋅,-1222CO (g)+H (g)=CO(g)+H O(g) ΔH=41.2kJ mol ⋅,在51.010Pa ⨯、()()始25始2n C H O H :n H O =1:3时,若仅考虑上述反应,平衡时2CO 和CO 的选择性及2H 的产率随温度的变化如图所示。
CO 的选择性⨯生成生成2生成n (C O )=100%n (C O)+n (C O ),下列说法正确的是A .图中曲线①表示平衡时2H 产率随温度的变化B .升高温度,平衡时CO 的选择性增大C .一定温度下,增大()()252n C H OH n H O 可提高乙醇平衡转化率D .一定温度下,加入CaO(s)或选用高效催化剂,均能提高平衡时2H 产率3.(2022·北京·高考真题)某MOFs 的多孔材料刚好可将N 2O 4“固定”,实现了NO 2与N 2O 4分离并制备HNO 3,如图所示:己知:2NO 2(g)ƒN 2O 4(g) ΔH<0下列说法不正确的是A .气体温度升高后,不利于N 2O 4的固定B .N 2O 4被固定后,平衡正移,有利于NO 2的去除C .制备HNO 3的原理为:2N 2O 4+O 2+2H 2O=4HNO 3D .每制备0.4molHNO 3,转移电子数约为226.0210⨯4.(2021·广东·高考真题)化学是以实验为基础的科学。
三年(2022-2024)高考化学真题分类汇编(全国通用)专题08化学反应速率与化学平衡(解析版)
三年真题二]4<08化肾反固速卑与化肾年衡昌字窖僵。
痹匆演考点三年考情(2022・2024)命题趋势考点1化学反应速率与化学平衡♦化学反应速率:2024安徽卷、2024江苏卷、2024甘肃卷、2023广东卷、2023山东卷、2023辽宁卷、2023浙江卷、2022广东卷、2022北京卷、2022河北卷、2022浙江卷♦化学平衡:2024黑吉辽卷、2024山东卷、2024江苏卷、2024浙江卷、2024湖南卷、2023北京卷、2023湖南卷、2023山东卷、2022天津卷、2022重庆卷、2022江苏卷、2022浙江卷、2022北京卷、2022辽宁卷、2022湖南卷选择题中对于化学反应速率和化学平衡内容的考查不算太多,这是因为在主观题中,化学反应速率和化学平衡才是考查的重头戏。
随着新高考单科卷的实行,选择题题量大增,有关化学反应速率和化学平衡试题的考查在选择题中开始有所增加,考查的核心知识还是有关化学反应速率的比较、计算和影响因素的判断,化学平衡常数、转化率、物质的浓度的计算,以及平衡移动原理的分析等,常结合坐标图像或表格进行考查。
考法01化学反应速率1.(2024.安徽卷)室温下,为探究纳米铁去除水样中SeO?-的影响因素,测得不同条件下SeC^-浓度随时间变化关系如下图。
"一。
点,0云下列说法正确的是A. 实验①中,。
〜2小时内平均反应速率v (SeO42-)=2.0mol ・L-i.h-i实验序号水样体积/mL纳米铁质量/mg 水样初始pH①5086②5026③5028B. 实验③中,反应的离子方程式为:2Fe+SeO 42+8H +=2Fe 3++Se+4H 2OC. 其他条件相同时,适当增加纳米铁质量可加快反应速率D. 其他条件相同时,水样初始pH 越小,SeCU2-的去除效果越好【答案】C【解析】A.实验①中,。
〜2小时内平均反应速率v (SeO ;)*5・0xl0 3-一3moi.L 』.h 」,A 不正确;B. 实验③中水样初始pH =8,溶液显弱碱性,发生反应的离子方程式中不能用H+配电荷守恒,B 不正确;C. 综合分析实验①和②可知,在相同时间内,实验①中SeO :浓度的变化量大,因此,其他条件相同时,适当增加纳米铁质量可加快反应速率,C 正确;D. 综合分析实验③和②可知,在相同时间内,实验②中Se 。
2011-2014新课标高考分类汇编——化学平衡
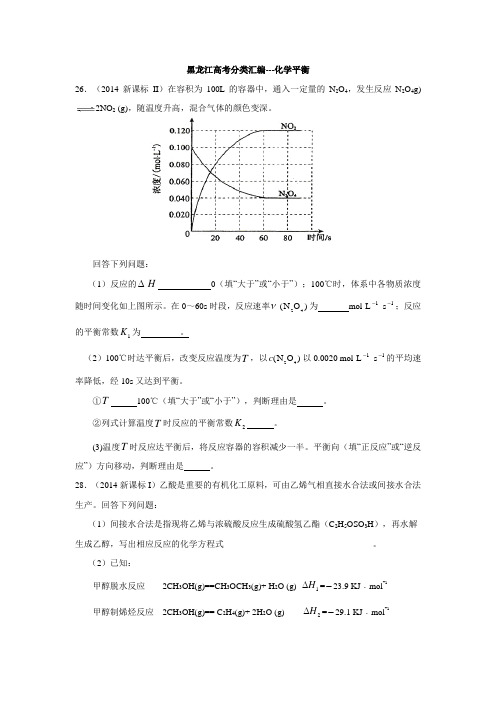
黑龙江高考分类汇编---化学平衡26.(2014新课标II )在容积为100L 的容器中,通入一定量的N 2O 4,发生反应N 2O 4g)2NO 2 (g),随温度升高,混合气体的颜色变深。
回答下列问题:(1)反应的∆H 0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。
在0~60s 时段,反应速率ν24(N O )为 mol·L1-·s 1-;反应的平衡常数1K 为 。
(2)100℃时达平衡后,改变反应温度为T ,以24(N O )c 以0.0020 mol·L1-·s 1-的平均速率降低,经10s 又达到平衡。
①T 100℃(填“大于”或“小于”),判断理由是 。
②列式计算温度T 时反应的平衡常数2K 。
(3)温度T 时反应达平衡后,将反应容器的容积减少一半。
平衡向(填“正反应”或“逆反应”)方向移动,判断理由是 。
28.(2014新课标I )乙酸是重要的有机化工原料,可由乙烯气相直接水合法或间接水合法生产。
回答下列问题:(1)间接水合法是指现将乙烯与浓硫酸反应生成硫酸氢乙酯(C 2H 5OSO 3H ),再水解生成乙醇,写出相应反应的化学方程式__________________________________。
(2)已知:甲醇脱水反应 2CH 3OH(g)==CH 3OCH 3(g)+ H 2O (g) 1H ∆=-23.9 KJ ﹒mol -1 甲醇制烯烃反应 2CH 3OH(g)== C 2H 4(g)+ 2H 2O (g) 2H ∆=-29.1 KJ ﹒mol -1乙醇异构化反应 C 2H 5OH(g) ==CH 3OCH 3(g) 3H ∆=+50.7KJ ﹒mol -1则乙烯气相直接水合反应C 2H 4(g)+H 2O(g)==C 2H 5OH(g)的H ∆=______KJ ﹒mol -1。
与间接水合法相比,气相直接水合法的优点是____________________________________。
高考化学5年真题分类汇编 专题11 水溶液中的离子平衡

冠夺市安全阳光实验学校【2011高考】(2011·江苏卷)下列有关电解质溶液中微粒的物质的量浓度关系正确的是A.在0.1 mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)B.在0.1 mol·L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3-)C.向0.2 mol·L-1NaHCO3溶液中加入等体积0.1 mol·L-1NaOH溶液:c(CO32-)> c(HCO3-)> c(OH-)>c(H+)D.常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1 mol·L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)此正确的关系是:c(HCO3-)>c(CO32-)> c(OH-)>c(H+)。
D.常温下,CH3COONa和CH3COOH混合溶液,包括CH3COO-水解和CH3COOH电离两个过程,既然pH=7, 根据电荷守恒式,不难得出c(Na+)=c(CH3COO-) =0.1 mol· L-1,c(H+)=c(OH-)=1×10-7mol·L-1。
水解是有限的,c(CH3COOH)>c(CH3COO-)。
【答案】B(2011·安徽卷)室温下,将1.000mol·L-1盐酸滴入20.00mL 1.000mol·L -1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。
下列有关说法正确的是A. a点由水电离出的c(H+)=1.0×10-14mol/LB. b点:c(NH4+)+c(NH3·H2O)=c(Cl-)C.c点:c(Cl-)= c(NH4+)D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热(2011·浙江卷)海水中含有丰富的镁资源。
高考化学化学反应速率与化学平衡综合题汇编附答案

高考化学化学反应速率与化学平衡综合题汇编附答案一、化学反应速率与化学平衡1.为了证明化学反应有一定的限度,进行了如下探究活动:步骤1:取8mL0.11mol L -⋅的KI 溶液于试管,滴加0.11mol L -⋅的FeCl 3溶液5~6滴,振荡; 请写出步骤1中发生的离子反应方程式:_________________ 步骤2:在上述试管中加入2mLCCl 4,充分振荡、静置;步骤3:取上述步骤2静置分层后的上层水溶液少量于试管,滴加0.11mol L -⋅的KSCN 溶液5~6滴,振荡,未见溶液呈血红色。
探究的目的是通过检验Fe 3+,来验证是否有Fe 3+残留,从而证明化学反应有一定的限度。
针对实验现象,同学们提出了下列两种猜想: 猜想一:KI 溶液过量,Fe 3+完全转化为Fe 2+,溶液无Fe 3+猜想二:Fe 3+大部分转化为Fe 2+,使生成Fe (SCN )3浓度极小,肉眼无法观察其颜色为了验证猜想,在查阅资料后,获得下列信息:信息一:乙醚比水轻且微溶于水,Fe (SCN )3在乙醚中的溶解度比在水中大。
信息二:Fe 3+可与46[()]Fe CN -反应生成蓝色沉淀,用K 4[Fe (CN )6]溶液检验Fe 3+的灵敏度比用KSCN 更高。
结合新信息,请你完成以下实验:各取少许步骤2静置分层后的上层水溶液于试管A 、B 中,请将相关的实验操作、预期现象和结论填入下表空白处:【答案】322222Fe I Fe I +-++=+ 若液体分层,上层液体呈血红色。
则“猜想一”不成立 在试管B 中滴加5-6滴K 4[Fe (CN )6]溶液,振荡【解析】 【分析】 【详解】(1) KI 溶液与FeCl 3溶液离子反应方程式322222FeI Fe I +-++=+;(2)①由信息信息一可得:取萃取后的上层清液滴加2-3滴K 4[Fe (CN )6]溶液,产生蓝色沉淀,由信息二可得:往探究活动III 溶液中加入乙醚,充分振荡,乙醚层呈血红色,实验操作预期现象结论若液体分层,上层液体呈血红色。
高考试题中的化学平衡问题

高考试题中的化学平衡问题化学平衡是中学化学里有重要意义的基本理论,是高考中的重点和难点。
从近五年的高考试题来看,既有体现高考命题的稳定性的基本题目,又出现了一些考察学科思维素质和心理素质的灵活性较强、难度较大的试题。
本文对近几年全国高考各种试卷中的有关化学平衡的考题作摘要的归类和解析,以便体会化学平衡考察的层次和趋势,并提出教学时的相应对策。
一.试题分析和教学要点考点一:化学平衡状态的含义、特征和判定例 1.(2002上海化学填空题24.(3))在一定体积的密闭容器中,进行如下化学反应:CO2g+H2gCOg+H2O(g),能判断该反应达到化学平衡状态的依据是(多选扣分)。
(a)容器中压强不变(b)混合气体中cCO不变(c)正H2=逆H2O (d)cCO2=cCO[评析]此题考查反应速率的表示及基本的平衡状态判断问题。
要求应试者了解正H2、逆H2O的含义。
看清这是一类反应前后气体体积相等,容器体积固定的反应。
答案:b、c。
例2.2005春MCE14一定条件下,在密闭容器中,能表示反应某(g)+2Y(g)定达到化学平衡状态的是A.容器内压强不随时间变化B.容器内各物质的浓度不随时间变化C.容器内某、Y、Z的浓度之比为1︰2︰2D.单位时间消耗0.1mol某同时生成0.2molZ[评析]此题考查基本的平衡状态判断问题,比较容易,但也有一定的迷惑性。
该反应前后气体体积不等,容器体积固定,压强不随时间变化,说明气体总物质的量不再改变,各物质浓度也不再变化。
所以A、B正确,C选项浓度比与化学计量数比一致,其实只是反应可能达到的一种巧合,并不能说明各物质浓度不再变化,C、D均不能说明达到平衡。
答案:AB。
[教学要点建议]1.必须使学生明确:有关平衡状态的含义和判定的直接依据只有两条:一看是否V正2Z(g),一=V逆且不为零;二看各组分含量是否保持不变(这正是一定条件下的平衡状态的含义)。
2.间接依据有很多,一般是从压强、密度、颜色等间接推出上述两条直接依据。
高三化学平衡练习题

高三化学平衡练习题在高三化学学习的过程中,平衡是一个重要的概念和知识点。
理解和掌握平衡反应的原理和计算方法对于化学学习的深入和应用至关重要。
下面将通过几个练习题来加深对化学平衡的理解。
1. 对于下列化学平衡反应N2(g) + 3H2(g) ↔ 2NH3(g)(1) 写出正向反应和逆向反应的反应物和产物。
(2) 写出平衡常数表达式并给出其计算公式。
(3) 当反应物的初始摩尔浓度分别为[N2] = 0.5 mol/L,[H2] = 0.8 mol/L时,平衡时氨气的摩尔浓度是多少?2. 对于下列化学平衡反应CO(g) + H2O(g) ↔ CO2(g) + H2(g)(1) 写出正向反应和逆向反应的反应物和产物。
(2) 写出平衡常数表达式并给出其计算公式。
(3) 当反应物的初始摩尔浓度分别为[CO] = 1.0 mol/L,[H2O] = 0.5 mol/L时,平衡时氢气的摩尔浓度是多少?3. 对于下列化学平衡反应N2O4(g) ↔ 2NO2(g)(1) 写出正向反应和逆向反应的反应物和产物。
(2) 写出平衡常数表达式并给出其计算公式。
(3) 当反应物的初始压强分别为[P(N2O4)] = 2.0 atm时,平衡时NO2的压强是多少?4. 对于下列化学平衡反应N2(g) + O2(g) ↔ 2NO(g)(1) 写出正向反应和逆向反应的反应物和产物。
(2) 写出平衡常数表达式并给出其计算公式。
(3) 当反应物的初始压强分别为[P(N2)] = 1.5 atm,[P(O2)] = 0.8 atm时,平衡时NO的压强是多少?在解答这些问题之前,我们首先要明确平衡常数的含义。
平衡常数(K)是描述平衡体系中浓度(或压强)的一个指标,它与反应物和产物的浓度(或压强)之间的关系密切相关。
对于一般的反应方程式:aA + bB ↔ cC + dD平衡常数的表达式可以表示为:K = [C]^c[D]^d / [A]^a[B]^b1. (1) 正向反应的反应物是N2和H2,产物是NH3;逆向反应的反应物是NH3,产物是N2和H2。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
百度文库 - 让每个人平等地提升自我五年高考试题汇编 -----化学平衡1.(2017 全国 I 卷)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。
通过计算,可知系统(Ⅰ)和系统(Ⅱ)制氢的热化学方程式分别为 ________________ 、______________,制得等量 H 2 所需能量较少的是 _____________。
( 3)H 2S 与 CO 2 在高温下发生反应: H 2S(g)+CO 2 (g)COS(g) +H 2O(g)。
在 610 K 时,将 mol CO 2 与 mol H 2S充入 2.5 L 的空钢瓶中,反应平衡后水的物质的量分数为。
① H 2S 的平衡转化率1 =_______%,反应平衡常数 K=________ 。
②在 620 K 重复试验,平衡后水的物质的量分数为, H 2S 的转化率2 _____ 1 ,该反应的H_____0。
(填“ >”“或“<”=)”③向反应器中再分别充入下列气体,能使H 2S 转化率增大的是 ________(填标号)A.HSB.2C22.(2017 全国 II 卷) 27.( 14 分)丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。
回答下列问题:( 1)已知:正丁烷( C 4H 10 )脱氢制 1- 丁烯( C 4H 8 )的热化学方程式如下:①C 4 H 10 gC 4 H 8 g H 2 gH 1② C 4H 10 g1O 2 gC 4H 8 g H 2 O gH 2119 kJ mol 12③ H 2 g1O 2 gH 2O gH 3242kJ mol 12反应①的H 1 为 ________ kJ mol 1 。
图(a )是反应①平衡转化率与反应温度及压强的关系图,x (填“大于”或“小于”) ;欲使丁烯的平衡产率提高,应采取的措施是__________ (填标号)。
A .升高温度B .降低温度C .增大压强D .降低压强( 2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。
图(b)为丁烯产率与进料气中n (氢气)/ n (丁烷)的关系。
图中曲线呈现先升高后降低的变化趋势,其降低的原因是___________ 。
( 3)图( c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。
丁烯产率在 590℃之前随温度升高而增大的原因可能是___________、____________;590℃之后,丁烯产率快速降低的主要原因可能是_____________ 。
3.(2017 全国 III 卷) 28.( 14 分)砷( As)是第四周期Ⅴ A 族元素,可以形成As 2S3、 As 2O 5、 H 3AsO 3、 H 3AsO 4等化合物,有着广泛的用途。
回答下列问题:(1)画出砷的原子结构示意图 ____________。
( 2)工业上常将含砷废渣(主要成分为As 2S3)制成浆状,通入 O 2氧化,生成 H 3AsO 4和单质硫。
写出发生反应的化学方程式________。
该反应需要在加压下进行,原因是________________________ 。
( 3)已知:As(s)3H 2 ( g)2O 2 ( g)H 3AsO 4 ( s)H 1 2H 2 ( g)1O 2 ( g )H 2 O(l)H 2 22As(s)5As 2O 5 ( s)H 3 O 2 (g)2则反应 As 2O 5 (s)3H 2O(l)2H 3AsO 4 (s) 的H=_________。
( 4) 298 K 时,将20 mL 3x-1-1I 2和 20 mL NaOH 溶液混合,mol·L Na3AsO3、 20 mL 3 x mol ·L发生反应: AsO33 (aq)I 2 ( aq)2OH(aq)AsO43 (aq)2I (aq )H 2O(l)溶液中 c( AsO43 ) 与反应时间(t) 的关系如图所示。
①下列可判断反应达到平衡的是__________ (填标号)。
a. 溶液的 pH 不再变化b.v(I )2v( AsO33 )c. c( AsO43) / c( AsO33)不再变化d.c( I)ymol L 1② t m时, v正_____ v逆(填“大于”“小于”或“等于”)。
③ t m时 v逆_____ t n时 v逆(填“大于”“小于”或“等于”),理由是_____________。
④若平衡时溶液的pH=14,则该反应的平衡常数K 为___________。
4.(2016.全国 II 卷 )27.丙烯腈( CH2 =CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈 CH3CN 等,回答下列问题:( 1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈( C3H3N)和副产物丙烯醛( C3H4O)的热化学方程式如下:①C3H6(g)+NH3(g)+ O2(g)=C3H3 N(g)+3H2O(g) △H=-515kJ/mol② C3H (g)+ O (g)=C H O(g)+H O(g) △H=-353kJ/mol ;两个反应在热力学上趋势均很大,其原因是;有623 42利于提高丙烯腈平衡产率的反应条件是;提高丙烯腈反应选择性的关键因素是。
( 2)图( a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460O C.低于 460O C 时,丙烯腈的产率(填“是”或者“不是”)对应温度下的平衡产率,判断理由是;高于460O C 时,丙烯腈产率降低的可能原因是(双选,填标号)A.催化剂活性降低B.平衡常数变大C.副反应增多D.反应活化能增大( 3)丙烯腈和丙烯醛的产率与n(氨) /n(丙烯)的关系如图( b)所示。
由图可知,最佳n(氨) / n (丙烯)约为,理由是。
进料氨、空气、丙烯的理论体积约为。
5.(2016.全国 III 卷)27.( 15 分)煤燃烧排放的烟气含有SO2和 NO x,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:(1) NaClO 2 的化学名称为 _______。
( 2)在鼓泡反应器中通入含有含有 SO 2 和 NO x 的烟气,反应温度为 323 K ,NaClO 2 溶液浓度为 5× 10-3mol ·L -1 。
反应一段时间后溶液中离子浓度的分析结果如下表》离子SO 2-2- - - -4 SO 3NO 3NO 2Cl- 1- 4- 6- 4- 5- 3c/ ( mol ·L ) ×10 × 10 × 10× 10× 10①写出 NaClO 2 溶液脱硝过程中主要反应的离子方程式 __________。
增加压强, NO的转化率 ______(填 “提高 ”“不变 ”或 “降低 ”)。
②随着吸收反应的进行,吸收剂溶液的pH 逐渐 ______(填 “提高 ”“不变 ”或 “降低 ”)。
③由实验结果可知,脱硫反应速率______脱硝反应速率(填 “大于 ”或 “小于 ”)。
原因是除了 SO 2 和 NO 在烟气中的初始浓度不同,还可能是 ___________。
( 3)在不同温度下, NaClO 2溶液脱硫、脱硝的反应中, 2和 NO 的平衡分压 x如图所示。
SO p ①由图分析可知, 反应温度升高, 脱硫、脱硝反应的平衡常数均 _______(填 “增大 ”“不变 ”或 “减小 ”)。
②反应 ClO 2- 3 2- 42 -- 的平衡常数 K 表达式为 ___________。
+2SO ===2SO +Cl( 4)如果采用 NaClO 、 Ca ( ClO ) 2 替代 NaClO 2,也能得到较好的烟气脱硫效果。
①从化学平衡原理分析,Ca ( ClO ) 2 相比 NaClO 具有的有点是 _______。
②已知下列反应:SO 2 (g)+2OH -32- 2 H 1(aq) ===SO (aq)+H O(l)-2-2 --H 2ClO (aq)+SO 3 (aq) ===SO 4 (aq)+Cl (aq)CaSO 4(s) ===Ca 2+(aq ) +SO 42- ( aq )H 3则反应 SO 2(g)+ Ca 2+( aq ) + ClO - (aq) +2OH - (aq) === CaSO 4(s) +H 2O(l) +Cl - (aq)的 H=______。
6.[2016 全·国卷Ⅰ ] 元素铬 (Cr)在溶液中主要以 Cr 3+ - (绿色 ) 、 Cr 2-2-(黄442 7色 )等形式存在, Cr(OH) 3 为难溶于水的灰蓝色固体。
回答下列问题:(1)Cr 3+与 Al 3+的化学性质相似,在Cr 2(SO 4)3 溶液中逐滴加入NaOH 溶液直至过量,可观察到的现象是_______________________________________________________ 。
2-2--1的 Na 2CrO 4 2-(2)CrO 4 和 Cr 2O 7 在溶液中可相互转化。
室温下,初始浓度为 mol ·L 溶液中 c(Cr 2O 7 )随 c(H+)的变化如图所示。
①用离子方程式表示Na 2CrO 4 溶液中的转化反应 ______________________ 。
②由图可知,溶液酸性增大, CrO 42-的平衡转化率 ____________( 填“增大”“减小”或“不变”)。
根据 A 点数据, 计算出该转化反应的平衡常数为____________ 。
③升高温度,溶液中CrO 42-的 平 衡 转 化 率 减 小 , 则 该 反 应 的H____________0( 填“大于”“小于”或“等于” )。
(3) 在化学分析中采用K 2CrO 4 为指示剂,以 AgNO 3 标准溶液滴定溶液中的Cl -,利用 Ag +与 CrO 42-生成砖红色沉淀,指示到达滴定终点。
当溶液中Cl -恰好完全沉淀 (浓度等于× 10- 5 mol · L -1)时,溶液中 c(Ag +)-1,此时溶液中--1。
(已知 Ag2CrO4、AgCl 的 K sp分为 ____________mol·L c(CrO 42 ) 等于 ____________mol L·别为× 10-12和× 10-10)。
(4) + 6 价铬的化合物毒性较大,常用NaHSO3将废液中的2-还原成Cr3+,反应的离子方程式为Cr2O7______________________________________________________ 。
