胡黄连检验标准操作规程
GMP认证全套文件资料09-糊精检验标准操作规程

糊精检验标准操作规程目的:规范糊精检验操作。
适用范围:糊精的检验。
责任:检验室验人员按本规程操作,检验室主任对本规程的有效执行承担监督检查责任。
规程:1.性状:本品为白色或类白色的无定形粉末;无臭,味微甜。
本品在沸水中易溶,在乙醇或乙醚中不溶。
2.鉴别:2.1仪器及用具:试管、试管架、吸管、滴管等。
2.2试剂及试液:纯化水、碘试液。
2.3测定法取本品10%的水溶液1ml,加碘试液1滴,即显紫红色。
3.检查3.1仪器及用具:万分之一天平、电炉、干燥箱、马弗炉、水浴锅、坩埚、称量瓶、烧杯、垂熔玻璃坩埚、试管、容量瓶、纳氏比色管、滤纸等。
3.2试剂及试液:纯化水、酚酞指示液、氢氧化钠滴定液(0.1mol/L)、碱性酒石酸铜试液、乙醇、乙醚、硫酸、盐酸、硝酸、标准铁溶液、过硫酸铵、30%硫氰酸铵溶液。
3.3测定法3.3.1酸度:取本品5.0g加水50ml,加热使溶解,放冷,加酚酞指示液2滴与氢氧化钠滴定液(0.1mol/L)2.0ml,应显粉红色。
3.3.2还原糖:取本品2.0g,加水100ml,振摇5分钟,静置,滤过,取滤液50ml,加碱性酒石酸铜试液50ml,煮沸3分钟,用105℃恒重的的垂熔玻璃坩埚滤过,滤渣先用水,再用乙醇、最后用乙醚分次先涤,在105干燥2小时,遗留的氧化亚铜不得过0.20g。
3.3.3干燥失重 取本品按《干燥失重测定法标准操作规程》检查,于105℃干燥至恒重,减失重量不得过10.0%。
结果计算:%100⨯--称量瓶重量的重量干燥前供试品与称量瓶重量干燥后供试品与称量瓶的重量干燥前供试品与称量瓶 3.3.4炽灼残渣 按《炽灼残渣检查法标准操作规程》检查,残渣 不得过0.5%。
结果计算:%100⨯--坩埚的重量重量炽灼前供试品与坩埚的坩埚的重量量炽灼后残渣与坩埚的重 3.3.5铁盐: 取本品2.0g,炽灼灰化后,残渣加盐酸1ml 与硝酸3滴,置水浴上蒸发至近干,放冷,加盐酸1ml 使溶解,用水移至50ml 量瓶中,加水稀释至刻度,摇匀,精密量取10ml ,依《铁盐检查法标准操作规程》(检查,与标准铁溶液2.0ml 制成的对照液比较,不得更深(0.005%)。
胡黄连提取物的含量测定及其肝保护作用

胡黄连提取物的含量测定及其肝保护作用阎雪莹;刁磊;唐晓飞;高宏伟;匡海学【期刊名称】《中医药学报》【年(卷),期】2009(037)006【摘要】目的:建立胡黄连提取物(AP)中胡黄连苦苷Ⅰ、Ⅱ的含量测定方法并研究其对小鼠急性化学性肝损伤的保护作用.方法:采用HPLC测定AP中胡黄连苦苷Ⅰ、Ⅱ的含量,流动相为甲醇-水(42∶58),流速为1.0mL·min-1,检测波长为267nm;腹腔注射四氯化碳(CCl4)制备小鼠急性肝损伤模型,检测血清丙氨酸氨基转移酶(ALT)和天门冬氨酸氨基转移酶(AST)活性、肝脏指数.结果:胡黄连苦苷Ⅰ、Ⅱ的线性范围分别为50~600μg·mL-1,r=0.9999和50~500μg/mL,r=0.9999,平均回收率分别为107.78%,RSD=8.86%和103.62%,RSD=3.93%;小鼠连续5天灌胃给予AP 15.0、30.0、60.0mg·(kg·d)-1及静脉注射给予AP 15.0、30.0mg·(kg·d)-1能明显抑制肝损伤小鼠血清ALT、AST活性的升高(P<0.01),减轻增加的肝脏重量指数(P<0.05).结论:该含量测定方法准确可靠,适合于测定AP中胡黄连苦苷Ⅰ、Ⅱ的含量;AP对CCl4引起的小鼠急性肝损伤具有保护作用.【总页数】3页(P13-15)【作者】阎雪莹;刁磊;唐晓飞;高宏伟;匡海学【作者单位】黑龙江中医药大学,黑龙江,哈尔滨,150040;黑龙江中医药大学,黑龙江,哈尔滨,150040;黑龙江中医药大学,黑龙江,哈尔滨,150040;黑龙江中医药大学,黑龙江,哈尔滨,150040;黑龙江中医药大学,黑龙江,哈尔滨,150040【正文语种】中文【中图分类】R969.1【相关文献】1.苦菊提取物的肝保护作用研究 [J], 王福鑫;林铌;邓安珺;秦海林;王爱平2.研究白茶提取物的抗氧化及肝保护作用 [J], 林秀菁3.金边桑叶多酚提取物抗氧化及肝保护作用研究 [J], 吴黉坦;张友珍;黄立森;庞海月;陈煜沛;王贵弘;叶子坚;刘华欣4.圆叶节节菜不同体积分数乙醇提取物的止血和肝保护作用研究 [J], 陈佳星; 陆群; 张兴国; 罗霄; 罗伦才; 李坤伦5.木香70%乙醇提取物对缺氧小鼠肝保护作用 [J], 靳婉君;郝颖;樊鹏程;杨林鹏;马慧萍因版权原因,仅展示原文概要,查看原文内容请购买。
胡黄连质量标准

标准依据:《中华人民共和国药典》(2010年版一部)、《全国中药炮制规范》(1988年版)。
原药材1【来源】本品为玄参科植物胡黄连Picrorhiza scrophulariiflora Pennell的干燥根茎。
秋季采挖,除去须根及泥沙,晒干。
2【性状】本品呈圆柱形,略弯曲,偶有分枝,长3~12cm,直径0.3~1cm。
表面灰棕色至暗棕色,粗糙,有较密的环状节,具稍隆起的芽痕或根痕,上端密被暗棕色鳞片状的叶柄残基。
体轻,质硬而脆,易折断,断面略平坦,淡棕色至暗棕色,木部有4~10个类白色点状维管束排列成环。
气微,味极苦。
3【鉴别】3.1升华法取本品粉末0.5g,置适宜器皿中,60~80℃升华4小时,置显微镜下观察,可见针状、针簇状、棒状、板状结晶及黄色球状物。
3.2薄层色谱法取【鉴别】3.1 项下的升华物,加三氯甲烷数滴使溶解,作为供试品溶液。
另取香草酸对照品、肉桂酸对照品,加三氯甲烷制成每1ml各含1mg的混合溶液,作为对照品溶液。
照ZT-TS-02-004-1《薄层色谱法》试验,吸取上述两种溶液各5μl,分别点于同一硅胶GF254 薄层板上,以正己烷-乙醚-冰醋酸(5:5:0.1) 为展开剂,展开,取出,晾干,置紫外光灯(254nm) 下检视。
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
4【检查】4.1照ZT-TS-02-001-1《水分测定法》第一法测定,水分不得过13.0%。
4.2照ZT-TS-02-002-1《灰分测定法》测定,灰分不得过7.0%。
4.3照ZT-TS-02-002-1《灰分测定法》测定,酸不溶性灰分不得过3.0%。
5【浸出物】照醇溶性浸出物测定法项下的热浸法ZT-TS-02-003-1《浸出物测定法》测定,用乙醇作溶剂,不得少于30.0%。
6【含量测定】照ZT-TS-02-005-1《高效液相色谱法》测定。
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;以甲醇-水-磷酸(35:65:0.1)为流动相;检测波长为275nm。
胡黄连

·167·胡黄连HuhuanglianRHIZOMA PICRORHIZAE本品为玄参科植物胡黄连Picrorhiza scrophulariiflora Pennell的干燥根茎。
秋季采挖,除去须根及泥沙,晒干。
【性状】本品呈圆柱形,略弯曲,偶有分枝,长3~12cm,直径0.3~lcm。
表面灰棕色至暗棕色,粗糙,有较密的环状节,具稍隆起的芽痕或根痕,上端密被暗棕色鳞片状的叶柄残基。
体轻,质硬而脆,易折断,断面略平坦,淡棕色至暗棕色,木部有4~10个类白色点状维管束排列成环。
气微,味极苦。
【鉴别】(1)取本品粉末0.5g,置适宜器皿中,60~80℃升华4小时,置显微镜下观察,可见针状、针簇状、棒状、板状结晶及黄色球状物。
(2)取本品粉末5g,加水50ml,置60℃水浴中温浸20分钟,滤过。
取滤液1ml,加三氯化铁乙醇溶液2滴,生成暗绿色沉淀;另取滤液1ml,加5%α-萘酚乙醇溶液2滴,摇匀,生成黄白色浑浊,缓缓沿管壁加硫酸0.5ml,两液接界处显紫色环,振摇后颜色变深,加水稀释生成暗紫色沉淀。
(3)取〔鉴别〕(1)项下的升华物,加三氯甲烷数滴使溶解,作为供试品溶液。
另取香草酸对照品、肉桂酸对照品,加三氯甲烷制成每1ml各含1mg的混合溶液,作为对照品溶液。
照薄层色谱法(附录Ⅵ B)试验,吸取上述两种溶液各5µl,分别点于同一硅胶GF254薄层板上,以正己烷-乙醚-冰醋酸(5:5:0.1)为展开剂,展开,取出,晾干,置紫外光灯(254nm)下检视。
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
【检查】水分照水分测定法(附录Ⅸ H第一法)测定,不得过13.0%。
总灰分不得过7.0%(附录Ⅸ K)。
酸不溶性灰分不得过3.0%(附录Ⅸ K)。
【浸出物】照醇溶性浸出物测定法项下的热浸法(附录X A)测定,用乙醇作溶剂,不得少于30.0%。
【含量测定】照高效液相色谱法(附录Ⅵ D)测定。
胡黄连检验标准操作规程

原药材检验标准操作规程目的:建立一个中药饮片原药材检验标准操作程序,确保检验结果准确可靠。
适用范围:中药原药材。
责任人:质量保证部主任、质量控制部主任、化验员。
标准来源:《中华人民共和国药典》2010年版一部、《安徽省中药饮片炮制规范》。
内容:1、性状取本品适量,放入白瓷盘中,用眼观察,可见以下性状特征:本品呈圆柱形,略弯曲,偶有分枝,长3~12cm,直径O.3~1cm。
表面灰棕色至暗棕色,粗糙;有较密的环状节,具稍隆起的芽痕或根痕,上端密被暗棕色鳞片状的叶柄残基。
体轻,质硬而脆,易折断,断面略平坦,淡棕色至暗棕色,木部有4~10个类白色点状维管束排列成环。
气微,味极苦。
2、鉴别主要使用仪器:电子分析天平、电子显微镜、紫外光灯等。
2.1显微鉴别:取本品粉末0.5g,置适宜器皿中,60~80℃升华4小时,置显微镜下观察,可见针状、针簇状、棒状、板状结晶及黄色球状物。
2.2 薄层鉴别取2.1.3项下的升华物,加三氯甲烷数滴使溶解,作为供试品溶液。
另取香草酸对照品、肉桂酸对照品,加三氯甲烷制成每1ml各含lmg的混合溶液,作为对照品溶液。
照薄层色谱法(《中华人民共和国药典》附录VI B)试验,吸取上述两种溶液各5μl,分别点于同一硅胶GF薄层板上,以正己烷一乙醚-冰醋酸(5:5:0.1)为展开剂,展开,取出,晾干,置紫外光灯(254nm)下检视。
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
3、检查主要使用仪器:电子分析天平、电热恒温干燥箱、马弗炉、坩埚等。
3.1 水分取供试品2-5g,平铺于干燥至恒重的扁形称量瓶中厚度不超过5mm,精密称定,打开瓶盖在100~105℃干燥5小时,将瓶盖盖好,移置干燥器中,冷却30分钟,精密称定,再在上述温度干燥1小时,冷却,称重,至连续两次称重的差异不超过5mg为止。
根据减失的重量,按下式计算即得。
W2-W3供试品中的含水量(%)=────────×100%W2-WW 称量瓶重(g)W2 烘前称量瓶和样品重之和(g)W3 烘后称量瓶和样品重之和(g)本品含水量不得过13.0%。
薄层色谱扫描法测定胡黄连中胡黄连苷I含量

薄层色谱扫描法测定胡黄连中胡黄连苷I含量孟琳;孙君辉【摘要】目的:建立胡黄连中胡黄连苷I的含量测定方法。
方法:采用双波长薄层色谱扫描法。
结果:胡黄连苷I在0.605-3.025μg范围内呈良好的显性关系,回归方程Y=1431.7X+189.67,r=0.999,平均回收率98.37%,RSD=1.90%。
结论:本方法操作简便,结果准确,精密度好。
%The objective of this thesis is to establish the quantitative method ot Picroslde -I in Plcrorhlza. TLC scanning method was selected. The results are that the calibration curves of Picroside - I was in good linearity from 0. 605 μg to 3. 025 μg , and the regression equation being Y = 1431.7X + 189.67 ( r = 0. 999 ), the average re- covery was 98.37% ,RSD = 1.90%. therefore, the conclusion is drawn that this method was simple, accurate and with a good precision.【期刊名称】《山东商业职业技术学院学报》【年(卷),期】2012(012)001【总页数】2页(P93-94)【关键词】胡黄连;薄层扫描;胡黄连苷I【作者】孟琳;孙君辉【作者单位】山东商业职业技术学院,山东济南250103:;山东商业职业技术学院,山东济南250103:【正文语种】中文【中图分类】S853.75胡黄连为玄参科植物胡黄连Picrorhizascrophulariiflora.Pennell的干燥根茎,具有退虚热,除疳热,清湿热的功效,用于骨蒸潮热,小儿疳热,湿热泻痢,黄疸尿赤,痔疮肿痛[1]。
胡黄连规范化生产标准操作规程(SOP)研究

胡黄连规范化生产标准操作规程(SOP)研究陈翠;郭承刚;徐中志;康平德;杨少华【摘要】In order to guarantee good quality of crude drugs, the production standardization of Pkrorhiza scrophidari-iflora Pennell is referred to requirements and contents of the Chinese Medicinal Materials Production Quality Manage ment Standard, which was promulgated and implemented by the State Drug Administration. The standard operation procedure (SOP) of Pkrorhiza scrophulariiflora Pennell was formulated. It includes the species, environmental requirements, production management and processing, quality and packaging, storage, transportation, and etc. Regulations and requirements of the entire production process are unified in order to adapt to the Picrorhiza scrophulariiflora Pennell production in alpine areas of northwest Yunnan.%参照国家药品监督管理局颁布实施的《中药材生产质量管理规范》有关要求和内容,规范胡黄连的生产以保证产品的质量.从种质、产地环境要求、生产管理和加工、质量要求以及包装、储存、运输等多方面对胡黄连的整个生产过程做出统一的规定和要求,以适应云南西北高寒山区该药材品种生产时的要求.【期刊名称】《世界科学技术-中医药现代化》【年(卷),期】2012(014)002【总页数】5页(P1519-1523)【关键词】胡黄连;规范化;标准操作规程【作者】陈翠;郭承刚;徐中志;康平德;杨少华【作者单位】云南省农业科学院高山经济植物研究所丽江674100;云南省农业科学院高山经济植物研究所丽江674100;云南省农业科学院高山经济植物研究所丽江674100;云南省农业科学院高山经济植物研究所丽江674100;云南省农业科学院高山经济植物研究所丽江674100【正文语种】中文胡黄连(Picrorhiza scrophulariiflora Pennell)为玄参科胡黄连属多年生草本药用植物,为云南省道地濒危药材,收载于《中华人民共和国药典》。
YL-11040黄连原料检验操作规程

云连按干燥品计算,以盐酸小檗碱(C20H18ClNO4)计,含小檗碱(C20H17NO4)不得少于7.0%。
计算公式:
A样×C对×f
含量% =×100%
m×(1-水分)×A对
式中:
A样-------------------------样品的面积。
仪器:粉碎机、药筛、分析天平、坩埚、箱式电阻炉等。
方法:取供试品2~3g,过二号筛混合均匀后,置炽灼至恒重的坩埚中称定重量,缓缓炽热,注意避免燃烧,至完全炭化时,逐渐升高温度至500~600℃,使完全灰化至恒重。根据残渣重量,计算供试品中总灰分的含量(%)。
计算公式:
W1-W0
总灰分% =×100%
雅连 髓部有石细胞。
云连 皮层、中柱鞘及髓部均无石细胞。
(2)薄层鉴别
仪器与试剂:分析天平、硅胶G薄层板、层析缸、乙酸乙酯、超声仪、三乙胺、黄连对照药材、环己烷、异丙醇、盐酸小檗碱对照品、甲醇等。
方法:(2)取本品粉末0.25g,加甲醇25ml,超声处理30分钟,滤过,取滤液作为供试品溶液。另取黄连对照药材0.25g,同法制成对照药材溶液。再取盐酸小檗碱对照品,加甲醇制成每1ml含0.5mg的溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述三种溶液各1μl,分别点于同一高效硅胶G薄层板上,以环己烷-乙酸乙酯-异丙醇-甲醇-水-三乙胺(3:3.5:1:1.5:0.5:1)为展开剂,置用浓氨试液预饱和20分钟的展开缸内,展开,取出,晾干,置紫外光灯(365nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显4个以上相同颜色的荧光斑点;对照品色谱相应的位置上,显相同颜色的荧光斑点。
中药材质量标准胡黄连

中药材质量标准胡黄连集团标准化办公室:[VV986T-J682P28-JP266L8-68PNN]中药材质量标准中文名胡黄连汉语拼音Huhuanglian英文名RHIZOMA PICRORRHIZAE来源本品为玄参科植物胡黄连Picrorrhiza kurroa Royle ex Benth.或西藏胡黄连Picrorrhiza scrophulariifloraPennell的干燥根茎。
性状本品呈圆柱形,少有分枝,略弯曲,多已折断,长3~15cm,直径~1cm。
表面灰褐色,栓皮脱落处呈棕黑色,节间短,形成密集环纹,腹侧有较多疣状须根,状如卧蚕。
近地上茎部分的根茎可见密集的鳞叶残基。
质脆,易断,折断时现粉尘,断面稍平坦,木栓层灰色至灰褐色,皮部及髓部淡棕色至棕褐色,维管束4~10个排列成环,木部灰白色。
细长柱状根茎,节间不明显,表面有浅纵皱,根痕少,栓皮及木部较发达,中心有髓,残存须根较粗壮。
气微,味极苦。
鉴别(1)取本品粗粉2g,加醋酸乙酯50ml,回流提取1小时,滤过,滤液挥干,残渣用甲醇溶解使成2ml,作为供试品溶液。
另取胡黄连对照药材2g,同法制成对照药材溶液。
照薄层色谱法(中国药典2000年版一部附录VIB)试验,吸取上述两种溶液各3μl,分别点于同一用2%氢氧化钠溶液制备的硅胶F254薄层板上使成条状,以氯仿-甲醇-水(70:30:10)10℃以下放置的下层溶液为展开剂,展开14cm,取出,晾干,置紫外光灯(254nm)下检视。
供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点。
(2)本品在[含量测定]项下所得色谱峰中,应呈现与对照品保留时间相同的色谱峰。
检查杂质取本品250g,通过二号筛,筛上物拣出杂质,与筛下的碎末合并计为杂质,不得过4%。
地上茎、叶及须根不得过9%。
水分照水分测定法(中国药典2000年版一部附录IX H第一法)测定,不得过%。
有机氯农药残留量六六六(总BHC)不得过千万分之二;滴滴涕(总DDT)不得过千万分之二;五氯硝基苯(PCNB)不得过千万分之一(中国药典2000年版一部附录IX Q)。
黄连质量标准及检验操作规程
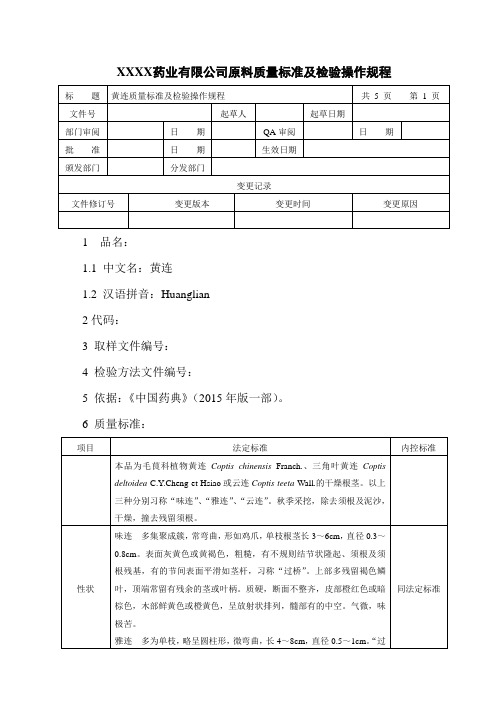
XXXX药业有限公司原料质量标准及检验操作规程1 品名:1.1 中文名:黄连1.2 汉语拼音:Huanglian2代码:3 取样文件编号:4 检验方法文件编号:5 依据:《中国药典》(2015年版一部)。
6 质量标准:7 检验操作规程:7.1 试药与试剂:甲醇、黄连对照药材、盐酸小檗碱对照品、环己烷、乙酸乙酯、异丙醇、水、三乙胺、氨水、乙腈、磷酸二氢钾、硫酸、乙醇、盐酸。
7.2 仪器与用具:显微镜、水浴锅、三用紫外分析仪、恒温鼓风干燥箱、马福炉、硅胶G薄层板、超声波清洗器、薄层色谱扫描仪、高效液相色谱仪。
7.3 性状:取本品适量,自然光下目测色泽,嗅闻气味。
7.4 鉴别:7.4.1 取本品制片置10×10显微镜下做显微观察。
7.4.2取本品粉末约0.25g,加甲醇25ml,超声处理30分钟,滤过,取滤液作为供试品溶液。
另取黄连对照药材0.25g,同法制成对照药材溶液。
再取盐酸小檗碱对照品,加甲醇制成每1ml含0.5mg的溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述三种溶液各1μl,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯-异丙醇-甲醇-水-三乙胺(3:3.5:1:1.5:0.5:1)为展开剂,置用浓氨试液预饱和20分钟的展开缸内,展开,取出,晾干,置紫外光灯(365nm)下检视。
供试品色谱中,在与对照药材色谱相应的位置上,显4个以上相同颜色的荧光斑点;对照品色谱相应的位置上,显相同颜色的荧光斑点。
7.5 检查:7.5.1 水分:不得过14.0%(附录15第一法)。
7.5.2 总灰分:不得过5.0%(附录17)。
7.5.3二氧化硫残留量照二氧化硫残留量测定法(附录58)测定,不得过150mg/kg。
7.6 浸出物:照醇溶性浸出物测定法(附录19)项下的热浸法测定,用稀乙醇作溶剂,不得少于15.0%。
7.7 含量测定:味连照高效液相色谱法(附录8)测定。
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;乙腈-0.05mol/L磷酸二氢钾溶液(50:50)(每100ml中加十二烷基硫酸钠0.4g,再以硫酸调节pH值为4.0)为流动相;检测波长为354nm。
GMP质量体系糊精检验操作规程

GMP质量体系糊精检验操作规程一、目的与适用范围本操作规程适用于糊精检验的操作流程和质量控制要求,以确保生产出符合质量标准的糊精产品。
二、引用文件1.国家药典(最新版)2.《药品生产质量管理规范》(GMP)(最新版)3.公司糊精生产质量管理程序三、设备与试剂1.粗筛、细筛2.分析天平3.pH计4.火焰燃烧器5.反应器6.甲醇、去离子水、乙醚7.国家药典指定试剂四、操作流程1.采样(1)按照国家药典要求,从反应器中取得糊精样品,并将样品编号标注在容器上。
(2)确保采样工具清洁无杂质,采用无菌操作方法。
(3)将样品送往质量控制实验室。
2.产品外观质量检验(1)检查糊精样品的外观,包括颜色、气味等。
(2)记录外观质量检验结果,并与标准进行比较。
3.粒度分析(1)使用粗筛和细筛进行粒度分析,按照国家药典要求,记录筛孔大小及通过筛孔的糊精颗粒重量。
(2)根据粒度分析结果,判断糊精颗粒的分布情况,并比较与标准要求的差异。
4.含水量测定(1)取适量糊精样品放入烘箱中烘干,根据国家药典要求,测定糊精的含水量。
(2)记录含水量测定结果,并与标准进行比较。
5.pH值测定(1)取适量糊精样品放入反应器中,并加入适量甲醇。
(2)使用pH计测定糊精样品的pH值,根据国家药典要求,记录结果。
(3)与标准进行比较,判断糊精样品的酸碱性。
6.残留溶剂测定(1)取适量糊精样品放入烘箱中烘干,然后将样品溶解于去离子水中。
(2)使用气相色谱法测定糊精样品中的残留溶剂含量,根据国家药典要求,记录结果。
(3)与标准进行比较,判断糊精样品的溶剂残留是否符合要求。
7.清洗验证(1)用清洁的容器将样品收集起来,并标注样品编号。
(2)使用火焰燃烧器进行糊精样品残留物的清洗验证,记录结果。
(3)与标准进行比较,判断清洗效果是否符合要求。
五、记录与报告1.每个检验项目的检测结果应记录在检验记录表中,并进行签名和日期确认。
2.如发现异常情况或不符合要求的情况,应及时采取纠正措施,并进行记录。
成品药材胡黄连质量标准

文件编号
起草
审核
批准
部门
质保部
质控部
质保部
技术部
质量技术副总
姓名
签名
日期
分发部门
质保部、质控部
【来源】本品为玄参科植物胡黄连Picorhiza scorphulaiifloraPennell的干燥根茎。秋季采挖,除去须根和泥沙,晒干。
【主要产地】西藏、云南等地。
【炮制】除去杂质,洗净,润透,切薄片干燥或用时捣碎。
测定法分别精密吸取对照品溶液与供试品溶液各10µl,注入液相色谱仪,测定,即得。
本品按干燥品计算,含胡黄连苷I(C24H28O11)与胡黄连苷Ⅱ(C23H28O13)的总量不得少于9.0%。
【性味与归经】苦、寒。归肝、胃、大肠经。
【功能与主治】退虚热,除疳热,清湿热。用于骨蒸潮热,小儿疳热,湿热泻痢,黄疸尿赤,痔疾肿痛。
【检查】 水分不得过13.0%(附录ⅨH第一法)。
杂质、灰屑检查不得过3.0%。
二氧化硫残留量不得过150mg/kg。
总灰分不得过7.0%(附录ⅨK)。
酸不溶性灰分不得过3.0%(附录ⅨK)。
【浸出物】照醇溶性浸出物测定法(附录X A)项下的热浸法测定,用乙醇作溶剂,不得少于30.0%。
【含量测定】照高效液相色谱法(附录ⅥD)测定。
【性状】本品呈不规则的圆形薄片。外表皮灰棕色至暗棕色。切面灰黑色或棕黑色,木部有4~10个类白色点状维管束排列成环,气微,味极苦。
【鉴别】(1)取本品粉末0.5g,置适宜器皿中,60~80℃升华4小时,置显微镜下观察,可见针状、针簇状、棒状、板状结晶及黄色球状物。
(2)取〔鉴别〕(1)项下的升华物,加三氯甲烷数滴使溶解,作为供试品溶液。另取香草酸对照品、肉桂酸对照品,加三氯甲烷制成每1ml各含1mg的混合溶液,作为对照品溶液。照薄层色谱法(附录ⅥB)试验,吸取上述两种溶液各5µl,分别点于同一硅胶GF254薄层板上,以正己烷-乙醚-冰醋酸(5:5:0.1)为展开剂,展开,取出,晾干,置紫外光灯(254nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
糊精检验标准操作规程

糊精检验标准操作规程1. 目的建立糊精检验标准操作规程,规范操作。
2. 范围适用于糊精的检验。
3. 依据:《中国药典》2010版二部。
4. 职责4.1 起草:QC 审核:质量保证部负责人批准人:质量管理负责人。
4.2 QC实施本规程。
4.3 QA监督本规程的实施。
5. 内容5.1性状本品为白色或类白色的无定形粉末;无臭,味微甜。
本品在沸水中易溶,在乙醇或乙醚中不溶。
5.2 鉴别5.2.1 试液及仪器一般实验仪器。
碘试液:可取用碘滴定液(0.05mol/L)。
取碘13.0g,加碘化钾36g与水50ml溶解后,加盐酸3滴与水适量使成1000ml,摇匀,用垂熔玻璃滤器滤过。
5.2.2 分析步骤取本品10%的水溶液1ml,加碘试液1滴,观察应显红色。
5.3 检查5.3.1 酸度5.3.1.1 试液及仪器一般实验仪器。
酚酞指示液:取酚酞1g ,加乙醇100ml 使溶解,即得。
氢氧化钠滴定液(0.1mol/L ):取氢氧化钠适量,加水振摇使溶解成饱和溶液,冷却后,置聚乙烯塑料瓶中,静置数日,澄清后备用。
取澄清的氢氧化钠饱和溶液5.6ml ,加新沸过的冷水使成1000ml ,摇匀。
5.3.1.2 分析步骤取本品5.0g ,加水50ml ,加热使溶解,放冷,加酚酞指示液2滴与氢氧化钠滴定液(0.1mol/L )2.0ml ,观察应显粉红色。
5.3.2 还原糖5.3.2.1 试液及仪器一般实验仪器。
碱性酒石酸铜试液:(1)取硫酸铜结晶6.93g ,加水使溶解成100ml 。
(2)取酒石酸钾钠结晶34.6g 与氢氧化钠10g ,加水使溶解成100ml 。
用时将两液等量混合,即得。
5.3.2.2 分析步骤取本品2.0g ,加水100ml ,振摇5分钟,静置,滤过;取滤液50ml ,加碱性酒石酸铜试液50ml ,煮沸3分钟,用105℃恒重的垂熔玻璃坩埚滤过,滤渣先用水、再用乙醇、最后用乙醚分次洗涤,在105℃干燥2小时,精密称定,重量用M (g )表示,恒重的垂熔玻璃坩埚重量用M 0(g )表示,照下式计算:遗留的氧化亚铜(g )=0-M M ………………公式① 遗留的氧化亚铜不得过0.20g 。
黄连质量标准及检验操作规程
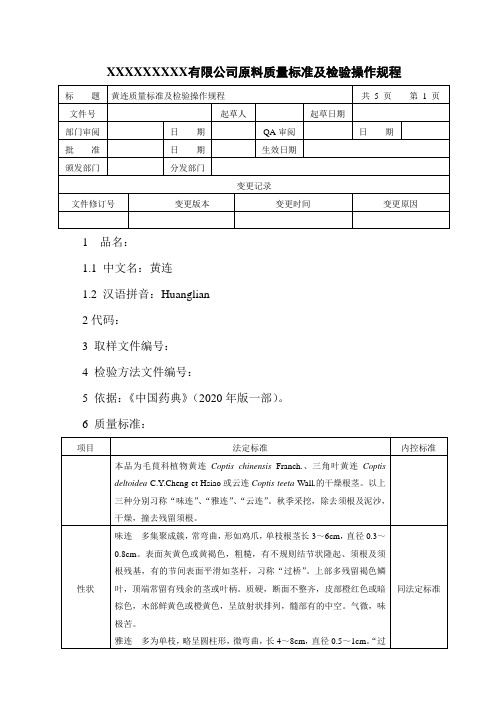
XXXXXXXXX有限公司原料质量标准及检验操作规程1 品名:1.1 中文名:黄连1.2 汉语拼音:Huanglian2代码:3 取样文件编号:4 检验方法文件编号:5 依据:《中国药典》(2020年版一部)。
6 质量标准:7 检验操作规程:7.1 试药与试剂:甲醇、黄连对照药材、盐酸小檗碱对照品、环己烷、乙酸乙酯、异丙醇、水、三乙胺、氨水、乙腈、磷酸二氢钾、硫酸、乙醇、盐酸。
7.2 仪器与用具:显微镜、水浴锅、三用紫外分析仪、恒温鼓风干燥箱、马福炉、硅胶G薄层板、超声波清洗器、薄层色谱扫描仪、高效液相色谱仪。
7.3 性状:取本品适量,自然光下目测色泽,嗅闻气味。
7.4 鉴别:7.4.1 取本品制片置10×10显微镜下做显微观察。
7.4.2取本品粉末约0.25g,加甲醇25ml,超声处理30分钟,滤过,取滤液作为供试品溶液。
另取黄连对照药材0.25g,同法制成对照药材溶液。
再取盐酸小檗碱对照品,加甲醇制成每1ml含0.5mg的溶液,作为对照品溶液。
照薄层色谱法(附录7)试验,吸取上述三种溶液各1μl,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯-异丙醇-甲醇-水-三乙胺(3:3.5:1:1.5:0.5:1)为展开剂,置用浓氨试液预饱和20分钟的展开缸内,展开,取出,晾干,置紫外光灯(365nm)下检视。
供试品色谱中,在与对照药材色谱相应的位置上,显4个以上相同颜色的荧光斑点;对照品色谱相应的位置上,显相同颜色的荧光斑点。
7.5 检查:7.5.1 水分:不得过14.0%(附录15第一法)。
7.5.2 总灰分:不得过5.0%(附录17)。
7.5.3二氧化硫残留量照二氧化硫残留量测定法(附录58)测定,不得过150mg/kg。
7.6 浸出物:照醇溶性浸出物测定法(附录19)项下的热浸法测定,用稀乙醇作溶剂,不得少于15.0%。
7.7 含量测定:味连照高效液相色谱法(附录8)测定。
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;乙腈-0.05mol/L磷酸二氢钾溶液(50:50)(每100ml中加十二烷基硫酸钠0.4g,再以硫酸调节pH值为4.0)为流动相;检测波长为354nm。
糊精标准操作规程(2015版药典)资料

文件编号页码共8页第1页文件名称糊精检验标准操作规程版次01制定人制定日期审核人审核日期批准人批准日期颁发部门GMP办公室颁发日期执行部门质管部生效日期分发部门:GMP办公室、质管部取代:目的:建立糊精检验标准操作规程。
范围:糊精的检验责任者: QC检验员、QC主管、质管部部长。
内容:1. 性状1.1 操作方法取本品,置明亮光线下,目测口尝法检测;称取供试品适量,于25℃±2℃分别用沸水、乙醇和乙醚溶解,每隔5分钟强力振摇30秒钟,观察30分钟内的溶解情况。
1.2 结果与判定本品为白色或类白色的无定形粉末;无臭,味微甜。
在沸水中易溶,在乙醇或乙醚中不溶,判为符合规定。
2.鉴别2.1 仪器与用具试管。
2.2 试药与试液碘试液。
2.3 操作方法取本品10%的水溶液1ml,加碘试液1滴,观察溶液的颜色。
2.4 结果与判定溶液显紫红色,判为符合规定。
文件编号页码共8页第2页文件名称糊精检验标准操作规程版次013.检查3.1 酸度3.1.1 仪器与用具试管。
3.1.2 试药与试液酚酞指示液、氢氧化钠滴定液(0.1mol/L)。
3.1.3 操作方法取本品5.0g,加水50ml,加热使溶解,放冷,加酚酞指示液2滴与氢氧化钠滴定液(0.1mol/L)2.0ml,观察溶液的颜色。
3.1.4 结果与判定溶液显粉红色,判为符合规定。
3.2 干燥失重3.2.1 简述药品的干燥失重,系指药品在规定的条件下干燥后所减失重量的百分率。
主要指水分、结晶水及其它挥发性物质如乙醇等,从减失的重量和取样量计算供试品的干燥失重。
3.2.2 仪器与用具烘箱(最高温度300℃,控温精度±1℃)、干燥器、扁形称量瓶、分析天平。
3.2.3 操作方法称取本品约1g,置干燥至恒重的扁形称量瓶中,精密称重,在105℃干燥至恒重。
3.2.4 记录与计算3.2.4.1 记录记录干燥的温度,称量的数据,计算和结果等。
3.2.4.2 计算计算式干燥失重% =132 1m mmm-+× 100%式中:1m———供试品的重量;文件编号页码共8页第3页文件名称糊精检验标准操作规程版次01m———恒重称量瓶的重量;2m——称量瓶与供试品干燥后的总重量。
高效液相色谱法测定万应胶囊中胡黄连苷Ⅰ和胡黄连苷Ⅱ的含量

高效液相色谱法测定万应胶囊中胡黄连苷Ⅰ和胡黄连苷Ⅱ的含
量
陈惠英;宋粉云
【期刊名称】《中国药房》
【年(卷),期】2006(17)13
【摘要】目的:建立以高效液相色谱法测定万应胶囊中胡黄连苷Ⅰ和胡黄连苷Ⅱ含量的方法.方法:色谱柱为 DiamonsidTM C18,流动相为乙腈-水-冰醋酸(20: 80: 0.5),检测波长为 266nm,流速为 1.0ml/min.结果:胡黄连苷Ⅰ、胡黄连苷Ⅱ检测浓度分别在 9.55~95.5μ g/ml(r=0.9 997)、 15.6~156μ g/ml(r=0.9 998)范围内线性关系良好,平均回收率分别为 99.7%(RSD=2.46%)、 101.2%(RSD=2.35%).结论:本方法简便、快速、准确、回收率好,可用于该制剂的质量控制.
【总页数】2页(P1011-1012)
【作者】陈惠英;宋粉云
【作者单位】广州经济技术开发区医院药剂科,广州市,510630;广东药学院,广州市,510224
【正文语种】中文
【中图分类】R927.2
【相关文献】
1.高效液相色谱测定清肝颗粒中胡黄连苷Ⅰ和胡黄连苷Ⅱ含量的研究 [J], 尚立霞;刘玲玲;王菲;张清华
2.RP-HPLC法测定清热八味胶囊中胡黄连苷Ⅰ的含量 [J], 石欣;鲍劲松;白雅静
3.反相HPLC法测定苏斯-12胶囊中胡黄连苷Ⅱ的含量 [J], 韩塔娜
4.高效液相色谱法测定蒙药清感九味中胡黄连苷的含量 [J], 白在贤;王栋;林燕
5.薄层色谱扫描法测定胡黄连中胡黄连苷I含量 [J], 孟琳;孙君辉
因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
原药材检验标准操作规程
目的:建立一个中药饮片原药材检验标准操作程序,确保检验结果准确可靠。
适用范围:中药原药材。
责任人:质量保证部主任、质量控制部主任、化验员。
标准来源:《中华人民共和国药典》2010年版一部、《安徽省中药饮片炮制规范》。
内容:
1、性状
取本品适量,放入白瓷盘中,用眼观察,可见以下性状特征:
本品呈圆柱形,略弯曲,偶有分枝,长3~12cm,直径O.3~1cm。
表面灰棕色至暗棕色,粗糙;有较密的环状节,具稍隆起的芽痕或根痕,上端密被暗棕色鳞片状的叶柄残基。
体轻,质硬而脆,易折断,断面略平坦,淡棕色至暗棕色,木部有4~10个类白色点状维管束排列成环。
气微,味极苦。
2、鉴别
主要使用仪器:电子分析天平、电子显微镜、紫外光灯等。
2.1显微鉴别:
取本品粉末0.5g,置适宜器皿中,60~80℃升华4小时,置显微镜下观察,可见针状、针簇状、棒状、板状结晶及黄色球状物。
2.2 薄层鉴别
取2.1.3项下的升华物,加三氯甲烷数滴使溶解,作为供试品溶液。
另取香草酸对照品、肉桂酸对照品,加三氯甲烷制成每1ml各含lmg的混合溶液,作为对照品溶液。
照薄层色谱法(《中华人民共和国药典》附录VI B)试验,吸取上述两种溶液各5μl,分别点于同一硅胶GF薄层板上,以正己烷一乙醚-冰醋酸(5:5:0.1)为展开剂,展开,取出,晾干,置紫外光灯(254nm)下检视。
供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。
3、检查
主要使用仪器:电子分析天平、电热恒温干燥箱、马弗炉、坩埚等。
3.1 水分
取供试品2-5g,平铺于干燥至恒重的扁形称量瓶中厚度不超过5mm,精密称定,打开瓶盖在100~105℃干燥5小时,将瓶盖盖好,移置干燥器中,冷却30分钟,精密称定,再在上述温度干燥1小时,冷却,称重,至连续两次称重的差异不超过5mg为止。
根据减失的重量,按下式计算即得。
W2-W3
供试品中的含水量(%)=────────×100%
W2-W
W 称量瓶重(g)
W2 烘前称量瓶和样品重之和(g)
W3 烘后称量瓶和样品重之和(g)
本品含水量不得过13.0%。
3.2总灰分
取供试品适量,粉碎使能通过二号筛混合均匀后,取3~5g,置炽灼至恒重的坩埚中,称定重量(准确至0.01g),缓缓炽热,注意避免燃烧,至完全炭化时,逐渐升高温度至500~600℃,使完全灰化并至恒重。
根据残渣重量,按下式计算即得。
W2-W1
供试品中总灰分的含量(%)=────────×100%
W
W1坩埚重(g)
W 样品重(g)
W2炽灼残渣与坩埚重之和(g)
本品总灰分不得过7.0%。
3.3酸不溶灰分
取上项所得的灰分,在坩埚中小心加入稀盐酸约10ml,用表面皿覆盖坩埚,置水浴上加热10分钟,表面皿用热水5ml冲洗,洗液并入坩埚中,用无灰滤纸滤过,坩埚内的残渣用水洗于滤纸上,并洗涤至洗液不显氯化物反应为止。
滤渣连同滤纸移置同一坩埚中,干燥,炽灼至恒重。
根据残渣重量,按下式计算即得。
W2-W1
供试品中酸不溶灰分的含量(%)=────────×100%
W
W1坩埚重(g)
W 样品重(g)
W2炽灼后残渣与坩埚重之和(g)
本品酸不溶灰分不得过3.0%。
3.4二氧化硫残留量
二氧化硫残留量按中国药典2010 年版第一增补本附录二氧化硫残留量测定法测定,取本品细粉10g,精密称定,置于两颈圆底烧瓶中,加水300ml—400 ml (应加水至没过氮气导气管的下端),取6mol/L盐酸10ml加入带刻度的分液漏斗中连接分液漏斗,并导入氮气至瓶底,。
锥形瓶内加水125ml和淀粉指示液1 ml作为吸收液,置于磁力搅拌器上不断搅拌。
连接回流冷凝管,在冷凝管上部连接导气管,将导气管插入250ml锥形瓶底部,开通氮气,调节氮气流量为0.2L/min,打开带刻度的分液漏斗的活塞,使盐酸流入烧瓶。
加热圆底烧瓶内的溶液至沸,并保持微沸约3分钟后开始用0.01mol/l, 的碘滴定液滴定,吸收液置于磁力搅拌器上不断搅拌,至吸收液显蓝色或蓝紫色,持续30秒不消失,并将滴定的结果用空白校正,每1毫升的碘滴定液(0.01mol/l)相当于0.6406mg的二氧化硫。
本品二氧化硫量不得过150mg/kg。
4 浸出物
主要使用仪器:电子分析天平、电热恒温干燥箱、水浴锅、蒸发皿等。
取供试品适量,粉碎使能通过二号筛,并混合均匀后,取约2~4g,精密称定,置100~250ml的锥形瓶中,精密加乙醇50~100ml,密塞,称定重量,静置1小时后,连接回流冷凝管,加热至沸腾,并保持微沸1小时。
放冷后,取下锥形瓶,密塞,再称定重量,用乙醇补足减失的重量,摇匀,用干燥滤器滤过,精密量取滤液25ml,置已干燥至恒重的蒸发皿中,在水浴上蒸干后,于105℃干燥3小时,置干燥器中冷却30分钟,迅速精密称定重量。
以干燥品按下式计算即得。
(W2-W1)×2
供试品中醇溶性浸出物的含量(%)=────────×100%
W×(1-W4)
W 样品重(g)
W1蒸发皿重(g)
W2残渣与蒸发皿重之和(g)
W4 供试品的含水量(%)。
本品浸出物不得少于30.0%。
5、含量测定
照高效液相色谱法(《中华人民共和国药典》附录VI D)测定。
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;以甲醇-水-磷酸(35:65:0.1)为流动相;检测波长为275nm。
理论板数按胡黄连苷Ⅱ峰计算应不低于3000。
对照品溶液的制备取胡黄连苷I对照品、胡黄连苷Ⅱ对照品适量,精密称定,加甲醇制成每1ml各含40μg的混合溶液,即得。
供试品溶液的制备取本品粉末(过三号筛)约0.1g,精密称定,置具塞锥形瓶中,精密加入甲醇50ml,密塞,称定重量,超声处理(功率250W,频率33kHz)30分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液1ml,置5m1量瓶中,加甲醇至刻度,摇匀,即得。
测定法分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,即得。
本品以干燥品按下式计算即得:
A x×C R×V x
供试品的含量(%)=────────——×100%
A R×G×(1-W)×106
A x 供试品的峰面积或峰高。
V x 供试品的体积(ml)
C R 对照品的浓度
A R 对照品的峰面积或峰高
G 供试品的重量(g)
W 供试品的含水量(%)
本品按干燥品计算,含胡黄连苷I(C24H28011)与胡黄连苷Ⅱ(C24H28011)的总量不得少于9.0%。
