从废钒催化剂中回收五氧化二钒-资料
废脱硝催化剂中五氧化二钒回收工艺研究

废脱硝催化剂中五氧化二钒回收工艺研究近年来,随着国家的大力推进环保政策,废脱硝催化剂中五氧化二钒(V2O5)的回收工艺研究变得日益重要。
V2O5是一种重要的综合利用资源,在催化剂原料、染料、农药、精细化工等行业中均有应用。
然而,由于无法完全分离V2O5成分,废脱硝催化剂中V2O5利用率较低,回收成本高。
因此,如何利用废脱硝催化剂中的V2O5成分,是当前面临的一个重要问题。
在硝催化剂中,V2O5是金属元素成分之一,主要来源于氮氧化物的烷基催化反应。
由于V2O5的亲水性,它非常抗腐蚀,是构成硝催化剂中的重要组成部分,而且V2O5含量较高,有利于提高反应效率。
因此,为了利用废脱硝催化剂中的V2O5,首先必须可靠地实现V2O5的回收利用,以提高V2O5的利用率和回收效率。
目前,回收V2O5工艺技术基本分为三类。
第一类是采用物理方法,如采用磁控溅射、湿法分离和萃取分离等方法,可以有效地从废脱硝催化剂中回收V2O5成分。
第二类是采用化学方法,如溶剂萃取、水溶液氧化等,可以将V2O5以及其他金属元素分离出来。
第三类是采用工艺化学方法,如吸附、还原等,也可以有效地分离V2O5,同时又能够有效地提高回收效率。
目前,V2O5工艺分离研究要求系统地研究不同回收工艺对V2O5回收效率和回收成本的影响。
研究发现,将湿法分离与萃取分离相结合,可以大大提高V2O5的回收效率,降低回收成本。
此外,可以通过改进水溶液的pH值、溶解剂的类型及浓度,改变溶剂萃取的工艺条件,不断改善回收效率,同时降低回收成本。
除了以上工艺外,V2O5回收技术还有待改进。
废旧硝催化剂中V2O5的回收效率低,在废弃物管理、高产量分离、新型回收工艺等方面存在空白。
因此,深入研究V2O5回收工艺,不仅可以更好地利用废旧硝催化剂中的V2O5,还可以环保、降低生产成本,具有重要的环境保护意义。
综上所述,废脱硝催化剂中的V2O5回收工艺研究引起了相当的重视,有着重大的环境保护意义。
2016年高考新课标全国卷Ⅲ理综化学真题(带解析)

2016年高考新课标全国卷Ⅲ理综化学真题(带解析)DC.浓盐酸与MnO2反应制备纯净Cl2气体产物先通过浓硫酸,后通过饱和食盐水l4萃取碘水中的I2先从分液漏斗下口放出有机层,后从上口倒出水层A.A B.B C.C D.D 4.已知异丙苯的结构简式如下,下列说法错误的是()A.异丙苯的分子式为C9H12B.异丙苯的沸点比苯高C.异丙苯中碳原子可能都处于同一平面D.异丙苯的和苯为同系物5.锌–空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH–+2H2O===2Zn(OH)。
下列说法正确的是()A.充电时,电解质溶液中K+向阳极移动B.充电时,电解质溶液中逐渐减小C.放电时,负极反应为:Zn+4OH–-2e–===Zn(OH)D.放电时,电路中通过2mol电子,消耗氧气22.4L (标准状况)6.四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性。
下列说法正确的是()A.简单离子半径:W< X<ZB.W与X形成的化合物溶于水后溶液呈碱性C.气态氢化物的热稳定性:W<YD.最高价氧化物的水化物的酸性:Y>Z7.下列有关电解质溶液的说法正确的是()A.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中减小B.将CH3COONa溶液从20℃升温至30℃,溶液中增大C.向盐酸中加入氨水至中性,溶液中D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中不变二、综合题(共6小题)8. 过氧化钙微溶于水,溶于酸,可作分析试剂、医用防腐剂、消毒剂。
以下是一种制备过氧化钙的实验方法。
回答下列问题:(一)碳酸钙的制备(1)步骤①加入氨水的目的是_______。
小火煮沸的作用是使沉淀颗粒长大,有利于____。
2020届高考化学三轮大题强化特训-《工业流程(八)》
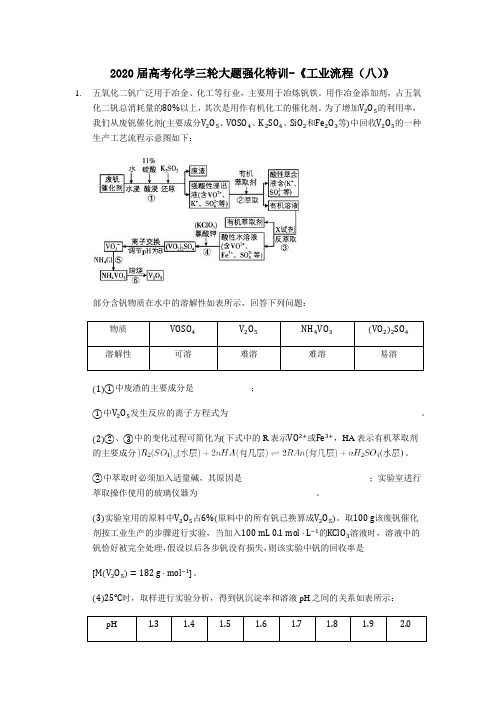
2020届高考化学三轮大题强化特训-《工业流程(八)》1.五氧化二钒广泛用于冶金、化工等行业,主要用于冶炼钒铁。
用作冶金添加剂,占五氧化二钒总消耗量的80%以上,其次是用作有机化工的催化剂。
为了增加V2O5的利用率,我们从废钒催化剂(主要成分V2O5、VOSO4、K2SO4、SiO2和Fe2O3等)中回收V2O5的一种生产工艺流程示意图如下:部分含钒物质在水中的溶解性如表所示,回答下列问题:(1)①中废渣的主要成分是_____________;①中V2O5发生反应的离子方程式为____________________________________________。
(2)②、③中的变化过程可简化为(下式中的R表示VO2+或Fe3+,HA表示有机萃取剂的主要成分。
②中萃取时必须加入适量碱,其原因是_____________________________;实验室进行萃取操作使用的玻璃仪器为___________________________。
(3)实验室用的原料中V2O5占6%(原料中的所有钒已换算成V2O5)。
取100g该废钒催化剂按工业生产的步骤进行实验,当加入100mL0.1mol·L−1的KClO3溶液时,溶液中的钒恰好被完全处理,假设以后各步钒没有损失,则该实验中钒的回收率是_____________[M(V2O5)=182g·mol−1]。
(4)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如表所示:试判断在实际生产时,⑤中加入NH4Cl调节溶液的最佳pH为_____________;若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则此时溶液中c(Fe3+)≤_____________(已知:25℃时K sp[Fe(OH)3]=2.6×10−39)。
【答案】(1)SiO2;(2)加入碱,中和H2SO4,使平衡正移;分液漏斗、烧杯(3)91.0%(4)1.7;2.6×10−3mol·L−1【解析】【分析】本题考查工艺流程,难度一般,是高频考点,涉及离子方程式的书写、化学平衡的移动、氧化还原反应的计算、溶度积的计算等,侧重分析能力和计算能力的考查。
工艺流程大题(一)(解析版)

工艺流程大题1.(2019·广西桂林十八中高三月考)亚氯酸钠( NaClO2)是一种高效氧化剂和漂白剂,主要用于棉纺、纸张漂白、食品消毒、水处理等。
已知:NaClO2饱和溶液在温度低于38 ℃时析出的晶体是NaClO2 3H2O,高于38 ℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
纯ClO2易分解爆炸。
一种制备亚氯酸钠粗产品的工艺流程如下:(1)ClO2发生器中的离子方程式为________,发生器中鼓人空气的作用可能是__________(选填序号)。
a.将SO2氧化成SO3,增强酸性b.稀释ClO2以防止爆炸c.将NaClO3还原为ClO2(2)吸收塔内反应的化学方程式为________,吸收塔的温度不能超过20℃,其原因是_____________。
(3)从“母液”中可回收的主要物质是__________________。
(4)从吸收塔中可获得NaClO2溶液,从NaClO2溶液到粗产品(NaClO2)经过的操作步骤依次为:①减压,55℃蒸发结晶;②______;③_______;④低于60℃干燥,得到成品。
(5)为测定粗品中NaClO2的质量分数,做如下实验:准确称取所得亚氯酸钠样品10.00 g于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴人适量的稀硫酸,充分反应(ClO2-+ 4I-+ 4H+= 2H2O+ 2I2+ Cl-)。
将所得混合液配成250mL待测溶液,取25.00 mL待测液,用2.000 mol.L-l Na2S2O3标准液滴定(I2+2S2O32-= 2I-+S4O62-),测得消耗Na2SO3溶液平均值为16.40mL。
该样品中NaClO2的质量分数为______________。
【答案】2ClO3-+SO2=2ClO2↑+SO42- b 2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2↑防止H2O2分解Na2SO4趁热过滤38-60℃温水洗涤74.21%【解析】【分析】NaClO3在酸性条件下与二氧化硫发生氧化还原反应生成ClO2,同时得到Na2SO4,然后与过氧化氢在碱性条件下反应生成NaClO2,将溶液蒸发浓缩、冷却结晶、过滤可得到NaClO3,母液中主要含有Na2SO4,据此分析解答。
2020届高考化学 化工流程中重要物质的确定(解题方法解析+题目专练有答案)

化工流程中重要物质的确定工艺流程题考查的目的性很强,考生应当从题干内容出发,找清题目的目的,按照目的去分析流程。
【典例解析】以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。
从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。
废钒催化剂的主要成分为:以下是一种废钒催化剂回收工艺路线:废矾催化剂V2O5浸液H2SO4KClO3KOH 淋洗液NH4Cl废渣1 废渣2 流出液(该题目的是制备V2O5,期中V价态是+5价,所以原材料+4的V应在流程中升价,SiO2、Fe2O3、Al2O3要通过沉淀法除去,K2SO4用其他方式除去。
初步分析之后对应到上面流程图,可以立刻分析得到,废渣1是SiO2,废渣2是铁和铝的相关沉淀,流出液是K2SO4的相关溶液,流程中氧化操作就是将+4价的V 氧化到+5价)【题目专练】1.废旧印刷电路板是一种电子废弃物,其中铜的含量达到矿石中的几十倍。
湿法技术是将粉碎的印刷电路板经溶解、萃取、电解等操作得到纯铜等产品。
某化学小组模拟该方法回收铜和制取胆矾,流程简图如下:流程中有三处实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是________。
循环使用的NH4Cl在反应Ⅰ中的主要作用是_________________________________________。
答案H2SO4防止由于溶液中的c(OH-)过高,生成Cu(OH)2沉淀解析操作④得到的H2SO4可以利用到反应Ⅲ中,所以第三处循环的试剂为H2SO4;NH4Cl水解溶液呈酸性,可以中和溶液中的OH―,防止由于溶液中的c(OH-)过高,生成Cu(OH)2沉淀。
2.毒重石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:加入NH3·H2O),滤渣Ⅱ中含________(填化学式)。
加入H2C2O4时应避免过量,原因是_____________________________________。
从废钒催化剂中回收钒氧化物的研究

St y o r c v r fv a i ud n e o e y o an d um x d r m s e c t y t c nt i i a ad u o i e f o wa t a al s o a n ng v n i m
Ha i i,igZ o  ̄ a HuBni oX c J h n in , i e a n j
o t ie . h e r c s a r a r e rs e ta d wi r g b t re o o c a d s c a b n f s b an d T e n w p o e sh s a ge tma k t o p c n l b i et c n mi n o il e e t. p l n e i
提供适宜的工艺条件 。在此工艺条件下 , 以制备 出质量优 于 G / 2 3 18 金 9 可 B T3 8- 9 7冶 9级标 准的五氧 化二钒产
品, 具有较好 的经济效益和社会效益 ; 离子交换 ; 五氧化二钒
中图 分 类号 :Q15 1 T 3 .1 文 献 标 识 码 : A 文 章 编 号 :06— 90 2 1 ) 1 0 4 0 10 4 9 f0 0 1 — 0 8— 3
t n , 2 5 hs qa tw s u ei e 9M t l g aa i O ieP d c S n a ( B T38 - 18 ) ol b i sV oe uly a spr ro h e l ryV ndc xd r u t t d r G / 23 9 7 cud e o Ow i ott 9 au o a d
老高考旧教材适用2023版高考化学二轮复习大题突破练1化学工艺流程题(含答案)

高考化学二轮复习小题提速练:大题突破练1 化学工艺流程题1.(2022江西新八校第二次联考)五氧化二钒(V2O5)是一种橙黄色片状晶体,具有强氧化性。
在冶金、催化剂、磁性材料等领域有重要作用。
实验室以含钒废料(含有V2O3、Fe2O3、Al2O3、CuO、有机物等)来制备V2O5的一种工艺流程如下:已知:“滤渣2”为Mg2(OH)2CO3。
请回答下列问题:(1)含钒废料中的有机物主要在工序中除去。
(2)常温时,若“调pH净化Ⅰ”工序中最终溶液pH=8,通过计算判断,此时Cu2+是否已经沉淀完全(填“是”或“否”),并写出计算过程(已知离子浓度<1.0×10-5mol·L-1认为沉淀完全,K sp[Cu(OH)2]=4.8×10-20)。
(3)“净化Ⅱ”时若加入过量的(NH4)2CO3,可能导致的后果为。
(4)煅烧反应同时有氨气生成,实验室检验该气体的方法为。
NH4VO3要在流动空气中煅烧的原因可能是。
(5)在硫酸酸化条件下,V2O5可与草酸(H2C2O4)溶液反应得到含VO2+的溶液,反应的离子方程式为。
(6)全钒液流电池的电解质溶液为VOSO4溶液,电池的工作原理为V+V2++2H+VO2++H2O+V3+电池充电时,阳极的电极反应为。
2.(2022广西桂林、梧州一模)市政污泥含大量金属(Cu、Zn、Ni、Fe、Ag等),不经处理直接填埋会对环境造成严重的污染。
市政污泥的综合利用能够使其得到科学、妥善的处置,并可以作为资源再次被我们利用,同时可以带来一定的经济价值。
某科研团队利用市政污泥回收皓矾(ZnSO4·7H2O)的工艺流程如下:已知:“沉铁”时若pH过高,会产生具有较强吸附性的氢氧化铁胶状沉淀。
回答下列问题:(1)为提高“酸浸”效率,可采取的措施有(任写一条)。
(2)“一系列操作”主要包括、、过滤、洗涤、干燥。
(3)用锌粉除铜、镍时,先除去铜,然后分离再置换除镍,用锌粉直接置换速率极慢,目前采用“锑盐净化法”,即置换时在酸性、含Ni2+溶液中同时加入锌粉和Sb2O3,得到金属Ni和Sb的混合物,该混合物可表示为NiSb,形成NiSb的离子方程式为。
从废铂钒催化剂中分步提炼五氧化二钒和海绵铂

中国资源综合利用China Resources Comprehensive Utilization Vol.35,No.52017年5月- 125 -工作研究从废铂钒催化剂中分步提炼五氧化二钒和海绵铂相亚波,赵栋云,王建忠,郁丰善,何志鸿,李永敏(江西省汉氏贵金属有限公司,江西 万年 335500)摘要:对失效铂炭催化剂中钒和铂的分离提纯进行研究,通过先分离提取钒来简化精炼铂金属的操作流程,优化回收工艺,且分离后对钒和铂进行分别回收,制得高纯度的五氧化二钒和海绵铂。
关键词:铂炭催化剂;钠化焙烧;五氧化二钒;海绵铂中图分类号:TF841.3 文献标识码:A 文章编号:1008-9500(2017)05-0125-02Recovery Vanadium Pentoxide and Platinum from Spent Pt/V CatalystXiang Yabo, Zhao Dongyun, Wang Jianzhong, Yu Fengshan, He Zhihong, Li Yongmin(Jiangxi Han's Precious Metals Co., Ltd., Wannian 335500, China)Abstract : Study on the technology of separation and purification process of vanadium and platinum from spent Pt-V/C catalyst. Simplifying the operation process of refined platinum metal by separating and extracting vanadium firstly, optimum recovery process. After separation, vanadium and platinum were recovered respectively, high purity Vanadium Pentoxide and Platinum sponge be prepared.Keywords : Pt-V/C catalyst; sodiumzation-roasting; Vanadium Pentoxide; platinum spongePt/C 催化剂广泛应用于石油化工、环境治理、制药、香料、染料及其他精细化工领域,在制备这些催化剂时,往往会加些助剂来加以修饰,如Fe、Sn、Bi、S、V、Cu、K 等,用来提高催化剂的选择性和使用寿命,而Pt-V/C 载体催化剂应用于卤代硝基物还原和还原烷基化反应。
五氧化二钒催化剂简介

五氧化二钒催化剂简介一、五氧化二钒的性质1、物理性质五氧化二钒英文名称Vanadium pentoxide,别名钒(酸)酐,摩尔质量181.88 g /mol,外观,橙黄色或红棕色固体,分子式V2O5 ,外观与性状橙黄色或红棕色结晶粉末,分子量181.88 ,熔点,690℃(963 K),溶解性,微溶于水,不溶于乙醇,溶于浓酸、碱,密度,相对密度(水=1)3.35 ,稳定性,稳定在水中的溶解度为0.8g/100ml,(20 °C),有剧毒,溶液呈微黄。
在670 °C时熔融,冷却时结晶成黑紫色正交晶体系的针状晶体,它的结晶热很大,当迅速结晶时会因灼热而发光。
2、化学性质五氧化二钒是两性氧化物,但是主要以酸性为主。
五氧化二钒是一种中等强度的氧化剂,可被还原成各种低价态的氧化物。
五氧化二钒酸性显著,碱性表现不强,既可溶于酸生成相应的黄色偏钒酸根,在PH2左右可沉淀为偏钒酸,也可溶于碱生成偏钒酸盐溶液。
五氧化二钒中的正五价钒可被还原,在酸性介质得到VIV,蓝色的VO(H2O)52+钒氧基离子。
以盐酸和氢溴酸作还原剂,氧化产物是相应的卤素单质。
二、五氧化二钒的应用V2O5是最重要的矾氧化物,在工业上用量最大,除用于生产合金外还和其他钒化合物主要用于玻璃与陶瓷工业的着色剂、硫酸和石油化工生产用的催化剂、以及用作苯胺黑染料和有机合成的催化剂等方面,它不仅价廉、活性大,且不易中毒。
三、五氧化二钒的生产方法1、用钒渣生产五氧化二钒钒渣是含钒较高的提钒原料,回收技术比较成熟。
首先将矿石进行预处理,如钒钛磁铁矿,经粉碎、磁选得到钒精矿;第二步将经过烧结的钒精矿用高炉生产含钒生铁,矿中80%以上的钒进入铁水,然后将熔融状态的含钒生铁在雾化炉吹炼或在转炉中吹炼,使铁水中的钒、锰、钛、磷等一些杂质同时进入渣中得到钒渣;第三步再以钒渣为原料提取钒。
从钒渣中提取钒主要是将低价钒氧化为,使之生成溶于水的钒酸钠,再用水浸出到溶液中使钒与固体分离,然后再从溶液中沉淀出钒酸盐,使钒与液相分离,最终将钒酸盐转化为五氧化二钒。
从废铂钒催化剂中分步提炼五氧化二钒和海绵铂

( 江西 省汉 氏贵 金属 有 限公 司,江 西 万年 3 3 5 5 0 0 )
摘 要 :对 失效 铂 炭催 化 剂 中钒 和 铂 的 分 离提 纯进 行 研 究 , 通 过 先 分 离提 取钒 来 简化精 炼铂 金属 的操 作 流程 , 优 化 回 收 工 艺 ,且 分 离后 对 钒和 铂 进 行 分 别 回收 ,制 得 高纯度 的五 氧 化二 钒 和 海 绵铂 。 关 键 词 :铂 炭 催 化 剂 ;钠 化 焙烧 ;五 氧 化二 钒 ;海 绵铂 中 图分 类号 :T F 8 4 1 . 3 文献标 识码 :A 文章 编号 :1 0 0 8 — 9 5 0 0 ( 2 0 1 7 ) 0 5 — 0 1 2 5 — 0 2
P t / C催化剂广泛应用 于石 油化工 、环境 治理 、制 药 、香料 、染料及其他精 细化工领域 ,在制备这些催
1 实验 1 . 来 加 以修饰 ,如 F e 、s n 、
B i 、s 、V、c u 、K等 ,用来提高催化剂 的选择性和使 用寿命 ,而 P t — V / C载体催 化剂 应用 于 卤代硝基 物还
a n d Pl a t i n u m s p o n g e b e p r e p a r e d . Ke y wo r ds : P t - V/ C c a t a l y s t ; s o d i u mz a t i o n - r o a s t i ng ; Va n a d i u m P e n t o x i d e ; p l a t i n u m s p o n g e
Abs t r a c t : S t u d y o n t h e t e c h n o l o g y o f s e p a r a t i o n a n d p u r i ic f a t i o n p r o c e s s o f v a n a d i um a n d p l a t i n u m f r o m s p e n t P t — V/ C c a t a l y s t . S i mp l i f y i n g t h e o p e r a t i o n p r o c e s s o f r e in f e d p l a t i n u m me t a l b y s e p a r a t i n g a n d e x t r a c t i n g v a n a d i u m ir f s t l y , o p t i mu m
分段溶解法从废钒催化剂中回收五氧化二钒

分段溶解法从废钒催化剂中回收五氧化二钒
蒋馥华;张萍;申照全
【期刊名称】《化学世界》
【年(卷),期】1995(36)12
【摘要】应用反浮选原理去除废钒催化剂中的大部分硅后,先在弱酸性介质中溶解出低价钒,然后对未溶物料进行高温焙烧,再在弱碱性介质中进行第二次溶解,使高价钒亦转入溶液中。
浸出液轻氧化、中和处理,并用离子交换法净化料液,一次沉钒即可获得纯度达99.5%的V2O5产品。
钒回收率在90%以上。
【总页数】5页(P661-665)
【关键词】废钒催化剂;五氧化二钒;回收;分段溶解法
【作者】蒋馥华;张萍;申照全
【作者单位】武汉冶金科技大学化工系,中南工业大学
【正文语种】中文
【中图分类】X783.05
【相关文献】
1.从废钒催化剂中回收五氧化二钒的研究 [J], 杨彦新;王致果
2.用天然碱浸法从废钒催化剂中回收五氧化二钒的试验 [J], 蒋馥华;张萍
3.从废钒催化剂中回收精制五氧化二钒的试验研究 [J], 王新文;雷兆敏
4.从废钒催化剂中回收五氧化二钒 [J], 孙德功;李健英
因版权原因,仅展示原文概要,查看原文内容请购买。
[题目]某学习小组欲从工业废钒催...
![[题目]某学习小组欲从工业废钒催...](https://img.taocdn.com/s3/m/3f09a741a517866fb84ae45c3b3567ec102ddc08.png)
从废钒催化剂中回收V2O5,由流程可知,“酸浸”时V2O5转化为VO2+,V2O4转成VO2+.氧化铁、氧化铝均转化为金属阳离子,只有SiO2不溶,则过滤得到的废渣1为SiO2,然后加氧化剂KClO3,将VO2+变为VO2+,再加KOH时,铁离子、铝离子转化为Fe(OH)3、Al(OH)3沉淀,同时中和硫酸,过滤得到的废渣2为Fe(OH)3、Al(OH)3,“离子交换”和“洗脱”可简单表示为:4ROH+V4O124-R4V4O12+4OH-,由ROH为强碱性阴离子交换树脂可知,碱性条件下利用反应正向移动,流出液中主要为硫酸钾,“沉钒”得到偏钒酸铵(NH4VO3)沉淀,“煅烧”时分解生成V2O5。
(5)“沉钒”是利用NH4Cl和K4V4O12反应得到偏钒酸铵(NH4VO3)沉淀,发生反应的化学方程式为4NH4Cl+K4V4O12=4NH4VO3+4KC1,故答案为:4NH4Cl+K4V4O12=4NH4VO3+4KC1。
(2)“氧化”的目的是使VO2+变为VO2+,写出该反应的离子方程式_______________。
(3)“中和”作用之一是使钒以V4O124-形式存在于溶液中,则“废渣2”的成分有_____________(用化学式表示)。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V4O124- R4V4O12+4OH-(ROH 为強碱性阴离子交换树脂)。“流出液”中阳离子最多的是___________;为了提高洗脱效率,淋洗液应该呈____________性(填“酸”、“碱”或“中”)。
【题目】某学习小组欲从工业废钒催化剂中回收V2O5,通过分析知该废钒催化剂的主要成分如下表:
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
浸
出
滤
洗
清
渣
抽
液
滤
滤 液
2020/4/4
四、实验步骤
3、氧化
1g
滤 液
加 热 近 沸
氯 酸 钾
加 热 搅 拌
黄 色 溶 液
2020/4/4
四、实验步骤
4、水解
90~95
℃ N
黄
加
a
色
热
O
溶
近
H
液
沸
溶
液
pH= 1~2
检
析
验
出
酸
沉
度
淀
0.5h 继 续 加 热
2020/4/4
四、实验步骤
5、分离
混 合 物
2020/4/4
一、目的要求
1.进一步锻炼设计实验的能力. 2.了解钒(V)的性质. 3.练习分离、沉淀、过滤等基本操作.
2020/4/4
二、实验原理
• ClO3- + 6VO2+ + 3H2O = 6VO2+ + Cl- + 6H+ • 2VO2+ +H2O=V2O5 + 2H+
2020/4/4
抽 滤
洗 涤
抽 干
称 量
2020/4/4
五、思考题
1. 写出各步的实验现象和反应方程式。
2020/4/4
三、仪器和试剂
2020/4/4
抽滤装置
烧杯
仪
器
量筒
研钵
蒸发皿
三、仪器和试剂
试 剂
2020/4/4
ቤተ መጻሕፍቲ ባይዱ
废催化剂 K2ClO3 pH试纸
H2SO4溶液 NaOH溶液
四、实验步骤
1、浸出
50g
120mL 1h
称 取 原 料
硫
充
酸
分
溶
搅
液
拌
混 合 物
2020/4/4
四、实验步骤
2、过滤 混 合 物
硫酸
倾
