乙醇优秀PPT课件
合集下载
乙醇的介绍ppt课件

用作药物合成原料,如合成镇痛药、麻醉药等。
乙醇在生产生活中应用
用作溶剂,如提取中药有效成分等。
日常生活应用
用作酒类饮品的原料,如啤酒、白酒、葡萄酒等 。
乙醇在生产生活中应用
01
用作调味品,如料酒、食用酒精 等。
02
用作清洁剂,如玻璃水、洗手液 等。
CHAPTER 02
乙醇生产工艺及流程
原料选择与预处理
分子式解读
乙醇分子由2个碳原子、6个氢原 子和1个氧原子组成,属于醇类有 机物。
物理性质与化学性质
物理性质 无色透明液体,有特殊香味。
易挥发,易燃烧,能与水以任意比互溶。
物理性质与化学性质
• 熔点为-114.1℃,沸点为78.3℃。
物理性质与化学性质
01
化学性质
02
03
04
具有醇的典型化学性质,如与 活泼金属反应、与羧酸发生酯
能源消耗
乙醇生产需要大量能源,如化石 燃料,其燃烧产生二氧化碳等温
室气体,加剧全球气候变化。
水资源消耗
生产过程中需要大量水资源,可 能导致水资源短缺和水污染问题
。
废气排放
发酵和蒸馏过程中产生的废气, 如二氧化碳、甲烷等,对大气环
境造成负面影响。
废弃物处理和资源回收利用方法探讨
废水处理
通过物理、化学或生物方法处理生产废水,降低有机物和悬浮物 含量,实现废水达标排放或回用。
实验操作步骤详解
建立健全环保法规和标准体系,加强生产 过程中的环保监管和执法力度,确保企业 达标排放。
推动循环经济
加强科技创新
鼓励企业开展循环经济实践,实现废弃物 资源化利用和能源梯级利用,降低生产过 程中的环境负荷。
乙醇在生产生活中应用
用作溶剂,如提取中药有效成分等。
日常生活应用
用作酒类饮品的原料,如啤酒、白酒、葡萄酒等 。
乙醇在生产生活中应用
01
用作调味品,如料酒、食用酒精 等。
02
用作清洁剂,如玻璃水、洗手液 等。
CHAPTER 02
乙醇生产工艺及流程
原料选择与预处理
分子式解读
乙醇分子由2个碳原子、6个氢原 子和1个氧原子组成,属于醇类有 机物。
物理性质与化学性质
物理性质 无色透明液体,有特殊香味。
易挥发,易燃烧,能与水以任意比互溶。
物理性质与化学性质
• 熔点为-114.1℃,沸点为78.3℃。
物理性质与化学性质
01
化学性质
02
03
04
具有醇的典型化学性质,如与 活泼金属反应、与羧酸发生酯
能源消耗
乙醇生产需要大量能源,如化石 燃料,其燃烧产生二氧化碳等温
室气体,加剧全球气候变化。
水资源消耗
生产过程中需要大量水资源,可 能导致水资源短缺和水污染问题
。
废气排放
发酵和蒸馏过程中产生的废气, 如二氧化碳、甲烷等,对大气环
境造成负面影响。
废弃物处理和资源回收利用方法探讨
废水处理
通过物理、化学或生物方法处理生产废水,降低有机物和悬浮物 含量,实现废水达标排放或回用。
实验操作步骤详解
建立健全环保法规和标准体系,加强生产 过程中的环保监管和执法力度,确保企业 达标排放。
推动循环经济
加强科技创新
鼓励企业开展循环经济实践,实现废弃物 资源化利用和能源梯级利用,降低生产过 程中的环境负荷。
乙醇PPT课件

(学生分组做乙醇与水反应比较实验)
2C2H5OH+2Na 2C2H5ONa+H2 现象:钠粒沉于无水酒精底部,钠块表面有气泡
产生.钠粒不熔成闪亮的小球,也不发出响声,反应 缓慢. 分析:乙醇分子中的羟基没有水分子中羟基活泼 反应实质:乙醇跟金属钠反应,钠置换羟基上的 H,生成乙醇钠,并放出氢气。 反应机理:氢氧共价键断裂
2、氧化反应:(一)
乙醇在空气里能够燃烧,发出 淡蓝色的火焰,同时放出大量的热。 C2H5 OH + 3 O2
点燃
2CO2 +3H2O+热
因此: 乙醇可用作内燃机的燃料,实验室里 也常用它作为燃料。
焊接银器、铜器时,表面会生成黑色的氧 化膜,银匠说,可以先把铜、银在火上烧热, 马上蘸一下酒精,铜银会光亮如初。这是什么 原理呢?
C—C—H
H O—H
启迪思考: 当--C上没有 氢或只有一个氢的情况又如 何氧化呢?
-C上氢原子数目与醇的氧化的关系
参考:与-OH相连的碳原子必须有H才能
被氧化。 H H H两个氢脱去与O结合源自水C—C—HH O—H
①在--C碳上有2个H时
RCH H Cu O RCH=O 0 ~300 C 生成醛 H
CH3CH2OH
五、乙醇的用途
乙 醇
溶 剂 燃料 化工原料
生活中两种常见的有机物---第一课时 乙醇
王向阳
一、乙 醇 结 构
化学式: C2H6O H 结构式: H H
C —C—O—H
乙醇分子的比例模型
H H CH3CH2OH 结构简式: 或C2H5OH
醇的官能团--羟基 写作-OH
二、物 理 性 质
乙醇俗称 颜 色 : 气 味 : 状 态 : 密 度 : 溶解性 : 酒精 无色透明 特殊香味 液体 比水小 跟水以任意比互溶 能够溶解多种无机物和有机物 易挥发
2C2H5OH+2Na 2C2H5ONa+H2 现象:钠粒沉于无水酒精底部,钠块表面有气泡
产生.钠粒不熔成闪亮的小球,也不发出响声,反应 缓慢. 分析:乙醇分子中的羟基没有水分子中羟基活泼 反应实质:乙醇跟金属钠反应,钠置换羟基上的 H,生成乙醇钠,并放出氢气。 反应机理:氢氧共价键断裂
2、氧化反应:(一)
乙醇在空气里能够燃烧,发出 淡蓝色的火焰,同时放出大量的热。 C2H5 OH + 3 O2
点燃
2CO2 +3H2O+热
因此: 乙醇可用作内燃机的燃料,实验室里 也常用它作为燃料。
焊接银器、铜器时,表面会生成黑色的氧 化膜,银匠说,可以先把铜、银在火上烧热, 马上蘸一下酒精,铜银会光亮如初。这是什么 原理呢?
C—C—H
H O—H
启迪思考: 当--C上没有 氢或只有一个氢的情况又如 何氧化呢?
-C上氢原子数目与醇的氧化的关系
参考:与-OH相连的碳原子必须有H才能
被氧化。 H H H两个氢脱去与O结合源自水C—C—HH O—H
①在--C碳上有2个H时
RCH H Cu O RCH=O 0 ~300 C 生成醛 H
CH3CH2OH
五、乙醇的用途
乙 醇
溶 剂 燃料 化工原料
生活中两种常见的有机物---第一课时 乙醇
王向阳
一、乙 醇 结 构
化学式: C2H6O H 结构式: H H
C —C—O—H
乙醇分子的比例模型
H H CH3CH2OH 结构简式: 或C2H5OH
醇的官能团--羟基 写作-OH
二、物 理 性 质
乙醇俗称 颜 色 : 气 味 : 状 态 : 密 度 : 溶解性 : 酒精 无色透明 特殊香味 液体 比水小 跟水以任意比互溶 能够溶解多种无机物和有机物 易挥发
人教版必修二乙醇优秀ppt课件

练 2.比较乙烷和乙醇的结构,下列说法错误的是( ) A.两个碳原子以单键相连
√B.分子里都含 6 个相同的氢原子
C.乙基与一个氢原子相连就是乙烷分子 D.乙基与一个羟基相连就是乙醇分子
人教版必修二3乙.3醇.1优乙秀醇ppt(课共件27张PPT)
人教版必修二3乙.3醇.1优乙秀醇ppt(课共件27张PPT)
人教版必修二3.3.1乙醇 (共27张PPT)
人教版必修二3.3.1乙醇 (共27张PPT)
思考:
(1)如何检验酒精是否含水? 取少量酒精,加入无水硫酸铜,若出现蓝 色,则证明酒精含水。
(2)如何由工业酒精制取无水酒精?
用工业酒精与新制生石灰混合蒸馏, 可得无水酒精。
人教版必修二3.3.1乙醇 (共27张PPT)
HH H C—C—H
HH
乙醇分子可以看作是乙 烷分子里的一个氢原子 被羟基所取代的产物。
HH
烃分子中的H原子被其他
原子或原子团所取代而生 H C—C—O—H 成的一系列化合物称为
HH
烃的衍生物。
人教版必修二3乙.3醇.1优乙秀醇ppt(课共件27张PPT)
人教版必修二3乙.3醇.1优乙秀醇ppt(课共件27张PPT)
2CH3CH2OH + Mg
人教版必修二3乙.3醇.1优乙秀醇ppt(课共件27张PPT)
(CH3CH2O)2Mg + H2↑
乙醇镁
人教版必修二3乙.3醇.1优乙秀醇ppt(课共件27张PPT)
【对比思考】
结论1.乙醇与钠发生反应断_O__-H__(C-H/O-H ), 说明O-H比C-H更加 活泼 。(活泼/不活泼)
四、用途
❖ 用作燃料,如酒精灯、汽车等。
❖ 用于制造饮料和香精。 ❖ 是一种重要的有机化工原料,如制造
√B.分子里都含 6 个相同的氢原子
C.乙基与一个氢原子相连就是乙烷分子 D.乙基与一个羟基相连就是乙醇分子
人教版必修二3乙.3醇.1优乙秀醇ppt(课共件27张PPT)
人教版必修二3乙.3醇.1优乙秀醇ppt(课共件27张PPT)
人教版必修二3.3.1乙醇 (共27张PPT)
人教版必修二3.3.1乙醇 (共27张PPT)
思考:
(1)如何检验酒精是否含水? 取少量酒精,加入无水硫酸铜,若出现蓝 色,则证明酒精含水。
(2)如何由工业酒精制取无水酒精?
用工业酒精与新制生石灰混合蒸馏, 可得无水酒精。
人教版必修二3.3.1乙醇 (共27张PPT)
HH H C—C—H
HH
乙醇分子可以看作是乙 烷分子里的一个氢原子 被羟基所取代的产物。
HH
烃分子中的H原子被其他
原子或原子团所取代而生 H C—C—O—H 成的一系列化合物称为
HH
烃的衍生物。
人教版必修二3乙.3醇.1优乙秀醇ppt(课共件27张PPT)
人教版必修二3乙.3醇.1优乙秀醇ppt(课共件27张PPT)
2CH3CH2OH + Mg
人教版必修二3乙.3醇.1优乙秀醇ppt(课共件27张PPT)
(CH3CH2O)2Mg + H2↑
乙醇镁
人教版必修二3乙.3醇.1优乙秀醇ppt(课共件27张PPT)
【对比思考】
结论1.乙醇与钠发生反应断_O__-H__(C-H/O-H ), 说明O-H比C-H更加 活泼 。(活泼/不活泼)
四、用途
❖ 用作燃料,如酒精灯、汽车等。
❖ 用于制造饮料和香精。 ❖ 是一种重要的有机化工原料,如制造
乙醇ppt课件

工业酒精:95%
医用酒精:75%
固体酒精燃料
乙醇汽油
针对训练
1、酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原
理是橙色的酸性K2Cr2O7水溶液遇乙醇迅速生成绿色的Cr3+。下列对乙醇的描述
C 与此测定原理有关的是( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧衍生物
A.②④ B.②③ C.①③
D.①④
针对训练
2、乙醇分子中不同的化学键如下图,下列关于乙醇在各种反应中断裂键的说
法不正确的是( D )
A.乙醇和钠反应,键①断裂 B.在Ag催化下和O2反应,键①③断裂 C.在Cu催化下和O2反应,键④⑤不可能断裂 D.乙醇是电解质,在水中键①断裂能电离出氢离子
针对训练
1、下列物质不属于烃的衍生物的是( D )
A.
B.CH3CH2OH
针对练习
C.
D.CH2=CH2
2、比较乙烷和乙醇的结构,下列说法错误的是( B )
A.两个碳原子以单键相连 B.分子里都含6种相同的氢原子 C.乙基与一个氢原子相连就是乙烷分子 D.乙基与一个羟基相连就是乙醇分子
三、乙醇的化学性质
1、乙醇与金属钠反应 (1)实验现象
(3)实验结论
密度: 水>钠>乙醇 . 剧烈程度: 钠与水反应比与乙醇反应更剧烈 . 乙醇与钠反应生成 H2 。
实验探究
三、乙醇的化学性质
深度解析
1、乙醇与金属钠反应
置换反应
①
HH
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑ H—C —C—O—H
乙醇钠
HH
2Na+2HOH=2NaOH+H2 ↑
PPT乙醇说播课优质课精品课件

宏观现象
微观本质
符号表征
五.教学过程 ——环节三掌握乙醇催化氧化反应
血液中酒精
浓度%
症乙
状
发生肇事
0.05
醇 精神愉快在,开始兴奋
有可能
人
知 识 线
0.10 0.20
失去控制,说体话含糊,走路不稳 内
动作不协的调,意识紊乱 代
增加 一定
0.40
麻醉状态谢,进入昏迷
一定
过
程
五.教学过程 ——环节三掌握乙醇催化氧化反应
➢宏观辨识与微观探析素养
通过实验探究,掌握乙醇的化学性质,
会书写乙醇相关的化学反应方程式,发 展学生宏观辨识与微观探析核心素养;
➢模型认知与证据推理素养
2
➢社会责任素养
掌握乙醇分子的结构, 1 发展模型认知与证据 推理核心素养;
3 感受乙醇的用途, 学会从化学的视角 认识生活,具备一 定的科学态度和社
K2Cr2O7
乙醇
(橙红色)
H+
Cr3+
(绿色)
知
滴加乙醇
识
线
2K2Cr2O7+3CH3CH2OH+8H2SO4→2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O
五.教学过程 ——环节四了解乙醇与强氧化剂反应
设计意图
素
这一体验性活
养
动让学生感受
线
化学与社会生
活的密切联系
。
五.教学过程 ——环节五感受乙醇的用途
环节一
教学 环节
情景线 活动线
乙醇与生 活的联系
观察 闻气味 涂抹
知识线
乙醇的物 理性质
乙醇公开课ppt课件

使用过程中安全问题及注意事项
远离火源和热源
乙醇易燃,使用时应远离火源和 热源,避免引发火灾和爆炸事故
。
防止静电
在乙醇的运输和使用过程中,应采 取防静电措施,如使用导电性良好 的容器和管道,避免静电积聚引发 火灾。
注意通风
在使用乙醇的场所,应保持良好的 通风,避免乙醇蒸气积聚引发中毒 和火灾事故。
废弃物处理与环保要求
主要生产国家及地区
美国、巴西、中国等是全球主要的乙 醇生产国家,其中美国和巴西以玉米 和甘蔗为原料生产乙醇,中国则主要 以粮食和木薯为原料。
产业发展特点
全球乙醇产业在技术创新、原料多元 化、市场拓展等方面取得显著进展, 生物燃料乙醇和化工乙醇成为发展重 点。
中国乙醇产业发展现状及挑战
中国乙醇产量及消费情况
废弃物分类
将乙醇废弃物与其他废弃物分类 收集,避免对环境造成污染。
回收利用
对于可回收利用的乙醇废弃物, 应进行回收处理,减少资源浪费
。
无害化处理
对于无法回收利用的乙醇废弃物 ,应进行无害化处理,如通过焚 烧或生物降解等方式,避免对环
境造成危害。
06
实验操作演示与互动环节
实验目的和原理介绍
01
实验目的
03
乙醇应用领域拓展
能源领域:生物柴油、燃料乙醇等
01
生物柴油
利用乙醇与脂肪酸或脂肪酸酯 进行酯交换反应,生成生物柴 油,具有可再生、环保等优点
。
02
燃料乙醇
将乙醇与汽油按一定比例混合 ,形成燃料乙醇,可有效降低 汽车尾气排放,改善空气质量
。
03
乙醇燃料电池
直接将乙醇转化为电能,具有 高效、清洁、可再生等特点, 是未来能源领域的研究热点。
乙醇 (最新课件ppt)
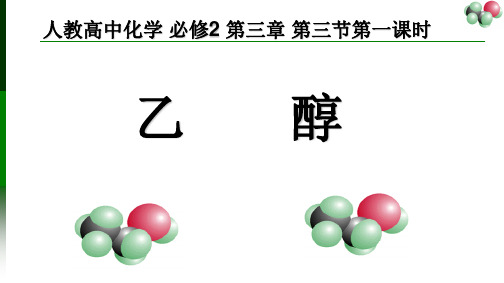
乙醇分子结构探究 1:你认为乙醇的结构式是哪种? 2:请小组交流,设计实验方案,探究 乙醇可能具有的结构式。
1. H2O(H-O-H) Na NaOH + H2↑
2. C 2H6O Na
乙醇分子结构探究
实验3-2 1:用装有钠块的注射器在试剂瓶中抽取约20ml无水乙 醇; 2:针头竖直向下,液体自然流入小烧杯; 3:待液体流尽,倒转注射器,轻轻推动活塞,点燃火 柴靠近针头。
乙醇分子结构探究
钠与水
钠与乙醇
反应现象 实验结论
浮熔游响
钠沉在针筒底部 反应比较缓慢
有气泡产生
钠的密度比水小,比乙醇大, 钠与乙醇的反应不如与水反应剧烈
2C2H5OH + 2Na → 2C2H5ONa+ H2↑ 羟基中的H原子的活泼性:醇<水
乙醇的燃烧反应
点燃
C2H5#43; 3H2O
加入乙醇
重铬酸钾 酸性溶 液
加入乙醇
高锰酸钾 酸性溶液
乙醇的用途
课堂练习
乙醇分子中不同的化学键,如右图:关于乙醇在各种反应 中断裂键的说法不正确的是( ) A.乙醇和钠反应,键①断裂 B.乙醇完全燃烧时键①②断裂 C.在铜催化下和O2反应,键①③断裂 D.在铜催化下和O2反应,键①②断裂
学以致用
乙醇的催化氧化微观分析
氢原子
水
乙醛
乙醇 HH H—C—C—O
-----
HH
-----
碳原子 H
氧原子
HH H—C—C—O
H
乙醇的催化氧化符号表征
2Cu + O2 △ 2CuO
CH3CH2OH + CuO
CH3CHO + Cu +H2O
新课标人教版化学必修2乙醇课件ppt

现象:
铜丝
Δ
①
插入乙醇 溶液中 ②
相关方程式:①:
。
②:
。
将上述①、②方程式叠加的总反应式为:
铜丝的作用:
病原体侵入机体,消弱机体防御机能 ,破坏 机体内 环境的 相对稳 定性, 且在一 定部位 生长繁 殖,引 起不同 程度的 病理生 理过程
醇催化氧化机理探究:
已知:连接-OH的碳原子上必须有H,才能发生 催化氧化
用工业酒精与新制生石灰混合蒸 馏,可得无水酒精。
想 一 想?
⑵ 如何检验酒精是否含水?
取少量酒精,向其中加入 无水硫酸铜,若无水硫酸 铜由白色变蓝色,则说明酒精中含有水,反之 则不含水 .
病原体侵入机体,消弱机体防御机能 ,破坏 机体内 环境的 相对稳 定性, 且在一 定部位 生长繁 殖,引 起不同 程度的 病理生 理过程
2CH3-C-O-H + O2 Cu / Ag 不能发生催化氧
CH3
化
病原体侵入机体,消弱机体防御机能 ,破坏 机体内 环境的 相对稳 定性, 且在一 定部位 生长繁 殖,引 起不同 程度的 病理生 理过程
醇催化氧化规律
a.-OH连接碳原子上有两个H原子,则该醇 被氧化生成醛
b.-OH连接碳原子上有一个H原子, 则该醇氧化生成酮
HH H C—C—O—H
④ H③H ② ①
①与金属Na的取代反应 ①
②氧化反应--燃烧 全部
--催化氧化 ① ③
*
---乙醇被重铬酸钾氧化
(用于酒驾检测)
HH
HH
H C—C—H
H C—C—O—H
HH
HH
烃的衍生物:烃分子中的氢原子
被其他原子或原子团所取代而生成的一
化学课件《乙醇》优秀ppt33(8份打包) 鲁科版

87.当一切毫无希望时,我看着切石工人在他的石头上,敲击了上百次,而不见任何裂痕出现。但在第一百零一次时,石头被劈成两半。我体会到,并非那一击,而是前面的敲打使它裂开。――[贾柯·瑞斯] 88.每个意念都是一场祈祷。――[詹姆士·雷德非]
89.虚荣心很难说是一种恶行,然而一切恶行都围绕虚荣心而生,都不过是满足虚荣心的手段。――[柏格森] 90.习惯正一天天地把我们的生命变成某种定型的化石,我们的心灵正在失去自由,成为平静而没有激情的时间之流的奴隶。――[托尔斯泰]
2CH3CH2OH+Mg→(CH3CH2O)2Mg+H2↑
④.此反应可检验-OH的存在,可计算分子中 -OH数目
牛刀小试
16g某一元醇与足量的金属钠完全反应,在标
准状况下得到5.6L氢气。该物质可能 A
A.CH3OH B.C2H5OH C.C3H7OH D.C4H9OH
思考 : O—H键最易断裂,那么C—H键和C—O键能否断 裂呢?
2、乙醇的氧化反应 点燃
(1)燃烧 CH3CH2OH+3O2 2 CO2+3 H2O 现象:淡蓝色火焰,放出大量的热。
H2、CO、CH4、乙醇、硫 思考 : 1mol乙醇的耗氧量和哪种烃是一样的?
例:在常压和100oC条件下,把乙醇汽化为蒸 气,然后和乙烯以任意比例混合,混合气体的 体积为VL。将其完全燃烧,需消耗相同条件
91.要及时把握梦想,因为梦想一死,生命就如一只羽翼受创的小鸟,无法飞翔。――[兰斯顿·休斯] 92.生活的艺术较像角力的艺术,而较不像跳舞的艺术;最重要的是:站稳脚步,为无法预见的攻击做准备。――[玛科斯·奥雷利阿斯] 93.在安详静谧的大自然里,确实还有些使人烦恼.怀疑.感到压迫的事。请你看看蔚蓝的天空和闪烁的星星吧!你的心将会平静下来。[约翰·纳森·爱德瓦兹]
89.虚荣心很难说是一种恶行,然而一切恶行都围绕虚荣心而生,都不过是满足虚荣心的手段。――[柏格森] 90.习惯正一天天地把我们的生命变成某种定型的化石,我们的心灵正在失去自由,成为平静而没有激情的时间之流的奴隶。――[托尔斯泰]
2CH3CH2OH+Mg→(CH3CH2O)2Mg+H2↑
④.此反应可检验-OH的存在,可计算分子中 -OH数目
牛刀小试
16g某一元醇与足量的金属钠完全反应,在标
准状况下得到5.6L氢气。该物质可能 A
A.CH3OH B.C2H5OH C.C3H7OH D.C4H9OH
思考 : O—H键最易断裂,那么C—H键和C—O键能否断 裂呢?
2、乙醇的氧化反应 点燃
(1)燃烧 CH3CH2OH+3O2 2 CO2+3 H2O 现象:淡蓝色火焰,放出大量的热。
H2、CO、CH4、乙醇、硫 思考 : 1mol乙醇的耗氧量和哪种烃是一样的?
例:在常压和100oC条件下,把乙醇汽化为蒸 气,然后和乙烯以任意比例混合,混合气体的 体积为VL。将其完全燃烧,需消耗相同条件
91.要及时把握梦想,因为梦想一死,生命就如一只羽翼受创的小鸟,无法飞翔。――[兰斯顿·休斯] 92.生活的艺术较像角力的艺术,而较不像跳舞的艺术;最重要的是:站稳脚步,为无法预见的攻击做准备。――[玛科斯·奥雷利阿斯] 93.在安详静谧的大自然里,确实还有些使人烦恼.怀疑.感到压迫的事。请你看看蔚蓝的天空和闪烁的星星吧!你的心将会平静下来。[约翰·纳森·爱德瓦兹]
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
铜丝
△
2Cu + O2
2CuO
变黑
C2H5OH+CuO
Δ
CH3CH+OCu +H2O
又变红 总反应方程式:
乙醛
产生刺
激性气 2CH3CH2OH + O2 Cu 2CH3CHO + 2H2O
味
(3)被酸性KMnO4 、K2Cr2O7 溶液氧化为乙酸
O=
[随堂检测] 1:下列反应可以用来检验司机是否酒后驾车
乙醇课件优秀 课件
中国的酒文化博大精深,源远 流长!
关于酒的诗词名句有很多,同 学们知道哪些?说说看。
明月几时有, 把酒 问青天。(苏轼)
借问中国酒家的何酒处文有流化,牧长博童!大遥精指杏深花,村源(远杜牧)
葡萄美酒夜光杯,欲饮琵琶马上催。(王翰 )
关于酒的诗词名句有很多,同 花间学一们壶知酒道,哪独些酌?无说相说亲。看(。李白)
乙醇与钠反应也产生氢气,
说明乙醇分子中有类似于水的结构,
有O-H键
HH H-C-C-O-H
HH
乙醇的结构
分子式: C2H6O 烃的衍生物
结构式:H--HC--CH-OH
--
HH
结构简式: CH3CH2OH
或C2H5OH
醇的官能团-羟 基(-OH)
乙醇分子可以看作是乙烷 分子里的一个氢原子被羟 基所取代的产物
白日放歌需 纵酒 ,青春作伴好还乡。(杜甫)
对酒 当歌,人生几何? 何以解忧? 唯有 杜康 。(曹操)
请大家,从颜
色、气味、状态、 水溶性等方面观 察总结说说乙醇 的物理性质。
一、乙醇的物理性质
颜 色:无色透明
气 味:特殊香味 状 态:液体 密 度:比水小
200C时的密度是0.7893g/cm3 挥发性:沸点78℃,易挥发 溶解性:和水可以以任意比互溶
(三) 乙醇的化学性质
1、乙醇与钠的反应
①
HH H—C —C—O—H , ①处O—H
键断开
HH
2 CH3CH2OH +2 Na →2CH3CH2ONa + H2↑
[练习]其它活泼金属如钾、镁和铝等也可与乙醇反
应,均可产生H2 ,请写出镁与乙醇反应的化学方程式。
2CH3CH2OH + Mg
(CH3CH2O)2Mg + H2↑
2K2Cr2O7 + 3CH3CH2OH + 8H2SO4
橙红色
2Cr2(SO4)3 + 3CH3-C-OH + 2K2SO4 + 11H2O
蓝绿色
上述反应中,被检测的气体是(CH3CH2OH ),
氧化剂是___K_2_C_r_2O__7 ____;氧化产物是_C_H_3_C_O_O_H_.
交警判断驾驶员是否酒后驾车的方法
1. A. CH3CH2OH B. CH3CH2CH2OH
பைடு நூலகம்
2. C. CH3OH
D. CH3-O-CH3
杜绝酒驾
K2Cr2O7 乙醇 Cr2(SO4)3
(橙红色)
(绿色)
2.下列有关乙醇的物理性质的应用中不正确的是( A )
A.由于乙醇的密度比水小,所以乙醇中的水可以通过 分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用 乙醇提取中药的有效成分
C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾 兑各种浓度的酒
5、比较乙烷和乙醇的结构,下列说法错误的是( B ) A.两个碳原子都以单键相连 B.分子里都含有6个完全相同的氢原子 C. 乙醇可以看成是乙烷分子中的一个氢原子被羟基 取代后的产物
D.乙醇与钠反应非常平缓,所以乙醇羟基上 的氢原子不如水中的氢原子活泼
6、某有机物6g 与足量钠反应生成 0.05molH2,该 有机物可能是( B )
能够溶解多种无机物和有机物
二、乙醇的分子结构
问题探究实:验测定乙醇的分子式为 C2H6O ,已知 该分子是由2个-C-,︱1个-O-,6个-H拼接而
︱
成,请问你能想出几种拼接方式?
A
B
HH
H—C—C—O—H
HH
思考:如何证明乙醇的分子结构究竟是 前者还是后者?
[实验3-2]乙醇与金属钠的反应
现象: 试管中有气体生成,可以燃烧, 烧杯内壁出现水滴,石灰水不变浑浊.
乙醇镁
2.氧化反应 (1)、燃烧 (彻底氧化)
点燃
C2H5OH +3O2 → 2CO2+3H2O
(2)乙醇的催化氧化
实验3-3把灼热的铜丝 插入乙醇中,观察铜丝 颜色变化,并小心闻试
管中液体产生的气味。
铜丝 Δ
变黑
插入乙醇 溶液中
又变红 有刺激性气味
(2)乙醇的催化氧化
实验现象:红热的铜丝,移离火焰变黑,迅速伸 入乙醇中,铜丝由黑变红,同时产生刺激性气味。
D.由于乙醇容易挥发,所以才有熟语“酒香不怕巷子 深”的说法
3:与钠反应时在何处断键( A )
HH
A: ① B: ② C: ③ D: ④
H
④
C—C—O—H
H
③
H②
①
4、将等质量的铜片在酒精灯上加热后,分别插
入下列溶液中,放置片刻,铜片质量增加的是( c)
A.硝酸 B.无水乙醇 C.石灰水 D.盐酸
