抗肾小球基底膜(GBM)病
抗肾小球基底膜病

临床表现
由于肺泡和肾小球的基底膜具有共同的抗原,且Ⅳ型 胶原的含量最为丰富,因此该病主要的受累脏器是肾 脏和肺。 肺、肾同时受累,称为Goodpasture综合征,也可以 各自单独受累,全身多系统受累不多见。 20%-60%的患者发病前可有上感或流感症状。 病程中可有乏力、消瘦等全身表现,但认为与贫血及 尿毒症有关,无特异性。 合并ANCA阳性的患者可以有小血管炎多系、吸烟以及其他的一些 因素均可使肺泡毛细血管壁受损,肺泡基底膜成分暴 漏或抗原释放,从而导致自身免疫反应,产生抗肺泡 基底膜抗体并与GBM有交叉反映,从而引起肾小球肾 炎和肺出血。 同样,在肾脏,尿路感染、肾结石、原有肾小球肾炎 等因素也可以使GBM抗原暴漏,诱导自身免疫反应, 并通过交叉反应引起肾小球肾炎和肺出血。
12
病因
有报道抗GBM病可以发生在多种肾小球肾炎的基础上 ,如典型的膜性肾病、IgA肾病、膜增生型肾炎、过敏 性紫癜性肾炎、膜性乙肝病毒相关性肾炎,但抗GBM 病产生的确切机制还有待于进一步研究。
13
遗传易感性
抗GBM病的遗传易感性与HLA-DR2密切相关,约 80%的患者HLA-DR2阳性。 有待进一步研究······ 因Alport遗传性肾炎的患者可先天缺乏GBM的抗原成 分,因此接受正常人肾移植的患者中有5%-10%会产 生抗GBM抗体而诱发抗GBM病。
7
背景知识
这一经典的被动转移试验证实了这种“肾毒性”抗体 (抗GBM抗体)是特异性针对GBM的,且在发病过程 中起着重要作用。 此后的研究进一步证实从肾组织中洗脱的抗体与同一 病人循环中的抗体所识别GBM上的抗原决定簇是相同 的。 因此,现在将这类疾病统称为抗GBM病,其肾脏损害 称为抗GBM肾小球肾炎。
14
抗肾小球基底膜疾病1

抗GBM抗体检测几乎阳性,对本病诊断有重要 价值,其滴度高低与病情严重及预后相关。
ANCA阳性为30%左右,多为P-ANCA。 其他血清学 补体一般正常,贫血,ESR、C反应 蛋白增高。
肾病实验室检查 肾功能短期内进行性恶化,尿 检示血尿,蛋白尿。 肺部相关检查 胸片可见弥漫或局限性由肺门
向肺野扩散的肺泡浸润影。慢性出血者痰液可见 含铁血红素细胞。支气管镜肺泡灌洗液可灌洗出 血性液体。
抗肾小球基底膜病(glomerular baseme膜病(glomerular basement membrane,GBM)是指循环中的抗肾小
球基底膜抗体在脏器中沉积所引起的一 组自身免疫性疾病。
该病最早见于1919年Ernest Goodpasture 对流感疫情流行中1例青年男性患者尸检 的报道。1958年Stanton和Tang报告了9例
GBM肾小球肾炎。
典型表现为急进性肾炎综合征伴或不伴肺出血
全身症状 起病前有流感样前驱症状,全身乏力, 不适,肌痛,关节痛,发热等。
肾脏损害 起病急骤,表现为急进性肾炎综合征, 短时间内出现水肿、少尿、肾功能进行性恶化, 尿液检查血尿,蛋白尿,肾病综合征少见。
肺损害 约2/3有肺出血,表现为咳嗽、痰中带 血或血丝,也可为大咯血
透析治疗及肾移植:急性肾功能衰竭符合透析指 征时及时透析,晚期予维持透析或肾移植。
早期未经治疗的病例中90%的患者进入 终末期肾功能衰竭或死亡。
经血浆置换及甲强龙、CTX治疗,约一半患 者预后明显改善经治疗。
一旦抗GBM病达到缓解,几乎不复发。
谢谢!
出现肺出血和肾炎的病例,并将其命名 为 Goodpasture综合征。其后发现部分病
人不发生肺出血而仅有肾炎表现,由于 均出现抗GBM抗体,因此统称为抗GBM 抗体相关疾病。
非典型肾炎

非典型肾炎医脉通导读非典型抗肾小球基底膜肾炎的临床病理特点总结,一起来了解一下吧!典型抗肾小球基底膜(GBM)病的临床表现为:急进性肾小球肾炎(GN)伴或不伴肺出血。
病理特点为:免疫荧光检查可见IgG 沿GBM多形线性沉积;光镜检查可见弥漫性新月体/坏死性GN。
《Kidney International》期刊发表的一篇综述对20例非典型抗肾小球基底膜肾炎患者的临床病理特点和预后进行了系统性总结,主要内容如下:病理特点光镜毛细血管内增生性肾小球肾炎(EPGN)(图1a,b)是最常见的肾损伤类型(共9例患者),其特点为毛细血管内细胞增多、白细胞浸润导致管腔堵塞。
3例患者(15%)表现为膜增生性肾小球肾炎(MPGN)(图 1b, 2a),其特点为肾小球基底膜弥漫性细胞增生。
6例患者(30%)表现为系膜增生性肾小球肾炎(MesPGN),其特点为系膜增生不伴毛细血管内细胞增生。
2例患者表现为肾病综合征,可见局灶性节段性肾小球硬化(FSGS)。
图1 毛细血管内增生性肾小球肾炎伴单形性IgG肾活检结果。
光镜:肾小球毛细血管内细胞增生伴单核细胞浸润,周围毛细血管堵塞(a,b)。
肾小球基底膜轮廓正常。
轻度间质性炎症 (a PAS染色,放大倍数 _200;b三色染色,放大倍数_400)。
电镜:肾小球周围毛细血管变窄,(c,d)。
肾小球基底膜轻度增厚伴阶段性缺血性褶皱。
未见电子致密物沉积(c 放大倍数_4000;d 放大倍数_10,000)。
免疫荧光:肾小球基底膜和少数远端小管IgG,lambda线性亮染(e)(左上放大倍数 _200,右上,左下,右下放大倍数_400)。
电镜20例患者均未见肾小球毛细血管壁电子致密物沉积(图1c和2c)。
14例患者(70%)未见肾小球电子致密物沉积。
其余的6例患者(35%)中有 3例患者可见少量系膜和/或内皮下电子致密物沉积,1例患者可见大量上皮下电子致密物沉积,1例患者可见大量膜内电子致密物沉积。
肾小球基底膜变薄和薄基底膜肾病.

肾小球基底膜变薄和薄基底膜肾病近年来,随着电镜和形态计量学检查在肾脏病理诊断中的应用,发现肾小球基底膜(glomerular basement membrane, GBM)变薄是部分无症状性血尿的唯一或主要病理改变,并提出了薄基底膜肾病(thin basement membrane nephropathy, TBMN)这一新的诊断名词。
随后发现GBM变薄尚可见于多种疾病,现就此方面的有关进展简述如下。
(一)GBM厚度的变异由于完全正常的肾组织来源困难,故通常以尸体肾、移植供肾以确定正常的GBM厚度[1]。
文献所报告的正常GBM厚度差异较大,除因肾组织来源不同外,尚与下列因素有关: 1.年龄及性别[1,2]:正常人出生时GBM厚度约为100 nm,2岁以内增厚较快,9岁以后则缓慢增厚,40岁左右达高峰。
儿童各年龄阶段GBM厚度范围(均值)如下:1~3岁100~340(220) nm,~5岁130~380(260) nm,~7岁160~410(280) nm,~9岁180~430(300) nm,~12岁190~440(310) nm。
男性GBM厚度显著厚于女性,成年男性GBM厚度为342~494 nm,女性为315~448 nm。
2.测量方法:GBM厚度在同一肾组织的不同肾小球之间、同一肾小球的不同毛细血管袢之间可存在一定的差异[3~5],前者称为球间变异,后者称为球内变异。
因此,应测定2~3个肾小球的多个血管袢的GBM厚度,求出均值以保证可靠。
测定GBM厚度的方法目前有算术均数(arithmetic mean)和调和均数(harmonic mean)法二种。
算术均数法需选择适宜测量的GBM节段:同时见到内皮细胞窗孔紧贴GBM内层呈线状分布和上皮细胞足突间隙,此目的是为避开正切面(tangential cuts),以减少因切片与GBM间角度的变异而造成GBM增宽的假象,Dische[1]认为这就增加了主观因素。
抗肾小球基底膜抗体合并抗中性粒细胞胞浆抗体阳性肺出血-肾炎综合征1例

1 病例介绍
患者,女,75 岁,因“咳嗽伴发热 7 天”入住肺病科,入院症见: 咳 嗽,痰 难 咳,活 动 后 易 胸 闷 心 慌,周 身 乏 力,24 小 时 尿 量 400500 mL,既 往 高 血 压 病 史 5 年,冠 心 病 病 史 5 年,口 服 药 物 控 制 可。 查 体:T、P、R 在 正 常 范 围 内,BP130-150/70-80 mmHg,双 肺 呼 吸 音 粗 ,双 肺 底 可 闻 及 少 量 湿 性 啰 音 ,双 下 肢 轻 度 水 肿 。 入 院后查 Scr150 umol/L,Bun9.0 mmol/L,Alb32.5 g/L,Hb91 g/L, 中 性 比 81%,血 沉 85 mm/h,尿 蛋 白 1+,潜 血 3+。 遂 转 入 肾 病 科,予 以 抗 炎、保 肾、降 肌 酐 治 疗。 一 周 后 复 查 Scr408 umol/L, Alb24.6 g/L,CO2 结 合 力 10.2 mmol/L,CRP177,PTH99 pg/mL, ANA 谱(-),MPO3+,抗 GBM 抗体 3+,89 Ru/mL,ANCA 阳性;胸 部 CT:双下肺间质性改变,双侧胸腔积液,少量腹水,胆结石;心脏 彩超:EF58%,左房增大。诊断为:急性肾损伤,ANCA 相关性肾 炎,抗肾小球基底膜抗体病。治疗方案:甲强龙 250 mg/d 冲击 3d 后改为 40 mg/d,血浆置换、床旁血透连续 3d 后改为隔日一次,辅 以抗感染、抗凝、抗血小板双抗等对症治疗。血浆置换 3 次后复 查抗 GBM 抗体 3+。患者于第 4 次血浆置换后突发阵发性房颤, 均逐渐恢复窦性心律,急查 cTnI7.65 ng/mL,NT-proBNP8587,D二聚体 15.59 ug/mL,Scr420 umol/L,复查胸部 CT:双肺纹理增多 模糊,双肺弥漫性以肺门为中心的磨玻璃影,呈蝶翼征,双上肺见 小 叶 间 隔 增 厚 ,双 下 肺 实 变 ,双 肺 胸 膜 下 多 发 网 织 影 ,右 肺 稍 著 , 双侧大量胸腔积液征象,考虑双侧肺水肿并感染,肺出血不除外, 必要时强化除外肺栓塞。迅速予以抗感染、抗凝、抗心衰等治疗。 次日患者出现胸闷、憋喘,咳吐血性痰,双肺满布哮鸣音,心率 130 次 / 分,经面罩高流量吸氧及强心、利尿、扩血管治疗后稍有好转, 吸 出 大 量 血 性 痰,继 而 患 者 意 识 丧 失,血 氧 饱 和 度 持 续 下 降,呼 吸 、心 跳 骤 停 ,经 心 肺 复 苏 、药 物 复 苏 、气 管 插 管 呼 吸 机 辅 助 呼 吸 治疗后,患者恢复自主心律,但仍处于深度昏迷状态,吸痰均为血 性,需应用大量血管活性药物维持血压,病情凶险、预后极差。后 患者家属放弃治疗。
内科辅导:急进性肾小球肾炎常见病因及RPGN分型

2010年内科辅导:急进性肾小球肾炎常见病因及RPGN分型
急进性肾小球肾炎(RPGN)指在肾炎综合征(血尿、蛋白尿、水肿和高血压)基础上短期内出现少尿、无尿,肾功能急骤进展,短期内到达尿毒症的一组临床综合征。
本病的病理改变特征为肾小囊内细胞增生、纤维蛋白沉积,又名新月体性肾炎。
该病病情危重、预后差,但如能早期明确诊断并根据各种不同的病因及时采取正确的治疗,可明显改善患者的预后。
RPGN分为三种类型,具有不同的肾脏病理改变:
①Ⅰ型又称抗肾小球基底膜(GBM)抗体型,血中存在抗GBM抗体,免疫荧光为IgG及C3沿肾小球毛细血管壁呈线条样沉积,电镜下肾小球内无电子致密物沉积,约占RPGN中20%。
②Ⅱ型又称免疫复合物型,血中存在循环免疫复合物,免疫荧光为IgG及C3呈颗粒样沉积于系膜区和毛细血管壁,光镜下可见肾小球内皮细胞和系膜细胞增生,约占RPGN中40%。
③Ⅲ型在免疫荧光上为少或无免疫复合物型,而光镜下常可见肾小球节段性纤维素样坏死,80%患者血中存在抗中性粒细胞胞浆抗体(ANCA)阳性,该型约占RPGN中40%。
应注意RPGNI型中约30%可同时ANCA阳性。
我国ANCA阳性的RPGN中pANCA多于cANCA,其特异性靶抗原分别为髓过氧化物酶(MPO)和蛋白酶3(PR3),分别多见于显微镜下多动脉炎和韦格纳肉芽肿这两种血管炎。
急诊检测血清中抗GBM抗体和ANCA往往可以在肾活检之前明确诊断,对早期、及时明确诊断及治疗具有重要意义。
医学检验·检查项目:抗肾小球基底膜抗体测定(AGBM)_课件模板

医学检验·各论:抗肾小球基底膜抗体测定(AGBM) >>>
相关疾病:
慢性肾盂肾炎、急进性肾炎、间质性肾炎、 肺出血-肾炎综合征、急性肾炎、隐匿性 肾小球肾炎、紫癜性肾炎、IgA肾炎、膜 性肾小球肾炎、狼疮性肾炎。
谢谢!
临床意义:
阳性: 抗GBM抗体阳性病人占自身免 疫性肾炎的5%,在肾小球性肾炎、咳血综 合征患者中有80%的阳性检出率,半月体 形成性肾小球肾炎患者中有20%~70%的阳 性检出率,也可在增殖性肾炎中检出。
医学检验·各论:抗肾小球基底膜抗体测定(AGBM) >>>
正常值: 间接免疫荧光、间接血凝法:阴性
医学检验·各 内容课件模板
医学检验·各论:抗肾小球基底膜抗体测定(AGBM) >>>
简介:
抗肾小球基底膜抗体是由肾小球毛细 血管内外透明层及中间致密层构成的网状 结构,以糖蛋白为主体。
检测GBM抗体的最常用方法是以肾脏 组织为抗原的IIF法(间接免疫荧光法), 其荧光特点是在肾小球基底膜处显示典型 的花瓣状、或斑点状、颗粒状着染。IIF 法可出现假阳性结果。以胶原酶消化
医学检验·各论:抗肾小球基底膜抗体测定(AGBM) >>>
简介:
0min,使抗原抗体充分结合,然后洗涤, 除去未结合的抗体。
第二步,加上荧光标记的抗球蛋白抗 体或抗IgG、IgM抗体。如果第一步发生了 抗原抗体反应,标记的抗球蛋白抗体就会 和已结合抗原的抗体进一步结合,从而可 鉴定未知抗体。
医学检验·各论:抗肾小球基底膜抗体测定(AGBM) >>>
(或血清滴度<4)。
医学检验·各论:抗肾小球基底膜抗体测定(AGBM) >>>
膜性肾病介绍演示培训课件

抗凝治疗
对于存在高凝状态的患者,可给 予抗凝药物如华法林、低分子肝
素等预防血栓形成。
急性肾损伤处理
立即停用可能导致肾损伤的药物 ,给予肾脏替代治疗如血液透析 或腹膜透析等支持治疗,同时积
极寻找并去除病因。
05
患者教育与心理支持工作部署
提高患者对疾病认知度
疾病知识普及
通过讲座、宣传册、视频等多种形式,向患者普及膜性肾病的基 本知识,包括病因、症状、治疗方法及预后等。
年龄与性别分布
MN可发生于任何年龄,但以中老年 男性多见。
临床表现与分型
临床表现
MN患者常表现为肾病综合征,包括大量蛋白尿、低白蛋白血症、水肿和高脂血症。此外,患者还可能出现血尿 、高血压和肾功能损害等症状。
分型
根据病因和发病机制的不同,MN可分为原发性膜性肾病(Idiopathic Membranous Nephropathy,iMN)和 继发性膜性肾病(Secondary Membranous Nephropathy,sMN)。iMN是一种自身免疫性疾病,而sMN则 是由其他疾病或药物使用引起的继发性肾小球损伤。
重病情,影响治疗效果。
血栓栓塞
膜性肾病患者存在高凝状态,易发 生血栓栓塞,如肾静脉血栓、下肢 深静脉血栓等,严重者可危及生命 。
急性肾损伤
部分患者可因药物使用不当、感染 等因素导致急性肾损伤,表现为肾 功能急剧下降,需要及时干预。
预防措施建议
01
02
03
04
保持良好生活习惯
注意个人卫生,避免过度劳累 ,保持充足睡眠,适当锻炼增
免疫抑制剂
如糖皮质激素、环磷酰 胺等,用于抑制免疫反
应,减轻肾脏损伤。
降压药
血浆置换治疗有效的疾病

(1)抗肾小球基底膜病: 抗肾小球基底膜(抗一GBM)病就是一种循环 抗体直接攻击肾小球基底膜抗原,导致急进性肾小 球性肾炎得疾病,伴随肺出血时,就Goodpasture综 合征。抗一GBM抗体得靶抗原就是Ⅳ胶原α3链得 非胶原(NC)1区域。超过90%得患者都能检测到循 环中抗一GBM抗体,而且循环抗体得滴度与疾病得 活动度有关。
(2)寡免疫性急进性肾小球肾炎:也称急性型 进展性肾小球肾炎(rapidly progressive glomeruloneph—titis,RPGN),患者血浆常有抗 中性粒细胞胞浆抗体(antineutrophil cytoplasmic autoantibodv,ANCA)阳性得系统性 小血管炎。通过作用于中性粒细胞、内皮细胞以 及其她炎症机制,ANCA在RPGN得发病机制方面起重 要作用,ANCA滴度与疾病得活动性相关。血浆置换 最初被引入治疗就是由于其组织学改变与 Goodpasture综合征得相似性。
推荐对出现透析依赖性肾衰竭或肺出血得小 血管炎患者给予血浆置换治疗。使用白蛋白作为 置换液,除非有出血危险。第1周时,血浆置换至少 每天1次,持续4天。监测尿量、血清肌酐值和ANCA 滴度来判断疗效。对于那些ANCA阳性、存在IgM亚 型ANCA得患者,肺出血得风险特别高。如果这些抗 体就是致病性得,需进行离心式血浆置换,因为膜 式血浆置换在去除大相对分子质量、含IgM得免疫 复合物时相对无效。
目前已报道了7个关于血浆置换治疗非抗一 GBM急进性肾小球肾炎得试验(表11—10一15)。
大多数早期得试验包括多种疾病得患者,使 用得血浆置换强度低,而且往往剔除了少尿/无尿 得患者。这些试验表明血浆置换联合常规得免疫 抑制剂治疗并没有额外得益处,但对于病情严重得 患者似乎有益。结合对照试验得结果,接受血浆置 换治疗得42例透析依赖得患者中31例(72%)肾功能 恢复,而单用药物治疗得25例患者中仅8例(32%)肾 功能恢复。
抗肾小球基底膜(GBM)病

预防措施建议
保持室内空气流通,避免到人 群密集场所,减少感染机会。
严格控制饮食,遵循低盐、低 脂、优质蛋白质的饮食原则,
减轻肾脏负担。
定期监测血压、心电图等指标 ,及时发现并处理心血管并发 症。
遵医嘱按时服药,不得随意更 改治疗方案或停药。
处理方法及时机选择
肺部感染
一经发现应立即就医,根据感染类型选择合适的 抗生素进行治疗,同时加强呼吸道护理和营养支 持。
血浆置换等非药物治疗方法
血浆置换
通过血浆置换机将患者的血液引出体外,去除血浆中的抗GBM抗体和免疫复合 物,然后将处理后的血液回输给患者。该治疗方法可迅速清除体内的有害物质 ,减轻肾脏损害。
肾脏替代治疗
对于病情严重、肾功能急剧恶化的患者,可考虑进行肾脏替代治疗,如血液透 析或腹膜透析等。部分患者经过积极治疗,肾功能可逐渐恢复,甚至摆脱透析 治疗。
03
治疗原则与方案
一般治疗原则
早期诊断和治疗
对于疑似抗GBM病的患者,应尽 早进行肾活检和免疫学检查以明 确诊断,并尽早开始治疗,以改 善预后。
个体化治疗方案
根据患者的年龄、性别、病情严 重程度、合并症等因素,制定个 体化的治疗方案。
积极治疗并发症
抗GBM病常合并肺部感染、高血 压等并发症,需要积极治疗,以 改善患者的生活质量和预后。
发病机制涉及循环中的抗GBM抗体与 肾小球和肺泡基底膜中的Ⅳ型胶原结 合,激活补体并吸引中性粒细胞,导 致局部炎症反应和组织损伤。
流行病学特点
该病较为罕见,发病 率较低,但病情严重 ,预后较差。
多数患者为散发性病 例,少数有家族聚集 现象。
发病年龄以中青年为 主,男性略多于女性 。
临床表现及分型
膜性肾病合并肾功能轻度受损的抗肾小球基底膜病一例报道及文献复习

膜性肾病合并肾功能轻度受损的抗肾小球基底膜病一例报道及文献复习包红梅;张建春;陈晓明;郭文岗;王素霞;章友康【摘要】目的通过1例典型病例分析结合文献资料的复习探讨膜性肾病合并抗肾小球基底膜(glomerular basement membrane,GBM)病的临床表现、发病机制、治疗方法和预后.方法对本院收治的1例膜性肾病合并抗GBM病患者的病理特点和临床治疗进行回顾性分析,复习相关文献资料.结果本例患者青年男性,既往体健,有吸烟病史,感染20 d后出现肺出血、肉眼血尿、大量蛋白尿、低蛋白血症、浮肿、血肌酐轻度增高,抗GBM抗体阳性,肾脏病理为膜性肾病合并有抗GBM病伴有亚急性肾小管间质肾病.前期给予甲泼尼龙0.5 g/d,共4d,环磷酰胺0.4 g/d、0.6 g/d,连续2d冲击治疗后尿蛋白明显减少,肉眼血尿消失,但肾功能和血色素无改善,同时出现胸闷、气短,活动后加重等症状,胸片显示肺出血加重,经8次双重血浆置换、配合激素、环磷酰胺治疗后,抗GBM抗体转为阴性,肺出血完全控制,尿蛋白定量明显降低,肾功能正常.结论膜性肾病合并抗GB病较少见,临床容易误诊或漏诊,治疗不及时多预后不佳,尤其合并肺出血者病情变化快.对临床可疑者需尽早行抗GBM抗体或肾穿刺检查明确诊断.对伴有肺出血、肾功能轻度受损者经积极血浆置换和激素、环磷酰胺治疗可改善预后.%Objective The clinicalmanifestations,treatment methods,pathogenesis and prognosis of rare membranous nephropathy combined with anti glomerular basement membrane disease were discussed through 1 typical case analysis and literature review.Methods The pathological characteristics and clinical treatment of one cases of membranous nephropathy combined with anti glomerular basement membrane disease were retrospectivelyanalyzed,and the related literature was reviewed.Results The patients were young men and past physical health,smoking history,Twenty days after infection appeared pulmonary hemorrhage,gross hematuria,large proteinuria,hypoproteinemia,edema,blood creatinine slight increase,anti GBM antibody positive renal pathology as membranous nephropathy with anti GBM disease with sub acute tubular interstitial nephropathy.Pre given methylprednisolone 0.5 g/d.A total of four days,cyclophosphamide 0.4g/d,0.6 g/d,continuous two days after shock treatment urinary protein was significantly reduced,the naked eye hematuria disappeared,but renal function and hemoglobin no improvement,also appear chest tightness,shortness of breath,activities after aggravating symptoms such as chest radiograph shows pulmonary blood increased,urine protein significantly reduced by eight double plasma exchange,with the hormone,cyclophosphamide,anti GBM antibody turn negative and pulmonary hemorrhage in complete control and renal function normal.Conclusions Membranous nephropathy combined with anti GBM disease is rare,clinical easy to misdiagnosis or missed diagnosis,treatment is not timely prognosis is not good,especially with the rapid change of the patient's condition.The diagnosis of clinical suspected as early as possible to anti GBM antibody or renal biopsy.The prognosis of patients with pulmonary hemorrhage,mild impairment of renal function by positive plasma exchange and hormone and cyclophosphamide therapy.【期刊名称】《临床肾脏病杂志》【年(卷),期】2017(017)004【总页数】5页(P221-225)【关键词】抗肾小球基底膜病;急性肾损伤;膜性肾病;肺出血【作者】包红梅;张建春;陈晓明;郭文岗;王素霞;章友康【作者单位】065201廊坊,京东誉美中西医结合肾病医院肾内科;065201廊坊,京东誉美中西医结合肾病医院肾内科;065201廊坊,京东誉美中西医结合肾病医院肾内科;065201廊坊,京东誉美中西医结合肾病医院肾内科;100034北京,北京大学第一医院肾内科;100034北京,北京大学第一医院肾内科【正文语种】中文患者王某,男,20岁,以“乏力20余天,肉眼血尿、浮肿伴血肌酐升高5天”于2015年7月5日入住京东誉美中西医结合肾病医院。
肾小球疾病。
非免疫因素:主要包括肾小球毛细血管内高压力、蛋白尿、高脂血症等
临床表现
血尿和/或蛋白尿–尿液分析检出血尿和/或蛋白尿时,应怀疑肾小球疾病。当存在红细胞管型(不论 多少)或棘红细胞占相当一部分比例时,可确诊肾小球性血尿。
肾小球的解剖学
肾小球解剖图
肾小球基底膜(GBM,以绿色表示) 是一层薄薄的细胞外基质蛋白,包 裹在毛细血管周围,提供支持和屏 障。 (A)肾小球和肾小球旁器。 (B)肾小叶的外周部分。
分类
原发性肾小球疾病可作临床和病理分型 ➢ 原发性肾小球疾病的临床分型 • 急性肾小球肾炎(acute glomerulonephritis) • 急进性肾小球肾炎(rapidly progressive glomerulonephritis) • 慢性肾小球肾炎(chronic glomerulonephritis) • 无症状性血尿和(或)蛋白尿(asymptomatic hematrotic syndrome)
注意:肾小球疾病病理分型的基本原则是依据病变性质和病变累及范围
发病机制
免疫反应:包括体液免疫和细胞免疫 ➢ 体液免疫中循环免疫复合物(circulating immune complex,CIC)、原位免疫复 合物(in situ immune complex)以及自身抗体在肾小球疾病发病机制中的作用 已得到公认,细胞免疫在某些类型肾小球疾病中的重要作用也得到重视
高凝状态–某些肾小球疾病可能会导致高凝状态,尤其是膜性肾病,其次是其他原因的肾病综合征。 肾小球疾病患者也可表现为血栓栓塞事件(如,肺栓塞)。 系统性表现–肾小球疾病可主要局限于肾脏,也可与感染、自身免疫性疾病、恶性肿瘤及药物反应 等系统性病症有关。 对于疑似肾小球疾病的患者,病史、体格检查和初始实验室检查应包括对系统性疾病的评估,例如: • 全身–发热、寒战、体重减轻、盗汗、乏力 • 眼–视网膜炎或葡萄膜炎 • 耳鼻喉–鼻出血、鼻窦炎、口腔溃疡 • 心血管–杂音、疼痛(心包炎)或心衰 • 肺–咯血、浸润或结节 • 腹部–小肠炎、结肠炎或胰腺炎 • 神经系统–抽搐或周围神经病变 • 四肢–指/趾缺血或梗死 • 皮肤–紫癜或皮疹 • 肌肉骨骼–关节炎、关节痛、肌痛 • 感染–特别是有葡萄球菌(Staphylococcus)、链球菌(Streptococcus)、肝炎病毒、HIV或梅毒的
伴IgA沉积的抗肾小球基底膜病1例报告并文献复习

伴IgA沉积的抗肾小球基底膜病1例报告并文献复习摘要:抗肾小球基底膜病(anti-GBM病)是一种少见的肾小球肾炎,其特点是肾小球基底膜上的IgG沉积。
一些病例也伴随着IgA沉积,且这种情况更少见。
本文报告了一例伴IgA沉积的抗肾小球基底膜病患者的临床病例,包括患者的临床表现、实验室检查、病理学特征和治疗情况。
关键词:抗肾小球基底膜病;IgA沉积;肾小球肾炎;肾脏病理学病例报告患者信息:男性,47岁,主要症状为气促和全身水肿。
临床表现:患者主要表现为气促,伴有全身水肿,尿量正常,血压偏高,呼吸音粗糙。
实验室检查:血清肌酐升高至238umol/L,尿常规检查显示蛋白尿2+,红细胞管型(+),24小时尿蛋白为3.6g,B超显示肾脏大小正常,肾实质回声增强。
肾脏病理学:患者行肾穿刺术,肾脏病理学显示:光镜下,肾小球毛细血管环绕免疫毒素颗粒,伴有明显的肾小管间质炎症细胞浸润。
免疫荧光染色显示IgA、IgG阳性,C3、C1q阴性。
诊断及治疗:结合临床表现和实验室检查结果,患者最终被诊断为伴IgA沉积的抗肾小球基底膜病。
给予免疫抑制治疗,包括糖皮质激素和环磷酰胺,同时行血液透析支持。
随访:经过6个月的治疗,患者的肾功能得到改善,血肌酐下降至94umol/L,尿蛋白减少至轻度阳性,无气促和全身水肿等不适症状。
讨论抗肾小球基底膜病是一种少见的自身免疫性疾病,其典型的临床特征是急性肾衰竭和肾小球性血尿。
在免疫病理学上,抗肾小球基底膜病的主要特点是肾小球基底膜上沉积IgG,导致肾小球毛细血管炎和肾小球毛细血管性肾炎。
有时候也会出现IgA沉积的情况,这种情况在文献中非常罕见。
目前关于伴IgA沉积的抗肾小球基底膜病的报道非常有限,因此对该疾病的临床表现、病理学特征和治疗方案等方面仍需进一步研究。
文献复习为了更好地了解伴IgA沉积的抗肾小球基底膜病,我们对相关文献进行了复习。
以下是我们找到的一些相关文献:1. Chen, W., & Chen, D. (2019). Clinical features and outcomes of patients with anti-GBM disease and IgA nephropathy. Kidney International Reports, 4(11),1615-1621.这项研究报告了一组患有抗肾小球基底膜病和IgA肾病的患者的临床特征和预后。
MPOPR3GBM临床意义
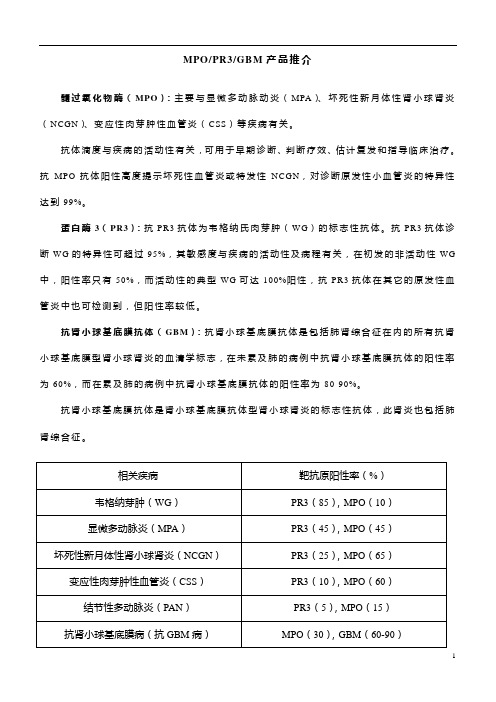
MPO/PR3/GBM产品推介
髓过氧化物酶(MPO):主要与显微多动脉动炎(MPA)、坏死性新月体性肾小球肾炎(NCGN)、变应性肉芽肿性血管炎(CSS)等疾病有关。
抗体滴度与疾病的活动性有关,可用于早期诊断、判断疗效、估计复发和指导临床治疗。
抗MPO抗体阳性高度提示坏死性血管炎或特发性NCGN,对诊断原发性小血管炎的特异性达到99%。
蛋白酶3(PR3):抗PR3抗体为韦格纳氏肉芽肿(WG)的标志性抗体。
抗PR3抗体诊断WG的特异性可超过95%,其敏感度与疾病的活动性及病程有关,在初发的非活动性WG 中,阳性率只有50%,而活动性的典型WG可达100%阳性,抗PR3抗体在其它的原发性血管炎中也可检测到,但阳性率较低。
抗肾小球基底膜抗体(GBM):抗肾小球基底膜抗体是包括肺肾综合征在内的所有抗肾小球基底膜型肾小球肾炎的血清学标志,在未累及肺的病例中抗肾小球基底膜抗体的阳性率为60%,而在累及肺的病例中抗肾小球基底膜抗体的阳性率为80-90%。
抗肾小球基底膜抗体是肾小球基底膜抗体型肾小球肾炎的标志性抗体,此肾炎也包括肺肾综合征。
114例抗肾小球基底膜抗体阳性结果分析

114例抗肾小球基底膜抗体阳性结果分析李丽娟;李晓梅;曾彩虹【摘要】目的探讨抗肾小球基底膜(GBM)抗体检测在抗GBM疾病及其他不同疾病中的应用.方法回顾分析经间接免疫荧光(IIF)法及酶联免疫吸附试验(ELISA)检测血清抗GBM抗体均为阳性的患者114例,比较抗GBM抗体在抗GBM疾病及其他疾病中的分布和抗体滴度差异,探讨其与临床表现及病理间的联系.结果 114例抗GBM抗体阳性患者,包括抗GBM疾病99例(86.84%),其中抗GBM肾炎65例(57.02%)、Goodpasture综合征26例(22.81%)、抗GBM肾炎合并其他肾病8例(7.02%);非抗GBM相关疾病15例(13.16%).Goodpasture综合征患者的男性、有机溶剂/工业粉尘暴露、咯血、合并少尿或无尿比例高于其他疾病组(P=0.022、0.014、0.001、0.001),抗GBM肾炎的吸烟比例小于其他组(P=0.006),抗GBM肾炎和Goodpasture综合征患者合并中性粒细胞细胞质抗体(ANCA)的比例小于抗GBM肾炎合并其他肾病和非抗GBM相关疾病组(P=0.014).抗GBM疾病患者血肌酐、抗GBM抗体水平、合并新月体病例及新月体比例均高于非抗GBM相关疾病组(均P=0.001).99例抗GBM疾病患者,抗GBM抗体水平与性别、年龄、合并咯血无关,与少尿或无尿、确诊时患者肌酐水平、肾小球中新月体比例呈正相关,与合并ANCA呈负相关.结论抗GBM抗体阳性主要见于抗GBM疾病中,特别是抗GBM抗体水平较高的患者,临床医生需及早诊断及鉴别诊断抗GBM疾病,及早治疗,改善预后.【期刊名称】《检验医学与临床》【年(卷),期】2018(015)021【总页数】5页(P3186-3190)【关键词】抗肾小球基底膜抗体;抗肾小球基底膜疾病;Goodpasture综合征【作者】李丽娟;李晓梅;曾彩虹【作者单位】南京军区南京总医院肾脏科/国家肾脏疾病临床医学研究中心/全军肾脏病研究所 ,南京 210016;南京军区南京总医院肾脏科/国家肾脏疾病临床医学研究中心/全军肾脏病研究所 ,南京 210016;南京军区南京总医院肾脏科/国家肾脏疾病临床医学研究中心/全军肾脏病研究所 ,南京 210016【正文语种】中文【中图分类】R446.62抗肾小球基底膜(GBM)疾病是循环中的抗GBM抗体在脏器中沉积所引起的一组自身免疫性疾病,病变局限在肾脏时多表现为新月体肾炎,称为抗GBM肾炎;若同时累及肺则表现为肺出血,称为Goodpasture综合征。
膜性肾病合并抗肾小球基底膜病研究进展

膜性肾病合并抗肾小球基底膜病研究进展宋曦玉;查阳;何春艳;何丽洁【期刊名称】《临床医学进展》【年(卷),期】2022(12)7【摘要】膜性肾病(membranous nephropathy, MN)的典型病理表现是上皮下存在免疫复合物,而在临床中观察到MN患者组织中有新月体的形成,这种情况是十分罕见的。
引起新月体型MN的常见原因之一是MN合并了抗肾小球基底膜病(glomerular basement membrane, GBM)。
近年来逐渐有MN合并抗GBM病的病例及相关研究报道。
在这一类疾病中,MN和抗GBM病可同时出现或先后发生,因此该病例既有MN的临床表现,又有抗GBM病的临床表现,在这些病例的血清中均未发现原发性MN的特征性抗体,但均存在抗GBM抗体阳性。
MN合并抗GBM病确切的机制尚不明确,患者的免疫学特点、人类白细胞抗原易感性以及基于动物实验等方面的研究能够为探寻该病的临床表现和发病机制提供一些线索。
由于抗GBM抗体的致病性,使得合并抗GBM病的MN患者往往肾脏预后不良,但临床医师对这一类疾病的认识尚不足,本文通过回顾近年来MN合并抗GBM病的病例报道,相关领域的研究进展,对其发病机制、临床病理特征、治疗及预后进行综述。
【总页数】7页(P6837-6843)【作者】宋曦玉;查阳;何春艳;何丽洁【作者单位】空军军医大学基础医学院西安;空军军医大学西京医院肾内科西安;空军第九八六医院肿瘤血液科西安【正文语种】中文【中图分类】R73【相关文献】1.膜性肾病合并抗肾小球基底膜肾炎1例2.膜性肾病合并肾功能轻度受损的抗肾小球基底膜病一例报道及文献复习3.膜性肾病合并抗基底膜性肾小球肾炎及Castleman病1例4.抗基底膜肾小球肾炎合并膜性肾病病例报告并文献复习5.膜性肾病合并抗肾小球基底膜病2例并文献复习因版权原因,仅展示原文概要,查看原文内容请购买。
一例IgA肾病合并抗肾小球基底膜病临床表现分析

一例IgA肾病合并抗肾小球基底膜病临床表现分析患者男,18岁,因“心累、气促1年余,双下肢水肿2月余,加重7+天”入院。
1年余前无明显诱因出现心累、气促,以活动后更明显,伴恶心不适,以夜间为主;于新疆当地医院就诊,完善相关检查提示贫血(具体不详),患者未予以重视,未作任何治疗。
2月前,患者出现双下肢对称性凹陷性水肿伴小便减少,夜尿增多,平均一天尿量约500ml左右,患者未予以重视及治疗。
7天前,患者上述症状加重,双下肢水肿明显,患者隧到宁南县医院就诊,当地医院建议上级医院进一步治疗,患者于2018年9月1日遂到乐至县人民医院住院治疗,诊断为“肾功能不全、高尿酸血症”,予以护肾、补液等对症治疗后症状无明显好转,建议患者转院治疗。
现为求进一步治疗,遂到我院就诊,急诊以“肾病”收入我科。
入院查体:BP132/80mmHg 步入病房,慢性病容,轻度贫血貌,心肺无特殊,双肾区无叩痛,双下肢膝关节以下对称性凹陷性水肿,神经反射正常。
辅助检查:血常规示:白细胞10.55×10^9/L,红细胞 4.08×10^12/L,血红蛋白 76g/L;尿常规示:蛋白+3、潜血+3。
24h尿蛋白定量 5856.0mg /24h;肾功:肌酐 237umol/L,尿酸 430umol/L;肝功:总胆红素5.1umol/L,直接胆红素 1.3umol/L,总蛋白 45.5g/L,白蛋白 25.4g/L,前白蛋白 218mg/l,谷丙转氨酶 5U/L,谷草转氨酶 12U/L。
葡萄糖 4.54mmol/L,抗GBM抗体阳性;胸片示胸腔积液,两肺、心膈未见异常;彩超示:肝、胆系、胰腺、脾脏超声未见明显改变。
双侧胸腔积液。
腹腔积液。
心脏形态结构及血流未见明显改变。
肾组织病理检查:光镜下可见14个肾小球,未见肾小球球性硬化,其中1个肾小球节段性硬化,其余肾小球中可见4个细胞性,5个细胞纤维性,1个小细胞性,2个小细胞纤维性新月体形成,其余1个肾小球系膜细胞和基质增生,系膜区嗜复红蛋白沉积。
抗肾小球基底膜病_-_ppt课件

概述
• 抗肾小球基底膜抗体( glomerular basement membrane, GBM)是各种因素 作用于肾小球基底膜,使其结构发生改变 或暴露,诱发机体产生的自身抗体。
• 抗GBM抗体为IgG型,偶见IgA型。
17
治疗
• • • • 强化血浆置换:清除抗GBM和补体 免疫抑制剂:甲基泼尼龙冲击+环磷酰胺 对症治疗:纠酸、水、电解质,抗感染 透析/肾移植:抗GBM转阴半年以上可肾移植
18
预后
• 早期未经治疗的病例中90%的患者进入终末期肾功 能衰竭或死亡 • 经血浆置换及免疫抑制剂治疗,约一半患者预后明 显改善经治疗
19
20
后面内容直接删除就行 资料可以编辑修改使用 资料可以编辑修改使用
资料仅供参考,实际情况实际分析
主要经营:课件设计,文档制作,网络软件设计、 图文设计制作、发布广告等 秉着以优质的服务对待每一位客户,做到让客户满 意! 致力于数据挖掘,合同简历、论文写作、PPT设计、 计划书、策划案、学习课件、各类模板等方方面面, 打造全网一站式需求
12
实验室检查
• 大约20~ 40%的抗GBM抗体阳性患者,可以同时出现血管 炎的标志性抗体—ANCA,多为P-ANCA。 • ANCA相关性小血管炎起病数周或数月之后也可出现抗 GBM抗体阳性。 • 两种抗体之间是否存在交叉反应性,目前研究尚无定论 。有研究发现MPO、PR3、GBM三种抗原结构不存在同 源性,不支持抗GBM抗体与ANCA存在交叉反应。 • GBM伴ANCA阳性患者全身表现类似单纯ANCA相关小血 管炎患者,但治疗效果及预后相对较差又类似于Anti-GBM 肾炎患者。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
case_fre 0.29 0.027 0.022 0.19 0.011
Control_fre Haplo.scor e 0.095 0.0078 0.1 0.09 0.092 0.034 0.056 8.838 4.118 -4.312 4.62 -4.48 3.5 -3.5
P-val 9.7×10-19 3.8×10-5 1.6×10-5 1.0×10-6 7.3×10-6 0.00042 0.00042
Allele-1 DRB1*1501 DRB1*1501 DRB1*1501 DRB1*1501 DQB1*0602 DQB1*0602 DQB1*0602 DQB1*0303 DQB1*0303 DQA1*0502 Allele-2 DQB1*0602 DRB1*0901 DQB1*0303 DQA1*0502 DRB1*0901 DQB1*0303 DQA1*0502 DRB1*0901 DQA1*0502 DRB1*0901 D' 0.562 1 0.817 0.243 0.685 1 0.46 0.641 1 0.148 r2 0.305 0.039 0.024 0.001 0.018 0.035 0.005 0.385 0.001 0 LOD score 51.22 10.41 4.44 1.03 2.81 8.55 0.82 56.05 0.47 0
– 1例18岁男性病人,咯血、急性肾衰竭 – 流感?
• 60%的患者发病前有前驱感染症状
– 病原微生物----分子模拟?
• 涉及感染、抗原递呈、抗原决定簇扩展、分子模拟
?
Linear to Conformational
16
Background ( HLA )
HLA gene
Location:
CHR 6p21.3 Classical HLA gene
MHC class II molecular:
: DCs、B cells、Mø Structure: hetero-dimer recognized by CD4+ T cell Ag processed 、presentation
表型?
7
7
23/M 间断咯血 4 个月,加重1个月
HGB: 71g/L; PO2 58mmHg; Scr 94.0 μmol/l
尿常规: protein (+), RBC 5-8/HPF 血清抗GBM抗体 (+), ANCA (-) 肾活检: IgG沿GBM线样沉积,肾小球轻微病变 治疗:Pred 1 mg/kg/d x 8w, 无PE和CTX 随访7年肾功能正常
Jia XY, et al. Kidney Int2014 Apr;85(4):945-52
抗GBM病的科学问题
• 病因
– 易感性:HLA? – 诱发因素 – 病因
• 表型差异
病因 遗传易 感背景 诱发因素?
自身 免疫
T细胞
3(IV)NC1 B细胞 免疫耐受?
表型?
15
抗GBM病的免疫学发病机制
T细胞 3(IV)NC1 B细胞 免疫耐受?
表型?
12
抗GBM病合并MN
• 个例报道
• MN → GBM damage:释放α3 → 抗GBM 病 • 抗GBM病→足细胞损伤:表达M-PLA2R →MN
13
13
• 8 patients with MN and anti-GBM disease
– – – – Sequential or simultaneous Better prognosis Anti-α3 (+): narrow antigen spectrum Anti-PLA2R (-)
Goodpasure EM. Am J Med Sci 1919;158: 863-870 Cui Z, Zhao MH. Nat Rev Nephrol. 2011 2 Dec 7:697-706
抗GBM病的发生情况
• 少见病:1-2/百万人口 • 本研究所:累计诊断500余例 抗GBM病仍然是我国 内科医生的重 大挑战
肾受累轻患者介于正常人与重症患者之间?转换机制?
8 Cui Z, et al. Kidney Int 2007;72:1403-8
8
既往:健康人血清无抗GBM抗体 发现天然抗GBM抗体:
Natural anti-GBM ab
中国和瑞典:各10名献血员 IgG成分---亲和层析
3 Ea、 Eb
3, 4 IgG2、IgG4
治疗个体化 T细胞调控
Cui Z, et al. Kidney Int 2006;69:894-9. Yang R, et al. J Am Soc Nephrol 2007;18(4):1338-43. Cui Z, et al. Kidney Int 2007;72(11):1403-8. Zhao J & Cui Z, et al. Kidney Int. 2009;76:1108-15. Cui Z, et al. Kidney Int 2010;78(6):590-7. 10 . 2013;8(1):51-8. Chen JL & Hu SY, et al. Clin J Am Soc Nephrol
0.1469 0.1544 0.0008347 0.1444 0.1494
OR
4.549 3.336 30.69 0.2885 0.3911
P_val
5.658E-28 2.032E-17 6.987E-7 8.575E-6 1.611E-4
Association of a novel HLA SNP(P<1.9E-4)
Distribution
MHC & disease:
MS、RA、IDDM、 SLE et al.
17
MHC II dominant protection
No gene dosage effect
Dominantly protective alleles DR1 and DR7
–HLA-DRB1*01:01 generates 3136-146 specific regulatory T cells. –HLA-DRB1*15:01 generates 3136-146 specific effector T cell precursors. –In HLA-DRB1*15:01x01:01 mice, 3136-146 specific effector T cell precursors are dominantly suppressed by 3136-146 specific regulatory T cells
LOD>3:Confirmed linkage. LOD<-2: No linkage. LOD=0: the possibility is equal Unpublished data 22
抗GBM病的科学问题
• 病因
– 易感性 – 诱发因素:环境? – 病因
• 表型差异
病因 遗传易 感背景 诱发因素?
DRB1*1501-DQA1*0102-DQB1*0602-DPB1*0201 0.084 DRB1*0901-DQA1*0302-DQB1*0303-DPB1*0501 0.0041
Unpublished data 21
21
Linkage analysis among the significant alleles
Association of HLA alleles (4 digits, P<3.55E-4)
Allele
DRB1*1501 DQB1*0602 DQA1*0502 DQB1*0303 DRB1*0901
Case_fre
0.4384 0.3840 0.025547 0.0471 0.06522
Control_fre
5
抗GBM病的科学问题
• 病因 • 表型差异
病因 遗传易 感背景 诱发因素? 自身 免疫
T细胞 3(IV)NC1 B细胞 免疫耐受?
表型?
6
6
抗GBM病的科学问题
• 病因 • 表型差异
• 肾受累轻重 • 1/3合并ANCA • 少数合并MN
病因 遗传易 感背景 诱发因素? 自身 免疫
T细胞 3(IV)NC1 B细胞 免疫耐受?
NATURE REVIEWS | NEPHROLOGY
Cui Z, Zhao MH. Nat Rev Nephrol. 2011 Dec;7:697-706.
抗GBM病的科学问题
• 病因 • 表型差异
• 肾受累轻重 • 1/3合并ANCA • 少数合并MN
病因 遗传易 感背景 诱发因素? 自身 免疫
– 国际上最大的临床资源库 – 治疗依赖血浆置换:昂贵,但多为时已晚
Cui Z, Zhao MH. Nat Rev Nephrol. 2011 Dec 7:697-706
3
抗GBM病是典型的自身免疫病
• 靶抗原
– 3(IV)NC1 (肺、肾)
• Epitope
– Ea和Eb---构象性
Saus J, et al. J Biol Chem 1988;15;263:13374-80 Salant DJ. N Engl J Med 2010;363;4:381-391
Extended haplotypes among HLA-DRB1, DQA1 ,DQB1,DPB1 in anti-GBM disease
Extended haplotype DRB1*1501-DQB1*0602 DRB1*1501-DRB1*0601 DRB1*0901-DQB1*0303 DRB1*1501-DQA1*0102-DQB1*0602 DRB1*0901-DQA1*0302-DQB1*0303
