2021新人教版高中化学选修三2.2《分子的立体结构》word教案
新人教版高二化学选修3:分子的立体结构(第1课时)教案 Word版

第二節分子的立體結構第一課時教學目標:1、認識共價分子的多樣性和複雜性;2、初步認識價層電子對互斥模型;3、能用VSEPR模型預測簡單分子或離子的立體結構;4、培養學生嚴謹認真的科學態度和空間想像能力。
重點難點:分子的立體結構;利用價層電子對互斥模型預測分子的立體結構教學過程創設問題情境:1、閱讀課本P37-40內容;2、展示CO2、H2O、NH3、CH2O、CH4分子的球輥模型(或比例模型);3、提出問題:⑴什麼是分子的空間結構?⑵同樣三原子分子CO2和H2O,四原子分子NH3和CH2O,為什麼它們的空間結構不同?[討論交流]1、寫出CO2、H2O、NH3、CH2O、CH4的電子式和結構式;2、討論H、C、N、O原子分別可以形成幾個共價鍵;3、根據電子式、結構式描述CO2、H2O、NH3、CH2O、CH4的分子結構。
[模型探究]由CO2、H2O、NH3、CH2O、CH4的球輥模型,分析結構不同的原因。
[引導交流]引導學生得出由於中心原子的孤對電子佔有一定的空間,對其他成鍵電子對存在排斥力,影響其分子的空間結構。
——引出價層電子對互斥模型(VSEPR models)[講解分析] 價層電子對互斥模型把分子分成兩大類:一類是中心原子上的價電子都用於形成共價鍵。
如CO2、CH2O、CH4等分子中的C原子。
它們的立體結構可用中心原子周圍的原子數來預測,概括如下:H2O和NH3中心原子上的孤對電子也要佔據中心原子周圍的空間,並參與互相排斥。
因而H2O分子呈V型,NH3分子呈三角錐型。
(如圖)課本P40。
[應用回饋]應用VSEPR理論判斷下表中分子或離子的構型。
進一步認識多原子分子的立體結構。
[練習]:1、下列物質中,分子的立體結構與水分子相似的是A、CO2B、H2SC、PCl3D、SiCl42、下列分子的立體結構,其中屬於直線型分子的是A、H2OB、CO2C、C2H2D、P43、寫出你所知道的分子具有以下形狀的物質的化學式,並指出它們分子中的鍵角分別是多少?①直線形②平面三角形③三角錐形④正四面體4、下列分子中,各原子均處於同一平面上的是A、NH3B、CCl4C、H2OD、CH2O5、下列分子的結構中,原子的最外層電子不都滿足8電子穩定結構的是A、CO2B、PCl3C、CCl4D、NO26、下列分子或離子的中心原子,帶有一對孤對電子的是A、XeO4B、BeCl2C、CH4D、PCl37、為了解釋和預測分子的空間構型,科學家在歸納了許多已知的分子空間構型的基礎上,提出了一種十分簡單的理論模型——價層電子對互斥模型。
新人教版高二化学选修3:2.2分子的立体结构(第2课时)教案 word版

前言我们分析每年考上清华北大的北京考生的成绩,发现能够考上清北的学生化学的平均分都在95分以上,先开始我们认为,学习能力强的孩子化学一定学得好。
可是在分析没有考上清北的学生的成绩的时候发现,很多与清北失之交臂的学生,化学的平均分要略低,数学物理的分数却不相上下。
我们仔细讨论其中的缘由,通过对学生的调查研究发现一个令人惊讶的结论:化学学的好的学生更容易在理综上考得高分!这是因为化学学的好的学生,能够用更快的速度在理综考试中解决100分的分值,之后孩子可以用更多的时间去处理没有见过的物理难题。
物理的难题在充分的时间中得到更多考虑的空间,使得考生在理综总分上能够有所突破。
所以想上好大学,化学必须学好,化学的使命就是在高考当中帮助考生提速提分。
因此这份资料提供给大家使用,主要包含有一些课件和习题教案。
后序中有提到一些关于学习的建议。
第二课时教学目标1、认识杂化轨道理论的要点2、进一步了解有机化合物中碳的成键特征3、能根据杂化轨道理论判断简单分子或离子的构型4、采用图表、比较、讨论、归纳、综合的方法进行教学5、培养学生分析、归纳、综合的能力和空间想象能力教学重点:杂化轨道理论的要点教学难点:分子的立体结构,杂化轨道理论教学过程:碳的价电子构型是什么样的?甲烷的分子模型表明是空间正四面体,分子中的C—H键是等同的,键角是109°28′。
说明什么?[结论]碳原子具有四个完全相同的轨道与四个氢原子的电子云重叠成键。
师:碳原子的价电子构型2s22p2,是由一个2s轨道和三个2p轨道组成的,为什么有这四个相同的轨道呢?为了解释这个构型Pauling提出了杂化轨道理论。
板书:三、杂化轨道理论1、杂化的概念:在形成多原子分子的过程中,中心原子的若干能量相近的原子轨道重新组合,形成一组新的轨道,这个过程叫做轨道的杂化,产生的新轨道叫杂化轨道。
[思考与交流]甲烷分子的轨道是如何形成的呢?形成甲烷分子时,中心原子的2s和2p x,2p y,2p z等四条原子轨道发生杂化,形成一组新的轨道,即四条sp3杂化轨道,这些sp3杂化轨道不同于s轨道,也不同于p 轨道。
新人教版高二化学选修3:2.2分子的立体结构(第1课时)教案word版

第二节分子的立体构造第一课时教课目的:1、认识共价分子的多样性和复杂性;2、初步认识价层电子对互斥模型;3、能用VSEPR模型展望简单分子或离子的立体构造;4、培育学生谨慎仔细的科学态度和空间想象能力。
要点难点:分子的立体构造;利用价层电子对互斥模型展望分子的立体构造教课过程创建问题情境:1、阅读课本P37-40内容;2、展现CO2、H2O、NH3、CH2O、CH4分子的球辊模型(或比率模型);3、提出问题:⑴什么是分子的空间构造?⑵相同三原子分子CO2和H2O,四原子分子NH3和CH2O,为何它们的空间构造不一样?[议论沟通]1、写出CO2、H2O、NH3、CH2O、CH4的电子式和构造式;2、议论H、C、N、O原子分别能够形成几个共价键;3、依据电子式、构造式描绘CO2、H2O、NH3、CH2O、CH4的分子构造。
[模型研究]由CO2、H2O、NH3、CH2O、CH4的球辊模型,剖析构造不一样的原由。
[指引沟通]指引学生得出因为中心原子的孤对电子据有必定的空间,对其余成键电子对存在排挤力,影响其分子的空间构造。
——引出价层电子对互斥模型(VSEPRmodels)[解说剖析] 价层电子对互斥模型把分子分红两大类:一类是中心原子上的价电子都用于形成共价键。
如CO2、CH2O、CH4平分子中的C原子。
它们的立体构造可用中心原子四周的原子数来展望,归纳以下:ABn立体构造典范n=2直线型CO2n=3平面三角形CH2On=4正四周体型CH4另一类是中心原子上有孤对电子(未用于形成共价键的电子对)的分子。
如H2O和NH3中心原子上的孤对电子也要据有中心原子四周的空间,并参与相互排挤。
因此H2O分子呈V型,NH3分子呈三角锥型。
(如图)课本P40。
[应用反应]应用VSEPR理论判断下表中分子或离子的构型。
进一步认识多原子分子的立体构造。
中心原子含有中心原子联合化学式空间构型孤对电子对数的原子数H2S 2 2 V形NH2-22V形BF303正三角形CHCl304四周体SiF404正四周体[练习]:1、以下物质中,分子的立体构造与水分子相像的是A、CO2B、H2SC、PCl3D、SiCl42、以下分子的立体构造,此中属于直线型分子的是A、H2OB、CO2C、C2H2D、P43、写出你所知道的分子拥有以下形状的物质的化学式,并指出它们分子中的键角分别是多少?①直线形②平面三角形③三角锥形④正四周体4、以下分子中,各原子均处于同一平面上的是A、NH3B、CCl4C、H2OD、CH2O5、以下分子的构造中,原子的最外层电子不都知足8电子稳固构造的是A、CO2B、PCl3C、CCl4D、NO26、以下分子或离子的中心原子,带有一对孤对电子的是A、XeO4B、BeCl2C、CH4D、PCl37、为认识释和展望分子的空间构型,科学家在归纳了很多已知的分子空间构型的基础上,提出了一种十分简单的理论模型——价层电子对互斥模型。
人教版化学选修三2.2《分子的立体构型(第2课时)分子的空间结构和价层电子对互斥理论》教学设计

第二章第二节分子的立体构造第 2 课时分子的空间构造与价层电子对互斥理论【学习目标】 1、能应用价层电子对互斥理论判断分子的空间构型。
【学习要点】σ键电子对、孤电子对和价层电子对的计算,VSEPR 模型【学习难点】分子立体构型的推测课前预习案一、价层电子对互斥理论(阅读课本 P37-38 达成填空)1、价层电子对互斥理论以为,分子的“立体构型”是的结果。
2、价层电子对是指;价层电子对 =+;( 1)σ键电子对数:可由确立。
比如,H2O的中心原子是______,构造式是 __________,有个σ键,故σ键电子对数是______;(2)中心原子上的孤对电子对数:依据公式 _______________________确立,此中 a 为,关于主族元向来说,价电子数等于;x 为;b 为;氢为 _____,其余原子等于。
阳离子: a 为中心原子的价电子数减去 _______________;阴离子:a为中心原子的价电子数加上(绝对值)。
2-的孤对电子数 =1/2(6+2-2*3 )=13比如: SO【预习检测】1、运用你对分子的已有的认识,达成以下表格,写出C、 H、N、O 的电子式,依据共价键的饱和性议论C、H、N、 O、F 的成键状况。
原子H C N O F 电子式可形成的共用电子对数讲堂研究案研究一:价层电子对空间构型(即VSEPR 模型)价层电子对互斥理论的基本内容:对AB n型的分子或离子,中心原子A 价层电子对(包含成键σ键电子对和未成键的孤对电子对)之间因为存在排挤力,将使分子的几何构型老是采纳电子对互相排挤最小的那种构型,以使相互之间斥力最小,分子系统能量最低、最稳固。
问题 1:请你依据价层电子对互斥理论的基本内容,总结出价层电子对的空间构型(即 VSEPR 模型)(利用牙签与橡皮泥模拟)空间构型价电子对数量234VSEPR 模型形形形问题 2:依据价层电子对互斥理论,计算出以下分子的中心原子含有的σ键电子对数、孤对电子数及价层电子数。
选修3第二章第2节《分子的立体结构》教案

选修3第二章第2节《分子的立体结构》教案教学目标:1.了解分子的立体结构及其对物质性质的影响。
2.学会运用VSEPR模型预测分子的立体结构。
3.能够运用杂化轨道理论解释分子的立体结构。
教学重点:1.分子的立体结构及其对物质性质的影响。
2.VSEPR模型预测分子的立体结构。
3.杂化轨道理论解释分子的立体结构。
教学难点:1.VSEPR模型的理解和应用。
2.杂化轨道理论的理解和应用。
教学准备:1.PPT课件2.教学模型3.分子模型教学过程:一、导入1.通过展示一些具有不同立体结构的分子模型,引发学生对分子立体结构的兴趣。
2.提问:你们知道分子的立体结构对物质性质有什么影响吗?二、新课讲解1.讲解分子的立体结构及其对物质性质的影响a.分子的立体结构是指分子中原子的空间排列方式。
b.分子的立体结构对物质的性质,如熔点、沸点、溶解性等有着重要影响。
2.讲解VSEPR模型预测分子的立体结构a.介绍VSEPR模型的原理和步骤。
b.通过实例演示如何运用VSEPR模型预测分子的立体结构。
3.讲解杂化轨道理论解释分子的立体结构a.介绍杂化轨道理论的基本概念。
b.通过实例演示如何运用杂化轨道理论解释分子的立体结构。
三、案例分析1.分析案例一:水分子H2O的立体结构a.运用VSEPR模型预测H2O的立体结构。
b.运用杂化轨道理论解释H2O的立体结构。
2.分析案例二:氨分子NH3的立体结构a.运用VSEPR模型预测NH3的立体结构。
b.运用杂化轨道理论解释NH3的立体结构。
四、互动环节1.学生分组,每组选择一个分子,运用VSEPR模型和杂化轨道理论预测和解释其立体结构。
2.各组汇报成果,其他组进行评价和讨论。
六、作业教学反思:本节课通过讲解和案例分析,让学生了解了分子的立体结构及其对物质性质的影响,学会了运用VSEPR模型和杂化轨道理论预测和解释分子的立体结构。
在教学过程中,要注意引导学生积极参与,培养学生的动手能力和思维能力。
2021年新人教版高二化学选修3:2.2分子的立体结构(第2课时)教案 Word版

第二课时教育方针1、知道杂化轨迹理论的关键2、进一步了解有机化合物中碳的成键特征3、能依据杂化轨迹理论判别简略分子或离子的构型4、选用图表、比较、评论、概括、概括的办法进行教育5、培育学生剖析、概括、概括的才能和空间幻想才能教育关键:杂化轨迹理论的关键教育难点:分子的立体结构,杂化轨迹理论教育进程:碳的价电子构型是什么样的?甲烷的分子模型标明是空间正四面体,分子中的C—H键是同等的,键角是109°28′。
阐明什么?[定论]碳原子具有四个完全相同的轨迹与四个氢原子的电子云重叠成键。
师:碳原子的价电子构型2s22p2,是由一个2s轨迹和三个2p轨迹组成的,为什么有这四个相同的轨迹呢?为了解说这个构型Pauling提出了杂化轨迹理论。
板书:三、杂化轨迹理论1、杂化的概念:在构成多原子分子的进程中,中心原子的若干能量附近的原子轨迹重新组合,构成一组新的轨迹,这个进程叫做轨迹的杂化,产生的新轨迹叫杂化轨迹。
[考虑与沟通]甲烷分子的轨迹是怎么构成的呢?构成甲烷分子时,中心原子的2s和2p x,2p y,2p z等四条原子轨迹产生杂化,构成一组新的轨迹,即四条sp3杂化轨迹,这些sp3杂化轨迹不同于s轨迹,也不同于p轨迹。
依据参加杂化的s轨迹与p轨迹的数目,除了有sp3杂化轨迹外,还有sp2杂化和sp杂化,sp2杂化轨迹表明由一个s轨迹与两个p轨迹杂化构成的,sp杂化轨迹表明由一个s轨迹与一个p轨迹杂化构成的。
[评论沟通]:使用轨迹杂化理论,探求分子的立体结构。
化学式杂化轨迹数杂化轨迹类型分子结构CH4C2H4BF3CH2OC2H2[总结点评]:引导学生剖析、概括、总结多原子分子立体结构的判别规则,完结下表。
化学式中心原子孤对电子对数杂化轨迹数杂化轨迹类型分子结构CH4C2H4BF3CH2OC2H2[评论]:怎样判别有几个轨迹参加了杂化?(提示:原子个数)[定论]:中心原子的孤对电子对数与相连的其他原子数之和,便是杂化轨迹数。
2021-2022学年人教版高中化学选修三教学案:第二章 第二节 分子的立体构型 Word版含答案
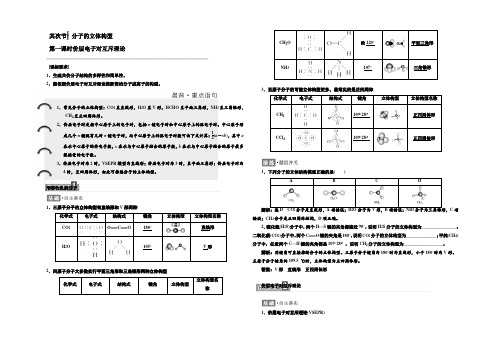
其次节⎪⎪分子的立体构型 第一课时价层电子对互斥理论————————————————————————————————————— [课标要求]1.生疏共价分子结构的多样性和简单性。
2.能依据价层电子对互斥理论推断简洁分子或离子的构型。
1.常见分子的立体构型:CO 2呈直线形,H 2O 呈V 形,HCHO 呈平面三角形,NH 3呈三角锥形,CH 4呈正四周体形。
2.价层电子对是指中心原子上的电子对,包括σ键电子对和中心原子上的孤电子对。
中心原子形成几个σ键就有几对σ键电子对,而中心原子上的孤电子对数可由下式计算:12(a -xb ),其中a表示中心原子的价电子数,x 表示与中心原子结合的原子数,b 表示与中心原子结合的原子最多能接受的电子数。
3.价层电子对为2时,VSEPR 模型为直线形;价层电子对为3时,呈平面三角形;价层电子对为4时,呈四周体形,由此可推想分子的立体构型。
形形色色的分子1.三原子分子的立体构型有直线形和V 形两种化学式 电子式结构式 键角 立体构型立体构型名称CO 2O===C===O180°直线形H 2O105°V 形2.四原子分子大多数实行平面三角形和三角锥形两种立体构型化学式电子式结构式键角立体构型立体构型名称CH 2O约120°平面三角形NH 3107°三角锥形3.五原子分子的可能立体构型更多,最常见的是正四周体化学式电子式结构式键角立体构型立体构型名称CH 4109°28′正四周体形CCl 4109°28′正四周体形1.下列分子的立体结构模型正确的是( )ABCD解析:选D CO 2分子是直线形,A 项错误;H 2O 分子为V 形,B 项错误;NH 3分子为三角锥形,C 项错误;CH 4分子是正四周体结构,D 项正确。
2.硫化氢(H 2S)分子中,两个H —S 键的夹角都接近90°,说明H 2S 分子的立体构型为________________;二氧化碳(CO 2)分子中,两个C===O 键的夹角是180°,说明CO 2分子的立体构型为______________;甲烷(CH 4)分子中,任意两个C —H 键的夹角都是109°28′,说明CH 4分子的立体构型为__________________。
人教版化学选修三2.2《分子的立体构型》实用教案设计

选修三第二章第二节分子的立体构型一、教材分析1.教材所处的地位和作用:本节内容在共价键概念的基础上,介绍了分子的立体结构,并根据价层电子对互斥模型和杂化轨道理论对简单共价分子结构的多样性和复杂性进行了解释。
在此之前学生已在化学2中学习了共价键基础,又在本章第一节“共价键”学习了共价键的主要类型σ键和π键,以及它们的差别。
这都为过渡到本节的学习起着铺垫作用。
在第二节“分子的立体结构”中,首先按分子中所含的原子数直间给出了三原子、四原子和五原子分子的立体结构,并配有立体结构模型图。
为什么这些分子具有如此的立体结构呢?教科书在本节安排了“价层电子对互斥模型”和“杂化轨道理论”来判断简单分子和离子的立体结构。
在介绍这两个理论时要求比较低,文字叙述比较简洁并配有图示。
还设计了“思考与交流”、“科学探究”等内容让学生自主去理解和运用这两个理论。
本节内容在基础结构化学中,占据非常重要的地位。
并为其他学科和今后的学习打下基础。
2.教育教学目标:(1)知识目标:①了解一些典型分子的立体结构,认识分子结构的多样性和复杂性;②通过对典型分子立体结构探究过程,学会运用观察、比较、分类及归纳等方法对信息进行加工,提高科学探究能力;③初步认识价层电子对互斥模型;④能用VSEPR模型预测简单分子或离子的立体结构。
(2)能力目标:通过教学培养学生严谨认真的科学态度和空间想象能力;培养学生收集处理信息,分析问题,解决实际问题的能力;通过师生双边活动,培养学生团结协作,语言表达能力;初步培养学生运用知识的能力,培养学生加强理论联系实际的能力。
(3)情感目标:通过本节的教学引导学生理论联系实际,通过电脑展示分子的立体结构,激发学习化学的兴趣,感受化学世界的奇妙。
3.重点、难点以及确定依据:重点:价层电子对互斥模型难点:能用价层电子对互斥模型解释分子的立体结构二、教学策略1.教学手段:教学方法:“构建数学立体模型与合作探究”。
①创设问题情景,让问题推动学生思考。
人教版选修3 化学:2.2 分子的立体构型 教案

分子的立体构型(课时1)一、教材分析本节课选自人教版选修三第二章第二节课时一,该部分是新课程改革之后新增的内容。
就整个高中化学课程而言,本节是具有强烈支撑作用的知识模块,本节内容承前启后,即解释了常见分子和离子的立体构型,又进一步为后面学习晶体及其在生活中的应用埋下铺垫。
所以本节内容至关重要。
按照新课程标准对物质结构与性质模块的要求,在必修2已介绍共价键的知识基础上,本节介绍了分子的立体结构,并根据价层电子对互斥理论对分子或离子结构的多样性和复杂性进行了解释。
通过学习,学生能在分子水平上,从分子结构的视角认识物质的性质,学生的科学素养能得到进一步提高。
对于前后知识逻辑性的延伸应用,可以增强学生对分子结构的有效理解与运用。
二、学生分析本节知识属于化学理论教学和已有知识关联度较少,通过设计引导希望尽可能取得较好的教学效果。
虽然学生已初步了解分子和离子的电子式、结构式,以及性质和结构的关系,但学生对分子和离子的空间立体构型还没有形成正确的深入理解,另一方面学生的空间想象思维略弱,相关知识的准确度把握不够,在教学过程中需要细致讲解。
三、三维目标分析1、知识与技能正确理解价层电子对互斥理论;学会计算分子或离子的孤电子对数(=(a-xb)÷2);能用VSEPR模型推测简单分子或离子的立体结构。
2、过程与方法通过对典型分子立体结构的探究过程,学会运用观察、比较、归纳等方法对信息进行加工,提高科学探究能力;通过推导分子的立体构型,培养学生空间想象能力。
3、情感态度与价值观培养学生独立思考的精神和严谨细致的科学态度;提高用数学的思想解决化学问题的计算能力;通过PPT和模型展示分子的立体结构,激发学生学习化学的兴趣,感受化学世界的奇妙。
四、重难点分析重点:分子的立体构型;价层电子对互斥理论;孤电子对数的计算;VSEPR 模型和分子模型的差别。
难点:价层电子对互斥理论;VSEPR模型和分子模型的差别。
五、教法学法分析教法是模型实物展示、探究式教学法、多媒体教学、讲授法、图表法、举例子。
新人教版高二化学选修3:分子的立体结构(第3课时)教案 Word版

第三課時教學目標1、配位鍵、配位化合物的概念2、配位鍵、配位化合物的表示方法3、採用圖表、比較、討論、歸納、綜合的方法進行教學4、培養學生分析、歸納、綜合的能力教學重點配位鍵、配位化合物的概念教學難點配位鍵、配位化合物的概念教學過程[創設問題情景]什麼是配位鍵?配位鍵如何表示?配位化合物的概念?學生閱讀教材,然後討論交流。
1、配位鍵⑴概念共用電子對由一個原子單方向提供給另一原子共用所形成的共價鍵。
⑵表示A B電子對給予體電子對接受體⑶條件:其中一個原子必須提供孤對電子。
另一原子必須能接受孤對電子軌道。
[提問]舉出含有配位鍵的離子或分子舉例:H3O+NH4+[過渡]什麼是配位化合物呢?[講解]金屬離子或原子與某些分子或離子以配位鍵結合而形成的化合物稱為配合物。
[過渡]配位化合物如何命名?[講解] 硫酸四氨合銅[學生練習命名][Cu(NH3)4]Cl2K3[Fe(SCN)6]Na3[AlF6][小結]本節主要講述了配位鍵和配位化合物。
[練習]1、銨根離子中存在的化學鍵類型按離子鍵、共價鍵和配位鍵分類,應含有A、離子鍵和共價鍵B、離子鍵和配位鍵C、配位鍵和共價鍵D、離子鍵2、下列屬於配合物的是A、NH4ClB、Na2CO3.10H2OC、CuSO4. 5H2OD、Co(NH3)6Cl33、下列分子或離子中,能提供孤對電子與某些金屬離子形成配位鍵的是①H2O ②NH3③F—④CN—⑤COA、①②B、①②③C、①②④D、①②③④⑤4、配合物在許多方面有著廣泛的應用。
下列敘述不正確的是A、以Mg2+為中心的大環配合物葉綠素能催化光合作用。
B、Fe2+的卟啉配合物是輸送O2的血紅素。
C、[Ag(NH3)2]+是化學鍍銀的有效成分。
D、向溶液中逐滴加入氨水,可除去硫酸鋅溶液中的Cu2+。
5.下列微粒:①H3O+②NH4+③CH3COO-④ NH3⑤CH4中含有配位鍵的是A、①②B、①③C、④⑤D、②④6.亞硝酸根NO2-作為配體,有兩種方式。
高中化学教学课例《化学人教版选修32.2分子的立体构型》课程思政核心素养教学设计及总结反思

态。
尊重、理解、关注、赏识”的新型师生关系,课堂教学
才能在和谐愉悦课堂氛围实现有效,甚至是高效。
引入:PPT 展示常见分子和离子的球棍模型。
提问:什么是分子的立体模型?原子数相同的分子 教学过程
为什么构型不同?(抛出问题,让学生产生认知冲突,
产生求知的欲望和探究的兴趣。)
提示:上节课所讲分子的构型和键参数有关。但并 非决定性因素。尝试根据球棍模型或比例模型,写出上 述分子和离子的电子式、结构式。
引出:价层电子对互斥理论(VSEPR):分子的立 体构型是“价层电子对”相互排斥的结果。
(抛出重点。) 公式:价层电子对=孤电子对+σ 键电子对;孤电 子对=(a-xb)÷2。 (注意:阴阳离子的算法。对于阳离子:a 为中心 原子的最外层电子数减去离子的电荷数;对于阴离子: a 为中心原子的最外层电子数加上离子的电荷数) (解决重点。) (PPT+板书)列表格,举例子,详解析,做练习。 (在这个环节,将突破本节课的重点,解决难点,
趣,感受化学世界的奇妙。
本节知识属于化学理论教学和已有知识关联度较
少,通过设计引导希望尽可能取得较好的教学效果。虽
然学生已初步了解分子和离子的电子式、结构式,以及 学生学习能
性质和结构的关系,但学生对分子和离子的空间立体构 力分析
型还没有形成正确的深入理解,另一方面学生的空间想
象思维略弱,相关知识的准确度把握不够,在教学过程
进一步为后面学习晶体及其在生活中的应用埋下铺垫。 教材分析
所以本节内容至关重要。
重点:分子的立体构型;价层电子对互斥理论;孤
电子对数的计算;VSEPR 模型和分子模型的差别。
难点:价层电子对互斥理论;VSEPR 模型和分子模
新人教版高二化学选修3:分子的立体结构(第2课时)教案 Word版

第二課時教學目標1、認識雜化軌道理論的要點2、進一步瞭解有機化合物中碳的成鍵特徵3、能根據雜化軌道理論判斷簡單分子或離子的構型4、採用圖表、比較、討論、歸納、綜合的方法進行教學5、培養學生分析、歸納、綜合的能力和空間想像能力教學重點:雜化軌道理論的要點教學難點:分子的立體結構,雜化軌道理論教學過程:碳的價電子構型是什麼樣的?甲烷的分子模型表明是空間正四面體,分子中的C—H鍵是等同的,鍵角是109°28′。
說明什麼?[結論]碳原子具有四個完全相同的軌道與四個氫原子的電子雲重疊成鍵。
師:碳原子的價電子構型2s22p2,是由一個2s軌道和三個2p軌道組成的,為什麼有這四個相同的軌道呢?為了解釋這個構型Pauling提出了雜化軌道理論。
板書:三、雜化軌道理論1、雜化的概念:在形成多原子分子的過程中,中心原子的若干能量相近的原子軌道重新組合,形成一組新的軌道,這個過程叫做軌道的雜化,產生的新軌道叫雜化軌道。
[思考與交流]甲烷分子的軌道是如何形成的呢?形成甲烷分子時,中心原子的2s和2p x,2p y,2p z等四條原子軌道發生雜化,形成一組新的軌道,即四條sp3雜化軌道,這些sp3雜化軌道不同於s軌道,也不同於p 軌道。
根據參與雜化的s軌道與p軌道的數目,除了有sp3雜化軌道外,還有sp2雜化和sp雜化,sp2雜化軌道表示由一個s軌道與兩個p軌道雜化形成的,sp雜化軌道表示由一個s軌道與一個p軌道雜化形成的。
[討論交流]:[總結評價]:引導學生分析、歸納、總結多原子分子立體結構的判斷規律,完成下[討論]:怎樣判斷有幾個軌道參與了雜化?(提示:原子個數)[結論]:中心原子的孤對電子對數與相連的其他原子數之和,就是雜化軌道數。
[討論總結]:三種雜化軌道的軌道形狀,SP雜化夾角為180°的直線型雜化軌道,SP2雜化軌道為120°的平面三角形,SP3雜化軌道為109°28′的正四面體構型。
2021年新人教版高二化学选修3:2.2分子的立体结构(第1课时)教案 Word版

第二节分子的立体结构榜首课时教育方针:1、知道共价分子的多样性和复杂性;2、开始知道价层电子对互斥模型;3、能用VSEPR模型猜测简略分子或离子的立体结构;4、培育学生谨慎仔细的科学态度和空间幻想才能。
重点难点:分子的立体结构;使用价层电子对互斥模型猜测分子的立体结构教育进程创设问题情境:1、阅览讲义P37-40内容;2、展现CO2、H2O、NH3、CH2O、CH4分子的球辊模型(或份额模型);3、提出问题:⑴什么是分子的空间结构?⑵相同三原子分子CO2和H2O,四原子分子NH3和CH2O,为什么它们的空间结构不同?[评论沟通]1、写出CO2、H2O、NH3、CH2O、CH4的电子式和结构式;2、评论H、C、N、O原子别离能够构成几个共价键;3、依据电子式、结构式描绘CO2、H2O、NH3、CH2O、CH4的分子结构。
[模型探求]由CO2、H2O、NH3、CH2O、CH4的球辊模型,剖析结构不同的原因。
[引导沟通]引导学生得出因为中心原子的孤对电子占有必定的空间,对其他成键电子对存在排挤力,影响其分子的空间结构。
——引出价层电子对互斥模型(VSEPR models)[解说剖析] 价层电子对互斥模型把分子分红两大类:一类是中心原子上的价电子都用于构成共价键。
如CO2、CH2O、CH4等分子中的C原子。
它们的立体结构可用中心原子周围的原子数来猜测,概括如下:ABn 立体结构典范n=2 直线型CO2n=3 平面三角形CH2On=4 正四面体型CH4另一类是中心原子上有孤对电子(未用于构成共价键的电子对)的分子。
如H2O和NH3中心原子上的孤对电子也要占有中心原子周围的空间,并参加相互排挤。
因此H2O分子呈V型,NH3分子呈三角锥型。
(如图)讲义P40。
[使用反应]使用VSEPR理论判别下表中分子或离子的构型。
进一步知道多原子分子的立体结构。
化学式中心原子含有孤对电子对数中心原子结合的原子数空间构型H2S 2 2 V形NH2- 2 2 V形BF30 3 正三角形CHCl30 4 四面体SiF40 4 正四面体[操练]:1、下列物质中,分子的立体结构与水分子类似的是A、CO2B、H2SC、PCl3D、SiCl42、下列分子的立体结构,其间归于直线型分子的是A、H2OB、CO2C、C2H2D、P43、写出你所知道的分子具有以下形状的物质的化学式,并指出它们分子中的键角别离是多少?①直线形②平面三角形③三角锥形④正四面体4、下列分子中,各原子均处于同一平面上的是A、NH3B、CCl4C、H2OD、CH2O5、下列分子的结构中,原子的最外层电子不都满意8电子安稳结构的是A、CO2B、PCl3C、CCl4D、NO26、下列分子或离子的中心原子,带有一对孤对电子的是A、XeO4B、BeCl2C、CH4D、PCl37、为了解说和猜测分子的空间构型,科学家在概括了许多已知的分子空间构型的基础上,提出了一种非常简略的理论模型——价层电子对互斥模型。
2021年高二人教版化学选修三教案集:2.2分子的立体结构(第3课时)

其次节分子的立体结构(第三课时)教学目标:1、配位键、配位化合物的概念2、配位键、配位化合物的表示方法3、接受图表、比较、争辩、归纳、综合的方法进行教学4、培育同学分析、归纳、综合的力气教学重点:配位键、配位化合物的概念教学难点:配位键、配位化合物的概念课前预习1、配位键:2、配位化合物(简称):学习过程[创设问题情景]什么是配位键?配位键如何表示?配位化合物的概念?阅读教材,争辩沟通。
1、配位键(1)概念(2)表示(3)条件:[提问]举出含有配位键的离子或分子举例:[过渡]什么是配位化合物呢?[讲解]金属离子或原子与某些分子或离子以配位键结合而形成的化合物称为协作物。
[小结]本节主要叙述了配位键和配位化合物。
【案例练习】1、在[Cu(NH3)4]2+配离子中NH3与中心离子Cu2+结合的化学键是A.离子键 B.非极性键 C.极性键 D.配位键2、与人体血液中血红蛋白以配位键结合的一种有毒气体是A.氯气 B.氮气 C.一氧化碳 D.甲烷3、向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,连续添加氨水,难溶物溶解得到深蓝色的透亮溶液。
下列对此现象说法正确的是A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变。
B.沉淀溶解后,将生成深蓝色的协作离子[Cu(NH3)4] 2+。
C.向反应后的溶液加入乙醇,溶液将会没有发生变化,由于[Cu(NH3)4] 2+不会与乙醇发生反应。
D.在[Cu(NH3)4] 2+离子中,Cu2+给出孤对电子,NH3供应空轨道。
4、下列属于协作物的是()A、NH4ClB、Na2CO3﹒10H2OC、CuSO4﹒5H2OD、Co(NH3)6Cl 3【课后作业】1、在AgNO3溶液中加入过量的氨水,先有沉淀,后沉淀溶解,沉淀溶解的缘由是形成了()A.AgNO3 B.[Ag(NH3)2]+ C.NH3·H2O D.NH4NO32、如图是卟啉协作物叶绿素的结构示意图(部分),有关的叙述正确的是()A.该叶绿素含有H、Mg、C、N元素 B.该叶绿素是协作物,中心离子是镁离子C.该叶绿素是协作物,其配体是N元素 D.该叶绿素不是协作物,而是高分子化合物3、对盐类物质可有下列分类:如氯化硝酸钙[Ca(NO3)Cl]是一种混盐,硫酸铝钾KAl(SO4)2是一种复盐,冰晶石(六氟合铝酸钠)Na3AlF6是一种络盐。
选修三 第二章 第2节 分子的立体结构 教案

第二节分子的立体结构第一课时教学目标:1.会判断一些典型分子的立体结构,认识分子结构的多样性和复杂性,理解价层电子对互斥模型。
2.通过对典型分子立体结构探究过程,学会运用观察、比较、分类及归纳等方法对信息进行加工,提高科学探究能力。
3.通过观察分子的立体结构,激发学习化学的兴趣,感受化学世界的奇妙。
教学重点:价层电子对互斥模型教学难点:能用价层电子对互斥模型解释分子的立体结构教学过程:【归纳】原子不同,可形成的电子对数目不同,共价键的饱和性不同【板演】写出CO2、H2O、NH3、CH2O、CH4的电子式和结构式;根据电子式、结构式描述CO2、H2O、NH3、CH2O、CH4的成键情况.分析分子内的原子总数、孤对电子数及空间结构。
分子CO2H2O NH3CH2O CH4电子式结构式O=C=O H-O-H原子总数33445孤对电子无21无无空间结构直线型V型三角锥形平面三角形正四面体发挥学生的主观能动性,强化学生对常见分子空间结构的了解和记忆【归纳】含有同种原子的分子,因为原子形成的键角不同,结构不同自主探究分析归纳【归纳小结】分子结构多样性的小结归纳完成环节释分子的空间构型?2、什么是价层电子对?对于ABn 型分子如何计算价层电子对数?3、什么是VSEPR模型?如何确定分子的VSEPR模型与空间构型?【归纳资料】分子CO2H2O NH3CH2O CH4分子内原子总数33445中心原子孤对电子数无21无无空间结构直线型V型三角锥形平面三角形正四面体【板书】二、价层电子对互斥理论1、价层电子对互斥理论:分子的立体构型是“价层电子对”相互排斥的结果。
讨论,归纳,回答归纳强调重点内容,加深学生印象3、VSEPR模型:【启发思考】如何应用价层电子对数确定VSEPR模型及空间构型?【归纳】对于ABn型分子,分子的构型同电子对数目和类型的关系归纳为:【教师活动】投影,引导观察【学生活动】观察,讨论,动手创建模型,思考归纳。
2021年新人教版高二化学选修3:2.2分子的立体结构(第3课时)教案 Word版

第三课时教育方针1、配位键、配位化合物的概念2、配位键、配位化合物的表明办法3、选用图表、比较、评论、概括、概括的办法进行教育4、培育学生剖析、概括、概括的才能教育要点配位键、配位化合物的概念教育难点配位键、配位化合物的概念教育进程[创设问题情形]什么是配位键?配位键怎么表明?配位化合物的概念?学生阅览教材,然后评论沟通。
1、配位键⑴概念共用电子对由一个原子单方向供给给另一原子共用所构成的共价键。
⑵表明A B电子对给予体电子对承受体⑶条件:其间一个原子有必要供给孤对电子。
另一原子有必要能承受孤对电子轨迹。
[发问]举出含有配位键的离子或分子举例:H3O+NH4+[过渡]什么是配位化合物呢?[解说]金属离子或原子与某些分子或离子以配位键结合而构成的化合物称为合作物。
[过渡]配位化合物怎么命名?[解说] 硫酸四氨合铜[学生操练命名][Cu(NH3)4]Cl2K3[Fe(SCN)6]Na3[AlF6][小结]本节首要叙说了配位键和配位化合物。
[操练]1、铵根离子中存在的化学键类型按离子键、共价键和配位键分类,应含有A、离子键和共价键B、离子键和配位键C、配位键和共价键D、离子键2、下列归于合作物的是A、NH4ClB、Na2CO3.10H2OC、CuSO4. 5H2OD、Co(NH3)6Cl33、下列分子或离子中,能供给孤对电子与某些金属离子构成配位键的是①H2O ②NH3③F—④CN—⑤COA、①②B、① ②③C、①②④D、①②③④⑤4、合作物在许多方面有着广泛的使用。
下列叙说不正确的是A、以Mg2+为中心的大环合作物叶绿素能催化光合作用。
B、Fe2+的卟啉合作物是运送O2的血红素。
C、[Ag(NH3)2]+是化学镀银的有效成分。
D、向溶液中逐滴参加氨水,可除掉硫酸锌溶液中的Cu2+。
5.下列微粒:①H3O+②NH4+③CH3COO-④ NH3⑤CH4中含有配位键的是A、①②B、①③C、④⑤D、②④6.亚硝酸根NO2-作为配体,有两种方法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
分子的立体结构第一课时教学目标1、认识共价分子的多样性和复杂性;2、初步认识价层电子对互斥模型;3、能用VSEPR模型预测简单分子或离子的立体结构;4、培养学生严谨认真的科学态度和空间想象能力。
重点难点分子的立体结构;利用价层电子对互斥模型预测分子的立体结构教学过程创设问题情境:1、阅读课本P37-40内容;2、展示CO2、H2O、NH3、CH2O、CH4分子的球辊模型(或比例模型);3、提出问题:⑴什么是分子的空间结构?⑵同样三原子分子CO2和H2O,四原子分子NH3和CH2O,为什么它们的空间结构不同?[讨论交流]1、写出CO2、H2O、NH3、CH2O、CH4的电子式和结构式;2、讨论H、C、N、O原子分别可以形成几个共价键;3、根据电子式、结构式描述CO2、H2O、NH3、CH2O、CH4的分子结构。
[模型探究]由CO2、H2O、NH3、CH2O、CH4的球辊模型,对照其电子式云哟内分类对比的方法,分析结构不同的原因。
[引导交流]引导学生得出由于中心原子的孤对电子占有一定的空间,对其他成键电子对存在排斥力,影响其分子的空间结构。
——引出价层电子对互斥模型(VSEPR models)[讲解分析] 价层电子对互斥模型把分子分成两大类:一类是中心原子上的价电子都用于形成共价键。
如CO2、CH2O、CH4等分子中的C原子。
它们的立体结构可用中心原子周围的原子数来预测,概括如下:另一类是中心原子上有孤对电子(未用于形成共价键的电子对)的分子。
如H2O和NH3中心原子上的孤对电子也要占据中心原子周围的空间,并参与互相排斥。
因而H2O 分子呈V型,NH3分子呈三角锥型。
(如图)课本P40。
[应用反馈]应用VSEPR理论判断下表中分子或离子的构型。
进一步认识多原子分子的立体结构。
补充练习:1、下列物质中,分子的立体结构与水分子相似的是 ( )A、CO2B、H2SC、PCl3D、SiCl42、下列分子的立体结构,其中属于直线型分子的是 ( )A、H2OB、CO2C、C2H2D、P43、写出你所知道的分子具有以下形状的物质的化学式,并指出它们分子中的键角分别是多少?(1)直线形(2)平面三角形(3)三角锥形(4)正四面体4、下列分子中,各原子均处于同一平面上的是 ( )A、NH3B、CCl4C、H2OD、CH2O5、下列分子的结构中,原子的最外层电子不都满足8电子稳定结构的是( )A、CO2B、PCl3C、CCl4D、NO26、下列分子或离子的中心原子,带有一对孤对电子的是 ( )A、XeO4B、BeCl2C、CH4D、PCl37、为了解释和预测分子的空间构型,科学家在归纳了许多已知的分子空间构型的基础上,提出了一种十分简单的理论模型——价层电子对互斥模型。
这种模型把分子分成两类:一类是;另一类是。
BF3和NF3都是四个原子的分子,BF3的中心原子是,NF3的中心原子是;BF3分子的立体构型是平面三角形,而NF3分子的立体构型是三角锥形的原因是。
8、用价层电子对互斥模型推测下列分子或离子的空间构型。
BeCl2;SCl2;SO32-;SF6参考答案:1、D2、BC3、(1)CO2、CS2、HCN 键角180°(2)BF3、BCl3、SO3、CH2O键角60°(3)NH3、PCl3键角107.3°(4)CH4、CCl4键角109°28′4、CD5、D6、D7、中心原子上的价电子都用于形成共价键中心原子上有孤对电子 B N BF3分子中B原子的3个价电子都与F原子形成共价键,而NF3分子中N原子的3个价电子与F原子形成共价键,还有一对为成键的电子对,占据了N原子周围的空间,参与相互排斥,形成三角锥形8、直线形 V形三角锥正八面体第二章分子结构与性质第二节分子的立体结构第2课时教学目标1.认识杂化轨道理论的要点2.进一步了解有机化合物中碳的成键特征3.能根据杂化轨道理论判断简单分子或离子的构型4.采用图表、比较、讨论、归纳、综合的方法进行教学5.培养学生分析、归纳、综合的能力和空间想象能力教学重点杂化轨道理论的要点教学难点分子的立体结构,杂化轨道理论[展示甲烷的分子模型][创设问题情景]碳的价电子构型是什么样的?甲烷的分子模型表明是空间正四面体,分子中的C—H键是等同的,键角是109°28′。
说明什么?[结论]碳原子具有四个完全相同的轨道与四个氢原子的电子云重叠成键。
师:碳原子的价电子构型2s22p2,是由一个2s轨道和三个2p轨道组成的,为什么有这四个相同的轨道呢?为了解释这个构型Pauling提出了杂化轨道理论。
板:三、杂化轨道理论1、杂化的概念:在形成多原子分子的过程中,中心原子的若干能量相近的原子轨道重新组合,形成一组新的轨道,这个过程叫做轨道的杂化,产生的新轨道叫杂化轨道。
[思考与交流]甲烷分子的轨道是如何形成的呢?形成甲烷分子时,中心原子的2s和2p x,2p y,2p z等四条原子轨道发生杂化,形成一组新的轨道,即四条sp3杂化轨道,这些sp3杂化轨道不同于s轨道,也不同于p轨道。
根据参与杂化的s轨道与p轨道的数目,除了有sp3杂化轨道外,还有sp2杂化和sp杂化,sp2杂化轨道表示由一个s轨道与两个p轨道杂化形成的,sp杂化轨道表示由一个s轨道与一个p轨道杂化形成的。
[讨论交流]:应用轨道杂化理论,探究分子的立体结构。
[总结评价]:引导学生分析、归纳、总结多原子分子立体结构的判断规律,完成下表。
[讨论]:怎样判断有几个轨道参与了杂化?(提示:原子个数)[结论]:中心原子的孤对电子对数与相连的其他原子数之和,就是杂化轨道数。
[讨论总结]:三种杂化轨道的轨道形状,SP杂化夹角为180°的直线型杂化轨道,SP2杂化轨道为120°的平面三角形,SP3杂化轨道为109°28′的正四面体构型。
[科学探究]:课本42页[小结]:HCN中C原子以sp杂化,CH2O中C原子以sp2杂化;HCN中含有2个σ键和2π键;CH2O中含有3σ键和1个π键补充练习:1、下列分子中心原子是sp2杂化的是( )A PBr3B CH4C BF3D H2O2、关于原子轨道的说法正确的是( )A 凡是中心原子采取sp3杂化轨道成键的分子其几何构型都是正四面体B CH4分子中的sp3杂化轨道是由4个H原子的1s 轨道和C原子的2p轨道混合起来而形成的C sp3杂化轨道是由同一个原子中能量相近的s 轨道和p轨道混合起来形成的一组能量相近的新轨道D 凡AB3型的共价化合物,其中中心原子A均采用sp3杂化轨道成键3、用Pauling的杂化轨道理论解释甲烷分子的四面体结构,下列说法不正确的是( )A、C原子的四个杂化轨道的能量一样B、C原子的sp3杂化轨道之间夹角一样C、C原子的4个价电子分别占据4个sp3杂化轨道D、C原子有1个sp3杂化轨道由孤对电子占据4、下列对sp3、sp2、sp杂化轨道的夹角的比较,得出结论正确的是( )A sp杂化轨道的夹角最大B sp2杂化轨道的夹角最大C sp3杂化轨道的夹角最大D sp3、sp2、sp杂化轨道的夹角相等5、乙烯分子中含有4个C—H和1个C=C双键,6个原子在同一平面上。
下列关于乙烯分子的成键情况分析正确的是( )A 每个C原子的2s轨道与2p轨道杂化,形成两个sp杂化轨道B 每个C原子的1个2s轨道与2个2p轨道杂化,形成3个sp2杂化轨道C 每个C原子的2s轨道与3个2p轨道杂化,形成4个sp3杂化轨道D 每个C原子的3个价电子占据3个杂化轨道,1个价电子占据1个2p轨道6、ClO-、ClO2-、ClO3-、ClO4-中Cl都是以sp3杂化轨道与O原子成键的,试推测下列微粒的立体结构7、根据杂化轨道理论,请预测下列分子或离子的几何构型:CO2, CO32-H2S , PH38、为什么H2O分子的键角既不是90°也不是109°28′而是104.5°?参考答案:1~5 C C D A BD6、直线;V型;三角锥形;正四面体7、sp杂化,直线;sp2杂化,三角形;sp3杂化,V型;sp3杂化,三角锥形8、因为H2O分子中中心原子不是单纯用2p轨道与H原子轨道成键,所以键角不是90°;O 原子在成键的同时进行了sp3杂化,用其中2个含未成对电子的杂化轨道与2个H原子的1s 轨道成键,2个含孤对电子的杂化轨道对成键电子对的排斥的结果使键角不是109°28′,而是104.5°。
第二章分子结构与性质第二节分子的立体结构第三课时教学目标4.配位键、配位化合物的概念5.配位键、配位化合物的表示方法3.采用图表、比较、讨论、归纳、综合的方法进行教学4.培养学生分析、归纳、综合的能力教学重点配位键、配位化合物的概念教学难点配位键、配位化合物的概念教学过程[创设问题情景]什么是配位键?配位键如何表示?配位化合物的概念?学生阅读教材,然后讨论交流。
1、配位键(1)概念共用电子对由一个原子单方向提供给另一原子共用所形成的共价键。
(2)表示A B电子对给予体电子对接受体(3)条件:其中一个原子必须提供孤对电子。
另一原子必须能接受孤对电子轨道。
[提问]举出含有配位键的离子或分子举例:H3O+NH4+[过渡]什么是配位化合物呢?[讲解]金属离子或原子与某些分子或离子以配位键结合而形成的化合物称为配合物。
[过渡]配位化合物如何命名?[讲解] 硫酸四氨合铜[学生练习命名][Cu(NH3)4]Cl2K3[Fe(SCN)6]Na3[AlF6][小结]本节主要讲述了配位键和配位化合物。
[练习]1、铵根离子中存在的化学键类型按离子键、共价键和配位键分类,应含有( )A、离子键和共价键B、离子键和配位键C、配位键和共价键D、离子键2、下列属于配合物的是( )A、NH4ClB、Na2CO3.10H2OC、CuSO4. 5H2OD、Co(NH3)6Cl33、下列分子或离子中,能提供孤对电子与某些金属离子形成配位键的是 ( )①H2O ②NH3③F—④CN—⑤COA、①②B、①②③C、①②④D、①②③④⑤4、配合物在许多方面有着广泛的应用。
下列叙述不正确的是 ( )A、以Mg2+为中心的大环配合物叶绿素能催化光合作用。
B、Fe2+的卟啉配合物是输送O2的血红素。
C、[Ag(NH3)2]+是化学镀银的有效成分。
D、向溶液中逐滴加入氨水,可除去硫酸锌溶液中的Cu2+。
5.下列微粒:①H3O+②NH4+③CH3COO-④ NH3⑤CH4中含有配位键的是( )A、①②B、①③C、④⑤D、②④6.亚硝酸根NO2-作为配体,有两种方式。
其一是氮原子提供孤对电子与中心原子配位;另一是氧原子提供孤对电子与中心原子配位。
