雷帕霉素
雷帕霉素Rapamycin又名Sirolimus

雷帕霉素Rapamycin又名Sirolimus
又称雷帕霉素(rapamycin),雷帕霉素(RAPA)是一种新型大环内酯类免疫抑制剂,为白色固体结晶,分子式为C51H79NO13,分子量991?914.18,熔点为183-185℃,亲脂性,溶解于甲醇、乙醇、丙酮、氯仿等有机溶剂,极微溶于水,几乎不溶于乙醚。
是一种疗效好,低毒,无肾毒性的新型免疫抑制剂。
用于治疗阿尔茨海默症(老年性痴呆)。
令他们颇感兴趣的是,雷帕霉素的主要成分也存在于复活岛隔离土壤中的细菌产物。
与普乐可复(FK506)的结构相似,但却有非常不同的免疫抑制机制。
密度:1.182 G/CM3,沸点:973.017°C,闪点:542.261°C,折射率:1.55,蒸汽压:0mmHg,【不相容性】强氧化剂。
储存温度:-20°C。
雷帕(合成)反应的

雷帕(合成)反应
雷帕霉素合成反应是一种复杂的微生物发酵过程,主要由放线菌雷帕霉菌(Streptomyces hygroscopicus)完成。
这个过程涉及到多个步骤和酶的催化作用,最终生成雷帕霉素(Rapamycin),这是一种具有免疫抑制作用的大环内酯类抗生素。
首先,雷帕霉素的生物合成开始于一系列的前体物质,这些物质通过放线菌的代谢途径生成。
这些前体物质包括多种氨基酸、脂肪酸和糖类,它们是雷帕霉素合成所需的基本构建块。
接着,这些前体物质进入雷帕霉素的生物合成途径,在一系列酶的催化作用下,经过缩合、氧化、环化等一系列化学反应,逐步转化成雷帕霉素的核心结构——一个包含21个碳原子的大环内酯环。
然后,这个大环内酯环上会进一步连接上其他的官能团,如羟基、酮基等,形成雷帕霉素分子的完整结构。
这些反应同样需要特定的酶来催化。
最后,经过修饰和修饰后的雷帕霉素分子会在细胞内积累,并通过发酵培养液被提取出来。
提取后的雷帕霉素需要经过纯化处理,以去除杂质,确保药物的质量和安全性。
整个雷帕霉素的合成过程是高度复杂的,涉及到许多基因和酶的协同工作。
近年来,随着基因组学和代谢工程的发展,研究者们已经开始解析雷帕霉素生物合成途径中的关键酶和调控机制,以期提高雷帕霉素的产量和降低生产成本。
通过基因编辑技术,可以对雷帕霉菌的代谢途径进行优化,从而实现更高效的雷帕霉素生产。
雷帕霉素通过下调Th17细胞调节性T细胞比值减轻实验性自身免疫性重症肌无力大鼠症状

24细胞与分子免疫学杂志(Chin J Cell M ol丨m m un〇l)2021 , 37( 1) .论著•文章编号:1007-8738(2021 )014)024>07雷帕霉素通过下调T h l7细胞/调节性T细胞比值减轻实验性自身免疫性重症肌无力大鼠症状高鑫雷\文玉军2,王钊\王国玮、郭加雨、余黎明、王振海3*C宁夏医科大学,2宁夏颅脑疾病重点实验室,3宁夏医科大学总医院神经内科,宁夏银川750004)[摘要]目的初步研究雷帕霉素(RAPA)对实验性自身免疫性重症肌无力(EAM G)大鼠的治疗作用,并研究相关免疫机制。
方法应用鼠源性乙酰胆碱受体a亚基97 ~ 116肽段(R97-116)免疫Lewis大鼠,建立EAMG动物模型,随机分为完全F reund 佐剂对照组(CFA组)、EAMG模型对照组、RAPA处理组[1 mg/(kg •d)]。
采用Lennon肌力评分量表隔日评估各组大鼠临床 症状并记录体质量,EUSA检测大鼠外周血中抗R97-116抗体水平。
制备脾细胞悬液,流式细胞术检测大鼠脾脏Thl7细胞、调节性T细胞(Treg)的数量;分别给予5 (jig/mL伴刀豆球蛋白A(ConA)、10 pg/mLIW-lW、R PM I1640培养液处理,C C K4法检 测大鼠脾脏细胞的增殖活性。
结果RAPA治疗可明显改善EAMG大鼠体质量及临床评分,与CFA组相比,EAMG组大鼠脾脏 Thl7细胞数量增加,Treg数量降低;与EAMG组相比,RAPA处理的大鼠脾脏Thl7细胞数量明显减少,Treg数量升高,血清中 抗R97-116抗体水平降低。
RAPA处理抑制R PM I1640、R97-116、ConA刺激引起的淋巴细胞增殖c结论RAPA可能通过下调 Thl7细胞/Treg比值,减轻EAMG大鼠的临床症状。
[关键词]实验性自身免疫性重症肌无力(EAM G);雷帕霉素(RAPA); Thl7细胞;调节性T细胞(Treg)[中图分类号]R746.1,R392.12, Q253 [文献标志码]ARapamycin alleviates the symptoms of experimental autoimmune myasthenia gravis rats by down-regulating Thl7 cell/regulatory T cell ratioGAO Xinlei1, WEN Yujun2, WANG Zhao1, WANG Guowei1, GUO Jiayu', YU Liming1, WANG Zhenhai3*1Ningxia M edical University,2Ningxia K ey L ab oratory of C erebrocranial Diseases,3D epartm ent of Neurology,G eneral H ospital of N ingxia M edical University,Yinchuan750004, C hina* C orresponding author,E-mail:139****9189@[A b s t r a c t]Objective To study the therapeutic effect of rapamycin (RAPA) on experimental autoimmune myasthenia gravis (E A M G) rats and to explore the related immune mechanisms. Methods The mouse-derived acetylcholine receptor alpha subunit 97-116 peptide (R97-116) was used to immunize Lewis rats to establish an EAMG rat model. The rats were randomly divided into three groups:complete F re u n d^adjuvant control group (C F A g ro u p), EAMG model control group, and RAPA treatment group [1 m g/(k g•d) ]■ The Lennon muscle strength scoring scale was used to evaluate rats’ clinical symptoms in each group once every two days, and their body mass was recorded. ELISA was performed to detect the level of ant卜R97-116 antibodies in the peripheral blood of rats. Flow cytometry was used to detect the numbers of Thl7 cells and regulatory T cells (T re g s) in rat splenocytes. Splenocytes were stimulated with 5 [ig/mL concanavalin A (C o n A), 10 pg/mL R97-116 and RPMI1640 medium, and the proliferation activity of rat splenocytes was tested by CCK-8 assay. Results RAPA treatment significantly improved the body mass and clinical scores in EAMG rats. Compared with the CFA group, the number of T hl7 cells in the spleen of the EAMG group increased, and the number of Tregs decreased. Compared with the EAMG group, the number of T h l7 cells in the spleen of RAPA-treated rats significantly dropped, the number of Tregs went up, and the level of anti-R97-116 antibodies in the serum went down. RAPA treatment inhibited the proliferation of lymphocytes induced by RPMI1640 medium, R97-116, and ConA stimulation. Conclusion RAPA may alleviate the clinical symptoms of EAMG rats by down-regulating the ratio of T hl7 cells/Tregs.[K e y words] experimental autoimmune myasthenia gravis;rapamycin;T hl7 cells;regulatory T cells (Treg s)收稿日期:2020«08-28;接受日期:2020-11 -26基金项目:2018年宁夏科技重点研发计划重大项目(2018BFG02017)作者简介:高鑫雷(1991 -),男,陕西榆林人,硕士研究生Tel:187****8874;E-mail:187*****************通讯作者,王振海,E-mail: 139****************1期高鑫雷,等.甫帕g素通过下调Thl7细胞/调节性T细胞比值减轻实验性身免疫性承症肌无力大鼠症状25重症肌无力(m yasthenia gravis,M G)是一种由抗 乙酰胆碱受体(acetylcholine receptor,AChR)抗体介 导、C D4+ T细胞依赖、补体参与的自身免疫性疾病,病理改变为突触后膜AchR破坏,不能产生足够的终 板电位,引起神经肌肉接头传递功能障碍,进而导致骨 豁肌无力和疲劳⑴。
雷帕霉素质量标准

雷帕霉素是一种广谱的抗生素,常用于治疗由细菌感染引起的疾病。
在医药领域,药品的质量标准至关重要,对保证药品的质量、安全和有效性起着至关重要的作用。
下面我们来详细了解一下雷帕霉素的质量标准。
一、雷帕霉素的药品名称和规格雷帕霉素的通用名称为Clarithromycin,商品名多为克拉霉素、巨红霉素等。
其规格包括25mg、50mg、100mg、125mg、200mg、250mg、500mg等。
二、雷帕霉素的外观特征雷帕霉素为白色或类白色结晶性粉末,有时也会呈黄色,无臭或微香气,味苦。
应该是抗生素中比较好认的一种药物,外观上也没有什么特别的要求。
三、雷帕霉素的质量指标1. 雷帕霉素的含量雷帕霉素的含量应在96.0%~102.0%之间,即每个剂量单位内雷帕霉素的质量应在标称质量的96.0%~102.0%之间。
2. 水分含量雷帕霉素的水分含量应不超过5.0%。
水分的含量对药品质量影响较大,如果水分含量过高会导致药品剂量不准确、易于吸湿变质。
3. 重金属含量雷帕霉素的重金属含量应符合国家标准。
重金属污染是制约药品质量的一个重要因素。
重金属过高会导致毒副作用增强。
4. 杂质含量雷帕霉素的杂质含量应符合国家标准。
杂质可能导致药物副作用增加,影响疗效。
5. 不溶性物含量雷帕霉素的不溶性物含量应不超过0.1%。
不溶性物是指在溶液中不能被完全溶解的物质,它可能影响药品的纯度。
四、雷帕霉素的质量检测方法1. 雷帕霉素的含量检测方法雷帕霉素的含量检测通常采用高效液相色谱法(HPLC)、气相色谱法(GC)等方法。
2. 水分含量检测方法雷帕霉素的水分含量检测通常采用干燥法或卡尔费伯法。
3. 重金属含量检测方法雷帕霉素的重金属含量检测通常采用原子吸收光谱法(AAS)、电感耦合等离子体质谱法(ICP-MS)等方法。
4. 杂质含量检测方法雷帕霉素的杂质含量检测通常采用高效液相色谱法(HPLC)、气相色谱法(GC)等方法。
5. 不溶性物含量检测方法雷帕霉素的不溶性物含量检测通常采用过滤法。
雷帕霉素对结节性硬化症合并难治性癫痫的临床疗效和安全性观察

雷帕霉素对结节性硬化症合并难治性癫痫的临床疗效和安全性观察《雷帕霉素对结节性硬化症合并难治性癫痫的临床疗效和安全性观察》引言:结节性硬化症(TSC)是一种常见的遗传性疾病,主要表现为皮肤、中枢神经系统和内脏器官的良性肿瘤的形成。
TSC患者常合并难治性癫痫,给患者生活和生理健康带来严重影响。
雷帕霉素是一种新型的抗癫痫药物,但其在TSC患者中的疗效和安全性还需进一步观察和评估。
材料与方法:选取2024年1月至2024年12月期间,在我院住院治疗并被确诊为TSC合并难治性癫痫的患者120例。
将其随机分为治疗组和对照组,每组各60例。
治疗组患者给予雷帕霉素治疗,对照组患者给予传统的抗癫痫药物治疗。
观察两组患者的临床疗效和安全性。
结果:治疗组患者的癫痫发作次数显著减少,癫痫控制率达到80%以上,而对照组患者的癫痫控制率只有60%。
治疗组的癫痫持续时间明显缩短,癫痫大发作和癫痫持续状态的发生率也较低。
同时,治疗组患者的癫痫相关认知功能也得到改善。
在安全性方面,治疗组和对照组患者的不良反应发生率相似,但治疗组患者的不良反应较轻,没有发生严重不良事件。
讨论:雷帕霉素是一种有效的抗癫痫药物,对TSC合并难治性癫痫的疗效显著。
它可以减少癫痫发作次数,提高癫痫控制率,并改善患者的认知功能。
此外,雷帕霉素在TSC患者中的安全性良好,不良反应较轻。
因此,雷帕霉素在TSC合并难治性癫痫的治疗中具有潜在的临床应用前景。
结论:雷帕霉素对结节性硬化症合并难治性癫痫具有良好的临床疗效和安全性。
它可以有效控制癫痫发作、改善认知功能,并减少不良反应的发生。
进一步的研究还需扩大样本量和延长随访时间,以确保研究结果的可靠性和临床应用的可行性。
雷帕霉素 原理

雷帕霉素原理
雷帕霉素(Rapamycin)是一种新型大环内酯类免疫抑制剂,其原理可能通过阻断IL-2启动的T细胞增殖而选择性抑制T细胞,用于抗移植排斥反应。
雷帕霉素的合成过程涉及多个步骤。
首先,它由七单位的乙酸盐和七单位的丙酸盐通过聚酮途径合成,所需的O-甲基来自于甲硫氨酸。
在氮源时,莽草酸经过还原后形成衍生物,并在从莽草酸形成环己烷衍生物的过程中保留了环己烷基的完整性。
接着,赖氨酸经过脱氨幻化形成羧酸哌啶,再由羧酸哌啶与聚酮乙酰键和酰胺键连接,形成了雷帕霉素的初始结构。
雷帕霉素是一种白色固体结晶,具有亲脂性,可以溶解于甲醇、乙醇、丙酮、氯仿等有机溶剂,但极微溶于水,几乎不溶于乙醚。
它的熔点为183-185℃。
总的来说,雷帕霉素的免疫抑制效果主要是通过对T细胞增殖的抑制作用实现的,其在抗移植排斥反应中的应用就是基于这一原理。
rapamycin促进自噬的原理

rapamycin促进自噬的原理
雷帕霉素(Rapamycin)是一种有效的自噬诱导剂,通过诱导自噬从而减轻炎症反应,可能是其发挥免疫抑制的机制之一。
研究发现,雷帕霉素能抑制70-KDaS6激酶(p70S6K)的活性,该酶与细胞周期中的许多关键的不同细胞过程有密切的关系。
自噬是指细胞通过降解自身成分来提供营养和能量的过程。
通常情况下,细胞内自噬处于一个较低的水平下,以保持内环境稳定。
但是,一旦受到外界条件(如饥饿、低氧、高温等)或内部条件(如损伤等)的刺激,自噬水平会快速上调。
雷帕霉素促进自噬的原理是通过诱导自噬从而减轻炎症反应,这可能是其发挥免疫抑制的机制之一。
国产雷帕霉素与依维莫司或佐他莫司药物洗脱支架治疗冠状动脉左主干开口及体部病变效果比较

国产雷帕霉素与依维莫司或佐他莫司药物洗脱支架治疗冠状动脉左主干开口及体部病变效果比较冠状动脉疾病是一种严重的心脏疾病,常见的治疗方法包括药物治疗和介入手术治疗。
在介入手术治疗中,药物洗脱支架是一种常用的治疗方法,能够明显改善患者的症状和预后。
国产雷帕霉素与依维莫司或佐他莫司药物洗脱支架治疗冠状动脉左主干开口及体部病变效果比较成为当前研究的焦点之一。
雷帕霉素是一种HMG-CoA还原酶抑制剂,能够降低胆固醇水平,减少冠状动脉粥样硬化斑块的形成。
雷帕霉素还能够抑制血小板聚集和减少血栓形成,具有抗血栓作用。
依维莫司和佐他莫司则是一种新型P2Y12受体拮抗剂,可以有效地抑制血小板聚集,减少血栓形成。
这三种药物在治疗冠状动脉疾病中都具有重要的作用。
在介入手术治疗中,药物洗脱支架是一种常用的治疗方法,它可以在支架植入的同时释放药物,防止血管内再度狭窄和血栓形成。
对于冠状动脉左主干开口及体部病变,药物洗脱支架的选择对于疗效具有重要影响。
针对这一问题,国内外的研究人员进行了大量的临床研究和实验研究,希望找到最适合患者的治疗方案。
国产雷帕霉素与依维莫司或佐他莫司药物洗脱支架治疗冠状动脉左主干开口及体部病变效果比较的研究也逐渐成为研究的热点之一。
一项来自中国的临床研究对比了国产雷帕霉素与依维莫司或佐他莫司药物洗脱支架在治疗冠状动脉左主干开口及体部病变患者中的疗效。
该研究纳入了大量患者,并对其进行了长期的随访观察,结果显示,国产雷帕霉素与依维莫司或佐他莫司药物洗脱支架在治疗冠状动脉左主干开口及体部病变中的效果相当,都能够显著改善患者的症状,降低心脏风险。
这一研究结果表明,国产雷帕霉素与依维莫司或佐他莫司药物洗脱支架在治疗冠状动脉左主干开口及体部病变中的疗效是相似的,患者在选择治疗方案时可以根据自身条件和医生建议进行选择。
也提示我们国产药物在治疗冠状动脉疾病中的疗效已经达到了国际水平,具有很高的临床应用价值。
但需要注意的是,以上研究结果仅代表目前的研究成果,具体的治疗方案还需要根据患者自身情况和医生建议进行选择。
雷帕霉素说明书
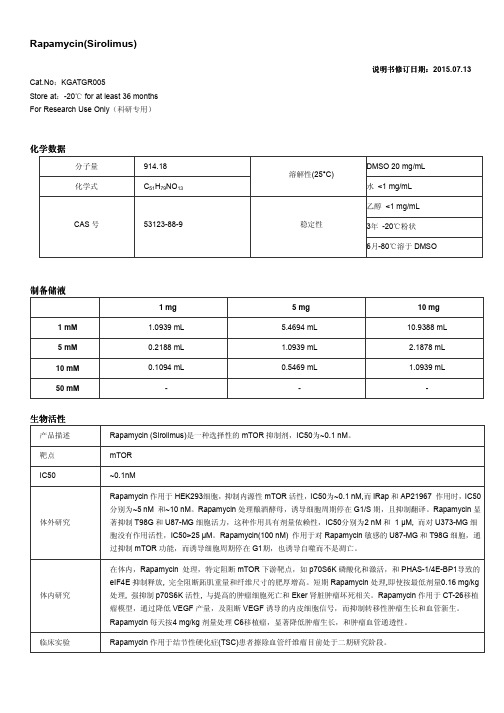
Rapamycin(Sirolimus)说明书修订日期说明书修订日期::2015.07.13Cat.No :KGATGR005Store at :-20 for at least 36 months ℃ For Research Use Only (科研专用)化学数据分子量 914.18DMSO 20 mg/mL化学式C 51H 79NO 13溶解性(25°C)水 <1 mg/mL 乙醇 <1 mg/mL3年 -20℃粉状 CAS 号53123-88-9稳定性6月-80℃溶于DMSO制备储液1 mg 5 mg 10 mg 1 mM 1.0939 mL 5.4694 mL 10.9388 mL 5 mM 0.2188 mL 1.0939 mL 2.1878 mL 10 mM 0.1094 mL0.5469 mL1.0939 mL50 mM---生物活性产品描述 Rapamycin (Sirolimus)是一种选择性的mTOR 抑制剂,IC50为~0.1 nM 。
靶点 mTOR IC50~0.1nM体外研究Rapamycin 作用于HEK293细胞,抑制内源性mTOR 活性,IC50为~0.1 nM,而iRap 和AP21967 作用时,IC50分别为~5 nM 和~10 nM 。
Rapamycin 处理酿酒酵母,诱导细胞周期停在G1/S 期,且抑制翻译。
Rapamycin 显著抑制T98G 和U87-MG 细胞活力,这种作用具有剂量依赖性,IC50分别为2 nM 和 1 µM, 而对U373-MG 细胞没有作用活性,IC50>25 µM 。
Rapamycin(100 nM) 作用于对Rapamycin 敏感的U87-MG 和T98G 细胞,通过抑制mTOR 功能,而诱导细胞周期停在G1期,也诱导自噬而不是凋亡。
体内研究在体内,Rapamycin 处理,特定阻断mTOR 下游靶点,如p70S6K 磷酸化和激活,和PHAS-1/4E-BP1导致的eIF4E 抑制释放, 完全阻断跖肌重量和纤维尺寸的肥厚增高。
雷帕霉素质量标准

雷帕霉素是一种广谱抗生素,用于治疗多种感染症状。
为确保药品的质量和安全性,制定严格的质量标准非常重要。
下面将详细介绍雷帕霉素的质量标准。
一、药品标准名称及含义药品标准名称:雷帕霉素(Repa)含义:本标准规定了雷帕霉素的质量要求、检查方法、试验规范、包装、标志及说明书等内容。
二、外观特征雷帕霉素为白色或类白色结晶粉末,无臭味或微有刺激性气味。
在水中溶解度较小,易溶于甲醇或乙醇,不溶于二氯甲烷。
三、质量指标1.鉴别取样品1mg,加入1mL的甲醇,摇匀后过滤,取上清液作为测试溶液。
将测试溶液扫描于紫外光谱仪中,波长范围为200nm~400nm,与对照品进行比较。
符合要求即可。
2.含量测定用高效液相色谱法(HPLC)进行含量测定,以雷帕霉素标准品作为对照品。
样品与对照品在同一条件下进行检测,计算出样品中雷帕霉素的含量。
3.外观与颗粒度使用显微镜对样品进行观察,并通过筛分测试来确定颗粒度指标是否符合要求。
4.溶解度将样品加入到不同的试剂中,并对其进行搅拌和加热,最后观察是否能够完全溶解。
5.纯度用气相色谱法(GC)或者高效液相色谱法(HPLC)等方法进行纯度检测,确保不含有任何杂质。
四、包装及标志1.包装:常规采用铝箔袋或塑料瓶,根据实际需要进行包装。
2.标志:药品必须明确标注药品名称、规格、生产厂家、生产批号、生产日期、保质期等信息。
此外,还需标注“仅供医院使用”等相关内容。
五、说明书药品说明书应详细描述药品的成分、性状、适应症、用法、用量、注意事项、不良反应等内容,并严格遵守国家有关规定。
总之,制定严格的雷帕霉素质量标准对保障患者用药安全至关重要。
药品生产企业应严格遵守相关规定,确保产品的质量和安全性,为广大患者提供更好的医疗服务。
雷帕霉素的作用与功效

雷帕霉素的作用与功效雷帕霉素是一种广谱抗生素,在临床应用中具有广泛的作用与功效。
本文将详细介绍雷帕霉素的作用、功效以及临床应用方面的相关知识。
一、雷帕霉素的简介雷帕霉素是一种微量青霉素类广谱抗生素,其化学名为6-[(4R,5S,6S,7R,9R,10R,11E,13E,16R)-12-(dimethylamino)-4,10,16-trihydroxy-3,4,9,10-tetraoxo-1-oxacyclohexadeca-11,13-dien-7-yl]-N,N-dimethyl-2,3,6-trideoxy-3-dimethylaminobeta-D-xylo-hexopyranoside,分子式为C58H99N9O13,相对分子质量为1014.6。
二、雷帕霉素的药理作用雷帕霉素具有广谱的抗菌活性,对许多革兰氏阳性和阴性细菌均有抑制作用,并具有抗麻风杆菌和忍耐性CRKP(碳青霉烯耐药幽门螺杆菌)的作用。
1. 抗菌作用雷帕霉素主要通过抑制细菌蛋白质的合成,进而发挥抗菌作用。
其与细菌核糖体上的50S亚基相互作用,阻止肽链的延长,从而抑制了细菌蛋白质的合成,导致细菌的死亡。
2. 抗麻风杆菌作用雷帕霉素可通过阻断麻风杆菌的蛋白质合成来发挥其抗麻风杆菌的作用。
麻风杆菌属于嗜酸性细菌,常侵犯皮肤和周围神经,导致麻风病的发生。
雷帕霉素通过与麻风杆菌的核糖体结合,阻断肽链的延长,抑制蛋白质的合成,从而达到杀菌的效果。
3. 对CRKP的作用CRKP(碳青霉烯耐药幽门螺杆菌)是一种耐药性强的细菌,常导致医院内感染,对临床治疗造成了一定的困扰。
雷帕霉素通过与CRKP的核糖体结合,抑制蛋白质的合成,从而达到抑制CRKP生长的效果。
三、雷帕霉素的临床应用1. 呼吸道感染雷帕霉素可用于治疗各种细菌引起的呼吸道感染,如肺炎、支气管炎等。
它对多种肺炎链球菌、卡他莫拉菌等常见致病菌具有很好的抗菌作用,可以有效控制感染并减轻炎症症状。
超级明星药物雷帕霉素的新作用

超级明星药物雷帕霉素的新作用[导读]移植抗排斥药物雷帕霉素(rapamycin)在一个致命性缺陷小鼠模型中对细胞的线粒体显示出了意外的益处。
罹患Leigh 综合征的儿童表现为进行性脑损伤、肌肉无力、丧失协调或肌肉控制能力,体重减轻,往往死于呼吸衰竭。
移植抗排斥药物雷帕霉素(rapamycin)在一个致命性缺陷小鼠模型中对细胞的线粒体显示出了意外的益处。
罹患 Leigh 综合征的儿童表现为进行性脑损伤、肌肉无力、丧失协调或肌肉控制能力,体重减轻,往往死于呼吸衰竭。
在发表于 11 月 15 日《科学》(Science)杂志上的一篇论文中,华盛顿大学的人员报告称他们发现用雷帕霉素治疗可大大地提高 Leigh 综合征小鼠模型生存,减缓疾病进程。
每天注射一次,这种药物可以延迟神经症状出现,减少大脑炎症,防止脑损害。
Leigh 综合征通常在1岁前得到确诊。
受累患儿很少能活过6岁或7岁。
目前,这一疾病可由几种不同的潜在病因所引起,没有有效的治疗方法。
在大部分生命历程中,治疗小鼠呼吸及运动正常,平均和最长寿命显著延长。
这种疾病小鼠的平均寿命是50天。
相比之下,治疗雄性小鼠平均存活了114天,雌性小鼠平均生活了111天。
治疗组的最长生存期是269天,是未处理动物的三倍以上。
研究的资深作者、华盛顿大学病理学副教授Matt Kaeberlein 博士说:“我们对这些研究结果感到非常兴奋,因为它有可能会影响罹患这一疾病以及相关线粒体病儿童的治疗。
相似的干预策略或许对于广泛的线粒体并或是由线粒体功能障碍导致的其他疾病有用。
”线粒体缺陷会减少细胞的能量利用。
这种能量耗尽可以损害或破坏重要组织。
疾病的症状或严重程度取决于受累的细胞类型,但是在很多情况下,线粒体功能障碍会造成多个器官运转不良。
除了一些特定的线粒体疾病,其中大部分疾病与遗传有关,线粒体功能衰退或障碍也促成了许多常见的健康问题,包括一些形式的心脏病,癌症,以及与衰老相关的肌肉、神经或脑退化。
雷帕霉素高产菌种和生产工艺技术

雷帕霉素高产菌种和生产工艺技术雷帕霉素(西罗莫司、Sirolimus、Rapamycin)雷帕霉素是新型大环内酯的抗排斥药物,是目前世界上最新的强效免疫抑制剂,临床上用于器官移植的抗排斥反应和自身免疫性疾病的治疗。
它的免疫抑制活性比现行临床广泛使用的环孢素强数十倍,毒性低,用量小,且与环孢素有协同免疫抑制作用,临床上与环孢素联合使用。
与环孢素和FK506(他克莫司)相比,西罗莫司是肾毒性最低的免疫抑制剂,且无神经毒性。
美国已在全球80个中心进行1295例肾移植试验,效果显著,副作用极小。
抑制原理:可能通过阻断IL-2启动的T细胞增殖而选择性抑制T细胞,用于抗移植排斥反应。
由于美国生产的雷帕霉素在我国未能获得行政保护,故国内企业可以生产雷帕霉素。
据了解,自2001年至今,SFDA已先后批准了7家企业生产雷帕霉素,其中浙江新昌制药厂、福建科瑞药业、杭州中美华东制药、华北制药科研开发公司4家为雷帕霉素原料药厂。
获批准的雷帕霉素统一命名为“西罗莫司”。
市场情况:近年来,国产雷帕霉素口服制剂类抗排异药的销量迅速上升。
有消息称,目前我国生产的环孢素A年产量已达2吨左右,而雷帕霉素产量则已超过环孢素。
这是因为国内企业经过工艺革新,突破了生产雷帕霉素的技术壁垒。
目前,四川宜宾韦希药业公司的雷帕霉素年产能力已达1吨。
此外,天津新美科技公司也有一定的雷帕霉素原料药生产能力,产品不仅供应国内市场,还有少量出口至海外市场。
估计国内雷帕霉素的总产能已达5吨(但实际产量可能没有那么多,因为药厂必须根据订单来制定产量),这已大大超过国内开发上市较早的环孢素A的年产量。
目前生产工艺介绍:菌种来源:美国工艺水平:生产上发酵单位1000-1200mg/L发酵周期为192-204小时。
提取收率:45%产品纯度:97-98%生产规模:5吨罐生产成本:约10000元/公斤产品国内售价:约700000元/公斤提供的服务:菌种;种子、发酵配方工艺,提炼工艺。
依诺雷帕霉素指南

依诺雷帕霉素指南
背景
依诺雷帕霉素是一种抗生素,常用于治疗各种感染疾病。
本指南旨在提供有关依诺雷帕霉素的使用方法和注意事项的信息。
使用方法
1. 用法和剂量:依诺雷帕霉素通常以口服药物形式使用。
剂量应根据患者年龄、体重和疾病严重程度而定。
请务必遵循医生的建议,按照准确的剂量和使用频率使用药物。
2. 使用时间:依诺雷帕霉素应在空腹时服用,最好在饭前至少1小时或饭后2小时内服用。
与乳制品、铁制品或铝镁抗酸药物同时使用可能会降低依诺雷帕霉素的吸收效果。
3. 使用时间长度:依诺雷帕霉素的使用时间长度应根据医生的建议和疾病的特点而定。
请不要自行停止使用药物,建议在医生指导下逐渐减少剂量。
注意事项
1. 过敏反应:如果您对依诺雷帕霉素过敏或其他抗生素类药物
过敏,请立即停止使用并告知您的医生。
2. 不良反应:依诺雷帕霉素可能引起一些不良反应,包括恶心、呕吐、腹泻等。
如果您出现严重不良反应,请立即就医。
3. 药物相互作用:请告知医生您正在使用的其他药物,包括处
方药、非处方药和补充剂,以避免药物之间的相互作用。
4. 孕妇和哺乳期妇女:如果您是孕妇或正在哺乳期,应在医生
的指导下使用依诺雷帕霉素。
总结
依诺雷帕霉素是一种常用的抗生素,用于治疗感染疾病。
使用时,请遵循医生的建议,按照准确的剂量和使用方法使用药物。
如
果出现不良反应,请及时就医并告知医生。
同时,如果您是孕妇或
正在哺乳期,请在医生的指导下使用该药物。
参考资料:。
一种抗真菌药,竟然会有助于癌症的治疗,或许肺癌患者也有希望用上

一种抗真菌药,竟然会有助于癌症的治疗,或许肺癌患者也有
希望用上
雷帕霉素原意是作为一种大环内酯类抗生素,原意是为了治疗真菌感染的,然而发现它的代谢产物能抑制变态免疫反应,比抗真菌更抢眼,因此科学家们就把它作为治疗器官移植的免疫排斥反应的药物。
然后又发现,它居然能协同其他癌症的治疗,发挥抗癌功效!
科学家们经过研究发现,体内存在一种名叫TOR的信号通路,它的活跃可以造成细胞分泌大量的蛋白质、核酸,并给癌细胞的无限增殖提供生物原料,而雷帕霉素则可以抑制这一过程。
美国FDA也早就批准将雷帕霉素用于治疗头颈部鳞状细胞癌、尤文氏肉瘤、骨肉瘤等癌种,和雷帕霉素机制一样的其他mTOR抑制剂也被用于非小细胞肺癌、黑色素瘤等多种癌症中,都取得了不错的成绩。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
雷帕霉素科技名词定义中文名称:雷帕霉素英文名称:rapamycin其他名称:西罗莫司(sirolimus)定义:一种新型大环内酯类免疫抑制药物。
通过与相应免疫嗜素RMBP结合抑制细胞周期G0期和G1期,阻断G1进入S期而发挥作用,其效应为:①抑制T和B细胞增殖;②抑制IL-1、IL-2、IL-6和IFN-γ诱导的淋巴细胞增殖;③抑制IgG和供者特异性抗体(细胞毒抗体)产生;④抑制单核细胞增殖。
可用于抗移植排斥反应和治疗类风湿性关节炎、红斑狼疮等自身免疫病。
应用学科:免疫学(一级学科);应用免疫(二级学科);免疫治疗(三级学科)本内容由全国科学技术名词审定委员会审定公布求助编辑百科名片雷帕霉素(RAPA)是一种新型大环内酯类免疫抑制剂。
雷帕霉素通过不同的细胞因子受体阻断信号传导,阻断T淋巴细胞及其他细胞由G1期至S期的进程,从而发挥免疫抑制效应。
目录编辑本段基本解释雷帕霉素(RAPA)是一种新型大环内酯类免疫抑制剂。
雷帕霉素通过不同的细胞因子受体阻断信号传导,阻断T淋巴细胞及其他细胞由G1期至S期的进程,从而发挥免疫抑制效应。
从临床应用来看,雷帕霉素有很好的抗排斥作用,且与环孢霉素A(CsA)和FK506等免疫抑制剂有良好的协同作用,是一种疗效好,低毒,无肾毒性的新型免疫抑制剂。
2010年3月,美国德克萨斯州大学的一项研究显示,雷帕霉素可用于治疗阿尔茨海默症,该药物成分也存在于复活岛土壤中细菌的分泌物。
编辑本段简介雷帕霉素分子式雷帕霉素(Rapamycin,RAPA,RPM),又名Sirolimus,属大环内酯类抗生素,与FK506的结构相似。
起初雷帕霉素被研究作为低毒性的抗真菌药物,1977年发现雷帕霉素具有免疫抑制作用,1989年开始把RAPA作为治疗器官移植的排斥反应的新药进行试用,目前(2010年)RAPA的I、II期临床试验已结束,III期临床试验正在进行之中。
编辑本段结构雷帕霉素的分子式为C51H79NO13,分子量991KD,为白色固体结晶,熔点为183-185℃,亲脂性,溶解于甲醇、乙醇、丙酮、氯仿等有机溶剂,极微溶于水,几乎不溶于乙醚。
从目前动物实验及临床应用的效果看,雷帕霉素是一种疗效好,低毒,无肾毒性的新型免疫抑制剂。
编辑本段作用机理雷帕霉素通过不同的细胞因子受体阻断信号传导,阻断T淋巴细胞及其他细胞由G1期至S期的进程,雷帕霉素可阻断T淋巴细胞和B淋巴细胞的钙依赖性和非钙依赖性的信号传导通路。
雷帕霉素和FK506一样,结合在相同的免疫亲和蛋白(immunophilin)FKBP12上,形成RAPA-FKBP12复合物,这种复合物不能与钙调素结合,并且雷帕霉素亦不抑制T细胞的早期激活或直接减少细胞因子的合成。
这种复合物的靶蛋白最早是在酵母菌中被确定,称为TOR1和TOR2。
编辑本段研究发现研究发现雷帕霉素能抑制70-KDaS6激酶(p70S6K)的活性,该酶与细胞周期中的许多关键的不同细胞过程有密切的关系。
但是在无细胞体系(cell-freesystem)中,RAPA-PKBP复合物却不能抑制p70S6K的活性,亦即RAPA-PKBP复合物与p70S6K 之间无直接的相互作用,故推测雷帕霉素可能作用于p70S6K之前的过程,抑制其他激酶或激活磷酸酶,其结果是雷帕霉素至少抑制二种底物:①促进蛋白合成的S6核糖体蛋白,②诱导增殖细胞核抗原(PCNA)基因的转录诱导的cAMP反应元件调节因子(CREM)。
雷帕霉素对DNA多聚酶δ来说是一种必要的过程因子,同时在细胞进入S期的过程中亦是需要的。
编辑本段细胞周期雷帕霉素能降低细胞周期依赖性激酶(cdk)和细胞周期蛋白(cyclin)复合物激酶的活性。
细胞周期全过程需要不间断的cdk和cyclin复合物的活化。
雷帕霉素对cdk2、cdk4、cyclinD和cyclinE的蛋白水平无任何影响,但却能降低cdk4-cyclinD 和cdk2-cyclinE复合物的激酶活性。
在G1期的中晚期进程中,这些激酶的活性包括从cyclin-cdk复合物中去除cyclin依赖的激酶抑制因子p27kip1,雷帕霉素通过抑制了cyclin-cdk复合物激酶的活性,从而预防了p27的清除,阻断了cdk4-cyclinD和cdk2-cyclinE复合物的活化,结果导致之后的细胞进程被抑制:视网膜母细胞瘤蛋白(Rb)的过磷酸化和Rb-E2F复合物的分离。
E2F转录因子的活化降低导致了细胞周期蛋白cdc2、cyclinA以及转录活性需要的丝氨酸/苏氨酸激酶的下调。
雷帕霉素对在细胞周期中有关键作用的原癌基因Bcl-2的转录有抑制作用,Bcl-2的表达减少可促使活化的淋巴细胞凋亡。
雷帕霉素也可预防CD-28介导的IKBα的下调,抑制了c-rel的细胞核易位。
c-rel是一种CD-28反应元件调节子结合因子,能使IL-2的基因表达持续下调。
此外,雷帕霉素对细胞由G1期至S期的发展的干扰作用,在体外实验证实它不是一种有效的细胞因子合成抑制剂,而是对活化T细胞和B细胞的生长因子和细胞因子等产生相反作用。
RAPA不局限于对免疫系统的细胞产生作用,它亦能抑制平滑肌细胞、内皮细胞、成纤维细胞等的增殖。
编辑本段临床应用药物分布与代谢雷帕霉素+小剂量激素可用于治疗FSGS雷帕霉素在动物实验和临床应用中的给药方式较多,有腹腔内注射、静脉注射及口服等。
口服用药后约1.5—2小时可达峰值,口服后的平均生物利用度在肾移植受者为15%,半衰期为62小时。
药物吸收入血后,95%分布于红细胞内,血浆中含量只占3%,游离状态存在的药物极少。
因此临床上以全血标本来监测雷帕霉素的血药浓度。
血药的Cmax和AUC值与剂量成正比。
检测血药浓度的最好方法是高效液相色谱法(HPLC),该方法灵敏度高。
Serkova等在猴肺移植实验中检测到雷帕霉素在组织中的分布以胆囊、胰腺、移植肺、小脑、肾、脾最高。
在人类雷帕霉素的浓度分布以肺、心、肾、胰腺、脾、肝等脏器中较高。
RAPA主要经细胞色素P450系统代谢,并经胆汁排出,故对细胞色素P450系统有影响的药物,可对雷帕霉素的药物动力学产生影响。
临床应用效果在大量的动物实验证实雷帕霉素是一种安全有效的新型免疫移植剂后,2000年以来已进行大量临床观察,目前(2010年)已进行到第Ⅲ期临床试验,试验采用RAPA 联合MMF或Aza及类固醇与CsA、FK506等做药效对比,或者是雷帕霉素联合CsA 或FK506等药物以探讨联合用药的疗效。
Kahan教授在一项多中心的Ⅱ期临床试验中将149名肾移植患者随机分成6组,3组为安慰剂、1或3mg/m2/day的雷帕霉素联合应用类固醇及全量CsA,3组为1、3或5mg/m2/day 的雷帕霉素联合应用类固醇及目标血浓度为全量的50%的CsA,结果显示移植后头6个月内,病理证实的急性排斥反应安慰剂组为30.0%,1、3mg/m2/day,雷帕霉素和全量CsA组为8.5%(P=0.028),应用雷帕霉素及减量的CsA治疗的病人的急性排斥反应较低,各组中1年的病人及移植物的存活率无明显差异,雷帕霉素的应用并未增加CsA的副作用,但在接受全量CsA及3mg/m2/day的RAPA的病人有肺炎增高的倾向。
肝移植后在一些病人中出现肝纤维化,这一过程可能是由于抗排斥治疗所致。
有学者应用雷帕霉素进行动物实验时观察到,雷帕霉素能抑制大鼠模型的细胞外基质沉积,降低血小板生长因子,从而减少肝脏星型细胞的增,但在人体中RAPA是否亦能抑制移植肝的纤维化,尚无明确证据。
慢性移植物血管病变(CGVD)已被定义为是一种常规移植免疫治疗过程中的慢性进行性血管病理变化,对移植物长期存活影响很大。
Poston应用雷帕霉素治疗同种心脏移植后的CGVD动物模型发现,雷帕霉素能明显抑制CD4+T细胞和巨噬细胞在移植物血管周边的浸润,降低移植物抗供者抗体的水平。
雷帕霉素与CsA、FK506、MMF等联合应用均有良好的协同作用,其益处在于①减少了治疗方案中各种免疫抑制剂的用量,②减少了免疫抑制剂的副作用,③增强了免疫抑制的效果。
编辑本段用量与监测雷帕霉素的治疗方案多种多样,且单独给药的剂量与联合CsA或FK506等药物使用的剂量区别较大。
维持血药浓度亦各有区别。
Groth等在以雷帕霉素为基础的免疫抑制治疗与CsA为基础的免疫抑制治疗对照研究中,雷帕霉素口服液的初始剂量为16-24mg/m2/day,随后7-10天用量为8-12mg/m2/day,血药浓度稳定在30ng/ml,2个月后调整雷帕霉素用量直至血药浓度稳定在15ng/ml,均在早晨以水或橙汁一次性冲服,一日一次,前12周每周监测1次血药浓度,之后每个月监测1次。
观察到血药浓度与药物毒性成正比,但其副作用是可逆的。
当血药浓度降低后,副作用均好转。
故Groth认为血药浓度以保持于10-20ng/ml为好。
Kahan认为血药浓度大于15ng/ml时,即与甘油三酯的升高及血红蛋白、白细胞或血小板减少有关。
当RAPA与FK506联合应用时,其血药浓度保持在6-12ng/ml即有降低急性排斥率的作用,且毒性小。
在一系列的肝,肾,胰腺移植的病人中服用5mg/day的RAPA 及低剂量的FK506(0.03mg/kg/day)预防急性排斥,且以各自浓度水平维持在3—7ng/ml及6-12ng/ml为准,均取得非常满意的移植物功能。
与CsA合用时,RAPA的用量较单独使用时要少,建议雷帕霉素的浓度维持于5-15ng/ml,同时CsA用量亦可减少,但CsA浓度最少要维持于50-150ng/ml。
目前(2010年)认为由于雷帕霉素的半衰期较长,故无需每天测定其浓度,首次测定可在服药后4天,第一个月内每周测定1-2次,第二个月每周测定1次,之后每月测定一次或在有临床需要时进行检测,例如停用或增加了对细胞色素P450系统代谢有影响的药物,或怀疑患者未遵医嘱服药,胃肠功能紊乱及毒副作用明显时。
编辑本段副作用雷帕霉素有与FK506相似的副作用。
在大量的临床试验中发现其副作用有剂量依赖性,并且为可逆的,治疗剂量的雷帕霉素尚未发现有明显的肾毒性,无齿龈增生。
主要毒副作用包括:头痛,恶心,头晕,鼻出血,关节疼痛。
实验室检查异常包括:血小板减少,白细胞减少,血色素降低,高甘油三酯血症,高胆固醇血症,高血糖,肝酶升高(SGOT,SGPT),乳酸脱氢酶升高,低钾,低镁血症等。
也有报道称服用雷帕霉素可产生眼皮浮肿,而导致血浆磷酸盐水平较低的原因被认为是以雷帕霉素为基础的免疫抑制治疗延长了磷酸盐自移植肾脏的排泄。
与其他免疫抑制剂一样,RAPA有增加感染的机会,有报道称特别有肺炎增加的倾向,但其他机会性感染的发生与CsA无明显差异。
