第十二周有机化学教案第六章醇酚醚
第12章 醇酚醚ppt课件

4 3 2 1 例如: CH 3CH2CHCH3 1 2
OH 2 - 丁醇
3 ︳
4
×
2、 醇的系统命名
1 / H 2 R O N a + 2
醇的酸性比水弱,RONa的碱性比NaOH强。 酸性:HOH > ROH > RC≡CH > NH3 > RH 醇反应活性顺序:CH3OH>伯醇>仲醇>叔醇。
RCH ONa HOH RCH OH Na 2 2
(二)与氢卤酸的反应
醇中的羟基被X亲核取代反应生成卤代烷和水,这是 卤代烷碱性水解的逆反应。
OH
CH OH 2CH 2
OH
CH
CH OH
2.根据饱和烃基还是不饱和烃基,醇分为 :
CH H 饱和醇 CH 3 2O
CH OH 2CH 2
CH CH OH
醇 不饱和醇 CH
O CH H
二、醇的分类
3.根据羟基所连C原子类型不同: 伯醇 CH H CH 3 2O
CH 3 醇 仲醇 CH 3 CH 2 CH
OH
邻苯二酚
连苯三酚
(2)按酚羟基所连的芳香环的类型分类: 苯酚 酚 萘酚 蒽酚
苯酚
OH
萘酚
蒽酚
2. 命名
酚类的命名可用芳烃作母体,也可用酚作母体。当 分子中只含有酚羟基或者只含有一个酚羟基时,一 般都以酚作母体。
CH 3
OH
OH
OH OH
苯酚
邻甲苯酚
醇酚醚jppt课件.ppt

OH | CHCHCH3
—OH
—OH
芳香醇:
—CH2OH
饱和一元醇的通式:CnH2n+1OH
病 原体侵 入机体 ,消弱 机体防 御机能 ,破坏 机体内 环境的 相对稳 定性, 且在一 定部位 生长繁 殖,引 起不同 程度的 病理生 理过程
一、醇的分类
按羟基数目分类:
一元醇: 二元醇:
多元醇:
CH3CH2OH
② 疏水基:非极性的,不易溶于水而易溶于非极性物 质的基团,如:—R
③ 一元醇:低级醇(CH3—OH,C2H5—OH等)能与水互 溶,随着碳链的增大,在水中溶解度显著降低。
H
R
R—O O—H····O
H
H
④ 多元醇一般可与水混溶。
H·····O H
病 原体侵 入机体 ,消弱 机体防 御机能 ,破坏 机体内 环境的 相对稳 定性, 且在一 定部位 生长繁 殖,引 起不同 程度的 病理生 理过程
化学性质。
似水性。 与酸反应。 醇的脱水。 氧化反应。
病 原体侵 入机体 ,消弱 机体防 御机能 ,破坏 机体内 环境的 相对稳 定性, 且在一 定部位 生长繁 殖,引 起不同 程度的 病理生 理过程
一、醇的分类
1. 按烃基不同分类:
饱和醇: 不饱和醇: 脂环醇:
CH3OH、CH3CH2OH CH2 CHCH2OH、CH2
四、化学性质—似水性
反应活性:
① 烷基增大,活性降低:叔醇 < 仲醇 < 伯醇﹤甲醇 ② 碱性:叔醇钠 > 仲醇钠 > 伯醇钠 > 甲醇钠 > NaOH
醇钠的水解:
CH3ONa + H2O
较强的碱 较强的酸
《专题四 第一节 醇 酚 醚》教学设计教学反思

《醇酚醚》教学设计方案(第一课时)中职化学课程《醇酚醚》教学设计方案(第一课时)一、教学目标1. 知识目标:学生能够区分醇、酚、醚,并了解它们的基本性质。
2. 能力目标:学生能够掌握醇、酚、醚的化学反应,并能够进行简单的实验操作。
3. 情感目标:通过本课程的学习,培养学生的科学态度和团队合作精神。
二、教学重难点1. 教学重点:醇、酚、醚的性质及其在化学反应中的应用。
2. 教学难点:学生对于化学反应的掌握,以及实验操作的正确性。
三、教学准备1. 准备实验器械:酒精灯、试管、试管夹、胶头滴管、钠块等。
2. 准备化学试剂:乙醇、苯酚、丙三醇等。
3. 制作PPT,准备相关图片和视频。
4. 安排学生分组,每组进行一种醇、酚、醚的化学反应实验。
5. 安置预习任务,让学生提前了解醇、酚、醚的基本观点和性质。
四、教学过程:(一)导入新课1. 展示实物:酒、葡萄酒、酒精灯、酒精喷灯、醋酸、乙醇、苯酚、甘油、葡萄糖等。
2. 引导学生观察,思考:酒是如何酿造的?酒精是如何制取的?酒精喷灯应用的燃料是什么?为什么不用汽油灯?为什么不用植物油制取蜡烛?这些物质有什么共同特点?3. 总结:这些物质都是有机化合物,即含碳的化合物。
它们大多数由碳氢氧或其他元素组成,它们的化学性质和无机物有很大差别。
它们是多种有机反应的基本物质,了解这些物质的性质和反应,对进一步学习有机化学及其它化学课程至关重要。
(二)讲授新课1. 醇的性质和制备(1)醇的分类和定名:展示各种醇类物质,如乙醇、丙醇、异丁醇等,引导学生观察并定名。
介绍醇的分类和定名规则。
(2)醇的物理性质:介绍醇的物理性质,如颜色、气味、状态等。
(3)醇的化学性质:展示乙醇与浓硫酸加热制备乙醛的实验装置图,引导学生观察并思考反应原理。
介绍醇的氧化反应、酯化反应等化学性质。
(4)醇的制取:介绍工业上如何制备醇类物质,如通过乙烯水化法制取乙醇。
2. 酚的性质和制备(1)酚的分类和定名:展示各种酚类物质,如苯酚、甲基苯酚等,引导学生观察并定名。
高三理化生第六章醇酚醚.ppt

CH3
CH3
C
+
CH2
CH3
CH3 H
CH3H
CH3 C C CH3 HCl CH3 C C CH3
H OH
H +OH2 _ H2O
CH3 H
CH3 H
CH3
C
+
C
CH3
CH3
C
C
+
CH3
H
H
_
CH3 H
Cl
CH3 C C CH3
Cl H
应用-伯、仲、叔醇的区别方法
(CH3)3OH
(CH3)3Cl
CH3 H
CH3CH2CHCH2
氢重排
伯碳正离子
-H CH3
CH3CH2-C=CH2
经历碳正离子中间体的 反应物可能发生的反应
取代反应 消除反应 重排反应
CH3 CH3CH2-C-CH3
叔碳正离子 -H CH3
CH3CH=C-CH3 主要产物
醇分子间脱水反应-制备简单醚
+ CH3 CH2 OH
HO CH2
用途 甲醇用途广泛,是基础的有机化 工原料和优质燃料。主要应用于 精细化工,塑料等领域,用来制 造甲醛等多种有机产品,也是农
药、医药的重要原料之一。
2、乙醇 (C2H5OH)
吸收与代谢
胃和小肠的
乙醇 毛细血管
血液
CO2 H2O
肝脏
(乙醇脱氢酶)
乙酸 乙醛
无色、透明,具有特殊香味 的液体(易挥发),密度比 水小,能跟水以任意比互溶
一、醇
(一)命名 (二)物理性质 (三)化学性质
1.似水性: 与活泼金属反应 2.与无机酸的作用:HNO3\H2SO4\H3PO4\HX 3.脱水反应 4.氧化或脱氢:KMnO4\MnO2 5. 邻二醇与高碘酸的作用
《医学有机化学教学》第六章醇酚醚课件

酚的物化性质
常见的酚是白色或淡黄色晶体, 具有典型的羟基氢键性质。
酚的物理性质
酚的溶解性
酚和水的亲和力不强,但亲多极性溶剂,如乙醇、甲醇等。
酚的熔沸点
酚分子因氢键的作用力较大,所以其熔沸点均高于相应氢氧化物。
酚的酸碱性
酚具有较弱的酸性,其酸性相当于苯乙烯。
酚的化学性质
1 酚的取代反应
酚的氢原子可被烷基或芳基等基团取代,常用的有碘化物、碳酸钾和正硝酸钠等试剂。
醇的性质
醇是有颜色的透明液体。它们具有醇基 (-OH),能够形成氢键和其他分子间的相互作用力。
醇的物理化学性质
溶解性
醇在水中具有良好的溶解性,特 别是碳数较少的醇类分子。
沸点和融点
醇的沸点和融点随碳链长度增加 而增加,与分子大小也有关系。
氧化性
醇可以被氧化剂如KMnO4氧化成 羧酸和醛。
醇的化学性质
1 亲核性
醇可以作为亲核试剂参与 重要反应,如酯化、醚化 和醛缩合等。
2 脱水反应
醇的α、β位于季碳原子的 醇分子容易发生β-消除脱 水反应,生成烯烃。
3 烷基化
醇可用以制备烷基化试剂, 例如,三甲基氧化铝 (Me3AlO)、四甲基铅 (Me4Pb)。
醇的合成方法
1
卤代烃与水合成法
当卤代烃和氢氧化钠或氢氧化钾在水中
2 酚的氧化反应
酚可以被氧化剂氧化成醛、羧酸等具有较高化学价的产物。
3 酚的醛素反应
酚可用于合成香料、染料、制药原料等有机合成反应中。
医学有机化学教学
欢迎来到《医学有机化学教学》第六章醇酚醚课件。本章节将会详细介绍醇 酚醚的概念、物理化学性质以及合成方法。
醇的概念及分类
醇是什么?
第六章 醇 酚 醚第2节酚

谢谢观看
OH
OH
OH
苯酚
α-萘酚
β-萘酚
2、根据酚羟基的数目的不同,可分为一元酚和多元酚
OH
HO
OH
HO
OH
一元酚
二元酚
OH
三元酚
(二)酚的命名
1、一元酚的命名
● 在母体芳香环后面加上“酚”字,芳香环上所连基团(-R、-X、 -NO2等)均被视为取代基,
● 在名字前面加上取代基的位次、名称和数目。
OH
OH
(一)弱酸性
OH + NaOH
微溶于水
ONa + H2O
苯酚钠(易溶于水)
苯酚能溶于NaOH、Na2CO3,而醇只能和Na反应。
取代苯酚的酸性强弱:
OH
OH
OH
O2N
NO2
CH3 pKa=10.9
NO2 pKa=8.2
NO2 pKa=0.4
苯环上连有强吸电子基团使酸性增强。 连有供电子基团使酸性减弱。
(二)与三氯化铁的显色反应
6C6H5OH + FeCl3
H3[Fe(C6H5O)6] + 3HCl
● 不同的酚类化合物遇FeCl3反应显示出不同的颜色
● 除了酚类化合物以外,大部分含有烯醇结构( C C OH)的化 合物都可以和FeCl3溶液发生显色反应。利用这一特性,可用FeCl3 溶液鉴别酚类和有烯醇式结构的化合物
有机化学
第六章 醇 酚 醚
学习目标
醚的分类 命名和性质 熟悉
了解
重要的 醇、酚、醚
掌握
醇、酚的命名 和分类 醇、酚的性质
1
第一节 醇
2
第二节 酚
3
初三化学醇酚醚教学大纲

初三化学醇酚醚教学大纲
【目的要求】
1.掌握醇、酚、醚的化学性质。
2.掌握苯环上取代反应的定位规则。
3.熟悉醇、酚、醚的定义、结构、分类、命名及同分异构现象。
4.熟悉醇、酚、醚的制备方法。
5.熟悉多元醇的特性。
6.了解重要的醇、酚、醚个别化合物。
7.了解醇、酚、醚的物理性质。
【教学内容】
1.醇的结构、分类、命名与同分异构现象。
2.醇的物理性质。
3.醇的化学性质:与活泼金属反应;取代反应;脱水反应(分子内、分子间);氧化和脱氢;多元醇的特性。
4.醇的制备:格氏试剂合成法;由醛酮还原制备。
5.醇的个别化合物。
6.酚的结构、分类与命名。
7.酚的物理性质。
8.酚的化学性质:酚羟基的反应;苯环上的亲电取代反应(卤代、硝化、磺化、傅-克反应等);氧化反应。
9.苯环上取代反应的定位规则:定位基的类型(邻、对位
定位基与间位定位基);定位规则的理论解释(邻、对位定位基的影响、间位定位基的影响、卤素的定位效应);二取代苯的定位规律;定位规律的应用。
10.酚的制备。
11.重要的酚。
12.醚的结构、分类、命名与同分异构现象。
13.醚的物理性质:状态,沸点,水溶性。
14.醚的化学性质:与无机强酸成盐;醚键的断裂;过氧化物的形成。
15.醚的制备:醇分子间脱水;威廉森合成法。
16.重要的醚。
【教学方式】
PPT授课、教师讲授。
有机化学醇酚醚ppt课件

§1 醇
§1.1 醇的分类
1)根据烃基不同:饱和醇、不饱和醇、脂环醇、 芳香醇。
2)根据-OH的数目不同:一元醇、二元醇、多元 醇。
3)根据-OH所连碳原子的类型不同:伯醇、仲醇、 叔醇。
结构特点:醇分子中,-OH与饱和碳相连接
3
Note:区别芳香醇和酚 芳香醇 酚
CH2OH OH
4
§1.2 醇的命名
醇与强酸共热可发生分子内或分子间的脱水 反应。
(1)分子内脱水 醇脱水成烯的反应速率:3o醇 > 2o醇 > 1o醇
17
如:CH3CH2CHCH3
OH
60% H2SO4 100 ℃
(CH3)3COH
20% H2SO4 85~90 ℃
CH3CH = CHCH3 80%
CH3
CH3-C = CH2 100%
1 、普通命名法
根据相应的烃基,在烃基后面+“醇”。
CH3 CH3 CH CH2OH
CH3 CH3 C OH
CH3
OH
CH2OH
异丁醇
叔丁醇
环己醇
苄醇
2、系统命名法
选择含有羟基的最长碳链为主链,以羟基的
位置最小编号,称为某醇。多元醇的命名,要选
择含-OH尽可能多的碳链为主链,羟基醇、酚、醚
醇、酚、醚都是烃的含氧衍生物, 可看成水分子中氢被烃基取代后的产物。
H-O-H
R-OH Ar-OH R-O-R Ar-O-R Ar-O-Ar
通 式: 醇R-OH , 酚C6H5-OH , 醚R-O-R
1
本章学习要求
掌握醇、酚、醚的命 名及醇、酚、醚的化学性 质;了解醇、酚、醚各主 要化合物的实际应用。
第十一周有机化学教案第六章醇酚醚

教案(章、节备课)1•俗名:如乙醇俗称酒精,丙三醇称为甘油等。
2•简单的一元醇用习惯命名法命名。
例如:CH 3CH 3CH 3 CH CH 2OH CH 3 C —0HCH 3异丁醇 叔丁醇3. 系统命名法结构比较复杂的醇,采用系统命名法。
选择含有羟基的最长碳链为主链,以羟基 的位置最小编号,称为某醇。
0HCH 3-CH-CH-CH 才CH-CH3CH 3ClCH 3-CH -CH 2-CH =CH 2I OHCH-CH 3OH2-甲基-5-氯-3-己醇4 -戊烯-2-醇1 -苯基乙醇(a 苯乙醇)2 -苯基乙醇(3苯乙醇)多元醇的命名,要选择含 -OH 尽可能多的碳链为主链,羟基的位次要标明。
例如:§ 8.2醇的性质§ 8.2.1醇的物理性质 1 .性状:(略) 2. 沸点: 3. 溶解度:4. 结晶醇的形成低级醇能和一些无机盐(MgCl 2、CaCl 2、CuSO 4等)作用形成结晶醇,亦称醇化MgCb 一 6CH 3OHCaCl 2 ' 4C 2H 5OH CaCl 2 - 4CH 3OHQO 0H环己醇CH 2OH例如:CH I 0H2-CH 2-CH 2 OH1, 3丙二醇不溶于有机溶剂,溶于水。
可用于除去有机物中的少量醇如:苄醇§ 8.1.2醇的化学性质1 •与活泼金属的反应CH 3CH 2OH + Na -------------- CH 3CH 2ONa + 1/2 H 2K K粘稠固体(溶于过量乙醇中)Na 与醇的反应比与水的反应缓慢的多,反应所生成的热量不足以使氢气自燃, 故常利用醇与Na的反应销毁残余的金属钠,而不发生燃烧和爆炸。
CH 3CH 2O -的碱性比-OH 强,所以醇钠极易水解。
CH 3CH 2ONa + H 2O —CH 3CH 2OH + NaOH较强碱较强酸较弱酸 较弱碱醇的反应活性:CH s OH>伯醇(乙醇)> 仲醇 >叔醇pKa 15.09 15.93> 19醇钠(RONa )是有机合成中常用的碱性试剂。
醇酚醚 教案

醇酚醚教案教案标题:醇酚醚教学目标:1. 了解醇酚醚的定义、性质和用途。
2. 掌握醇酚醚的合成方法和反应特点。
3. 学会应用醇酚醚进行有机合成和实验操作。
教学重点:1. 醇酚醚的定义、性质和用途。
2. 醇酚醚的合成方法和反应特点。
教学难点:1. 醇酚醚的合成方法和反应特点的理解和应用。
教学准备:1. PowerPoint幻灯片。
2. 实验室设备和试剂。
教学过程:导入:1. 利用幻灯片向学生介绍醇酚醚的定义,并简要说明其在化学领域中的重要性和应用范围。
知识讲解:1. 通过幻灯片和板书,详细介绍醇酚醚的性质,包括物理性质和化学性质。
2. 解释醇酚醚的合成方法,如Williamson合成和Williamson改进合成等,并重点讲解各种方法的反应机理和适用范围。
案例分析:1. 提供几个醇酚醚的合成案例,让学生运用所学知识进行分析和解答。
2. 引导学生思考醇酚醚在有机合成中的应用,并讨论其在生活中的实际应用。
实验操作:1. 在实验室中进行一次醇酚醚的合成实验,让学生亲自参与操作,并记录实验步骤和观察结果。
2. 引导学生分析实验结果,总结醇酚醚合成实验的注意事项和常见问题。
课堂练习:1. 提供一些选择题和应用题,检测学生对醇酚醚的理解和应用能力。
总结:1. 简要回顾本节课的内容,并强调醇酚醚在化学领域中的重要性和应用前景。
2. 鼓励学生进一步学习和探索有关醇酚醚的知识。
教学反思:1. 教学过程中是否能够引起学生的兴趣和参与度?2. 学生在实验操作中的表现是否能够达到预期的效果?3. 学生对醇酚醚的理解和应用能力是否得到提高?教学扩展:1. 鼓励学生进行相关的实验研究或文献阅读,进一步了解醇酚醚的合成方法和应用。
2. 组织学生进行小组讨论,分享有关醇酚醚的实际应用案例,并展示给全班。
高二化学 竞赛辅导教案:醇、酚、醚 苏教版

化学竞赛辅导教案醇、酚、醚第八课时醇、酚、醚学习要求:1.掌握醇、酚的结构特点与化学性质的差异。
2.熟练掌握醇、酚、醚的基本反应与鉴别方法。
3.掌握醇、酚、醚的主要制备方法和重要用途。
4.初步掌握消除反应历程及其影响因素,理解和判断消除反应与亲核取代的竞争。
醇、酚、醚都是烃的含氧衍生物,故合在一起讨论。
一、醇的结构、分类和命名1.结构醇可以看成是烃分子中的氢原子被羟基(OH)取代后生成的衍生物(R-OH)。
2.分类1)根据羟基所连碳原子种类分为:一级醇(伯醇)、二级醇(仲醇)、三级醇(叔醇)。
2)根据分子中烃基的类别分为:脂肪醇、脂环醇、和芳香醇(芳环侧链有羟基的化合物,羟基直接连在芳环上的不是醇而是酚)。
3)根据分子中所含羟基的数目分为:一元醇、二元醇和多元醇。
两个羟基连在同一碳上的化合物不稳定,这种结构会自发失水,故同碳二醇不存在。
另外,烯醇是不稳定的,容易互变成为比较稳定的醛和酮。
3.醇的命名1) 俗名 如乙醇俗称酒精,丙三醇称为甘油等。
2) 简单的一元醇用普通命名法命名。
例如: 3) 系统命名法结构比较复杂的醇,采用系统命名法。
选择含有羟基的最长碳链为主链,以羟基的位置最小编号,……称为某醇。
例如:多元醇的命名,要选择含-OH 尽可能多的碳链为主链,羟基的位次要标明。
例如:二、醇的物理性质 1.性状:(略) 2.沸点:1)比相应的烷烃的沸点高100~120℃(形成分子间氢键的原因), 如乙烷的沸点为-88.6℃,而乙醇的沸点为78.3℃。
2) 比分子量相近的烷烃的沸点高,如乙烷(分子量为30)的沸点为-88.6℃,甲醇(分子量32)的沸点为64.9℃。
3)含支链的醇比直链醇的沸点低,如正丁醇(117.3)、异丁醇(108.4)、叔丁醇(88.2)。
3.溶解度:甲、乙、丙醇与水以任意比混溶(与水形成氢键的原因);C 4以上则随着碳链的增长溶解度减小(烃基增大,其遮蔽作用增大,阻碍了醇羟基与水形成氢键);分子中羟基越多,在水中的溶解度越大,沸点越高。
初三化学醇酚醚教学大纲

初三化学醇酚醚教学大纲
【目的要求】
1.掌握醇、酚、醚的化学性质。
2.掌握苯环上取代反应的定位规那么。
3.熟悉醇、酚、醚的定义、结构、分类、命名及同分异构现象。
4.熟悉醇、酚、醚的制备方法。
5.熟悉多元醇的特性。
6.了解重要的醇、酚、醚个别化合物。
7.了解醇、酚、醚的物理性质。
【教学内容】
1.醇的结构、分类、命名与同分异构现象。
2.醇的物理性质。
3.醇的化学性质:与活泼金属反应;取代反应;脱水反应〔分子内、分子间〕;氧化和脱氢;多元醇的特性。
4.醇的制备:格氏试剂合成法;由醛酮还原制备。
5.醇的个别化合物。
6.酚的结构、分类与命名。
7.酚的物理性质。
8.酚的化学性质:酚羟基的反应;苯环上的亲电取代反应〔卤代、硝化、磺化、傅-克反应等〕;氧化反应。
9.苯环上取代反应的定位规那么:定位基的类型〔邻、对位定
位基与间位定位基〕;定位规那么的理论解释〔邻、对位定位基的影响、间位定位基的影响、卤素的定位效应〕;二取代苯的定位规律;定位规律的应用。
10.酚的制备。
11.重要的酚。
12.醚的结构、分类、命名与同分异构现象。
13.醚的物理性质:状态,沸点,水溶性。
14.醚的化学性质:与无机强酸成盐;醚键的断裂;过氧化物的形成。
15.醚的制备:醇分子间脱水;威廉森合成法。
16.重要的醚。
【教学方式】
PPT授课、教师讲授。
大学有机化学醇酚醚教案

一、教学目标1. 知识目标:(1)掌握醇、酚、醚的分类、命名、结构和性质;(2)了解醇、酚、醚的化学性质及反应条件;(3)熟悉醇、酚、醚的制备方法及在有机合成中的应用。
2. 能力目标:(1)培养学生分析、解决有机化学问题的能力;(2)提高学生的实验操作技能和实验安全意识。
3. 情感目标:(1)激发学生对有机化学的兴趣,培养科学素养;(2)培养学生严谨求实的科学态度。
二、教学内容1. 醇(1)醇的分类、命名、结构和性质;(2)醇的化学性质及反应条件;(3)醇的制备方法及在有机合成中的应用。
2. 酚(1)酚的分类、命名、结构和性质;(2)酚的化学性质及反应条件;(3)酚的制备方法及在有机合成中的应用。
3. 醚(1)醚的分类、命名、结构和性质;(2)醚的化学性质及反应条件;(3)醚的制备方法及在有机合成中的应用。
三、教学过程1. 导入(1)回顾有机化学基础知识,引导学生关注醇、酚、醚这一类有机化合物;(2)介绍醇、酚、醚在生活中的应用,激发学生的学习兴趣。
2. 讲授(1)醇的分类、命名、结构和性质;(2)酚的分类、命名、结构和性质;(3)醚的分类、命名、结构和性质;(4)醇、酚、醚的化学性质及反应条件;(5)醇、酚、醚的制备方法及在有机合成中的应用。
3. 实验操作(1)演示醇、酚、醚的制备实验;(2)学生分组进行实验操作,观察实验现象,记录实验数据;(3)分析实验结果,总结醇、酚、醚的制备方法及反应条件。
4. 课堂小结(1)回顾本节课所学内容,强调重点、难点;(2)布置课后作业,巩固所学知识。
四、教学评价1. 课堂表现:关注学生的课堂参与度,评价学生的提问、回答、实验操作等;2. 课后作业:检查学生的课后作业,了解学生对知识的掌握程度;3. 实验报告:评估学生的实验操作技能和实验安全意识。
五、教学反思1. 教学内容是否符合学生实际需求,是否能够激发学生的学习兴趣;2. 教学方法是否有效,是否能够提高学生的实验操作技能和实验安全意识;3. 教学过程中是否存在问题,如何改进教学方法,提高教学效果。
有机化学教案-醇、酚、醚

第七章 醇、酚、醚醇、酚和醚都是烃的含氧衍生物,羟基与脂肪烃基直接相连的叫醇,羟基与芳香烃基直接相连的叫酚,两烃基与氧直接相连的叫醚。
例:乙醇 乙醚 苯酚第一节 醇 一:分类:醇中羟基(—OH )为其官能团。
饱和一元醇的通式:C n H 2n+1OH 。
一元醇 CH 3CH 2OH 乙醇 醇 二元醇 HOCH 2CH 2OH 乙二醇 (按羟基的数目) CH 2 CH 2 CH 2 多元醇 | | | 丙三醇 OH OH OH饱和脂肪醇 CH 3CH 2CH 2OH 丙醇;脂肪醇不饱和脂肪醇 CH 2=CHCH 2OH 2-丙烯醇饱和脂环醇 例如:2-甲基环己醇醇 脂环醇 (羟基所连的烃基不同)不饱和脂环醇 例如:2-环己烯醇芳香醇 例如:苯甲醇伯醇 CH 3CH 2CH 2 CH 2OH 丁醇 仲醇 CH 3CHCH 3 异丙醇 醇 | 所连碳原子的种类不同) OH叔醇 (CH 3)3 C OH 叔丁醇二:命名:1:普通命名法:简单醇常采用普通命名法,即在相应的烷基名称后加一个“醇”字。
例如: CH 3 OH (CH 3)3CH 2CH 2OH CH 2=CHCH 2OH 甲醇 新戊醇 烯丙醇苄醇C H 3C H 2O HC H 3C H 2O C H 2C H 3O HO HCH 3O HC H 2O HC H 2O H2:系统命名法命名原则同前几章,以醇为母体,选取含有羟基的最长链为主链,从离羟基近的一端开始编号。
书写时,末尾加上“醇”字,“醇”字前写上羟基的位号,在位号与“醇”之间加上短横。
如果是不饱和醇,则选含有羟基和不饱和键的最长链为主链,从离羟基近端编号。
书写时,将表示链中碳原子个数的字放在“烯”或“炔”的前面。
分子中含有多个羟基时,则选 含羟基数目尽可能多的最长链为主链,根据羟基的数目称为某元醇。
3-甲基-1-丁醇 E-3-氯-3-戊烯-2-醇 3-环戊烯醇 1,3-环己二醇 2-苯基乙醇芳香醇命名时,常常把芳环作为取代基。
醇酚醚教师讲义.

CH3 CH3―C―O
丙酮
―
有机物分子中加入氧或脱去氢的反应叫做氧化反应。 有机物分子中失去氧或得到氢的反应叫做还原反应。
三、重要的醇 1.甲醇(又称木精或木醇) CH3−OH 无色液体,沸点64.7℃,易燃烧,有酒的气味,但毒性很强
误服10ml失明,30ml致死。 2.乙醇(俗称酒精) CH3−CH2−OH 无色液体,沸点78.5℃,易燃烧,能与水及大多数有机溶剂
CH3
6
5
4
3
2
1
CH3− CH−CH− C− CH−CH3
OH 4CH− CH3
CH3 CH2 OH CH3
5 CH3
CH3
3、4−二甲 −2−戊醇 基
2,3,5-三甲基-4-乙基 −3−己醇
命名芳香醇时,将芳环看作取代基。
−CH2−OH 苯甲醇
−CH2 −CH2 −OH 2−苯乙醇
3
2
1
−CH2 −CH−CH3
混溶,毒性小。 φB=75%的乙醇溶液作外用消毒剂,称为消毒酒精。 φB=25%~50%乙醇溶液给高烧病人擦浴,称为擦浴酒精。 φB=50%的乙醇溶液还可以防止褥疮。
3.丙三醇(俗名甘油) 无色粘稠带有甜味的液体,能与水和乙醇互溶。临床上
用甘油栓治疗便秘。
甘油具有两个相邻羟基能与氢氧化铜反应生成深蓝色的溶 液,利用此特性可鉴别甘油。
学习目的:
酚、醚
1、理解酚、醚的结构和分类。 2、掌握酚、醚的命名和酚的化学性质。 3、了解酚的物理性质、常见的酚和醚。
重点:酚、醚的结构、命名和酚的化学性质
难点:酚、醚的结构
复习: 1、学生进行醇的命名 2、醇的主要化学性质
醇能与活泼金属反应;与氢卤酸发生取代反应;在酸的 作用下,发生分子内和分子间脱水反应;在一定条件下, 伯醇氧化生成醛,仲醇氧化生成酮;甘油与新制的氢氧化 铜作用溶液显深蓝色。 3、学生版书:苯、甲苯、苯甲醇的结构式
第6章-醇酚醚PPT课件
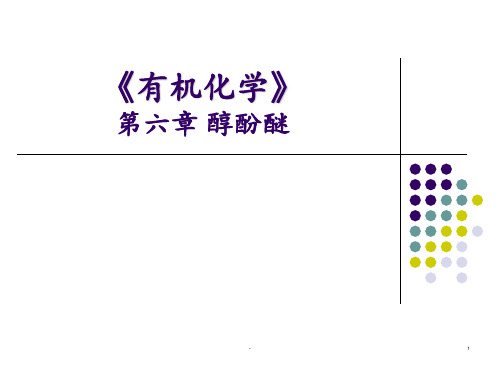
B. (CH3)2C(OH)CH2CH3
C. CH3CH2CH2OH
D. (CH3)3COH
2.下列化合物与卢卡斯试剂作用最快的是( B)
A. 2-丁醇
B. 2-甲基-2-丁醇
C. 2-甲基-1-丙醇 D. 1-丙醇
3.能区别6个碳以下的伯、仲、叔醇的试剂为 ( )B 。
A:高锰酸钾 D: 溴水
CH2 CH CH2 OH OH OH
甲醇 乙二醇 丙三醇
-
7
一、结构、分类、命名法
(二)命名:
1.普通命名法
根据烃基的名称称为“某醇”。
CH3-CH2-CH2OH
正丙醇
CH3-CH2-CH2-CH2OH
正丁醇
CH3-CH-CH3
OH 异丙醇、仲丙醇
CH2=CH-CH2-OH
烯丙醇
-
8
一、结构、分类、命名法
CH2CH3
CH3-CH-C-CH-CH2-CH3
CH3 OH CH3
- 2,4-二甲基-3-乙基-3-己醇
9
一、结构、分类、命名法
2.系统命名法
(2)不饱和醇 n 选择含有羟基和不饱和键(双键或叁键)在
内的最长碳链为主链,根据主链上所含碳原 子的数目称为“某烯醇或某炔醇”。 从靠 近羟基一端开始编号,注明不饱和键和羟基 的位次,命名为“m-某烯(炔)-n-醇”。
H-O-H + Na R-O-H + Na
NaOH + H2 RONa + H2
(反应激烈) (反应缓和)
酸性:H2O>ROH;碱性:NaOH<RONa
醇钠呈强碱性,遇水迅速水解为醇和氢氧化钠,溶液滴入酚酞试液呈红色 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
大于6个碳的醇(苄醇除外)不溶于卢卡斯试剂,易混淆实验现象。
3.与酸反应(成酯反应)
1)与无机酸反应
醇与含氧无机酸硫酸、硝酸、磷酸反应生成无机酸酯。
高级醇的硫酸酯是常用的合成洗涤剂之一。如C12H25OSO2ONa(十二烷基磺酸钠)。
2)与有机酸反应
利用醇、酚与NaOH和NaHCO3反应性的不同,可鉴别和分离酚和醇。
当苯环上连有吸电子基团时,酚的酸性增强;连有供电子基团时,酚的酸性减弱。
(2)与FeCl3的显色反应
酚能与FeCl3溶液发生显色反应,大多数酚能起此反应,故此反应可用来鉴定酚。
不同的酚与FeCl3作用产生的颜色不同。见P292表10-6。
§8.2.2酚的化学性质
羟基即是醇的官能团也是酚的官能团,因此酚与醇具有共性。但由于酚羟基连在苯环上,苯环与羟基的互相影响又赋予酚一些特有性质,所以酚与醇在性质上又存在着较大的差别。
1.酚羟基的反应
(1)酸性
酚的酸性比醇强,但比碳酸弱。
故酚可溶于NaOH但不溶于NaHCO3,不能与Na2CO3、NaHCO3作用放出CO2,反之通入CO2于酚钠水溶液中,酚即游离出来。利用酚的这种能溶于碱,而又可用酸将它从碱溶液中有离出来的性质,工业上常被用来回收和处理含酚污水。
叔醇一般难氧化,在剧烈条件下氧化则碳链断裂生成小分子氧化物。
2)脱氢:伯、仲醇的蒸气在高温下通过催化活性铜时发生脱氢反应,生成醛和酮。
§8.2酚(1.5学时)
§8.2.1酚的结构及命名
1.结构
酚是羟基直接与芳环相连的化合物(羟基与芳环侧链的化合物为芳醇),即酚是烃的羟基衍生物。
2.命名
酚的命名一般是在酚字的前面加上芳环的名称作为母体,再加上其它取代基的名称和位次。特殊情况下也可以按次序规则把羟基看作取代基来命名。
2.脂肪醇、脂环醇和芳香醇
3.一元醇、二元醇和多元醇。
两个羟基连在同一碳上的化合物不稳定,这种结构会自发失水,故同碳二醇不存在。另外,烯醇是不稳定的,容易互变成为比较稳定的醛和酮。
三、醇的命名
1.俗名:如乙醇俗称酒精,丙三醇称为甘油等。
2.简单的一元醇用习惯命名法命名。
例如:
3.系统命名法
结构比较复杂的醇,采用系统命名法。选择含有羟基的最长碳链为主链,以羟基的位置最小编号,称为某醇。
教案(章、节备课)
学时:4
章、节
第六章醇、酚、醚
教学目的和要求
1.掌握醇、酚、醚的结构、分类、命名;
2.掌握醇、酚、醚的主要化学性质;
3.掌握醇、酚、醚的鉴别方法
教学
重点
难点
重点:醇、酚、醚的命名;醇、酚、醚的主要化学性质和鉴别方法
难点:醇、酚、醚的主要化学性质
教学进程(含章节教学内容、学时分配、教学方法、教学手段、辅助手段)
备注
涉及到醇的酸性可能学生难以理解,要以相对性来解释;醇和酚的性质上差异和化学鉴别方法是重点。
•《有机化学》汪小兰主编(第四版)高等教育出版社,2010
•《有机化学》王积涛主编(第二版)南开大学出版社,2009
•《有机化学》胡红纹主编(第三版)高等教育出版社,2006
•《有机化学》邢其毅主编(第三版)高等教育出版社,2005
/
2.与氢卤酸反应(制卤代烃的重要方法)
1)反应速度与氢卤酸的活性和醇的结构有关。
HX的反应活性:HI>HBr>HCl
2)醇的活性次序:烯丙式醇>叔醇>仲醇>伯醇>CH3OH
例如,醇与卢卡斯(Lucas)试剂(浓盐酸和无水氯化锌)的反应:
Lucas试剂可用于区别伯、仲、叔醇,但一般仅适用于3—6个碳原子的醇。
4.脱水反应
醇与催化剂共热即发生脱水反应,随反应条件而异可发生分子内或分子间的脱水反应。
醇的脱水反应活性:3°R-OH>2°R-OH>1°R-OH
例如:
醇脱水反应的特点:
主要生成札依采夫烯,例如:
5.氧化和脱氢
1)氧化:伯醇、仲醇分子中的α-H原子,由于受羟基的影响易被氧化。
伯醇被氧化为羧酸。
仲醇一般被氧化为酮。脂环醇可继续氧化为二元酸。
1.烊盐的生成
醚的氧原子上有未共用电子对,能接受强酸中的H+而生成烊盐。
烊盐是一种弱碱强酸盐,仅在浓酸中才稳定,遇水很快分解为原来的醚。利用此性质可以将醚从烷烃或卤代烃中分离出来。
醚还可以和路易斯酸(如BF3、AlCl3、RMgX)等生成烊盐。
烊盐的生成使醚分子中C-O键变弱,因此在酸性试剂作用下,醚链会断裂。
(1)卤代反应苯酚与溴水在常温下可立即反应生成2,4,6三溴苯酚白色沉淀。
反应很灵敏,很稀的苯酚溶液(10ppm)就能与溴水生成沉淀。故此反应可用作苯酚的鉴别和定量测定。
如需要制取一溴代苯酚,则要在非极性溶剂(CS2,CCl4)和低温下进行。
(2)硝化苯酚比苯易硝化,在室温下即可与稀硝酸反应。
邻硝基苯酚易形成分子内氢键而成螯环,这样就削弱了分子内的引力;而对硝基苯酚不能形成分子内氢键,但能形成分子间氢键而缔合。因此邻硝基苯酚的沸点和在水中的溶解度比其异构体低得多,故可随水蒸气蒸馏出来。
Na与醇的反应比与水的反应缓慢的多,反应所生成的热量不足以使氢气自燃,故常利用醇与Na的反应销毁残余的金属钠,而不发生燃烧和爆炸。
CH3CH2O-的碱性比-OH强,所以醇钠极易水解。
醇的反应活性:CH3OH>伯醇(乙醇)>仲醇>叔醇
pKa 15.09 15.93>19
醇钠(RONa)是有机合成中常用的碱性试剂。金属镁、铝也可与醇作用生成醇镁、醇铝。
与FeCl3的显色反应并不限于酚,具有烯醇式结构的脂肪族化合物也有此反应。
(3)酚醚的生成
醚不能分子间脱水成醚,一般是由醚在碱性溶液中与烃基化剂作用生成。
在有机合成上常利用生成酚醚的方法来保护酚羟基。
酚也可被卤素取代,但不象醇那样顺利;酚也可以生成酯,但比醇困难。
2.芳环上的亲电取代反应
羟基是强的邻对位定位基,由于羟基与苯环的P-π共轭,使苯环上的电子云密度增加,亲电反应容易进行。
蒸馏放置过久的乙醚时,要先检验是否有过氧化物存在,且不要蒸干。
检验方法:硫酸亚铁和硫氰化钾混合液与醚振摇,有过氧化物则显红色。
除去过氧化物的方法:(1)加入还原剂(5%的FeSO4)于醚中振摇后蒸馏。
(2)贮藏时在醚中加入少许金属钠。
教法:启发、互动教学,培养自主学习能力
1.通过设问、启发来引导学生深入思考、激发兴趣
例如:
多元醇的命名,要选择含-OH尽可能多的碳链为主链,羟基的位次要标明。
例如:
§8.2醇的性质
§8.2.1醇的物理性质
1.性状:(略)
2.沸点:
3.溶解度:
4.结晶醇的形成
低级醇能和一些无机盐(MgCl2、CaCl2、CuSO4等)作用形成结晶醇,亦称醇化物。
如:
§8.1.2醇的化学性质
1.与活泼金属的反应
2.醚链的断裂
在较高温度下,强酸能使醚链断裂,使醚链断裂最有效的试剂是浓的氢碘酸(HI)。
醚键断裂时往往是较小的烃基生成碘代烷,例如:
芳香混醚与浓HI作用时,总是断裂烷氧键,生成酚和碘代烷。
3.过氧化物的生成
醚长期与空气接触下,会慢慢生成不易挥发的过氧化物。
过氧化物不稳定,加热时易分解而发生爆炸,因此,醚类应尽量避免暴露在空气中,一般应放在棕色玻璃瓶中,避光保存。
教学内容及学时分配:
醇、酚和醚都是烃的含氧衍生物,它们可以看作是水分子中的氢原子被烃基取代的化合物。
§8.1醇(2学时)
§8.1.1醇的结构、分类和命名
一、醇的结构
醇可以看成是烃分子中的氢原子被羟基(OH)取代后生成的衍生物(R-OH)。
二、醇的分类
1.一级醇(伯醇)、二级醇(仲醇)、三级醇(叔醇)。
5).多元醚:首先写出潜含多元醇的名称再写出另一部分烃基的数目和名称,最后加上“醚”字。
§8.3.2醚的化学性质
醚是一类不活泼的化合物,对碱、氧化剂、还原剂都十分稳定。醚在常温下与金属Na不起反应,可以用金属Na来干燥。醚的稳定性仅次于烷烃。但其稳定性是相对的,由于醚键(C-O-C)的存在,它又可以发生一些特有的反应。
1)简单醚在“醚”字前面写出两个烃基的名称。例如,乙醚、二苯醚等。
2)混醚是将小基排前大基排后;芳基在前烃基在后,称为某基某基醚。
例如:
3)结构复杂的醚用系统命名法命名。可以看作是烃的衍生物来命名,将较大的烃基作母体,剩下的RO-部分看作取代基。
例如:
4)环醚:命名常采用俗名,没有俗名的称为氧杂某烷
2.通过讲授、讨论解决问题
3.“教、学、做”相结合
手段:多媒体课件、板书、课堂练习
h, i)、8.5(b, d, h)、8.6(b, c)、8.8、8.9(a, c, e, g, h)
完成作业看参考书的相关内容
预习第七章醛、酮、醌
主要
参考资料
•《有机化学》范望喜,张爱东主编华中师范大学出版社,2007
3.氧化反应
酚易被氧化为醌等氧化物,氧化物的颜色随着氧化程度的深化而逐渐加深,由无色而呈粉红色、红色以致深褐色。例如:
多元酚更易被氧化。
对苯二酚是常用的显影剂。
酚易被氧化的性质常用来作为抗氧剂和除氧剂。
四、重要的酚(自学)
§8.3醚(0.5学时)
§8.3.1醚的结构,分类和命名
1.结构
2.分类
3.命名
