分析化学第6章氧化还原滴定法解析
分析化学06 氧化还原滴定法

越大, K’ 越大,反应越完全。
/ 1 / 2
例题:p139
6.2.2 化学计量点时反应进行的程度
O' O' n2 Ox1 + n1 Red2 = n2 Red1 + n1 Ox2 lg K = (1 2 )n
0.059
?
/ 1 / 2
(2) 如果两个电对反应完全,应满足什么条件? n2 Ox1 + n1 Red2 = n2 Red1 + n1 Ox2 氧化还原反应进行的程度可用平衡常数的大小来 衡量。
n2 Ox1 + n1 Red2 = n2 Red1 + n1 Ox2 两个半电池反应的电极电位为: 0.059 cOx1 O' 1 1 lg n1 cRed1
n2 Ox1 + n1 Red2 = n2 Red1 + n1 Ox2
lg K =lg[(
cRe d1 cox1
)n2(
cox2 cRe d2
(1O' 2O' )n1n2 (1O' 2O' )n )n1 ]= = 0.059 0.059
K’ 与两电对的条件电极电位差和 n1 、n2有关。
略不计。
2. 副反应的影响 主要影响因素
ox/Red
O ox/Red
ox Red cox cox RT RT O' ln ox/Red ln nF Red ox cRed nF cRed
电对的氧化态(cOX)生成沉淀(或配合物)时,电极电位降低;
还原态(cRed)生成沉淀(或配合物)时,电极电位增加。
在特定条件下,氧化态与还原态的总浓度均为1mol.L-1(即 cox/cRed = 1) 时的实际电极电位叫条件电极电位。条件电极电位 能更准确判断氧化还原反应进行的方向、次序及反应完成的程 度。
分析化学 氧化还原滴定法
a 与 C的关系为:
aOx
Ox
Ox
C Ox Ox Ox
aRed
Red
Re d
C Red Red Red
-活度系数 -副反应系数
Ox / Re d
Ox / Re d
RT ln γOx Red cOx nF γ c Red Ox Red
Ox / Re d
RT ln γOxRed
Red
增大,
0
值增大。
Eg. 2Fe3+ + 2I = I2 + 2Fe2+
Fe3+ + e = Fe2+ φFe3+/Fe2+ =0.771V I2 + 2e = 2I- ΦI2/I- =0.54V
例如,用间接碘量法测定Cu2+时,反应为
2Cu2 4I
2CuI I2
若试液中有Fe3+共存时,Fe3+也可以氧化I-生成I2,
0' 0 0.059lg OxRed
n
Red Ox
从条件电位的定义式知道,影响条件电位的因素 就是影响电对物质的活度系数和副反应系数的因素。
主要包括:盐效应 酸效应 生成沉淀 生成配合物
活度系数 副反应系数
1.盐效应:溶液中的电解质浓度对条件电位 的影响作用。
电解质浓度 离子强度 活度系数
*以标准氢电极为参照电极的相对值。
2、书写Nernst方程式时注意的问题:
(1)固体、溶剂的活度为1mol/L;
(2)气体以大气压为单位;
(3)如果半电池中除了氧化态和还原态外, 还有其他组分如:H+、OH参加, 活度也要包 括到Nernst方程式中;
学习氧化还原滴定法(分析化学课件)

sp
n11 (n1
n22 n2)
如果 n1=n2
sp
1
2
2
④化学计量点后
通常由滴定剂氧化还原电对的浓度比求得电极电位
1
1
0.059 n1
lg
cOx1 c Re d1
设x为所加入氧化剂按化学计量的百分数
当x>100时
1
0.059 n1
lg
x
100 x
当x=100.1时
1
0.059 n1
3
当x=101.0时
条件电极电位是指在某一特定条件下,电对的氧化态总浓度和还 原态的总浓度均为1mol/L时的实际电极电位,它在条件不变时为一 常数
2.条件电极电位
(Ox / Red) (Ox / Red) 0.059 lg cOx
n
cRed
(Ox / Red) (Ox / Red) 0.059 lg Ox Red
受诱反应
MnO
4
5Fe2
16H
2Mn 2
5Fe3
8H2O
作用体
诱导体
诱导反应
注意诱导反应和催化反应的区别: 诱导反应:诱导体参与反应变为其他物质 催化反应:催化剂参与反应恢复到原来的状态
第六章 氧化还原滴定法
第二讲 氧化还原滴定原理及指示剂
一、氧化还原滴定原理 二、氧化还原指示剂
一、氧化还原滴定原理
二、平衡常数和准确滴定的判据
1、氧化还原反应的平衡常数——衡量反应进行的完全程度
n2Ox1 + n1Red2=n2Red1 + n1Ox2
1
1
0.059 n1
lg
cOx1 c Re d1
2
水分析化学6 氧化还原滴定法

的大小由电对的氧化态和还原态的材料自身性质及温度 决定。当二者一定时, 为常数。
第六章 氧化还原滴定法
2、条件电极电位
以HCl溶液中Fe(Ⅲ)/Fe(Ⅱ)这一电对为例,在298.15K时,由能 斯特方程式可得:
在盐酸溶液中,Fe(Ⅲ)以Fe3+、FeOH2+、FeCl2+、FeCl63-等形 式存在;而Fe(Ⅱ)也以Fe2+、FeOH+、FeCl+、FeCl42-等形式 存在。那么,Fe(Ⅲ)与Fe(Ⅱ)的分析浓度与游离Fe3+和Fe2+的 平衡浓度之间的关系并不相等。
第六章 氧化还原滴定法
生成沉淀的影响
在氧化还原反应中,当加入一种可以与氧化态或者还原态生成 沉淀的沉淀剂时,会改变电对的电极电位。根据能斯特方程式, 若电对的氧化态生成沉淀,则电位降低;反之,还原态生成沉 淀则使电对的电位增高。 例如,碘量法测铜是基于以下反应:
从标准电极电位看,应该是I2氧化Cu+,但是由于Cu2+/ Cu+中 Cu+生成的了CuI沉淀使得电对的电位升高,超过了0.54V,从而 氧化还原反应的方向发生了转变。
第六章 氧化还原滴定法
第六章 氧化还原滴定法
主要内容:
氧化还原平衡
氧化还原反应的速度
氧化还原滴定过程及滴定曲线
氧化还原滴定的指示剂
氧化还原滴定法在水质分析中的应用
第六章 氧化还原滴定法
氧化还原滴定法:是以氧化还原反应为基础的滴定 方法。 氧化还原反应的特点:
是电子转移反应(反应机理复杂); 反应常分步进行; 反应速率慢,且多有副反应。
发生氧化还原反应的两个电对的条件电极电位相差 得越大,其K’越大,说明反应进行得越完全。还可 以根据两电对的 ' 以及各自转移的电子数n1、n2 推导出用于判别可否用于氧化还原滴定分析的通式。
第6章 氧化还原滴定法(课件)

0.09V
电对的电极电位衡量氧化或还原能力的强弱 电对的电极电位越高,其氧化态的氧化能力 越强。
(还原态的还原能力越弱)——氧化剂
电对的电极电位越低,其还原态的还原能力 越强。
(氧化态的氧化能力越弱)—— 还原剂
Ox/Red
O Ox/Red
RT aOx 0.059 aOx O ln Ox/Red lg nF a Red n a Red
Cu2+ +e I2 + 2e Fe3+ + e Cu+ 2I' Cu
I
2
2
Cu
0.87V
I
0.535V
Fe 2+ Fe 3
Fe2
0.771V
Fe3+的氧化能力强,干扰Cu2+的测定
[F ]
F (H )
cF
0.2 1.1 10 m ol/ L H 1 k HF [ H ]
氧化还原电对:I2/I-,S4O62-/S2O32-,Fe3+/Fe2+ 氧化还原半反应:
Ox ne
Red
由物质的氧化态和其对应的的还原态所构成。
若干电对的标准电极电位(298.15K)
电对
K+/K Zn2+/Zn Fe2+/Fe H+/H2 Cu2+/Cu Ag+/Ag F2/F-
氧化态+ne-
第六章
氧化还原滴定法
+1
+2
-1
+3
NaClO +2FeSO4+ H2SO4 = NaCl
氧化剂 还原剂 还原产物
+ Fe2(SO4)3 + H2O
第六章氧化还原滴定法解析
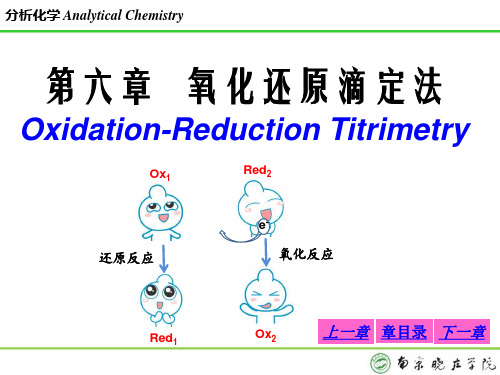
= ox/ Red
+
RT nF
ln oxRed Red ox
当cOx/cRed = 1 时,条件电极电位是在特定条件下,校正了各 种外界因素(活度系数、副反应影响)后的实际电极电位。
(P437)
分析化学— 氧化还原滴定法
三、 影响条件电极电位的因素
(一)离子强度 (二)沉淀或络合等副反应的影响
K Sp[CuI]
Cu 2 =I =1.0mol / L
Cu I 1.11012
> Cu 1.11012 1.11012 1.0
Cu2+ /Cu+ = 0.87 V
I2/I
条件电极电位 能更准确判断氧化还原反应进行的方向
分析化学— 氧化还原滴定法
(二)沉淀或络合等副反应的影响
'(Fe3+ / Fe2+ ) = (Fe3+ / Fe2+ ) + 0.059lg Fe2+
Fe3+
= 0.77 - 0.059 7.7 = 0.32 V < 0.54 V = (I2 / I- )
2. 生成络合物
例:用碘量法测定铜矿中的铜 (铜矿中含有少量铁)
2Cu2+ + 4I- 2CuI + I2
θ (Fe3+ / Fe2+ ) = 0.77V, (I2 / I- ) = 0.54V
How? Fe3+也能氧化I-,因而干扰Cu2+的测定。
加入NaF,则Fe3+与F-形成很稳定的络合物,Fe3 Fe2 电 对的电极电位显著降低,Fe3+失去氧化I-的能力。
分析化学— 氧化还原滴定法
分析化学答案第六章 氧化还原滴定法

计算锌电对的实际电位值。
解:(1)求[NH3]:查 的Ka=5.7×10-10
(2)求 :查附表VII-1得:
查附表VII-2得:pH = 10时,lgαZn(OH)=2.4,则αZn(OH)=251.2
习题:
1.配平下列氧化还原反应方程式
2.写出下列电对电位的Nernst方程式
3.测定样品铁含量常用SnCl2将Fe3+预还原为Fe2+,然后用氧化剂标准液滴定,
求25℃时反应平衡常数,判断该反应是否可行。
解:SnCl2将Fe3+预还原为Fe2+的反应:
n=2,
4.电对Zn2++2e Zn, ,忽略离子强度的影响,计算在pH=10.00,CNH3=
解:(1)求反应的平衡常数反应电对的半电池反应和标准电位为:
n = 5
(2)求[Br2]
6.精密称取0.1936g基准试剂级K2Cr2O7,溶于水后加酸酸化,随后加入足够量的KI,用Na2S2O3标准溶液滴定,用去33.61mL达终点。计算Na2S2O3标准溶液的浓度。
解:
7.精密称取漂白粉样品2.622g,加水溶解,加入过量KI,用H2SO4(1mol/L)酸化。析出I2,立即用Na2S2O3标准溶液(0.1109mol/L)滴定,用去35.58mL到达终点。计算样品有效氯的含量。
解:
有效氯含量即Cl2%
8.精密称取苯酚样品0.4083g,用少量10%NaOH溶解,转入250mL容量瓶,稀释至刻度,摇匀。吸取25.00mL放入碘量瓶,加溴液(KBrO3+KBr)25.00mL,盐酸和适量KI。最后用Na2S2O3标准溶液(0.1084mol/L)滴定,用去20.04mL至终点。另取25.00mL溴液做空白试验,用去相同浓度Na2S2O3溶液41.60ml滴至终点。计算样品中苯酚的质量分数。( )
分析化学(第六版)第六章习题详解

第六章 氧化还原滴定法思考题答案1. 处理氧化还原平衡时,为什么引入条件电极电位?外界条件对条件电极电位有何影响?答:(1) 在能斯特方程中,是用离子的活度而非离子的浓度计算可逆氧化还原电对的电位。
实际上通常知道的是离子的浓度而不是活度,往往忽略溶液中离子强度的影响,以浓度代替活度进行计算。
但实际上,溶液浓度较大时,溶液中离子强度不可忽略,且溶液组成的改变(即有副反应发生)也会影响电极的电对电位,为考虑此两种因素的影响,引入了条件电极电位。
(2) 副反应:加入和氧化态产生副反应(配位反应或沉淀反应)的物质,使电对电极电位减小;加入和还原态产生副反应(配位反应或沉淀反应)的物质,使电对电极电位增加。
另外有H +或OH -参加的氧化还原半反应,酸度影响电极电位,影响结果视具体情况而定。
离子强度的影响与副反应相比一般可忽略。
2. 为什么银还原器(金属银浸于1 mol.L -1 HCl 溶液中)只能还原Fe 3+而不能还原Ti(Ⅳ)?试由条件电极电位的大小加以说明。
答:金属银浸于1 mol.L -1 HCl 溶液中产生AgCl 沉淀。
+sp +-(Ag /Ag)0.059lg[Ag ](AgCl) (Ag /Ag)0.059lg[Cl ]K ϕϕϕθθ+θ=+=+ 在1 mol.L -1HCl 溶液中+sp 9.50(Ag /Ag)0.059lg (AgCl) 0.800.059lg100.24(V)K ϕϕ'θθ-=+=+=在1mol·L -1 HCl 中,3+2+(Fe /Fe )=0.70ϕ'θ, ()()()04.0/T i T i '-=ⅢⅣθϕ,故银还原器(金属银浸于1 mol.L -1 HCl 溶液中)只能还原Fe 3+而不能还原Ti(Ⅳ)。
3. 如何判断氧化还原反应进行的完全程度?是否平衡常数大的氧化还原反应都能用于氧化还原滴定中?为什么?答:(1) 根据条件平衡常数判断,若滴定允许误差为0.1%,要求lg K ≥3(n 1+ n 2),即(E 10,-E 20,)n / 0.059≥3(n 1+ n 2),n 为n 1,n 2的最小公倍,则n 1 = n 2 =1, lg K ≥3(1+1)≥6, E 10’-E 20’≥0.35V n 1 =1, n 2 =2,lg K ≥3(1+2)≥9, E 10’-E 20’≥0.27V ;n 1= n 2 =2, lg K ≥3(1+1)≥6, E 10’- E 20’≥0.18V (E 0’=ϕθ')(2) 不一定。
分析化学第六章氧化还原滴定法

从0.771 降为0.29 V,即
Fe3 Fe2
I2 I
因而Fe3+不再能氧化I-,
从而消除了Fe3+的干扰。
(三)溶液酸度对电极电位的影响
有些氧化剂的氧化作用必须在酸性溶液中才能发生,而且酸性 越强,其氧化能力往往越强。例如:KMnO 4 、K2Cr2O7 和 (NH 4 )S2O8 等。许多有H+或OH-参加的氧化还原反应,当溶液的酸度发生变 化时,就有可能改变反应进行的方向。
需要引进一个经验校正系数 γ(活度系数),以表示实际溶液
与理想溶液的偏差。
离子强度与活度系数的关系
德拜-休克尔公式
lg A zz I
z+和z-分别表示正、负离子所带电荷,在298K时的水溶 液中A值为0.509,I表示离子强度。
0.059 lg aox
n
aRed
由此式可以看出:影响氧化还原反应电位的因素是:氧化还 原电对的性质( ),氧化型和还原型活度。书后附录有常 见氧化-还原电对的 值。
则 Fe3 = cFe3 8.71014 mol/L α Fe 3
Fe 2 c 2 1.0 10 5mol/L Fe
根据能斯特方程式得:
Fe3
= Fe2
Fe3
Fe2
0.059lg
Fe 3 Fe 2
=0.
771
0.
059lg
8. 7 1014 1. 0 105
=0.29V
说明加入NaF后,Fe3+与F-生成了稳定的氟络合物,使 Fe3 Fe2
Ox n e Red
根据能斯特方程式:
0.059 lg aox
n
aRed
为标准电极电势, n为半反应中1mol/L氧化剂或还原剂电子
水分析化学第6章氧化还原滴定法

6.1 氧化还原平衡
6.1.2 电极电位与能斯特方程
1. 氧化还原反应的实质—电子的转移 氧化还原反应平衡式: Ox1 + Red2 → Red1+ Ox2 氧化还原半反应: Ox + ne- →Red 其中:n表示电子转移数。
接受电子倾向越大的物质是强的氧化剂; 给出电子倾向越大的物质是强的还原剂;
O /R d x eO /R d x e 0 .0 nl5 g R O 9 d R e x O d ex 0 .0 nl5 [ g [ O R d 9 ] ] x e
θ 称条件电极电位
O/x RdeO ’ /x Rde0.0 n5lg 9[[O Rd]]e x
e.g. F3eeF2e C 2 O 7 2 r 6 e 1H 4 2 C 3 r 7 H 2 O
②条件电位差对氧化还原反应速度的影响
当Δθ’增大时,氧化还原反应的反应速度增大。
③反应物浓度对氧化还原反应速度的影响 反应物浓度c增加,反应速率增大(质量作用定律)。
6.2 氧化还原反应的速度
氧化还原反应能否进行不仅与Δθ有关, 还与反应速度有关。
影响反应速度的因素:
电子层结构与
化学键
速
氧化剂、还原剂的性质
度 的
浓度的影响
电极电位
影
温度的影响
反应历程
响
因
催化剂的作用
素
诱导作用
6.2 氧化还原反应的速度
①电子层结构与化学键对氧化还原反应速度的影响 一般规律:只涉及电子转移的反应快;涉及断键的反应慢
所以:
Ce4 /Ce3
化工分析-第六章:氧化还原滴定法解析

2.标定 ①基准物质:H2C2O4·2H2O 、Na2C2O4 As2O3、 Fe丝、(NH4)2Fe(SO4)2·6H2O 等
②滴定反应条件: ❖ (1)温度 70~85℃
❖ (2)酸度 0.5~1mol·L-----H2SO4介质 ❖ (3)滴定速度: 先慢后快再慢
❖ (4)终点的判断:淡粉红色,30秒不退色。
❖ 2. 优点
❖ ( 1)K2Cr2O7容易提纯,且很稳定,可作基准物质; (2)选择性较高,可以盐酸作为介质; (3)指示剂:二苯胺磺酸钠、邻苯胺基苯甲酸。
二、标准溶液的配制
❖ 1.直接配制法:独立完成实验操 作
❖ 2.间接配制法:标定法
三、应用示例
(一)铁矿石中全铁的测定
试样 浓HCl溶解 Fe3+ ,Fe2+ SnCl2还原 Fe2+ HgCl2除Sn2+
❖ 2、方法特点
(1). KMnO4是强氧化剂,可以测定多种无机物 和有机物,应用广泛。在不同的酸度条件下, KMnO4的还原产物不同。
(2).KMnO4是自身指示剂 (3).选择性差 由于KMnO4的强氧化性,许多 物质都能使其还原,因此共存物质的干扰严 重,例如,KMnO4法不能用HCl作为介质。
氧化还原反应比较复杂,往往是分步进行, 各步反应快慢不一,反应速率将决定于最 慢的那一步
❖
1.浓度对反应速度的影响
❖
2.温度的影响
❖
3.催化剂的影响
❖ 三、氧化还原指示剂
1.氧化还原指示剂 (1)二苯胺磺酸钠 (2)邻二氮杂菲亚铁盐 2.其它指示剂 (1)自身指示剂:如KMnO4 (2)专属指示剂:如碘量法中的淀粉
二、标准溶液的配制与标定
❖ 以Na2S2O3标准溶液的制备为例进行实验:
分析化学6-1氧化还原滴定法ppt课件

精选ppt课件
10
氧化还原滴定法/外界条件对电极电位的影响
精选ppt课件
11
氧化还原滴定法/外界条件对电极电位的影响
精选ppt课件
12
氧化还原滴定法/外界条件对电极电位的影响
• 酸度的影响 若有 H+或 OH- 参加氧化还原半反应,则酸 度变化直接影响电对的电极电位。
精选ppt课件
13
精选ppt课件
14
氧化还原滴定法/外界条件对电极电位的影响
精选ppt课件
15
氧化还原滴定法/外界条件对电极电位的影响
精选ppt课件
16
此课件下载可自行编辑修改,供参考! 感谢您的支持,我们努力做得更好!
精选ppt课件
17
• 在特定条件下,当氧化态和还原态的浓度均为1 mol/L时的实际电极电位。它在特定条件不变的情 况下为一常数。
精选ppt课件
3
氧化还原滴定法/氧化还原反应平衡
对称电对:氧化态与还原态的系数相同。 如: Fe3+ + e = Fe2+
MnO4- + 8H+ + 5e = Mn2+ + 4H2O
不对称电对:氧化态与还原态系数不同。 如: I2 + 2e = 2 ICr2O72- + 14H+ + 6e = 2Cr3+ + 7H2O
精选ppt课件
1
氧化还原滴定法
• 氧化还原滴定法----以氧化还原反应为基础的摘定分析法 • 特点 • 基于电子转移的反应,反应机理比较复杂 • 常伴随有副反应,没有确定的计量关系 • 许多反应速率较慢 • 常有诱导反应发生
精选ppt课件
第六章氧化还原滴定法

2)反应温度与滴定速度 温度应在15℃以下。 温度高:
HNO2分解与逸失。可采用“快速滴定法”
3)苯环上取代基团的影响
在苯胺环上:有吸电子基团取代 如: -NO2、-SO3H、-COOH等 使反应加速;
有斥电子基团(-OH、 -OR)使反应 减慢。
三、亚硝酸钠法的指示剂
•高锰酸钾法
标准溶液:高锰酸钾。 指示剂:自身指示剂。 测定条件:控制在1~2mol/L H2SO4溶液测定
还原性物质。
•亚硝酸钠法
(1)重氮化滴定法:在酸性介质中,用亚硝酸 钠标准溶液滴定芳伯胺化合物,发生重氮化反 应; (2)亚硝化滴定法:用亚硝酸钠标准溶液滴定
芳仲胺化合物,发生亚硝基化反应。
氧化还原反应的程度也是用平衡常数 的大小来衡量。氧化还原反应的平衡常数 与有关电对的电极电位有关。
(二)氧化还原反应进行的速度
氧化还原反应平衡常数的大小,可以 表示反应进行的程度,但不能说明反应的 速度。有许多氧化还原反应,虽然从理论 上看可以进行完全,但实际上由于反应速 度太慢而几乎觉察不出反应的进行。例如, 水溶液中的溶解氧:
2、书写Nernst方程式时注意几点:
(1)固体、溶剂的活度为1mol/L (2)气体以大气压为单位 (3)半反应中有其它组分参加,其它组分的
活度应包括在Nernst方程式中
3、条件电极电位 为了讨论方便,我们以下式为例来
进行讨论:
Ox + n e Red
• 二、氧化还原反应进行的程度和速度 (一)氧化还原反应进行的程度
101.0 110.0 150.0 200.0
100.0 95.0 90.0 80.0 60.0 50.0 40.0 10.0 1.0 0.1
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
6.1 氧化还原反应平衡
6.1.1 条件电极电位(Conditional Electrode Potential)
氧化还原半反应(Redox Half-Reaction)为:
Ox(氧化态) + n e- = Red(还原态)
可逆电对的电位可用能斯特方程式( Nernst Equation)
2020年10月12日4时17分
诱导反应(共轭反应):
MnO4- + 5Fe2++ 8H+ = Mn2+ + 5Fe3+ + 4H2O (诱导反应 ) 2MnO4- + 10Cl- + 16H+ = 2Mn2+ + 5Cl2 + 8H2O (受诱反应)
MnO4- 称为作用体; Fe2+ 称为诱导体; Cl- 称为受诱体; 实际滴定时可以不加 Mn2+,利用反应开始后生成 的Mn2+的自动催化作用。
n1n2
cOx1
cRed2
0.059 lg
n1n2
K
2020年10月12日4时17分
K’ 越大,反应越完全。K’ 与两电对的条件电极电位 差和 n1 、n2有关。若要求反应完全程度达到 99.9%以 上,即在到达化学计量点时:
cOx2 / cRed2 ≥ 103 ; cRed1 / cOx1 ≥ 103
n2 Ox1 + n1 Red2 = n2 Red1 + n1 Ox2 两个半电池反应的电极电位为:
1
1O'
0.059 n1
lg
cOx1 cRed1
2
O' 2
0.059 n2
lg
cOx2 cRed2
滴定过程中,达到平衡时(1 = 2):
O' 1
O' 2
0.059 lg( cRed1 )n2 ( cOx2 )n1
RT nF
ln cox cRed
条
件电ຫໍສະໝຸດ 极电位:
O' ox/Red
O ox/Red
RT nF
ln
ox Red Red ox
当cox/cRed = 1 时,条件电极电位等于实际电极电位。 用条件电极电位能更准确判断氧化还原反应进行的方
向、次序及反应完成的程度。
2020年10月12日4时17分
6.1.2 外界条件对电极电位的影响
例:判断二价铜离子能否与碘离子反应
2Cu2+ + 4I- = 2CuI + I2
Cu2/Cu 0.16 V ;
I2 /I 0.54 V
从数据看,不能反应,但实际上反应完全。
原因:反应生成了难溶物CuI,改变了反应的方向。
Ksp(CuI) = [Cu+][I-] = 1.1 10-12
Cu 2/Cu
O Ox/Red
0.059 lg aOx
n
aRed
物质的氧化还原能力取决于其电位的高低,而其电位
的大小又与 及ɑOx/ɑRed有关。而ɑOx =γ Ox [Ox],
[Ox]= [Ox'] /αOx ,即电位的大小与外界条件的影响有 关,如金属离子在溶液中可能发生: 络合,沉淀等副
反应,故引入条件电位以表示有外界条件影响下实际
2020年10月12日4时17分
例:在高锰酸钾法滴定中
(1) KMnO4与C2O42-的滴定反应需要在75-85C下进行, 以提高反应速率。但温度太高将使草酸分解。 (2) 在反应开始时,需要Mn2+。
二价锰的作用: 催化剂 降低 Mn3+/Mn2+ 电对的电位,防止诱导反应(共 轭反应)的发生。
6.2.1 条件平衡常数
在氧化还原滴定反应过程中,需要判断: (1) 反应是否进行完全,即终点误差是否满足要求; (2) 如果两个电对反应完全,应满足什么条件?
n2 Ox1 + n1 Red2 = n2 Red1 + n1 Ox2 氧化还原反应进行的程度可用平衡常数的大小来 衡量。
2020年10月12日4时17分
表示:
Ox/Red
O Ox/Red
RT nF
ln
aOx aRed
O Ox/Red
0.059 lg n
aOx aRed
: 电对的标准电极电位(Standard Electrode Potential)
2020年10月12日4时17分
Ox/Red
O Ox/Red
RT ln aOx nF aRed
第六章 氧化还原滴定法
6.1 氧化还原反应平衡 6.2 O.R反应进行的程度 6.3 O.R反应的速率与影响因素 6.4 O.R滴定曲线及终点的确定 6.5 O.R滴定法中的预处理 6.6 高锰酸钾法 6.7 重铬酸钾法 6.8 碘 量 法 6.9 其他氧化还原滴定法 6.10 氧化还原滴定结果的计算
O C u2 /C u
[Cu2 ] 0.059 lg [Cu ]
O
[Cu2 ][I ] 0.059 lg
C u2 /C u
KSp[CuI]
若控制[Cu2+] = [I-] = 1.0 mol ·L-1则: Cu2/Cu 0.87 V
2020年10月12日4时17分
6.2 氧化还原反应进行的程度
O 1
O 2
0.059 lg(103n1103n2 n1n2
)
0.059 n1n2
3(n1
n2 )
n1 = n2时
K'≥106
n1 = n2 = 1 时,为保证反应进行完全:
两电对的条件电极电位差必须大于0.4 V。
2020年10月12日4时17分
6.3 氧化还原反应的速率与影响因素
化学平衡:反应的可能性; 反应速率:反应的现实性。 影响反应速率的主要因素有: 1. 反应物浓度 反应物浓度↑,反应速率↑; 2. 催化剂 改变反应过程,降低反应的活化能; 3. 温度 温度每升高10℃,反应速率可提高2~3倍。 4. 诱导作用 由于一种氧化还原反应的发生而促进 另一种氧化还原反应进行的现象。
1.离子强度的影响
一般情况忽略离子强度的影响。
2. 副反应的影响 主要影响因素
电对的氧化态(cOX)生成沉淀(或配合物)时,电极电位降低; 还原态(cRed)生成沉淀(或配合物)时,电极电位增加。
3.酸度的影响
若有H+或OH-参加氧化还原半反应,则酸度变化直接影响电 对的电极电位。
2020年10月12日4时17分
的电位。
2020年10月12日4时17分
条件电极电位(Conditional Electrode Potential):
ox/Red
O ox/Red
RT nF
ln
aox aRed
ox/Red
O ox/Red
RT nF
ln ox c Red ox Red c ox Red
O' ox/Red
