硫及其化合物性质
硫和氮及其化合物的性质

4、硝酸的化学性质
⑪不稳定性:
4HNO3
hν,
4NO2 + O2 + 2H2O
浓硝酸应保存在棕色瓶中并置于阴凉处。
⑫强氧化性
③硝酸能氧化很多低价态的化合物,如S2- 、 SO32- 、I- 、Fe2+ 在酸性条件下NO3 - 与S2- 、SO32- 、 I - 、Fe2+ 因发生氧化还原反应不能共存于同一溶液中。
(3)装置D的目的是探究SO2 与品红作用的可逆性, 请写出实验操作及现象 ; 品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精 灯加热,溶液恢复为红色 。
例4.某化学兴趣小组为探究SO2的性质,按下图所示 装置进行实验。请回答下列问题:
(4)尾气可采用
NaOH
溶液吸收。
(2)还原性
在水溶液中二氧化硫是一种还原性较强的物质, 能使氯水(溴水、碘水)、三价铁盐溶液、酸性 高锰酸钾溶液褪色。 ①SO2+ X2+2H2O =4H++2X-+ SO42-(X=Cl、Br、I) ②SO2+2Fe3++2H2O=SO42-+2Fe2++4H+; ③5SO2+ 2MnO4-+2H2O =2Mn2++ 5SO42-+4H+
例2. [2012年普通高等学校招生全国统一考试
(山东卷)]下列由相关实验现象所推出的结论正 确的是 A . Cl2 、 SO2 均能使品红溶液褪色,说明二者 均有氧化性 B .向溶液中滴加酸化的 Ba(NO3)2 溶液出现白 色沉淀,说明该溶液中一定有SO42-
例2. [2012年普通高等学校招生全国统一考试
NO2 ⑤ ① NH4Cl ② NH3 ③ ⑨ N2 ④ NO ⑧ ⑩ HNO3 ⑥ ⑦
2025年高考化学总复习(人教版)第19讲硫及其化合物

第19讲 硫及其化合物【课程标准】 1.掌握硫及其重要化合物的主要化学性质及应用。
2.了解硫的氧化物对大气的污染与防治。
考点一 硫单质的性质1.自然界中的硫形态,游离态火山喷口附近或地壳的岩层里,化合态主要以硫化物和硫酸盐的形式存在 2.物理性质3.化学性质(1)氧化性:(0价→-2价)(2)还原性:(0价→+4价) S +O 2=====点燃SO 2(3)与碱发生歧化反应(如NaOH 溶液): 3S +6NaOH=====△2Na 2S +Na 2SO 3+3H 2O 。
[正误辨析]1.硫在自然界中仅以化合态存在( )2.硫在空气中燃烧的产物是SO 2,在纯氧中燃烧的产物是SO 3( ) 3.硫与铁粉和铜粉分别反应,都可生成二价金属硫化物( )4.等质量的S 6和S 8分子分别与足量的KOH 反应,消耗KOH 的物质的量相同( ) 5.常温下硫单质主要以S 8形式存在,加热时S 8转化为S 6、S 4、S 2属于物理变化( )6.汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理( ) 答案:1.× 2.× 3.× 4.√ 5.× 6.√正误判断(1)(2022·山东卷)“能化……银、铜、铁,奇物”,石硫黄(S)表现氧化性( ) (2)(2019·浙江卷)硫元素在自然界中的存在形式有硫单质、硫化物和硫酸盐等( ) 答案:(1)√ (2)√硫是生物必需的营养元素之一,下列关于自然界中硫循环(如图所示)说法正确的是( )A .含硫杆菌及好氧/厌氧菌促进了硫的循环B .硫循环中硫的化合物均为无机物C .上述硫循环中硫元素均被氧化D .烧煤时加石灰石,可减少酸雨及温室气体的排放 答案:A解析:硫酸盐和亚硫酸盐等在含硫杆菌及好氧/厌氧菌作用下缓慢转化成植物R 1-S -R 2,含硫杆菌及好氧/厌氧菌促进了硫的循环,故A 正确;硫循环中硫的化合物有含硫的有机物,不全是无机物,故B 错误;含硫杆菌及好氧/厌氧菌将硫酸盐、亚硫酸盐中的硫还原成R 1-S -R 2,硫循环中硫元素有时被氧化,有时被还原,故C 错误;烧煤时加石灰石,CaCO 3+SO 2=====△CaSO 3+CO 2可减少酸雨,除上述反应外石灰石分解生成二氧化碳,会增加温室气体的排放,故D 错误。
硫和硫的化合物
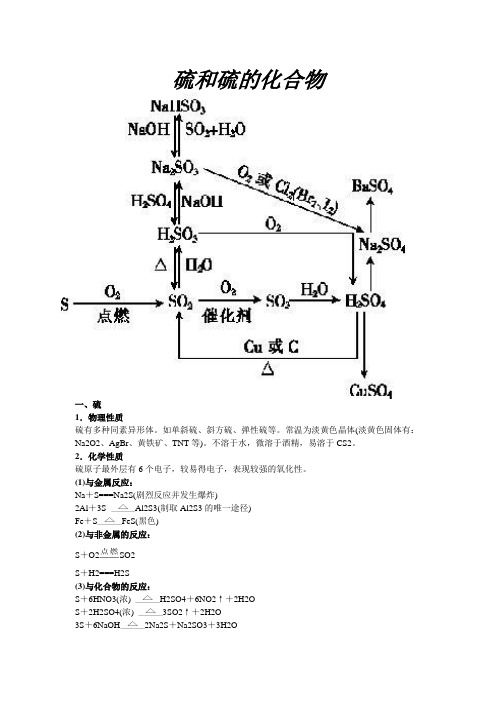
硫和硫的化合物一、硫1.物理性质硫有多种同素异形体。
如单斜硫、斜方硫、弹性硫等。
常温为淡黄色晶体(淡黄色固体有:Na2O2、AgBr、黄铁矿、TNT等)。
不溶于水,微溶于酒精,易溶于CS2。
2.化学性质硫原子最外层有6个电子,较易得电子,表现较强的氧化性。
(1)与金属反应:Na+S===Na2S(剧烈反应并发生爆炸)2Al+3S Al2S3(制取Al2S3的唯一途径)Fe+S FeS(黑色)(2)与非金属的反应:S+O2SO2S+H2===H2S(3)与化合物的反应:S+6HNO3(浓) H2SO4+6NO2↑+2H2OS+2H2SO4(浓) 3SO2↑+2H2O3S+6NaOH2Na2S+Na2SO3+3H2O例题:将m g铁粉和n g硫粉均匀混合,在密闭容器中加热到红热,冷却后加入L b mol·L-1的盐酸就不再产生气体。
若把已放出的气体收集起来,在标准状况下的体积是。
由Fe+S FeS,FeS+2HCl===FeCl2+H2S↑,得Fe~2HCl;又由Fe+2HCl===FeCl2+H2↑,得Fe~2HCl,即产生气体的总体积和消耗的盐酸的量与硫粉量无关,只由铁的量确定。
设加入b mol·L-1盐酸的体积为V,则×2=V×b mol·L-1得V=L或mL标准状况下产生气体的体积为×22.4 L·mol-1=0.4m mL二、硫的氧化物1.SO2的性质2.SO2的实验室制法3.几种物质漂白原理的比较4.SO2的危害和治理SO2是大气主要污染物,直接危害人类身体健康,酸雨为SO2产生的二次污染物。
SO2的主要来源为燃烧含硫的燃料(如煤),消除SO2污染的最有效的途径是减少SO2的排放。
5.三氧化硫SO3是硫的最高价氧化物,为白色易挥发晶体,是典型的酸性氧化物。
将SO2气体分别通入下列溶液中:①品红溶液,现象是溶液褪色。
②溴水溶液,现象是溶液褪色。
硫及其化合物知识点

硫及其化合物一、硫及其重要化合物的主要性质及用途: 1.硫:(1)物理性质:硫为淡黄色固体;不溶于水,微溶于酒精,易溶于CS 2(用于洗去试管壁上的硫);硫有多种同素异形体:如单斜硫、斜方硫、弹性硫等。
(2)化学性质:硫原子最外层6个电子,较易得电子,表现较强的氧化性。
①与金属反应(与变价金属反应,均是金属氧化成低价态)2S (剧烈反应并发生爆炸) 2S 3(制取Al 2S 3的唯一途径) Fe+S (黑色)2Cu + S Cu 2S (黑色)②与非金属反应SO 2S+H 2 H 2S (说明硫化氢不稳定)③与化合物的反应S+6HNO H 2SO 4+6NO 2↑+2H 2OS+2H 2SO 2SO 2↑+2H 2O3S+6NaOH 2Na 2S+Na 2SO 3+3H 2O (用热碱溶液清洗硫)(3)用途:大量用于制造硫酸、硫化天然橡胶,也用于制药和黑火药。
三药一柴:医药、火药、农药、和火柴的原料。
2.硫的氢化物:①硫化氢的物理性质:H 2S 是无色、有臭鸡蛋气味的有毒气体;能溶于水,密度比空气略大。
②硫化氢的化学性质A .可燃性:当22/O S H n n ≥2/1时,2H 2 2S+2H 2O (H 2S 过量) 当22/O S H n n ≤2/3时,2H 2S+3O 2 点燃 2SO 2+2H 2O (O 2过量) 当23222<<O SH n n 时,两种反应物全部反应完,而产物既有硫又有SO 2 B .强还原性:常见氧化剂Cl 2、Br 2、I 2、Fe 3+、HNO 3、浓H 2SO 4、KMnO 4等,甚至SO 2均可将H 2S 氧化。
③H 2S 的水溶液叫氢硫酸,是二元弱酸。
除杂:用CuSO 4溶液除去H 2S : CuSO 4+H 2S===CuS ↓+H 2SO 4 3.硫的氧化物:(1)二氧化硫:①SO 2是无色而有刺激性气味的有毒气体,密度比空气大,容易液化,易溶于水。
硫及其化合物性质ppt课件

2.硫的化学性质 学案P1 练习1
S + H2
△
H2
与非金属反应
S + Fe S + 2 Cu
△ +2
FeS
△ +1
Cu2S
与金属反应
学案 练习2、3
4
二、二氧化硫的性质
1. 物理性质:
状态: 气体 颜色: 无色 气味: 有刺激性 溶解度:易溶于水,在常温、常压下,
一般无明显现象
一般为含氢、氧元素的 有机物。H、O原子按 2:1 的比脱去
有机物脱水后有黑色 固体(不是全部都有)
应用
干燥剂
有机反应中作脱水剂
浓硫酸能干燥的气体:H2、O2、Cl2、HCl、CO2、
CO、SO2等
19
现象:蔗糖颜色逐渐变黑,混合物体积迅速膨胀, 产生有刺激性气味气体
请写出有关反应的方程式
SO2 + Ba(OH)2溶液
SO2 + Ba(OH)2 =BaSO3 ↓ + H2O
SO2 过量,沉淀溶解
8
(3)酸性氧化物 + 碱性氧化物→含氧酸盐
SO2 + CaO = CaSO3 能与饱和NaHCO3溶液作用
SO2 + 2NaHCO3 = Na2SO3+ 2CO2 + 如何除去CO2 中H2的OSO2?
物质。无色物质受热则很快分解。
11
如果把SO2和Cl2分别通入品红溶液或紫色石蕊试液, 能观察到什么现象? 化合反应
通入 SO2 褪色 加热至沸
红色
品红溶液
通入 Cl2
褪色
加热至沸
不显红色
氧化反应
紫色石蕊
硫及其化合物

硫及其化合物讲义第一部分、知识梳理一、硫【物理性质】硫为固体、溶于水、溶于酒精、溶于CS2【化学性质】硫原子最外层个电子,较易电子,硫元素的常见化合价有,通常表现。
①与金属反应(与变价金属反应,金属均被氧化成低价态)Na + SHg + SFe + SCu + S②与非金属反应S + O2③与化合物的反应S + HNO3(浓)S + H2SO4(浓)S + NaOH④黑火药的反应【用途】大量用于制造硫酸、硫化天然橡胶,也用于制药和黑火药。
二、硫的氧化物1、二氧化硫【物理性质】色、有气味的气体,密度比空气,容易液化,溶于水。
【化学性质】①和水反应:SO2 +H2O此反应属于。
②与碱和碱性氧化物反应:SO2 +NaOHSO2 +Na2O SO2 +CaO③ 既有氧化性又有还原性:SO 2 + O 2 此反应属于 SO 2 + H 2S SO 2 + Cl 2+ H 2O SO 2 + KMnO 4 + H 2O SO 2 + H 2O 2 ④ 漂白性:SO 2通入品红溶液,现象品红 ,然后稍稍加热,恢复到原来的红色。
SO 2漂白性的特点:有选择的暂时的化合漂白。
【实验室制法】Na 2SO 3 + H 2SO 4(浓) === Na 2SO 3 + H 2O +SO 2↑或Cu + 2H 2SO 4(浓) === CuSO 4 + 2H 2O + SO 2↑2、三氧化硫【物理性质】标况下为无色 、常温下为无色 、熔点 、沸点【化学性质】具有酸性氧化物的通性。
☆ 性质对比三、硫的氢化物【物理性质】 色、有 气味的有毒气体; 溶于水,密度比空气 。
【化学性质】① 强还原性:常见氧化剂Cl 2、Br 2、Fe 3+、HNO 3、KMnO 4等,甚至SO 2均可将H 2S 氧化。
② 不稳定性:300℃以上易受热分解③ H 2S 的水溶液叫氢硫酸,是二元弱酸。
△④可燃性四、硫酸1、稀硫酸无色水状液体,密度大于水具有酸的通性2、浓硫酸无色、难挥发的油状液体,密度大于水,熔沸点。
1硫及其化合物人教版高一化学必修二

结论:氯气的氧化性比硫强
2、硫与非金属的反应
硫
在
0
S + O2
点燃
====
+4
SO2
硫作为还原剂
氧 气 中
具有还原性
燃 烧
注意:硫在空气中燃烧、纯氧中燃烧的现象;硫在 氧气中的燃烧产物只能是二氧化硫SO2。
0 △ -2
H2 + S == H2S
硫作为氧化剂,具有氧化性。
1、关于硫的叙述正确的是 ( C)
第一节 硫及其化合物
第1课时 硫和二氧化硫
一、自然界中的硫
火
山 口 的 硫
火 山 爆
发
1.自然界硫元素的存在形态:游离态、化合态 2.自然界中含硫化合物:
化学式 BaSO4 CaSO4·2H2O
ZnSO4·7H2O FeSO4·7H2O Na2SO4·10H2O
名称 重晶石
石膏
皓矾 绿矾 芒硝
3、硫的物理性质
A、硫的非金属性较强,所以只以化合态存在于 自然界中 B、S与金属或非金属反应时均作氧化剂 C、S的两种单质之间的转化属于化学变化 D、硫在空气中的燃烧产物是SO2,在纯氧中燃烧 产物是SO3
2、下列反应中,硫表现还原性的是( A)
A、硫与氧气
B、硫与氢气
C、硫与铁
D、硫与铜
二氧化硫(SO2)
(一)、物理性质 无色、有刺激性气味的有毒气体,密度比空
应用:实验室常用此检验二氧化硫!
几种具有漂白性物质的性质比较:
具有漂白性的物质
物质 HClO、O3、 H2O2、Na2O2
实质 氧化漂白
SO2 化合漂白
木炭
物理吸附
效果 范围
硫及其化合物知识点

硫及其化合物知识点硫(S)是一种化学元素,原子序数为16,位于第三周期的第六族元素,属于非金属元素。
它的分子式是S,原子量为32.06 g/mol。
硫的性质:1.物理性质:硫是一种黄色的固体,在常温下为单斜晶系。
它呈现为柔软的颗粒状或结晶状,有一股特殊的气味。
硫的熔点为115.21°C,沸点为444.60°C。
硫在常温下无法溶于水,但可溶于许多有机溶剂。
2.化学性质:硫是一种不活泼的非金属。
它可与氧气直接反应生成二氧化硫(SO2),还可与许多金属反应生成相应的硫化物。
硫与氧气的反应通常会伴随着一种特殊的刺激性气味,这也是硫的一种特征。
硫的化合物:1.二氧化硫(SO2):二氧化硫是一种常见的硫化物,它是由硫与氧气反应生成的。
它是一种无色的气体,具有刺激性气味。
二氧化硫是一种重要的工业原料和气体污染物,对环境和人体健康都有一定的危害。
2.三氧化硫(SO3):三氧化硫是由硫与氧气进一步反应生成的硫化物。
它是一种白色固体,常以无定形或结晶形式存在。
三氧化硫是许多硫酸制造过程中的中间产物,也是一种重要的工业化合物。
3.硫化氢(H2S):硫化氢是由硫和氢反应生成的化合物。
它是一种具有刺激性气味的无色气体,有时也被称为“臭鸡蛋气味”。
硫化氢在工业生产中被广泛用作硫化剂、还原剂和中间体。
4.硫酸(H2SO4):硫酸是一种强酸,由硫、氧和氢反应生成。
它是一种无色的粘稠液体,具有强腐蚀性。
硫酸是化学工业中最重要的化合物之一,广泛用于制造肥料、炼油、清洁剂等。
5.硫化物:硫还与许多金属反应生成相应的硫化物化合物,如硫化铁(FeS)、硫化镉(CdS)等。
硫化物是一种常见的硫化合物,在地质学、材料科学和电子工程等领域具有重要的应用价值。
硫的应用:1.农业:硫是植物生长所需的重要营养元素之一、硫肥可以提供植物所需的硫元素,促进植物生长和发育。
2.化工工业:硫及其化合物广泛应用于化学工业中。
硫酸和硫酸盐是许多化学反应和工业过程的重要原料。
硫及其化合物的性质

硫及其化合物第一部分基础知识一、硫(一)结构和存在1、结构(1)硫位于第三周期第ⅥA族电子排布式为 [Ar]3s23p4(2)结构式 S8 (斜方硫和单斜硫的化学式均为S8,除此之外还有其他分子种类,如S2、S3、S4、S5、S6、S7……S20和其他硫链等。
)2、存在形式(1)游离态:存在火山喷口附近或地壳岩层里。
原因:气体中还有的SO2与H2S气体相遇生成硫单质沉积在火山口附近。
(2H2S+SO2=3S↓+2H2O)(2)化合态:硫化物:硫铁矿(FeS2)、黄铜矿(CuFeS2)硫酸盐:芒硝(Na2SO4·10H2O)、石膏(CaSO4·2H2O)其他:蛋白质、化石燃料(煤、石油、天然气)(二)物理性质1、颜色状态:黄色晶体、质脆、易研成粉末。
俗称:硫磺2、溶解性:不溶于水,微溶于酒精,易溶于二硫化碳(CS2)。
可以用二硫化碳洗涤内壁附着硫单质的试管。
(三)化学性质1、氧化性(1)与Na反应 2Na + S Na2S将硫粉和金属钠混合在研钵中研磨,可以听到轻微的爆炸声。
(2)与比价金属反应时生成低价金属硫化物Fe + S FeS , 2Cu + S CuS研磨(3)硫蒸气与H2反应 H2+ S H2S2、还原性(1)与O2反应S + O2 SO2硫在空气中燃烧产生微弱的淡蓝色火焰,在纯氧中燃烧产生蓝紫色火焰,都产生刺激性气味的气体。
(2)与浓硫酸反应S + 2H2SO4(浓) 3SO2↑ + 2H2O 归中反应3、既表现氧化性,又表现还原性——与NaOH反应3S + 6NaOH 2Na2S + Na2SO3+ 3H2O(四)用途1、制农药:如硫合剂(石灰、硫磺),可用于杀死果树的害虫。
2、制黑火药:“一硫二硝三木炭”S + 2KNO3 + 3C K2S + N2↑ +3CO2↑3、消除汞蒸气:实验室里不慎洒落一些汞,可以撒上硫粉处理。
二、硫的化合物(一)二氧化硫 SO21、物理性质无色、具有刺激性气味的气体,密度大于空气,易溶于水(1:40),沸点较低,易液化,有毒2、化学性质(1)酸性氧化物与H2O反应 H2O + SO2= H2SO3与碱反应SO2 + NaOH = NaHSO3SO2过量SO2 + 2NaOH = Na2SO3+ H2O SO2少量SO2 + Ca(OH)2= CaSO3↓ + H2OSO2 + Ba(OH)2= BaSO3↓ + H2O与碱性氧化物反应 SO2 + CaO = CaSO3与某些盐反应 SO2(少) + 2NaHCO3= Na2SO3 + H2O +2CO2点燃点燃SO2(过) + NaHCO3= NaHSO3 + CO2 (2)氧化性与H2S反应 2H2S+SO2=3S↓+2H2O(3)还原性①使卤族单质水溶液褪色Cl2 + SO2+ 2H2O = H2SO4+ 2HClBr2 + SO2+ 2H2O = H2SO4+ 2HBrI 2 + SO2+ 2H2O = H2SO4+ 2HI②使KMnO4(H+)褪色2KMnO4 + 5O2+2H2O = K2SO4+ 2MnSO4+ 2H2SO4③使FeCl3由黄色变为浅绿色2FeCl3 + SO2+ 2H2O = FeCl2+ FeSO4+ 4HCl④催化氧化2SO2 + O22SO3(4)漂白性SO2与某些有色物质化合成不稳定的无色物质,这种无色物质受热易分解,而使有色物质恢复原来的颜色。
第2讲-硫及其化合物

基础盘点
一、硫 1.自然界中硫元素的存在 硫元素广泛存在于自然界,游离态的硫存在于 火山喷口 附近或地壳的岩层里。化合物的硫主要以 硫矿石 和 硫酸盐 的 形 式 存 在 。 如 FeS2 、 CaSO4·2H2O、Na2SO4·10H2O。
2.硫的物理性质 硫俗称 硫黄 ,是一种 黄 色晶体,质脆,易研成粉 末,不溶于 水 ,微溶于 酒精 ,易溶于 CS2(用于洗涤
提醒 (1)SO2通入石蕊试液中,溶液只变红色, 而Cl2通入该溶液中则先变红后又褪色。(2)不一定; SO2和Cl2对品红溶液虽然具有漂白性,但因为发生反 应SO2+Cl2+2H2O===H2SO4+2HCl,显然漂白性减 弱,两者等物质旳量相混时,漂白性消失。
2.三氧化硫 (1)物理性质 熔点:16.8℃,沸点:44.8℃,常温下为 液 态,标准 状况下为 固态 。
③计算时注意电子守恒旳应用 ①开始产生SO2(加热)
(3)不活泼金属(如Cu) ②浓度变小,稀H2SO4不 再与Cu反应
2. 浓、稀硫酸旳鉴别措施
现象
浓 H2SO4
稀 H2SO4
物 加水
放出大量热
无明显现象
理 观状 性态
黏稠状液体
黏稠度较小
质
密度
用手掂分量:浓 H2SO4 密度较大(1.84 g/mL), 相同体积时,浓 H2SO4 质量大很多
(2)化学性质 酸性氧化物,与 H2O、CaO、Ca(OH)2 反应的方程式分 别为 SO3+H2O===H2SO4 ; CaO+SO3===CaSO4 ; SO3+Ca(OH)2===CaSO4+H2O 。 三、硫的氧化物对大气的污染 1.来源: 含硫化石燃料 害:危害人体健康,形成 酸雨 (pH 小于 5.6 )。 3.治理:燃煤 脱硫 ,改进燃烧技术。 四、硫酸、SO42-的检验 1.硫酸
硫及硫的有关化合物知识点整理

硫一、物理性质1、纯净的硫是一种黄色或淡黄色的固体,俗称硫磺2、不溶于水,易溶于二硫化碳,微溶于酒精。
3、熔点 112.8 ℃,沸点444.8℃。
4、硫蒸汽急剧冷却的过程叫做硫华。
二、化学性质(1)与金属反应Fe + S现象:继续保持红热状态,生成黑褐色固体。
Cu + SHg + S (反常反应)干态制法:Mg + SAl + S(MgS,Al2S3) 与水反应小结:硫能和许多金属化合反应生成金属硫化物,在金属化合物中,硫元素的化合价是-2 价,金属一般呈低价, Hg 反常。
(2)与非金属反应S+SO2H2+S小结:硫的化学性质与氧相似,但氧化性比氧弱,跟金属反应时显示氧化性,跟氧化性较高的非金属反应,显示还原性,跟还原性较强的物质反应,显示氧化性。
(3)与化合物反应S+2H2SO4( 浓)3S+6NaOH三、用途①主要用于制硫酸②植物生长必不可少的元素③橡胶工业的重要添加剂④有杀虫、杀螨、杀菌作用,可用作农作物的杀菌剂和治疗皮肤的杀菌软膏⑤染色、制革、国防工业、火柴、火药、烟火等行业用到。
(注:单质硫只存在于火山口附近,化合态硫存在于硫铁矿FeS2 )四、黑火药(主要成分:硫磺、硝石、木炭)的爆炸:S+2KNO3+3C硫化氢一、物理性质1)无色有毒气体,有臭鸡蛋气味(硫化氢独有气味,可用此鉴别气体)2)密度比空气大。
3)在水中的溶解性为 1:2.6,能溶于水。
4)H2S 的水溶液叫氢硫酸。
(弱酸性)二、化学性质1)可燃性气体O2 充足2H2S+O2O2 不足2H2S+3O22) 还原性①与活泼的非金属反应H2S+Cl2现象:气体 H2S 与Cl2 不共存,反应时瓶壁留有淡黄色固体。
溶液 H2S 与 Cl2 不共存,反应时溶液变浑浊且PH 值变小。
H2S+Br2现象:H2S 使溴水褪色,同时产生沉淀,PH 减小。
H2S+I2现象:碘水使澄清的硫化氢溶液变浑浊,PH 减小。
在碘水的淀粉溶液中通入H2S 气体,溶液蓝色褪去。
硫及其重要化合物的性质和应用

硫及其重要化合物的性质和应用一、知识梳理1.硫(1)游离态:硫单质俗名硫黄,主要存在于火山口附近或地壳的岩层里。
(2)化合态:主要以金属硫化物和硫酸盐的形式存在,如硫铁矿(FeS 2)、黄铜矿(CuFeS 2)、石膏(CaSO 4·2H 2O)和芒硝(Na 2SO 4·10H 2O)等。
(3)物理性质:硫为淡黄色固体;不溶于水,微溶于酒精,易溶于CS 2(用于洗去试管壁上的硫);硫有多种同素异形体:如单斜硫、斜方硫、弹性硫等。
(4)化学性质:硫原子最外层6个电子,较易得电子,表现较强的氧化性。
①与金属反应(与变价金属反应,均是金属被氧化成低价态)2Na+SNa 2S (剧烈反应并发生爆炸) 2Al+3S Al 2S 3(制取Al 2S 3的唯一途径)Fe+S FeS (黑色) 2Cu + S Cu 2S (黑色) ②与非金属反应S+O 2 点燃SO 2 S+H 2 H 2S (说明硫化氢不稳定)③与化合物的反应S+6HNO 3(浓)H 2SO 4+6NO 2↑+2H 2O S+2H 2SO 4(浓)2SO 2↑+2H 2O 3S+6NaOH2Na 2S+Na 2SO 3+3H 2O (用热碱溶液清洗硫)(5)用途:大量用于制造硫酸、硫化天然橡胶,也用于制药和黑火药。
2、硫的氢化物 (1)硫化氢的制取Fe+H 2SO 4(稀)FeSO 4+H 2S↑(不能用浓H 2SO 4或硝酸,因为H 2S 具有强还原性)——H 2S 是无色、有臭鸡蛋气味的有毒气体;能溶于水,密度比空气略大。
(2)硫化氢的化学性质A .可燃性:当22(H S)(O )21n n 时,2H 2S+O 2 点燃2S+2H 2O (H 2S 过量)当22(H S)(O )23n n ≤时,2H 2S+3O 2 点燃2SO 2+2H 2O (O 2过量) 当22(H S)(O )223n n 〈〈时,两种反应物全部反应完,而产物既有S 又有SO 2 B .强还原性:常见氧化剂Cl 2、Br 2、Fe 3+、HNO 3、KMnO 4等,甚至SO 2均可将H 2S 氧化。
硫与其化合物的性质与应用

硫与其化合物的性质与应用硫(S)是一种常见的非金属元素,存在于自然界中的许多矿石和有机物中。
它具有多种化合物,拥有独特的性质和广泛的应用。
本文将探讨硫及其化合物的性质和应用。
一、硫的性质硫是一种黄色的固体,无味,无毒。
它具有较低的熔点和沸点,能在常温下蒸发。
硫在空气中加热后会燃烧,产生剧烈的蓝色火焰和刺激性气味。
1. 物理性质硫具有单斜晶系结构,晶体呈现六角形的螺旋结构。
它的密度约为2 g/cm³,硬度较低。
在常温下,硫为柔软的固体,可以被切割成薄片或压成粉末。
2. 化学性质硫具有较强的化学活性。
它可以与许多元素反应,形成各种化合物。
例如,硫与氧气反应会生成二氧化硫(SO₂),该化合物是大气污染的主要来源之一。
硫还能与金属反应形成金属硫化物,如铁与硫反应生成硫化铁(FeS)。
此外,硫还与氢反应生成硫化氢(H₂S),具有强烈的恶臭味道。
二、硫化物的性质与应用1. 金属硫化物金属硫化物是硫与金属元素形成的化合物,具有重要的性质和应用。
例如,硫化铁是一种黑色的固体,可以用于制备磁性材料和矿石的磁选。
硫化铜是一种红色的固体,广泛应用于电镀、颜料和催化剂等领域。
此外,硫化锌也是一种重要的无机材料,广泛用于制备橡胶增塑剂、涂料和橡胶产品。
2. 有机硫化物有机硫化物是含有硫原子的有机化合物,具有独特的性质和广泛的应用。
其中,二硫化物是一类重要的有机硫化合物,具有良好的润滑性能和耐热性。
二硫化钼(MoS₂)常用于制备润滑油和减摩剂。
含有硫的有机化合物还常用作药物和农药的中间体。
硫醇是含有硫原子和氢原子的有机化合物,常用于金属表面防锈和抗氧化剂。
3. 硫酸及其盐类硫酸(H₂SO₄)是一种强酸,广泛应用于化工、冶金、制药和环保等领域。
硫酸可用于制备肥料、染料和塑料等工业产品。
此外,一些硫酸盐如硫酸铜、硫酸锌等也具有重要的应用,如用于制备电池、电镀和农药等。
4. 硫化氢硫化氢(H₂S)是一种无色有毒气体,具有刺激性气味。
硫及其化合物

(1)酸性氧化物 酸性氧化物
①与水反应 ②与碱反应
具有酸性氧化物的通性
SO2+H2O=H2SO3 SO2+2NaOH=Na2SO3+H2O
SO2+NaOH=NaHSO3 ③与碱性氧化物反应 SO2+CaO=CaSO3 (除去燃煤中的 2) 除去燃煤中的SO 除去燃煤中的 ④与盐反应 SO2+2NaHCO3=Na2SO3+CO2+H2O SO2+NaHCO3=NaHSO3+CO2
思考: 对应的酸的酸性: 均为酸性氧化物, (1)两者均为酸性氧化物 但对应的酸的酸性:
H2SO3>H2CO3 (2)两者都有弱氧化性 2H2S+SO2=3S↓+2H2O )两者都有弱氧化性
高温
C+CO2===2CO 都能使澄清的石灰水变浑浊, (3)两者都能使澄清的石灰水变浑浊,再通入过量又变澄清。 )两者都能使澄清的石灰水变浑浊 再通入过量又变澄清。 SO2+Ca(OH)2=CaSO3↓+H2O CaSO3+SO2+H2O=Ca(HSO3)2 品红、 )、氯水 氯水、 褪色, : ) 能使品红 异(1)SO2能使品红、KMnO4(H+)、氯水、溴水等溶液 褪色, CO2不能 (2)SO2具有还原性 ) (3)对环境的影响: )
最佳方案 试液 方案乙: 方案乙:
无沉淀
BaCl2溶液
白色沉淀
先加盐酸无沉淀,排除 的存在,再加BaCl2溶液,在酸性 溶液, 先加盐酸无沉淀,排除Ag+的存在,再加 溶液中生成白色沉淀,证明有SO 溶液中生成白色沉淀,证明有 42-。 方案丙: 方案丙:试液 足量稀硝酸 无沉淀 Ba(NO3)2溶液 白色沉淀 如有SO 会被硝酸氧化成SO 溶液生成白色沉淀。 如有 32- , 会被硝酸氧化成 42- ,加Ba(NO3)2溶液生成白色沉淀。
硫及其重要化合物-PPT课件

【答案】
32
技能归纲 检验气体混合物的成分时一般首先用无水硫酸铜检 验水蒸气的存在;检验二氧化碳与二氧化硫气体时,应 先检验二氧化硫气体,后检验二氧化碳,在检验二氧化 碳前先要将二氧化硫气体排除。
33
学以致用 3.一定量的浓硫酸与足量Zn充分反应时,有SO2和H2生 成。某校化学研究性学习小组对此进行研究。按图组 装好实验装置,微热试管A,观察到C、D、E中均有气泡 产生;随后气泡量减少,品红溶液褪色,D中先出现浑浊 后浑浊消失;反应较长时间后,C、D、E中的气泡量又 会明显增加。
第3讲 硫及其重要化合物
1
一、硫 1.物理性质:硫通常是一种①淡黄色、质脆的固体,不溶
于水,微溶于②酒精,易溶于CS2。
2.化学性质:单质硫是一种弱氧化剂,在反应中既可以表
现出氧化性又可以表现出还原性。
(1)氧化性:①硫与铜反应:S+2Cu
②硫与铁反应:Fe+S
④FeS
③Cu2S
③硫与氢气反应:H2+S
4
二、二氧化硫
1.物理性质 二氧化硫是⑦无色,有⑧刺激气味的有毒气体,密度比 空气大,易溶于水。 2.化学性质 ①SO2是⑨酸性氧化物,有⑩酸性氧化物的通性。
与H2O反应: SO2+H2O
H2SO3(亚硫酸不稳定,易分
解,易被氧化成硫酸,是还原性的二元弱酸。)
与NaOH作用: 2NaOH+SO2
Na2SO3+H2O。
B.在反应HCOOH 表现脱水性
CO↑+H2O中,浓H2SO4只
C.在反应Cu+2H2SO4(浓) H2SO4只表现氧化性
CuSO4+SO2↑+2H2O中,浓
硫及其化合物

硫及其化合物1、硫元素的存在:硫元素最外层电子数为6个,化学性质较活泼,容易得到2个电子呈-2价或者与其他非金属元素结合成呈+4价、+6价化合物。
硫元素在自然界中既有游离态, 又有化合态。
(如火山口中的硫就以游离态存在) 2、硫单质:①物质性质:俗称硫磺,淡黄色固体,不溶于水,微溶于酒精,易溶于二硫化碳,熔点低。
②化学性质:S+O2 ===(点燃) SO2(空气中点燃淡蓝色火焰,纯氧中为蓝紫色)Fe+S==FeS 2Cu+S==Cu2S 2Na+S=Na2S Hg+S==HgS(汞滴处理)3S+6NaOH(浓)=== 2Na2S+Na2SO3+3H2O(洗硫)3、二氧化硫(SO2)(1)物理性质:有刺激性气味有毒气体, 可溶于水(1:40),易液化。
(2)化学性质:①SO2能与水反应:SO2+H2O H2SO3亚硫酸为中强酸,此反应为可逆反应。
可逆反应定义:在相同条件下,正逆方向同时进行的反应。
②SO2为酸性氧化物,可与碱反应生成盐和水。
与NaOH溶液反应:SO2(少量)+2NaOH=Na2SO3+H2OSO2(过量)+NaOH=NaHSO3对比CO2与碱反应:CO2(少量)+Ca(OH)2=CaCO3↓(白色)+H2O2CO2(过量)+Ca(OH)2=Ca(HCO3) 2 (可溶)将SO2逐渐通入Ca(OH)2溶液中先有白色沉淀生成,后沉淀消失,与CO2逐渐通入Ca(OH)2溶液实验现象相同,故不能用石灰水来鉴别SO2和CO2。
能使石灰水变浑浊的无色无味的气体一定是二氧化碳,这说法是对的,因为SO2是有刺激性气味的气体。
b、SO2将通入酚酞变红的溶液,溶液颜色褪去,体现了SO2和水反应生成亚硫酸,是酸性氧化物的性质,而不是漂白性,SO2不能漂白指示剂。
③SO2具有强还原性,能与强氧化剂(如酸性KMnO4溶液、Cl2、O2(催化剂:粉尘、V2O5)等)反应。
SO2能使酸性KMnO4溶液、新制氯水褪色,显示了SO2的强还原性(不是SO2的漂白性)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
矿产资源开发利用方案编写内容要求及审查大纲
矿产资源开发利用方案编写内容要求及《矿产资源开发利用方案》审查大纲一、概述
㈠矿区位置、隶属关系和企业性质。
如为改扩建矿山, 应说明矿山现状、
特点及存在的主要问题。
㈡编制依据
(1简述项目前期工作进展情况及与有关方面对项目的意向性协议情况。
(2 列出开发利用方案编制所依据的主要基础性资料的名称。
如经储量管理部门认定的矿区地质勘探报告、选矿试验报告、加工利用试验报告、工程地质初评资料、矿区水文资料和供水资料等。
对改、扩建矿山应有生产实际资料, 如矿山总平面现状图、矿床开拓系统图、采场现状图和主要采选设备清单等。
二、矿产品需求现状和预测
㈠该矿产在国内需求情况和市场供应情况
1、矿产品现状及加工利用趋向。
2、国内近、远期的需求量及主要销向预测。
㈡产品价格分析
1、国内矿产品价格现状。
2、矿产品价格稳定性及变化趋势。
三、矿产资源概况
㈠矿区总体概况
1、矿区总体规划情况。
2、矿区矿产资源概况。
3、该设计与矿区总体开发的关系。
㈡该设计项目的资源概况
1、矿床地质及构造特征。
2、矿床开采技术条件及水文地质条件。
