含卤素及含金属药物的分析共58页
药物分析重点整理

1.标准品: 用于鉴别、检查、含量测定的标准物质。
标准品指用于生物检定、抗生素或生化药品中含量或效价测定的标准物质。
2.空白试验: 在与供试品试验完全相同的条件下除不加供试品外其它试剂均同样加入而进行的试验3.鉴别试验: 根据药物的分子结构、理化性质采用化学、物理化学或生物方法来药物的真伪。
4.灵敏度反应: 一定条件下在尽可能稀的溶液中检出尽可能少的供试品反应对这一要求所能满足的程度。
5.热分析法: 在程序控制温度下测量物质的物理化学性质与温度关系的一类技术。
6.差示扫描量热法: 在程序控制温度下测量传输给待测物质和参比物的能量差与温度或时间关系的一种技术。
7灵敏度法: 在供试品溶液中加入一定量的试剂在一定反应条件下不得有正反应出现从而判断供试品中所含杂质是否符合限量规定。
8.比较法: 指取供试品一定量依法检查测定特定待检杂质的参数与规定的限量比较不得更大9重复性: 在较短时间间隔内在相同的操作条件下由同一分析人员测定所得结果的精密度10重现性: 在不同实验室由不同分析人员测定结果的精密度11.中间精密度:在同一实验室由于实验室内部条件的改变如不同时间由不同分析人员用不同设备测定所得结果的精密度。
12.检测限: .分析方法能够从背景信号中区分出药物时所需样品中药物的最低浓度13.定量限:样品中被测物质能被定量测定的最低量其结果应具有一定的准确度和精密度14.耐用性: 在测定条件有小的变动时测定结果不受影响的承受程度15.酶活力: 酶催化一定化学反应的能力16.酶活力测定: 酶活力测定是指以酶为分析对象目的在于测定样品中某种酶的含量或活性的酶分析法。
17.酶法分析: 酶法分析是以酶为分析工具或分析试剂主要用以测定样品中酶以外的其他物质的含量。
18.生物检定法: 利用药物对生物体或离体器官组织等所起的药理作用来检定药物的效价或生物活性的方法用于无适当理化方法进行检定的药物。
1.药品检验工作的基本程序有哪些原始记录和检验报告的要求是什么取样、鉴别、检查、含量测定、检验报告的书写。
第四章第一节富集在海水中的元素考点卤素及卤素离子的检验-课件新高考化学一轮复习

――加―入―C―Cl―4―下振―层―荡或―汽―油――上―层―→
自贫褴有信困褛志是 教 衣 的成会内人功贫可战的困藏天第者志斗一一。地秘切,诀。无志有的人机怨天层恨地呈。 红紫棕色色、或浅橙紫红色色或,紫表红明色有,表B明r-有
I-
(3)氧化——淀粉检验 I-
未知液―加―入―适―量―新―制―振―饱―荡和―氯―水――双―氧―水→ ―淀―振 粉―荡 溶―液→ 蓝 色溶液,表明有 I-
[题点全盘查]
题点(一) 卤素的性质及递变规律
1.鉴别 NaCl 溶液、NaBr 溶液、NaI 溶液可以选用的试剂是
()
①碘水、淀粉溶液 ②氯水、CCl4 ③溴水、苯 ④硝酸、AgNO3 溶液
⑤氯水、苯 ⑥CCl4、淀粉溶液
A.①②④
B.②③⑥
C.②④⑤
D.④⑤⑥
解析:①无法鉴别三溶液,③无法鉴别 NaCl 和 NaBr 溶液,⑥无法鉴别
2F2+2H2O===4HF+O2 )。 ④都能与碱溶液反应: X2+2NaOH===NaX+NaXO+H2O (F2 例外)。
(2)性质的递变性
颜色
熔、沸点 密度
水溶性 氧化性
―气―体――――气―体―逐―渐―升―高―液―体――――固―体→ ―逐―渐―增―大→
―反―应――――溶―解―逐―渐―减―小―溶―解――――微―溶→ ―氯―、―溴―与、―氢―碘气―单―化质―合氧―或化―与性―水强―反弱―应―顺由―序―易是―到C―难l2―>B―r2―>I→2
题点(二) 卤素离子的检验
3.下列能够检验出 KI 中是否含有 Br-的实验是
()
A.加入足量的新制氯水,溶液变色则有 Br-
B.加入酸性 KMnO4 溶液,观察溶液颜色是否褪去 C.加入少量的碘水,再加入 CCl4 振荡,有机层有色,则有 Br-
卤素检测报告

卤素检测报告
卤素检测报告通常包含对样品中卤素元素(氟、氯、溴、碘等)的定量或定性分析。
卤素检测可涉及环境、食品、化学品等不同领域。
以下是可能包含在卤素检测报告中的一些关键信息:
1.样品信息:
•样品来源和类型,例如大气沉降、水样、土壤、食品等。
•采样日期、地点和方法。
2.检测方法:
•使用的卤素检测方法,如离子色谱法、电感耦合等离子体质谱法(ICP-MS)、气相色谱法等。
•检测方法的灵敏度、准确性和可重复性等性能参数。
3.检测结果:
•各种卤素元素的浓度,通常以毫克/升(mg/L)或其他适当的单位表示。
•结果可能包括总卤素含量或单独报告氟、氯、溴、碘等元素的含量。
4.对比标准和法规:
•将检测结果与相应的法规、标准或限值进行对比,以评估样品的合规性。
•如果适用,报告可能会提及环境、饮用水或食品安全标准。
5.质控信息:
•质控样品的检测结果,以确保检测方法的准确性和可靠性。
•检测过程中采取的质控措施,例如仪器校准、空白样品等。
6.数据解释和建议:
•对检测结果的解释,包括结果的可能影响因素。
•根据检测结果提出的建议,例如环境治理、产品改进等。
7.实验室信息:
•进行检测的实验室信息,包括实验室名称、地址、联系方式。
•实验室的认证和资质信息,以确保检测结果的可信度。
请注意,具体的卤素检测报告的内容和格式可能会因实验室、检测目的和行业领域的不同而有所变化。
若要详细了解特定卤素检测报告的内容,建议联系进行检测的实验室或机构。
初级药师基础知识讲义-药物分析

药物分析考试大纲的三个要求层次:了解掌握熟练掌握考试要求:细目要点1.概述(1)药品质量控制目的与质量管理的意义(2)全面控制药品质量2.药品质量标准(1)药品质量标准(2)中国药典(3)制定药品质量标准的基本原则与依据3.常用的分析方法(1)定性方法:化学鉴别法、光谱鉴别法、色谱鉴别法(2)定量方法:滴定法、分光光度法、色谱法一、概述(一)药品质量控制的目的、质量管理的意义保证用药的安全、合理和有效常见的质量管理文件:《药品非临床研究质量管理规范》(GLP)、《药品经营质量管理规范》(GSP)、《药品生产质量管理规范》(GMP)《药品临床试验管理规范》(GCP)。
(二)全面质量控制:研制、生产、供应、临床使用静态分析综合评价、动态分析二、药品质量标准(一)药品质量标准是国家对药品质量、规格及检验方法所做的技术规定,是药品生产、供应、使用、检验和药政管理部门共同遵循的法定依据。
国内药品标准:《中国药典》(Ch.P.)、药品标准;国外药品标准:美国药典(USP)、美国国家处方集(NF)、英国药典(BP)、日本药局方(JP)、欧洲药典(Ph.Eup)和国际药典(Ph.Int)。
(掌握各自的简称)(二)《中国药典》1.历史沿革:建国之后至今共出了十版:1953、1963、1977、1985、1990、1995、2000、2005、2010、2015年版1963:开始分一、二两部。
2005:开始分三部,第三部收载生物制品。
2015:开始分四部。
2.基本结构和主要内容《中国药典》由一部、二部、三部、四部组成,首次将通则、药用辅料单独作为《中国药典》四部。
凡例(重点掌握一些概念和解释)凡例是为解释和使用中国药典,正确进行质量检验提供的指导原则。
关于检验方法和限度的规定检验方法:《中国药典》规定的按药典,采用其他方法的要与药典方法对比。
仲裁以《中国药典》方法为准。
关于标准品和对照品的规定标准品、对照品系指用于鉴别、检查、含量测定的标准物质,由国务院药品监督管理部门指定的单位制备、标定和供应。
2010.3 卤素的氧化物、含氧酸及其盐资料

卤素的氧化物、含氧酸及其盐(2010.3)王振山一、卤素的氧化物概述:卤素与电负性比它大的氧化合时,除氟外都能形成氧化数为正值的氧化物、含氧酸及其盐。
卤素的氧化物显著特点:大多数是不稳定的,受到撞击或光照即可发生爆炸性分解。
所以不能用直接法,只能用间接法制取。
稳定性:在已知的卤素氧化物中,碘的氧化物是最稳定的;碘氧化物>氯氧化物>溴氧化物;氯和溴的氧化物在高温下明显分解,溴的氧化物特别不稳定,低于室温也分解。
高价态的卤素氧化物比低价态的卤素氧化物稳定。
卤素氧化物中氯的较重要:Cl2O、Cl2O6 、Cl2O7、ClO2均为强氧化剂,不稳定易爆炸。
⑴、氧的氟化物:由于氟的电负性(3.98)大于氧的电负性(3.44),所以氟与氧生成的二元化合物是氧的氟化物(OF2),而不是氟的氧化物,而其它卤素与氧化合生成的二元化合物都是卤素的氧化物。
OF2的O原子sp3杂化。
⑵、二氟化氧(OF2)熔点49 K,沸点128 K,为无色气体,是比较稳定的氟氧二元化合物。
可由单质氟与2%氢氧化钠水溶液反应制备:2 F2(g)+ 2 NaOH-(aq) ═ OF2(g) + 2 NaF(aq) + H2O(l)OF2是一种强的氧化剂和氟化剂,但氟化能力弱于F2。
由于OF2中,氧为+2氧化数,所以它是比氧气更强的氧化剂它能与金属、硫、磷、卤素等剧烈反应生成氟化物和氧化物。
在OF2分子中,氧的氧化数是+2,氟的氧化数是-1,其构型为角型分子。
⑶、近年来由于合成技术的发展,已合成了一系列氟氧化合物,如O2F2、O3F2、O4F2、O5F2、O6F2等。
这些化合物都具有较低的熔点和沸点,并仅能在很低的温度下稳定存在,它们在很低的温度(低于83K)下都是比单质氟更加活泼的氟化剂。
二氟化二氧(O2F2 ):不与玻璃起反应,是个强的氧化剂和氟化剂,但弱于F2本身:比OF2、ClF3有更强的氟化作用,能在OF2、ClF3不能完成的反应中将金属钚和钚的化合物氧化:Pu(s) + 3O2F2(g) →PuF6(g) + 3O2(g) 该反应用来从废核燃料中以挥发性PuF6的形式除去强放射性的金属Pu。
卤素报告资料

卤素化合物在化工领域的应用
卤素化合物在制药领域的应用
• 制备卤化氢:氢氟酸、氢氯酸、氢溴酸
• 药物原料:氟尿嘧啶、氯霉素、溴化钾
• 制备卤化碳:四氯化碳、四溴化碳
• 药物辅料:碘化钾、碘酸钙
• 制备卤化硫:六氟化硫
• 药物中间体:氯化亚砜、溴化氢酸
卤素化合物在其他新兴领域的应用及潜力
卤素化合物在新能源领域的应用
• 皮肤接触:工业生产、生活污水
卤素化合物的风险分析
• 健康风险:氟中毒、氯中毒、溴中毒、碘中毒
• 生态风险:水体污染、土壤污染、生物死亡
• 社会风险:经济损失、社会影响
卤素的安全防护与风险控制措施
卤素的安全防护
卤素的风险控制措施
• 佩戴口罩:防止吸入
• 加强监测:监测大气、水体、土壤污染
• 穿戴防护服:防止皮肤接触
• 氧化性:F最强,I最弱
• 与金属反应:生成卤化金属
• 与非金属反应:生成卤化氢
03
卤素元素的物理性质
• 密度:F最大,I最小
• 熔沸点:F最高,I最低
• 挥发性:F最高,I最低
• 颜色:F无色,Cl绿,Br红棕,I紫黑
卤素元素在元素周期表中的位置及其与其他元素的关系
卤素元素在元素周期表中的位置
• 污染治理:治理工业废气、废水、废渣
• 饮食安全:避免食用污染食物
• 健康教育:提高公众安全意识
• 政策法规:制定排放标准、安全法规
CREATE TOGETHER
THANK YOU FOR WATCHING
谢谢观看
DOCS
• 水生生物:氟化物、氯化物污染导致生物死亡
• 氯:过量摄入导致氯中毒
• 农作物:氟化物、氯化物污染导致生长受阻
影响卤素的能量因素分析

影响卤素单质稳定性的因素分析内容摘要卤素是中学化学的重要内容,而有关物质稳定性问题也是中学化学常见的问题,但现行的教材却对稳定性的概念未做明确阐述。
并且在中学化学学习中是通过一些反应和现象来判断卤素单质的稳定性的,难道只能通过这些判断吗?还有没有其它的判断方法呢?因此提出问题影响卤素单质稳定性的因素。
本文首先介绍了卤素的定义及其性质,再者讲述稳定性的一些知识。
然后系统的从键能、电离能、电子亲和能、分子间作用力和环境介质等几个方面具体分析了各自的一些概念和相关性质,得到卤素的键能、电离能、电子亲和能的大小及其如何影响它的稳定性;分子间作用力和环境介质对卤素稳定性的影响。
最后得到结论卤素单质的稳定性从F2→I2依次增加的。
关键词卤素稳定性影响因素1问题的提出在新人教版化学必修二第一章第一节元素周期表的第二课时教材中讲述了卤族元素,从而揭示元素的性质与原子结构的关系。
在卤族元素的学习中,主要从其原子结构、物理性质、化学性质等来学习,并做出了如下总结: 在元素周期表中,同主族元素从上到下原子核外电子层数依次增多,原子半径逐渐增大,得点子能力逐渐减弱。
所以,非金属性逐渐减弱,也即卤素单质活泼性逐渐减弱,卤素单质稳定性逐渐增强。
在教材中只是根据卤素单质与氢气反应的剧烈程度和生成氢化物的稳定性来判断卤素的性质,以及相互间的置换反应的现象来得出结论的,或者根据元素周期律的变化来判断。
那么还有什么方法或者从哪些因素也可以判断卤素单质的稳定性呢?因此提出问题卤素稳定性(活泼性)的强弱顺序可以由哪些因素决定的呢?这是作为一名教师应该了解并掌握的知识。
2卤族元素卤族元素的定义为:第ⅦA主族的所有元素包括包括氟(F)、氯(Cl)、溴(Br)、碘(I)、砹(At),简称卤素。
砹元素为放射性元素,暂不做探究。
它们在自然界都以典型的盐类存在,是成盐元素。
卤族元素原子结构有一个共同点就是最外层电子均为7个,导致卤素的一些相似的性质。
卤素化学方程式及性质

卤素化学方程式及性质1、与非金属反应(HX:卤化氢/氢卤酸)F 2 + H 2 ====2HF Cl 2+H 2====2HCl Br 2+H 2 ====2HBr I 2+H 2垐垎?噲垐?加热2HI 反应条件越来越苛刻,且HX 稳定性降低,HI 在加热下易分解4HF+SiO 2===SiF 4↑+2H 2O (HF 保存在塑料瓶的原因,此反应广泛应用于测定矿样或钢样中SiO 2的含量)HF 为弱酸,酸性比较:HF<HCl<HBr<HI (写出6大强酸)3Cl 2+2P===2PCl 3 PCl 3+Cl 2===PCl 52、与金属反应3Cl 2+2Fe===2FeCl 3 (棕色烟) 3Br 2+2Fe===2FeBr 3 I 2+Fe===FeI 2Cl 2+Cu===CuCl 2(棕黄色烟,浓溶液为绿色,稀溶液为蓝色)Br 2+Cu===CuBr 2 I 2+2Cu===2CuI总结:1.F 2、Cl 2可与任何金属化合,Br 2、I 2与大多数金属化合(除Au 、Pt 外)。
2.对于变价金属,如Fe 、Cu ,Cl 2、Br 2将金属氧化到最高价,I 2将金属氧化到较低价。
Zn+I 2==ZnI 2(H 2O 为催化剂) 滴水生紫烟,放热反应3、与水反应(X 2+H 2O 垐?噲?HX+HXO 除F 2外)Cl 2+H 2O 垐?噲?HCl+HClO Br 2+H 2O 垐?噲?HBr+HBrO I 2+H 2O 垐?噲?HI+HIO反应程度减弱2F 2 +2H 2O===4HF+O 2(氧化性:F 2>O 2,置换反应)4、与碱反应(以NaOH 为例)X 2+2NaOH===NaX+NaXO+H 2OCl 2+2NaOH===NaCl+NaClO+H 2O 3Cl 2+6NaOH===5NaCl+NaClO 3+3H 2OBr 2+2NaOH===NaBr+NaBrO+H 2O 3Br 2+6NaOH===5NaBr+NaBrO 3+3H 2OI 2+2NaOH===NaI+NaIO+H 2O 3I 2+6NaOH===5NaI+NaIO 3+3H 2O3Na 2CO 3+3Br 2==5NaBr +NaBrO 3+3CO 2↑以上均为歧化反应。
练习题2017

1 药物中对氯化物杂质检查的一般意义在于()A. 它是有疗效的物质B. 它是对药物疗效有不利影响的物质C. 它是对人体健康有害的物质D. 可以考核生产工艺中容易引入的杂质2 不是我国解放后出版的药典是()A. 1953年B. 1963年C. 1973年D. 1977年3 干燥失重法中,要求连续两次重量差异不超过()A. 0.1 mgB. 0.3 mgC. 1.0 mgD. 3.0 mg4 薄层色谱法(TLC)用于药物鉴别,具有优点,但常须采用对照品是因为()A. 一些药物的R f值数据不足B. 硅胶G等试剂的性质欠稳定C. 为了消除实验因素的影响,使结构稳定D. 质量标准的例行要求5 滴定液浓度的单位系指()A. %(g/g)B. %(mL/mL)C. mol/LD. g/1OOmL6 鉴别反应常采用多种条件提高选择性,何种药物在加入AgNO3试液和酸后,加热生成银镜的药物是()A. 水杨酸B. 对乙酰氨基酚C. 三氯叔丁醇D. 异丙肼7 以下药物可与FeCl3反应,产生紫菫色的是()A. 苯甲酸B. 泛影酸C. 氨甲苯酸D. 丙磺舒8 对于不宜使用刷子刷洗的精密玻璃仪器(例如容量瓶、比色管、移液管、滴定管),一般使用的洗涤液是()A. 洗衣粉B. KOH的乙醇液C. KOH液D. 铬酸洗液9 药物中的有害杂质限量很低,有的不允许检出如( )A. 硫酸盐B. 碘化物C. 氰化物D. 重金属10 制备阿司匹林片或其肠衣片时,常加入某些有机酸作稳定剂,故其含量测定方法采用()A. 亚硝酸钠滴定法B. 紫外分光光度法C. 直接酸碱滴定法D. 高效液相色谱法法11 对药物杂质检查项目和杂质限量的原则,描述错误的是()A. 检查药物在生产和储存过程中引入的杂质B. 杂质检查要结合实际的生产条件和分析水平C. 与化学试剂检查要求的不同D. 杂质检查项目和杂质限量一般经中国药典确定后就不再予以更改12 具芳氨基或经水解生成芳氨基的药物可用亚硝酸钠滴定法,其反应条件是()A. 适量强酸环境,加适量溴化钾,室温下进行B. 弱酸酸性环境,40℃以上加速进行C. 酸浓度高,反应完全,宜采用高浓度酸D. 酸度高反应加速, 宜采用高浓度酸13 对化学结构差别较小的药物的鉴别与区别,如盐酸普鲁卡因和苯佐卡因的鉴别,最适宜采用的方法是()A. 重氮化—偶合反应B. 紫外光谱法C. 红外光谱法D. 甲醛—硫酸法14 以药品质量标准为准则,药品分为()A. 优质药品和劣质药品B. 合格药品和不合格药品C. 保健药品和治疗药品D. A、B、C都成立15 炽灼残渣检查法用来检查药物中的无机金属杂质,方法是将药物在高温(600℃~700℃)加热,使其分解或挥发,所得残渣经过()酸化处理,精密称量所得金属酸盐的重量。
药物分析习题集-11药本用 2

一、单选题(A1型题-最佳选择题)1. 英文缩写字母GLP代表A.《药品非临床研究质量管理规定》B.《药品生产质量管理规范》C.《药品经营质量管理规范》D.《药品临床试验管理规范》2. 现有一种未经检验的药物需进行质量检测,你检测时应采用下列哪种书上规定的方法:A、药物分析B、广西药品规范C、药品检验方法原理D、中国药典3. 药品质量标准的基本内容包括A、凡例、注释、附录、用法与用途B、正文、索引、附录C、取样、鉴别、检查、含量测定D、凡例、正文、附录E、性状、鉴别、检查、含量测定、贮藏4. 中国药典(2000年版)中规定,称取“2.00g”系指A.称取重量可为1.5-2.5gB.称取重量可为1.95-2.05gC.称取重量可为1.995-2.005gD.称取重量可为1.9995-2.0005g5. 药典规定酸碱度检查所用的水是指A、蒸馏水B、离子交换水C、蒸馏水或离子交换水D、反渗透水E、新沸并放冷至室温的水6. 药典规定取用量为“约”若干时,系指取用量不得超过规定量的A.±0.1%B.±1%C.±5%D.±l0%7. 我国药典正确的名称写法是A.中华人民共和国药典(2005年版)B.药典C.中华人民共和国药典D.中国药品标准(2005年版)E.中国药典8. 下列关于药典收载的药品项下鉴别试验的叙述,不正确的是:A. 鉴别试验不需具有专属性B. 鉴别试验仅适用于鉴别药物的真伪C. 鉴别试验不可以鉴别未知物D. 鉴别试验可分为一般鉴别试验和专属鉴别试验9. 2009年以前,中华人民共和国共出版了几版药典A.6版B.7版C.8版D.9版10. 按药典规定,精密标定的滴定液(如盐酸及其浓度)正确表示为A、盐酸滴定液(0.1520M)B、盐酸滴定液(0.1524mol/L)C、盐酸滴定液(0.1520M/L)D、0.1520M盐酸滴定液E、0.1520mol/L盐酸滴定液11. 滴定液的浓度系指:A.mol/LB.mmol/LC.g /100mlD.%(ml/ml)12. 药典所指的“精密称定”,系指称取重量应准确到所取质量的A、百分之一B、千分之一C、万分之一D、十万分之一E、百万分之一13. 关于中国药典,最正确的说法是A.一部药物分析的书B.收载所有药物的法典C.一部药物词典D.国家监督管理药品质量的法定技术标准E.我国中草药的法典14. 药物的鉴别试验是证明A.未知药物真伪B.已知药物真伪C.已知药物疗效D.未知药物纯度15. 重金属检查法中以硫化氢或硫代乙酰胺为显色剂时,溶液最适宜的pH值为A、3~5B、2~4C、3~3.5D、3~716. 古蔡法检砷时,砷化氢气体与下列哪种物质作用生成砷斑:A.碘化汞B.溴化汞C.硫化汞D.氯化汞17. Ag-DDC法检查砷盐时,判断结果的依据是A.吸收度的大小B.生成AsH3的多少C.砷斑D.溶液红色的深浅18. 热重分析法简称为A、TGAB、DTAC、DSCD、TMPE、USP19. 在药物的杂质检查中,其限量一般不超过百万分之十的是A.氯化物B.硫酸盐C.醋酸盐D.砷盐20. 氯化物检查中以50ml中含稀硝酸多少ml 为宜:A、8mlB、10mlC、12mlD、5ml21. 炽灼残渣检查法一般加热恒重的温度是:A.800~1000℃B. 700~800℃C.500~600℃D.600~700℃22. 磷酸可待因中检查吗啡,取本品0.20g,加HCL溶液使溶解成5ml,加亚硝酸钠试液2ml,放置15min,加氨试液3ml,所显颜色与吗啡溶液(取无水吗啡2.0mg,加HCL溶液溶解成100ml)5.0ml用同一方法制成的对照液比较不得更深,其限量是A、0.10%B、0.20%C、0.05%D、0.25%E、0.005%23. 药物中杂质的限量是:A.所含杂质的最大允许量B.杂质的检查量C.杂质是否存在D.杂质的合适含量24. 药物中氯化物杂质检查,是使该杂质在酸性溶液中与硝酸银作用生成氯化物浑浊,所用的酸是A、稀硫酸B、稀硝酸C、稀盐酸D、稀醋酸E、稀磷酸25. 检查某药品杂质限量时,称取供试品W(g),量取标准溶液V(ml),其浓度为C(g/ml),则该药的杂质限量(%)是A.%100⨯CVWB.%100⨯VCWC.%100⨯WVCD.%100⨯CVW26. 0.120与9.6782相乘结果为A、1.16B、1.1616C、1.2D、1.16227. 减少分析测定中偶然误差的方法为A、进行对照实验B、进行空白实验C、进行仪器校正D、增加平行实验次数28. 欲提取尿中某一碱性药物,其Pka为7.8要使99.9%的药物能被提取出来,尿样PH应调节到A、5.8 B、9.8C、4.8以下D、10.8或10.8以上29. 氧瓶燃烧法中最常用的吸收液是A、水B、氢氧化钠C、水-氢氧化钠D、过氧化氢30. 回收率属于药物分析方法效能指标中的A、精密度B、准确度C、检测限D、定量限31. 方法误差属A、偶然误差B、不可定误差C、随机误差D、系统误差32. 制备血浆时,在采取的血液中加入的抗凝剂是:A. 甲醛B. 苯丙酸C. 丙酮D. 肝素33. 测定卤素原子和脂肪碳链相连的含卤素有机药物(如三氯叔丁醇)的含量时,通常选用的方法是A、碱性氧化还原后测定法B、直接溶解后测定法C、碱性还原后测定法D、直接回流后测定法34. 精密度是指A、测得的值与真值接近的程度B、测得的一组测量值彼此符合的程度C、表示该法测量的正确性D、在各种正常实验条件下,对同一样品分析所得结果的准确程度35. 可见分光法的波长范围是A.400 ~ 760nmB.4000 ~ 667cm-1C.200 ~ 760nmD.200 ~ 400nm36. 用AgNO3液(0.1mol/L)滴定碘化钠(NaI=150)注射溶液,取检品2ml,置25ml 容量瓶中,加水到刻度,取此稀释液5ml进行滴定,消耗滴定液2.54ml,则此药液的百分浓度为:A.9.525%B.10%C.10.82%D.8.525%37. 配制5%某注射液,按其含量标准应为标示量的97.0~103.0%,则下面哪一种含量是合格的:A.4.80%B.4.84%C.5.08%D.5.19%38. 进行复方制剂各成分的含量测定时,选用下列哪一种分析方法直截了当,准确性较高A.紫外分光光度法B.薄层色谱法C.高效液相色谱法D.容量分析法39. 药物制剂的含量以A.制剂的浓度表示B.制剂的重量或体积表示C.以剂量表示D.以标示量百分数表示40. 配制5%注射液,按其含量标准应为97.0%~103.0%,下列哪一种含量是合格的?A. 5.14%B. 5.17%C. 4.84%D. 4.82%41. 原料药的含量是A.以理化常数值表示B.以百分数表示C.以标示量百分数表示D.以杂质总量表示42. 测定富马酸亚铁片的含量时,为防强氧化剂滴定时带来误差,常用下列那种方法进行测定A.高锰酸钾法B.碘量法C.重铬酸钾法D.硫酸铈法43. 单剂量固体制剂含量均匀度的检查是为了A.控制小剂量固体制剂、单剂中含药量的均匀程度B.严格重量差异的检查C.严格含量测定的可信程度D.避免制剂工艺的影响44. 制剂分析中,主要影响碘量法、亚硝酸钠滴定法、铈量法测定的添加剂是A. 滑石粉B. 磷酸钙C. 亚硫酸钠、亚硫酸氢钠D. 硬脂酸镁45. 安全试验所进行的项目与下列哪项无关:A、异常毒性B、热原C、降压物质D、PH值46. 在中国药典含量均匀度检查法的一个判别式A+1.80S=15.0中,A是A、初试中以mg表示的标示量与测定均值之差B、复试中以mg表示的标示量与测定均值之差C、初试中以100标示的标示量和测定均值之差的绝对值D、复试中以100表示的标示量与测定均值之差的绝对值E、初试中以100表示的标示量与测定均值之差。
化学中的金属有机化学及其应用

化学中的金属有机化学及其应用金属有机化学是一门化学分支领域,它研究的是含有金属元素和有机基团的化合物的合成、结构、反应机理以及应用。
这种化学分支的发展史可以追溯至19世纪初期,当时学者们就开始了解和试图合成一些含有金属-碳键的有机化合物,并研究这些化合物的性质。
在经过很长一段时间的研究和发展之后,金属有机化学的应用不断扩展,目前已经涉及到众多领域,如金属有机催化、金属有机材料、光电材料、生物药物等。
以下将具体论述金属有机化学的相关内容及其应用。
一、金属有机化学的基础金属有机化学的基础是金属与有机分子之间的配位作用。
金属在配位过程中会失去几个电子,形成正离子,而有机分子则通过配位,向金属离子提供自己的一些电子。
如此一来,这两者之间便形成了一种包括金属原子、有机基团、配体等在内的配位化合物。
这些化合物具有比单一的金属或有机分子更为复杂的性质和结构。
例如,多数金属有机化合物都是可溶于有机溶剂的,同时也具有较高的热稳定性,这些都是因为在这些化合物中金属与有机分子产生了一定的作用所导致的结果。
二、金属有机化学的主要反应金属有机化合物的特殊结构和性质使得它们能够进行很多独特的反应。
这些反应在应用中具有广泛的用途,如合成、催化反应等。
下面列举其中几种较为常见的金属有机化学反应。
1. 烷基化反应烷基化反应是指在金属有机化合物与烷烃反应时,烷基与有机基团之间发生的烷基迁移反应。
这种反应可用于合成一些化合物的同分异构体,如香豆素的同分异构体。
2. 插入反应插入反应是指一个分子中的一个原子(通常是一个碳原子)插入到一个金属有机化合物分子中,形成新的有机-金属化合物。
例如,钯催化下,苯乙烯可以与乙烯发生插入反应,得到底物插入到钯上的产物。
3. 消除反应消除反应是指金属有机化合物中的有机基团与氢、卤素等原子发生反应,使金属原子和其他原子形成新的化合物。
例如,苯乙烯可以与卤素反应,形成脱卤亚烷基化物。
三、金属有机化学的应用金属有机化学的应用可以广泛涉及到许多领域,如光电材料、生物药物、多相催化等。
第十一章吩噻嗪类药物分析
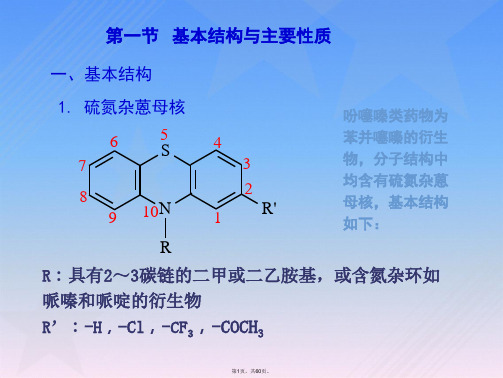
H3C N CH3 CH2
N
Cl
S O 3-(2-氯-10H-吩噻嗪-10-基)-N,N-二甲基-1-丙胺S-氧化物(Ⅴ)
O H3C N CH3
CH2
N
Cl
S
3-(2-氯-10H-吩噻嗪-10-基)-N,N-二甲基-1-丙胺N-氧化物(Ⅵ)
第23页,共60页。
❖ 有关物质的检查方法: (ChP2010)
❖ 显色反应
药物名称 硫 酸
硝酸
过氧化氢
盐酸氯丙嗪
显红色, 渐变淡黄色
—
盐酸异丙嗪 显樱桃红色,放置 生成红色沉淀,加热即溶解,
后颜色渐变深 溶液由红色转变为橙黄色
奋乃静
—
—
显深红色;放置后
红色渐褪去
盐酸氟奋乃静 显淡红色, 温热
—
—
后变成红褐色
盐酸三氟拉嗪
—
生成微带红色的白色沉淀; 放 —
置后, 红色变深, 加热后变黄色
优点:钯离子比色法可选择性地用于未被氧化的吩噻嗪类药 物的测定
第42页,共60页。
讨论:
(1)钯离子试剂: PdCl2和十二烷基硫酸酯钯盐。
用PdCl2时,形成的有色络合物水中溶解度小,样品量大时
,产生沉淀。
十二烷基硫酸酯钯盐,其络合物溶解度大,吸收强度增大 (约2倍)。
第43页,共60页。
第35页,共60页。
双波长分光光度法
波长选择:测定波长测,参比波长参
⊿A样
⊿A样=A测’ - A参’ ⊿A标= A测 - A参
测
⊿A标
参 C样=
第36页,共60页。
⊿A样 C标
⊿A标
(3)必要条件
① 干扰组分在两个波长处吸收度相等
p区非金属元素(一)(卤素、氧、硫)(3学时)

p区非金属元素(一)(卤素、氧、硫)(3学时)
卤素是无机元素,它的原子结构由海德兰(Heldelberg)系统中的17种元素构成,
这些元素包括氟(F)、氯(Cl)、溴(Br)、碘(I)和氙(Xe)。
在常温常压下,它
们分别以气体、液体和固体的形式存在。
除了碘外,卤素之间互相极其易溶,但已知性质
又有很大的不同。
由于卤素具有高的电负性,它们能够通过组装到多种特定的构型中形成电离软下化合物,如盐和硫酸盐。
因此,它们不仅可以提供对多种非金属元素的易溶性,还可以提供其
他种类的化学反应。
卤素最初发现于18月,由爱因斯坦(Einstein)等人发现,被称为“阿里斯王子”(Prince Albert)。
在20世纪开始以来,卤素则被广泛应用于农业、工业和放射性元素
提取等领域,包括催化芳烃反应、用合成药物等。
此外,卤素还有重要的作用,特别是当与其他物质(如氧、硫等元素)结合时,能够
丰富和改善空气质量。
例如,氯可以与水混合形成消毒剂,用于净化水;溴可以与水混合
形成净化剂,可用于净化工厂污水、污泥等;硫也可以改善空气质量,用于降低空气污染。
由于其许多特性,卤素对当今社会至关重要,它给改善生活质量和保护环境带来巨大
的贡献。
因此,在未来,卤素将继续被广泛应用于许多领域,并将一直是人类发展的重要
元素。
卤代苯与金属制格氏试剂

卤代苯与金属制格氏试剂一、引言卤代苯是一种重要的有机化合物,由于其特殊的结构和性质,在有机合成、药物合成、染料合成等领域有着广泛的应用。
格氏试剂是一种常用的有机合成中间体,可用于制备各种有机化合物。
近年来,卤代苯与金属反应制备格氏试剂成为研究的热点。
本文将对卤代苯的结构与性质、格氏试剂的合成与应用、卤代苯与金属的反应机制、卤代苯与金属制格氏试剂的条件与影响、反应实例与产物分析等方面进行综述。
二、卤代苯的结构与性质卤代苯是一种含有卤素原子的芳香族化合物,其基本结构与苯类似,不同的是苯环上的氢原子被卤素原子取代。
常见的卤代苯包括氯苯、溴苯、碘苯等。
由于卤素原子的电负性较强,卤代苯的电子云分布发生偏移,使得卤代苯具有一定的极性。
此外,卤素原子的吸电子效应使得卤代苯具有一定的反应活性。
三、格氏试剂的合成与应用格氏试剂是一种由镁和卤代烃反应制备的有机镁化合物,由于其具有很强的亲核性和反应活性,在有机合成中具有重要的应用价值。
格氏试剂可以用于制备各种有机化合物,如醇、醚、醛、酮等,还可用于烯烃的氢化、羰基化合物的还原等反应。
四、卤代苯与金属的反应机制卤代苯与金属的反应机制主要涉及电子转移和配位作用。
在反应过程中,金属原子首先与卤代苯的π键发生电子转移,形成络合物。
然后,金属原子与卤代苯的碳原子发生配位作用,形成稳定的络合物。
这个过程需要一定的能量和合适的反应条件才能进行。
五、卤代苯与金属制格氏试剂的条件与影响卤代苯与金属制格氏试剂的反应条件主要包括温度、压力、溶剂等。
一般来说,反应需要在一定的温度和压力下进行,并使用适当的溶剂作为反应介质。
不同的反应条件会对反应速率和产物产率产生影响。
例如,提高温度可以加快反应速率,但同时也可能导致副反应的发生和产物产率的下降;适当的压力可以提高产物产率;适当的溶剂可以提高反应速率和产物产率。
此外,反应过程中使用的金属种类也会对反应结果产生影响。
常见的用于制备格氏试剂的金属包括镁、锌、钙等。
7.1.1 碳原子的成键特点 烷烃的结构 课件 高一下学期化学人教版(2019)必修第二册

思考讨论 与甲烷结构相似的有机化合物还有很多,还有乙烷、丙烷、丁烷
等一系列有机化合物。
C2H6
C3H8
C4H10
仔细观察:结构上有哪些共同特点?分子式具有什么规律?
结构特点:
2.烷烃的结构特点
① 元素组成上只含 碳、氢 两种元素; ② 分子中的碳原子之间以 碳碳单键 结合成 链状 ; ③ 碳原子的剩余价键均与氢原子结合,化合价达到“饱和”
②多个碳原子可以相互结合成 链状, 也可以结合成 环状 (且可带支链)。
③碳原子还可以和 H、O、N、S、P、卤素 等多种非金属原子形 成共价键。
(2)组成有机物的碳原子数目灵活 有机物分子中可能只含有1个或几个碳原子,也可以含有成千上万 个碳原子。
思考讨论 请结合下图显示的 4 个碳原子相互结合的几种方式,分析以碳为
一、有机化合物中碳原子的成键特点
1.甲烷的分子结构
甲烷是最简单的有机物,甲烷分子中的碳原子以最外层的 4 个电子与 4 个
氢原子的电子形成 4 个 C—H 共价键,分子式: CH4 ;
电子式为
,结构式为
。
球棍模型
比例模型
2.有机物中碳原子的结构及成键特点
3.有机物种类繁多的原因 (1)碳原子间成键方式多样 ①碳碳之间的结合方式有单键、双键、三键。
这样一类的有机化合物称为饱和烃,也称为烷烃。
链状烷烃的通式: CnH2n+2(n≥1)
C5HX
12
C8HY
18
(1)下列有机物中,属于烷烃的是__C__F_D___
【课堂练习】
(2)写出下列各烷烃的分子式。
①烷烃A在同温同压下蒸气的密度是H2的43倍:___C_6_H_1_4____。 ②烷烃B的分子中含有200个氢原子:__C__99_H__20_0___。 ③分子中含有26个电子的烷烃:____C_3_H_8____。
ICPMS

定性和定量方式
(1)通过质荷比进行定性分析 (2)半定量分析,不需要标准溶液,多 数元素测定误差小于20% 3)用标准溶液校正进行定量 Quantitative Analysis) 中, 对于需进行分析测量的每一种元素都必 须提供标准溶液, 在完成标准曲线后才能 进行分析测定;
质量分析器
质量分析器是将离子源产生的离子按质 荷比(m/ z) 不同分开。常用的是四极杆型, 其次还有双聚焦、飞行时间(TOF) 和离 子阱型 ,其原理均与有机质谱中所用的质 量分析器相同。
离子检测器
离子的检测主要使用电子倍增器和法拉 第杯。法拉第杯是一个没有增益的金属 电极,具有较高的灵敏度,可扩展动态线性 范围的上限。
因此,有人提出用ICP-MS来进行药物、 药物中间体以及原料药的一般杂质检查 工作,以取代《美国药典》、《英国药 典》等收载的重金属限量检查和砷盐的 检查方法。
中药材质量评价和控制
中药材是我国的传统医药,其质量评价 的依据之一就是中药中的微量元素。但 由于中药具有成分复杂、微量元素含量 低、形态复杂等特点,因此,对其测定 方法选择的首要条件就是要灵敏度高、 选择性好。ICP-MS问世后,因被公认为 元素分析最有效的方法,而被引入到中 药微量元素的分析中。
体内药物分析
与常规药物分析相比,体内药物分析在 选择性、灵敏度和分析对象等方面都有 许多差异。生物样品更为复杂:微量药 物分布在大量生物介质中,并伴有大量 内源性物质和代谢物的干扰,这大大增 加了分析的难度,同时生物样品量少, 不易重新获得。因此,选择灵敏度高和 选择性好的分析方法较为重要。
从理论上说,ICP-MS的高灵敏度和选择 性为分析来自生物样品中含有可被其检 测的元素提供了较为理想的分析手段。 ICP-MS在含砷、铋、铝和铂等药物的体 内药物分析中有很好的分析效果。特别 是对AAS无法测定的含铂类药物分析, ICP-MS更是理想的方法。
