第4节 羧酸 氨基酸和蛋白质
4羧酸氨基酸和蛋白质(鲁科版选修5)

【对点演练】1.下列物质中,属于饱和一元脂肪酸的是( )A.乙二酸 B.苯甲酸 C.硬脂酸 D.石炭酸2.由—CH3、—OH、、—COOH四种基团两两组合而成的化合物中,其水溶液能使紫色石蕊试液变红的有( )A.1种 B.2种 C.3种 D.4种【自主学习】二、化学性质(以R—COOH为例)1.弱酸性(1)与碳酸氢钠反应:________________________________________(2)与氨气或氨水常温反应:___________________________________2.羟基被取代(1)制备酯类物质如R—COOH与R′—OH的反应:_____________________________________(2)制备酰胺如R—COOH与氨气加热反应:______________________________________3.αH被取代——合成卤代酸,进而制得氨基酸、羟基酸等如RCH2COOH与Cl2的反应:________________________________________4.还原反应——实现羧酸向醇的转化如R—COOH转化为醇:__________________________________________【对点演练】3.下列关于乙酸的说法正确的是( )A.乙酸有酸性,其酸性比碳酸酸性还强B.乙酸发生酯化反应时断裂羧基中的氢氧键C.乙酸分子中含有,类似于醛酮,易发生加成反应D.在一定条件下,乙酸能与Cl2发生取代反应,反应时-Cl取代最活泼的羧基氢原子4.已知溶液中存在平衡:,当与CH3CH2OH发生酯化反应时,不可能生成的是( )【课堂聚焦】2.酯化反应类型 (1)生成链状酯, ①一元羧酸和一元醇反应:②一元羧酸和二元醇反应:CH 3C OH OOHCH CH HO COOH HOOC 22--+-③二元羧酸和一元醇反应:HOOC-COOH +CH 3CH 2OH④无氧酸与醇反应:(2)生成环酯①多元醇和多元酸反应:OHCH CH HO COOH HOOC 22--+-②羟基酸分子间反应: 2CH 3CHOHCOOH③羟基酸分子内反应: HOCH 2CH 2CH 2COOH课堂 小结 作业 板书 设计 教学 反思课题第四节羧酸氨基酸和蛋白质(二)教具学案多媒体课件教学目的1.认识酯的结构,理解酯的性质。
第4节 羧酸、氨基酸和蛋白质(第2课时 氨基酸和蛋白质)

第4节羧酸、氨基酸和蛋白质(第2课时氨基酸和蛋白质)【学习目标】1..明确构成蛋白质的氨基酸的结构特点,氨基酸的两性。
2.掌握氨基酸的化学性质由羧基和氨基共同决定,肽键形成及水解,3.了解酶的催化作用特点【自主学习】二、氨基酸和蛋白质1、氨基酸的结构从结构上看,氨基酸是。
天然蛋白质水解后得到的均为,其结构可表示为。
常见的α-氨基酸有多种如:(写出其结构简式)甘氨酸: 缬氨酸: 苯丙氨酸:2、氨基酸的性质α-氨基酸结构上含有和,使其既有酸性,又有碱性,是典型的两性化合物,以甘氨酸为例写方程式①与盐酸反应。
②与氢氧化钠溶液反应。
[思考]:既能与强酸反应又能与强碱反应的物质有哪些?。
3、多肽、蛋白质(1)肽键的形成。
(写出甘氨酸和丙氨酸形成二肽,并用虚线框出肽键),由3个以上氨基酸缩合而成的酰胺均可称为多肽。
(2)肽键的水解:肽键易发生水解反应,生成。
蛋白质是由不同的α-氨基酸通过肽键结合成的复杂,常见的高分子化合物有那些?。
蛋白质的性质有哪几点?。
4、酶酶是具有生物活性的(类别),具有很强的作用,在催化方面具有什么特点?①. ②. ③.【课堂达标】1.下列五个不同基团中两个不同基团两两组合,形成的有机物能与NaOH反应的有( )①-OH ②-CH3③-COOH ④-C6H5⑤-CHOA.2种B.3种C.4种D.5种2.是一种由三种α-氨基酸分子脱水缩合生成的五肽的结构简式。
这种五肽彻底水解时,不可能产生的氨基酸是()3.某种解热镇痛药主要成分的结构简式为当它彻底水解时,可得到种产物,它们的结构简式分别为。
4.能使蛋白质变性的物质是( )①硫酸钾②甲醛③硝酸汞④氯化铵⑤氢氧化钠5.下列关于蛋白质的叙述错误的是( )A.在世界上我国首先合成了具有生命活力的蛋白质B.蛋白质是组成细胞的基础物质,它是一种纯净物质C.分子中含有羧基的物质溶于水后,溶液一定显酸性D.高温灭菌消毒的原理是加热后蛋白质变性,从而使细菌死亡6.下列有关蛋白质的叙述正确的是()A.蛋白质溶液中,加入浓的硫酸铵溶液有沉淀析出,加水后沉淀不溶解B.蛋白质水解的最后产物是氨基酸C.蛋白质的分子能透过半透膜D.蛋白质都能跟浓硝酸作用呈黄色7.甘氨酸和丙氨酸混合,在一定条件下发生缩合反应生成的二肽化合物共有( )A.4种B.3种C.2种D.1种4.扑热息痛是一种优良的解热镇痛药,其结构为,下列推测一定不正确的是( )A.能与盐酸反应B.能与NaOH反应C.能与溴水反应D.它是一种氨基酸5.下列物质中既能与NaOH溶液反应,又能与盐酸反应的是( )①②③④⑤⑥A.①②③B.①②③④C.①②③④⑥D.①②③④⑤⑥。
高中化学第2章第4节羧酸氨基酸和蛋白质第3课时氨基酸和蛋白质课件鲁科版选修5

3.你如何鉴别想要购买的毛线是“纯毛”的还是“腈 纶”的?
【提示】 可以用灼烧的方法,“纯毛”毛线灼烧后有 烧焦羽毛的气味。
休息时间到啦
同学们,下课休息十分钟。现在是休息时间,你们休 睛,
看看远处,要保护好眼睛哦~站起来动一动,久坐对 哦~
酶
氨基酸、蛋白质和酶的结构特点及主 要化学性质
【问题导思】 ①氨基酸为什么具有两性? 【提示】 氨基酸分子中既有氨基(显碱性)又有羧基(显 酸性),因此氨基酸具有两性。
浓硝酸可使含 有苯环的蛋白 质分子显黄色
化学变化
化学变化
鉴别酚类、鉴别 鉴别某些蛋白
淀粉
质
利用焰色反应只能鉴别某些金属元素,如碱金属及 Ca、Ba、Cu等;利用颜色反应只能鉴别含有苯环的蛋白 质。
能用于鉴别淀粉、肥皂和蛋白质三种溶液的试
剂是( )
A.碘水
B.烧碱溶液
C.浓硝酸
D.MgSO4溶液
【解析】 蛋白质与浓硝酸作用变黄色;肥皂液与浓硝 酸作用会产生难溶于水的高级脂肪酸沉淀;而淀粉与浓硝酸 不反应。
【答案】 D
解答此类题目的关键是找准肽键的断裂位置,并使氨 基、羧基复原。
1.苯丙氨酸的结构简式为:
(1)该分子中的碱性基是________,苯丙氨酸与盐酸反 应的化学方程式为_________________________。
(2)该分子中的酸性基是________,苯丙氨酸与 NaOH(aq)反应的化学方程式是_____________________。
人体中的蛋白质与重金属盐作用而解毒。
【答案】 A
2.(2013·大同高二质检)误食重金属盐会使人中毒, 可以解毒的急救措施是( )
A.服用鸡蛋清或牛奶
2.4 羧酸 氨基酸和蛋白质开课

第一课时 羧酸
资料卡片
自然界和日常生活中的有机酸
安息香酸 (苯甲酸)
COOH COOH COOH
草酸 (乙二酸)
蚁酸(甲酸) HCOOH
醋酸(乙酸)
CH3COOH
未成熟的梅子、李子、杏子等 水果中,含有草酸、安息香酸 等成分
苹果酸
CH2—COOH
CH2COOH CH(OH)COOH
反应
反应
【课堂练习】
1.下列物质中不能发生银镜反应的是 A. B. C. D.
OH CHCH2COOH
(D )
2.某有机物的结构简式为HO 它可以发生的化学反应的 反应类型有:
取代,加成,消去,酯化,中和,缩聚
3、下列5个有机化合物中,能够发生酯化, 加成和氧化3种反应的是( C ) ①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH2=CHCH2OH ④CH2CH2CH2OH ⑤CH3CH(OH)CH2CHO A ①③④ B ②④⑤ C ①③⑤ D ①②⑤
硬脂酸 饱和酸
油酸 软脂酸 不饱和酸 饱和酸
(3)羧酸命名
①选含羧基的最长的碳链作为主链,按主 链碳原子数称“某酸”; ②从羧基开始给主链碳原子编号; ③在“某酸”名称之前加上取代基的位次 号和名称。 CH3 3 2 1 6 5 4 例如:
CH3–C–CH2–CH–CH2–COOH CH3 CH3
–COOH 由-OH和 C=O直接相连 O || R—C—O—H
(2)分类
一元羧酸 CH3COOH
CH2—COOH HO—C—COOH
根据分子中羧基的数目 二元羧酸 HOOC-COOH 多元羧酸 根据烃基的不同 芳香酸
第四节 羧酸 氨基酸和蛋白质(共33张PPT)

第三十二页,编辑于星期一:二十点 五十五分。
C 1、以下过程中,不可逆的是〔 〕
A.蛋白质的盐析 B.酯的水解
C.蛋白质的变性 D.氯化铁的水解
2、欲将蛋白质从水中析出而又不改变它的性
C 质应参加〔 〕 A.甲醛溶液
B.CuSO4溶液
C.饱和Na2SO4溶液 D.浓硫酸
33
第三十三页,编辑于星期一:二十点 五十五分。
5、一环酯化合物,结构简式如下:
试推断:
1.该环酯化合物在酸性条件下水解的产物是什么?
写出其结构简式;
2.写出此水解产物与金属钠反响的化学方程式;
3.此水解产物是否可能与FeCl3溶液发生变色反响?
24
第二十四页,编辑于星期一:二十点 五十五分。
25
第二十五页,编辑于星期一:二十点 五十五分。
26
13
第十三页,编辑于星期一:二十点 五十五分。
3.酯的通式
饱和一元羧酸和饱和一元醇生成的酯 〔1〕一般通式:RCOOR' 〔2〕组成通式:CnH2nO2
14
第十四页,编辑于星期一:二十点 五十五分。
二、酯的结构、性质及用途
1.酯的物理性质
①低级酯是具有芳香气味的液体。
②密度比水小。
③难溶于水,易溶于乙醇和乙醚等有机溶 剂。
〔3〕CH3CH218OOCCH3
〔4〕以上都不对
11
第十一页,编辑于星期一:二十点 五十五分。
12
第十二页,编辑于星期一:二十点 五十五分。
酯的命名——“某酸某酯〞 说出以下化合物的名称:
〔1〕CH3COOCH2CH3 乙酸乙酯
〔2〕HCOOCH2CH3 甲酸乙酯
〔3〕CH3CH2O—NO2 硝酸乙酯
高中化学 第二章第四节 羧酸 氨基酸和蛋白质 鲁科版选修5

【思考、讨论】
1、误服重金属怎么解毒? 2、为什么医院用高温,照紫外线,喷 洒苯酚和酒精溶液消毒? 3、为什么用甲醛保存动物标本?
盐析与变性的对比
盐析
变性
相同点
加入某种物质后有沉淀生成
不 同
盐 加入某些浓盐溶液,
不 如: Na2SO4 同 (NH4)2SO4等
重金属盐、醛、 加热或剧烈震动
一、氨基酸
什么是氨
1、几种常见的氨基酸:
基酸?
(1) 甘氨酸
CH2—COOH
羧酸分 子里烃
NH2
(2) 丙氨酸
基上的 氢原子
CH3—CH—COOH 被氨基
(3) 谷氨酸
NH2
取代后 的生成
HOOC—(CH2)2—CH—COOH
物叫氨 基酸。
NH2
2、氨基酸的性质
(1)既能与酸反应又能与碱反应 与氢氧化钠的反应: NH2CH2COOH+NaOH→NH2CH2COO-Na++H2O
+ H 2NC H 2 CN HC H 2 CO HH 2O
肽键
两个氨基酸分子(可以相同,也可以不同),在酸 或碱的存在下加热,通过一分子的氨基与另一分子 的羧基间脱去一分子水,缩合形成含有肽键的化合 物,成为成肽反应。
二、蛋白质的结构与性质
• 蛋白质分子中含有 C、O、H、N、S 等元素。1965年 我国科技工作者成 功合成了具有生物 活性的——结晶牛 胰岛素。这是科学 史上的一大成就, 可以说是科学史上 又一“丰碑”。
SARS病毒的电子图片
SARS病的凶手——冠状病毒, 有自 己的核酸和蛋白质。它进入人体后, 借助人体内的原料合成病毒。当我们 人体发病时,就是它的蛋白质对我们 起了作用。
羧酸 氨基酸和蛋白质

第4节羧酸氨基酸和蛋白质教材分析与本章第3节类似,本节教材是由体现有机化合物官能团体系的羧酸和生命活动中的重要化学物质一一蛋白质、氨基酸两部分组成的。
本节教材讨论了三类与羧基有关的物质:羧酸、羧酸衍生物(酯)和取代羧酸(氨基酸),它们与学生己学过的烃、卤代烃、醇、酚、醛、酮构成了以官能团为线索的有机化合物知识体系。
本节是全章教材的最后一节,也是本模块中按照物质类别系统学习有机化合物知识的最后一节。
通过《化学2(必修)》和本模块前面章节的学习,学生对有机化合物结构与性质的关系、有机化学反应类型已有了丰富的知识积累和较为深刻的理解,所以本节教材改变直接讨论羧基化学性质的方法,引导学生充分运用已有知识进行预测和演绎,分析羧基官能团的结构特点,并将羧基与前面学习过的羟基和羰基进行比较,得出"羧基与羟基和羰基的性质既有一致的地方,又由于官能团间的相互影响而有特殊之处"的结论。
本节教材的学习既是新知识的形成,又是对前面所学知识的总结、应用和提高。
在以往的中学化学教材中很少讨论取代羧酸,但取代羧酸在生产、生活和生命活动中有着极为广泛的应用。
例如,氨基酸是由氨基取代了羧酸分子中烃基上的氢原子形成的取代羧酸,它是合成多肽、蛋白质的基石;另外,生活中常见的乳酸、柠檬酸等都是取代羧酸。
因此,本节教材以氨基酸为代表物初步介绍了取代羧酸的性质,同时又以氨基酸为核心介绍蛋白质的构成及性质。
本节教材以化学必修教材内容为基础,从化学本质上揭示氨基酸是怎样构成蛋白质的,以及蛋白质为什么会具有复杂而多样的生理活性。
通过这部分内容的学习,学生可以感受到化学与人类的生命活动息息相关,化学工作者为生命科学的发展做出了巨大贡献。
本节教材内容结构如下:教学目标1.了解羧酸的结构特点、主要化学性质及从羧酸到醇、酯的转化,能举例说明羧基与羰基、烃基性质的差别,并进一步体会官能团之间的相互作用对有机化合物性质的影响。
2.能举例说明什么是羧酸衍生物,认识酯的结构特点和主要性质,并能结合肥皂的制备说明酯在碱性条件下水解的应用。
高中化学 第4节 羧酸、氨基酸和蛋白质课件 鲁科版选修5

按烃基的不同脂芳肪香酸酸::如如CC6HH3C5CHO2OCOHO苯H甲丙酸酸 按羧基的数目一二元元羧羧酸酸::CHHO2O==C=—CCHO—OCHOO乙H二丙酸烯 酸
栏 目 链 接
低级脂肪酸:CH3COOH乙酸 按碳原子数目高级脂肪酸CC1177HH3353CCOOOOHH硬油脂酸酸
第七页,共75页。
第二十页,共75页。
(4)氨基酸的等电点是氨基酸水溶液中阴、阳离子浓度 相等时的pH;达到等电点时,氨基酸在水中的溶解度最小。
(5)可发生缩合(suōhé)反应。
栏
目
2.多肽。
链 接
(1)酰胺键的结构式为
,可简写为___________。
它又称为________,它是由一个 α氨基酸分子的________
栏 目
羟基上的氢原子________以离子形式电离出来,所以羧酸有酸 更易
链 接
性。与醛、酮的羰基相比,羧基中的羰基较________发生加成
反应。羧酸________通过催化加氢的方法被还原,用强还原剂 如氢化难铝锂(LiAlH4)时才可以将羧酸很还难原为相应的醇。与羧基
相连的αH较活泼,易被取代。
栏
目
5.认识人工合成多肽、蛋白质和核酸的意义,体会
链
接
化学科学在生命科学发展中的重要意义。
第四页,共75页。
栏 目 链 接
第五页,共75页。
一、羧酸(suō suān)
1.羧酸概述。
(1)定义。
叫做(ji分ào子zu由ò)_羧__酸烃__,基__官_(能或团氢是原—子C)和OO__H_。___羧__相基连(su而ō组jī)成的有机化合物
栏 目 链 接
(2)羧酸的分类。
鲁科版《有机化学基础》第2章第4节羧酸 氨基酸和蛋白质 第2课时氨基酸蛋白质教学课件
温故 知新
1、定义:
自主
氨基酸是羧酸分子里烃基上的氢原子被氨
合作
基取代的化合物。
精讲 2、结构:α-氨基酸的结构简式可表示为
突破
R—CH—COOH
检测
反馈
NH2
反思 含有两种官能团-------氨基和羧基
批判
3、物理性质
温故
知新 天然的氨基酸都是无 色晶体,熔点较 低, 自主 在2000C-3000C熔化时分解。它们能溶 合作 于强酸 或 强碱 溶液中,除少数外一般 精讲 都 能 溶于水,而 难 溶于乙醇、乙醚。
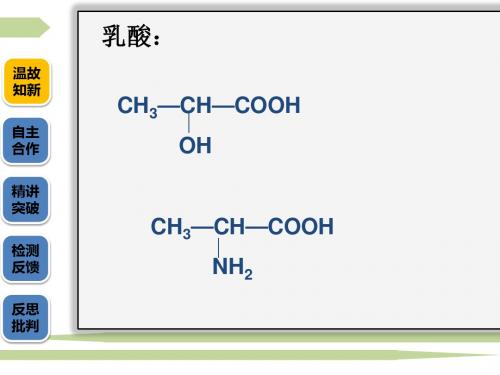
乳酸:
温故
知新
CH3—CH—COOH
自主
合作
OH
精讲
突破
CH3—CH—COOH
检测
反馈
NH2
反思 批判
鲁科版 第2章 第4节
氨基酸和蛋白质
高二化学备课组
学习目标
1.掌握氨基酸的组成、结构特点和主要化学性质;
2.了解蛋白质的组成、结构和性质。
学习重点
氨基酸的结构和性质,蛋白质的性质。
Hale Waihona Puke 一、氨基酸的结构与性质批判
酶作催化剂时催化效率与温度的关系曲线
温故
知新 速 率
自主 合作
精讲 突破
检测 反馈
0
反思 批判
37℃左右
温度(℃)
1.下列说法错误的是 (AB)
温故
知新 A.蔗糖、果糖和麦芽糖均为双糖
自主 B.酶是一类具有高选择催化性能的蛋白质 合作 C.植物油含不饱和脂肪酸酯,能使Br2/CCl4褪色
温故
知新 ①由蛋白质变性引起的蛋白质凝结是不可逆
的,是化学变化;
化学《羧酸氨基酸和蛋白质》

羧酸的命名通常以烃基为基础, 将“酸”字加在烃基名称之后,
如乙酸、丙酸等。
羧酸性质及反应
羧酸具有酸性,能与碱反应生成盐和水。其酸性来源于羧基中的羟基氢原子具有一 定的离解能力。
羧酸能与醇发生酯化反应,生成酯和水。这是羧酸的一种重要反应类型,也是生物 体内许多重要化学反应的基础。
蛋白质组学的意义
有助于深入了解生命的本质和疾病的发生发展机制,为药物设计、疾病诊断和治疗提供新的思路 和方法。同时,蛋白质组学也为生物技术的发展提供了新的契机和挑战。
THANKS FOR WATCHING
感谢您的观看
盐析法
层析法
通过加入中性盐使蛋白质溶解度降低而析 出,常用于蛋白质的初步分离。
利用蛋白质在固定相和流动相之间的分配 平衡原理进行分离,包括凝胶层析、离子 交换层析、亲和层析等。
电泳法
超滤法
在电场作用下,蛋白质因所带电荷和分子 大小不同而迁移速率不同,从而实现分离 。包括凝胶电泳、等电聚焦电泳等。
利用超滤膜对溶液中不同分子量的蛋白质 进行分离,常用于蛋白质的浓缩和脱盐。
设计与合成。
非天然氨基酸设计合成挑战与机遇
非天然氨基酸的设计原则
基于天然氨基酸的结构和性质,通过改变侧链基团或引入新的官能团,设计出具有独特功 能和性质的非天然氨基酸。
非天然氨基酸的合成方法
包括化学合成、生物合成和组合化学等方法,其中化学合成方法具有反应条件温和、合成 步骤简单等优点。
非天然氨基酸的应用前景
羧酸在生物体内具有多种作用,如参与能量代谢、合成脂肪酸和酮体等。
氨基酸在生物体内代谢途径及作用
氨基酸代谢途径
氨基酸在生物体内主要通过转氨基作 用、脱氨基作用等代谢途径进行分解 和合成。
高二化学第4节 羧酸 氨基酸和蛋白质知识精讲一 鲁教版

高二化学第4节羧酸氨基酸和蛋白质知识精讲一鲁教版一. 本周教学内容:第4节羧酸氨基酸和蛋白质(一)教学目的:1. 了解羧酸,掌握乙酸的性质。
2. 掌握羧酸的性质。
二. 重点、难点:羧酸的化学性质知识分析:(一)羧酸1. 羧酸概述(1)定义:分子由烃基(或H原子)和羧基相连组成的有机物叫羧酸。
官能团-COOH,饱和一元羧酸的通式为CnH2nO2。
(2)分类①根据羧基所连接的烃基的不同,羧酸可分为脂肪酸(如:乙酸、丙酸)和芳香酸。
(如:苯甲酸)。
②根据羧酸分子中含有羧基的数目来分类,含有一个羧基的叫一元羧酸,含有两个羧基的叫二元羧酸。
(如:乙二酸、己二酸等。
)③根据碳原子数目可分为低级酸和高级酸。
高级脂肪酸:通常把脂肪酸分子中含碳原子数较多的称为高级脂肪酸。
硬脂酸C17H35COOH 软脂酸C15H31COOH油酸C17H33COOH(3)命名①选主链:选取包含羧基的最长碳链作主链,按主链碳原子数称为某酸;②编位次:从羧基一端开始给主碳原子编号;③定名称:在某酸名称之前加上取代基的位次号和名称。
例如:CH3CH(CH3)CH2CH2COOH CH3CH2CH(CH3)CH(CH2CH3)COOH4-甲基戊酸3-甲基-2-乙基戊酸(4)同分异构体写出CH3CH(CH3)CH2COOH的同分异构体同类异构—(碳链异构)CH3CH2CH(CH3)COOH (CH3)3CCOOH CH3CH2CH2CH2COOH类别异构—(官能团异构)HCOOCH2CH2CH2CH3HCOOCH(CH3)CH2CH3HCOOCH2CH(CH3)2HCOOC(CH3)3CH3COOCH2CH2CH3CH3COOCH(CH3)2说明:官能团异构除了羧酸与酯外,还可以与羟基醛,此处省略。
*取代羧酸:羧酸分子中烃基上的羟基被其他原子或原子团取代所得的产物。
如:氯乙酸:CH 3COCl α-氨基乙酸 H 2NCH 2COOH 乳酸 CH 3CH(OH)COOH2. 羧酸性质(1)物理性质:在多种羧酸分子中,由于和羧基直接相连的烃基的不同,它们的物理性质又有所不同:如溶解性,低级脂肪酸易溶于水,而高级脂肪酸难溶于水;熔沸点,高级脂肪酸要高于低级脂肪酸。
化学:3..4《羧酸 氨基酸和蛋白质》素材(鲁科版选修5)

第4节羧酸氨基酸和蛋白质氨基酸一、氨基酸的概念氨基酸<amino acid):含有氨基和羧基的一类有机化合物的通称。
生物功能大分子蛋白质的基本组成单位,是构成动物营养所需蛋白质的基本物质。
是含有一个碱性氨基和一个酸性羧基的有机化合物,氨基一般连在α-碳上。
fUjTnXaUaE氨基酸的结构通式:构成蛋白质的氨基酸都是一类含有羧基并在与羧基相连的碳原子下连有氨基的有机化合物,目前自然界中尚未发现蛋白质中有氨基和羧基不连在同一个碳原子上的氨基酸。
fUjTnXaUaE二、氨基酸的分类www.天然的氨基酸现已经发现的有300多种,其中人体所需的氨基酸约有22种,分非必需氨基酸和必需氨基酸<人体无法自身合成)。
另有酸性、碱性、中性、杂环分类,是根据其化学性质分类的。
fUjTnXaUaE1. 必需氨基酸<essential amino acid):指人体<或其它脊椎动物)不能合成或合成速度远不适应机体的需要,必需由食物蛋白供给,这些氨基酸称为必需氨基酸。
共有8种其作用分别是:fUjTnXaUaE①赖氨酸<Lysine ):促进大脑发育,是肝及胆的组成成分,能促进脂肪代谢,调节松果腺、乳腺、黄体及卵巢,防止细胞退化;fUjTnXaUaE②色氨酸<Tryptophane):促进胃液及胰液的产生;③苯丙氨酸<Phenylalanine):参与消除肾及膀胱功能的损耗;④蛋氨酸<又叫甲硫氨酸)<Methionine);参与组成血红蛋白、组织与血清,有促进脾脏、胰脏及淋巴的功能;fUjTnXaUaE⑤苏氨酸<Threonine):有转变某些氨基酸达到平衡的功能;⑥异亮氨酸<Isoleucine ):参与胸腺、脾脏及脑下腺的调节以及代谢;脑下腺属总司令部作用于甲状腺、性腺; fUjTnXaUaE⑦亮氨酸<Leucine ):作用平衡异亮氨酸;⑧缬氨酸<Valine):作用于黄体、乳腺及卵巢。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第4节羧酸氨基酸和蛋白质【基础导学单】一、羧酸1、羧酸概述羧酸的定义:____________________________________________;官能团:_________.1)羧酸的分类根据分子里的烃基是否饱和______________________ ; __________________________根据烃基种类数目的不同羧酸可分为:___________________ 和_____________________根据分子中羧基数目的不同羧酸可分为:______________ ________________________ _______________________2)羧酸命名i 选取含有羧基的最长碳链作为主链,按主链碳原子数称为“某酸”。
ii 从羧基开始给主链碳原子编号。
iii 在“某酸”名称前加上取代基的位次号和名称。
3)羧酸的溶解性分子中碳原子数在4以下的羧酸能与水互溶。
随着分子中碳链的增长,羧酸在水中的溶解度迅速减小,直至与相对分子质量相近的烷烃的溶解度相近。
4)羧酸的沸点较高,而且比相应的醇沸点高。
请你用学过的知识解释羧酸的溶解性规律和沸点较高的原因。
_____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________5)常见的羧酸2、羧酸的化学性质下式是丙酸的结构式H H O 可发生化学反应的部位可发生反应的类型| | || ___________________________________________H — C —C —C —O —H| | ___________________________________________H H___________________________________________羧酸的化学性质_______________________________________________________________________________ 化学性质 化学反应举例 用途举例_______________________________________________________________________________酸性(具有酸的通性)_______________________________________________________________________________羟基被取代的反应_______________________________________________________________________________α—H 被取代的反应_______________________________________________________________________________还原反应_______________________________________________________________________________3、羧酸衍生物——酯知识支持:羧酸衍生物的定义:_____________________________________________________; 羧酸分子中的羧基去掉羟基后剩余的基团称为____________; 酰卤、酸酐、酰胺、酯。
酰卤:分子由酰基与卤素原子(-X)相连组成的羧酸衍生物。
酸酐:分子由酰基与酰氧基(R -C-O-)相连组成的羧酸衍生物。
酰胺:分子由酰基与氨基(-NH 2)相连组成的羧酸衍生物。
羧酸酯 :分子由酰基与烃氧基(RO -)相连组成的羧酸衍生物。
1)酯的结构及性质知识支持:多角度认识酯化反应反应条件:___________________________;反应物:_____________________________; 反应机理反:_________________________; 应方方式:___________________________①一元羧酸与一元醇反应通式:___________________________________________________ ②二元羧酸与二元醇,可以酯化成链,并形成高分子化合物,也可形成酯化成环状小分子酯。
如乙二酸和对苯二甲酸的反应生成高分子化合物,(缩聚反应)O‖方程:_________________________________________________________________________乙二酸与乙二醇酯化成环状小分子酯,方程:________________________________________③羟基羧酸可自身酯化形成环状内酯,也可以分子间酯化形成环状小分子酯或链状高分子化合物(酯)。
请写出α—羟基丙酸(乳酸)形成环状内酯、分子间子间酯化形成环状小分子酯和链状高分子化合物(酯)涉及的三个方程:______________________________________________________________________________________________________________________________________________________________________________________________________________________________________(2)酯的结构______________________________________(3)酯的物理性质①_________________________________;②_________________________________;③_________________________________。
(4)酯的水解在有酸、碱存在和加热条件下,酯可以发生水解反应,生成对应的________________。
酯的水解反应是酯化反应的______________________.水解通式:________________________________________________二、氨基酸和蛋白质联想·质疑蛋白质在机体中发挥着多种生理功能________、______________、______________、_____________、________________、_________等都是由不同的蛋白质构成的。
蛋白质能够供给________ 、_________ 、________、_________ 、______________等。
_________也是一种在生命过程中有着十分重要作用的物质。
_________ 和__________都由_______组成。
1.分子结构(1)氨基酸是氨基取代了羧酸分子中烃基上的氢原子形成的。
(2)官能团:天然蛋白质水解的最终产物都是。
(3)α-氨基酸:______________________________________2.氨基酸的性质(1)两性:①解离形式②应用当调节溶液的pH为某一特定值时,可以使溶液中阴、阳离子的相等,为零,此时溶液的pH称为该氨基酸的。
达到此点时,氨基酸在水中的最小。
可以根据此来。
(2)成肽反应:氨基酸形成二肽的断键原理:羧基断键,氨基断键。
有三个氨基酸分子脱水缩合形成的是三肽,三肽以上可称____________。
官能团:__________键,又叫________,表示为_________________。
以甘氨酸和丙氨酸为例,写出形成二肽的方程式。
_______________________________________________________________________3.蛋白质蛋白质是由不同的氨基酸通过肽键结合而成的复杂高分子化合物,结构和组成十分复杂。
目前,人类对蛋白质的结构,特别是空间结构的认识还十分有限。
(1)物质基础:___________________。
(2)核心官能团:_______________________。
(3)分子大小:相对分子量一般在_____________以上,含肽键______个以上(4)蛋白质的基本性质①水解:蛋白质在__________作用下水解,最终产物为________(天然蛋白质水解产物全部是________________)。
②两性:仍具有_________的性质,能跟_________________反应。
③盐析:加入_______________________,可以_____________________的溶解度,从而析出蛋白质。
盐析是______的过程,盐析后的蛋白质仍具有生命力。
因而盐析可用于______和___________-蛋白质。
④变性:热、紫外线、强碱、强酸、重金属盐、乙醇、甲醛等都能使蛋白质____________(产生凝结现象)。
变性是________________,利用此性质可进行消毒,但也能引起中毒。
⑤颜色反应:某些蛋白质和浓HNO3作用显__________,称为“黄蛋白反应”。
用于鉴别蛋白质(变黄的蛋白质结构中含有____________)。
⑥灼烧时产生_________________气味。
用于区别合成纤维与纯毛。
4.酶是一类,是一种高效。
酶催化的主要特点是(1)需要;(2)具有高度的;(3)。
【问题生成单】1、羧酸与酯存在同分异构现象试写出C5H10O2 的同分异构(羧酸类和酯类)、羧酸类:_____________________________________________________________________;酯类:_______________________________________________________________________________________________________________________________________________________2、讨论:酸、碱性条件下酯的水解哪个更彻底;请用文字和方程做一解释。
