酞菁的制备和纯化
酞菁铁Ⅱ的制备及表征

酞菁铁(Ⅱ)的制备及表征武汉大学化学与分子科学学院王小尚 200331050033摘要:通过制备Fe(OH)2·4H2O制备酞菁铁(Ⅱ), 并对产品进行纯化,通过紫外及红外的方法分析确定其组成关键字:酞菁铁(Ⅱ);制备;纯化;红外;紫外分光法1.前言酞菁类化合物可以看成四氮杂卟啉的衍生物,具有D2h点群对称性。
其在染料工业和光电功能材料等方面获得了巨大的应用,并具有电致变色效应,在室温下有很好的液晶相,也在催化剂,抗辐射剂等方面也有重要作用。
酞菁类化合物的合成一般采用Linstead合成方法,其提纯比较困难。
反应产物中含有大量的杂质,包括原料和一些其他高分子聚合物,常用的提纯方法有微热丙酮索氏萃取除杂,真空升华,浓H2SO4再沉淀或色谱柱提纯。
合成酞菁铁的前体有:邻苯二甲酸,邻苯二甲酸酐,邻苯二甲氰,邻苯二甲酸氨酯等。
本实验以邻苯二甲酸酐,Fe(OH)2·4H2O(自制),尿素为原料,以(NH4)2MoO4为催化剂,采用固相熔融法合成FePc,用真空升华法提纯产物,纯产物经元素分析,红外及紫外可见光谱表征。
2.实验部分2.1试剂及仪器:1.试剂还原铁粉,6mol/L盐酸,邻苯二甲酸酐,尿素,乙醇,10%氢氧化钠,酸铵,浓硫酸2.仪器减压过滤装置,旋转蒸发仪,真空干燥器,量筒(50mL),三口瓶(250mL,100mL),滤纸,烧杯(250mL),24#圆底烧瓶(100mL),24#空气冷凝管,24#磨口弯头,24#磨口塞,油泵,19#导气管,橡皮管,电热套(250mL), 研钵,温度计(3000C),长玻棒,容量瓶(50mL)表面皿,牛角勺,天平,氮气钢瓶,管式电炉,旋子流量计,石英管,烘箱,小瓷舟,UV-Vis 分光光度计,红外光谱仪。
2.2实验步骤:1. FeCl2·4H2O的制备称取5.67g还原铁粉放入100 mL的三口烧瓶中,并向其中加入30 mL6mol/L的盐酸溶液,缓缓通入氮气至液面下,烧瓶上的一个瓶口用导气管将逸出气体(包括反应的生的H2和为了防止氧化而通入的N2以及少量HCl气体)通经过安全瓶(防倒吸)导入稀碱溶液(中和逸出的少量HCl气体)。
金属酞菁的合成及表征
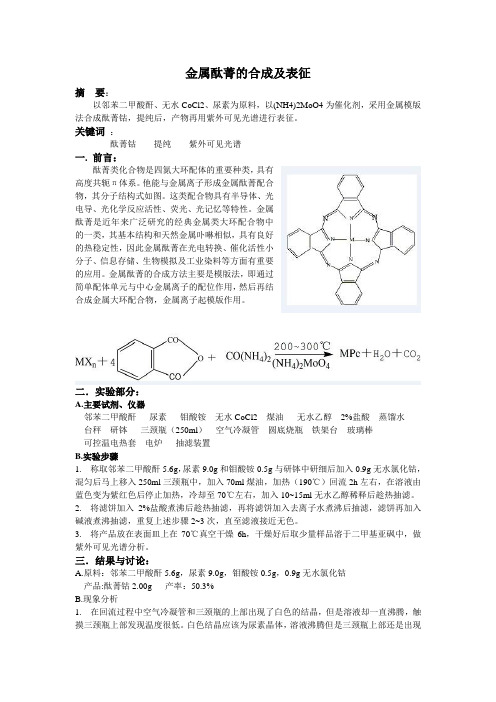
金属酞菁的合成及表征摘要:以邻苯二甲酸酐、无水CoCl2、尿素为原料,以(NH4)2MoO4为催化剂,采用金属模版法合成酞菁钴,提纯后,产物再用紫外可见光谱进行表征。
关键词:酞菁钴提纯紫外可见光谱一. 前言:酞菁类化合物是四氮大环配体的重要种类,具有高度共轭π体系。
他能与金属离子形成金属酞菁配合物,其分子结构式如图。
这类配合物具有半导体、光电导、光化学反应活性、荧光、光记忆等特性。
金属酞菁是近年来广泛研究的经典金属类大环配合物中的一类,其基本结构和天然金属卟啉相似,具有良好的热稳定性,因此金属酞菁在光电转换、催化活性小分子、信息存储、生物模拟及工业染料等方面有重要的应用。
金属酞菁的合成方法主要是模版法,即通过简单配体单元与中心金属离子的配位作用,然后再结合成金属大环配合物,金属离子起模版作用。
二.实验部分:A.主要试剂、仪器邻苯二甲酸酐尿素钼酸铵无水CoCl2 煤油无水乙醇2%盐酸蒸馏水台秤研钵三颈瓶(250ml)空气冷凝管圆底烧瓶铁架台玻璃棒可控温电热套电炉抽滤装置B.实验步骤1. 称取邻苯二甲酸酐5.6g,尿素9.0g和钼酸铵0.5g与研钵中研细后加入0.9g无水氯化钴,混匀后马上移入250ml三颈瓶中,加入70ml煤油,加热(190℃)回流2h左右,在溶液由蓝色变为紫红色后停止加热,冷却至70℃左右,加入10~15ml无水乙醇稀释后趁热抽滤。
2. 将滤饼加入2%盐酸煮沸后趁热抽滤,再将滤饼加入去离子水煮沸后抽滤,滤饼再加入碱液煮沸抽滤,重复上述步骤2~3次,直至滤液接近无色。
3. 将产品放在表面皿上在70℃真空干燥6h,干燥好后取少量样品溶于二甲基亚砜中,做紫外可见光谱分析。
三.结果与讨论:A.原料:邻苯二甲酸酐5.6g,尿素9.0g,钼酸铵0.5g,0.9g无水氯化钴产品:酞菁钴2.00g 产率:50.3%B.现象分析1. 在回流过程中空气冷凝管和三颈瓶的上部出现了白色的结晶,但是溶液却一直沸腾,触摸三颈瓶上部发现温度很低。
酞菁合成方法的研究进展

酞菁合成方法的研究进展作者:薛科创来源:《当代化工》2015年第10期摘要:酞菁一个18个π电子的大环共轭体系,它可以应用在染料、光动力学治疗、催化剂、半导体材料等方面。
为了得到性能优良的酞菁,人们开发了邻苯二甲腈方法、苯酐—尿素方法、二亚氨基异吲哚啉方法、锂酞菁或者自由酞菁置换方法。
关键词:酞菁;性能;合成方法中图分类号:TQ 028 文献标识码: A 文章编号: 1671-0460(2015)10-2368-03Research Progress of Phthalocyanine Synthesis MethodsXUE Ke-chuang(School of Chemical Engineering, Shaanxi Institute of Technology,Shaanxi Xi’an 710302, China)Abstract:Phthalocyanines are a conjugated macrocyclic system with 18 π el ectrons, which can be used in dyes, photodynamic therapy, catalyst, semiconductor materials and so on. To obtain excellent performance phthalocyanines, many synthesis methods have been developed,such as phthalonitrile method, benzene bitter wine-urea method, and so on.Key words: Phthalocyanine; Performance; Synthesis method酞菁一个18个π电子的大环共轭体系,由于酞菁具有良好的热稳定性[1],难溶解性和化学稳定性[2],加之酞菁呈现出蓝色或蓝绿色,在涂料、油漆、印刷品行业中经常作为燃料来使用[3],此外由于酞菁的共轭性质,使它具有良好的电子传递能力,可应用在液体催化剂[4]、光动力学治疗[5]、半导体材料[6]、非线性光学材料[7]等等,长期以来,人们对酞菁的研究从未间断。
肽菁颜料生产工艺

肽菁颜料生产工艺肽菁颜料是一种高性能有机颜料,广泛应用于塑料、涂料、印刷油墨等领域。
其生产工艺主要包括原料准备、反应合成、纯化和干燥四个步骤。
首先是原料准备。
肽菁颜料的主要原料是苯胺和酚类化合物。
其中,苯胺是通过苯的硝化、还原和氨解反应得到的。
而酚类化合物可以是多种选择,如二酚类、三酚类和多酚类等。
这些原料需要经过精确的称量和配比,以确保最终产品的质量。
接下来是反应合成。
原料经过混合后,加入催化剂进行缩合反应。
在高温和高压的条件下,苯胺和酚类化合物会发生亲核取代反应,形成肽菁分子结构。
反应时间一般在2-3小时内,使反应达到平衡。
反应后,得到的混合物需要进行冷却和过滤,去除杂质。
然后是纯化。
纯化的目的是去除合成过程中产生的副产物和杂质。
首先,通过结晶和过滤,将混合物分离得到肽菁颜料的晶体。
然后使用溶剂进行洗涤,去除不溶性杂质。
洗涤后,再次进行结晶,获得纯净的肽菁颜料。
这个过程需要进行多次,以确保产品的纯度。
最后是干燥。
纯化后的肽菁颜料需要经过干燥才能得到最终的产品。
通常使用真空干燥的方法,将湿润的颜料放入真空干燥器中,通过减压和加热使其脱水。
干燥的温度和时间需要根据具体情况进行调节,以避免产生不良的质量影响。
除了以上的主要步骤,肽菁颜料的生产过程中还需要进行质量控制和检测。
比如,在合成反应中需要定期采集样品进行反应进程的分析,确保反应达到预期的效果。
在纯化和干燥过程中,需要进行产品的质量分析,如氯离子含量、杂质含量等。
通过这些质量控制的手段,可以保证肽菁颜料的质量符合要求。
总的来说,肽菁颜料的生产工艺涉及原料准备、反应合成、纯化和干燥四个步骤。
每个步骤都需要精确控制和多次操作,以确保最终产品的质量。
同时,质量控制和检测也是不可或缺的环节,用于检验产品是否合格。
通过这些工艺和控制手段,可以生产出高质量的肽菁颜料。
金属酞菁的合成实验报告

金属酞菁的合成实验报告
实验目的:通过合成过程了解金属酞菁分子结构和性质,掌握实验中各种试剂的使用
方法和实验操作技能,以及掌握操作规范与安全常识。
实验原理:金属酞菁是由酞菁分子与金属离子配位形成的配合物,其中金属离子常见
的有Co、Cu、Fe等。
合成金属酞菁一般采用先制备酞菁钠,将其与金属盐在适当反应条件下反应即可得到金属酞菁。
实验步骤:
1. 酞菁钠的制备
取称量好的酞菁(0.2g)放入三颈瓶,加入甲苯(50ml)和氢氧化钠(1g),用磁力
搅拌器搅拌至溶解,然后在75℃下进行热反应2小时,反应完毕后离心,将上层透明的溶液过滤,过滤液收集并去掉甲苯,冷却后得到暗绿色的酞菁钠晶体,为下一步反应的原料。
(反应方程式为:H2C2N4M + NaOH → Na2H2C2N4 + H2O + M(OH)2)
结果分析:金属酞菁制备成功,样品为暗绿色结晶,红外光谱图中有明显的吸收峰,
符合金属酞菁的典型结构;元素分析结果为C:64.17%、H:2.79%、N:18.84%、Cu:
6.87%,符合理论值,说明金属酞菁合成得到。
结论:通过实验合成了金属酞菁,得到了暗绿色结晶的样品,且经元素分析、红外光
谱验证得到的样品符合金属酞菁的理论结构,合成过程成功。
溶剂热法制备金属酞菁晶体的研究进展

2008 年的铜酞菁晶体 [15-16] 。
2. 1 铜酞菁
铜酞菁是金属酞菁家族中被研究得最深入、衍生产品最多、首先实现工业化的金属酞菁。 铜酞菁晶体拥
有 α、β、γ、δ、ε、π、X、R 等众多晶型,其中能够作为颜料使用的常用晶型为 α 和 β 晶型,它们展示出牢固而稳
定的蓝色色泽 [2,17] 。 以铜酞菁为原料制备的十六氯铜酞菁即酞菁绿,拥有鲜艳的绿色 [18] 。 这些铜酞菁基
蓝、绿色颜料是有机颜料中地位最高、产量最大的重要品种。
2008 年,夏道成等 [15-16] 使用邻苯二甲腈和甲醇钠作为原料制备 1,3-二异吲哚啉,再将其与二水乙酸铜、
处于临界状态,不仅产生了压力变化,同时改变了溶剂的密度、黏度、分散作用等性质,使反应原料处于特殊
反应环境并使其处于传统实验方法不能创建的反应路径,因此实现了新材料、新结构的产生。 相比传统方
法,溶剂热法实验参数更易于控制。 溶剂热法制备晶体材料已发展了近三十年的时间,许多新材料均已实现
溶剂热制备。 然而,应用溶剂热法制备金属酞菁晶体材料的研究起步较晚,目前可经溶剂热法制备的金属酞
法一步制备金属酞菁晶体的研究进展,总结了能够通过该方法制备的金属酞菁晶体种类及其相应的反应条件和产物
结构,综合评价了该方法的技术优势,并对应用溶剂热法制备的金属酞菁晶体的未来发展进行了展望。
关键词:金属酞菁;晶体材料;平面大环配合物;晶体生长;溶剂热法;绿色化学
中图分类号:O641. 4
文献标志码:A
注:钪酞菁、钛酞菁、钒酞菁、锰酞菁、钴酞菁、砷酞菁、银酞菁、汞酞菁、铅酞菁、铀酞菁、磷酞菁可由锂酞菁置换制备。
酞菁系颜料生产工艺

酞菁系颜料生产工艺1.酞菁铜生产工艺将原料邻苯二甲酸酐、尿素、氯化亚铜加入缩合釜中,常压下在钼酸铵为催化剂的条件下(195℃,导热油加热)进行缩合反应,反应过程中产生的氨气经吸收塔(稀酸硫)吸收成硫酸铵回收;反应完成后在酸煮罐中进行加水酸煮(93%硫酸,95℃),然后进行压滤和水洗,压滤液(10~15%酸性水溶液)回收,水洗液进入循环水池;压滤滤饼经干燥、粉碎后成成品酞菁铜(详见工艺流程图)。
2.三氯化铝生产工艺将高纯铝锭投入密闭的熔融槽中加热熔化(煤加热),在熔融状态下通入氯气进行氯化,氯化后的三氯化铝蒸汽经一级和二级浦集器收集成成品三氯化铝;尾气经喷淋吸收后排放(详见工艺流程图)。
3.酞菁蓝生产工艺将酞菁铜粗产品加入酸溶釜中溶于浓硫酸(98%)在常压下进行酸溶,酸溶后放入稀释罐中加水进行析出,待晶体完全析出后,在酸煮罐中进行加热(95℃,蒸汽加热)酸煮,保持一定时间后进行压滤和水洗。
滤液(10%酸性水溶液)回收,洗水液进入循环水池;滤饼进入碱煮罐中加入固体氢氧化钠和少量水进行碱煮,然后进行压滤和水洗。
滤液(PH8~9碱性水溶液)回收,洗水液进入循环水池;滤饼经干燥后成成品酞菁蓝(详见工艺流程图)。
4.酞菁绿生产工艺以酞菁铜为母体,以三氯化铝和盐为溶剂在氯化亚铜为催化剂的条件下在熔料釜中进行熔料(导热油),熔好的料在氯代釜中通入定量的氯气生成带有14~15个氯的产品,并将其放入稀释罐中加入水和盐酸(氯代反应生成的HCl气体,经盐酸吸收塔吸收所产的30%盐酸)进行稀释,经压滤和水洗,压滤液(10%酸性水溶液)回收,水洗液进入循环水池;压滤滤饼则进入颜料化罐中以一氯苯为溶剂、碱性(PH 9~10)且压力为0.20~0.25MP下加入助剂进行颜料化。
颜料化后即通过苯分离器将一氯苯分离回收并循环使用,脱苯后的颜料化液经压滤、水洗,滤液(PH8~9碱性水溶液)回收,洗水液进入循环水池;滤饼经表面处理和干燥得到酞菁绿。
6 金属酞菁的合成、表征和性能测定

实验6 金属酞菁的合成、表征和性能测定(一) 金属酞菁的合成一、 实验目的1.通过合成酞菁金属配合物,掌握这类大环配合物的一般合成方法,了解金属模板反应在无机合成中的应用。
2.进一步熟练掌握合成中的常规操作方法和技能,了解酞菁纯化方法。
二、 实验原理自由酞菁(H 2Pc )的分子结构见图6.1(a)。
它是四氮大环配体的重要种类,具有高度共轭π体系。
它能与金属离子形成金属酞菁配合物(MPc),其分子结构式如图6.1(b)。
这类配合物具有半导体、光电导、光化学反应活性、荧光、光记忆等特性。
金属酞菁是近年来 NN N H N N N N N H图6.1(a) 自由酞菁分子结构图图6.1(b) 金属酞菁分子结构图广泛研究的经典金属大环配合物中的一类,其基本结构和天然金属卟啉相似,且具有良好的热稳定性和化学稳定性,因此金属酞菁在光电转换、催化活化小分子、信息储存、生物模拟及工业染料等方面有重要的应用。
金属酞菁的合成一般有以下两种方法:(1) 通过金属模板反应来合成,即通过简单配体单元与中心金属离子的配位作用,然后再结合形成金属大环配合物。
这里的金属离子起着一种模板作用。
(2)与配合物的经典合成方法相似,即先采用有机合成的方法制得并分离出自由的有机大环配体,然后再与金属离子配位,合成得到金属大环配合物。
其中模板反应是主要的合成方法。
金属酞菁配合物的合成主要有以下几种途径(以2价金属M 为例):(1) 中心金属的置换:MX + LiPc MPc + 2LiX 室温(2)以邻苯二甲腈为原料:MX + 4 MPc CN CN 300 C o n(3)以邻苯二甲酸酐、尿素为原料:MX ( M ) + 4 或+n COCO O CO(NH 2)2200~300 C o(NH 4)2MoO 4 MPc + H 2O + CO 2(4)以2—氰基苯甲酸胺为原料:M + 4 M CN CONH 2250 C o本实验按反应(3)制备金属酞菁,原料为金属盐、邻苯二甲酸酐和尿素,催化剂为钼酸铵。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
钼酸铵
4邻苯二甲酸酐+4尿素+M2+MPc+H2O+CO
2
2.1.2 金属酞菁的制备和纯化
金属酞菁(MPc)按如下模板反应制备:(M=Mn,Cu,Ni,Co)
()
对于不同的中心离子M2+,具体制备方法也不同。
(1)酞菁锰(MnPc)的制备和纯化
苯酐5.92g
尿素9.01g
锰1.69g
钼酸铵2.47*10-3 g
加入量:苯酐5.92 (0.04 mol),尿素9.01(0.15mol),钼酸铵2.47*10-3(2*10-6mol),锰1.69(0.01mol)。
一定量的苯酐和尿素置于250ml三颈烧瓶中,加入千分之二的钼酸铵作催化剂,再加入150ml二甲苯作溶剂。
加热至120℃使固体完全溶解,趁热加入硫酸锰。
升温至140℃下回流,20min后溶液变混浊,升温至150℃回流1h,溶液变清,底部有浅黄色沉淀。
倒出二甲苯,160o C下恒温3h蒸出溶剂。
粗产品用6M HCl 浸泡12h,在烧杯中静置后,倒掉上层清液体,反复用蒸馏水洗涤,静置,直至倒出液体为无色且中性。
再用丙酮浸泡,静置,洗至倒出的上层清液为无色。
再用1mol/L的NaOH溶液浸泡(时间?),静置,倒掉上层清夜,再用蒸馏水洗至倒出液为无色且为中性。
在100℃下干燥12h,即得MnPc。
(2)酞菁铜(CuPc)的制备和纯化
在250ml三颈烧瓶中将苯酐、尿素和氯化铜按4:4:1的摩尔比混合,再加入千分之二的钼酸铵作催化剂,加入150ml二甲苯作溶剂。
加热,在160℃下回流,20min后溶液变混浊,在此温度下继续回流0.5h,溶液变清,并呈浅蓝色,烧瓶底部有蓝色沉淀。
在200℃下继续回流4h,蒸出溶剂。
粗产品置于6N HCl 中,浸泡12h,过滤,用蒸馏水将蓝色沉淀洗至滤出液为无色,再用丙酮洗至滤出液为无色。
在120℃下干燥12h,即得CuPc。
(3)酞菁镍(NiPc)的制备和纯化
苯酐、尿素和硫酸镍配料的摩尔比为4:4:1,先将苯酐、尿素置于250ml
三颈烧瓶中,加入千分之二的钼酸铵作催化剂,再加入150ml二甲苯作溶剂。
加热,在120℃使固体完全溶解,趁热加入硫酸锰。
升温至150℃下回流,15min 后溶液变混浊,继续回流0.5h,溶液变清。
升温至180℃回流1h,溶液变无色,底部有黑色固体,然后升温至200℃下回流3h。
蒸出溶剂,粗产品用6N HCl 浸泡48h,过滤,用蒸馏水将黑色沉淀洗至滤出液为无色,再用丙酮洗至滤出液为无色。
在120℃下干燥12h,即得NiPc。
(4)酞菁钴(CoPc)的制备和纯化
在250ml三颈烧瓶中将苯酐、尿素和二氧化钴按4:4:1的摩尔比混合,再加入千分之二的钼酸铵作催化剂,加入150ml二甲苯作溶剂。
加热,温度升至140℃时,溶液微沸,并开始回流,10min后溶液变混浊,在此温度下继续回流0.5h,然后升温至160℃,20min后,溶液变清,并呈浅蓝色,烧瓶底部有深蓝色沉淀。
在此温度下回流0.5h,然后升温至200℃下回流2.5h,蒸出溶剂。
所得粗产品置于浓硫酸中,过滤。
滤液用蒸馏水稀释,析出深蓝色沉淀。
用蒸馏水将沉淀洗至滤出液为无色,在120℃下干燥8h,即得CoPc。
