原发灶不明癌的诊断
不明原发灶颈部转移癌的诊断和治疗

不明原发灶颈部转移癌的诊断和治疗张智显【摘要】不明原发灶颈部转移癌原发灶的检出与否直接影响患者的生存率和生活质量.目前颈部转移癌原发灶的检测以传统检查方法为主,近年来全内镜检查随机活检、氟脱氧葡萄糖正电子发射断层摄影术、激光介导荧光内镜和基因检测等技术提高了原发灶的检口率.根据淋巴结转移部位、病理类型、N分期等对不明原发灶颈部转移癌制订合理的治疗方案.现重点对不明原发灶颈部转移癌的传统和新近发展的诊治方法进行综述,以期对临床工作有所帮助.【期刊名称】《医学综述》【年(卷),期】2010(016)010【总页数】3页(P1491-1493)【关键词】颈部转移癌;不明原发灶;诊断;治疗【作者】张智显【作者单位】昆明医学院第二附属医院肿瘤科,昆明650101【正文语种】中文【中图分类】R937.91;R73-37大部分颈部转移癌可通过临床检查及各种辅助检查找到原发灶,但是 2%~9%的患者经过全面仔细检查后仍然无法发现原发灶[1],此类患者查寻原发灶的过程是费时、费力的,中位生存期却大约只有 8个月[2]。
对于此类疾病的诊断和治疗尚无大型随机、对照、前瞻性研究,因此存在很多争论。
转移癌虽容易明确诊断,但寻找原发灶则有困难。
原发灶隐匿的原因可能与以下因素有关:[3]①机体免疫机制控制了原发灶,原发灶自行消退;②原发灶太小,不能被目前的检查方法所发现;③原发灶位置隐匿,暂时不易被发现;④原发灶恰位于放射野内,在转移灶放疗的同时被控制;⑤原发灶在颈部软组织内,颈清术时被一并切除或虽未被切除;⑥转移癌的生物学特性与原发灶不同,使原发灶尚未发现,患者就死于转移癌。
不明原发灶颈部转移癌(unknown primary cervicalmetastaticcarcinoma,UPCMC)的定义包括:①一个或多个颈部肿块经组织学或细胞学检查诊断为癌;②没有恶性肿瘤病史或不明病灶手术史;③没有明确的某器官系统相关症状;④没有原发肿瘤的临床和实验报告证据。
原发灶不明转移癌的临床诊断

原发灶不明转移癌的临床诊断陈金影;蔡虎;徐清华【摘要】原发灶不明转移癌是一类经病理学诊断确诊为转移性,但是无法明确原发位点的恶性肿瘤.在全球范围内,原发灶不明转移癌是最常见的十大恶性肿瘤之一,死亡率位列第4.原发灶不明转移癌的治疗以经验性化疗为主,患者预后普遍较差.明确肿瘤的原发部位,有助于临床医生制定针对性的治疗方案,缓解患者焦虑情绪,从而提高生存率和改善生存质量.目前临床用于原发灶不明转移癌的方法主要有临床评估、影像学检查和组织病理学检查.近年来,随着分子生物学和生物信息学技术的飞速发展,基因分子检测显示出巨大的潜力,并已逐渐应用于原发灶不明转移癌的临床诊断.本文就原发灶不明转移癌的临床诊断方法相关进展作一综述.【期刊名称】《分子诊断与治疗杂志》【年(卷),期】2017(009)001【总页数】6页(P67-72)【关键词】原发灶不明转移癌;分子诊断;基因检测【作者】陈金影;蔡虎;徐清华【作者单位】杭州可帮基因科技有限公司,浙江,杭州311188;杭州可帮基因科技有限公司,浙江,杭州311188;杭州可帮基因科技有限公司,浙江,杭州311188【正文语种】中文原发灶不明转移癌(carcinomas of unknown primary,CUP)是指一类经病理学检查证实为转移性,但是经过详细检查和评估仍不能确定原发位点的恶性肿瘤。
大约有15%的癌症是由于转移灶的症状而被发现。
通过临床、影像和病理诊断可以明确大部分的原发位点,但仍有1/3的转移癌原发位点不明,即真正意义上的CUP[1]。
世界范围内,CUP大约占所有新发癌症的3%~5%,位列最常见的十大癌症之一,死亡率排名第4位。
CUP中位诊断年龄约为60岁,男性发病率略高于女性[2⁃4]。
瑞典的一项研究发现2.8%的CUP患者存在家族遗传性[5]。
CUP具有病史短,非特异性全身症状;80%的患者有腺上皮分化;约30%的患者出现3~4个器官累及;预后差等临床特征[6⁃7]。
原发灶不明肿瘤的诊断技术现状及进展

doi:10.3971/j.issn.1000-8578.2023.23.0770原发灶不明肿瘤的诊断技术现状及进展戚鹏1,2,孙益丰3,4,徐清华4,5,周晓燕1,2Current Status and Progress of Diagnostic Techniques for Cancer of Unknown Primary QI Peng 1,2, SUN Yifeng 3,4, XU Qinghua 4,5, ZHOU Xiaoyan 1,21. Department of Pathology, Fudan University Shanghai Cancer Center, Shanghai 200032, China;2. Department of Oncology, Shanghai Medical College, Fudan University, Shanghai 200032, China;3. Shanghai Key Laboratory of Medical Epigenetics, Institutes of Biomedical Sciences, Fudan University, Shanghai 200032, China;4. Canhelp Genomics Co., Ltd., Hangzhou 311100, China;5. Xuzhou Engineering Research Center of Medical Genetics and Transformation, Department of Genetics, Xuzhou Medical University, Xuzhou 221004, China CorrespondingAuthor:ZHOUXiaoyan,E-mail:135****************戚鹏 医学博士,副研究员,中华医学会病理学分会技术学组委员,中国研究型医院学会超微与分子病理专业委员会技术组委员,中国抗癌协会肿瘤病理专业委员会技术学组成员。
肺癌诊断指南2023诊断标准

肺癌诊断指南2023一、概述肺癌是全球范围内导致逝去的主要癌症之一。
根据全球癌症统计数据,肺癌在各国均为高发病种,且病死率居首位。
随着医学技术的不断发展和临床研究的深入,肺癌的诊断标准也在不断更新和完善。
本文旨在介绍2023年肺癌诊断指南的最新诊断标准,供临床医生及患者参考。
二、原发性肿瘤的诊断标准1. 影像学检查(1)胸部CT扫描:对于怀疑肺癌的患者,首要进行的检查是胸部CT 扫描。
CT检查有助于发现肺内肿块、结节、磨玻璃样阴影等病变,对肺癌的诊断十分重要。
(2)PET-CT检查:PET-CT检查具有较高的敏感性和特异性,可用于评估肿瘤的代谢活性和测量肿瘤的大小,对于肺癌的初步诊断和分期具有重要价值。
2. 组织学检查(1)支气管镜检查及活检:对于经CT或PET-CT筛查发现可疑病变的患者,应进行支气管镜检查,并取活检标本进行病理学分析,以明确肺癌的组织学类型和分级。
(2)内窥镜检查:对于胸腔积液或痰液细胞学阳性的患者,可进行内窥镜检查,以便获取组织学标本进行病理学诊断。
3. 分子生物学检查(1)EGFR、ALK、ROS-1等分子标志物检测:对于非小细胞肺癌患者,应进行EGFR、ALK、ROS-1等分子标志物的检测,以确定治疗的靶向药物选择。
(2)PD-L1蛋白表达水平检测:对于晚期非小细胞肺癌患者,PD-L1蛋白表达水平的检测有助于选择免疫检查点抑制剂治疗。
三、淋巴结转移的诊断标准1. 影像学检查(1)胸部CT扫描:对于初诊患者,CT扫描可发现肺门、纵隔、锁骨上等淋巴结的转移情况。
(2)PET-CT检查:PET-CT检查对于淋巴结转移的定位和评估有重要意义,可以指导术前辅助治疗的选择和手术方案的制定。
2. 组织学检查淋巴结活检:对于CT或PET-CT检查显示淋巴结转移的患者,应进行淋巴结活检,以明确转移的类型和范围。
3. 分子生物学检查淋巴结转移处PD-L1蛋白表达水平检测:对于晚期非小细胞肺癌患者,淋巴结转移处的PD-L1蛋白表达水平的检测有助于选择免疫检查点抑制剂治疗。
细胞学检查在不明原发灶恶性腹水诊断的意义

细胞学检查在不明原发灶恶性腹水诊断的意义
细胞学检查是一种常见的检查方法,通常用于检查体液或组织中的异常细胞。
当患者
出现不明原因的恶性腹水时,细胞学检查可以帮助医生尽早诊断该病症,确定治疗方案并
监测疗效,具有极其重要的意义。
恶性腹水是指腹膜外异常细胞转移所引起的腹水,常见于消化系统恶性肿瘤、乳腺癌、淋巴瘤等恶性肿瘤。
恶性腹水临床表现为腹胀、腹泻、腰痛等,严重影响患者的生活质量。
了解腹水的成因和性质对临床方案制定及治疗起到至关重要的作用。
对于疑似恶性腹水的患者,细胞学检查可以判断腹水细胞类型、发现肿瘤细胞的存在
及其数量,并确定肿瘤细胞的密度、形态、异型等特征。
这种方法具有非侵入性、、简单
快捷、可重复性好且有较高的准确性,被广泛地应用于患者的诊断及治疗。
细胞学检查的方案通常是利用特定的技术,直接在腹水样本中观察和鉴定肿瘤细胞的
存在和数量。
细胞学检查的i优点在于检测精度高、快速、和操作简便。
通过细胞学检查,可以及早发现恶性腹水并尽早做出诊断,优化治疗方案,提高治疗效果。
此外,细胞学检查还常被用于监控疗效。
根据患者的体液中的细胞形态、数量和异型
性的变化,医生可以随时调整治疗方案。
这有益于及时判断治疗的效果,并及时采取必要
的措施调整治疗方案,提高治疗的效果,减轻患者的痛苦。
总之,细胞学检查在不明原发灶恶性腹水诊断中具有非常重要的意义。
通过及时检测,可以尽早诊断疾病、制定科学合理的治疗方案、监测疗效,最大程度地提高治疗效果,向
患者提供更好的生活保障。
原发不明恶性肿瘤的诊治

MUO
IHC:(结合LM,临床) ❖ IPS(Immunopeoxidase Staining)应用最广
可用于福尔马林固定过的蜡块 针对
➢ 细胞成分/产物(酶类:PSA, NSE)
➢ 正常组织成分(Keratin, Desmin, Vimentin, Neurofilaments, CLA)
原发不明恶性肿瘤的诊治
MUO
原发不明恶性肿瘤 (Metastatic tumor of Unknown Origin,
MUO)
❖ 于转移部位出现症状或体征,
在转移部位经活检作出诊断,
经病史、体检及其他相应评价未能确证原发部位
❖ 发生率:5%-10%
· 美国 SEER(1973-1987) 2% · 国际:(其他7国) 2.3%-7.8%
细胞学
➢ 提供确诊:诊断5%-15%(尤胸、腹水) ➢ 确定类型常有困难
➢ 难以确诊应开放活检
❖ 重作开放活检
要求:争取配合,部位适当,量足质好
多部位中选取最少病残部位
➢ 外周淋巴结 ➢ 骨髓 ➢ 细胞渗液 ➢ 可疑皮肤病变
MUO
LM:确定恶性肿瘤,并分为四类
❖ 差分化肿瘤 (Poorly Differentiated Neoplasms, PDN)
进一步IPS、EM,仍难定按PDC
MUO:差分化癌/ 腺癌
临床评价:
* 胸、腹CT
* 血清:HCG、AFP
特殊病理
* IPS
* EM
亚型及治疗
* PET scan * 其他:按症状/体征
* MG
亚型
治疗
预后
1. 不典型生殖细胞肿瘤(由染色 按生殖细胞肿瘤治疗 CR: 40%-50% 体12证实)
ESMO 指南:原发灶不明肿瘤的诊疗

ESMO 指南:原发灶不明肿瘤的诊疗原发灶不明癌症(cancers of unknown primary site,CUPs)是一类转移性肿瘤的统称,该类肿瘤无法通过常规诊断方法确定原发性癌灶的位置。
原发性不明癌症约占所有恶性肿瘤的 3%~5%。
目前尚未发现该类型肿瘤所共有的生物学特征。
不过,最新证据已经表明:即使在原发性肿瘤静息的情况下,肿瘤细胞本身的转移性特质、循环肿瘤细胞的位置特异性转化、转移部位的致癌性诱导等多种因素均可能促使肿瘤的转移性扩散。
诊断原发灶不明癌症的诊断需要借助病理学评估。
根据病理学特征,可以讲原发灶不明癌症分类为:(1)高度和中度分化腺癌、(2)低度分化癌(包括低度分化腺癌)、(3)鳞状细胞癌、(4)未分化肿瘤、(5)神经内分泌分化性癌。
免疫组织化学主要用于确定原发灶不明癌症的起源组织、排除化疗敏感性和可治愈性肿瘤(例如淋巴瘤和生殖细胞肿瘤)肿瘤标记物检查:某些生殖细胞肿瘤会分泌特殊的胎儿蛋白(α-fetoprotein, AFP)、人类绒毛膜性腺激素(β-human chorionic gonadotropin, β-HCG),可做为诊断及治疗的参考依据,同时也是完成治疗后追踪的重要检查之一。
(图 1)。
如果检查结果确诊是癌或腺癌,建议男性患者进行前列腺特异性抗原(PSA)免疫学染色或伴有腋窝淋巴结转移女性患者进行雌激素和孕激素受体免疫学染色,以排除激素敏感性肿瘤并进行特殊治疗。
角蛋白(keratins)CK7 和 CK20 染色可能会提供原发性癌灶的位置信息,嗜铬粒蛋白 A CgA (chromogranin A)和突触小泡蛋白(synaptophysin)染色主要用于判断神经内分泌分化(表 1)。
CK7,卵巢、肺和乳腺癌阳性,胃结肠、前列腺阴性。
CK20,用于胃肠道腺癌、卵巢黏液性癌阳性。
鳞癌、乳腺癌、肺癌、子宫内膜癌和卵巢非黏液性肿瘤常阴性。
KI-67,(细胞增殖标志指数)数值越高,肿瘤增殖越快,恶性程度越高。
原发灶不明的转移灶诊断详述

原发灶不明的转移灶诊断详述
*导读:原发灶不明的转移灶症状的临床表现和初步诊断?
如何缓解和预防?
原发灶不明性转移性癌肿病人占所有癌症病人的0.5%~0.7%,由于癌症治疗常随其组织型别而异,因而必须全面评估。
详细询问病史和体检,要特别注意乳腺和盆腔,前列腺,直肠和消化道疾病的症状和体征。
实验室检查包括全血细胞计数,尿液分析,大便隐血试验,血清化学检查(男性包括酸性磷酸酶,特异性抗原试验)。
X线检查仅限于胸部X线检查,乳房摄片和腹部CT。
上消化道系列检查和钡剂灌肠不作为常规。
取得的癌肿组织宜进行免疫球蛋白的免疫过氧化物酶染色,基因重排检查以及电镜检查,这些有助于大细胞淋巴瘤的诊断。
甲胎蛋白或β-人绒毛膜促性腺激素的过氧化物酶染色检查有助于胚细胞癌的诊断。
雌激素和孕酮受体的组织检查有助于识别乳腺癌。
前列腺特异性抗原免疫过氧化物酶染色检查有助于诊断前列腺癌。
即使不能作出精确的组织学诊断,病灶邻近或在中线区域(如纵隔,腹膜后)的低分化的癌症病人,应当接受两个疗程以顺铂为基础的化疗。
若有效应给予3~4个疗程。
将近50%患者因而获得长期无病生存期。
对其他患者,有些医生试用阿霉素或紫杉醇
为基础的方案,然而疗效中等且短暂。
然而由于多数患者潜伏隐性原发癌肿,以后的治疗运用对多数类型肿瘤较有效的化疗方案也许是有益的。
*结语:以上就是对于原发灶不明的转移灶的诊断,原发灶不明的转移灶怎么处理的相关内容介绍,更多有关原发灶不明的转移灶方面的知识,请继续关注或者站内搜索了解更多。
肺癌的CT诊断

肺癌的CT诊断肺癌的CT诊断解放军总医院放射诊断科蔡祖龙肺癌是最多见的恶性肿瘤之一。
工业化国家死于肺癌者,女性占全数恶性恶肿的1/5,男性那么高达1/3。
最近几年来,我国肺癌的发病率呈明显上升的趋势。
在北京、上海、天津、江苏和辽宁省的城市,云南固旧地域,肺病的发病率和\或死亡率已占各类恶性肿瘤的首位。
因肺癌确认时多已至中晚期,70-80%患者已失去根治机遇,五年生存率较低,因此肺癌的初期诊断和医治关于改善肺癌予后,提高五年生存率是十分重要的。
影像学检查方式关于肺癌的检出及分期有十分重要的价值。
一、肺癌的CT表现(一)中央型肺癌CT能显示中央型肺癌的一系列病理改变,要紧有段以上支气管腔内肿块,支气管壁增厚:支气管腔狭小与阻塞,肺门区肿块等肺癌直接征象。
继发性改变有阻塞性肺炎与肺不张,阻塞远端支气管扩张形成的粘液栓塞,和病灶周围或(和)肺门的淋巴结肿大等;螺旋CT,专门是多层面CT,采纳薄层扫描并冠状与矢状位重建可清楚显示支气管腔内沿管壁浸润的初期肺癌。
CT平扫难以区分肿瘤与其远侧的肺不张,增强扫描可清楚显示肿瘤的实际大小与不张的肺。
(二)周围型肺癌:周围型肺癌在CT上显示有必然特点,即便小于的初期肺癌,也多有明确的恶性征象。
以下重点简述直径〈3cm的周围型小癌的CT征象特点及其病理基础。
⒈肿瘤边缘征象特点:⑴分叶征:是周围型小肺癌最多见的大体征象。
作者100 例直径小于3cm的小肺癌分叶征的发生率为84%。
绝大多数小肺癌呈深分叶,(弦距与距长之比大于2/5。
其病理基础一是与肿瘤边缘各部位肿瘤细胞分化程度不一,生长速度不同有关;二是肺的结缔组织距离,进入肿瘤的血管、支气管分支、从肿瘤内向外生长的血管和结缔组织等引发肿瘤生长受限并产生凹陷,从而形成份叶的形态。
⑵边缘毛糙:可见细短毛刺,棘状突起或锯齿状改变。
此为肺癌的常见征象,发生率约为80%-85%,这些表现是由于肿瘤间质,血管向瘤外生长和肿瘤细胞周围蔓延所致。
伴PDGFRB基因突变原发灶不明转移癌1例并文献复习

伴PDGFRB基因突变原发灶不明转移癌1例并文献复习颜金花;温燕华;吕小斌;唐小凤;李萍;邬国和【期刊名称】《江西医药》【年(卷),期】2018(053)004【总页数】4页(P356-358,363)【关键词】原发灶不明转移癌;全基因组测序;PDGFRB基因;酪氨酸激酶抑制剂【作者】颜金花;温燕华;吕小斌;唐小凤;李萍;邬国和【作者单位】南昌大学第三附属医院血液科,南昌 330008;南昌大学第三附属医院血液科,南昌 330008;南昌大学第三附属医院血液科,南昌 330008;南昌大学第三附属医院血液科,南昌 330008;南昌大学第三附属医院血液科,南昌 330008;南昌大学第三附属医院血液科,南昌 330008【正文语种】中文【中图分类】R738.1原发灶不明转移癌(carcinoma of unknown primary,CUP)是一类经活检病理学检查,组织学上确诊为转移癌,但经过详细检查和评估仍找不到原发解剖部位的转移性恶性肿瘤。
由于病灶较小,部位隐匿或位于黏膜下等原因而不易发现,临床上大约有15%的癌症是由于转移病灶的症状而被发现,通过临床、影像和病理诊断可以明确一部分转移癌的原发病灶,但仍有1/3的转移癌原发病灶无法明确,被称为真正意义上的CUP[1]。
据国内外研究报道,CUP约占人类所有新发癌症的3%~5%,是人类第7~8位常见的恶性肿瘤,也是第4位常见的致死性癌症[2,3]。
与原发灶明确的肿瘤不同,CUP的自然病程具有早期转移、转移方式不可预知、侵袭性较强的特点[4]。
目前临床上CUP的治疗仍然以经验性化疗联合对症支持治疗为主,患者预后普遍较差,中位生存期仅9个月[5]。
因此,如果能够明确肿瘤的原发部位或者基因学特性,将有助于临床医生制定针对性的治疗方案,从而提高此类患者的生存期及改善其生存质量。
现将我院新近发现的1例CUP患者报告如下,并对相关文献进行复习,以提高对CUP诊断及治疗的认识。
未知来源骨转移癌病人的诊断流程
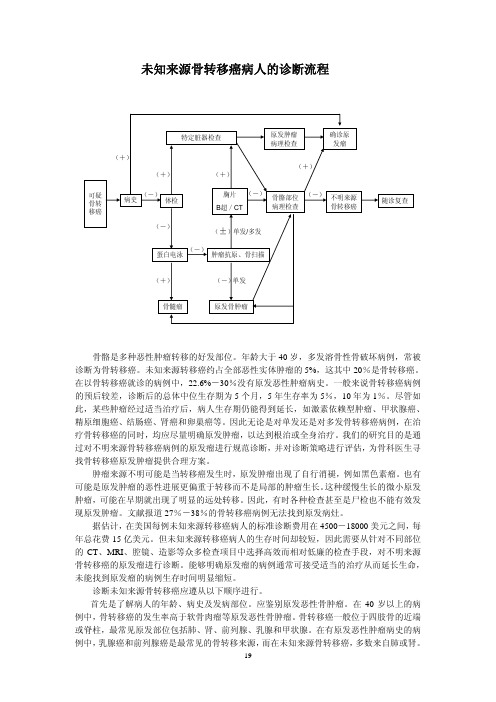
未知来源骨转移癌病人的诊断流程骨骼是多种恶性肿瘤转移的好发部位。
年龄大于40岁,多发溶骨性骨破坏病例,常被诊断为骨转移癌。
未知来源转移癌约占全部恶性实体肿瘤的5%,这其中20%是骨转移癌。
在以骨转移癌就诊的病例中,22.6%-30%没有原发恶性肿瘤病史。
一般来说骨转移癌病例的预后较差,诊断后的总体中位生存期为5个月,5年生存率为5%,10年为1%。
尽管如此,某些肿瘤经过适当治疗后,病人生存期仍能得到延长,如激素依赖型肿瘤、甲状腺癌、精原细胞癌、结肠癌、肾癌和卵巢癌等。
因此无论是对单发还是对多发骨转移癌病例,在治疗骨转移癌的同时,均应尽量明确原发肿瘤,以达到根治或全身治疗。
我们的研究目的是通过对不明来源骨转移癌病例的原发瘤进行规范诊断,并对诊断策略进行评估,为骨科医生寻找骨转移癌原发肿瘤提供合理方案。
肿瘤来源不明可能是当转移癌发生时,原发肿瘤出现了自行消褪,例如黑色素瘤。
也有可能是原发肿瘤的恶性进展更偏重于转移而不是局部的肿瘤生长。
这种缓慢生长的微小原发肿瘤,可能在早期就出现了明显的远处转移。
因此,有时各种检查甚至是尸检也不能有效发现原发肿瘤。
文献报道27%-38%的骨转移癌病例无法找到原发病灶。
据估计,在美国每例未知来源转移癌病人的标准诊断费用在4500-18000美元之间,每年总花费15亿美元。
但未知来源转移癌病人的生存时间却较短,因此需要从针对不同部位的CT、MRI、腔镜、造影等众多检查项目中选择高效而相对低廉的检查手段,对不明来源骨转移癌的原发瘤进行诊断。
能够明确原发瘤的病例通常可接受适当的治疗从而延长生命,未能找到原发瘤的病例生存时间明显缩短。
诊断未知来源骨转移癌应遵从以下顺序进行。
首先是了解病人的年龄、病史及发病部位。
应鉴别原发恶性骨肿瘤。
在40岁以上的病例中,骨转移癌的发生率高于软骨肉瘤等原发恶性骨肿瘤。
骨转移癌一般位于四肢骨的近端或脊柱,最常见原发部位包括肺、肾、前列腺、乳腺和甲状腺。
颈部转移癌

放射治疗
应根据不同的病理类型及分化程度, 颈淋巴结转移部位,疾病分期,肿瘤对 放射的反应,以及病人的自身条件等, 个别对待,选用不同的放射技术。
(一)照射野
全颈部加全咽部野 适用于上、中颈部鳞癌、 低分化癌或未分化癌。 单纯颈部照射 适用于腺癌,或仅有颊下、颌 下或下颈淋巴结转移;年龄大,情况差,不能 耐受全咽部大面积照射,排除鼻咽癌和口咽病 变可能的患者。 局部放疗 适用于锁骨上区转移灶,或伴有身 体其他部位转移者。
2)掌握淋巴结转移规律
颈部转移癌大约75%来源于头颈部原发肿瘤, 尤其是上、中颈部淋巴结转移更多见于颌面部 原发性肿瘤。 典型的淋巴结转移是向同侧颈部引流,但是软 腭、扁桃体、舌根、咽后壁,尤其是鼻咽病变 常向双侧颈部引流。 声带、鼻窦和中耳淋巴引流很少或无淋巴管网。 上颈深后组淋巴结主要引流口咽、鼻咽病变, 而口腔、喉或下咽病变很少有此处转移。
颈部解剖
第I区(level I)包括颏下区及颌下区淋巴结。 第 II 区(level II)为颈内静脉淋巴结上组, 即二腹肌下,相当于颅底至舌骨水平,前界 为胸骨舌骨肌侧缘,后界为胸锁乳突肌后缘, 为该肌所覆盖。
第III区(level III)为颈内静脉淋巴结中组,从 舌骨水平至肩胛舌骨肌与颈内静脉交叉处,前 后界与II区同。 第IV区(level IV)为颈内静脉淋巴结下组,从 肩胛舌骨肌到锁骨上。前后界与II区同。 第V区(level V)为枕后三角区或称副神经链 淋巴结,包括锁骨上淋巴结,后界为斜方肌, 前界为胸锁乳突肌后缘,下界为锁骨。
口腔癌可转移到颌下或须下淋巴结。 鼻咽、下咽和喉病变极少有I 区淋巴结转移。 颈后三角Va 区主要引流鼻咽、口咽和后头皮 的皮肤病变,Vb 区更多引流甲状腺病变。 咽后淋巴结转移最常见是鼻咽癌,其次是咽壁 和软腭肿瘤。 其他班区淋巴结转移多见于声门下喉、梨状窝、 甲状腺、上段食管和气管病变。 需要注意的是大约有2%~10%左右的颈部 淋巴结为跳跃性转移。
原发灶不明癌24例临床分析

CUP 的发病率约占实体瘤的 2. 3% 一 2% , 4. 男女发病比
2. 1 总体生存情况 2 位患者中位生存期 3. 2 个月( 1. 8 4 5 1 . 1 个月) 。生存曲线见图 1。
, n 月 U
:
例相当, 男性稍高, 发病平均年龄约6 岁[ 。本组男性发病 0 : ] 者稍高于女性, 8 . 2 岁。 平均5
疗 + 全身热疗的患者 n 例, 中位生存时间为5. 6 个月,g Lo
P <0. 001) 。进一步比较发现, 采用铂类 + 紫杉类化疗 + 全身 热疗 的患者生存期长于用铂类 + 紫杉类化疗 的患者 ( 尸二
受累器官:受累器官数目< 3 个有 1 例, 0 受累器官数 目 杂3 个有 1 例。转移部位最多见的是:淋巴结 1 例, 9 例, 4 肺 骨 1 例, 7 例, 2 例J 单一转移最多见的部位是: 骨 3 0 肝 脑 例, 例, 脑2 淋巴结 1 例, 皮肤软组织 1 例。 病理来源( 诊断部位) :浅表淋巴结或皮肤软组织穿刺活 检或切除活检 8 例, 实质器官手术活检 5 例, 骨穿刺或手术活 检 6 例, 胸腹水中找到恶性肿瘤细胞 5 例。 治疗方案:仅用支持治疗者 8 例, 采用铂类加紫杉类化疗 者5 例, 包括紫杉醇 + DDP I 例, 紫杉醇 + 卡铂 2 例, 多西他 赛 +DDP I 例, 多西他赛+ 卡铂 1 例;采用铂类+ 紫杉类化疗 + 全身热疗 1 例, 中萦杉醇 + DDP 3 例, 其 紫杉醇 + 卡铂 3 例, 多西他赛+ DDP Z 例, 多西他赛 + 卡铂 3 例;全身热疗采 用 VHR 一 0 型高能聚束微波热疗, Z 200 治疗温度达到 40℃ 42℃之间, Z b。 持续 1. 3 随访情况 全组患者均随访至 20 7 年 6 月, 0 均采用电 话随访, 无失访患者, 其中4 例患者至随访结束仍存活。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
些特征并不非常敏感和特异,分析时候应结合
其他发现。相应的病理线索见下 o 印戒细胞癌:胃肠道、乳腺、卵巢 o 乳头样结构:甲状腺、卵巢、间皮瘤 o 非腺样细胞巢:类癌、黑色素瘤、神经节旁
瘤
Initial Light Microscopic Diagnosis
腺癌(高中分化) adenocarcinoma
分化不良的原发灶不明癌
EPIDEMIOLOGY
占UPC 30%。分化不良癌占20%,
分化不良腺癌10%
仅靠光镜不能区分敏感与不敏感肿瘤 IP、EM、GA有助于评价分化不良癌
EPIDEMIOLOGY
这些肿瘤虽然与分化较好腺癌在组织学上有类似 地方,但的确存在实质性差异:
同高分化腺癌相比中位年龄较轻 侵犯部位常见于淋巴结、腹膜、纵隔、腹膜后, 而非内脏器官和骨 症状进展迅速 对化疗非常敏感,对以铂类为基础的化疗可以 完全缓解
乏力等
包含的疾病种类繁多。
EPIDEMIOLOGY
临床较常见பைடு நூலகம்
占癌症诊断的5%
关注不够,研究滞后
对治疗和预后过分悲观,研究设计困难
目前,多种高度可治肿瘤已能识别, 非特异性方案有效率已大有提高
CLINICAL FEATURE AND GENERAL CONSIDERATION
最常见的转移位置为肺、肝脏、骨骼系统。
目前最常用的肿瘤分类辅助手段 适于多种标本 可原位标记多种细胞成分或蛋白产物 如:酶、中间丝或其他细胞正常成分、激素、
癌胚抗原,
以及其他肿瘤标志。
独立不能作出诊断,必须结合光镜
IMMUNOPEROXIDASE STAINING
工作要点
结合病史,减少检测抗体的数量 结果解释要慎重 首要任务在于识别高度可治肿瘤
IMMUNOPEROXIDASE STAINING
四大任务
1. 区分lymphoma和 carcinoma
LCA、 keratin 2. 识别neuroendocrine carcinoma NSE、 chromogranin, synaptophysin
IMMUNOPEROXIDASE STAINING
淋巴结37.1%
骨骼28.%
肝脏30.7%
肺27.7%
胸膜及胸膜腔11.6%
脑7.6%
诊断主要依靠转移部位的活检。标本应够量
DIAGNOSTIC EVALUATION
基本目的
识别能治愈或治疗有效的病例
明确病变属局限或广泛期
识别急需局部手段解除的病变
DIAGNOSTIC EVALUATION
POORLY DIFFERENTIATED NEOPLASMS
non-Hodgkin lymphoma:
34~60%
Neuroendocrine carcinoma:10~15%
melanoma + sarcoma: ≤ 15%
POORLY DIFFERENTIATED NEOPLASMS
CHROMOSOMAL ANALYSIS
对肿瘤预后估计日益重要,诊断价值有限
研究最多的属血液和淋巴肿瘤
多数B-cell 、T-cell non-Hodgkin lymphomas
可检测到肿瘤特异性免疫球蛋白基因、TCR基
因重排,有诊断意义
CHROMOSOMAL ANALYSIS
例证
DIAGNOSTIC EVALUATION
能明确原发灶的病人仅13-25%
明确原发灶的病人中,肺癌和胰腺癌为主
即便是尸检,也只有70%明确的原发灶
DIAGNOSTIC EVALUATION
有例外,明确诊断为第一步。例如:颈部可切除 的孤立肿块,不伴有其他明显病变(非锁骨上肿 块)。这些病人原发灶一般位于头颈部,应详尽 检查,采用各种内窥镜、鼻窦摄片、对可疑部位 盲目活检,PET可能有帮助。如果仍不能明确诊 断,可以肿块切除活检。注意应当遵循该顺序, 如果病灶发现则可按照相应疾病的规范处理
DIAGNOSTIC EVALUATION
推荐措施
详细病史和体格检查 常规实验室检查、胸片和腹部CT 特殊检查需要有明确依据 不过度检查和无指征侵袭性检查
GENERAL CONSIDERATION
初步检查提纲
年轻男性病人分化不良癌应当做AFP\HCG
女性腋窝淋巴结肿大应该乳腺摄片 男性成骨性骨转移应检查PSA 颈部淋巴结转移性鳞癌在头颈部寻找原发灶 腹股沟淋巴结鳞状细胞癌原发灶经常位于会阴区域。 女性应仔细检查阴户、阴道和宫颈。男性应仔细检查 阴茎和阴囊。肛镜排除肛门和直肠区域病变。
化不良肿瘤的明确诊断
一个重要的明确病理类型的保留手段。
ELECTRON MICROSCOPY
应用
可靠区分淋巴瘤与其他分化不良肿瘤
识别neuroendocrine tumors ( neurosecretory granules)、melanoma (premelanosomes) 识别腺癌intracellular lumina 、 surface microvilli ;鳞癌desmosomes 、prekeratin
常用方法
可用FISH、PCR、comparative
genomic hybridization technique
可用存档蜡块、新鲜组织等
POORLY DIFFERENTIATED NEOPLASMS
分化不良肿瘤
POORLY DIFFERENTIATED NEOPLASMS
分化不良肿瘤
病理确定为恶性肿瘤,但不能区分为癌或其它 肿瘤如:淋巴瘤、黑色素瘤,或肉瘤 占所有UPC的 5%,是极有必要进一步明确诊 断的一类肿瘤
诊断治疗原则
首先应当活检标本够量,而非针吸活检
彻底的病理学评价。大部分光镜下的分化
不良肿瘤在特殊的病理学染色后,将会 有明确的类别发现。 分化不良肿瘤如果不能归属特殊细胞类型。 治疗原则类似于原发灶不明的腺癌。
POORLY DIFFERENTIATED CARCINOMA OF UNKNOWN PRIMARY SITE
四大任务
3. 识别 prostate carcinoma 男性转移腺癌,PSA + 4. 识别 amelanotic melanoma 、 sarcoma、S-100、 Hmb-45 antigen、vimentin,desmin、vimentin、 factor VIII
IMMUNOPEROXIDASE STAINING
filaments
ELECTRON MICROSCOPY
缺陷
取材后需马上特殊固定
相对昂贵 设备不普及
缺乏特殊超微结构细胞,电镜无助于诊断
超微结构为依据的诊断,治疗及预后意义不清
ADDITIONAL PATHOLOGIC STUDIES
染色体分析
CHROMOSOMAL ANALYSIS
POORLY DIFFERENTIATED CARCINOMA OF UNKNOWN PRIMARY SITE
genetic analysis enables definitive diagnosis by
原发灶不明癌的诊断与处理
Cancer of unknown primary site
孙太振
原发灶不明癌指:
因转移灶症状而发现,常规病史、体格检 查、胸部放射线及实验室检查不能明确原 发灶的一类恶性肿瘤。
EPIDEMIOLOGY
临床表现多样,症状和体征因转移部
位而异
一般性症状常见。厌食、体重减轻、
TREATMENT
尽管某些临床特征与中位生存超过40个月相 关:年轻、不抽烟、神经内分泌特征、单一转
移部位(少于3处)、肿瘤位于纵隔、腹膜后、
外周淋巴结 缺乏上述临床特征的病人,化疗选择应个体 化。基于病人的PS状况和对经验性、试验性 毒性治疗的迫切程度。
POORLY DIFFERENTIATED CARCINOMA OF UNKNOWN PRIMARY SITE
鳞状细胞癌 squamous cell carcinoma
分化不良癌 poorly differentiated arcinoma 分化不良肿瘤 poorly differentiated neoplasm 应视为进一步明确诊断的最主要线索
SPECIALIZED PATHOLOGIC STUDIES
TREATMENT
治疗的基本观点
对全身治疗有效的病例或病变限于淋 巴结,应积极治疗,以治愈和显著延长 生存时间为目的。该类病人为25%。
TREATMENT
治疗的基本观点
其余病人,治疗效果多不乐观,但新 的治疗方法出现,这些病人依然有获得有 效治疗的机会。
一般以提高生活质量、减轻痛苦的姑
息治疗为主 。
t(14:18)、t(8:14)、t(11:14):提示淋巴瘤
T(11:22):提示外周原始神经外胚层肿瘤以及 Ewing肉瘤
T(2:13)见于腺泡型横纹肌肉瘤 其它:生殖细胞肿瘤12p等臂染色体、小细胞 肺癌3p删除。神经母细胞瘤1p删除。滑膜肉瘤 t(X:18)
CHROMOSOMAL ANALYSIS
几点注意
需经验医师操作和解释 结果应可重复 多数抗原不特异(除LCA、PSA等) 假阳性和假阴性常见 单一结果多不能确立或排除诊断
ADDITIONAL PATHOLOGIC STUDIES
电镜
ELECTRON MICROSCOPY
ELECTRON MICROSCOPY
通过对特殊超微结构的识别,获得某些分
