第2课时 一氧化碳
人教版九年级化学上册教案 第6单元 课题3 第2课时一氧化碳的性质及用途

第二课时 一氧化碳的性质及用途【知识与技能】(1)知道一氧化碳的物理性质和化学性质。
(2)了解一氧化碳使人中毒的原因及防护措施。
(3)认识一氧化碳在冶金工业的重要用途。
(4)学会鉴别一氧化碳和二氧化碳的方法。
【过程与方法】(1)根据实验现象总结一氧化碳的性质。
(2)通过一氧化碳和二氧化碳性质的对比,学习对比的学习方法。
【情感态度与价值观】(1)通过全面认识一氧化碳的性质,体会事物的两面性。
(2)通过了解一氧化碳的毒性和防止一氧化碳中毒的措施,增强自我保护意识。
【重点】一氧化碳的性质及用途。
【难点】一氧化碳还原氧化铜的实验。
知识点 一氧化碳的性质和用途 【自主学习】阅读教材第121~122页,完成下列填空: 1.一氧化碳的物理性质一氧化碳是无色无味的气体,难溶于水,密度比空气略小。
2.一氧化碳的化学性质(1)可燃性:一氧化碳可以在空气中燃烧,生成__二氧化碳__(2CO +O 2=====点燃2CO 2),火焰呈__蓝色__,煤炉里上层的蓝色火焰就是一氧化碳在燃烧。
一氧化碳与空气混合后再点燃,容易发生爆炸,因此点燃一氧化碳前必须__检验其纯度__。
(2)毒性:一氧化碳极易与血液中的__血红蛋白__结合,导致血红蛋白不能很好地与氧气结合,造成生物体内__缺氧__,严重时会危及生命。
因此冬天使用煤炉取暖时,一定要装烟囱,并保持室内通风,防止一氧化碳中毒。
如果发生一氧化碳中毒,轻者应呼吸大量新鲜空气,重者要立即送医院救治。
(3)还原性:一氧化碳能与一些金属氧化物反应,生成__金属单质__和__二氧化碳__。
3.一氧化碳的用途(1)一氧化碳具有可燃性,是一种很好的气体燃料,煤气的主要成分就是一氧化碳。
(2)一氧化碳具有还原性,工业上常用一氧化碳还原铁的氧化物矿石来炼铁。
4.实验室用一氧化碳还原氧化铜【合作探究】一氧化碳和二氧化碳的性质有哪些不同?答:一氧化碳和二氧化碳都是由碳元素和氧元素组成的,但是它们的分子结构不同,它们的性质也就有很大差异。
人教版九年级化学上第六单元课题三第二课时《一氧化碳》优秀教学案例

3.介绍一氧化碳的防护措施,如通风、检测设备、中毒急救等。
4.通过实验演示一氧化碳的生成和反应过程,让学生直观地了解一氧化碳的危害。
(三)学生小组讨论
1.布置讨论题目:“请你们小组讨论一下,如何预防一氧化碳中毒?”
2.学生分组讨论,鼓励他们发表自己的观点和见解。
人教版九年级化学上第六单元课题三第二课时《一氧化碳》优秀教学案例
一、案例背景
本案例背景基于人教版九年级化学上第六单元课题三第二课时《一氧化碳》的教学内容,以提高学生对一氧化碳的性质、危害及防护措施的理解和应用能力为目标。在教学设计中,我充分考虑了学生的年龄特点、知识背景和认知水平,力求通过生活实例和实验探究,激发学生的学习兴趣,培养学生的实践能力和科学素养。
(三)情感态度与价值观
1.培养学生对化学学科的兴趣和好奇心,激发他们学习化学的内在动力。
2.培养学生关注生活、关爱生命的情感态度,提高他们的社会责任感和使命感。
3.通过对一氧化碳危害的学习,培养学生珍惜生命、安全第一的价值观念。
4.引导学生正确面对科学知识,树立科学精神,培养严谨求实的科学态度。
本章节的教学目标旨在全面提高学生的知识与技能、过程与方法、情感态度与价值观,使他们在掌握一氧化碳相关知识的同时,培养良好的学习习惯和价值观,为今后的学习和人生奠定坚实的基础。
二、教学目标
(一)知识与技能
1.了解一氧化碳的化学性质,掌握一氧化碳的分子构成、生成途径和反应特点。
2.掌握一氧化碳的毒性,了解一氧化碳对人体的危害及其作用机理。
3.学习一氧化碳的防护措施,如通风、检测和中毒急救等,提高自我保护能力。
4.能够防措施。
人教版初中九年级化学《一氧化碳》精品教学课件
课堂小结
物 没有生成新物质的变化
理 物变 质 化 只是形状、状态的变化 的
变 化
化 有其他物质生成的变化 学
变 常伴随有颜色的改变、 化 放出其他、生产沉淀等
现象,还有能量的变化
随堂训练
1.人类生活需要能量,下列能量主要由化学变化产生 的是( D ) A.电熨斗通电产生的能量 B.电灯通电发出的光 C.水电站利用水力产生的电 D.液化石油气燃烧放出的能量
× 么变化?
甲同学:有发光放热的现象,所以是化学变化。
√ 乙同学:没有生成新的物质,所以是物理变化。
【总结】此类现象可帮助我们判断是否发生了化学 变化,但不能作为判断依据。 判断物质变化类型的标准是:“是否生成新物质”。
讲授新课
例2 分析蜡烛燃烧的过程:
蜡烛熔化 蜡烛燃烧
物理变化 化学变化
同时 发生
新物质生成
有水蒸气放出, 液态的水 玻璃片上出现小
无
水珠
(2) 块状的胆矾 块状变成粉末 粉末状的胆矾
无
(3)蓝色的硫酸铜 有蓝色沉淀生成 蓝色的氢氧化
溶液
铜沉淀
有
(4)颗粒状石灰石 有气泡放出,澄 二氧化碳气体
有
(或大理石) 清石灰水变浑浊 等
讲授新课
归纳与小结
物理变化
化学变化
概念 没有生成其他物质的变化 生成其他物质的变化
①作燃料:如管道煤气 2CO+O2 点燃
2CO2
②冶炼金属:如炼铁等 CO+CuO △ Cu+CO2
讲授新课
5.一氧化碳的来源 大量CO的会造成大气的污染 ,主要来源:
汽车排放的尾气,其余来自煤等含碳燃料的燃烧和石油 的炼制等。
6.3.2 一氧化碳

8.一氧化碳和二氧化碳只有一字之差。
知2-练
(1)有人认为,两者就像孪生兄弟,这是因为( B )
A.它们由同种分子构成
B.它们由相同的元素组成
C.它们都有毒
D.它们都能溶于水
(来自《典中点》)
(2) 也 有 人 认 为 , 二 者 化 学 性 质 相 差 甚 远 , 原知因2-是练 __二__者__的__分__子__构__成__不__同_______。
用途 作燃料、冶炼金属
化学性质
可燃性:2CO+O2 =点=燃===== 2CO2
还原性: CuO+CO ==△===== Cu+ CO2
毒性:与血液中的血红蛋白相结合, 造成生物体内缺氧
2 易错小结
9.一氧化碳是一种无色、无味的有毒气体,下列关于 它的说法正确的是( D )
A.在炭火炉上放一盆水就能防止一氧化碳中毒 B.煤燃烧一定会发生一氧化碳中毒 C.发现煤气泄漏,应立即打开换气扇 D.CO能与金属氧化物反应,具有还原性
• You have to believe in yourself. That's the secret of success. 人必须相信自己,这是成功的秘诀。
•
问 题(一)
知1-导
煤气中毒是由什么气体引起的?它使人中毒
的原理是什么?
问 题(二)
有人用炉火取暖,为防止煤气中毒,在火炉 上放一盆水,这样做行吗?
13、He who seize the right moment, is the right man.谁把握机遇,谁就心想事成。2021/9/72021/9/72021/9/72021/9/79/7/2021 •14、谁要是自己还没有发展培养和教育好,他就不能发展培养和教育别人。2021年9月7日星期二2021/9/72021/9/72021/9/7 •15、一年之计,莫如树谷;十年之计,莫如树木;终身之计,莫如树人。2021年9月2021/9/72021/9/72021/9/79/7/2021 •16、教学的目的是培养学生自己学习,自己研究,用自己的头脑来想,用自己的眼睛看,用自己的手来做这种精神。2021/9/72021/9/7September 7, 2021 •17、儿童是中心,教育的措施便围绕他们而组织起来。2021/9/72021/9/72021/9/72021/9/7
06-03 课题3:二氧化碳和一氧化碳第2课时 一氧化碳的性质

1
课题3 二氧化碳和一氧化碳
——第2课时 一氧化碳的性质与用途
班级: 姓名: 日期:2014年12月11日
[导语] CO 作为生活中一种常用的气体,有它的两面性,一方面它本身有剧毒,是空
气污染物之一,不合理的使用可能会造成煤气中毒;另一方面它又是水煤气的主要成份,具有可燃性和还原性,生活中可用作燃料,工业上可以冶炼金属,为人类提供服务。
通过本节课的学习,我们要知道一氧化碳的性质和用途。
[关键词] 可燃性 毒性 还原性
[课内探究](寄语:严密的实验加推理,可以帮你获取新知。
)
1.通过自主学习中的2和3你可以总结下CO 的哪些化学性质? ① ②
2.如图是一氧化碳还原氧化铜的实验装置,请回答:
①氧化铜是 色粉末。
②实验开始时,要先通入一氧.....化碳一段时间,再点燃左边的.............
酒精灯...
,目的是。
③实验结束时,先熄灭左边的......
[课堂小结]请简要总结你知道了一氧化碳的哪些性质和用途。
[达标检测]
1.火炉中有淡蓝色火焰时,你知道煤炉中发生了哪些化学反应?试写出相关的化学方程式。
2.家用煤气的主要成分CO 没有气味, CO 泄漏时我们能闻到一种难闻性气味,它起什么作用?当发现煤气泄漏时你该怎么办?
3.什么原因会导致煤气中毒?如何防止煤气中毒?
4.请用文字或化学方程式表示CO 2和CO 的化学性质。
5.完成图中所示的化学反应方程式,并注明反应的基本类型及反应条件。
① ② ③ ④ ⑤ ⑥
⑦ ⑧。
九年级化学上册第六单元碳和碳的氧化物课题3二氧化碳和一氧化碳第2课时一氧化碳导学案新版新人教版

第2课时 一氧化碳【学习目标】1.了解一氧化碳的性质和用途。
2.认识一氧化碳还原氧化铜的原理及使人中毒的原因。
3.学会鉴别一氧化碳和二氧化碳的方法。
【重点难点】1.一氧化碳的性质和用途。
2.一氧化碳还原氧化铜的原理。
学习内容 一氧化碳的性质和用途 【学习指导】阅读课本第121-122页的有关内容,完成下列填空。
1.一氧化碳的物理性质:一氧化碳是一种没有颜色,没有气味的气体,难溶于水,相对分子质量是28,密度比空气略小。
收集时采用排水集气法。
2.一氧化碳的化学性质:(1)可燃性:一氧化碳燃烧时火焰呈蓝色,放出大量的热,因而可作燃料。
CO 是可燃性气体,当里面混有空气或氧气,点燃时有可能发生爆炸,所以点燃前一定要验纯。
CO 燃烧的化学方程式为2CO +O 2=====点燃2CO 2。
煤炉里常发生的反应:下层C +O 2=====点燃CO 2;中层CO 2+C=====高温2CO ;上层2CO +O 2=====点燃2CO 2,所以煤炉里煤层上方的蓝色火焰,就是CO 在燃烧。
(2)毒性:CO 极易与血液中的血红蛋白结合,从而使血红蛋白不能很好地与氧结合,造成生物体内缺氧,严重时会危及生命。
因此冬天用煤取暖时,一定要装烟囱,并且注意室内通风,防止一氧化碳中毒。
(3)还原性:用CO 还原CuO 时,试管中的CuO 由黑色逐渐变为红色;将生成的气体通入澄清的石灰水中,可以看到澄清的石灰水变浑浊。
前一个反应的化学方程式为:CO +CuO=====△Cu +CO 2,其中还原剂是CO,氧化剂是CuO,CuO 被还原,被氧化的是CO 。
CuO 发生了还原反应,CO 发生了氧化反应。
这个反应不是(填“是”或“不是”)化学反应的基本类型。
CO 具有还原性,所以可以用来冶铁。
【讨论交流】1.煤气厂为什么常在家用煤气中掺入微量具有难闻气味的气体?如发生煤气泄漏应当怎么办?2.如何除掉CO 2中的CO ?如何除掉CO 中的CO 2? 【温馨点拨】1.便于我们及时发现煤气泄漏。
第六单元课题2碳的氧化物 第2课时一氧化碳2024-2025学年九上化学人教版上册

1
2
3
4
5
6
7
8
9 10
3. 下列物质中不能用来鉴别CO和CO2两种气体的是( D )
A. 澄清石灰水
B. 紫色石蕊溶液
C. 灼热的氧化铜
D. 稀盐酸
4. (六安金安期末)如果要除去二氧化碳中混有的少量一氧化碳,应该 采用的方法是( B ) A. 将混合气体点燃 B. 将混合气体通过灼热的氧化铜 C. 将混合气体通过澄清石灰水 D. 将混合气体从一个容器倾倒到另一个容器中
1
2
3
4
5
6
7
8
9 10
5. 将CO2、CO、O2、N2的混合气体依次通过灼热的铜网、澄清石灰水、 灼热的CuO,充分反应后冷却至室温,最后剩余的气体是( B )
A. N2
B. CO2和N2
C. O2和N2
D. CO2和CO
1
2
3
4
5
6
7
8
9 10
6. (2023·六安模拟)下列关于如图所示的碳和碳的化合物知识网络图
2CO2
。
在燃烧,
第9题
1
2
3
4
5
6
7
8
9 10
(2) 煤炉的进气口在煤炉的下方,在进气口,煤的燃烧一般都很充
点燃
分,其反应的化学方程式为 C+O2
CO2
。
1
2
3
4
5
6
7
8
9 10
(3) 煤炉中的一氧化碳有两个来源:① 煤的不充分燃烧,反应的化学
方程式为
点燃
2C+O2
2CO
2024年秋新人教版九年级化学上册 6.2.2 一氧化碳(课件)

3.碳元素是世界上最大的元素家族。下列有关碳的氧化物的说法 正确的是( B ) A.CO2的排放是导致酸雨的原因 B.在一定条件下,CO和CO2可以相互转变 C.在煤炉上放一盆水能防止CO中毒 D.CO能用于冶炼金属,是因为CO具有可燃性
一 一氧化碳的物理性质
CO通常状况下为无色、无臭 的气体,难溶于水,密度比空 气略小。
一氧化碳分子(CO)
二 一氧化碳的化学性质
1.可燃性 现象: 一氧化碳能够燃烧,燃烧时放 出大量的热,火焰呈蓝色。
点燃
2CO + O2 2CO2 注意: 一氧化碳是可燃性气体,点燃
之前要验纯。
用途: 用作燃料
2.与某些氧化物的反应
与氧化反应
在一定条件下具有氧化性 C+CO2 高温 2CO
能与某些氧化物反应 CO+CuO △ Cu+CO2
思考与交流 1.鉴别CO和CO2的方法?
①气体分别通入紫色石蕊溶液中,溶液变红的是CO2,不变的是CO。 ②气体分别通入澄清石灰水中,石灰水变浑浊的是CO2,不变的是CO。 ③在尖嘴玻璃管口点火,气体被点燃的是CO,不能被点燃的是CO2。
一氧化碳
血红蛋白
氧气
比较一氧化碳和二氧化碳的物理性质
一氧化碳
颜色、状态、
物理
气味
无色、无臭、 气体
性质
密度
比空气密度略小
溶解性
难溶于水
二氧化碳
无色、无臭、 气体
比空气密度大 能溶于水
思考与交流
1.我们的家用煤气中常常会添加一些具有难闻气味的气体(如乙硫醇), 你知道为什么吗?
为了让人们易于察觉一氧化碳泄漏, 以免一氧化碳中毒 2.如果发生煤气泄露怎么办?
教学案:人教版第六单元课题3第二课时:《一氧化碳的性质与用途》说课稿

(二)新知讲授
在新知讲授阶段,我将逐步呈现知识点,引导学生深入理解:
1.一氧化碳的物理性质:通过实验观察,让学生了解一氧化碳的颜色、气味、密度等物理性质。
2.一氧化碳的化学性质:结合实验,讲解一氧化碳的氧化还原性、毒性等化学性质,并与其他碳的氧化物进行对比。
小组合作法:通过小组合作学习,促进学生之间的交流与合作,培养学生的团队精神和沟通能力,同时也能提高学习效率。
(二)媒体资源
我将使用以下教具、多媒体资源和技术工具来辅助教学:
1.实验器材:用于进行一氧化碳的制备、性质验证等实验,帮助学生直观地理解一氧化碳的相关知识。
2.多媒体课件:通过展示一氧化碳的结构、反应原理等图片和动画,帮助学生更好地理解抽象的概念。
(二)学习障碍
学生在学习本节课之前,已经掌握了碳的基本性质、氧化还原反应等前置知识。然而,可能存在以下学习障碍:
1.对一氧化碳的认识不够全面,容易将其与二氧化碳混淆。
2.对一氧化碳的化学性质理解不深,难以理解其毒性的原因。
3.在实验操作过程中,可能对一氧化碳的毒性防护意识不足。
(三)学习动机
为了激发学生的学习兴趣和动机,我将采取以下策略或活动:
教学案:人教、教材分析
(一)内容概述
本节课的教学内容是人教版第六单元课题3第二课时:《一氧化碳的性质与用途》。该课题位于化学课程中的“碳及其化合物”部分,是学生在学习碳的基本性质后,对碳的氧化物——一氧化碳的学习。本节课在整个课程体系中起到承上启下的作用,既巩固了学生对碳的基本认识,又为一氧化碳的进一步学习奠定了基础。
板书在教学过程中的作用是帮助学生构建知识结构,突出教学重点,便于学生记录和理解。为确保板书清晰、简洁且有助于学生把握知识结构,我将:
课题3 二氧化碳和一氧化碳教学设计2(第2课时)

课题3 二氧化碳和一氧化碳课时2 一氧化碳一、教学目标1.通过引导学生比较一氧化碳和二氧化碳的性质和用途,让学生体会物质的结构、性质、用途之间的关系;2.掌握一氧化碳的可燃性和还原性,能用化学方程式表示一氧化碳可燃性、一氧化碳还原性等反应;3.了解一氧化碳的物理性质、毒性及对环境的污染,并培养学生的安全意识。
二、教学重难点重点:CO 的可燃性、毒性、还原性。
难点:CO 还原氧化铜的实验注意事项。
三、教学过程【新课导入】在前面的学习中,我们已知道碳在氧气充足的情况下燃烧会生成二氧化碳,而在氧气不充足的情况下燃烧会生成一氧化碳,C+O 2=====点燃CO 22C+O 2=====点燃2CO【交流讨论】观察二氧化碳与一氧化碳的分子区别在哪里?CO 2和CO 的性质会相同吗?【总结与交流】从分子结构看:一个CO 2分子是由一个碳原子和两个氧原子构成的;一个CO 分子是由一个碳原子和一个氧原子构成的。
元素组成相同,但分子构成不同,因此这使得它们的性质有很大不同。
【过渡】那一氧化碳有哪些性质呢?我们一起来学习一下吧!【讲解】一氧化碳具有可燃性,在燃烧时发出蓝色的火焰(图片展示)。
2CO+O 2=====点燃2CO 2【思考】在CO 燃烧的火焰上方,分别罩冷而干燥的烧杯和内壁沾有澄清石灰水的烧杯,观察到什么现象?【交流讨论】在北方,人们还常用蜂窝煤炉来取暖、烧饭,但必须也要加装烟囱,你知道在下面的燃烧很旺的蜂窝煤炉中发生了哪些反应吗?【总结】最下层:C +O 2=====点燃CO 2中层:2C+O 2=====点燃2CO ,CO 2+C =====高温2CO上层:2CO +O 2=====点燃2CO 2【过渡】人们常说:不能在密闭房间里烧炭取暖,还有经常有新闻报道称“煤气(主要成分CO )中毒” ,你知道是为什么吗?【讲解】一氧化碳具有毒性,它极易与血液中的血红蛋白结合,从而使血红蛋白不能再与氧气结合,造成体内缺氧,危及生命。
6.3.2一氧化碳课件—九年级化学人教版上册

(3)反应③在工业上常用于_____炼__铁_____。 ____________________
(2)实验进行一段时间后,A装置中观察到的现象为________________________,反应的化学方程式是__________________________。 3.【2021·威海模拟】用“W”形玻璃管进行如图所示的微型实验,下列有关说法错误的是( ) A.C2O3中碳元素的化合价为+3价 C.③可通过与澄清石灰水反应实现 (3)反应③在工业上常用于____________。 6.【2021·营口】下列关于二氧化碳与一氧化碳用途的说法,错误的是( ) (提示:氧化铁为红色固体) 【点拨】CO不能与澄清石灰水反应,三氧化二碳化学性质与一氧化碳相似,可判断C2O3不能使澄清石灰水变浑浊,故D选项说法错误 。 9.【2020·甘孜】CO、CO2和CaCO3的转化关系如图所示。 (提示:氧化铁为红色固体) 实验开始时应先________(填“Ⅰ”或“Ⅱ”),然后________(填“Ⅰ”或“Ⅱ”)。 【点拨】一氧化碳具有还原性,在加热的条件下,一氧化碳还原氧化铜生成铜和二氧化碳,即①可通过物质的还原性实现,选项A正确 ;
11.实验室用一氧化碳还原氧化铜的装置如图所示,试回答下列问题。
(提示:氧化铁为红C色.固体将) CO通入澄清石灰水中,澄清石灰水会变浑浊
D.高温下,CO气体可与Fe2O3等含铁氧化物反应
【点拨】将CO气体通入澄清石灰水中,CO与澄清 石灰水不反应,澄清石灰水不会变浑浊,故C选项 错误。
【答案】C
(用化学方程式表示)。
生煤炉取暖时容易发生中毒,有人说在煤炉上放一盆 水可以防止煤气中毒,你认为这种说法对吗?_不__对___, 理由是_____C__O_难__溶__于__水_________。
九年级化学人教版上册第六单元课题3二氧化碳和一氧化碳第2课时一氧化碳的化学性质教学设计

五、作业布置
1.完成课本第六单元课题3中的课后练习题,重点是一氧化碳的化学性质、应用与防护等方面的题目。
-选择题:检测学生对一氧化碳基本概念的理解。
-填空题:考查学生对一氧化碳化学性质的掌握。
-简答题:培养学生运用一氧化碳知识解决实际问题的能力。
-一氧化碳的危害及防护措施。
-个人对于一氧化碳安全意识的认识和体会。
4.预习下一节课内容,了解一氧化碳的制备与性质,为课堂学习做好准备。
5.收集与一氧化碳相关的新闻、案例等资料,下节课分享,提高学生的安全意识和环保意识。
2.结合本节课所学内容,设计一道家庭实验题目,要求学生在家中利用简单材料进行实验,观察一氧化碳的化学性质,并记录实验过程和结果。
例:用蜡烛、火柴、小烧杯等材料,观察一氧化碳的燃烧现象,并分析其可燃性。
3.撰写一篇关于一氧化碳在生活中的应用与防护的小论文,要求不少于500字。内容包括:
-一氧化碳在生活中的应用实例。
1.将学生分成小组,讨论以下问题:
a.一氧化碳的可燃性和还原性在实际生活中有哪些应用?
b.如何防范一氧化碳中毒?
c.举例说明一氧化碳与二氧化碳在化学性质上的区别。
2.各小组汇报讨论成果,教师点评并进行讲解。
(四)课堂练习
1.设计具有针对性的练习题,检查学生对一氧化碳化学性质的理解。
2.练习题包括选择题、填空题、简答题等,涵盖一氧化碳的物理性质、化学性质、应用与防护等方面。
(二)讲授新知
1.介绍一氧化碳的基本概念,包括其化学式、物理性质和化学性质。
2.详细讲解一氧化碳的可燃性、还原性、毒性等化学性质,并通过实验现象进行验证。
【初中化学】人教版九年级上册第2课时 一氧化碳(练习题)
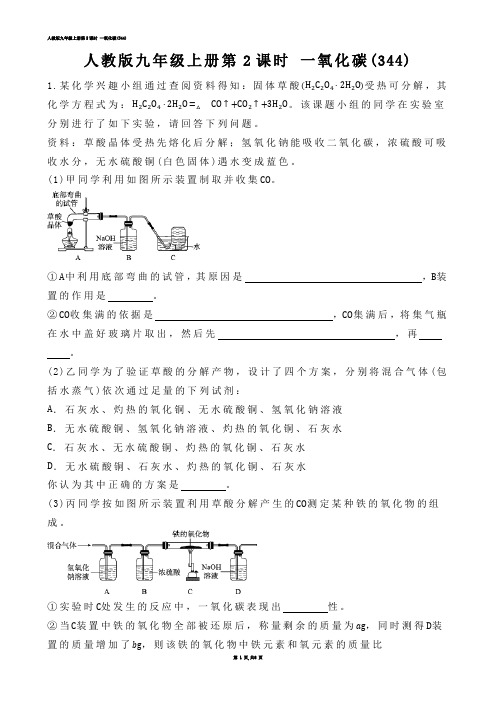
人教版九年级上册第2课时一氧化碳(344)1.某化学兴趣小组通过查阅资料得知:固体草酸(H2C2O4·2H2O)受热可分解,其化学方程式为:H2C2O4·2H2O=△CO↑+CO2↑+3H2O。
该课题小组的同学在实验室分别进行了如下实验,请回答下列问题。
资料:草酸晶体受热先熔化后分解;氢氧化钠能吸收二氧化碳,浓硫酸可吸收水分,无水硫酸铜(白色固体)遇水变成蓝色。
(1)甲同学利用如图所示装置制取并收集CO。
①A中利用底部弯曲的试管,其原因是,B装置的作用是。
②CO收集满的依据是,CO集满后,将集气瓶在水中盖好玻璃片取出,然后先,再。
(2)乙同学为了验证草酸的分解产物,设计了四个方案,分别将混合气体(包括水蒸气)依次通过足量的下列试剂:A.石灰水、灼热的氧化铜、无水硫酸铜、氢氧化钠溶液B.无水硫酸铜、氢氧化钠溶液、灼热的氧化铜、石灰水C.石灰水、无水硫酸铜、灼热的氧化铜、石灰水D.无水硫酸铜、石灰水、灼热的氧化铜、石灰水你认为其中正确的方案是。
(3)丙同学按如图所示装置利用草酸分解产生的CO测定某种铁的氧化物的组成。
①实验时C处发生的反应中,一氧化碳表现出性。
②当C装置中铁的氧化物全部被还原后,称量剩余的质量为ag,同时测得D装置的质量增加了bg,则该铁的氧化物中铁元素和氧元素的质量比为。
③丁同学认为去掉A装置,对测定结果无影响,他的观点(填“正确”或“不正确”),你的判断理由是。
而戊同学认为在D装置后还应再增加某装置,该装置是;若无此装置,对测定结果是否有影响?(填“有”或“没有”)。
2.下列关于一氧化碳的说法错误的是()A.一氧化碳能使紫色石蕊溶液变红B.一氧化碳难溶于水C.一氧化碳有毒,污染空气D.一氧化碳可作为燃料3.对比分析不同物质的共性与差异是学习化学的有效方法。
下列关于CO2和CO 的各项对比,有错误的是()A.AB.BC.CD.D4.下列说法正确的是()A.可用紫色石蕊溶液鉴别一氧化碳和二氧化碳B.CO常用于人工降雨C.用闻气味的方法能够区别CO2和COD.一氧化碳和二氧化碳均可用于冶炼金属5.一氧化碳与氧化铜在加热的条件下反应,叙述正确的是()A.一氧化碳被还原B.固体粉末由红变黑C.氧元素存在形态不变D.铜元素的质量减少6.三氧化二碳(C2O3)是某星球大气的成分之一,其化学性质与一氧化碳相似。
(新)人教版化学九年级《第2课时 一氧化碳》导学案(精品)

第2课时一氧化碳【学习目标】1.了解一氧化碳的物理性质。
2.掌握一氧化碳的可燃性、毒性、复原性等化学性质。
3.知道一氧化碳的用途以及中毒的机理。
【学习重点】一氧化碳的化学性质,一氧化碳复原金属氧化物的实验步骤和本卷须知。
【学习难点】一氧化碳复原金属氧化物的实验步骤和本卷须知。
【学习过程】 一、自主学习1.CO 是一种无色无味的气体,其密度比空气略小,难溶于水。
2.一氧化碳的化学性质:〔1〕可燃性,反响的化学方程式为2CO+O 2=====点燃2CO 2;〔2〕复原性〔以CuO 为例〕,反响的化学方程式为CO +CuO =====△Cu +CO 2。
3.一氧化碳的毒性:煤气中毒即CO 中毒,原因是CO 很容易与血液里的血红蛋白相结合,使血红蛋白不能再与O 2结合,从而造成人体缺氧。
二、新知导学知识点一一氧化碳的物理性质【引导自学】请学生自主阅读教材P121,了解一氧化碳的物理性质。
【讨论】有人用炉火取暖,为了防止煤气中毒,在炉火上放一盆水行吗?为什么?不行,因为CO 难溶于水,不能用水吸收CO知识点二 一氧化碳的化学性质 1.可燃性一氧化碳能够燃烧,燃烧时放出大量的热,火焰呈蓝色。
将一个内壁涂有澄清石灰水的烧杯罩在火焰上方,发现澄清石灰水变浑浊,证明一氧化碳燃烧后生成了二氧化碳。
一氧化碳燃烧的化学方程式为2CO+O 2=====点燃2CO 2。
2.毒性【引导自学】请学生自主阅读教材P121,了解CO 的毒性及其救治方法。
CO 极易与人体血液中的血红蛋白结合,从而使氧气不能很好地与血红蛋白结合,造成生物体内缺氧,严重时会危及生命。
冬天用煤火取暖时,一定要装烟囱,并且注意室内通风,防止CO 中毒。
如果发生CO 中毒,轻度的应呼吸大量新鲜空气,严重的要立即送到医院进行救治。
【小组讨论】1.为什么家用煤气中掺入具有难闻气味的气体?让人们及时发现煤气泄漏 如果发生煤气泄漏应当怎么办?关闭气阀,开窗通风2.如以下图,煤炉中常发生哪些化学反响?请写出反响的化学方程式。
一氧化碳

△
Cu+CO2 +
CO CO2 得到氧,被氧化,CO是还原 得到氧,被氧化, 是还原 具有还原性; 剂!具有还原性; 具有还原性 CuO Cu 失去氧,被还原, 失去氧,被还原, CuO 是氧化剂,具有氧化性。 是氧化剂,具有氧化性。
三大还原剂 氢气
CO+CuO + C+2CuO + H2+CuO
可以用它做肥料,提高产量。 可以用它做肥料,提高产量。 4、干冰可以作制冷剂,人工降雨。 、干冰可以作制冷剂,人工降雨。
一氧化碳
当碳燃烧不充分时,生成一氧化碳。 当碳燃烧不充分时,生成一氧化碳。
2C+O2 +
点燃
2CO
一 . 一氧化碳的性质 1.物理性质: 物理性质: 物理性质 一氧化碳 CO 化学式 颜色 状态 气味 密度 水溶性 无色 气态 无味 略小于空气 1:0.02 :
二、CO2的化学性质: 1、CO2不能燃烧,也不能支持燃烧; 2、CO2可以和水反应生成碳酸;
CO2 +H2O = H2CO3 H2CO3 = CO2↑+H2O
3、CO2和澄清石灰水反应生成 碳酸钙和水;
CO2 +Ca(OH)2= CaCO3 ↓+ H2O
的用途: 三、CO2的用途: 1、CO2可以用于灭火; 、 可以用于灭火; 2、 2、CO2可以制汽水; 可以制汽水; 3、 CO2是光合作用的原料;温室里 是光合作用的原料; 、
碳、氢气、一氧化碳的性质比较 氢气、
CO C H2 性质 可燃性 点燃 2H2+O2 点燃 2H2O 2CO+O + 2 作燃料 C+O2 点燃 CO2 2C+O2 2CO 2CO2 还原性 C+2CuO △ + 冶炼金 2Cu+CO ↑ + 2 属 H2+CuO Cu+H2O +
初三化学第六单元课题3第2课时:一氧化碳的性质

三、一氧化碳的化学性质
【想一想】煤炉里的煤在燃烧过程中,发生了哪些化学反应?
点燃
2CO + O2
2CO2
点燃
2C + O2
2CO
高温
C + CO2
2CO
点燃
C + O2
CO2
液化气、天然气等含 碳燃料在不充分燃烧 时都会有CO生成。
【思考】向一盆燃烧旺盛的炭火中洒少量的水,火焰更旺且为蓝色;但洒入较多的水,炭火熄灭,为什么?
4.区别CO2、CO、O2三种气体,最简便的方法是( B )
A.用带火星的木条
B.用燃着的木条
C.用澄清石灰水
D.用灼热的氧化铜
六、课堂小结
一、一氧化碳的物理性质 无色无味的气体、密度比空气略小、难溶于水。 二、一氧化碳的化学性质 (1)一氧化碳的毒性 (2)一氧化碳的可燃性: 2CO + O2 点燃 2CO2 (3)一氧化碳的还原性: CuO + CO 高温 Cu + CO2 三、一氧化碳的用途 (1)气体染料 (2)冶炼金属
解毒方法:如果发生一氧化碳中毒,轻度的应立即撤离中毒环境,呼 吸大量新鲜空气或氧气,严重的应进行人工呼吸并立即到医院进行治疗。
防止措施:①冬天用煤火取暖时一定要装烟囱,并且注意室内通风, 防止一氧化碳中毒。②CO通常状况下为无色、无味的气体,煤气泄漏时不 易被人察觉,所以煤气厂在家用煤气中掺入微量具有难闻气味的气体,使 人在煤气泄漏时及早察觉。如果发现煤气泄漏,应立即关闭阀门,然后开 窗通风。
还原性或氧化性
二氧化碳
不能燃烧 , 一般也不能支持燃烧 ,也 不能供给呼吸
跟水反应 CO2 + H2O = H2CO3
九年级化学上册第六单元课题3二氧化碳和一氧化碳第2课时一氧化碳随堂练习

第2课时一氧化碳1.对比是学习化学的重要方法,下列关于CO2与CO的比较,错误的是( )A.CO2可用于人工降雨,CO可用于光合作用B.通常情况下,CO2能溶于水,CO难溶于水C.CO2无毒,CO易与血液中的血红蛋白结合引起中毒D.一个二氧化碳分子比一个一氧化碳分子多一个氧原子2.近年来,媒体常报道煤气中毒的惨剧,煤气中毒是由于含碳燃料不充分燃烧生成CO引起的。
下列做法可以有效地避免煤气中毒发生的是( )A.严寒的冬天,在狭小密闭的房间内烧炭取暖,在炭盆旁边放一盆水B.在清洗偏远的水井时,边用柴油作为能源的抽水机放到井内抽水,边派人戴着口罩到井下洗井C.将液化石油气热水器安装在密闭的冲凉房内D.将液化石油气热水器安装在冲凉房外面,且要通风透气3.可区别CO、CO2两种气体的方法是( )A.看颜色 B.用澄清的石灰水鉴别C.闻气味 D.看组成物质的元素种类4.以下几种气体只能用排水法收集的是( )A.CO B.CO2C.H2D.O25.在一定条件下,一氧化碳、木炭都能与氧化铜发生发应,下列叙述正确的是( )A.反应产生的气体都有毒B.反应中都有红色固体生成C.反应前后C、Cu、O三种元素的化合价均有变化D.反应的生成物不同6.按要求写出煤炉中的煤在燃烧过程中反应的化学方程式:(1)煤炉底部在煤充分燃烧过程中所发生的反应:_ __。
(2)煤炉中部产生毒气的反应:__ _。
(3)煤炉表面产生蓝色火焰的反应:__ _。
7.为证明木炭在一定条件下燃烧的产物中既有CO2,也有CO,可以先将气体通过澄清的石灰水,观察到__ _,证明有CO2存在,反应的化学方程式为_ _。
接着将气体干燥后通过灼热的氧化铜,观察到__ _,即证明有CO存在。
8.除去二氧化碳气体中混有的少量一氧化碳,最合理的方法是( )A.使混合气体通过澄清的石灰水B.将混合气体点燃C.使混合气体通过灼热的氧化铜D.使混合气体通过灼热的焦炭9.三氧化二碳(C2O3)是某星球大气的成分之一,其化学性质与一氧化碳相似,下列关于三氧化二碳的说法中错误的是( )A.有毒B.可以燃烧C.密度比空气的小 D.能还原氧化铁10.在如图装置中通入X气体,并在管口P处点燃,实验结果澄清石灰水变浑浊,则X可以是( )A .H 2B .COC .CO 2D .O 211.CO 是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业。
第六单元 课题2 碳的氧化物 第2课时 一氧化碳课件(共21张PPT内嵌视频)人教版九年级化学上册
习题练习5. 选择氧气、二氧 Nhomakorabea碳或一氧化碳填空,并写出有关反应的化学方程式。
(1)能使带火星的木条复燃的是 氧气 ,能用于灭火的是 二氧化碳 。
(2)绿色植物进行光合作用吸收的是 二氧化碳 ,释放的是 氧气 ;
能产生温室效应的气体的是 二氧化碳 。
(3)能在空气中燃烧的是 一氧化碳 ,反应的化学方程式是
学完本课题你应该知道
1. 一氧化碳是无色、无臭的气体,难溶于水,密度比空气略小。 2. 一氧化碳能够燃烧,具有还原性和毒性。
习题练习
1. 下列对一氧化碳的认识中,错误的是( C ) A.一氧化碳有可燃性,可用作燃料 B.一氧化碳有还原性,可用于冶炼金属 C.一氧化碳密度比空气小,可采用向上排空气法收集 D.一氧化碳能与血液里的血红蛋白结合,致使人体缺氧中毒。
课程讲授
知识目标
初步认识
1.了解一氧化碳的性质。 2.认识一氧化碳在冶金工业的重要用途。 3.知道生活中一氧化碳的产生途径,致人中毒的机理及其 对环境的污染。
课程讲授
初步认识
一氧化碳
1.一氧化碳的物理性质
碳的氧化物:二氧化碳,一氧化碳 两者都是由碳元素和氧元素组成 1个CO2分子比1个CO分子多1个氧原子 ,这就使得它们的性质有很大的不同 。物理性质: CO是一种无色、无臭的气体,难溶于水,密度比空气略小。
课程讲授
一氧化碳
初步认识
1.一氧化碳的物理性质 收集一氧化碳气体
一氧化碳的密度比空气略小,因此 不宜用排空气法收集;一氧化碳难 溶于水,可用排水法来收集。
课程讲授
初步认识
一氧化碳
2.一氧化碳的化学性质
可燃性 燃烧时放出大量的热,火焰呈蓝色。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
略
①说明一氧化碳具有还原性 ②说明一氧化碳氧化后的产物是二 氧化碳 ③可以防止有毒的一氧化碳污染空气 ④既能说明一氧 化碳具有可燃性,又充分地利用了能源 A.①② B.①②③ C.②③④ D.全部
第六单元
ห้องสมุดไป่ตู้
第2课时 一氧化碳
知识要点基础练 综合能力提升练 中考高频冲刺练
-4-
3.( 佛山中考 )“归纳与比较”是化学学习的重要方法。下列有关 CO2和CO的知识归纳,错误的是 ( B ) A.组成:一氧化碳和二氧化碳都是由碳元素和氧元素组成的 B.性质:都是无色、无味的气体;都能溶于水,水溶液显酸性;都能与 石灰水反应;都能燃烧等 C.用途:CO2可用于光合作用、灭火、化工产品的原料和气体肥 料,“干冰”可用于人工降雨等;CO可用作气体燃料、冶炼金属的还 原剂等 D.危害:CO2会造成“温室效应”;CO极易与血液中的血红蛋白结合 引起中毒
试管中观察到的实验现象是 程式为 CO2+Ca( OH )2
澄清石灰水变浑浊 ,反应的化学方 CaCO3↓+H2O 。
,这样做
( 4 )实验结束时,应先 停止加热 ,再 继续通入CO直到玻璃管冷却 的目的是 防止炽热的铜被空气氧化 。
第六单元
第2课时 一氧化碳
知识要点基础练 综合能力提升练 中考高频冲刺练
第六单元 碳和碳的氧化物
课题3 二氧化碳和一氧化碳
第六单元
第2课时 一氧化碳
知识要点基础练 综合能力提升练 中考高频冲刺练
-3-
知识点1 一氧化碳的物理性质 1.一氧化碳是一种 无色 、 无味 的气体,密度比空气 小 , 难 溶于水,收集一氧化碳最好选用 排水 法。 知识点2 一氧化碳的化学性质 2.下列有关如图所示装置的叙述正确的是 ( D )
第六单元
第2课时 一氧化碳
知识要点基础练 综合能力提升练 中考高频冲刺练
-6-
据图回答下列问题: ( 1 )图A中,薄铜片受热时生成氧化铜的化学方程式为
2Cu+O2
2CuO 。
( 2 )趁热将图A中的薄铜片插入图B所示的装置中( 如图C所示 ), 可观察到薄铜片的颜色变化是 由黑色变成红色 ;振荡集气瓶, 可观察到的现象是 澄清石灰水变浑浊 。 ( 3 )实验结束后,用燃着的木条点燃集气瓶中剩余的气体,有明显 的淡蓝色火焰出现,该反应的化学方程式为 2CO+O2 2CO2 。
第六单元
第2课时 一氧化碳
知识要点基础练 综合能力提升练 中考高频冲刺练
-7-
6.某同学设计如图所示实验装置进行一氧化碳还原氧化铜的实验。试回答下列问题
( 1 )该装置存在的一个主要问题是 缺少尾气处理装置 ,你的改进方法是 用 酒精灯点燃尾气( 合理即可 ) 。 ( 2 )实验开始时,是先加热氧化铜,还是先通入一氧化碳? 先通入一氧化碳 ,目 的是 排尽装置中的空气,防止发生爆炸 。 ( 3 )实验过程中,玻璃管中观察到的实验现象是 黑色粉末逐渐变 成红色 ,反应的化学方程式为 CO+CuO Cu+CO2
第六单元
第2课时 一氧化碳
知识要点基础练 综合能力提升练 中考高频冲刺练
-5-
4.把二氧化碳、一氧化碳和氮气的混合气体依次通过足量澄清石 灰水、足量灼热的氧化铜,冷却后剩下的气体是 ( C ) A.二氧化碳和一氧化碳 B.氮气 C.二氧化碳和氮气 D.一氧化碳和氮气 5.为加深对一氧化碳还原性的理解,减少一氧化碳对环境的污染,某 同学设计了如图所示的实验。
-8-
7.( 安徽中考 )我国科学家在CO低温氧化的研究上取得了突破性 进展,利用四氧化三钴纳米棒作催化剂,可将汽车尾气中的CO在低 温下氧化为CO2,示意图如图。下列关于该反应的说法错误的是 ( C ) A.可有效降低汽车尾气对大气的污染 B.属于化合反应 C.反应前后四氧化三钴纳米棒的化学性质发生变化 D.反应前后氧原子数不发生变化
