β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识

β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶(ESBLs)、头孢菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler 分类法),将β-内酰胺酶分为丝氨酸酶(包括A类、C类酶和D类酶)及金属酶(B类酶)。
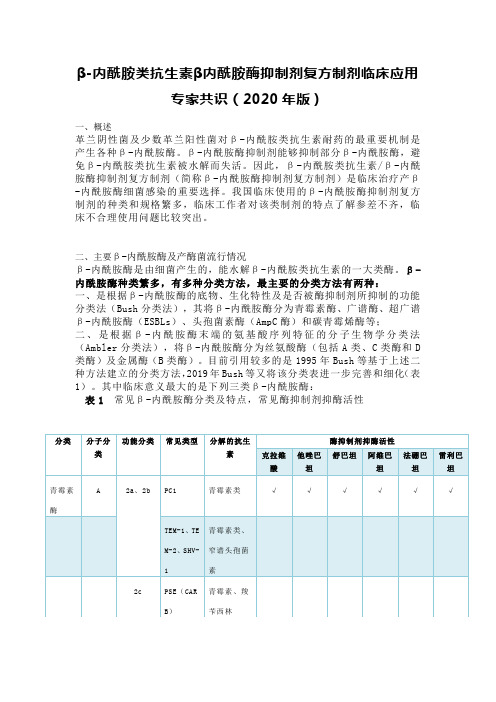
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表1常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性1、ESBLs主要属2be\2br\2ber类酶,是由质粒介导的能水解青霉素类、头孢菌素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M型、OXA型和其他型共5大类型。
2、AmpC酶属C类酶,通常由染色体介导,可以被β-内酰胺类抗生素诱导。
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶(ESBLs)、头孢菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler分类法),将β-内酰胺酶分为丝氨酸酶(包括A类、C类酶和D 类酶)及金属酶(B类酶)。
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表1 常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M 型、OXA型和其他型共5大类型。
2、AmpC酶属C类酶,通常由染色体介导,可以被β-内酰胺类抗生素诱导。
部分由质粒介导,常呈持续高水平表达。
产超广谱β内酰胺酶细菌感染防治专家共识

产超广谱β-内酰胺酶细菌感染防治专家共识产超广谱β-内酰胺酶细菌感染防治专家委员会超广谱β-内酰胺酶(β)是肠杆菌科细菌对β-内酰胺类抗菌药物产生耐药的主要机制之一,其预防与治疗已成为临床医生需要面对的重要问题[1],但国内外缺少相关问题处理的指导性意见。
《中华实验和临床感染病杂志(电子版)》编辑部和《医学参考报·感染病学频道》编辑部组织国内部分专家制定本《共识》,以对相关问题的处理提供指导。
一、超广谱β-内酰胺酶及相关概念1.β-内酰胺酶及分类:β-内酰胺酶是指细菌产生的能水解β-内酰胺类抗菌药物的灭活酶,是细菌对β-内酰胺类抗菌药物耐药的主要机制。
其分类见表1。
2.超广谱β-内酰胺酶:细菌在持续的各种β-内酰胺类抗菌药物的选择压力下,被诱导产生活跃的及不断变异的β-内酰胺酶,扩展了其耐受头孢他啶、头孢噻肟、头孢吡肟等第3代及第4代头孢菌素,以及氨曲南等单环β-内酰胺类抗菌药物的能力,这些新的β-内酰胺酶被称为。
属于分类的A类和D类酶,按分类属2。
根据质粒所携带编码基因同源性的不同,主要有、、、型。
还有一些少见的型别,如、、、、、等。
引起临床感染的产β-内酰胺酶细菌依次为肺炎克雷伯菌、铜绿假单孢菌、大肠埃希菌、阴沟肠杆菌等。
二、产细菌感染的流行因素及发展趋势自1982年在英格兰首先发现产克雷伯菌后,产细菌的流行在世界各地广泛报道。
主要存在于临床分离的革兰阴性杆菌,其中又多见于肠杆菌科细菌[2-4]。
在肠杆菌科细菌中以大肠埃希菌和克雷伯菌最为常见,克雷伯菌包括肺炎克雷伯菌和产酸克雷伯菌。
其他常见产细菌有产气肠杆菌、变形杆菌、沙门属菌、阴沟肠杆菌、粘质沙雷菌、铜绿假单胞菌、不动杆菌属等。
各个国家和地区产细菌的发生率明显不同。
日本、荷兰等国家产细菌的发生率很低,而法国、印度等国家产细菌的发生率很高,可有高达50%以上的克雷伯菌属的细菌产生,而且具有较严重的耐药性。
我国大陆不同研究者报告的产细菌发生率各有不同,大肠埃希菌发生率大约在40%,肺炎克雷伯菌发生率更低一些。
内酰胺类抗生素内酰胺酶抑制剂合剂临床应用专家共识

内酰胺类抗生素内酰胺酶抑制剂合剂临床应用专家共识一、本文概述《内酰胺类抗生素内酰胺酶抑制剂合剂临床应用专家共识》旨在汇集国内外关于内酰胺类抗生素与内酰胺酶抑制剂合剂在临床应用中的最新研究成果和实践经验,为临床医生提供科学、规范、实用的用药指导。
内酰胺类抗生素是一类具有广泛应用价值的抗菌药物,而内酰胺酶抑制剂则能够增强抗生素的疗效,减少耐药性的产生。
本文将从合剂的临床应用、作用机制、适应症、用法用量、不良反应、药物相互作用等方面进行全面深入的探讨,以期为广大临床医生提供有益的参考和借鉴。
本文也期望能够促进内酰胺类抗生素与内酰胺酶抑制剂合剂在临床实践中的合理应用,提高抗生素的治疗效果,降低耐药性的风险,保障患者的用药安全。
二、内酰胺类抗生素概述内酰胺类抗生素,也称为β-内酰胺类抗生素,是一类广泛应用于临床的抗菌药物。
这类药物的主要作用机制是通过抑制细菌细胞壁的合成,从而达到杀菌或抑菌的目的。
β-内酰胺类抗生素主要包括青霉素类、头孢菌素类、碳青霉烯类、单环β-内酰胺类等多个亚类。
自首个内酰胺类抗生素青霉素问世以来,这类药物在感染性疾病的治疗中发挥了重要作用。
随着药物研发的深入,新型的内酰胺类抗生素不断涌现,其抗菌谱更广,对耐药菌的活性更强,不良反应也更少。
然而,随着抗生素的广泛使用,细菌对内酰胺类抗生素的耐药性也逐渐增强,这成为了全球公共卫生面临的一大挑战。
为了应对这一挑战,研究人员在开发新型内酰胺类抗生素的同时,也在探索如何通过联合用药、优化治疗方案等方式,提高内酰胺类抗生素的临床治疗效果。
内酰胺类抗生素酶抑制剂合剂的出现,为解决这一问题提供了新的思路。
酶抑制剂能够抑制细菌产生的β-内酰胺酶,从而保护内酰胺类抗生素免受水解失活,增强抗生素的抗菌活性。
通过合理的合剂组合,可以进一步拓宽内酰胺类抗生素的抗菌谱,提高其对耐药菌的治疗效果。
因此,对于内酰胺类抗生素及其酶抑制剂合剂的临床应用,需要制定科学、规范的专家共识,以指导临床医师合理、有效地使用这些药物,提高治疗效果,减少耐药性的发生,保障患者的用药安全。
详解β-内酰胺类抗生素和β-内酰胺酶抑制剂

详解B—内酰胺类抗生素和B—内酰胺酶抑制剂一、B-内酰胺类抗生素内酰胺类抗生素系指化学结构式中具有内酰胺环的一大类抗生素,包括青霉素类、头孢菌素类、头霉素类、单环内酰胺类及其他典型内酰胺类抗生素。
此类抗生素具有抗菌活性强、毒性低、临床疗效好的优点。
侧链的改变形成许多不同抗菌谱和抗菌作用以及各种临床药理学特性的抗生素。
(一) 青霉素类抗生素青霉素类抗生素是一类重要的内酰胺类抗生素。
这类抗生素可由发酵液提取或半合成制成。
临床常用的青霉素有以下几类:1 .青霉素(青霉素G ,penicillin G 亦称苄青霉素benzylpenicilli )。
2.苯氧青霉系( phenoxy lpenicillins )包括青霉素V (penicillinV ,phenoxymethylpencillin )、非奈西林( phonethicillin ,phenoxyethylpenicillin )、芬贝西林( phenbenicillin ,phenoxybenzylpenicillin )、丙匹西林(propicillin ,phenoxypropy ,lpenicillin )等。
本组青霉素不宜用于严重感染。
3.耐酶青霉素耐酶青霉素经半合成制取,具有抵抗金黄色葡萄球菌内酰胺的能力,常用的青霉素有甲氨西林( methicillin )、苯唑西林( oxacillin )、邻氯青霉素( cloxacillin ) (邻氯青霉素又称氯唑青霉素钠,氯唑西林钠) ,另外还有双氯青霉素,乙氯青霉素等。
本类青霉素应限用于治疗产青霉素酶的金葡菌和凝固酶阴性的葡萄球菌感染,包括败血症,心内膜炎,肺炎等,也可作为术后预防葡萄球菌感染用。
4 .广谱青霉素广谱青霉素包括:氨苄西林(ampicillin 安比西林)、匹氨西林(pivampicillin )、美坦西林( metampicillin )、酞氨西林( talam picillin )、巴氨西林( baca mpicillin )、海他西林( hlacillin )。
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)
β-酰胺类抗生素β酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对β-酰胺类抗生素耐药的最重要机制是产生各种β-酰胺酶。
β-酰胺酶抑制剂能够抑制部分β-酰胺酶,避免β-酰胺类抗生素被水解而失活。
因此,β-酰胺类抗生素/β-酰胺酶抑制剂复方制剂(简称β-酰胺酶抑制剂复方制剂)是临床治疗产β-酰胺酶细菌感染的重要选择。
我国临床使用的β-酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-酰胺酶及产酶菌流行情况β-酰胺酶是由细菌产生的,能水解β-酰胺类抗生素的一大类酶。
β-酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将β-酰胺酶分为青霉素酶、广谱酶、超广谱β-酰胺酶(ESBLs)、头孢菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据β-酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler 分类法),将β-酰胺酶分为丝氨酸酶(包括A类、C类酶和D类酶)及金属酶(B类酶)。
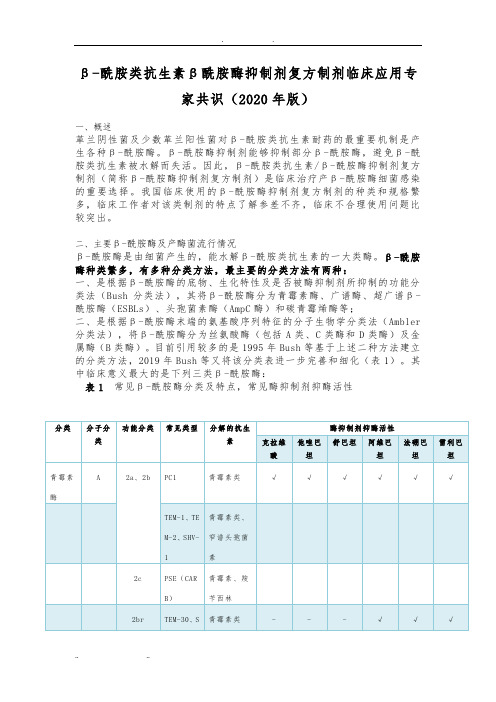
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-酰胺酶:表1 常见β-酰胺酶分类及特点,常见酶抑制剂抑酶活性素及单环酰胺类等β-酰胺类抗生素的β-酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M 型、OXA型和其他型共5大类型。
2、AmpC酶属C类酶,通常由染色体介导,可以被β-酰胺类抗生素诱导。
部分由质粒介导,常呈持续高水平表达。
其对第一、二、三代头孢菌素水解能力强,但对碳青霉烯类抗生素和第四代头孢菌素的水解能力弱。
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020版)

β-内酰胺类抗生素β 内酰胺酶抑制剂复方制剂临床应用专家共识( 2020 年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法( Bush 分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶( ESBLs)、头孢菌素酶( AmpC 酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler 分类法),将β-内酰胺酶分为丝氨酸酶(包括 A 类、C 类酶和D 类酶)及金属酶( B 类酶)。
目前引用较多的是 1995 年 Bush 等基于上述二种方法建立的分类方法,2019 年Bush 等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表 1 常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性1、ESBLs 主要属 2be\2br\2ber 类酶,是由质粒介导的能水解青霉素类、头孢菌素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs 主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs 可分为 TEM 型、SHV 型、CTX-M 型、OXA 型和其他型共 5 大类型。
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)

β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶(ESBLs)、头孢菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler分类法),将β-内酰胺酶分为丝氨酸酶(包括A类、C类酶和D 类酶)及金属酶(B类酶)。
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表1 常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性1、ESBLs主要属2be\2br\2ber类酶,是由质粒介导的能水解青霉素类、头孢菌素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M型、OXA型和其他型共5大类型。
2、AmpC酶属C类酶,通常由染色体介导,可以被β-内酰胺类抗生素诱导。
β-内酰胺酶抑制剂复合制剂

革兰阳性菌
• 氨苄西林/舒巴坦 • 阿莫西林/克拉维酸 • 替卡西林/克拉维酸 • 头孢哌酮/舒巴坦 • 哌拉西林/他唑巴坦 • 头孢他啶/阿维巴坦 • 头孢洛扎/他唑巴坦 • 美罗培南/法硼巴坦
常用的β-内酰胺酶抑制剂复方制剂抗菌谱
来源于2020年 β-内酰胺酶类抗生素/β-内酰胺酶抑制剂复方制剂专家共识
头孢菌素类:轻度炎性脑膜的透过性很低, 严重炎性脑膜炎时约15%穿透性。
美罗培南: 轻度炎性4.7%~25%; 严重脑膜炎的透过率39%
粒缺伴发热
由于免疫力明显下降,发热可能是感染的唯一征象。
容易发展为感染性休克,威胁生命安全。
中性粒细胞缺乏伴发热: 口腔温度>38.3℃ 或者 2 小时内连续两次体温>38.0℃ 且中性粒细胞绝对计数(absolute neutrophil count, ANC)<0.5×109/L 或预计降至 0.5×109/L 以下
大肠埃希菌(30%~50%)
肠球菌属、克雷伯菌属、变形杆 菌属细菌、铜绿假单胞菌
急性单纯性下尿路感染 口服阿莫西林/克拉维酸
急性上尿路感染建议静脉给药: 轻度:阿莫西林/克拉维酸、氨苄西林/舒巴坦
中重度:哌拉西林/他唑巴坦、头孢哌酮/舒巴坦
舒巴坦本身对鲍曼不动杆菌有很好的抗菌活性
常见临床感染部位—中枢神经系统
粒缺伴发热
根据危险分层和耐药危险 因素评估后,尽快使用抗 菌药物初始经验性治疗。
其原则是覆盖可迅速引起 严重并发症或威胁生命的 最常见和毒力较强的病原 菌。
同时必须考虑本区域、本 院及本科室感染的流行病 学覆盖耐药菌,直至获得 准确4年-2019年血流感染的耐药菌检出率
复杂性腹腔感染、院内获得性腹腔感染:多是革兰阳性菌与革兰阴性菌混合感染。 腹腔感染若存在积脓或病灶,应积极进行脓液引流或外科干预祛除感染灶。
β-内酰胺类抗生素

精选ppt
6
学习要求
掌握常用青霉素类药物的药理作用、临床应 用、不良反应及抢救措施
熟悉β-内酰胺类抗生素的共同结构特点
了解β-内酰胺类抗生素的分类,青霉素过 敏反应、β-内酰胺类抗生素交叉过敏的物 质基础
发现青霉素的历史
1928年 Fleming 发现
1942年 Chain 等合成
Fleming, Chain and Flory获1945年诺贝尔生理学和医学奖学金
精选ppt
27
历史
阶段
阶段
阶段
阶段
一
二
三
四
1948年意 大利科学家 从萨丁岛的 排水沟中的 顶头孢菌中 获得一些分 泌物
能抵抗伤 寒杆菌导 致的伤寒
牛津大学 成功提炼 出对β内 酰胺酶稳 定的头孢 菌素C
证实核心 基团是7氨基头孢 烯酸(7ACA)
阶段 五
1964年礼 来公司发 布头孢噻 吩
头孢菌素类(Cephalosporins)
天然青霉素(Natural Penicillins)
耐药 性
01 PBPs的结构的差异或改变形 成低抗生素亲和力分子
细菌产生β-内酰胺酶(β02 lactamase, G+菌产生大量青
霉素酶)
G-菌的外膜或孔蛋白阻止大 03 分子及水溶性差的药物通过
天然青霉素的抗菌谱(spectram)
勾端螺旋体、 苍白密螺旋体、 回归热螺旋体
根据稠和环 的不同分为
青霉素类(Penicillins) 头孢菌素类(Cephalosporins) 碳青霉烯类(Carbapenems) 单环β-内酰胺类(Monobactams)
精选ppt
5
青霉素类抗生素(Penicillins)
β-内酰胺酶抑制剂复合剂的临床应用及配比的科学性

没有 的, 比克拉维酸稳定且不会产生诱导酶 , 比舒 巴坦的抑酶 它 它
作 用强 , 对 B类 及 大部 分 C类 抑 制 作用 弱 。 B一内酰胺 类 抗 生 但 与
B一内酰 胺 类 抗 生 素 是 目前 临 床 膻 用 广 泛 、 效 较 好 的 一类 抗 疗 生 素 , 其 细 菌 耐药 性 已成 为 一 个 严 重 问 题 。 菌 耐 药 机 制之 一 是 但 细 通 过 产 酶 来 破 坏 B一内酰 胺 环 使 之 失 去 抑 菌 活 性 , 决 巾 药 性 的 解 讨 途 径 之 一 是 将 p一内酰 胺 类 抗 牛 素 jp一内酰 胺 酶 抑 制 剂 组 合 成 复 合 剂 . 而 提 高 其 临 床 疗 效 。 就 B一内 酰胺 酶抑 制剂 搜 其 复 合 从 现 剂 的 临床 应 用 、 合 剂 配 比 的科 学性 作 慨 述 。 复
维普资讯
综 述报告
20 年第 1 卷第7 08 7 期
B一内酰胺酶抑制剂复合剂 的临床应用及配 比的科学性
许恒 忠
( 山东 省聊城 市 第二 人 民医院 , 山东 临清 2 2 0 ) 5 6 1
摘要 : 目的 介 绍 B一内酰 胺 酶  ̄ - 利 、 r, e 复合 剂的 临 床 应 用 , 合 剂 配 比方 面 的 研 究进展 法 对 近 年 来 的 有 关 文献 进 行 分析 、 纳 。 果 J 复 方 归 结 B一 内酰 胺 类 抗 生 素 与 B一内酰 胺 酶 抑 制 剂联 合 使 用是 减 少 p一内酰 胺 类 抗 生 素 产 生 耐 药性 的 有 效 方 法 : 论 p一内酰 胺 酶 抑 制 剂复 合 结
β-内酰胺类β-内酰胺酶抑制剂合剂临床应用专家共识

有:
①阿莫西林/克拉维酸;②替卡西林/克拉维酸; ③氨苄西林/舒巴坦;④头孢哌酮/舒巴坦; ⑤哌拉西林/他唑巴坦。
其共同的特点
①除舒巴坦合剂对不动杆菌属抗菌活性增强,其他β-内酰胺酶 抑制剂仅具有微弱的抗菌作用;②β-内酰胺酶抑制剂对多数质 粒介导的和部分染色体介导的β-内酰胺酶有较强的抑制作用, 与阿莫西林,氨苄西林,哌拉西林,替卡西林,头孢哌酮等联 合后可保护该类抗生素不被细菌产生的灭活酶水解;③β-内酰 胺酶抑制剂不增强与其配伍药物对敏感细菌或非产β-内酰胺酶 的耐药细菌的抗菌活性;④β-内酰胺酶抑制剂合剂的抗菌作用 主要取决于其中β-内酰胺类药物的抗菌谱和抗菌活性;⑤β-内 酰胺酶抑制剂合剂中两药的药代动力学性质相近,具协同抗菌 作用;⑥两药联合应用后不良反应无明显增加
均可达40%以上.
3 头孢哌酮钠/舒巴坦钠
头孢哌酮/舒巴坦的PK/PD特点是时间依赖性药物并且半衰期较短。头孢 哌酮钠/舒巴坦钠3g,q8h给药对铜绿假单胞菌T〉MIC%可达82%以上。头 孢哌酮/舒巴坦3.0g q8h静脉滴注治疗多重耐药鲍曼不动杆菌HAP,头孢 哌酮对泛耐药鲍曼不动杆菌MIC小于48,且T〉MIC%大于100%时,可以 获得较好的临床和微生物学疗效,鲍曼不动杆菌全被清除,可作为临床应 用的推荐方案。
合制剂的特性,目前我国使用种类多,规格不一, 美国抗菌药物使用率20%,我国60%。半衰期:头孢曲 松在人体6小时,舒巴坦、他唑巴坦、克拉维酸约1H。
β-内酰胺酶抑制剂合剂的组成原则
组方配比原则:
β-内酰胺类抗生素与β-内酰胺酶抑制剂组成复合制剂必须考虑组方 和配比的合理性。基本组成原则如下:
β内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识及相关医保政策解读

<10/5.7~8.2
80~90/85
头孢洛扎 / 他唑巴坦*(患者)
1/0.5, iv 1 h
65.7/17.8
3~4/2~3
16~21/30
>95/>80
2/1, iv 1 h
105/26.4
美罗培南 / 法硼巴坦*
2/2, iv 3 h
43.4/55.6
1.22/1.68
2/33
2020 专家共识总结近五年产酶 (ESBLs) 菌的流行情况:
有所升高
近五年产ESBLs大肠埃希菌检出率居高不下, 产ESBL肺炎克雷伯菌检出率有所上升1-2
近五年肺炎克雷伯菌、铜绿假单胞菌和鲍曼不动杆菌对碳青霉素类抗生素耐药率均有不同程度地升高
76.5%为KPC-2
2020 专家共识总结近五年产酶 (碳青霉烯) 菌的流行
检测方法
适用的菌株
区分的碳青霉烯表型
Carba NP
肠杆菌科、铜绿假单胞菌和不动杆菌属细菌
对KPC、NDM、VIM、SPM 和 SME 型敏感性和特异性好
eCIM联合mCIM
肠杆菌科细菌
区分产丝氨酸碳青霉烯酶还是金属酶
eCIM联合酶抑制剂(硼酸、EDTA)试验
β‐内酰胺酶分类及产酶菌流行情况及检测
1/1
28/38
75~85/75~85
哌拉西林 / 他唑巴坦
4/0.5, iv
298/34
0.7~1.2/0.7~1.2
30/30
68/80
替卡西林 / 克拉维酸2
3/0.1, iv
324/8.0
1.1/1.1
45/25
60~70/35~45
β-内酰胺酶抑制剂的临床选择

他唑巴坦、舒巴坦、克拉维酸的区别
β-内酰胺酶抑制剂复方制剂
• 临床常用的β-内酰胺酶抑制剂复方制剂主要有: • 哌拉西林他唑巴坦 • 氨苄西林舒巴坦 • 阿莫西林克拉维酸
三种β-内酰胺酶抑制剂的抗菌谱
三种β-内酰胺酶抑制剂的抗菌谱
• 氨苄西林舒巴坦、阿莫西林克拉维酸对肠杆菌科细菌 抗菌活性总体不如哌拉西林他唑巴坦。
• 氨苄西林舒巴坦、阿莫西林克拉维酸可经验性用于革 兰阳性菌感染的治疗,对链球菌、甲氧西林敏感金黄 色葡萄球菌、肠球菌有一定抗菌活性。
三种β-内酰胺酶抑制剂的抗菌谱
• 哌拉西林他唑巴坦不作为单纯革兰阳性菌感染的治疗 药物。
• 氨苄西林舒巴坦对肠球菌效果更强,但对肠杆菌属无 效。
• 哌拉西林他唑巴坦对铜绿假单胞菌效果更强,那两者 均无作用。
β-内酰胺酶抑制剂的临床选择
概述
• 临床上常用的β-内酰胺酶抑制剂主要有: • 克拉维酸 • 舒巴坦 • 他唑巴坦
• β-内酰胺酶抑制剂其结构与β-内酰胺类抗生素相似 ,本身仅有很弱的抗菌作用,但与β-内酰胺类抗生素 联合应用可增强抗菌作用。
他唑巴坦、舒巴坦、克拉维酸
• 三者均具有β-内酰胺结构,与β-内酰胺酶形成稳定 而且不可逆的竞争性结合,抑制其对β-内酰胺类抗生 素的水解作用,从而提高了青霉素类和头孢菌素类抗 生素对产酶菌株的敏感性。
演示完毕,感谢聆听。
三种β-内酰胺酶抑制剂的抗菌谱
• 三者药物对嗜麦芽窄食单胞菌均无作用。 • 氨苄西林舒巴坦对不动杆菌作用强于哌拉西林他唑巴
坦,阿莫西林克拉维酸无作用。
三种β-内酰胺酶抑制剂的药代动力学
常见呼吸道感染的药物选择
常见呼剂应用时的注意事项
兽用β-内酰胺类抗生素的规范使用 (1)

β-内酰胺类抗生素是指化学结构中具有β-内酰胺环的一大类抗生素,包括临床最常用的青霉素、头孢菌素、β-内酰胺酶抑制剂。
此类抗生素具有杀菌活性强、毒性低、适应症广及临床疗效好的优点。
要规范使用抗生素,尽量减量使用,直至不用。
一、青霉素类(一)青霉素G青霉素钾、钠由青霉菌等的培养液中分离而得,是青霉素G(一种不稳定的有机酸)与金属钠、钾离子结合而成的盐。
1.作用与应用。
常作为治疗革兰氏阳性和阴性球菌、革兰氏阳性杆菌、放线菌、螺旋体等感染的首选药。
对青霉素敏感的病原菌有链球菌、葡萄球菌、肺炎球菌、脑膜炎球菌、丹毒杆菌、化脓棒状杆菌、炭疽杆菌、破伤风梭菌、李氏杆菌、产气荚膜梭菌、牛放线杆菌和钩端螺旋体等。
大多数革兰氏阴性杆菌、支原体对青霉素不敏感;对结核分枝杆菌、病毒、立克次氏体完全无作用;抗菌作用不受脓血及组织分解产物影响;仅对繁殖期细菌有作用,而对静止期无作用;哺乳动物细胞无细胞壁,故对动物毒性小。
主要用于青霉素敏感菌所引起的各种感染。
(1)革兰氏阳性球菌,如链球菌、葡萄球菌、乳房炎(每个乳室10万单位灌注)、子宫内膜炎、化脓性腹膜炎、猪淋巴脓肿、关节腔内注入治疗关节炎和创伤感染;(2)革兰氏阳性杆菌:炭疽、猪丹毒、放线菌、肾盂肾炎、膀胱炎、恶性水肿等,钩端螺旋体病,梅毒螺旋体病等;(3)还可内服用于治疗禽巴氏杆菌病及鸡球虫病并发的肠道梭菌感染。
治疗破伤风时宜与破伤风抗毒素合用。
2.用法与用量。
注射用青霉素G钾(钠)临用前加灭菌注射用水适量使溶解,肌内注射。
马、牛1万~2万单位/kg体重,羊、猪、驹、犊2万~3万单位/kg体重,犬、猫3万~4万单位/kg体重,禽5万单位/kg体重,2~3次/d,严重感染时可每4~6h一次。
乳管内注入,牛每次每乳室10万单位,1~2次/d。
3.注意事项。
(1)青霉素G钠(钾)易溶于水,在水中β-内酰胺环易裂解为无活性的青霉酸和青霉噻唑酸,后者降低水溶液的pH,进一步加强青霉素水解,水解率随温度升高而加速。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
3-内酰胺类抗生素B内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对3 -内酰胺类抗生素耐药的最重要机制是产生各种3 -内酰胺酶。
3 -内酰胺酶抑制剂能够抑制部分3 -内酰胺酶,避免3 -内酰胺类抗生素被水解而失活。
因此,3 -内酰胺类抗生素/ 3-内酰胺酶抑制剂复方制剂(简称3 -内酰胺酶抑制剂复方制剂)是临床治疗产3 -内酰胺酶细菌感染的重要选择。
我国临床使用的3 -内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要3-内酰胺酶及产酶菌流行情况3-内酰胺酶是由细菌产生的,能水解3 -内酰胺类抗生素的一大类酶。
3-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据3 -内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将3 -内酰胺酶分为青霉素酶、广谱酶、超广谱3-内酰胺酶(ESBLs)、头抱菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据3-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler分类法),将3 -内酰胺酶分为丝氨酸酶(包括A类、C类酶和D类酶)及金属酶(B类酶)。
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类3 -内酰胺酶:表1常见B-内酰胺酶分类及特点,常见酶抑制剂抑酶活性1、E SBLs主要属2be\2br\2ber 类酶,是由质粒介导的能水解青霉素类、头抱菌素及单环酰胺类等B -内酰胺类抗生素的B -内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M型、OXA型和其他型共5大类型。
2、A mpC酶属C类酶,通常由染色体介导,可以被B -内酰胺类抗生素诱导。
部分由质粒介导,常呈持续高水平表达。
其对第一、二、三代头抱菌素水解能力强,但对碳青霉烯类抗生素和第四代头抱菌素的水解能力弱。
该酶主要存在于肠杆菌属、柠檬酸杆菌属、普鲁菲登菌属、黏质沙雷菌属和摩根菌属等细菌,非发酵菌中主要见于铜绿假单胞菌。
质粒介导的B -内酰胺酶可分为CMY-2组、CMY-1组、MIR-1/ACT-1 组、DHA-1 组和ACC-1 组等。
3、碳青霉烯酶是指能水解碳青霉烯类抗生素的一大类B -内酰胺酶,分别属于Ambler分子分类中的A类、B类和D类酶。
A类、D类为丝氨酸酶,B类为金属酶,以锌离子为活性中心。
A 类碳青霉烯酶可由染色体介导,也可由质粒介导。
前者包括SME、NMC 和IMI 酶等,后者包括KPC 和GES 酶等。
KPC 酶是近年来肠杆菌科细菌尤其是肺炎克雷伯菌对包括碳青霉烯类抗生素在内的几乎所有B -内酰胺类抗生素耐药的最主要机制,我国最常见的是KPC-2 ,其对头孢吡肟和头孢他啶的水解能力相对较弱。
A 类碳青霉烯酶可被新型酶抑制剂阿维巴坦、雷利巴坦和法硼巴坦抑制,部分被克拉维酸所抑制,但不被乙二胺四乙酸(EDTA)所抑制。
D类碳青霉烯酶(OXA 酶),对苯唑西林水解活性强,主要见于不动杆菌属细菌。
包括OXA-23 、OXA-24/OXA-40 、OXA-48 、OXA-58 和OXA-51 酶等。
目前临床应用的酶抑制剂对其没有很好的抑制作用(除OXA-48 可被阿维巴坦抑制外),不同OXA 酶对碳青霉烯类抗生素水解活性不相同,B -内酰胺酶抑制剂的抑酶活性也不同。
B 类碳青霉烯酶(金属酶)能灭活青霉素类、头孢菌素类、碳青霉烯类抗生素,但对氨曲南水解活性弱,不能被B -内酰胺酶抑制剂所抑制,可被EDTA或巯基类化合物抑制。
常见于铜绿假单胞菌、不动杆菌属细菌和肠杆菌科细菌,包括IMP、VIM 、GIM 、SPM、SIM、NDM 酶等。
中国细菌耐药监测网(CHINET )数据显示(自2016年以来没有常规检测ESBLs, 以头抱噻肟耐药的数据替代),2018年我国产ESBLs大肠埃希菌检出率为61.8%,与2013年的61.0%持平。
大肠埃希菌所产ESBLs基因型90%以上为CTX-M型,但各地区CTX-M的基因亚型分布不一。
肺炎克雷伯菌产生的ESBLs基因型也以CTX-M型为主。
据2018年CHINET数据显示,我国各地区肺炎克雷伯菌的ESBLs检出率为52.9%,较2013年的43.6%检出率有所上升。
2018年CHINET数据显示,肠杆菌科细菌对碳青霉烯类抗生素的耐药率达到11.8%,其中肺炎克雷伯菌对碳青霉烯类抗生素耐药已达到26.3%,主要是产KPC型碳青霉烯酶(KPC酶),绝大多数为KPC-2(76.5% ),在大肠埃希菌、肺炎克雷伯菌,黏质沙雷菌、奇异变形杆菌等肠杆菌科细菌中均有发现,流行地区包括浙江、上海、江苏、湖南、北京、山东等省市。
由于产KPC-2的菌株常常同时产ESBLs和(或)AmpC酶,甚至同时合并有外膜蛋白缺失,常表现为广泛耐药或全耐药。
大肠埃希菌对碳青霉烯类抗生素的耐药率约为2%,主要由NDM 介导(52.1% ),其中NDM-5 (52.1% )、NDM-1 (18.4% )为最主要的NDM亚型。
CHINET近5年的监测数据显示,我国碳青霉烯类抗生素耐药鲍曼不动杆菌检出率从2013年的62.8%上升至2018年的78.1% , OXA-23是介导鲍曼不动杆菌对碳青霉烯类抗生素耐药的最主要机制。
碳青霉烯类抗生素耐药铜绿假单胞菌检出率从2013年的27.1%上升至2018年的30.1%,产金属B-内酰胺酶是铜绿假单胞菌最主要的耐药机制。
三、三种主要B-内酰胺酶的检测根据B-内酰胺酶的水解底物、水解活性及酶抑制剂的抑酶活性差异,建立了多种B -内酰胺酶表型检测方法,其对临床合理选用抗菌药物有重要的参考价值,但其检测结果易受多种因素的影响,必要时可采用分子生物学技术进一步确认酶的类型1、ESBLs的检测:通常采用美国临床与实验室标准化研究所(CLSI)推荐的ESBLs初筛和表型确证试验,适用于肺炎克雷伯菌、大肠埃希菌、产酸克雷伯菌和奇异变形杆菌,头抱他啶或头抱噻肟,联合克拉维酸后抑菌圈直径扩大 5 mm或最低抑菌浓度(MIC )下降8倍及以上,判断为ESBLs阳性。
CLSI建议采用新折点的B -内酰胺类抗生素,不再需要将ESBLs阳性菌株对头抱菌素类、单环酰胺类的氨曲南和青霉素类抗生素的敏感结果修正为耐药。
目前ESBLs检测仅用于流行病学或院感监测。
对头抱尼西、头抱孟多、头抱哌酮等折点没有进行评估的B -内酰胺类抗生素,如ESBLs阳性,应报告为耐药。
ESBLs 检测还可采用三维试验、Etest ESBLs条和自动化仪器等。
2、AmpC酶的检测:微生物室没有常规开展AmpC酶的检测,药敏表型为:三代头抱菌素(头抱他啶、头抱噻肟)和头霉素类(头抱西丁MIC>8 他/ml )耐药、头抱吡肟敏感的菌株,提示去阻遏表达AmpC酶或质粒型AmpC酶,但ACC-1型质粒介导的AmpC酶不水解头抱西丁。
同时根据ApmC酶活性能被氯唑西林和硼酸抑制的特点,可表型筛选AmpC酶。
头抱西丁三维试验是检测AmpC酶的经典方法。
质粒型AmpC酶还可以用PCR等分子生物学技术确认。
3、碳青霉烯酶的检测:CLSI推荐碳青霉烯酶表型检测方法主要有:Carba NP 试验、改良碳青霉烯灭活试验(mCIM )、EDTA协同碳青霉烯灭活试验(eCIM )。
Carba NP可用于肠杆菌科、铜绿假单胞菌和不动杆菌属细菌碳青霉烯酶的表型检测,对KPC、NDM、VIM、SPM和SME型碳青霉烯酶具有较好的敏感性和特异性,对OXA-48型碳青霉烯酶敏感性低;mCIM试验用于肠杆菌科和铜绿假单胞菌碳青霉烯酶的表型检测;eCIM 与mCIM 联合用于区分产碳青霉烯酶肠杆菌科细菌是产丝氨酸碳青霉烯酶还是金属B -内酰胺酶。
也可联合酶抑制剂(硼酸、EDTA )试验区分肠杆菌科细菌中的丝氨酸碳青霉烯酶和金属B-内酰胺酶。
目前已有多种商品化的分子生物学技术如Xpert Carba-R 用于快速检测常见的碳青霉烯酶基因型包括KPC、NDM 、OXA-48 、IMP 、VIM四、主要B-内酰胺酶抑制剂B -内酰胺酶抑制剂能抑制细菌产生的部分B -内酰胺酶,常与B-内酰胺类抗生素联合使用,能使B-内酰胺环免遭水解,保护B-内酰胺类抗生素的抗菌活性。
临床上常用的B -内酰胺酶抑制剂主要有:克拉维酸、舒巴坦、他唑巴坦、阿维巴坦、雷利巴坦、法硼巴坦。
前三者均含有B -内酰胺环结构,为不可逆竞争性抑制剂,能抑制除碳青霉烯酶外的大部分A类B-内酰胺酶,但对B、C、 D 类酶的绝大多数没有抑制能力。
阿维巴坦和雷利巴坦是属于三乙烯二胺类(DABCOs)的酶抑制剂,不具有B - 内酰胺酶结构,因此不易被水解,具有更加广谱的B -内酰胺酶抑制作用和可逆的抑酶效果,能够抑制包括碳青霉烯酶在内的A类、C类B-内酰胺酶。
阿维巴坦还对 D 类酶中的OXA-48 具有抑制作用,但是雷利巴坦无法抑制OXA-48 。
法硼巴坦是属于硼酸复合物的新一代酶抑制剂,能够抑制包括碳青霉烯酶在内的 A 类、C类B-内酰胺酶,但对包括OXA-48在内的D类碳青霉烯酶无抑制作用。
B -内酰胺酶抑制剂的出现很大程度上解决了B -内酰胺类抗生素的耐药问题(表 1 )。
五、禺内酰胺酶抑制剂复方制剂的组成原则1、B-内酰胺酶抑制剂复方制剂必须考虑组方和配比的合理性。
基本组成原则如下:(1 )B-内酰胺类抗生素本身在临床治疗中的地位,细菌对其耐药性增长严重影响了其单独使用的疗效,细菌产生耐药的主要机制是产B -内酰胺酶,组方中B -内酰胺酶抑制剂可有效抑制该B -内酰胺酶,组合后恢复B -内酰胺类抗生素对产B -内酰胺酶细菌的抗菌活性。
(2 )B-内酰胺酶抑制剂具有或不具有抗菌活性,但需阐明B -内酰胺酶抑制剂对不同B -内酰胺酶有不同抑制活性,其抑酶谱及保护B -内酰胺类抗生素不被细菌产生的灭活酶水解的强度。
(3)B-内酰胺类抗生素和酶抑制剂均需适当剂量。
在已上市的B -内酰胺类抗生素/ B-内酰胺酶抑制剂复方制剂基础上增加新配比的品种,必须有充足依据说明现有配比不能完全满足临床需要,临床前和临床研究结果证明新配比合剂与已上市配比合剂相比,在有效性或安全性上具有临床价值的明显优势和(或)新配比合剂有特殊适应证范围等。
(4)B-内酰胺类抗生素与B -内酰胺酶抑制剂的药代动力学特征基本吻合,如消除半衰期相近和分布相似,两者在体内的有效浓度能共同维持足够的作用时间,以发挥更好的协同杀菌效果(5)B-内酰胺类抗生素与B -内酰胺酶抑制剂药动学/药效学(PK/PD )特性,包括组合后B -内酰胺类抗生素预测其体内疗效和达到抑菌和杀菌获得的最佳PK/PD指数,以及B -内酰胺酶抑制剂高于域值(抑制B -内酰胺酶活性最低浓度)时间占给药间隔百分率(%T>CT )。
