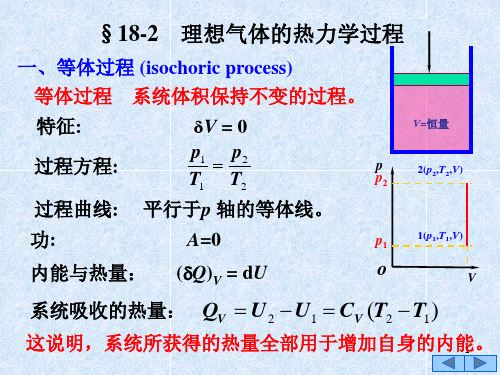
13-3理想气体的等体过程和等压过程
理想气体的热力学过程
6
dV d p 0 V p
式中
Cp CV
, 在温度变化不很大时,可以看作常量。
将上式积分,得
ln V + ln p = 恒量
pV γ 恒量 或 这个关系称为泊松 (S.D.Poisson)公式。
根据泊松公式和理想气体物态方程, 可以分别得到
TV γ 1 恒量
T γ pγ 1 恒量
Qp = H 气 H水
= (2676.3103 419.06103 ) Jkg1
= 2257.2103 Jkg1
16
17
经绝热过程压缩气体做的功:
CV 20.44J mol K
1
1
m 4 A CV T2 T1 4.70 10 J M
在等压过程中,系统从外界获得的热量,一部分用 以增大内能,一部分用以对外作功。 三、等温过程 (isothermal process) 等温过程 特征: 过程方程: 系统的温度保持恒定的过程。 T=0
p1V1 p2V2
p p1
T=恒量
恒温热源
1(p1,V1,T)
过程曲线:
内能增量:
等温线为等轴双曲线。
=1.40,可得:
p2 T2 T1 p 1
1 /
1 300 50
0.286
98.0K
19
例6 一定质量的理想气体先后经历 P 两个绝热过程即1态到2态,3态到4
态(如图所示)且T1=T3、T2=T4,在 1态与3态,2态与4态之间可分别连 接 两 条 等 温 线 。 求 证 :
考虑到 T1=T3,T2=T4,
T2 V1 1 2 T1 V2
理想气体等容过程定容摩尔热容理想气体等压过程定

V2 V
E1
W
E2
绝热压缩
p
p2
2( p2,V2,T2)
p1
o V2
( p1,V1,T1)
W1 V1 V
E2
E1
W
三 绝热线和等温线
p
T 常量
Q0
pA papT A C
B
o VA V VB V
绝热线的斜率大于 等温线的斜率.
绝热过程曲线的斜率
pV 常量
pV 1dV V dp 0
( dp dV
与外界无热量交换的过程
特征 dQ O
p
p1
1( p1,V1,T1)
热一律 dW dE 0
dW dE
p2
( p2,V2,T2 )
2
dE
m M
CV ,mdT
W
V2 V1
pdV
T2 T1
m M
CV
,m
dT
mo V1 dV V2 V
绝热的汽缸壁和活塞
由热力学第一定律有
W E
CV ,mdT
分离变量得 dV CV ,m dT
V
RT
dV V
1 dT 1 T
p
p1
1( p1,V1,T1)
Q0
p2
o V1
( p2,V2,T2 ) 2
V2 V
绝 V 1T 常量
热 方
pV
常量
程 p 1T 常量
绝热膨胀
p
p1
1( p1,V1,T1)
p2
( p2,V2,T2 )
W2
o V1
W
m M
CV ,m (T1
T2 )
若已知 p1,V1, p2 ,V2 及
物理课件4.4理想气体的等体过程和等压过程

特点上的比较
比较:等体过程气体体积不变,等 压过程气体压力不变
添加标题
添加标题
添加标题
添加标题
等压过程:气体压力不变,体积可 以变化
结论:等体过程和等压过程在特点 上有明显区别
理想气体等体过程和等 压过程的实例分析
等体过程的实例分析
等体过程的概念和特点 等体过程的实例:水银柱的升降实验 等体过程中气体状态的变化 等体过程在日常生活中的应用
07 理想气体等体过程和 等压过程的应用前景
添加章节标题
理想气体等体过程的定 义和特点
Байду номын сангаас
等体过程的定义
等体过程是指气体 体积不变的过程
温度是理想气体内 能变化的量度
等体过程中,气体 吸收的热量全部转 化为内能
等体过程中,气体 的状态参量如压强 和温度随时间发生 变化
体积不变:等体过程中气体的体积 始终保持不变。
实验验证的结果分析和讨论
实验数据整理:对实验数据进行整理,包括实验数据表格和图表 结果分析:对实验结果进行分析,包括数据变化趋势、误差分析等
讨论:对实验结果进行讨论,包括理想气体等体过程和等压过程的原理、影响因素等
结论:总结实验验证的结果,得出结论
理想气体等体过程和等 压过程的应用前景
在物理学中的应用前景
在航天工程中,理想气体等体过程和等压过程可以用来 研究航天器内部的热环境,对于航天器的设计和运行具 有重要意义。
在能源工程中,理想气体等体过程和等压过程可以用来 研究热能转换和传输过程中的效率和优化,对于提高能 源利用效率和减少能源浪费具有重要意义。
在工程和技术领域的应用前景
能源领域:利用理想气体等体和等压过程的理论,可以优化能源转换和储存效率,提高能源利用效 率。
理想气体的等体过程和等压过程

CV ,m
dQV dT
dQV CV ,mdT
单位 J mol1 K1
3
mol 理想气体
CV ,m
dQV dT
dQV dE CV ,mdT
由热力学第一定律
QV CV ,m (T2 T1) E2 E1
4
p
等 p2
体
升 压
p1
o
2 ( p2,V ,T2 )
1 ( p1,V ,T1)
V
V
摩尔热容比
Cp,m CV ,m
8
三个量:
W p(V2 V1) R(T2 T1) Qp C p,m (T2 T1)
E2 E1 CV ,m (T2 T1)
9
p
等 p ( p,V1,T1) ( p,V2,T2)
压
1
2
膨
W
胀 o V1
V2 V
Qp
E2
E1
W
p
等 p ( p,V2,T2) ( p,V1,T1)
压2
1
压
W
缩 o V2
V1 V
Qp E1
W
E2
10
四 比热容
热容
C dQ dT
比热容
c dQ C mdT m
11
p
等 p1
体
降 压
p2
o
1( p1,V ,T1)
2( p2,V ,T2 )
V
V
QV
E1
E2
E1
QV
E2
5
二 等压过程 摩尔定压热容
特性 p 常量
过程方程 VT 1 常量 p
功 W p(V2 V1)
p ( p,V1,T1) ( p,V2,T2)
工程热力学第四章理想气体热力过程

03
CHAPTER
等容过程
等容过程是指气体在变化的整个过程中,其容积保持不变的过程。
定义
特点
适用场景
气体在等容过程中,气体温度和压力会发生变化,但容积保持不变。
等容过程常用于高压、高温或低温等极端条件下的气体处理。
03
02
01
等容过程定义
在等容过程中,气体吸收的热量等于气体所做的功和气体温度升高所吸收的热量之和。
多变过程的具体形式取决于气体所经历的压力和温度的变化规律。
多变过程定义热力学第一定律 Nhomakorabea热力学第二定律
理想气体状态方程
热效率
多变过程的热力学计算
01
02
03
04
能量守恒定律,用于计算多变过程中气体吸收或释放的热量。
熵增原理,用于分析多变过程中气体熵的变化。
描述气体压力、体积和温度之间的关系,可用于多变过程的计算。
衡量多变过程能量转换效率的指标,通过比较输入和输出的热量来计算。
提高热效率的方法
优化多变过程参数,如压力和温度的变化规律,以减少不可逆损失和提高能量转换效率。
热效率与熵增的关系
根据熵增原理,不可逆过程会导致熵的增加,从而降低热效率。因此,减少不可逆损失是提高多变过程热效率的关键。
热效率计算公式
$eta = frac{Q_{out}}{Q_{in}}$,其中$Q_{out}$为输出热量,$Q_{in}$为输入热量。
计算公式
通过优化气体的初态和终态,以及选择合适的加热和冷却方式,可以提高等容过程的热效率。同时,也可以通过改进设备结构和操作方式来提高热效率。
提高热效率的方法
等容过程的热效率
04
CHAPTER
大学物理-热力学基础-课件
Wa
CV m (T2
T1)
p1V1 p2V2
1
本题用 Wa E 计算较方便
关键用绝热方程
T2
T1
( V1 V2
)
1
先求出 T2
p
p2
2 T2
T2' T1
Q0
p2'
2'
p1
TC
T1
1
o V2 V2' V1 10 V1 V
18.
*四. 多方过程 — 实际过程( 满足 PV n C)
绝热 n = ( CPm / CVm )
等温 n = 1 等压 n = 0
W p1V1 p2V2 n 1
满足 E CV (T2 T1)
Q Cn (T2 T1)
等体 n = ∞
p
可以证明
n= n=∞
n=1
Cn
(
n
n 1
)CV
n=0
o
V
19.
13 – 5 循环过程 卡诺循环
一. 循环过程
1. 特点 E 0 W = Q ( 热功转换 )
1
2
W
(2)热一定律 dQP dE PdV
o V1
V2 V
QP
E
V2 PdV
V1
v
i 2
R(T2
T1 )
P(V2
V1 )
7.
2.摩尔定压热容 CPm
1mol
:
CPm
dQp dT
理论值:
CPm
dE pdV dT
CVm
R
i2R 2
(近似)
实验值:查表 (精确)
QP
dQP
10 13-3 理想气体的等体过程和等压过程 摩尔热容

PV RT PV RT
C p,m CV ,m R
理想气体的定压摩尔热容比定体摩尔热容大一个恒量R •在等体过程中,气体吸收的热量全部用来增加系统的内能 •等压过程中,气体吸收的热量,一部分用来增加系统的内能, 还有一部分用于气体膨胀时对外界作功 气体升高相同的温度,在等压过程吸收的热量要比在等温过 程中吸收的热量多。
3
水蒸气
m
蒸气 0.598kg m
3
水
100 C 热源
W pdV pV pm(
1
蒸气
1
1
水
1
)
E Q W m L pm(
蒸气
水
)
E 1 1 L p( ) 2.09106 J kg1 m 蒸气 水
四、多方过程
2、比热容:
单位质量的热容称为比热容。
C 1 dQ c m m dT
13-4 理想气体的等温过程和绝热过程
一、等温过程
•特点:
理想气体的温度保持不变, T=const
•过程曲线:
在PV图上是一条双曲线, 叫等温线。
恒 温 热 源 T
•过程方程:
p1V1 p2V2
p p1
p2
1 ( p1 ,V1 , T )
p
T 常量
Q0
papT
13-3理想气体的等体、等压和等温过程

19
物理学
第五版
13- 理想气体的等体、 13-3 理想气体的等体、等压和等温过程 热容 摩尔热容比
γ = Cp,m CV,m
等压过程的三个量
W = p (V2 − V1 ) = ν R (T2 − T1 )
Q p = νC p,m (T2 − T1 )
E2 − E1 =νCV ,m (T2 − T1 )
由热力学第一定律
p2
2
V1
o
dQT = dWT = pdV
dV
V2 V
QT = W T =
∫
V2
V1
pdV
10
第十三章 热力学基础
物理学
第五版
13- 理想气体的等体、 13-3 理想气体的等体、等压和等温过程 热容
QT = WT = ∫ pdV
V1
V2
RT p =ν V
V2
p1V1 = p 2V2
RT V2 QT = W = ∫ ν dV = ν RT ln V1 V V1
p1 = νRT ln p2
第十三章 热力学基础
11
物理学
第五版
13- 理想气体的等体、 13-3 理想气体的等体、等压和等温过程 热容 等温过程热量与功的转换情况 等温膨胀 等温膨胀 等温压缩 等温压缩
p p1
1 ( p1 , V1 , T )
14
第十三章 热力学基础
物理学
第五版
13- 理想气体的等体、 13-3 理想气体的等体、等压和等温过程 热容
(一)摩尔定体热容
d 理想气体,等体过程, 1mol 理想气体,等体过程, QV ,dT 。
CV ,m
∵
13-4理想气体的等温过程和绝热过程

13
物理学
第五版
1313-4 理想气体的等温过程和绝热过程
后为P 例1,一定量的理想气体 1,V1,T1,后为 2,V2, ,一定量的理想气体P T2, 已知 V2>V1, T2=T1 以下说法哪种正确? 以下说法哪种正确? (A)不论经历什么过程,气体对外净作功一定为正值 )不论经历什么过程, (B)不论经历什么过程,气体对外界净吸热一定为正值 )不论经历什么过程, (C)若是等温过程,气体吸的热量最少 )若是等温过程, (D)若不知什么过程,则A,Q的正负无法判断 )若不知什么过程, , 的正负无法判断 [D]
第十三章 热力学基础
14
物理学
第五版
1313-4 理想气体的等温过程和绝热过程 态到b态 例2,一定量的理想气体从 态到 态,这个过程 ,一定量的理想气体从a态到 是什么过程? 是什么过程?
P
b
a
T
(A)绝热压缩(B)等容吸热 )绝热压缩( ) (C)吸热压缩(D)吸热膨胀 )吸热压缩( )
第十三章 热力学基础
γ
E
0
p1V1 p 2V2 γ 1
νcV T
物理学
第五版
1313-4 理想气体的等温过程和绝热过程
P
T
D
A
B
C
T
图中曲线为等 温线.问A, B,C,D状态 时系统的温度 关系.
V
T
PV = νRT
等压过程中,体积越大温度越高;等体过程 中,压强越大温度越大. 在PV图中,等温线上方温度较高,等温线 下方温度较低.
第十三章 热力学基础
8
物理学
第五版
1313-4 理想气体的等温过程和绝热过程
1-理想气体的等体过程和等压过程摩尔热容

2019年10月25日星期五
理学院 物理系
大学物理
§13-3 理想气体的等体过程和等压过程 摩尔热容
4.摩尔热容量C 和热量 Q 的关系 dQ=νCdT
5.摩尔定容热容CV (molar heat capacity at constant volume) (1)CV 和热量的关系 (dQ)V=vCVdT (2)CV 和内能的关系 vCVdT=(dE)V (3)内能 E 和状态 (T, V, P) 的关系
PV RT
P dV RdT
d Q CV dT P dV
d Q CV dT R dT
CV RdT
d Q CP dT
CP CV R
2019年10月25日星期五
理学院 物理系
§13-3 理想气体的等体过程和等压过程 摩尔热容
7.迈耶公式及其物理意义
(1)迈耶公式
CP
CV
R
i 2
R
R
Байду номын сангаас
i 2
1
R
(2)迈耶公式的物理意义
(3)摩尔气体常数R
(4)热容比
CP
i 2
1
R
i2
CV
iR
i
2
2019年10月25日星期五
理学院 物理系
8.7
28.8 20.4
8.4
28.6 20.4
8.2
29.3 21.2
8.1
28.9 21.0
7.9
36.2 27.8
8.4
35.5 27.2
8.4
理想气体的等容过程和等压过程

(理想气体的状态函数)
(4) 各等值过程的特性 .
一 等 容过程 定容摩尔热容
特性 过程方程
V 常量 1 pT 常量
p2
p1
p
( p2 ,V , T2 )
( p1 ,V , T1 )
dV 0 ,
热力学第一定律
dW 0
dQV dE
dQV dT
1
o
V
V
定容摩尔热容: 1mol 理想气体在等容过程中吸 收的热量 dQV ,使温度升高 dT , 其定容摩尔热容为
V
( p1 ,V , T1 )
等 p1 容 降 p 2 压
p
1 ( p1,V , T1 ) 2
( p2 ,V , T2 )
o
V
o
E1
V
V
QV
E1
E2
QV
E2
二 等压过程 定压摩尔热容
特性 过程方程
p 常量
1
p
功
VT 常量 W p(V2 V1 )
dQ p dE dW
p
( p,V1, T1 ) ( p,V2 ,T2 ) 1 2
热力学第一定律的应用 --理想气体等容过程、定容摩尔热容 --理想气体等压过程 、定压摩尔热容
计算各等值过程的热量、功和内能的理论基础
( 1)
m pV RT M
(理想气体的共性) 解决过程中能
量转换的问题
dQ dE pdV
( 2)
Q E pdV
V1
V2
( 3)
E E (T )
CV ,mol
单位
1
dQV CV ,moldT
J mol K
13-(2) 理想气体的等温过程和绝热过程
等体放热,内能减少.
o
等温膨胀过程 V E = 0 ;Q = W > 0
Q Δ E W 等温吸热,对外做功.
依 据
Δ
E
i 2
R
ΔT
等压压缩过程 W < 0 ; E < 0 ;Qp < 0
PV RT
外界做功,内能减少且放出热量.
绝热膨胀过程
Q = 0 ;W > 0;E < 0 绝热对外做功,内能减少.
解:把氮气视为理想气体, 其液化过程为绝热过程。
p1 501.013105 pa,p2 1.013105 pa,T1 300K
i5
γ C p,m
CV,m
i
i
2
1.40
p 1T 常量
p T p T 1 11
1 22
T2
T1 (
p2 p1
1
)
300 (
1
1.401
) 1.40
等温膨胀
p
p1 1 ( p1,V1,T )
p2
o V1
( p2 ,V2 ,T ) 2
W
V2 V
等温压缩
p
p1 1 ( p1,V1,T )
p2
o V1
( p2 ,V2 ,T ) 2
W
V2 V
QT E W
QT E
W
上 页 下 页 返回 5
物理学 §13-4 理想气体的等温过程和绝热过程
例1 将 500J 的热量传给标准状态下 2mol 的氢气。 (1) 若体积不变,这热量变为什么?氢气温度变为多少? (2) 若温度不变,这热量变为什么?氢气的体积和压强各 变为多少? (3) 若压强不变,这热量变为什么?氢气的温度和体积各 变为多少?
13-03 理想气体的等体过程和等压过程《大学物理学》

二 等压过程 定压摩尔热容 特 性 p 常量 过程Q p dE dW
1
p
( p,V1, T1 ) ( p,V2 ,T2 ) 1 2
W
o
V1
V2 V
定压摩尔热容定义: 1mol 理想气体在等压过程中吸 收的热量 dQ p ,温度升高 dT,其定压摩尔热容为
13-3 理想气体的等体过程和等压过程 摩尔热容(陈世红) 第十三章热力学基础
计算各等值过程的热量、功和内能的理论基础
( 1)
m pV RT (理想气体的共性) M dQ dE pdV 准静态过程 热
( 2)
m i E RT (理想气体的状态函数) ( 3) M 2
(4) 各等值过程的特性 .
Q E pdV
V1
V2
力学第一定律
13-3 理想气体的等体过程和等压过程 摩尔热容(陈世红) 第十三章热力学基础
本节要求会推导,会求W,Q,E2-E1 一 等体过程 定体摩尔热容 特性 V 常量
过程方程
1
p2
p
( p2 ,V , T2 )
( p1 ,V , T1 )
pT 常量 p1 dV 0 , dW 0 o 热力学第一定律 dQV dE
定义摩尔热容比(比热比)
m R (T2 T1 ) W p(V2 V1 ) M m m Q p C p ,m (T2 T1 ), E2 E1 CV ,m (T2 T1 ) M M
C p,m CV ,m
13-3 理想气体的等体过程和等压过程 摩尔热容(陈世红) 第十三章热力学基础
dQV dT
等 p2 体 升 p1 压
p
2 ( p ,V , T ) 2 2 1
13-3 等体、等压过程,摩尔热容.

C
CV
i 2
R
Cp CV R i2 R 2
等温 T= 恒量 p量V 恒
0
RT ln V2 或 RT ln p1
V1
p2
理想气体的等体、等压、等温过程
例2 把压强为1.013×105pa, 体积为100cm3的氮
气压缩到20cm3时,气体内能的增量、吸收的热
量和所做的功各是多少?假设经历的是如下两
a→b 等压过程,做功为
b
a
Ap p1(V2 V1)
pV RT
T pV
R
6. 内能变化
QV
V R
CV (
p2
p1 )
νmol理想气体 E QV CV (T2 T1)
(适应于理想气体的一切过程)
二、等压过程 在等压过程中, 理想气体的压强保持不变。
1. 特征 p = C, dp = 0
2. 过程方程
pV RT V C
T 3. 过程曲线
平行于V 轴的等压线。
(盖-吕萨克定律)
p p
O V1
V2 V
4. 功 (A 等于等压线下的面积 )
A pdV p V2 dV pV p
V1
p
pV RT
A
A p(V2 V1) R(T2 T1) O V1 V2 V
定压摩尔热容Cp
在等压过程中, 1mol 理想气体经吸热 Q, 温度变化 T
106
ln
20 106 100 106
16.3J
负号表示在等温压缩过程中, 外界向气体 做功而气体向外界放出热量。
(2)a→b →c ,先等压压缩,后等体升压
热学理想气体的等容过程与等压过程

热学理想气体的等容过程与等压过程热学是研究热量和能量转化规律的学科,而理想气体是热学中经常被用到的模型。
在理想气体的研究中,等容过程和等压过程是非常重要的两种过程。
本文将详细介绍热学理想气体的等容过程和等压过程,并分析其特点和应用。
一、等容过程等容过程是指在气体容积不变的条件下发生的热学过程。
在等容过程中,气体的体积固定,因此气体分子只能通过传递热量来改变其内能。
根据理想气体的状态方程PV=nRT,我们可以推导出等容过程的关系式为:Qv = ΔU = nCvΔT其中,Qv表示等容过程中的传热量,ΔU表示气体内能的变化,n表示气体的摩尔数,Cv表示定容摩尔热容量,ΔT表示气体温度的变化。
等容过程的特点是气体的压强和温度成正比变化,即P ∝ T。
由于气体体积固定,所以无法完成机械功,因此等容过程中的ΔU完全由传热量Qv来改变。
等容过程在工程实践中有重要应用,比如在内燃机中的压缩过程,这是通过使燃烧室内的气体体积保持不变来提高气体温度和压强,从而提高内燃机的效率。
二、等压过程等压过程是指在气体压强不变的条件下发生的热学过程。
在等压过程中,气体的压强保持不变,使得气体可以通过体积的变化来完成功。
根据理想气体的状态方程PV=nRT,我们可以推导出等压过程的关系式为:Qp = ΔH = nCpΔT其中,Qp表示等压过程中的传热量,ΔH表示气体焓的变化,n表示气体的摩尔数,Cp表示定压摩尔热容量,ΔT表示气体温度的变化。
等压过程的特点是气体的体积和温度成正比变化,即V ∝ T。
在等压过程中,气体可以通过扩张或压缩完成功,因此可以利用等压过程来实现热机的工作。
蒸汽机和内燃机中的工作过程就是通过等压过程来完成能量转化的。
三、等容过程与等压过程的比较等容过程和等压过程是热学中的两种重要过程,它们有以下几点不同:1. 条件不同:等容过程的条件是气体容积不变,而等压过程的条件是气体压强不变。
2. 性质不同:等容过程中无法完成功,完全由传热量改变气体内能;等压过程中可以通过体积的变化完成功,以改变气体的焓。
第4章 热力学基础 [2]
![第4章 热力学基础 [2]](https://img.taocdn.com/s3/m/cf009a0c52ea551810a68724.png)
绝热线比等温线更陡
p
PQ 绝热线
P
Q = E + A
PT O V
等温线
(P1,V1,T1) 等温线 (P2,V2,T1) 绝热线 (P2,V2,T2)
V
O
V1
V2
V
2 p nεt 3
3 εt kT 2
pV vRT
等温过程:温度不变,压 强降低是由于体积膨胀。 绝热过程:压强降低是由 于体积膨胀和温度降低。
§4.3.5 几个典型过程的总结及热力学第一定律的应用 等容过程 等压过程
过程 P 恒量 方程 T 内能 增量 功 热量
V 恒量 T
等温过程
绝热过程
E νC v,m (T2 T1 )
0 dE = dQ
i dE RdT 2
p V C1 PV 恒量 T V 1 C 2 p 1 T C 3 i dE RdT 2 0 E νCv,m (T2 T1 )
QT AT pdV
V2 V1
V2 V1
p[Pa] p1
a
7.02 102 J
(吸热)
p1V1 V2 p2 dV p1V1 ln V V1 O
c V1
b V2V[m3]
(2) 在 ac 等容降温和 cb 等压膨胀过程中,因 a、 b 温相同,故 E = 0。
Qacb Aacb Acb p2 V2 V1 5.07 102 ( J )
例 5-2
理想气体经如图所示的直线过程从状态 a
过渡到状态 b。求此过程中系统内能的改变、做功 和热传递?(已知 CV , m
p(105Pa) a
5 R) 2
理想气体的等体、等压、等温过程

理想气体等体、等压、等温过程
1 理想气体等体过程 2 理想气体等压过程 3 理想气体等温过程
(1)热力学第一定律 dQ vCV,mdT pdV
(2)焦耳定律
dU
CV ,mdT
或
ΔU
m M mol
i 2
R(T2
T1
)
(3)状态方程
PV RT + 具体过程
1. 等体(积)过程(isochoric process)
d Q v C p,m d T
p
Q
v
T2 T1
C
p ,m
dT
C p,m T
其内能改变仍为
1( p0,V1) p0
2( p0,V2 )
U 2 U 1 v
T2 T1
C V ,m
dT
C V,m T
W
V2 V1
pdV
p(V2
V1 )
m M mol
R(T2
T1)
O V1
V2 V
3. 等温过程(isothermal process) 过程方程:pV 常量 理想气体在等温过程中内能 不变,故。 dU 0
dQ dW pdV
p p1 1( p1,V1)
p2 O V1
2( p2 ,V2 )
V2 V
在准静态等温膨胀中
Q =W R T ln V2
V1 在准静态等温膨胀中把吸收的热量全部对外作功
l理想气体的摩尔热容
Um
i 2
RT
理想气体的定体摩尔热容为
CV ,m
dU m dT
iR 2
单原子分子气体
CV ,m
3 2
R
理想气体的等体过程和等压过程 摩尔热容

2014年5月24日星期六
大学物理
§13-3
理想气体的等体过程和等压过程 摩尔热容
(5) CP,m表达式 (dQ)P=vCP,mdT=(dE)P+(dA)P
E V CP,m d T d T P d T T P T P
理学院 物理系
大学物理
§13-3
理想气体的等体过程和等压过程 摩尔热容
二、热力学第一定律对理想气体的应用 —等体过程
1. 热量Q和内能表达式
dQ=dE
dQ=vCV,mdT dE=vCV,mdT
或
或 或
Q=E2 - E1
Q=vCV,m(T2 - T1) E2 - E1= vCV,m(T2 - T1)
2014年5月24日星期六
理学院 物理系
大学物理
§13-3
理想气体的等体过程和等压过程 摩尔热容
2.内能和CV,m的普遍关系
关系式dE=vCV,mdT或 E2 - E1=vCV,m(T2 - T1)虽然是
由等容过程得到的,但是对理想气体,无论其经过
什么过程,只要起初温为T1,终温为T2,内能和CV,m
d E V
E dT T V
CV,m d T d E V
CV,m
E dT T V
1 E 1 e e T V T V T V
(6)理想气体CV,m表达式
的关系都成立。
dE dE dE i ( )V ( )p CV,m R dT dT dT 2
d E CV,m d T
2014年5月24日星期六
13-3理想气体的等体过程和等压过程

可得摩尔定压热容和摩尔定体热容的关系 可得摩尔定压热容和摩尔定体热容的关系 定压热容和摩尔定体
C p,m = CV ,m + R
J 单位: 单位: ⋅ mol ⋅ K
迈耶公式
−1
−1
摩尔热容比
γ = Cp,m CV ,m
第十三章 热力学基础
8
物理学
第五版
1313-3 理想气体的等体和等压过程 摩尔热容
pV = νRT
三个量: 三个量:
W = p (V2 − V1 ) = ν R (T2 − T1 )
Qp = ν C p,m (T2 − T1 )
C p ,m i+2 = R 2
E2 − E1 =ν CV ,m (T2 − T1) CV ,m
第十三章 热力学基础
i = R 2
9
物理学
第五版
1313-3 理想气体的等体和等压过程 摩尔热容
四 比热容
如果系统不是理想气体, 如果系统不是理想气体,或经历非等 值过程的气体, 值过程的气体,则有
dQ 热容 C = d T
比热容
dQ C c= = m′dT m′
是系统的质量. m′是系统的质量
第十三章 热力学基础
12
物理学
第五版
1313-3 理想气体的等体和等压过程 摩尔热容
单原子理想气体, 例1 10mol单原子理想气体,在压 单原子理想气体 缩过程中外界对它作功209J, 其温度 缩过程中外界对它作功 , 升高1K.试求气体吸收的热量与内能的 升高 试求气体吸收的热量与内能的 增量.已知 已知C 增量 已知 V,m=12.465 J ⋅ mol -1 ⋅ K -1 . 解 ∆E = ν CV ,m (T2 − T1 ) = 124.65J
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
三个量:
W p(V2 V1 ) R(T2 T1 )
Qp C p,m (T2 T1 )
E2 E1 CV ,m (T2 T1 )
第十三章 热力学基础
12
13-3 理想气体的等体和等压过程 摩尔热容
等 p 压 膨 胀
p
( p,V1, T1 ) ( p,V2 , T2 )
1
2
W
o
V1
V2
V
等 p 压 压 缩
p
( p,V2 , T2 ) ( p,V1, T1 )
2
1
W
o
V2
V1
V
Qp
E2
E1
W
Qp
E1
W
E2
13
第十三章 热力学基础
13-3 理想气体的等体和等压过程 摩尔热容 3、关于摩尔热容的讨论
•Mayer公式
推导
C P ,m-CV ,m=R
C p,m CV ,m R
由热力学第一定律
QV CV ,m (T2 T1 ) E2 E1
第十三章 热力学基础
5
13-3 理想气体的等体和等压过程 摩尔热容
p
等 体 升 p1 压
p2
2 ( p ,V , T ) 2 2 1
( p1 ,V , T1 )
p
o
等 体 降 p2 压
p1
1 ( p1,V , T1 )
m dQ p C p ,m dT dE pdV M m m dE CV ,m T2 T1 pdV RdT M M
可得摩尔定压热容和摩尔定体热容的关系
M
C p ,m
摩尔热容比
i2 CV ,m R R 2
C p,m CV ,m
第十三章 热力学基础
11
13-3 理想气体的等体和等压过程 摩尔热容
15
气体
CV,m
γ 1.67
He 12.47 Ne H2 20.78 N2 O2 H2O 24.93 CH4 CHCl3
20.09
1.40
33.24
1.33
第十三章 热力学基础
13-3 理想气体的等体和等压过程 摩尔热容
三、比热容
1、热容:
使物质温度升高1K所需要的热量称为该物质的热容。
2、比热容:
o
V
2
第十三章 热力学基础
13-3 理想气体的等体和等压过程 摩尔热容 •内能、功和热量的变化
dV 0, W pdV 0
p
p2
由热力学第一定律
( p2 ,V , T2 )
( p1 ,V , T1 )
V
dQV dE
QV E E2 E1
p1
o
V
•特征: 系统对外界不作功,系统吸收的热量全 部用来增加系统的内能。
理论值 CP,m 20.78
C P ,m CV ,m
CV,m 12.61 12.53 20.47 20.56 21.16 27.8 27.2 63.7 实验值 CP,m 20.95 20.90 28.83 28.88 29.61 36.2 35.2 7ห้องสมุดไป่ตู้.0 γ 1.66 1.67 1.41 1.40 1.40 1.31 1.30 1.13
系统吸收热量 系统放出热量
4
T2 T1 0 T2 T1 0
QV 0 QV 0
第十三章 热力学基础
13-3 理想气体的等体和等压过程 摩尔热容 •气体内能的增量
m E E 2 E1 CV ,m T2 T1 M
mol 理想气体
dQV dE CV ,mdT
第十三章 热力学基础
3
13-3 理想气体的等体和等压过程 摩尔热容
2、定体摩尔热容
•定义
1mol理想气体在等体过程中,温度升高1K时所吸 收的热量,称为该物质的定体摩尔热容。
CV ,m
dQV dE i R dT dT 2
单位 J mol K
1
1
•等体过程的热量公式
m QV CV ,m (T2 T1 ) M
m Qp C p ,m (T2 T1 ) M
系统吸收热量
系统放出热量
9
•等压过程的热量公式
T2 T1 0 T2 T1 0
Qp 0 Qp 0
第十三章 热力学基础
13-3 理想气体的等体和等压过程 摩尔热容 •气体内能的增量
m E E 2 E1 CV ,m T2 T1 M
( p2 ,V , T2 )
V
2
V
V
V
o
QV
E1
E2
QV
E1
E2
第十三章 热力学基础
6
13-3 理想气体的等体和等压过程 摩尔热容
二、等压过程 定压摩尔热容
1、等压过程 •特点:
理想气体的压强保持不变,p=const
•过程曲线:
p ( p,V1, T1 ) p
1 W
V1
( p,V2 ,T2 )
在PV 图上是一条平行于V 轴的直线, 叫等压线。
第十三章 热力学基础
1
13-3 理想气体的等体和等压过程 摩尔热容
一、等体过程 定体摩尔热容
1、等体过程 •特点:
理想气体的体积保持不变, V=const
p
p2
•过程曲线:
在PV图上是一条平行于
( p2 ,V , T2 )
( p1 ,V , T1 )
V
p轴的直线,叫等体线。 •过程方程:
p1
p1 p2 T1 T2
mol 理想气体
CV , m dQV dT
dQV dE CV ,mdT
由热力学第一定律
QV CV ,m (T2 T1 ) E2 E1
第十三章 热力学基础
10
13-3 理想气体的等体和等压过程 摩尔热容
•气体内能的增量 E E E m C T T 2 1 V ,m 2 1
dQ C dT
单位质量的热容称为比热容。
C 1 dQ c m m dT
第十三章 热力学基础
16
13-3 理想气体的等体和等压过程 摩尔热容
计算各等值过程的热量、功和内能的 理论基础.
(1) (2)
pV RT (理想气体的共性)
dQ dE pdV
V2 V1
解决过程中能
Q E pdV 量转换的问题
(3) E E (T )(理想气体的状态函数) (4) 各等值过程的特性 .
V2
V
•特征: 系统吸收的热量一部分用来增加系统的内能, 另一部分使系统对外界作功。
第十三章 热力学基础
8
13-3 理想气体的等体和等压过程 摩尔热容 2、定压摩尔热容 •定义
1mol理想气体在等压过程中,温度升高1K时所吸收 的热量,称为该物质的定压摩尔热容。
C p ,m
dQp dT
J mol1 K 1 单位
理想气体的定压摩尔热容比定体摩尔热容大一个恒量R •在等体过程中,气体吸收的热量全部用来增加系统的 内能 •等压过程中,气体吸收的热量,一部分用来增加系统 的内能,还有一部分用于气体膨胀时对外界作功 气体升高相同的温度,在等压过程吸收的热量要比 在等温过程中吸收的热量多。
第十三章 热力学基础
14
13-3 理想气体的等体和等压过程 摩尔热容 •摩尔热容比
2
•过程方程:
V1 V2 T1 T2
第十三章 热力学基础
o
V2
V
7
13-3 理想气体的等体和等压过程 摩尔热容
•内能、功和热量的变化
W
V2
pdV p(V2 V 1)
V1
p ( p,V1, T1 ) p
1
( p,V2 ,T2 )
由热力学第一定律
2
W
o
V1
dQ p dE dW
Qp E2 E1 p(V2 V1 )
