理想气体基本热力过程
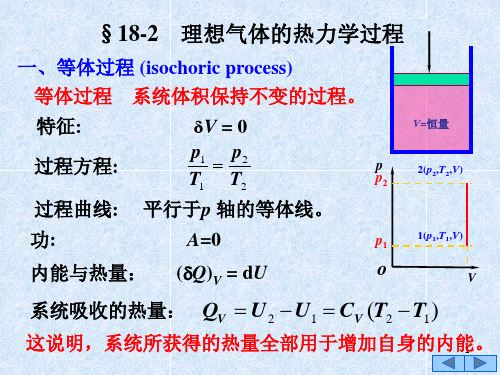
理想气体的热力学过程
6
dV d p 0 V p
式中
Cp CV
, 在温度变化不很大时,可以看作常量。
将上式积分,得
ln V + ln p = 恒量
pV γ 恒量 或 这个关系称为泊松 (S.D.Poisson)公式。
根据泊松公式和理想气体物态方程, 可以分别得到
TV γ 1 恒量
T γ pγ 1 恒量
Qp = H 气 H水
= (2676.3103 419.06103 ) Jkg1
= 2257.2103 Jkg1
16
17
经绝热过程压缩气体做的功:
CV 20.44J mol K
1
1
m 4 A CV T2 T1 4.70 10 J M
在等压过程中,系统从外界获得的热量,一部分用 以增大内能,一部分用以对外作功。 三、等温过程 (isothermal process) 等温过程 特征: 过程方程: 系统的温度保持恒定的过程。 T=0
p1V1 p2V2
p p1
T=恒量
恒温热源
1(p1,V1,T)
过程曲线:
内能增量:
等温线为等轴双曲线。
=1.40,可得:
p2 T2 T1 p 1
1 /
1 300 50
0.286
98.0K
19
例6 一定质量的理想气体先后经历 P 两个绝热过程即1态到2态,3态到4
态(如图所示)且T1=T3、T2=T4,在 1态与3态,2态与4态之间可分别连 接 两 条 等 温 线 。 求 证 :
考虑到 T1=T3,T2=T4,
T2 V1 1 2 T1 V2
《热力学》理想气体的热力过程

p2 p1
v1 v2
n
T2 T1
v1 v2
n1
T2 T1
p2 p1
(n1) / n
n lnp2 lnp1 lnv2 ln v1
(2)利用已知或可求的与n有关的能量求解
2020年10月20日
第四章 理想气体的热力过程
28
例4-3(p80) 有一台空气压缩机,压缩前空气的温度为27 ℃、 压力为0.1 MPa,气缸的容积为5 000 cm3;压缩后空气的温度升 高到213 ℃。压缩过程消耗的功为1.166 kJ。试求压缩过程的多变 指数n。
15
(2)图表法 由
ds
cp0
dT T
Rg
dp p
对可逆绝热过程可得
ln
p2 p1
1 Rg
T2
T1
c
p
0
dT T
A:利用热力性质表中的标准状态熵
ln
p2 p1
1 Rg
T1
T0
c
p
0
dT T
c T2
T0
p0
dT T
1 Rg
s0 T2
s0 T1
T2 工质的热力性质表中还提供了u与h的数值。
2020年10月20日
第四章 理想气体的热力过程
19
例4-2 (p76) 一台燃气轮机装置,从大气吸入温度为17 ℃、压 力为0.1 MPa的空气,然后在压气机中进行绝热压缩,使空气 的压力提高到0.9MPa。试求压气机消耗的轴功:(1)按定值比 热容计算;(2)按空气热力性质表计算。
思路:
定值比热容
2020年10月20日
第四章 理想气体的热力过程
14
变比热容分析
08理想气体的基本热力过程(完整版)

实际过程的多变指数可能是变化的,如果变化不 大,可取一平均值;变化较大时,可分段表示,每一段 近似为n值不变。
¾初、终态参数的关系
p2 p1
=
⎜⎜⎝⎛
v1 v2
⎟⎟⎠⎞n
T2 T1
=
⎜⎜⎝⎛
v1 v2
⎟⎟⎠⎞n−1
n−1
T2 T1
= ⎜⎜⎝⎛
p2 p1
⎟⎟⎠⎞
n
Δu = cV (T2 − T1) Δh = cp (T2 − T1)
n=∞
n=∞
过相同点1的四种基本热力过程线
Ⅰ Ⅰ
Ⅲ
Ⅲ
原则上,n可为-∞→ 0 →+ ∞之间的任一数值
但工程中所遇到的n一般都是正值(n>0)
dp = −n p dv v
若n<0,则 dp > 0 意味着: dv
工质膨胀时,压力增大,压缩时,压力降低,工程上一般看 不到这样的过程,所以n为负的过程不必考虑。
v1
v v1
=
RgT
ln
v2 v1
=
p1v1
ln
v2 v1
= − p1v1 ln
p2 p1
wt = w
9绝热可逆过程
δqrev = 0 ⎪⎫
ds
=
δqrev
T
⎬ ⎪⎭
ds = 0
s = const.
á 绝热可逆过程是定熵过程
¾ 过程方程
ds
= cp
dv v
+ cV
dp p
=0
γ dv + dp = 0
cV
¾ 多变指数
cn
=
n−γ
工程热力学第四章理想气体热力过程

03
CHAPTER
等容过程
等容过程是指气体在变化的整个过程中,其容积保持不变的过程。
定义
特点
适用场景
气体在等容过程中,气体温度和压力会发生变化,但容积保持不变。
等容过程常用于高压、高温或低温等极端条件下的气体处理。
03
02
01
等容过程定义
在等容过程中,气体吸收的热量等于气体所做的功和气体温度升高所吸收的热量之和。
多变过程的具体形式取决于气体所经历的压力和温度的变化规律。
多变过程定义热力学第一定律 Nhomakorabea热力学第二定律
理想气体状态方程
热效率
多变过程的热力学计算
01
02
03
04
能量守恒定律,用于计算多变过程中气体吸收或释放的热量。
熵增原理,用于分析多变过程中气体熵的变化。
描述气体压力、体积和温度之间的关系,可用于多变过程的计算。
衡量多变过程能量转换效率的指标,通过比较输入和输出的热量来计算。
提高热效率的方法
优化多变过程参数,如压力和温度的变化规律,以减少不可逆损失和提高能量转换效率。
热效率与熵增的关系
根据熵增原理,不可逆过程会导致熵的增加,从而降低热效率。因此,减少不可逆损失是提高多变过程热效率的关键。
热效率计算公式
$eta = frac{Q_{out}}{Q_{in}}$,其中$Q_{out}$为输出热量,$Q_{in}$为输入热量。
计算公式
通过优化气体的初态和终态,以及选择合适的加热和冷却方式,可以提高等容过程的热效率。同时,也可以通过改进设备结构和操作方式来提高热效率。
提高热效率的方法
等容过程的热效率
04
CHAPTER
第4章-理想气体的热力性质和热力过程

m
pRgVT1w
1
Ts
0.098MPa36m3 0.28[7kJ/(kgK)]
2
1 73K
1 308K
5.117kg
9
第二节 理想气体的比热容
10
• 热容:指工质温度升高1K所需的热量。
C Q dT
• 比热容:1kg(单位质量)工质温度升高1K所
k
nn1n2n3 ni nk ni i 1
• 第 i 种组元气体的摩尔分数 (mole fraction of a mixture):
xi
ni n
(433)
xi nni nni 1
各组元摩 尔分数之
和为1
37
换算关系
mnM
mi niMi
• 根据热力学第一定律,任意准静态过程:
q d u p d v d h v d p
u是状态参数: uf(T,v)
du(T u)vdT(uv)Tdv
q( T u)vdT[p( u v)T]dv
单位物量的物质 在定容过程中温 度变化1K时热 力学能的变化值
q u
• 定容: dv0 cv (dT)v (T)v 12
3
第一节 理想气体及其状态方程
4
• 理想气体 ideal gas定义:
– 遵循克拉贝龙(Clapeyron)状态方程的气体,
即基本状态参数 p、v、T 满足方程
pv 常数 T 的气体称为理想气体。
理想气体的基本假设:
• 分子为不占体积的弹性质点 uu(T)
• 除碰撞外分子间无作用力
理想气体是实际气体在低压高温时的抽象
热工流体第四章 理想气体的基本热力过程

第一节定容过程
气体比体积保持不变的热力过程称为定容过程。
1、过程方程式
v=c(4-1)
2、状态方程
或 (4-2)
3、过程曲线
图4-1
4、 、 的计算
理想气体的热流学能,焓是温度的单值函数
(4-3)
(4-4)
5、容积变化功与传热量
定容过程比体积变化量Δv=0,所以定容过程体积变化功为
及q=0(4-19)
根据熵的定义,可逆绝热过程有
(4-20)
即
s=c(4-21)
所以可逆绝热过程为定熵过程。
1、过程方程式
(4-22)
κ---绝热指数,理想气体绝热指数,也等于理想气体比热容比。
2、状态方程
(4-23)
(4-24)
(4-25)
3、过程曲线
图4-4
4、 、 的计算
(4-26)
(4-27)
当n=0时, ,为比定压热容;
当n=1时, ,为比定温热容;
当n=κ时, ,为比定熵热容;
当n= 时, ,为比定容热容。
例空气在压气机中被压缩,初始状态为V1=0.052m3,p1=0.1Mpa,t1=40°c,可逆多变压缩至p2=0.565Mpa,V2=0.013 m3,然后排到储气罐,求多变过程的多变指数n,压缩终温t2,容积变化功与换热量,以及压缩过程中气体热力学能、焓的变化值。
当n=1时, ;
当n=κ时, ;
当n= 时, 。
2、状态方程
(4-32)
(4-33)
(4-34)
3、过程曲线
图4-5
4、 、 的计算
(4-35)
(4-36)
5、多变过程容积变化功与传热量
第四章 理想气体的热力过程

p
T
cn cn 0
cn cv
s
v
(4) 当 n = p isochoric v const v C
1 n
理想气体 p 过程的p-v,T-s图
T dT ( )p ? cp ds
T2
已知p1,T1,T2 , 求p2 若是空气,查附表2
p2 p1exp
s s
0 T2
0 T1
R
理想气体 s u, h, s,的计算
状态参数的变化与过程无关 内能变化 焓变化 熵变化
u cv dT
h cp dT
s 0
理想气体 s w,wt ,q的计算
膨胀功 w
h>0 q>0 u> 0 p w>0
q Tds
T
qw
T
h>0 u>0
n0
n 1 wt>0
w>0
n0
wt>0
n
n 1
nk
n
q>0
nk
v
s
u,h,w,wt,q在p-v,T-s图上的变化趋势
u,h↑(T↑) w↑(v↑) wt↑(p↓) q↑(s↑) h>0 q>0 u> 0 T p w>0 w>0 n 0 h>0 u>0
q0
4-6 理想气体热力过程综合分析
一、过程线分布规律
顺时针方向n增大
二、过程特性和过程中能量传递的方向
u在p-v,T-s图上的变化趋势
u = T u> 0 p
工程热力学理想气体的热力性质及基本热力过程

气体 CV,m Cp,m 种类 [J/(kmol· K)] [J/(kmol· K)] 单原子 3×R/2 5×R/2 双原子 5×R/2 7×R/2 多原子 7×/2 9×R/2
Cm c M
Cm c' 22 .4
22
对1kg(或标态下1m3)气体从T1变到T2所需热量为:
q cdT c dT cT2 T1
17
比较cp与cv的大小:
结论:cp>cv
18
理想气体定压比热容与定容比热容的关系 迈耶公式: c p
令
cV Rg (适用于理想气体)
cp / c k , . V 称为比热比或绝热指数
当比热容为定值时,К为一常数,与组成气体的 原子数有关。如:
单原子气体 К=1.66;
双原子气体 К=1.4;
R 8314 J /( kmol K )
各种物量单位之间的换算关系:
1kmol气体的量 Mkg气体的量 标态下22.4m 气体的量
3
7
气体常数Rg与通用气体常数R的关系:
m pV nRT RT M pV mRg T
R 8314 Rg 或 R MRg M M
w
0 4
2 3 v
q 0 4 3 s
w pdv
1
2
q Tds
1
14
2
3-2 理想气体的比热容
一、比热容的定义及单位
1.比热容定义
热容量:物体温度升高1K(或1℃)所需的热量 称为该物体的热容量,单位为J /K.
比热容:单位物量的物质温度升高1K(或1℃) 所需的热量称为比热容,单位由物量单位决定。
理想气体的热力性质及其热力过程

第三节 理想气体的热力学能与焓 理想气体的状态方程及比热容确定后,利用热力学第一定律就可方便地求得理想气体的热力学能和焓的计算式。
第七章 理想气体的热力性质及其热力过程
第七章 理想气体的热力性质及其热力过程
图7-3 例7-3图
第七章 理想气体的热力性质及其热力过程
第七章 理想气体的热力性质及其热力过程
第七章 理想气体的热力性质及其热力过程
第七章 理想气体的热力性质及其热力过程
图7-7 绝热过程在p-v、T-s图上的表示
Cycle Diagram
Text
Text
Text
Text
Text
Cycle name
Add Your Text
Diagram
Your Slogan here
第七章 理想气体的热力性质及其热力过程
二、四个基本热力过程分析 1.定容过程
第七章 理想气体的热力性质及其热力过程
第七章 理想气体的热力性质及其热力过程
图7-4 定容过程在p-v、T-s图上的表示
第七章 理想气体的热力性质及其热力过程
第七章 理想气体的热力性质及其热力过程
2.定压过程
第七章 理想气体的热力性质及其热力过程
第七章 理想气体的热力性质及其热力过程
热工设备中实际进行的热力过程均是多变过程,且通常要比理论的多变过程更为复杂。例如,制冷压缩机气缸中制冷剂蒸汽的压缩过程,在整个过程中指数n是变化的。压缩开始时,工质温度低于缸壁温度,工质是吸热的,随着对工质不断地压缩,温度升高,高于缸壁温度后开始放热,瞬时多变指数约从1.4左右变化到1.0左右。制冷压缩机压缩过程的多变指数大小还与制冷剂的种类、制冷剂蒸汽与气缸壁的热交换情况、活塞与气缸壁的密封情况等因素有关。通常,制冷压缩机压缩多变指数要小于活塞式空气压缩机压缩多变指数。对多变指数n是变化的实际过程,热工计算中为简便起见常常这样处理:若n的变化范围不大,则用一个不变的平均多变指数近似地代替实际变化的n;如果n的变化较大,可将实际过程分段,每段近似为n值不变,各力性质及其热力过程
第3章理想气体的性质与热力过程

矩形面积的高度即为平均比热容。
平均比热容图表:
q
t2 cdt
t1
t2 cdt
0
t1 0
cdt
c
|
t2 0
t2
c
|
t1 0
t1
其中:
c
|
t 0
温度自0-t的平均比热容值。
因此气体的平均比热容表示为:
c
|
t2
t1
c
|
tt2
02
t2
c| t1
tt1
01
只要确定了
c
| t1
0
和
c
| t2
0
3-2-1 热容的定义(Heat capacity):
1. 热容:物体温度升高1K(或1℃)所需要的热量,
用C表示,单位J/K。
C Q Q
2. 根据物质计量单位不同,热容分三类: dT dt
(1)比热容(specific heat)
q
c
单位质量物质的热容量(质量热容)
dT
用c表示 ,单位 J / (kg . K) (2)摩尔热容(molar heat)
q1 2 t2 t1
t2cd t
t1
t2 t1
c c a0 a1T a2T 2 a3T 3 q1-2
热量:
q
c
|
t2 t1
(t2
t1 )
c
|
t2 t1
几何意 义
c |t2 t1
0
t1 dt t2 t
q1-2为过程线下面的面积。如果过程线下面的面 积可以用一个相同宽度的矩形面积来代替,则该
当温度变化趋于零的极限时的比热容。 它表示某瞬间温度的比热容。
第五章 理想气体热力过程

u 0
q u w 0
定温吸热膨胀
v2 v1
p
1
w0
T
1 2
2
v
s
5、确定△ u、 △ h、 △ s、w、wt、q:
u cv T 0
h cp T 0
ds
q
T
2
v2 RT ln v1 v2 p1 q s R ln R ln T T v1 p2
4、基本热力过程与多变过程的关系:
k 1n c c n v n k 1 基本过程是多变过程的特例 c c n 1 n v pv const n 1 n
n
p T
s
v
0 pv const p C cn kcv cp (1) 当 n = 0
p T s
(2) 当 n = 1 pv pv const RT T C
2
qrev
2
1
1
第二节 基本热力过程
一、定容过程 isochoric
1、定义: 在状态变化过程中,工质的比容 始终保持不变的热力过程 2、过程方程式:
v=c
p 2 T2 p1 T1
3、初终状态参数间关系:
v1 v2
4、理想气体定容过程的p-v,T-s图
dT T T ( )Tds q cv dT 0 T v ds cv cv p 1-2: T 2
第五章 理想气体热力过程
The First Law of Thermodynamics
学习目标:
熟练掌握定容、定压、定温、绝热以及多变过程 (1)初、终状态参数p、v、T、之间的关系 (2)△u、△h、△s、q、w、wt的计算
理想气体的热力过程

= − ∫ v dp = v ( p1 − p 2 )
1
2
(4-5) )
热能工程教研室
理想气体 v 的参数关系
求过程的△ 、 求过程的△U、 △ H、 △ S 、
du = c v dT dh = c p dT
取定值 比热容
∆ u = cv ∆ T ∆h = c p ∆T
显然,过温度相同的同一点的定容线斜率大于定压线斜率。 显然,过温度相同的同一点的定容线斜率大于定压线斜率。 定容线斜率大于定压线斜率
热能工程教研室
理想气体 P 的参数关系
对于定压过程,其初、终态状态参数间的关系: 对于定压过程 其初、终态状态参数间的关系: 其初
du = c v dT dh = c p dT
δwt = −vdP = 0 可逆定压过程的技术功: 10) 可逆定压过程的技术功: (4-10) 它表明:定压过程中系统不对外作技术功。 它表明:定压过程中系统不对外作技术功。 适用于 工质,不限于理想气体 上述式(4 8)、(4-9)和(4-10)适用 任何工质 不限于理想气体。 (4上述式(4-8)、(4-9)和(4-10)适用于任何工质 不限于理想气体。
(4-4) )
结论:定容过程中工质不输出膨胀功, 结论:定容过程中工质不输出膨胀功,其获得的热量等于工质的 热力学能的增量。它直接由热力学第一定律推出, 热力学能的增量。它直接由热力学第一定律推出,适用于所有气 体。
q v的计算结果为正,是吸热过程,反之是放热过程。 的计算结果为正,是吸热过程,反之是放热过程。
取定值 比热容
∆ u = cv ∆ T ∆h = c p ∆T
dP = 0
dT ds = c p T dv ds = c p v
理想气体的热力性质及基本热力过程

注:在T-s图中,定容线比定压线陡。
03-理想气体的热力性质及基本热力过
程--SCH
9
概念:定温过程是工质在变化过程中温度保持不
变的热力过程。对理想气体,定温过程也是定热
力学能过程和定焓过程。
Байду номын сангаасu 0
12、、过基程本方状程态式参:数间T =的关定系值式:h 0
p1v1 p2v2
T1
T2
13
3、功量与热量的分析计算
1)膨胀功为: w q u u cV T1 T2
上式说明:在绝热过程中,工质膨胀对外做的容积功 等于工质内能的减少。
2)定熵过程技术功:wt q h h CP T1 T2
上式说明:在绝热膨胀过程中,工质对外做的技术功 等于工质焓的减少量。
理想气体的定温过程,在数值上,体积功、技术功 和热量三者相等。
03-理想气体的热力性质及基本热力过
程--SCH
11
4、过程曲线
1
wt 2
定温过程的p-v图及T-s图
定温过程在P-V图中为一条等轴双曲线,在 T-S图中为一条平行于S轴的平行直线。
1-2为定温加热过程,气体定温吸热膨胀;
2-1为定温放热过程,气体定温放热压缩。
因而定容过程实质上是个热变功的准备过程
03-理想气体的热力性质及基本热力过
程--SCH
4
利用比热计算:当比热容为定值时
2
q 1 cV dT cV T
利用热力学一定律计算:因容积功为零,即系统接受的 热量全部用于增加工质的内能。当比热为定值时:
q u w u cV T
4-1 理想气体的基本热力过程
理想气体的热力性质和热力过程

况,进而找出影响转化的主要因素。 2、一般方法
(1)、对实际热力过程进行分析,将各种过程近似地概括为 几种典型过程,即定容、定压、定温和绝热过程。为使问题 简化,暂不考虑实际过程中的不可逆的耗损而作为可逆过程。
(2)、用简单的热力学方法对四种基本热力过程进行分析计算。
c t2 p,0℃
t2
-
c t1 p,0℃
t1
c t2 p,t1
c
t2 p,0℃
t2
-ct1 p,0℃来自t1t2 t1
p267附录A-4a给出了一些常用气体的平均比热容表
c c R t2
t2
v,t1
p,t1
g
(3)、平均比热容直线关系
qp
2 1
cp
(t)dt
2 1
(a
bt)dt
[a
b 2
所以MRg与物质的种类无关。(也与状态无关)令R= MRg , R 称为摩尔气体常数。取标准状态参数得
R MRg
p0Vm0 T0
101325Pa 0.02241325m3/mol 273.15K
8.3143 J/(mol.K)
对于各种气体的气体常数的
Rg
R M
(3 5)
理想气体状态方程可有以下四种形式:
(t1
t2
)](t2
t1 )
c t2 p,t1
a
b 2
(t1
t2
)
(3 19)
上式称为比热容的线
性关系。附录A-5p268给 出了一些常用气体的平
均比热容直线关系式。
(4)、定值比热容
cp a
由分子运动论也可导出1mol理想气体的热力学能
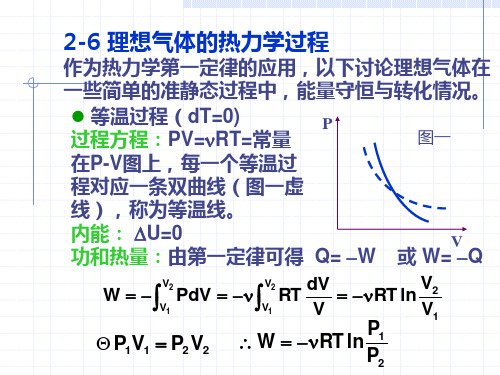
理想气体的热力学过程
P
1
2
4
0
T1 3
T2
V1
V4 V2
V3
Q
34:与温度为T2的低温热源接触,T2不变, 体积由V3压缩到V4,从热源放热为 V3 Q 2 RT2 ln V4 41:绝热压缩,体积由V4变到V1,吸热为零。
在一次循环中,气体 对外作净功为 |W|= Q1-Q2 ( 参见能流图)
T1 Q1
1
1
2
1
W3 4
RT3 1
T4 1 T3
在两条等温线之间, 沿任意两条绝热线, 系统对外界作功相等。
考虑到 T1=T3 T2=T4 W12=W34
2-7 循环过程
历史上,热力学理论最初是在研究热机工作过 程的基础上发展起来的。 在热机中被用来吸收热量并对外作功的物质叫 工质。工质往往经历着循环过程,即经历一系 列变化又回到初始状态。
气体在多方过程中从外界吸的热量
R Q C mV T2 T1 C v T2 T1 n 1
当1 n 时,Cmn 0。说明气体在过程中对 外界所作的功大于它从外界吸收的热量。多作 的功是由于消耗了本身的内能,故虽然吸热, 但温度反而下降,产生负热容。
V2 dV W PdV RT RT ln V1 V1 V V1 P1 P1V1 P2 V2 W RT ln P2
V2 V2
等容过程(dV= 0)
过程方程:V=常数 在P-V图上,等容线为一条垂直 于V轴的直线。(图二虚线)
P
功:W=0 内能与热量: 由第一定律可得:U=Q 理想气体内能表达式
|W|
例举出理想气体的四个基本热力过程及其过程方程式。

例举出理想气体的四个基本热力过程及其过程方程式。
理想气体是指在恒定温度下,所有气体分子间不存在相互作用力的气体体系。
对于理想气体,四个基本热力过程依次是等温过程、绝热过程、等压过程和等体过程,下面我们来一一介绍这四个过程。
一、等温过程等温过程是指理想气体在恒定温度下发生的过程,此时系统内的温度不变。
在等温过程中,理想气体的压强与体积成反比例关系,即PV = 常数,其中P为气体的压强,V为气体的体积。
二、绝热过程绝热过程是指理想气体在没有任何能量交换的情况下发生的过程。
在绝热过程中,由于没有热量的交换,温度会发生变化。
绝热过程中理想气体的状态方程为PV^{γ} = 常数,其中γ为理想气体的绝热指数。
三、等压过程等压过程是指理想气体在恒定压强下发生的过程。
在等压过程中,理想气体的体积与温度成正比例关系,即V/T = 常数。
等压过程的状态方程为V/T = 常数,其中V为气体的体积,T为气体的绝对温度。
四、等体过程等体过程是指理想气体在恒定体积下发生的过程。
在等体过程中,理想气体的压强与温度成正比例关系,即P/T = 常数。
等体过程的状态方程为P/T = 常数,其中P为气体的压强,T为气体的绝对温度。
通过以上介绍,我们可以看出四个基本热力过程对应的状态方程式分别是:等温过程 PV = nRT、绝热过程PV^{γ} = 常数、等压过程 V/T = 常数、等体过程 P/T = 常数。
在实际应用中,这四个基本热力过程是非常重要的。
通过对这些过程的掌握,我们可以更好地理解理想气体的物理变化规律,为一些实际问题的解决提供指导意义。
第4章 理想气体的热力过程

① 闭口系: w =
由于定温时:
dp d dv
=−
T
p v
⎛ dp ⎞ ⎛ dp ⎞ ⎜ ⎟ 〉 ⎜ ⎟ ⎝ dv ⎠ s ⎝ dv ⎠T
∫ pdv = ∫ pv
1 1 2
2
k
dv vk
2
因 pvk 为常数,所以: 为常数 所以 w = pv k ∫ 同时,因 pv=RgT ,可得:
2
2 1− k pv dv k v = = pv k ∫ v − k dv = pv k 1− k 1 1 − k 1 1 v
② 开口系: wt = − ∫ vdp = − ∫
1
1
2
2
RgT dp p
5、功与热量的计算 ①闭口系: w =
∫
1
2
RgT dv pdv = ∫ v 1
2
2
= −RgT ∫
1
2
⎛ p1 ⎞ ⎛ v2 ⎞ dp = RgT ln⎜ ⎜p ⎟ ⎟ = RgT ln⎜ ⎜v ⎟ ⎟ p ⎝ 2⎠ ⎝ 1⎠
2
⎤ ⎥ ⎥ ⎥ ⎦
n= k n= ± ∞
可见,绝热过程wt 是 w 的 k 倍 。热量q 为零。
2、状参关系式
3、绘制过程曲线
p 2 ⎛ v1 =⎜ p1 ⎜ ⎝ v2
T2 ⎛ v1 =⎜ T1 ⎜ ⎝ v2
⎞ ⎟ ⎟ ⎠
⎞ ⎟ ⎟ ⎠
n
n −1
由 pvn= const,pv=RgT
得
n −1
⎛ p2 T2 = ⎜ ⎜ p T1 ⎝ 1
如电厂中各种换热设备中的加热或冷却过程。 1、过程方程: 2、状参关系式 根据: p= const dp= 0
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
理想气体的基本热力过程热力设备中,热能与机械能的相互转化,通常是通过气态工质的吸热、膨胀、放热、压缩等热力过程来实现的。
实际的热力过程都很复杂,而且几乎都是非平衡、非可逆的过程。
但若仔细观察会发现,某些常见过程非常近似一些简单的可逆过程。
常见的主要有四种简单可逆过程-基本热力过程,指系统某一状态参数保持不变的可逆过程。
包括定容过程、定压过程、定温过程和绝热过程。
我们以1kg理想气体的闭口系统为例来分析这几种基本热力过程,分析方法包括5点:(1)依据过程特点建立过程方程式;(2)由过程方程和理想气体状态方程确定初、终态基本状态参数之间的关系,即P1、v1、T1和P2、v2、T2之间的关系;(3)绘制过程曲线;我们主要绘制两种坐标图P-v图和T-s图,因为P-v图上可以表示过程中做功量的多少,而T-s图上可以表示过程中吸收或放出热量的多少;(4)分析计算△u,△h,△s;(5)分析计算过程的热量q和功w。
一、定容过程定容过程即工质的容积在整个过程中维持不变,dv=0,通常是一定量的气体在刚性容器中进行定容加热或定容放热。
(1)依据过程特点建立过程方程式定容过程的特点是体积保持不变,所以建立过程方程式:v=常数;或dv=0或v1=v2(2)由过程方程和理想气体状态方程确定初、终态基本状态参数之间的关系过程方程式:v1=v2理想气体状态方程:112212Pv P v T T = 由以上两个方程可以得到初末基本状态参数之间的关系:122211v v P T P T =⎧⎪⎨=⎪⎩ 即定容过程中工质的压力与温度成正比。
(3)绘制过程曲线;定容过程有两种情况:定容加热和定容放热。
(4)分析计算△u ,△h ,△s ;2211v v u u u c dT c T ∆=-==∆⎰ 2211p p h h h c dT c T ∆=-==∆⎰ 222111ln ln ln p v v v P P s c c c v P P ∆=+=或222111ln ln ln v v T v T s c R c T v T ∆=+= (5)分析计算过程的热量q 和功w 。
容积变化功:210w Pdv ==⎰ 根据q=△u+w 可得:v q u c T =∆=∆总结:定容过程中系统与外界无容积变化功,加给工质的热量全部用于增加工质的热力学能,而没有热能与机械能的转化。
二、定压过程定压过程即工质的压力在整个过程中维持不变,dP=0,工程上使用的加热器、冷却器、燃烧器、锅炉等设备都是在接近定压的情况下工作的。
(1)依据过程特点建立过程方程式定压过程的特点是压力保持不变,所以建立过程方程式:P=常数;或dP=0或P 1=P 2(2)由过程方程和理想气体状态方程确定初、终态基本状态参数之间的关系过程方程式:P 1=P 2 理想气体状态方程:112212Pv P v T T = 由以上两个方程可以得到初末基本状态参数之间的关系:122211P P v T v T =⎧⎪⎨=⎪⎩ 即定压过程中工质的比容与温度成正比。
(3)绘制过程曲线;定压过程有两种情况:定压加热和定压放热。
T-s 图上曲线是对数曲线,从上图可知,定容过程与定压过程在T-s 图上都是对数曲线,但定压线的斜率小,更为平坦。
(4)分析计算△u ,△h ,△s ;2211v v u u u c dT c T ∆=-==∆⎰ 2211p p h h h c dT c T ∆=-==∆⎰ 222111ln ln ln p v p v P v s c c c v P v ∆=+=或222111ln ln ln p p T P T s c R c T P T ∆=-= (5)分析计算过程的热量q 和功w 。
容积变化功:22121211()w Pdv P v v Pv Pv RT RT R T ==-=-=-=∆⎰ 根据q=△u+w 可得:v p q u w c T R T c T =∆+=∆+∆=∆总结:工质在定压过程中吸入的热量等于焓的增加量,放出的热量等于焓的降低量。
三、定温过程定温过程即工质的温度在整个过程中维持不变,dT=0。
(1)依据过程特点建立过程方程式定温过程的特点是温度保持不变,所以建立过程方程式:T=常数;或dT=0或T 1=T 2(2)由过程方程和理想气体状态方程确定初、终态基本状态参数之间的关系过程方程式:T 1=T 2 理想气体状态方程:112212Pv P v T T = 由以上两个方程可以得到初末基本状态参数之间的关系:122112T T P v P v =⎧⎪⎨=⎪⎩ 即定温过程中工质的压力与比容成反比。
(3)绘制过程曲线;定容过程有两种情况:定容加热和定容放热。
(4)分析计算△u ,△h ,△s ;22110v v u u u c dT c T ∆=-==∆=⎰ 22110p p h h h c dT c T ∆=-==∆=⎰ 222111ln ln ln p T P P s c R R T P P ∆=-=-或222111ln ln ln v T v v s c R R T v v ∆=+= (5)分析计算过程的热量q 和功w 。
容积变化功:22221111ln ln v RT w Pdv dv RT v RT v v ====⎰⎰ 根据q=△u+w 可得:21ln v q w RT v == 总结:定温过程中内能变化为零,吸热量全部用于对外做膨胀功。
四、绝热过程绝热过程是指与外界无热量交换的过程,即0q δ=或q=0;(1)依据过程特点建立过程方程式0q δ=或q=0 另外根据revq ds T δ=得到:ds=0即可逆的绝热过程是熵不变的过程,定熵过程。
现实中严格的绝热过程是不存在的,但当过程进行的无限快时,工质与外界来不及换热,这种过程可近似认为是绝热的。
绝热过程的过程方程式有另外一种表达方式:P k v =常数 其中k pv c c =,是比热容比,又叫绝热指数,当比热取定值比热时,k 是与状态无关的常数。
(2)由过程方程和理想气体状态方程确定初、终态基本状态参数之间的关系过程方程式:1122k k Pv P v = 理想气体状态方程:112212Pv P v T T = 由以上两个方程可以得到初末基本状态参数之间的关系:22111211212211()()()kk k k P v P v T v T v T P T P --=== (3)绘制过程曲线;定容过程有两种情况:定容加热和定容放热。
(4)分析计算△u ,△h ,△s ;2211v v u u u c dT c T ∆=-==∆⎰ 2211p p h h h c dT c T ∆=-==∆⎰ 0s ∆=(5)分析计算过程的热量q 和功w 。
绝热过程q=0;根据q=△u+w 得:w=-△u=v c T -∆绝热(定熵)过程是内能与膨胀功之间的转换。
多变过程前面我们讨论的几种基本热力过程,定容、定压、定温和绝热,都会有一个参数保持不变,要么是体积,要么是压力、温度或熵。
但在实际热机中,有些过程,工质的状态参数都会有显著的变化,即PVT 没有一个是恒定不变的,而且工质与外界之间的换热量也不可以忽略不计,即s 也是变化的非绝热过程。
这时,我们就不能将实际过程简化为上述几种基本热力过程。
但通过实验发现,多数过程的P-v 关系曲线往往比较接近指数方程式,即 P n v =常数热力学中个,热力过程符合该式的变化过程称做多变过程。
其中,n 为多变指数,取值在(-∞,﹢∞)之间。
n 为定值。
实际的热力过程往往非常复杂,主要有两种情况:(1)整个过程并不完全符合P n v =常数,但整个过程中n 值变化不大,比如:前半段过程符合2P v =常数,中间段过程符合 2.1P v =常数,后半段过程符合2.2P v =常数,那么我们可以用一个不变的n 的平均值来代替实际中变化的n 。
(2)n 的变化较大时,则将热力过程分成几段,每一段作为一个n 不变的简单的多变过程。
我们对于多变过程的分析,同样有前面的5项内容。
(1)依据过程特点建立过程方程式多变过程的过程方程式为:P n v =常数这个方程式比较具有普遍性,将n 取不同的值,它可以代表前面我们讲的四种基本热力过程中的任意一种。
定压过程:n=0定容过程:n=±∞定温过程:n=1绝热过程:n=k(2)由过程方程和理想气体状态方程确定初、终态基本状态参数之间的关系过程方程式:1122n n Pv P v =理想气体状态方程:112212Pv P v T T = 由以上两个方程可以得到初末基本状态参数之间的关系:22111211212211()()()nn n n P v P v T v T v T P T P --=== (3)绘制过程曲线;在P-v 图和T-s 图上,可逆的多变过程是一条任意的双曲线,过程线的相对位置取决于n 的值,我们先把前面讲的四种基本热力过程的过程曲线画在图上,然后再找n 值不同时的曲线。
P-v 图和T-s 图上都以定容线为分界线,多变指数n 按顺时针方向递增。
在热机和制冷、热泵循环中,最常遇到的过程是介于1<n<k 之间,即大多数的实际热力过程介于定温和绝热过程之间。
(4)分析计算△u ,△h ,△s ;2211v v u u u c dT c T ∆=-==∆⎰ 2211p p h h h c dT c T ∆=-==∆⎰ 222111ln ln ln p T P P s c R R T P P ∆=-=-或222111ln ln ln v T v v s c R R T v v ∆=+=或222111ln ln ln p v p v P v s c c c v P v ∆=+=(5)分析计算过程的热量q 和功w 。
n n q c T =∆其中n c 称为多变比热1n v n k c c n -=- 根据根据q=△u+w 得:w=q-△u= ()1v v n k c c T n --∆- 过程曲线比较重要的一个作用是判断过程中△u 、w 、q 的正负。
1、判断△u 的正负以定温线为界,在T-s 图上,任何同一起点的多变过程,若变化曲线位于定温线上方,则△u 为正,若变化过程曲线位于定温线下方,则△u 为负。
在P-v 图上,任何同一起点的多变过程,若变化曲线位于定温线右上方,则△u 为正,若变化曲线位于定温线左下方,则△u 为负。
2、判断w 的正负以定容线为界,在T-s 图上,任何同一起点的多变过程,若变化曲线位于定容线右下方,则w 为正,若变化过程曲线位于定容线左上方,则w 为负。
在P-v 图上,任何同一起点的多变过程,若变化曲线位于定容线右方,则w 为正,若变化曲线位于定温线左方,则w 为负。
