肺部超声(心衰与ARDS鉴别)
ARDS

肺毛细血管内皮细胞损伤
II型肺泡细胞破坏
肺毛细血管通透性↑ 肺间质和肺泡水肿
PS ↓ 肺不张,透明膜形成
肺顺应性↓ 肺容积↓ 缺O2
V/Q比例失调 弥散功能障碍
六、临床特征
ALI/ARDS具有以下临床特征:
①急性起病,在直接或间接肺损伤后12-48h内发病; ②常规吸氧后低氧血症难以纠正;
急性呼吸窘迫综合征
(acute respiratory distress syndrome,ARDS) 同济医院重症医学科 李永胜
一、概念
ARDS是在多种原发病和诱因作用下发生的严重急
性呼吸衰竭,以非心源性肺水肿和顽固性低氧血症为特 征的综合征。
需要说明的几个问题: ● 概念的引出 1967年 Alshbugh首先提出 ● 急性而非成人:adult→acute,急性能反映ARDS起病的过程。 ● 急性肺损伤(acute lung injury, ALI)与ARDS是连续的病理 生理过程。有助于早期识别和早期处理。 ● ARDS是SIRS的肺部表现,MODS的一部分。
(二)呼吸支持治疗
1.氧疗
ALI/ARDS患者吸氧治疗的目的是改善低氧血 症,使动脉氧分压(PaO2)达到60-80mmHg。 可根据低氧血症改善的程度和治疗反应调整氧 疗方式,首先使用鼻导管,当需要较高的吸氧 浓度时,可采用氧气面罩。 ARDS患者往往低氧血症严重,大多数患者一 旦诊断明确,常规的氧疗常常难以奏效,机械 通气仍然是最主要的呼吸支持手段。
●
通气/血流(V/Q)比例失调
①V/Q ↓及真性分流
肺泡萎缩 间质肺水肿压迫小气道,小气道痉挛收缩 广泛肺不张、肺泡水肿,即真性分流。
ARDS诊断标准

一、关于急性呼吸窘迫综合征(acuterespiratorydistresssyndrome,ARDS)名称变迁和确定:1967年由ashbaugh首先提出了“发生于成人的呼吸窘迫综合征Acute Respiratory Distress Syndrome in Adult”来区别于“婴儿呼吸窘迫综合征(Infant Respiratory Distress Syndrome in Children)”。
4年后由petty等使用了“发生于成人的呼吸窘迫综合征”ARDS中的“a”指“adult”,ARDS诊断名词由此沿用下来。
20世纪80年代初,国内学者提出ARDS既可发生于成人,又可发生于儿童,所以把发生于成人的称为“成人型呼吸窘迫综合征(Acute Respiratory Distress Syndrome)”,而有别发生于儿童者,但未被国际学术界广泛接受。
1992年,美欧ARDS联合委员会(aecc)提出急性肺损伤(Acute Lung Injury, ALI)概念,ALI为ARDS前期,ARDS为ALI重度表现,将ARDS中的“a”由adult改为acute,中文译名相应改为“急性呼吸窘迫综合症”,英文缩写维持不变。
二、关于ARDS定义ARDS是由于多种原发病和诱因作用下发生的急性呼吸衰竭,以非心源性肺水肿和顽固性低氧血症为特征。
表现为严重呼吸困难,呼吸窘迫;是全身炎症反应综合征(Systemic Inflammatory Response Syndrome, SIRS),代偿性抗炎反应综合征(Compensatory Antiinflammatory Response Syndrome, CARS),在肺部的表现,其病理基础是ALI,常引发或合并多脏器功能障碍综合征(Multiple Organ Dysfunction Syndrome, MODS)甚至多脏器功能衰竭(Multiple Organ Failure, MOF),是临床常见的急危病。
急性呼吸窘迫综合征(ARDS)的-影像学表现

Fig. 3. Computed tomogram in ARDS shows bilateral reticulation and ground-glass opacification, containing areas of bronchial dilatation in the upper lobes. In the acute phase of ARDS, bronchial dilatation may indicate fibrosis or may be reversible.
ARDS肺部CT检查中涉及的重要概念
病变的CT表现不均匀,因上侧、肺腹侧重量增加而导致下侧、肺背侧压缩性不张 (该理论已被患者体位由仰卧位转到俯卧位后浓度梯度快速重新分配所证实)。 ARDS早期(<1周)典型肺部CT表现:仰卧位,肺部阴影自腹侧到背侧、从头 侧到足侧的密度梯度,即从非重力依赖区( non-dependent )正常或过度膨胀的 肺脏移行过渡为弥漫性磨玻璃影,直至重力依赖区(dependent)的致密实变影。
图A ARDS病人,CT显示双肺重力依赖区实变 ,以及在非重力依赖区肺野的磨玻璃影。
图B 同一病人在1年后的随访显示实变和 磨玻璃影消散,伴左肺前部囊肿形成。
A: Computed tomogram shows bilateral dependent consolidation in a patient with ARDS, as well as ground-glass opacities in the non-dependent lung. B: Follow-up computed tomogram after 1 year shows resolution of the consolidation and ground glass opacification with cyst formation in the anterior left lung.
肺部超声的临床应用及研究进展

肺部超声的临床应用及研究进展在现代医学的领域中,各种诊断技术不断发展和创新,为疾病的诊断和治疗提供了越来越多的可能性。
肺部超声作为一种新兴的诊断手段,正逐渐在临床中展现出其独特的价值和广阔的应用前景。
过去,肺部被认为是超声检查的“禁区”,主要是因为肺部充满气体,声波在气体中会发生强烈的反射和散射,难以获得清晰的图像。
然而,随着技术的进步和对肺部超声原理的深入理解,这一“禁区”正在被逐渐打破。
肺部超声在临床中的应用范围广泛。
在呼吸系统疾病的诊断方面,它对于肺炎的诊断具有重要意义。
通过超声图像,可以观察到肺部实变的区域、有无胸腔积液等特征性表现。
对于急性呼吸窘迫综合征(ARDS)的患者,肺部超声能够及时发现肺部的水肿、肺泡的塌陷等病变,为治疗方案的制定提供依据。
而且,在慢性阻塞性肺疾病(COPD)的评估中,肺部超声可以帮助医生了解肺过度充气的程度以及小气道的病变情况。
在重症监护领域,肺部超声更是发挥着不可或缺的作用。
对于重症患者,尤其是那些无法进行频繁移动的患者,肺部超声具有明显的优势。
它可以在床边快速进行,无需将患者转运至专门的超声检查室,大大减少了检查过程中的风险。
在监测机械通气患者的肺部情况时,肺部超声能够实时评估肺的顺应性、有无气胸等并发症,有助于及时调整通气参数,提高治疗效果。
此外,肺部超声在诊断肺栓塞方面也有一定的价值。
虽然它不能直接看到栓塞的血管,但可以通过间接征象,如右心功能的改变、肺动脉高压的表现等,为肺栓塞的诊断提供线索。
在研究进展方面,肺部超声的技术不断改进和完善。
图像分辨率的提高使得对肺部细微结构的观察更加清晰,有助于发现早期的病变。
同时,新的超声探头和成像模式的出现,也进一步拓展了肺部超声的应用范围。
例如,三维肺部超声能够更全面地展示肺部的整体结构,为疾病的评估提供更丰富的信息。
另外,肺部超声与其他诊断技术的联合应用也成为研究的热点。
将肺部超声与胸部 X 线、CT 等检查相结合,可以取长补短,提高诊断的准确性。
急性呼吸窘迫综合征(ARDS)的影像表现

急性呼吸窘迫综合征(Acute Respiratory Distress Syndrome)成人呼吸窘迫综合征(ADULT RESPIRATORY DISTRESS SYNDROME ,ARDS)•ARDS,不是一个独立的呼吸系统疾病。
•它是一种继发于机体严重损伤时出现的以急性、进行性、缺氧性呼吸窘迫(困难)及顽固性低氧血症为临床特征的综合征,是急性呼吸衰竭的一种类型。
与急性呼吸窘迫综合征 (Acute Respiratory Distress Syndrome,ARDS)此综合征曾被称为成人透明膜肺、休克肺、创伤肺、肺毛细血管渗透综合征等。
以上命名均有局限,不能反映该综合征本质及重要临床特征。
ARDS不仅发生于成人,也见于儿童。
ARDS的概念演变第一次世界大战 1914-1918 创伤相关性大片肺不张第二次世界大战 1939-1945 创伤性湿肺越南战争 1961-1975 休克肺1967 Ashbaugh首先报道 Acute Respiratory Distress Syndrome in adult1971 Petty正式称为 Adult Respiratory Distress Syndrome,ARDS1992 美国胸科协会提出将此征命名为 Acute Respiratory Distress Syndrome,ARDS 1994 欧美ARDS会议 Acute Lung Injury (ALI.急性肺损伤)ARDS = 严重的ALIAdult → Acute(同时发生于小孩)2000年美国心肺与血液研究院(NHBLI)的ARDS net多中心系列研究2011年10月德国柏林欧洲重症医学年会Ranieri教授提出ARDS新的诊断标准-柏林标准A R D S病因、病理、发病机制•严重肺部感染•胃内容物吸入•肺挫伤•吸入有毒气体•淹溺•氧中毒•严重感染•严重的非胸部创伤•急性重症胰腺炎•大量输血•体外循环•弥漫性血管内凝血间接肺损伤因素病 因发病机制及病理ARDS发病机制比较复杂,目前仍在研究之中较统一的认识:为各种病因直接或通过炎症反应→毛细血管内皮细胞和肺泡壁Ⅱ型上皮细胞。
重症肺部超声

重症肺部超声肺部超声(Lung Ultrasound)是一种非侵入性的影像学检查方法,利用超声波技术来获得对肺部组织结构和功能的详细信息。
近年来,肺部超声在重症医学领域得到了广泛应用,并显示出了其在评估和诊断重症患者肺部病变方面的独特优势。
本文将介绍肺部超声在重症情况下的应用及其意义。
一、肺部超声的原理与技术肺部超声是通过超声传感器发出超声波并接收其反射信号来生成影像。
由于肺部组织的气体含量较高,使得常规超声波在肺部的传播受到阻碍。
因此,肺部超声通常采用B模式(Brightness Model)或M模式(Motion Model)进行检查。
在B模式下,肺部超声可以显示肺间质、肺脏表面、胸膜和肺部血管等结构。
通过调整超声波的频率和探头的方向,可以获得不同角度和深度的图像,帮助医生进行准确定位和评估。
M模式是一种时间-深度图像,在某一特定位置追踪动态变化的过程。
通过M模式,可以观察患者的肺部运动情况,如胸膜游离,膈动及呼吸运动的幅度和频率等。
二、肺部超声在重症医学中的应用1. 肺部积液和肺水肿的评估肺部超声可以快速准确地评估患者是否存在肺部积液或肺水肿。
肺部积液在超声图像上呈现为位于肺叶间的黑色区域,而肺水肿则可观察到肺泡水肿和胸膜间质增厚等特征。
通过肺部超声,医生可以及时诊断和监测患者的肺部病变,为及早干预提供依据。
2. 气胸的检测和定位气胸是一种严重的急症,如果不及时处理可能会导致氧合不足和呼吸衰竭。
肺部超声可以迅速检测和定位气胸的存在。
在超声图像中,气胸呈现为无声阴影,通过扫描不同的区域,医生可以确定气胸的范围和位置,指导穿刺引流或其他治疗措施。
3. 急性呼吸窘迫综合征(ARDS)的监测ARDS是一种严重的肺部疾病,常见于重症监护病房。
肺部超声可以评估患者的肺不张和肺泡充气情况,及时发现ARDS的存在并跟踪疾病的进展。
此外,肺部超声还可以检测肺内纤维化、肺尘埃沉积等病变,为ARDS的诊断和治疗提供重要参考。
ards的定义及诊断标准

ards的定义及诊断标准
ARDS是一种严重的肺部疾病,也称为急性呼吸窘迫综合症,通常是由于感染、创伤或心血管系统的疾病引起的肺部炎症和水肿。
以下是ARDS的诊断标准:
1. 急性呼吸衰竭发生时间小于一周;
2. 患者的动脉血氧分压(PaO2)/吸入氧浓度(FiO2)比值小于或等于
300mmHg,或小于100mmHg(不接受氧气的情况下);
3. 必须通过肺容积法、X线、CT等检查来排除左心衰竭;
4. 必须有肺充血的证据,包括肺内阻力增加、弥散障碍、体液外渗及肺泡膜损伤等。
如果符合以上标准,即可诊断患者患有ARDS。
同时,还需要进行相关的检查,如血液检查、血气分析和呼吸功能测试等,以进一步鉴定病情和制定治疗方案。
危重患者的肺部超声检查

・综述・危重患者的肺部超声检查张丹 席修明 正常肺组织因含气体,超声波不能在其间传导。
因此,在正常情况下声像图难以显示正常的肺内结构,只有在周边肺组织发生病变时,声像图才可显示。
目前,肺部的超声检查多用于周边肺组织肿瘤的囊实性鉴别及肺癌与其他良性病变的观察。
急性肺损伤(acute lung injury,AL I)或急性呼吸窘迫综合征(acute res p irat ory distress syndr ome,ARDS)(简称AL I/ARDS)是患者原心肺功能正常,由于肺外或肺内严重疾病导致的急性渗透性肺水肿和进行性缺氧。
虽其病因各异,但肺组织损伤的病理和功能改变大致相同。
临床表现均为急性呼吸窘迫和难治性低氧血症。
AL I/ARDS起病急骤,发展迅猛,如不及早诊治,其病死率高达50%以上(25%~90%),常死于多脏器功能衰竭。
1995年,L ichtenstein[1]首先报道床边胸部超声检查对危重患者的诊断价值,之后多篇关于AL I/ARDS患者肺部超声改变的报道认为,在AL I/ARDS早期超声检查优于X线胸片及CT检查。
本文将相关文献综述如下。
一、正常肺部的扫查方法及声像图特点1.肺部超声扫查的基本方法:超声扫查分为4个步骤,第1步为仰卧位,扫查前胸壁,观察有无气胸或肺气肿;第2步仍为仰卧位,扫查范围从前胸壁扩展到侧壁,观察有无胸腔积液和肺部实变;第3步,略抬高患者的同侧身体,尽可能向背部扫查,在这个体位可以观察到在前两步检查看不到的少量胸腔积液和小片实变区;第4步为完全侧卧位或坐位检查,观察整个背部。
其中第3步和第4步可以简化为一步,即抬高患者的同侧身体,做背部扫查。
2.正常肺的声像图特点:肺是含气性器官,胸膜和肺泡壁与肺泡内气体的交界部构成软组织与气体之间的界面。
超声在穿过两种不同声阻抗组织构成的界面时,当声阻抗差大于0.1%,即产生反射。
反射的强弱取决于两种组织声阻抗差的大小。
ARDS

斑片状阴影以周边肺野多见,可见气 心影常增大,以肺门为中心的 柱征。 蝶翼状斑片影,治疗后消失快。
抗 心衰治疗无效,常规吸氧难以纠 正低氧
抗心衰治疗有效,常规吸氧可 纠正低氧
鉴别非心源性肺水肿
ARDS是非心源性肺水肿的一种,但非心源性肺水肿决非仅为ARDS,
尚可见于多种情况。 输液过量
血浆胶体渗透压降低如肝硬化、肾病综合征等。
SIRS发病机制
致病因素
直接组织损伤
激活炎症细胞(中性粒、巨噬)
炎症介质释放(TNF-a、IL-1等)
免疫功能失调(炎症介质或抗炎介质过度释放)
血管内皮细胞损害,毛细血管通透性增加,内源性凝血启动,血小板黏附(PLT 减少),纤维蛋白沉积(微血栓)
局部组织及远隔器官的损害(肺、肝、肾、脑等)
MODS
由于ARDS患者大量肺泡塌陷,肺容积明显减少,常规或大潮气量通气 (10~15ml/kg)易导致肺泡过度膨胀和气道平台压过高,加重肺及肺外器官的损 伤。
(二) 呼吸支持治疗
气道平台压能够客观反映肺泡内压,其过度升高可导致呼吸机相关肺损伤 5项多中心RCT研究显示:
若按气道平台压分组(<23、23~27、27~33、>33cmH2O),随气道平台压升高, 病死率显著升高(P=0.002)。 而以气道平台压进行调整,不同潮气量通气组(5~6、7~8、9~10、11~12ml/kg) 病死率无显著差异(P=0.18),并随气道平台压升高,病死率显著增加(P<0.001) 。
NIV禁忌症
①神志不清
②血流动力学不稳定 ③气道分泌物明显增加而且气道自洁能力不足 ④因脸部畸形、创伤或手术等不能佩戴鼻面罩
⑤上消化道出血、剧烈呕吐、肠梗阻和近期食管及上腹部手术
ards柏林诊断标准及分级

ARDS即急性呼吸窘迫综合征,ARDS柏林定义是指2012年发表在《美国医学会杂志》的关于ARDS的新定义,具体的定义和诊断标准如下。
一、定义:
1、发病时机:已知临床诱因后,或新出现或原有呼吸系统症状加重后1周内发病;
2、胸部影像学检查:通过胸片或CT扫描,可观察到双肺透光度减低,且不能完全用胸腔积液、肺叶不张或结节解释;
3、肺水肿来源:无法用心功能衰竭或液体负荷过多解释的呼吸衰竭,如果没有危险因素,则需要客观评估(如心脏超声检查)排除静水压升高的肺水肿。
二、诊断标准:柏林定义依据患者的不同氧合情况,将病情分为轻、中和重度。
1、轻度:PEEP/CPAP≥5cmH20时,200mmHg<PaO2/FiO2≤300mmHg;
2、中度:PEEP/CPAP≥5cmH20时,100mmHg<PaO2/FiO2≤200mmHg;
3、重度:PEEP/CPAP≥5cmH20时,PaO2/FiO2≤100mmHq。
CPAP即持续气道正压,PEEP即呼气末正压,如果海拔超过1000m,应根据如下公式进行校正:[PaO2/FiO2 X(大气压/760)]。
ARDS柏林的诊断标准解读

表1 ARDS柏林的诊断标准指标数值起病时间从已知临床损害,以及新发或加重呼吸系统症状至符合诊断标准时间,≤7 d胸部影像学*双侧浸润影,不能用积液、大叶/肺不张或结节来完全解释肺水肿原因呼吸衰竭不能用心力衰竭或液体过度负荷来完全解释;如无相关危险因素,需行客观检查(如超声心动图)以排除静水压增高型肺水肿氧合情况#轻度△:PEEP或CPAP≥5 cm H2O时,200 mm Hg<PaO2/FiO2≤300 mm Hg;中度:PEEP≥ 5 cm H2O时,100 mm Hg <PaO2/FiO2≤200 mm Hg;重度:PEEP≥5 cm H2O时, PaO2/FiO2≤100 mm Hg注:*胸部影像学包括胸片或CT;#如果海拔超过1000 m,PaO2/FiO2值需用公式校正,校正后PaO2/FiO2=PaO2/FiO2×(当地大气压/760);△轻度ARDS组,可用无创通气时输送的持续气道正压;CPAP:持续气道正压;FiO2:吸入氧分数;PEEP:呼气末正压;1 mm Hg=0、133 kPa;1 cm H2O=0、098 kPa柏林定义沿用了1994年欧美ARDS专题研讨会(AECC)制订的诊断ALI/ARDS 的4项标准[7],简单易记,方便临床应用。
粗瞧起来,与AECC标准改变不大,但仔细比较有以下不同。
1.对“急性”的概念做出明确时间规定,从已知临床损害至符合诊断标准时间≤7 d。
Hudson等[8]对695例危重病的调查发现,脓毒症(sepsis)与创伤患者在24 h内发生ARDS的分别为54%与29%;在ARDS危险因素出现后的5 d内,90%以上患者发生ARDS;到7 d时,所有患者均发生ARDS。
这有利于ARDS与间质性肺疾病的鉴别,因后者的发生常历时数周至数月,而且病因不明。
2.胸部影像学:AECC标准只提X线胸片“双侧浸润影”,过于笼统,在不同瞧片者之间对同一胸片常缺乏一致的可靠解释。
ARDS诊断和治疗指南

直接因素(肺内ARDS)
肺或胸部挫伤
间接因素(肺外ARDS)
败血症,脓毒症 严重的非胸部创伤 休克
危 险 因 素
误吸 淹溺
严重肺部感染 吸入有毒气体
氧中毒 脂肪栓塞 肺移植再灌注损伤
大量输血(输液) 重症胰腺炎
药物过量 体外循环 DIC
临床症状与体征
1. 2. 急性起病,在直接或间接肺损伤后12-48h内发病;常规吸氧低氧血症难以纠正 肺部体征无特异性,急性期双肺可闻及湿啰音或呼吸音减低
定义变迁
第一次世界大战 1914-1918 创伤相关性大片肺不张
第二次世界大战 1939-1945
越南战争 1967 1992 1961-1975
创伤性湿肺
休克肺
Ashbaugh首次报道 Adult Respiratory Distress Syndrome AECC欧美联席会议 Adult → Acute Acute Lung Injury (ALI)
2 2
气流为减速波,可以使肺泡内的气体分布更均匀,有利于肺泡复张
肺复张注意事项
1. 2. 3. 4. 动脉收缩压低于90mmHg或下降30mmHg HR达140次/分或增加20次/分 SpO2下降至90%以下或下降超过5% 出现心律失常
肺复张效果判定:影像学、功能学和力学判断肺的可复张性
1. 动脉血氧合:当FiO2为100%,PaO2 >350 ~ 400 mm Hg或反复肺复张后
气道平台压能够客观反映肺泡内压,其过度升高可导致呼吸机相关肺损伤
若按气道平台压分组(<23、23~27、27~33、>33cmH2O),随气道平台压升高,病死率显著升高
(P=0.002)。而以气道平台压进行调整,不同潮气量通气组(5~6、7~8、9~10、11~12ml/kg)病死率无
ARDS2012诊断标准

Trauma
SARS
ARDS概念的转变
1967年Ashbaugh第一次提出了成人呼吸窘迫综合征(ARDS) 1.呼吸频率增快 2.低氧血症 3.肺顺应性下降 4.常规呼吸支持治疗效果较差
Acute respiratory distress in adults. Lancet. 1967; 2(7511):319-323
时 间
首先看看对起病时间的界定。 我们发现,ARDS的常见危险因素出现后,在 一周之内累积ARDS的发病率逐渐接近于 100%,也就是说可以将1W以内作为ARDS的 诊断时间点。
胸部影像学改变
1.仍然认定双肺浸润改变诊断ARDS 2.可以行CT检查较胸片更准确 3.病变累及的范围(≥3/4肺野)可能作为重度ARDS诊断的 附加标准
AECC诊断标准的局限
AECC定义 时间 急性起病 AECC局限性 柏林定义修正 缺乏“急性”定义 指定的急性时
4
限
ALI分类
PaO2/FiO2
当PaO2/FiO2=201 通过严重程度
<300mmHg
-300时,容易混淆 分为3个不同的
AIL和ARDS 亚型,并去除 ALI
AECC诊断标准的局限
Interobserver variation in interpreting chest radiographs for the diagnosis of acute respiratory distress syndrome. Am J Respir Crit Care Med 2000; 161:85–90
AECC诊断标准的局限
AECC定义 PAWP 测量 PAWP≤18m AECC局限性 高PAWP与ARDS可 能同时存在 柏林定义修正 去除PAWP; 定义为非流体静力型肺
肺部超声

胸腔积液
胸腔积液
胸腔积液 镜像伪影
胸腔积液 镜像伪像
胸腔积液 右侧胸腔积液
胸腔积液 如何判断胸腔积液量 脏层和壁层胸膜的距离大于3CM,积液量至少 大于500CC
脏层和壁层胸膜的距离大于1CM,可进行胸腔 穿刺术
肺实变 如何看
肺实变产生的原因 肺水肿(水分) 肺炎(脓)
肺挫伤(血液)
第三步:识别胸膜
第四步:寻找肺滑动征象
“ A” 线
充气的肺组织 下可以看见A线
A线可能出现的病理情况
气胸 扫描技术
气胸 胸膜滑动征 胸膜滑动征可排除气胸 (但紧限于排除探头下方的图像)
为提高敏感性,因在每侧胸部多个肋间隙 进行扫描
气胸 无胸膜滑动征的其他可能原因 呼吸减弱 呼吸暂停 肺炎 肺不张 胸膜粘连 胸膜固定术史 右主支气管插管
气胸 肺点征(前沿征)
诊断气胸的特异度达到 99%
气胸 肺点=气胸
气胸 M型超声检查气胸
使用线性探头和 M 型 超声
气胸 M型超声检查气胸(海岸征)
气胸 M型超声检查气胸(条码征)
肺水肿
肺部超声伪影:A线和B线
肺水肿 肺部超声伪影A线和B线
肺水肿 B线产生的病因 心衰、肾衰、肝失代偿下的容量负荷过重 肺炎 肺挫伤 ARDS急性肺损伤 正常情况可见于下肺叶(由于气血比例失衡)少 量 B线
a线和b线32肺水肿肺部超声伪影a线和b线33肺水肿b线产生的病因心衰肾衰肝失代偿下的容量负荷过重肺炎肺挫伤ards急性肺损伤正常情况可见于下肺叶由于气血比例失衡少量b线34胸腔积液35胸腔积液36胸腔积液镜像伪影37胸腔积液镜像伪像38胸腔积液右侧胸腔积液39胸腔积液如何判断胸腔积液量脏层和壁层胸膜的距离大于3cm积液量至少大于500cc脏层和壁层胸膜的距离大于1cm可进行胸腔穿刺术40如何看41肺实变产生的原因肺水肿水分肺炎脓肺挫伤血液肿瘤细胞42此区域内的肺的含气区被可透过超声的物质填充43是实变还是镜像伪影45是实变还是镜像伪影46肺超声bule策略47腹部超声blue策略的诊断流程图48肺部超声bule策略诊断的流程图49
肺部超声检查
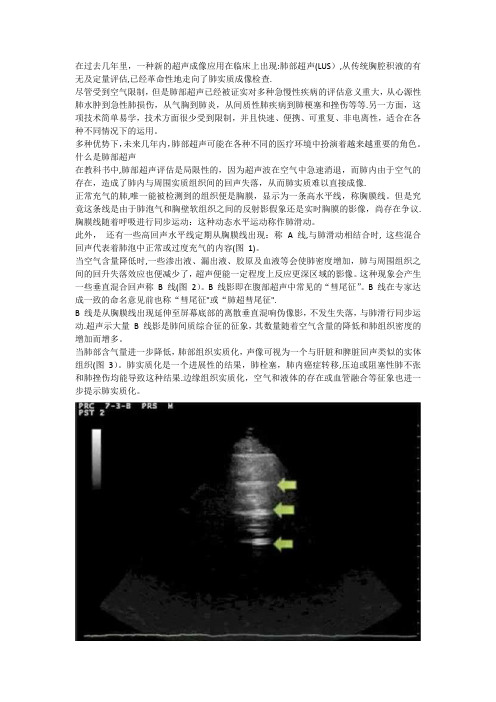
在过去几年里,一种新的超声成像应用在临床上出现:肺部超声(LUS),从传统胸腔积液的有无及定量评估,已经革命性地走向了肺实质成像检查.尽管受到空气限制,但是肺部超声已经被证实对多种急慢性疾病的评估意义重大,从心源性肺水肿到急性肺损伤,从气胸到肺炎,从间质性肺疾病到肺梗塞和挫伤等等.另一方面,这项技术简单易学,技术方面很少受到限制,并且快速、便携、可重复、非电离性,适合在各种不同情况下的运用。
多种优势下,未来几年内,肺部超声可能在各种不同的医疗环境中扮演着越来越重要的角色。
什么是肺部超声在教科书中,肺部超声评估是局限性的,因为超声波在空气中急速消退,而肺内由于空气的存在,造成了肺内与周围实质组织间的回声失落,从而肺实质难以直接成像.正常充气的肺,唯一能被检测到的组织便是胸膜,显示为一条高水平线,称胸膜线。
但是究竟这条线是由于肺泡气和胸壁软组织之间的反射影假象还是实时胸膜的影像,尚存在争议.胸膜线随着呼吸进行同步运动:这种动态水平运动称作肺滑动。
此外,还有一些高回声水平线定期从胸膜线出现:称 A 线,与肺滑动相结合时, 这些混合回声代表着肺泡中正常或过度充气的内容(图1)。
当空气含量降低时,一些渗出液、漏出液、胶原及血液等会使肺密度增加,肺与周围组织之间的回升失落效应也便减少了,超声便能一定程度上反应更深区域的影像。
这种现象会产生一些垂直混合回声称B 线(图2)。
B 线影即在腹部超声中常见的“彗尾征”。
B 线在专家达成一致的命名意见前也称“彗尾征"或“肺超彗尾征".B 线是从胸膜线出现延伸至屏幕底部的离散垂直混响伪像影,不发生失落,与肺滑行同步运动.超声示大量B 线影是肺间质综合征的征象,其数量随着空气含量的降低和肺组织密度的增加而增多。
当肺部含气量进一步降低,肺部组织实质化,声像可视为一个与肝脏和脾脏回声类似的实体组织(图3)。
肺实质化是一个进展性的结果,肺栓塞,肺内癌症转移,压迫或阻塞性肺不张和肺挫伤均能导致这种结果.边缘组织实质化,空气和液体的存在或血管融合等征象也进一步提示肺实质化。
肺损伤超声评分在ARDS患者中的临床应用价值

肺损伤超声评分在ARDS患者中的临床应用价值吴敬医;张霞;王涛;刘华;袁荆;王箴;鲁卫华【期刊名称】《实用医学杂志》【年(卷),期】2015(31)24【摘要】目的:探讨肺损伤超声评分在急性呼吸窘迫综合征(ARDS)患者中的临床应用价值.方法:前瞻性收集2013年1月至2015年2月收治于本院ICU且符合条件的ARDS患者,行肺损伤超声评分,以胸部CT为“金标准”,评价超声对肺不张/实变的诊断价值,并采用Pearson相关性检验比较肺损伤超声评分与氧合指数、ARDS的诊断相关性,ROC曲线法判断肺损伤超声评分预测重度ARDS的阈值.结果:共纳入32例ARDS患者,11例完成先后2次CT和超声评分,共进行43次检查、评分,检查516个肺区.CT诊断肺不张/实变123区,超声诊断有106区,超声诊断的敏感性、特异性、阳性预测值、阴性预测值以及诊断正确率分别为76.4%、96.9%、88.6%、92.9%、92.1%,肺损伤超声评分与氧合指数有相关性(r=-0.552).11例患者治疗前后的对比研究发现超声评分与氧合指数有相关性(r=-0.658).以超声评分23.5为阈值判断重度ARDS的ROC曲线下面积为0.777,敏感性为87.1%,特异性58.1%.结论:肺损伤超声评分可用于ARDS患者的肺损伤评估、动态观察,值得临床推广.【总页数】4页(P4065-4068)【作者】吴敬医;张霞;王涛;刘华;袁荆;王箴;鲁卫华【作者单位】241000 安徽省芜湖市,皖南医学院弋矶山医院ICU;241000 安徽省芜湖市,皖南医学院弋矶山医院超声医学科;241000 安徽省芜湖市,皖南医学院弋矶山医院ICU;241000 安徽省芜湖市,皖南医学院弋矶山医院超声医学科;241000 安徽省芜湖市,皖南医学院弋矶山医院ICU;241000 安徽省芜湖市,皖南医学院弋矶山医院ICU;241000 安徽省芜湖市,皖南医学院弋矶山医院ICU【正文语种】中文【相关文献】1.肺损伤预测评分在ALI/ARDS早期诊断中的应用 [J], 夏炎火;童秋玲;林锡芳;王丹;朱海萍;戴震宇2.格拉斯哥昏迷-瞳孔反应评分在ICU重型颅脑损伤患者中的临床应用价值 [J], 余菲;张琳3.肺部超声评分在ARDS患者中临床应用价值 [J], 张磊;陈国忠;王华英;姚丽娜;周成杰;安敏飞;俞万钧4.肺损伤超声评分在急性呼吸窘迫综合征患者中的临床应用 [J], 刘荔龙5.功能残气量与肺部超声评分在ARDS俯卧位通气患者中的应用效果评价 [J], 金永浩;李晓东;李甜;胡占升;邸兴伟因版权原因,仅展示原文概要,查看原文内容请购买。
ARDS和CPE:不再傻傻分不清

ARDS和CPE:不再傻傻分不清急性呼吸窘迫综合征(ARDS)多发生于心肺功能正常的患者,由于肺外或肺内的严重疾病引起肺毛细血管炎症性损伤,通透性增加,继发急性高通透性肺水肿和进行性缺氧性呼吸衰竭,被称为「休克肺」、「非心源性肺水肿」、「白色肺综合征」。
主要表现为突发性进行性呼吸窘迫、气促、发绀,常伴有烦燥、焦虑、出汗等症状。
其呼吸窘迫的特点是呼吸深快,伴明显的紫绀,而且不能用通常的吸氧疗法改善。
早期体征可无异常,或仅闻少量细湿罗音,后期可闻水泡音或管状呼吸音等。
心源性肺水肿是指心脏瓣膜、心肌等出现损伤引起心肌收缩力降低进而导致肺部循环障碍,表现为缺氧、呼吸困难、肺水肿等。
X 线表现为典型的蝶翼征改变,与ARDS 相似,但该病有心脏病史,不能平卧,端坐呼吸,咳粉红色泡沫样血痰,心影明显增大,常伴有胸膜腔积液及间隔线,短期内病变改变明显。
而ARDS 可以平卧,肺部病变变化较慢,多无间隔线出现[1]。
急性呼吸窘迫综合征与心源性肺水肿临床表现相似,各种辅助检查包括X 线胸片、血气分析均有相似或明显重叠。
血流动力学指标,如心排血量、肺毛细血管楔压,也并不是在任何情况下都能对二者准确鉴别[2]。
通常使用快速正性肌力药物西地兰和能一过性增加容量负荷的药物甘露醇,观察其治疗反应来鉴别。
首先,ARDS 的病发部位主要是在肺部的大血管和微血管。
心源性肺水肿的病变主要在心肌,而洋地黄类药物在人体只对衰竭的心肌呈正性肌力作用,有改善临床症状的效果,对正常心肌的正性肌力作用则并无改善临床症状的效果。
注射西地兰后症状缓解提示有心源性肺水肿存在。
其次,使用西地兰后静滴 20% 甘露醇,其作用在于渗透压和血容量负荷。
前者对肺血管和心肌无不良后果,而超容量负荷常易累及心脏功能。
静滴甘露醇后未呼吸、心率的不良变化,提示当时心肌功能良好;如出现恶化表现则意味患者原来隐匿的心源性肺水肿被诱发。
在临床治疗过程中发现,ARDS 患者即使没有心脏病史,也可能会由于心肌收缩力降低引发心源性肺水肿并发。
ARDS患者的结构化诊断流程

ARDS患者的结构化诊断流程因急性呼吸衰竭入住ICU的患者通常符合ARDS的标准。
诊断基于“柏林定义”(中描述的放射学、生理学和临床标准。
然而,确定急性呼吸窘迫综合征的诊断本身的治疗结果有限,因为现有的循证干预措施主要与尽量减少医源性损伤(例如,呼吸机引起的肺损伤[VILI]和液体超负荷)有关,而不是使用特定的治疗方法。
虽然该综合征本身的干预选择有限,但对基础病因进行充分和及时的治疗对ARDS患者结局的改善有重大影响。
ARDS的经典描述依赖于继发于其他疾病的弥漫性肺泡损伤的组织学发现(表1中描述的临床危险因素之一)。
弥漫性肺泡损伤是无法治愈的发现,必须与大量同样符合ARDS综合征定义但可治疗的疾病相鉴别。
表2概述了疑似ARDS患者必须考虑的鉴别诊断。
绝大多数ARDS患者在发病后7天内应该可以建立明确的病因诊断。
然而,临床现实往往是混乱的,这可能导致对根本原因的延迟和草率的寻找,特别是对有多个重要问题的病人。
本综述旨在为符合柏林定义的ARDS标准的患者提供一个结构化的诊断方法,以使潜在的原因能够得到快速和充分的治疗。
诊断步骤分三个阶段逐点描述,并在流程图中进行了总结。
我们还总结了与临床医生管理ARDS患者有关的最重要的不确定因素。
ARDS患者的诊断步骤流程图。
*包括接触药物、动物、有毒烟气、吸烟。
**胸部计算机断层扫描(CT)的高分辨率(HR)图像,最好有吸气保持。
***qPCR定量聚合酶链反应,CMV巨细胞病毒,BAL支气管肺灌洗,ILD间质性肺病。
通过这里描述的步骤和时间框架,我们打算在必要时进行早期和积极的诊断性检查,以及在适当时采取更简单的方法之间取得平衡。
然而,作者的经验是植根于资源丰富的学术医学环境中。
因此,我们方法的细节应适应当地的资源和可能性。
这里描述的方法最重要的方面不是实验室检查或成像方式的数量,而是诊断评估的结构化和及时性。
ARDS的诊断ARDS 的诊断主要基于缺氧性呼吸衰竭和肺水肿的检测,必须从中排除静水性心源性肺水肿。
ARDS 诊断标准

ARDS 诊断标准《广东省医疗常规汇编》acute respiratory distress syndrome 的缩写急性呼吸窘迫综合征(注:很多人说成人adult 呼吸窘迫综合征是不对的,早在93年已修正,老病名还有“湿肺”“休克肺”“肺透明膜病”)摘自《广东省医疗诊疗常规汇编》2002年出版李培武医师协助摘录整理【诊断】一、临床表现(一)具有ARDS的高危因素。
(二)进行性呼吸频数和/或呼吸窘迫。
(三)肺湿罗音,或实变体征,紫绀。
(四)X线表现为双侧肺部出现斑片状乃至融合的大片状阴影,两肺呈广泛实变,可见支气管充气相。
二、诊断标准 93年欧美ARDS专题联席会议标准国内亦沿用此标准(一)具有发病的高危因素。
(二)急性起病,呼吸频数和呼吸窘迫。
(三)难以纠正的低氧血症;氧合指数PaO2/FiO2≦200mmHg(26.7kPa,不论PEEP高低)。
(四)正位X线胸片可显示双肺浸润影。
(五)临床排除左心衰或肺毛细血管禊压(PCWP)≦18mmHg(2.39kPa)。
凡符合以上五项可诊断ARDS。
如PaO2/FiO2≧200≦300mmHg则称为急性肺损伤(ALI,acute lung injury)。
#2 最基本的概念要点患者原来心肺功能正常由于肺内或肺外原因引起肺泡上皮细胞损伤肺毛细血管通透性增加导致严重呼吸困难、窘迫,顽固性低氧血症,肺顺应性降低,渗出性肺水肿病理学基础是弥漫性肺损伤#3 【治疗要点】简要!一、治疗原发病。
二、氧疗与机械通气(一)氧疗要保证机体的氧供应,维持动脉血氧分压大于60mmHg(8kPa)或氧饱和度大于90%,在患者开始恢复时,在保证氧合的情况下,吸入氧浓度尽快降至0.6以下。
(二)机械通气为保证患者的氧合功能,吸入氧浓度大于0.5时,机械通气往往不可避免。
在ARDS中机械通气的模式并没有统一标准。
1.无创人工通气:早期可试用无创面罩人工通气:包括有持续正压通气(CPAP)和双相正压通气(BiPAP),CPAP尽可能小于20cmH2O,BiPAP 设置建议IPAP10——30 cmH2O、EPAP4——10 cmH2O。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Lung ultrasound How I do
什么是肺部超声
设备,扫描技术
肺部超声的解读
肺部正常超声表现
蝙蝠征
肺部正常超声表现
A线 与胸膜平行 等间距 逐渐减弱
沙滩征(M型)
肺部正常超声表现
B线 自胸膜发出 垂直胸膜 彗星尾征
在一个切面<3个
肺部正常超声表现
胸膜滑动征
肺部正常超声表现
肺搏动征/肺脉
心脏搏动引起的
肺的运动
肺部异常超声表现
B线
肺组织实变
胸膜下结节
胸膜改变
胸膜滑动征消失
平流层征
胸腔积液
肺部异常超声表现:B线
肺部异常超声表现:B线
B线间距为7mm时,由增厚的小叶间隔导致,
表征间质性肺水肿;
B线间距为3mm或更小时,符合CT检查见到
肺部超声在APE和ARDS的鉴别
肺部 超声 表现
B线
胸膜线 异常
肺滑征 减弱或 消失
幸免 区域
肺实变
胸水
肺脉
ALI/ ARDS
100%
100%
100%
100%
83.3%
66.6%
50%
APE
100%
%
0
0
0
95%
0
总结
• 肺部超声是一种无创的、临床导向的、
床旁动态评估的一种重要检查手段。
胸膜滑动征消失
不稳定:引流术 肺脉征消失 胸腔 引流 ? 循环 稳定 ?
稳定:其他检查
B 线消失
肺部超声的解读:
超声表现 病历资料
空气 系统硬化 支气管征 无明确心衰 B线增多 心功能低下 双侧对称弥漫B线 肺实变
临床结论
肺纤维化
肝
血管外肺水
ARDS ?
肺部超声的解读:
B线增多
空气 支气管征
ALI/ARDS ? APE ?
肺部异常超声表现:胸腔积液
胸腔积液
肺不张
肺部超声的解读:例1
胸膜滑动征减弱
是什么疾病?
肺部超声的解读:例2
多条B线
是什么疾病?
肺部超声的解读:例3
肺实变 肺实变 空气 支气管征
肝
是什么疾病?
肺部超声的解读:
肺实变 OR 空气 支气管征 OR
肝
每个检查都有局限性, 需要汇总患者所有资料
肺部超声的解读:
的毛玻璃样变区,表征肺泡性肺水肿。
肺部异常超声表现:肺实变
肺回声似肝脏
空气支气管征
肺部异常超声表现:胸膜下结节
胸膜下低回声结节 三角形、圆形、多边形
肺部异常超声表现:胸膜改变
胸膜增厚、不光滑
或呈锯齿状
肺部异常超声表现:平流层征
胸膜滑动征消失 M超为平流层征 B线消失 肺点
肺部异常超声表现:肺点
