叶绿体色素提取分离及理化性质
叶绿体色素的提取分离及其理化性质

2020/3/8
乙醇提取液操作步骤:
水研磨匀浆操作步骤:
2020/3/8
1.提取液中各成分分离:
用色层分析的原理加以分离
因吸附剂(本试验为滤纸)对不同物质的 吸附力不同,当用适当的溶剂推动时,混合物中 各成分在两相(流动相和固定相)间具有不同的 分配系数,所以它们的移动速度不同,经过一定 时间层析后,便将混合色素分离。
2020/3/8
三、 结果记录:填写记载表
2020/3/8
洗刷干净,器皿摆放整齐 研钵壁上易吸附色素,用什么洗刷? 节约使用试剂
2020/3/8
2020/3/8
(5)、H+和Cu2+对叶绿素分子中 Mg2+的取代作用
2020/3/8
Cu2+ H+
2020/3/8
叶绿素中的 可Mg2+被H+所取代 而成褐色的去镁 叶绿素,后者遇 铜则成为绿色的 铜代叶绿素,铜 代叶绿素很稳定, 在光下不易破坏, 故常用此法制作 绿色多汁植物的 浸渍标本。
透 射 光
反 射 光
2020/3/8
取一支20ml刻度试管
加入5ml 浓的 色素乙醇提取液
观察溶液的透射光 与反射光有何变化?
如果提取液的浓度较低,无法观察到荧光。 (荧光强度太弱)
2020/3/8
(3)、皂化作用
叶绿素是一种二羧酸---叶绿酸与甲醇和叶绿醇形 成的复杂酯,可与碱起皂化反应,生成醇和叶绿酸的盐, 产生的盐能溶于水,用此法可将叶绿素与类胡萝卜素分 开。
步骤:
1#小试管
加乙醇色素提取液2ml
稀释3倍 加5%盐酸1滴
取出1/3放到2#(CK1)
摇均匀
叶绿体色素的提取分离理化质和定量测定

六、实验结果观察及计算
(1)实验结果观察描述
(2)计算组织中叶绿体色素含量
(用mg/g鲜重或干重表示)
公式
叶绿素的浓度(C) 提取液体积 稀释倍数
叶绿体色素含量=
样品鲜重(或干重)
七、思考题
(1)叶绿素a、b在蓝光区也有吸收峰,能否 用这一吸收峰波长进行叶绿素a、b的定量分析? 为什么?
叶绿素中镁可被H+取代而形成褐色去镁叶绿素。 去镁叶绿素遇铜则成为铜代叶绿素。 皂化反应: 叶绿素可与碱起皂化反应而形成醇(甲醇和叶绿 醇)和叶绿酸的盐,产生的盐能溶于水--分开叶绿素 与类胡萝卜素。
2. 定量测定
根据叶绿体色素提取液对可见光谱的吸收,利用分 光光度计在某一特定波长下测定其光密度,即可用 公式计算出提取液中各色素的含量。
四、 实验步骤
1. 提取叶绿素
研磨法 材料剪碎 加入有机溶剂
研磨、匀浆 过滤 提取液
研磨法提取光合色素
荧光现象
(2)纸层析分离现象观察
去镁叶绿素
(3)叶绿素荧光现象观察
(4)H+和Cu2+对叶绿素 中Mg2+的取代作用
(5)皂化反应现象观察
铜代叶绿素 绿黄色素分层现象
五、定量测定
(1)定量用叶绿素提取液制备 (2)分光光度计测定 (3)实验数据及其处理
(2)用不含水的有机溶剂如无水乙醇、无水 丙酮等提取植物材料,特别是干材料的叶绿体 色素往往效果不佳,原因何在?
(3)研磨提取叶绿素时加入CaCO3. 石英砂 各有什么作用?
Ca=12.72D663 - 2.59D645 (1) Cb=22.88D645 - 4.67D663 (2) 将Ca与Cb相加即得叶绿素总量(CT): CT=Ca+Cb=20.2D645+8.05D663(3) 或:
【VIP专享】叶绿体色素的提取分离和理化性质实验报告

生物学导论实验报告叶绿体色素的提取分离和理化性质一、提取与分离1、实验目的学习应用薄层色谱法分离叶绿体色素的实验方法。
2、实验原理提取:叶绿体色素为有机酯类化合物,根据相似相容原理,常用有机溶剂提取。
如酒精、丙酮、乙酸乙酯、氯仿等。
分离:薄层层析法是将吸附剂均匀的涂抹在玻璃板上形成一薄层,将此吸附剂薄层作为固定相,把待测分离的样品溶液点在薄层板的下端,然后用一定量的溶剂作流动相,将薄层板的下端浸入到展开剂中。
流动相通过毛细管作用由下而上逐渐浸润薄层板,并带动样品在板上也向上移动,样品中各组成分在吸附剂和展开剂之间发生连续不断的吸附、脱吸附、再吸附……的过程。
由于吸附剂对不同物质的吸附能力大小不同,吸附能力强的物质相对移动慢一些,儿媳妇能力弱的物质相对移动快一些,从而使各组分有不同移动速度而彼此分开。
3、实验材料与试剂(1)新鲜的菠菜叶;(2)体积分数为95%的乙醇,碳酸钙粉末、展开剂(3)钵体、漏斗、三角瓶、剪刀、点样本、毛细管、层析缸、硅胶预制板、滤纸。
4、实验步骤(1)色素提取液的制备取叶4~5片新鲜叶片,洗净,擦干叶表面,去中脉剪碎,放入钵体中。
加入少量碳酸钙,加2~3ml体积分数为95%的乙醇,研磨至糊状,再加入10ml乙醇,上清液过滤,残渣再用10ml乙醇冲洗过滤。
(2)叶绿体色素的分离取硅胶预制板一个,用点样毛细管取上述提取液,平行于硅胶板的短边,距下边缘1cm处用毛细管划线,风干,重复操作3~4次;在干燥的层析缸中加入适量展开剂,高度0.5cm,将硅胶预制板带有色素一端放入,使其下端浸入展开剂中;当色素较好分离,展开剂前沿接近硅胶预制板的上端边缘时,取出,画线。
Rf=斑点中心到原点距离/溶剂前沿到原点距离5、实验结果与分析从上至下为胡萝卜素(橙色):Rf=6.95/7.35=0.946叶绿素a(蓝绿色):Rf=5.35/7.35=0.728叶绿素b(黄绿色):Rf=4.95/7.35=0.673叶黄素(黄色):Rf=4.10/7.350.558可知,胡萝卜素、叶绿素a、叶绿素b、叶黄素极性依次增大,与硅胶吸附能力依次增强。
17叶绿体色素的提取分离及其理化性质

实验目的
以植物叶片组织为材料,提取叶绿体色素;以纸层析法分离其成 分;鉴定叶绿体色素的理化性质.
实验器材和试剂
1、材料:菠菜
2、用具:天平、研钵、三角漏斗、滤纸、层析缸、毛细管、 分光镜、量筒、烧杯、试管等
3、试剂:丙酮、碳酸钙、层析液(石油醚:丙酮=25:3), 20%KOH-甲醇、乙醚、1%HCl、醋酸铜
理化性质的观察: 叶绿素是一种二羧酸酯,在碱作用下,发 生皂化反应;在弱酸作用下,叶绿素中镁可被氢原子取代而 成为褐色的去镁叶绿素,后者遇铜则成为绿色的铜代叶绿素, 叶绿素具有荧光,故从与入射光相垂直的方向观察叶绿素溶 液呈血红色。叶绿素的化学性质不稳定,易受强光氧化,特 别是当叶绿素与蛋白质分离后,破坏更快。
纸层析分离叶绿体色素
1.层析样纸制备,将优质滤纸剪成3cm×9cm的长条,将一端剪成中央留约 1cm×0.5cm的窄条; 2.点样,用细玻璃棒蘸取叶绿体色素提取液点于层析纸的窄条上端中央部, 用吹风机吹干后在原处重复点样7-8次; 3.展层,在层析缸中加入3-5ml层析推动液,然后将已点样的层析纸插入缸的 側壁槽内,调节纸条使窄条1/2部分浸入推动液中,盖好盖子,于阴暗处展层 约10min,即可在层析纸上分辨出4种不同的清楚色层;
实验步骤
叶绿体理化性质的观察
荧光现象的观察 取浓的叶绿体色素提取液化5ml,在透射 光和反射光下观察叶绿体色素提取液的颜色.
皂化作用 在观察过荧光现象的叶绿体色素提取液中加 入1.5ml的20%KOH-甲醇溶液,充分混匀.再加入5ml的苯液, 并混匀;沿试管壁缓慢加入1.5ml的蒸馏水,边滴加边摇动,直 至看到溶液逐渐分为两层为止.
叶绿素a:C55H72O5N4Mg,MW=893.4891
实验五 叶绿体色素的提取、分离及理化性质的鉴定

• 二、叶绿体色素的理化性质 • 1、叶绿体的荧光现象:取上述色素提取液少许于试管
中,分别观察反射光和透射光,比较观察到的颜色不同 并分析原因。
• 2、光对叶绿素的破坏:取上述色素提取液少许分别加 入两个试管中,一支试管放在暗处,一支试管放在强光 下照射,2 h后观察颜色变化,分析原因。
• 3、铜代反应:取上述色素提取液加入试管,逐滴加入 浓盐酸,直至溶液呈现褐色,此时叶绿素分子已经遭到 破坏,称为去镁叶绿素,然后加入醋酸铜结晶少许,慢 慢加入溶液,直至出现鲜亮的绿色,此时即形成了铜代 叶绿素。
• 4、黄色素与绿色素的分离:取上述色素丙酮提取液10 ml,加入盛有20 ml乙醚的分液漏斗,并沿漏斗边缘加 入30 ml蒸馏水,轻轻摇动分液漏斗,静止片刻,溶液 分为两层。色素已经全部转入上层乙醚总,弃去丙酮和 水,再加入5 ml30%KOH甲醇溶液,用力摇动分液漏斗, 静置10分钟,再加入蒸馏水10 ml,摇动后静置分离, 得到黄色素层和绿色素层,分别保留,分析实验结果和 原因。
• 2、把展层用的驴子中间搞一个圆洞,把新华滤纸 剪成20 cm的长条卷成圆柱,一端多次滴上色素提取 液,插入圆形滤纸中间孔中,上面与圆形滤纸齐平
• 3、在培养皿中加入展层用的四氯化碳,把上部做 成的滤纸下的含色素圆柱下端浸入展层液,盖上培 养皿上盖,开始展层。等展层液扩散到培养皿边缘 时,取出滤纸,观察同心圆色素带,做好记录。
• 三、器材与试剂
• •仪器:带盖培养皿、台天平、研钵、量筒、 烧杯、漏斗、软木塞、新华滤纸、毛细滴 管、剪刀、分液漏斗、移液管、分光计。 • 实验试剂:丙酮、甲酯、醋酸铜、盐酸、 氢氧化钾、石英砂、碳酸钙、无水硫酸钠、 四氯化碳、乙醚。 •材料:菠菜叶片
• 一、叶绿体色素的提取与分离
叶绿体色素的提取分离和理化性质

叶绿体色素的提取分离和理化性质主讲:张海森博士一、实验目的因此,测定叶绿体色素含量便成为研究光合作用与氮代谢必不可少的手段,在实际生产中也有着广泛的应用。
1、学习叶绿体色素的提取方法。
2、了解叶绿素和类胡萝卜素的一些主要理化性质。
绿色植物的光合作用是离不开叶绿体色素的,了解叶绿体色素的组成和性质对于理解光合作用的本质很有帮助。
叶绿体色素分为叶绿素和类胡萝卜素两类。
它们与类囊体膜上的蛋白质相结合,成为色素蛋白复合体,不溶于水,溶于有机溶剂,因此,可用乙醇或丙酮等有机溶剂提取。
二、叶绿体色素的提取原理三、实验材料:菠菜叶片五、叶绿体色素的理化性质1.光对叶绿素的破坏作用叶绿素(a,b)的化学性质很不稳定,容易受强光的破坏,特别是当色素分子与蛋白质分离以后,破坏更快,而类胡萝卜素则较稳定。
水提取液暗光乙醇提取液暗光1) 取四支小试管,分别加入两种提取液2ml,稀释2-3倍;2) 各取两只试管放于暗处; 另两只试管置于强光下,进行光破坏;3) 30min后,对比观察光破坏的结果。
光对叶绿素破坏的操作步骤:2.提取液中各成分分离:用色层分析的原理加以分离因吸附剂对不同物质的吸附力不同,当用适当的溶剂推动时,混合物中各成分在流动相和固定相之间具有不同的分配系数,所以它们的移动速度不同,经过一定时间层析后,便将混合色素分离。
叶绿体色素的结构决定了它们极性的不同,因而在滤纸上的迁移速率不同。
叶绿体色素叶绿素类胡萝卜素叶绿素a 叶绿素b叶黄素胡萝卜素问题:请根据这四种色素分子的结构比较它们极性的大小。
步骤:(1)取圆形滤纸1张,用细头的吸管在其中心戳一圆形小孔。
(滤纸直径为11cm)(2)另取一张长方形滤纸条(5cm×1.5cm),沿纸条长边方向涂抹色素,风干后,重复涂抹数次。
十次涂抹之后,沿长边方向卷成纸捻。
(3)纸捻带有色素的一端插入圆形滤纸的小孔中,使之与滤纸刚刚平齐(勿凸出)。
(4)将康维皿置于培养皿内,向康维皿中央小室加入推动剂。
实验3叶绿体色素的提取、分离及理化性质的测定

实验3叶绿体⾊素的提取、分离及理化性质的测定实验三叶绿体⾊素的提取、分离及理化性质的测定【实验原理】叶绿体⾊素⼜称光合⾊素,在⾼等植物中可分为叶绿素和类胡萝⼘素两⼤类,前者包括叶绿素a(蓝绿⾊)和叶绿素b(黄绿⾊),后们类囊体膜上的蛋者包括胡萝⼘素(橙⾊)和叶黄素(黄⾊),它与⽩质结合形成⾊素蛋⽩复合体,不溶于⽔,易溶于酯,因此可⽤丙酮、⼄醇、⽯油醚等有机溶剂进⾏提取。
叶绿体⾊素的分离有多种⽅法,本实验仅介绍纸层析法。
层析的基本原理:在分离过程中,由⼀种流动相(即⼀种液体或⽓体)带动着试样经过固定相(⼀种⽀持物,如纸)向外扩散,由于试样在两相中的溶解度不同和固定相对试样中不同成分的吸附程度有别,当⽤适当的溶剂推动时,混合物中各成分在两相间具有不同的分配系数,所以它们的移动速度不同,经过⼀定时间层析后,可使试样中的各种组分得到分离,在做纸层析时,由于纸对光合⾊素中各种⾊素分⼦的吸附程度不同,以及这些⾊素分⼦在溶剂四氯化碳(推进剂)中溶解度也有差异,以致溶剂带动⾊素分⼦向四周移动时,各种⾊素分⼦沿纸扩散的速度也就不同,使混合⾊素分离,出现不同颜⾊的环。
将提取的叶绿素溶液置于光下,在透射光呈绿⾊,在反射光下呈这现象称为荧光现象。
在反射光下叶绿素溶液之所以呈樱桃红⾊,种发态,激发态的叶樱桃红⾊,是因为叶绿⾊分⼦吸收光能后处于激状绿素分⼦很不稳定,当它回到基态时,将所获得的能量以辐射能的形式发射出红光量⼦。
叶绿素的化学性质很不稳定,容易受强光、⾼温等的破坏,特别是当叶绿素与蛋⽩质分离以后,破坏更快,⽽类胡萝⼘素则较稳定。
叶绿素中的镁可以被H+所取代⽽成褐⾊的去镁叶绿素,后者遇铜后,其中的氢(H+)⼜被铜(Cu2+)取代,形成了铜代叶绿素,便由褐⾊转变成蓝绿⾊,铜代叶绿素很稳定,且⽐原来的绿⾊还要稳定些,在光下也不易被破坏。
设备试剂】【材料、与1. 材料新鲜的菠菜或⼩⽩菜等其他绿⾊植物叶⽚。
2. 设备电⼦天平、研钵、烧杯、量筒、培养⽫、刻度试管、试管夹、试管架、酒精灯、剪⼑、圆形滤纸、⼩漏⽃等。
叶绿体色素的提取分离和理化性质实验报告

生物学导论实验报告叶绿体色素的提取分离和理化性质一、提取与分离1、实验目的学习应用薄层色谱法分离叶绿体色素的实验方法。
2、实验原理提取:叶绿体色素为有机酯类化合物,根据相似相容原理,常用有机溶剂提取。
如酒精、丙酮、乙酸乙酯、氯仿等。
分离:薄层层析法是将吸附剂均匀的涂抹在玻璃板上形成一薄层,将此吸附剂薄层作为固定相,把待测分离的样品溶液点在薄层板的下端,然后用一定量的溶剂作流动相,将薄层板的下端浸入到展开剂中。
流动相通过毛细管作用由下而上逐渐浸润薄层板,并带动样品在板上也向上移动,样品中各组成分在吸附剂和展开剂之间发生连续不断的吸附、脱吸附、再吸附……的过程。
由于吸附剂对不同物质的吸附能力大小不同,吸附能力强的物质相对移动慢一些,儿媳妇能力弱的物质相对移动快一些,从而使各组分有不同移动速度而彼此分开。
3、实验材料与试剂(1)新鲜的菠菜叶;(2)体积分数为95%的乙醇,碳酸钙粉末、展开剂(3)钵体、漏斗、三角瓶、剪刀、点样本、毛细管、层析缸、硅胶预制板、滤纸。
4、实验步骤(1)色素提取液的制备取叶4~5片新鲜叶片,洗净,擦干叶表面,去中脉剪碎,放入钵体中。
加入少量碳酸钙,加2~3ml体积分数为95%的乙醇,研磨至糊状,再加入10ml乙醇,上清液过滤,残渣再用10ml乙醇冲洗过滤。
(2)叶绿体色素的分离取硅胶预制板一个,用点样毛细管取上述提取液,平行于硅胶板的短边,距下边缘1cm处用毛细管划线,风干,重复操作3~4次;在干燥的层析缸中加入适量展开剂,高度0.5cm,将硅胶预制板带有色素一端放入,使其下端浸入展开剂中;当色素较好分离,展开剂前沿接近硅胶预制板的上端边缘时,取出,画线。
Rf=斑点中心到原点距离/溶剂前沿到原点距离5、实验结果与分析从上至下为胡萝卜素(橙色):Rf=6.95/7.35=0.946叶绿素a(蓝绿色):Rf=5.35/7.35=0.728叶绿素b(黄绿色):Rf=4.95/7.35=0.673叶黄素(黄色):Rf=4.10/7.350.558可知,胡萝卜素、叶绿素a、叶绿素b、叶黄素极性依次增大,与硅胶吸附能力依次增强。
叶绿体色素的提取分离和理化性质
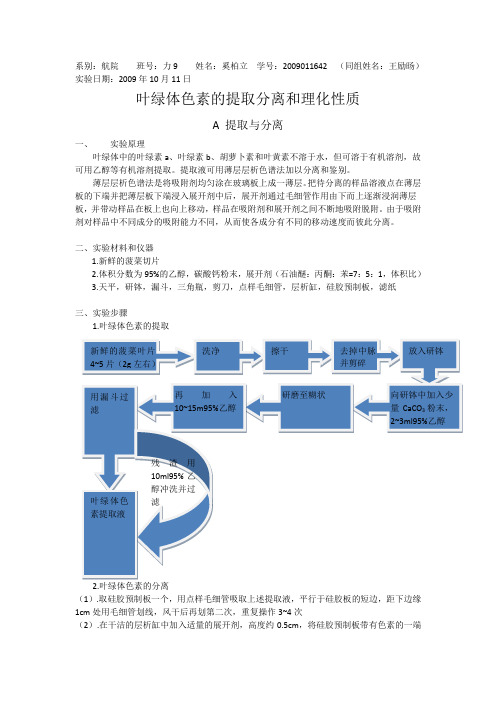
系别:航院班号:力9 姓名:奚柏立学号:2009011642 (同组姓名:王励旸)实验日期:2009年10月11日叶绿体色素的提取分离和理化性质A 提取与分离一、实验原理叶绿体中的叶绿素a、叶绿素b、胡萝卜素和叶黄素不溶于水,但可溶于有机溶剂,故可用乙醇等有机溶剂提取。
提取液可用薄层层析色谱法加以分离和鉴别。
薄层层析色谱法是将吸附剂均匀涂在玻璃板上成一薄层。
把待分离的样品溶液点在薄层板的下端并把薄层板下端浸入展开剂中后,展开剂通过毛细管作用由下而上逐渐浸润薄层板,并带动样品在板上也向上移动,样品在吸附剂和展开剂之间不断地吸附脱附。
由于吸附剂对样品中不同成分的吸附能力不同,从而使各成分有不同的移动速度而彼此分离。
二、实验材料和仪器1.新鲜的菠菜切片2.体积分数为95%的乙醇,碳酸钙粉末,展开剂(石油醚:丙酮:苯=7:5:1,体积比)3.天平,研钵,漏斗,三角瓶,剪刀,点样毛细管,层析缸,硅胶预制板,滤纸三、实验步骤1.叶绿体色素的提取2.叶绿体色素的分离(1).取硅胶预制板一个,用点样毛细管吸取上述提取液,平行于硅胶板的短边,距下边缘1cm处用毛细管划线,风干后再划第二次,重复操作3~4次(2).在干洁的层析缸中加入适量的展开剂,高度约0.5cm,将硅胶预制板带有色素的一端放入,使其下端浸入展开剂中(勿使待测样品浸入展开剂中)。
迅速盖好层析缸盖。
(3).观察。
当看到各种色素得到较好分离,展开剂前沿接近硅胶预制板上端近边缘处时,取出硅胶预制板,并迅速用铅笔标出展开剂前沿和各色素带的位置。
四、实验结果经过薄层色谱分离后,叶绿素a为蓝绿色,叶绿素b为黄绿色、胡萝卜素为橙黄色和叶黄素为鲜黄色。
各色素条带在薄层中的位置可用相对比移值R f来表示,即B 理化性质一、实验原理叶绿素是一种由叶绿酸与甲醇和叶绿醇形成的复杂酯,故可与碱起皂化反应而生成甲醇和叶绿醇及叶绿酸盐,产生的盐能溶于水中,可用此法将叶绿素与类胡萝卜素分离。
实验一叶绿体色素的分离及理化性质测定

目录
• 实验目的 • 实验原理 • 实验步骤 • 结果分析 • 实验总结与展望
01
CATALOGUE
实验目的
掌握叶绿体色素的分离方法
叶绿体色素的提取
通过使用有机溶剂(如丙酮、乙醇等 )从植物组织中提取叶绿体色素。
叶绿体色素的分离
采用色谱法(如薄层色谱、高效液相 色谱等)将叶绿体色素中的不同组分 进行分离。
研磨与过滤
将叶片放入研钵中,加入 适量的石英砂和无水乙醇 ,研磨至匀浆。通过纱布 过滤,收集滤液。
离心分离
将滤液倒入离心管中,用 离心机离心,分离叶绿体 色素。
叶绿体色素的分离
制备滤纸条
将滤纸剪成长约5cm,宽约1cm的纸条,标明起点。
点样与展开
用毛细管将色素提取液点在滤纸条的起点线上,然后将其放入展开 剂中(如石油醚、乙醚、丙酮等)进行展开。
色素组成
02
实验结果显示,叶绿体色素主要由叶绿素a、叶绿素b、胡萝卜
素和叶黄素组成。
含量变化
03
实验中观察到不同植物或同一植物不同部位叶绿体色素含量存
在差异。
叶绿体色素理化性质测定结果分析
溶解性
实验结果表明,叶绿体色素易溶 于有机溶剂,如丙酮、氯仿等, 难溶于水。
稳定性
在一定温度和光照条件下,叶绿 体色素稳定性较高,但在高温和 强光下易分解。
学习叶绿体色素的应用价值
生物指示剂
叶绿体色素可以作为生物指示剂,用于监测环境污染 和生态变化。
食品添加剂
叶绿体色素可用于食品加工中,如绿色饮料、果蔬汁 等,增加食品的色泽和营养价值。
生物燃料
叶绿体色素可以作为生物燃料的原料,通过微生物发 酵技术转化为生物燃料,如乙醇、生物柴油等。
实验3、叶绿体色素的提取、分离理化性质 及光合速率测定

分离原理:分离色素的方法有多种, 分离原理:分离色素的方法有多种,纸层析法是用滤 纸作为支持物的层析方法。当层析液(流动相) 纸作为支持物的层析方法。当层析液(流动相)不断 地从层析滤纸(固定相)上流过时, 地从层析滤纸(固定相)上流过时,由于要分离的混 合物中的各种成分在两相间具有不同的分配系数( 合物中的各种成分在两相间具有不同的分配系数(不 同色素在层析液中的溶解度不同,因而随层析液的扩 同色素在层析液中的溶解度不同, 散速度也不同),所以它们移动速度也就不同, 散速度也不同),所以它们移动速度也就不同,经过 ),所以它们移动速度也就不同 一定时间后,便会使样品中的混合物得到分离。 一定时间后,便会使样品中的混合物得到分离。
V:体积流速(L/min) 体积流速(L/min) Ta:空气温度(K) 空气温度( p:大气压力(bar) 大气压力(bar) A:叶面积(cm2) 叶面积( Co:出气口CO2浓度(uL/L) 出气口CO 浓度(uL/L) Ci:进气口CO2浓度(Ul/l) 进气口CO 浓度(Ul/l)
可调整,可流量计读出 可调整, 待测 一般认为一个大气压 固定为叶室窗口面积 待测 待测
4.H+和Cu2+对叶绿色分子中Mg2+的取代作用 对叶绿色分子中Mg
(1)取两支试管,一支试管加叶绿体色素提取液 )取两支试管, 2ml,作为对照。另一支试管加叶绿体色素提取液 ,作为对照。 5ml,再加入 %HCl数滴摇匀,观察溶液颜色变化 数滴摇匀, ,再加入5% 数滴摇匀 小粒, (2)当溶液变褐后,再加醋酸铜晶体 小粒,微微 )当溶液变褐后,再加醋酸铜晶体1小粒 加热,观察记载溶液颜色变化情况, 加热,观察记载溶液颜色变化情况,并与对照试 管相比较。解释其颜色变化原因。 管相比较。解释其颜色变化原因。 (3)另取醋酸-醋酸铜溶液 )另取醋酸-醋酸铜溶液20ml,置于烧杯中。取 ,置于烧杯中。 新鲜植物叶两片,放入烧杯中,用酒精慢慢加热, 新鲜植物叶两片,放入烧杯中,用酒精慢慢加热, 随时观察并记录叶片颜色的变化, 随时观察并记录叶片颜色的变化,直至颜色不再 变化为止。解释原因。 变化为止。解释原因。
叶绿体色素的提取及理化性质的

3
叶绿体色素在酸性和碱性溶液中的溶解度不同, 因此可以通过调节pH值进行提取和分离。
稳定性
01
叶绿体色素对光、热、酸、碱等条件敏感,容易发生降解。
02
在酸性环境中,叶绿素a和叶绿素b容易被氧化成脱镁叶绿素,
导致颜色变化。
在光照条件下,叶绿体色素会发生光降解,导致颜色变淡。
03
荧光性质
叶绿体色素具有荧光性质,其 中叶绿素a的荧光强度最强,
其次是叶绿素b。
荧光光谱分析可用于研究叶 绿体色素的结构和组成,以 及其在不同环境条件下的变
化。
荧光性质可用于叶绿体色素的 定量分析,通过测量荧光强度 可以计算出样品中叶绿体色素
的浓度。
03 叶绿体色素的应用
在农业上的应用
促进光合作用
叶绿体色素能够吸收光能,并将其转化为化学能,用于植物的光 合作用,促进植物生长。
不同植物种类的叶绿体色 素组成和含量不同,影响 植物对不同光照环境的适 应性。
植物分类学
叶绿体色素的组成和含量 可作为植物分类的依据之 一。
提取原理
根据相似相溶原理:叶绿体色素易溶 于有机溶剂,如丙酮、乙醇等,而不 溶于水。因此,通过加入有机溶剂, 可以将叶绿体中的色素提取出来。
色素分子在有机溶剂中的溶解度与温 度、压力、有机溶剂的种类和浓度等 因素有关。
提取过程中要保持低温,防止色素降解。 过滤时选用合适的滤纸,确保色素完全收集。
研磨时要充分,以释放出更多的色素。
避免使用金属器具直接接触有机溶剂,以防发生化学反 应。
02 叶绿体色素的理化性质
溶解性
1
叶绿体色素不溶于水,易溶于酒精、丙酮、氯仿 等有机溶剂。
2
叶绿素a和叶绿素b在层析液中的溶解度不同,因 此可以通过纸层析法进行分离。
实验一叶绿体色素的提取分离及理化性质

•光学特性:
( 1 )吸收光谱:色素溶液随波长改变而发生光吸收 变化的图谱 Chla Chlb的吸收光谱有二个强吸收峰 640——660nm 红光部分 叶绿素特有 410——470nm 蓝紫光部分 卟啉环化合物共有 (2)荧光和磷光 荧光现象:Chl溶液在透射光下呈绿色,而反射 光下呈红色的现象。强度大,寿命短(10-9秒) 磷光: Chl溶液停止光照后,仍能在一定时间内 放出暗红色的光。 寿命长(10-2秒——10-3秒)
叶绿体色素的提取分离及理化 性质的鉴定
一. 实验原理
1.1 叶绿素: 主要包括叶绿素a和b
分子式: Chla C55H72O5N4Mg Chlb C55H70O6N4Mg 结构式: 卟啉环化合物 四个吡咯环与四个=CH-组成一 个大环 , 共轭双键形成一个大 π 键 , 环中央有一个镁原子 , 卟啉环决定叶绿素颜色 , 也是吸收可见光 , 并以诱导共振 方式传递光能的根本所在 , 叶醇尾是由四个异戊二烯单 位组成的双萜 Chla 蓝绿色 Chlb 黄绿色 脂溶性: 难溶于水,仅溶于酒精、丙酮、已醚、已烷等有 机溶剂 卟啉环头部呈极性, 具亲水性; 叶醇尾部具亲脂性
皂化反应: Chla、Chlb 是双羧酸的酯 一个羧基被甲基酯化 可发生皂化反应 另一个羧基被叶醇基酯化 COOCH3 C32H30ON4Mg +2KOH COOC20H39 COOK C32H30ON4Mg +CH3OH+C20H39OH COOK 取代反应:卟啉环中的 Mg2+ 可被 H2+ 、 Cu2+ 、 Zn2+取代,被Cu2+、Zn2+取代后仍保持绿色
不同花色素的取代基和颜色
花色素 花葵素 花青素 花翠素 芍药素 甲花翠素 二甲花翠素
叶绿体色素的提取、分离及理化性质鉴定

叶绿体色素的提取、分离及理化性质鉴定
实验目的了解叶绿素提取分离原理、方法,验证理化性质
实验原理叶绿素易溶于乙醇、丙酮,类胡萝卜素更易溶于苯;
叶绿素是双羧酸脂类,能与强碱发生皂化反应;
叶绿素分子中络合的镁能依次被H+、Cu2+取代;
叶绿素溶液光照后有荧光现象。
实验器材试管、研钵、太平、毛细滴管、剪刀、移液管、展层缸、滤纸、漏斗、50ml容量瓶、酒精灯、试管夹
实验试剂乙醇、丙酮、苯、盐酸氯化铜混和液、甲醇、氢氧化钾、石英砂
实验材料菠菜叶片
实验步骤
一、叶绿体色素的提取、分离
1、提取:叶片2g剪碎,放入研钵,加乙醇(或丙酮)5ml研磨匀浆,再加10ml,
过滤。
2、分离:滤纸一张,用毛细管在圆心处分次滴加提取液,圆心处穿孔,然后
插入滤纸圆芯;将其放入盛有展层液(汽油或丙酮:苯:石油醚=9:1:
0.1混和液)的展层缸内,30min.后观察结果。
叶绿体色素被分离成从内
到外的篮绿(叶绿素a)、黄绿(叶绿素b)、浅黄(叶黄素)、橙黄(胡萝卜素)四个同心圆环。
二、叶绿素理化性质鉴定
1、荧光现象观察:浓提取液向光观察呈绿色,背光观察呈血红色(荧光)
2、皂化反应:加提取液0.5ml至试管,加入氢氧化钾的甲醇饱和液2ml,沿
管壁加水2ml,管内有乳白色沉淀出现(皂化)。
加苯1ml,静置5min,上层苯层呈深黄色(类胡萝卜素)。
3、取代反应:加提取液0.5ml至试管,加水2ml,加盐酸氯化铜混和液2ml,
用酒精灯慢慢加热,仔细观察溶液颜色依次有绿变褐(氢取代)再变篮绿(铜取代)。
实验七叶绿体色素的提取分离及理化性质的鉴定讲解

实验七叶绿体色素的提取及理化性质的鉴定一、目的1、学习应用提取分离叶绿体色素的实验方法。
2、验证叶绿素的理化性质。
3、了解叶绿体色素的荧光现象、皂化反应等理化性质。
二、原理1、叶绿体色素:植物叶绿体色素主要有三类:1)叶绿素2)类胡萝卜素3)藻胆素。
高等植物叶绿体中含有前两类,藻胆素仅存在于藻类植物中。
高等植物体内叶绿素(chlorophyll两种)主要有两种:叶绿素a、b(简写为chla、chlb,其结构式见图7-3),chla通常呈蓝绿色,而chlb呈黄绿色,chlb是chla局部氧化的衍生物。
chla是chlb的三倍,二十世纪30年代,知道了叶绿素的分子结构,50年代末期,人工合成了叶绿素a,其它色素也几乎在同时发现。
叶绿体中的类胡萝卜素主要包括胡萝卜素(carotene)和叶黄素(lutein)两种,前者呈橙黄色,后者呈黄色。
叶黄素是胡萝卜素的二倍。
一般植物叶绿素是类胡萝卜素的三到四倍;胡萝卜素:C40H56 (有α、β、γ三种同分异构体)叶黄素:C40H54(OH)2 (同分异构体很多)。
2、理化性质:这二大类四种色素都不溶于水,而溶于有机溶剂,如乙醇、丙酮等。
通常用80%的丙酮或丙酮:乙醇:水为4.5:4.5:1的混合液来提取叶绿素。
按化学性质来说,叶绿素是叶绿酸的酯,在碱的作用下,可使其酯键发生皂化作用,生成叶绿酸的盐,能溶于水,但由于它保留有Mg核的结构,仍保持原来的绿色。
而类胡萝卜素中,胡萝卜素是不饱和的碳氢化合物,β—胡萝卜素水解可生成2分子维生素A,叶黄素是由胡萝卜素衍生的二元醇,不能与碱发生皂化反应,根据这一点,可以将叶绿素和类胡萝卜素分开。
此外,叶绿素还可以在酸的作用下,其中的Mg被H所代替形成褐色的去Mg叶绿素:去Mg叶绿素能与其他金属盐中的铜、锌、铁盐等代H,又重新呈现绿色,比原来的绿色更稳定。
根据这一原理可用醋酸铜处理来保存绿色标本。
3、功能:1.叶绿体色素的功能叶绿素和类胡萝卜素都包埋在类囊体膜中,与蛋白质结合在一起,组成色素蛋白复合体,根据功能来区分,叶绿体色素可分为二类:(1)作用中心色素:叶绿素分子含有一个卟啉环的“头部”和一个叶绿醇的“尾部”,呈蝌蚪型,大卟啉环由四个小吡咯环以四个含有双键的甲烯基(-CH=)连接而成。
叶绿体色素的提取分离理化性质鉴定及含量测定

内容:
①叶绿素a和b含量差异; ②绿色素与黄色素的含量差异
色素提取分离的原理; 叶绿素测定的方法及其原理; 绿色素与黄色素的纯化原理及步骤; 叶绿素的理化性质的鉴定方法
实验原理
Photosynthesis
Thermosynechococcus
elongatus(蓝细菌)
研钵、剪刀、漏斗、滤纸、移液管(1mL)、 试管及试管架、洗耳球、酒精灯等。 • 试剂:丙酮、80%丙酮、醋酸酮、5%盐酸、 碳酸钙、石英砂等
实验步骤
鲜叶4 g,加丙酮10 ml及少许碳酸
1
钙和石英砂,匀浆,以漏斗过滤之
再加丙酮20 ml洗并过滤,即为色素提取液。放于暗处备用。
取少许于另 3 一试管中
实验步骤 叶绿素a和b的测定
鲜叶0.5 g,加丙酮5 ml及少许碳酸钙和石英砂,匀浆,将 匀浆转入量筒中,并用适量80%丙酮洗涤研钵,用80%丙酮 定容至10ml
吸取2.5ml加入有10ml80%丙酮的量筒中,过滤,滤液备用
取上述色素提取液4ml,以80%丙酮为对照,分别测定 663nm、645nm和 440nm处的光密度值。
Ca=12.7 OD663-2.69 OD645
(3)
Cb=22.9 OD645-4.68 OD663
(4)
CT= Ca+ Cb=8.02 OD663+20.21 OD645
பைடு நூலகம்
• Ck=4.7OD440- 0.27Ca+b
(5)
叶绿体色素的理化性质
(1)叶绿素与类胡萝卜素都有一定的吸收光谱, 可用分光镜检查或用分光光度计精确测定;
第二单线 态10-12 S
叶绿体色素的提取分离及理化性质检测实验报告

叶绿体色素的提取分离及理化性质检测实验报告一、实验目的:1. 学习应用薄层色谱法分离叶绿体色素的实验方法。
2. 了解叶绿素的组成、性质和测定叶绿素有助于理解光合作用的本质。
二、实验原理:叶绿体是进行光合作用的细胞器。
叶绿体中的叶绿素a,叶绿素b,胡萝卜素和叶黄素与类囊体膜结合成为色素蛋白复合体。
这些色素都不溶于水,而溶于有机溶剂,故可用乙醇等有机溶剂提取。
提取液可用薄层色谱法加以分离和鉴别。
薄层层析色谱法是将吸附剂均匀地涂在玻璃板上成一薄层,将此吸附剂薄层作为固定相,把待分离的样品溶液点在薄层板的下端,然后用一定量的溶剂作流动相,将薄层板的下端浸入到展开剂当中。
由于吸附剂对不同物质的吸附能力大小不同,吸附力强的物质相对移动慢一些,而吸附力弱的物质则相对移动快一些,从而使各组分有不同的移动速度而彼此分开。
植物活性成分的分离常用薄层层析法和柱层析法,其中柱层析适用于大量制备。
本实验采用薄层层析色谱法,其中固定相用硅胶预制板。
三、实验材料与试剂:1. 新鲜的菠菜叶片。
2 体积分数为95%的乙醇,碳酸钙粉末,展开剂〈石油醚:丙酮:苯=75:1,体积比>。
3.研钵,漏斗,三角瓶,剪刀,点样毛细管,层析缸,硅胶预制板,滤纸。
四、实验步骤:(一) 色素提取液的制备1. 取新鲜叶片4“5片,洗净,擦干叶表面,去除中脉剪碎,放入研钵中。
2. 向研钵中加入少量CaCO₃**,再加2*3ml体积分数为 95%的乙醇,充分研磨至糊状,再加10°15ml体积分数为95%的乙醇,上清液用漏斗过滤出。
残渣再用10ml体积分数为95%的乙醇冲洗一次,一同过滤于三角瓶中,即制成叶绿体色素提取液。
提取液应避光保存,因提取量较大,可用于其他相关实验(如后面的叶绿素理化性质的验证)。
(二) 叶绿体色素的分离1.取硅胶预制板一个,用点样毛细管吸取上述提取液,平行于硅胶板的短边,距下边缘1cm处用毛细管划线,保证划线细直。
叶绿体色素的提取

实验名称叶绿体色素的提取、分离和理化性质实验原理1.提取:根据相似相溶原理,叶绿体色素都不溶于水,而溶于有机溶剂,所以可用乙醇等有机溶剂提取。
2.分离:提取液可用薄层色谱法分离和鉴别。
由于吸附剂对不同物质的吸附能力大小不同,吸附力强的物质相对移动慢一些,吸附力弱的物质相对移动快一些,从而使各组分有不同的移动速度而彼此分开。
3.理化性质:(1)叶绿素可与碱起皂化反应生成醇(甲醇和叶绿醇)和叶绿酸的盐(盐能溶于水中),可用此法将叶绿素与类胡萝卜素分开。
(2)叶绿素吸收光量子而转变成激发态,激发态的叶绿素分子很不稳定,当它变回基态时可发射出红光量子,因而产生荧光。
(3)叶绿素的化学性质很不稳定,容易受强光的破坏,特别是当叶绿素与蛋白质分离以后,破坏更快,而类胡萝卜素则较稳定。
(4)叶绿素中的镁可以被H+所取代而成褐色的去镁叶绿素。
去镁叶绿素遇铜则成为铜代叶绿素,铜代叶绿素很稳定,在光下不易破坏。
实验仪器和材料1.提取与分离:(1)材料:新鲜的菠菜叶片(2)仪器设备:天平、研钵、漏斗、三角瓶、剪刀、点样毛细管、层析缸、硅胶预制板、滤纸(3)试剂:95%乙醇、碳酸钙粉末、展开剂(石油醚:丙酮:苯=7:5:1 V/V)2.理化性质:(1)材料:菠菜叶片(2)仪器设备:刻度试管、小试管、试管架、烧杯、水浴锅、玻棒、刻度吸量管(3)试剂:95%乙醇、苯、醋酸铜粉末、5%稀盐酸、醋酸-醋酸铜溶液、KOH-甲醇溶液实验步骤色素提取液的制备叶绿体色素的分离理化性质:光对叶绿素的破坏作用荧光现象的观察皂化作用(绿色素与黄色素的分离)H +和Cu 2+对叶绿素分子 中Mg 2+的取代作用数据记录表格实验讨论1.菠菜叶样品要取够,否则色素分子过少做层析时颜色过浅。
2.皂化时出现三层,因为发生了乳化作用。
3.用毛细吸管划直线时,直接划会划破硅胶层,应沿着预先画好的线点划。
4.CaCO3不宜多加。
5.层析前要等到乙醇挥发殆尽,否则会影响测得的R f值。
实验9-叶绿体色素的提取分离及理化

叶绿素的背景知识介绍
叶绿素分子是由两部分组成的:核心部分是 一个卟啉环(porphyrin ring),其功能是光吸收; 另一部分是一个很长的脂肪烃侧链,称为叶 绿醇(phytol),叶绿素用这种侧链插入到类囊 体膜。与含铁的血红素基团不同的是,叶绿 素卟啉环中含有一个镁原子。叶绿素分子通 过卟啉环中单键和双键的改变来吸收可见光。 各种叶绿素之间的结构差别很小。如叶绿素a 和b仅在吡咯环Ⅱ上的附加基团上有差异:前 者是甲基,后者是甲醛基。
二. 试剂与材料
2.1 实验试剂: 石油醚(沸程60℃∽90℃)、丙酮、甲 醇、氢氧化钾、石英砂、碳酸镁、氯化钠、 醋酸铜。 2.2 仪器和器皿: 分光光度计、台秤、剪刀、 研钵、移液 管、漏斗、大试管、层析缸 2.3 材料: 新鲜菠菜叶片,不同颜色的花和果实。
三.实验操作
丙酮研磨提取叶绿素 ↓过滤、洗研钵及残渣 ↓ 余下的色素提取液用石油醚萃取 ↓ ↓ ↓ ↓ 纸层析 荧光 皂化反应 光破坏 ↓ 分离色素
五. 结果与分析
对实验现象作好详细记录, 并加以解释 请对皂化反应现象做出合理解释,而不是 单单用反应方程式来表示
六. 注意事项
实验中注意安全,石油醚、丙酮等试剂要 远离火源。 研磨过程中丙酮要少量多次加入,以免研 磨时四处飞溅。 过滤时不要使用滤纸而使用棉花,棉花塞 在漏斗基部要松紧适当。 叶绿素要避光保存。
↓ 2mL丙酮提取液 ↓ 加入6N HCl (脱镁叶绿素) ↓ Cu取代
四. 实验内容 4.1 叶绿素的荧光现象观察:
取叶绿体色素提取液少许于1支试管中,用反射光和 透射光观察提取液的颜色有何不同,反射光下观察 到的提取液颜色即为叶绿素产生的荧光颜色。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、目的与要求
掌握叶绿素的分离、提取方法; 了解叶绿体色素的种类、性质和功能;
2020/11/14
2
二、实 验 原 理 叶绿体色素? 叶绿体色素分离原理? 叶绿体色素性质?
2020/11/14
3
(一)叶绿体色素:
叶绿素
叶绿素a 叶绿素b
3:1 (阳生) 2:1 (阴生)
类胡萝卜素
2020/11/14
胡萝卜素 叶黄素
2:1
3:1
4
叶绿体在细胞中的分布与结构
2020/11/14
5
类囊体膜的结构及功能
2020/11/14
6
2020/11/14
7
类胡萝卜素的结构式
2020/11/14
8
(二)叶绿体色素分离原理?
色素分离的方法有多种,纸层析是最简 便的一种。当溶剂(有机推动剂)不断 从纸上流过时,由于混合物(叶绿素提 取液)中各种成分在固定相(滤纸纤维 素所吸附的水分)和流动相(有机推动 剂)间具有不同的分配系数,所以移动 速度不同,经过一定时间后,可将各种 色素分开
是单单用反应方程式来表示
2020/11/14
22
谢谢观赏
2020/11/14
9
(三)叶绿体色素性质?
物理性质:不溶于水,易溶于有机溶剂 化学性质:皂化反应,置换反应
功能:吸收光能、电子传递、光能转化 (少量叶绿素a)
2020/11/14
10
叶绿素的吸收光谱
叶绿素溶液
2020/11/14
11
叶绿素的吸收光谱
2020/11/14
12
叶绿素的荧光现象
甲醇
叶绿醇
15
三、材料与试剂
新鲜的植物叶片。 80%乙醇、CaCO3、醋酸铜结晶、无水硫酸钠、1N盐酸。 量筒,新华滤纸,大试管一支,长滴管,剪刀。
2020/11/14
16
四、操作步骤
提取 :
称取1g左右的鲜叶
研磨
过滤
色素提取液
2020/11/14
ห้องสมุดไป่ตู้
17
层析:
2020/11/14
18
四、操作步骤
2020/11/14
13
置换反应
2020/11/14
14
皂化反应:
Chla、Chlb 是双羧酸的酯可发生皂化反应 一个羧基被甲基酯化 另一个羧基被叶醇基酯化
C32H30ON4Mg
COOCH3 +2KOH
COOC20H39
COOK
C32H30ON4Mg COOK
叶绿酸盐
2020/11/14
+ CH3OH + C20H39OH
研磨提取叶绿素(80%乙醇)
↓过滤、洗研钵及残渣
↓
↓
2mL乙醇提取液
余下的色素提取液
↓
↓↓
↓↓
加入1N HCl
纸层析 荧光 皂化反应 光破坏
(脱镁叶绿素) ↓
↓
分离色素
Cu取代
↓
扫描光谱
2020/11/14
19
荧光
2020/11/14
20
酮取代反应
2020/11/14
21
四. 结果与分析
对实验现象作好详细记录, 并加以解释 请对皂化反应现象做出合理解释,而不
