苯亚甲基苯乙酮(精)
苯亚甲基苯乙酮的制备与紫外测定

实验原理
OH CHO + H3COC NaOH 25-30 ℃ -H2O O O CHCH2C
实验步骤
10%NaOH, 乙醇, 乙醇,苯乙酮 滴加苯甲醛 2525-30 ℃ 1-1.5 h, 晶体析出 2525-30 ℃ 冰浴冷却 10-15 min
抽滤,水洗涤至中性, 抽滤,水洗涤至中性, 95%乙醇洗涤, 95%乙醇洗涤,
95% 95%乙醇重结晶 抽滤,干燥 抽滤, 粗产品 (活性碳脱色) 活性碳脱色)
产品
测熔点 紫外
紫外光谱的测定
样品准备 1mg溶在 溶在100mL乙醇 溶在 乙醇 仪器初时化 选择测定条件 设定各种参数
测 试
绘制谱图
保存数据
解析谱图
注意事项
有部分人对苯亚甲基苯乙酮产生皮肤过敏,操作 有部分人对苯亚甲基苯乙酮产生皮肤过敏, 时请勿触及皮肤。 时请勿触及皮肤。 本实验的反应温度以25-30度为宜, 本实验的反应温度以25-30度为宜,温度偏高 度为宜 则副产物较多,过低则产物发粘,不易过滤。 则副产物较多,过低则产物发粘,不易过滤。 纯粹的苯亚甲基苯乙酮有几种不同的晶体形态, 纯粹的苯亚甲基苯乙酮有几种不同的晶体形态, 其熔点有所差别,通常得到的是片状的a体 其熔点有所差别,通常得到的是片状的 体(m.p. 58-59 ℃)。 。
苯亚甲基苯乙酮的制 备与紫外测定
实验目的
学习由羟醛缩合反应制备苯亚甲基苯 乙酮的原理和方法。 乙酮的原理和方法。
掌握紫外光谱仪的操作方法。 掌握紫外光谱仪的操作方法。
实验药品
药品 名称 规格 用量
苯甲醛
AR
苯乙酮
AR
NaOH溶 溶 液
10% %
乙醇
95%2.5 mL3 mL12.5 mL 7.5 mL
芳酰腙配体与Ni(Ⅱ)和Co(Ⅱ)配合物的水热合成与晶体结构(英文)

无
机
化
学
学
报
Vo . 8 No3 1 . 2
6 — 2 37 64
CHI S 0UR NE E J NAL OF I NOR GANI C CHEMI T S RY
芳酰 腙 配体 与 Ni ) C () ( 和 0Ⅱ配合 物 的水 热 合成 与 晶体 结构 Ⅱ
ae p eoewt ezy yrz e(bb)T ocodntncm on s nme M(ah2 y2 M= i1 ct hnn i bnolhdai H ah. w oriai o pu d, a l o h n o y[ bb)p) ( ]( N, ;
C , ; b b = e zl e ea e p e o eb nol y rzn , y p r ie h v e nh doh r l y tei d o 2 H ah b nyi n ct h n n e zy daoe p = yi Байду номын сангаас) aeb e y rtema ysnh s e d o h d , l z
ta iin me a o lx so s mme rc lS hf a e r nsto tlc mp e e fa y ti a c i b s
积 形 成 二 维 片 状超 分子 层 。
关键 词 : 夫 碱 ; 腙 配 体 ; 热合 成 ;配 合 物 ;晶 体 结构 席 酰 水
中 图分 类 号 : 6 48+ ; 648 0 1 .1 O 1.13 2
文献标识码 : A
文 章 编 号 :10 —8 1 0 20 —6 70 0 1 6 ( 1)30 3 —6 4 2
苯乙酮安全技术说明书
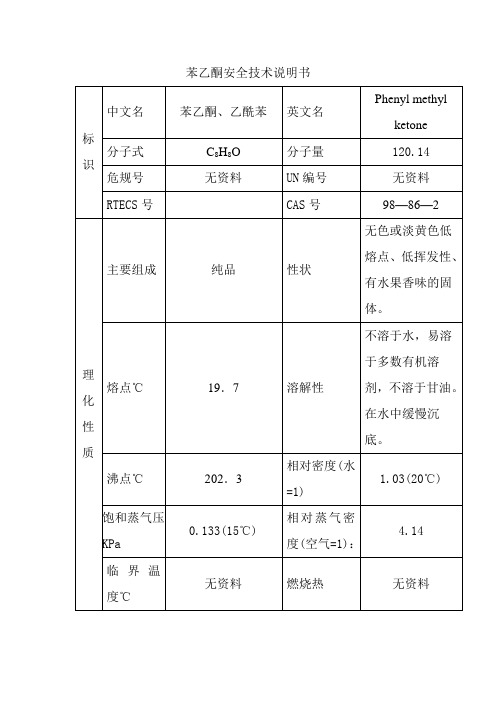
苯乙酮安全技术说明书标识中文名苯乙酮、乙酰苯英文名Phenyl methylketone分子式C8H8O分子量120.14危规号无资料UN编号无资料RTECS号CAS号98—86—2理化性质主要组成纯品性状无色或淡黄色低熔点、低挥发性、有水果香味的固体。
熔点℃19.7溶解性不溶于水,易溶于多数有机溶剂,不溶于甘油。
在水中缓慢沉底。
沸点℃202.3相对密度(水=1)1.03(20℃)饱和蒸气压KPa0.133(15℃)相对蒸气密度(空气=1):4.14临界温度℃无资料燃烧热无资料临界压力MPa 无资料最小引燃能量mJ无资料燃烧爆炸危险性燃烧性可燃燃烧分解产物一氧化碳、二氧化碳。
闪点℃82℃(开杯);77℃(闭杯)聚合危险无资料爆炸极限%无资料稳定性无资料引燃温度℃571禁忌物强氧化剂、强酸。
危险特性遇高热、明火或与氧化剂接触,有引起燃烧的危险。
若遇高热,容器内压增大,有开裂和爆炸的危险。
灭火方法如果该物质或被污染的流体进入水路,通知有潜在水体污染的下游用户,通知地方卫生、消防官员和污染控制部门。
在安全防爆距离以外,使用雾状水冷却暴露的容器。
若冷却水流不起作用(排放音量、音调升高,罐体变色或有任何变形的迹象),立即撤离到安全区域。
灭火剂泡沫、二氧化碳、干粉、砂土。
毒性前苏联MAC(mg/m3):5[皮] TLVTN:ACGIH 49mg/m3 TLVWN:未制订标准LD50:900—3000mg/kg(大鼠经口);1070mg/kg(小鼠腹腔内)空气中嗅觉阈浓度: 2ppb; 0.17ppm; 0.60ppm。
水中嗅觉阈浓度: 0.17mg/L; 0.065mg/L; 68ppm。
BOD5(五天生化需氧量): 0.5g(氧)/g(样品) COD(化学需氧量):2.532g(氧)/g(样品) ThOD: 2.532g(氧)/g(样品)对人体伤害人吞服本品可发生麻醉和止痛作用。
对人的危害主要是对眼和皮肤的刺激作用,可引起皮肤局部灼伤。
12、新实验:苯亚甲基苯乙酮的制备

实验名称:苯亚甲基苯乙酮的制备一、实验目的:1 掌握羟醛缩合反应原理和方法;2掌握反应温度控制方法;巩固滴液漏斗、搅拌器的使用。
巩固重结晶。
二、实验原理:强碱性条件下发生的羟醛缩合反应。
反应式如下:反应历程:苯亚甲基苯乙酮又称查耳酮(cha-lcone)。
有顺(Z)-,反(E)-异构体。
(E)-构型:淡黄色棱状晶体,熔点58℃,沸点345~348℃(分解),219℃(2.4kPa)。
(Z)-构型:淡黄色晶体,熔点45~46℃。
合成的混合体:熔点55~57℃,沸点208℃(3.3kPa),相对密度1.0712,1.6458。
溶于乙醚、氯仿、二硫化碳和苯,微溶于乙醇,不溶于石油醚。
吸收紫外光。
有刺激性。
能发生取代、加成、缩合、氧化、还原反应。
由苯乙酮在碱性条件下与苯甲醛缩合而成。
用作有机合成试剂和指示剂。
查耳酮广泛应用于医药和日用化学品等领域。
查耳酮经典的合成方法是在乙醇水溶液中,强碱氢氧化钠或氢氧化钾催化苯甲醛和苯乙酮羟醛缩合后脱水而得到。
近年来,在无溶剂条件下的固相有机反应由于具有反应效率高、操作简单和环境友好等优点而深受关注。
1990年首次报道了在无溶剂条件下使用氢氧化钠催化取代苯甲醛和苯乙酮羟醛缩合,以比较高的收率得到相应的查耳酮。
1997年有人采用球磨技术进一步改善了有机固相反应的效率,克服了反应底物不能充分接触的缺点。
在无溶剂条件下利用氢氧化钠和碳酸钾混合碱作为催化剂,使用球磨技术促进取代苯甲醛和苯乙酮的固相羟醛缩合,反应时间明显缩短,收率可达到90%~98%。
苯亚甲基苯乙酮是由苯甲醛与苯乙酮在10%氢氧化钠溶液催化下缩合而合成。
为了使反应顺利进行和控制苯甲醛的滴加速度,通常在装有搅拌器、温度计和滴液漏斗的三颈瓶中进行。
反应时间由滴加苯甲醛算起至加入晶种继续搅拌待反应瓶中有结晶止,需1.5~2.0h,产率67~72%。
三、物理常数试剂用量减半:苯乙酮3g,0.025mol;苯甲醛2.65g, 0.025mol ,理论产量:5.2g四、反应步骤在装有搅拌器、温度计和恒压漏斗的50 ml三口烧瓶中,加入12.5ml10%氢氧化钠溶液、7.5 ml 95%乙醇和3 ml苯乙酮。
《苯乙酮的制备》课件

苯乙酮是一种重要的化学品,在化学催化、医药和食品工业中得到广泛应用。
苯乙酮介绍
物理特性
白色晶体,微溶于水,易溶于乙醇、甲醇等有机溶剂。
化学性质
可以发生自由基反应、亲电加成反应和亲核取代反应等多种化学反应。
产业应用
主要应用于日化、医药、化学合成、生物科技等领域。
苯乙酮合成
醋苯的羟基化
通过将醋苯与顺式双羟乙基苯烷加热反应后,加入 氢氧化钠使其分解生成苯乙酮。
苯乙酮的应用
作为光引发剂
苯乙酮可用作照相学中的无色光敏剂和非黄色变色 剂,还可用于固化丙烯酸等工业生产中。
作为防晒剂
由于苯乙酮对紫外线有很强的吸收能力,所以它经 常被用于防晒产品中。
作为香料
苯乙酮是一种有醇香的化合物,常用于制作香囊、 蜡烛等香氛产品。
在食品工业中的应用
苯乙酮可以用作饮料、寿司、口香糖、果酱等食品 的防腐剂。
结论和未来方向
结论
在本次课程中,我们学习了苯乙酮的制备、性质、 合成和应用等方面的知识,并了解了苯乙酮的环保 和健康问题。
未来方向
虽然苯乙酮在许多领域都有广泛的应用,但其环保 和与人类健康有关的问题不能忽视,我们需要在制 备和应用过程中寻找更加环保和健康的替代方法。
将三氯化铝和醋酸加入反应瓶中,并加
入适量的苯,将硫酸的冷却溶液加入反
应瓶,同时滴加苯乙烯。
3
反应过程
ቤተ መጻሕፍቲ ባይዱ
将反应瓶密封后在沸水中进行加热,观
察溶液的颜色变化。反应结束后,冷却
分离与提纯
4
至室温。
通过蒸馏、结晶和有机相和水相的分离, 获得初步纯化的苯乙酮产物。
苯乙酮的分析
检查项目 蒸汽压 密度 折射率
工业催化实验

实验二指示剂法测定表面固体酸的分布一、实验目的1. 学会用指示剂判断催化剂酸强度范围。
2. 掌握用Hammett指示剂法测定催化剂表面酸性。
二、实验原理在催化剂中有一大类反应,其催化剂的活性来自其表面上的酸中心,它们的活性与催化剂的表面酸性质密切相关。
大多数金属氧化物以及由它们组成的复合氧化物都具有酸性或者碱性,有时甚至同时具有这两种性质。
按照酸和碱的定义,固体酸可以分成两类:一类是能给出质子的物质,叫Brönsted酸,简称B酸;另一类是能够接受电子对的物质,叫Lewis酸,简称L酸。
在固体催化剂的表面上,酸中心的分布是不均匀的,这时由于其表面上能量分布的不均匀性造成的。
催化剂表面酸分布是指其表面酸浓度随酸强度变化的情况。
以每克催化剂样品上酸量来表示酸浓度(即酸中心的数目),在不同酸强度下酸的总量称为总酸量。
固体表面酸性质就包括以上所述的酸类型、酸强度和酸量。
固体酸的类型可以通过吡啶吸附的红外光谱来测定。
酸强度和酸浓度可以通过Hammett指示剂法来测定,但该方法所测定的是B酸和L酸的总结果。
以B代表碱性的Hammett指示剂,当它吸附在催化剂的表面上时,与表面上的H+发生相互作用生成相应的共轭酸BH+:B + H+ = BH+ (1)碱型 酸型则共轭酸的解离平衡常数为:)/()(/)(+++++==BH BH H B B BH H B a f c a f c a a a K (2) 式中:a 为催化剂表面吸附层上的活度;c 为表面吸附层上的浓度;f 为表面吸附层上的活度系数。
指示剂与催化剂表面作用后显什么颜色取决于c BH+ / c B ,由上式:)/()(/+++=BH a H B B BH f K a f c c (3)所以c BH+ / c B 是由K a 、a H+、f B 和f BH+所决定的。
对于给定的指示剂,由于K a 是一常数,故c BH+ / c B 由f B a H+ / f BH+来决定。
超声辐射合成苯亚甲基苯乙酮的研究

超声辐射合成苯亚甲基苯乙酮的研究阿布力米提·阿布都卡德尔;孙亚栋;张永红;张增鹏【摘要】以乙醇为溶剂,苯甲醛和苯乙酮为原料,在无机碱NaOH为催化剂作用下通过超声辐射合成了苯亚甲基苯乙酮,产物经IR和1HNMR分析表征,并考察了原料配比、催化剂用量、超声辐射时间和功率等因素对产物收率的影响.实验结果表明,当苯甲醛与苯乙酮的的摩尔比为1:1,催化剂的用量为8.3 mL,超声波辐射功率为700W,超声波辐射40 min,苯亚甲基苯乙酮产率达92%.此合成方法与传统的合成方法相比,具有反应时间短、产率高、易纯化、物耗低及污染少等优点,体现了有机合成教学绿色化的改革目标.%Benzylidene acetophenone was synthesized with ethanol as solvent,benzaldehyde and acetophenone as raw material and inorganic alkali NaOH as catalyst under ultrasonic radiation.The products were characterized by IR and 1HNMR analysis.Meanwhile,the raw-material ratio,the amount of catalyst,ultrasonic irradiation time and other factors on the yield were examined as well.Experimental results show that when the molar ratio of benzaldehyde and acetophenone is 1:1,the amount of catalyst is 8.3 mL,ultrasonic radiation power is 700 W,for 40 min,benzylidene acetophenone was obtained in 92% yield within 40 min under ultrasonic pared to traditional synthetic methods this protocol has the advantages of short reaction time,high yield,easy purification,low material consumption and less pollution,etc.,which reflects the green organic synthesis teaching reform objectives.【期刊名称】《新疆大学学报(自然科学版)》【年(卷),期】2017(034)004【总页数】4页(P426-428,434)【关键词】苯亚甲基苯乙酮;超声波辐射;绿色合成【作者】阿布力米提·阿布都卡德尔;孙亚栋;张永红;张增鹏【作者单位】新疆大学化学化工学院,新疆乌鲁木齐830046;新疆大学化学化工学院,新疆乌鲁木齐830046;新疆大学化学化工学院,新疆乌鲁木齐830046;新疆大学化学化工学院,新疆乌鲁木齐830046【正文语种】中文【中图分类】Q939.97苯亚甲基苯乙酮又称查尔酮,具有多种药理作用和生物活性,广泛应用于医药和日用化学品等领域[1,2],苯亚甲基苯乙酮的合成实验是高等院校化学专业有机化学实验中必做的综合性实验.关于它的合成方法较多,主要有使用强碱或者强酸催化苯乙酮和苯甲醛的羟醛缩合,但是副反应较多,产率偏低[3].传统合成方法是以乙醇为反应溶剂,10%的氢氧化钠水溶液催化苯乙酮与苯甲醛发生羟醛缩合脱水而得,目前有机化学实验教材普遍采用该方法来合成苯亚甲基苯乙酮[4−7].在实验过程中,人们在如何更加简单高效的获得苯亚甲基苯乙酮方面做了很多的努力.如无溶剂条件下,发展了苯乙酮和苯甲醛在双组份固体碱氢氧化钠和碳酸钾催化下合成苯亚甲基苯乙酮的方法[8],固相条件下的机械振荡技术[9],还有功能化离子液体催化方法[10]等.人们也发展了微波辅助制备苯亚甲基苯乙酮的方法[11,12].20世纪80年代以来,随着声化学的发展,超声辐射(U.S.)在有机合成中的应用研究呈蓬勃发展之势,已广泛应用于氧化、还原、取代、缩合和水解等反应中,几乎涉及有机反应的各个领域[13−15].而且,近期也有文献报道使用超声技术[16,17]合成苯亚甲基苯乙酮.因此,我们也将超声波技术引入有机合成实验中,这样可以使有机反应速率比普通加热反应快数十倍甚至数万倍.既可以节约能源,缩短实验时间,又能提高反应产率.加之进行的是半微量反应实验,既减少了污染,也更符合当今“节能减排”和“绿色化学”的理念[18].合成路线见图1.图 1 超声辐射合成苯亚甲基苯乙酮1 实验部分主要仪器与试剂仪器:XH-2008D型智能温控低温超声波催化合成/萃取仪,超声波功率:1 500 W,频率:25 KHz,加热功率:300 W,制冷功率:450 W,北京祥鹄科技发展有限公司;CSF-3A型超声波清洗器,500 W,25 KHz,上海超声波仪器厂;B¨UCHI(M-560)型熔点仪;Bruker Equinox 55 FT-IR分光光度计(KBr压片);VARIAN INOVA-400型核磁共振仪.试剂:10%NaOH水溶液;95%乙醇;苯乙酮;新蒸苯甲醛;无水乙醇.2 实验步骤2.1 苯亚甲基苯乙酮的合成将10%NaOH水溶液6.3 mL,95%EtOH 7.5 mL,苯乙酮3 mL(3 g,25 mmol),依次加入50 mL锥形瓶中,冷却至室温,再加入新蒸苯甲醛2.5 mL(2.65 g,25 mmol).将反应瓶置于超声波催化合成仪或超声波清洗槽中,启动超声反应器.于25◦C∼30◦C反应至有结晶析出,反应需要30∼35 min,停止反应.2.2 苯亚甲基苯乙酮的分离与提纯反应混合液于冰浴中冷却,使其结晶完全.抽滤,用冷水洗涤(至滤液呈中性),然后用2.5 mL冰乙醇洗涤结晶,干燥,称量,计算收率.2.3 苯亚甲基苯乙酮的结构分析熔点:56◦C∼57◦C.1H NMR(400 MHz,CDCl3):δ 8.08-7.97(m,2H),7.81(d,J=15.7 Hz,1H),7.68-7.46(m,6H),7.45-7.36(m,3H).IR(KBr压片):3 053 cm−1和3 031 cm−1吸收峰是苯环C-H键的伸缩振动;1 663cm−1是羰基键C=O的伸缩振动;1 573 cm−1和1 607 cm−1吸收峰归属于苯环C=C键的面内伸缩振动;750 cm−1,749 cm−1和685 cm−1吸收峰是芳环单取代面外弯曲振动,说明有单取代苯存在;与标准图谱吸收峰的强度及位置一致,最终可以确定产物为苯亚甲基苯乙酮.3 结果与讨论3.1 超声辐射时间对苯亚甲基苯乙酮产率的影响量取10%NaOH水溶液6.3 mL,95%EtOH 7.5 mL,保持n(苯乙酮):n(苯甲醛)=1:1,反应温度25◦C∼30◦C等条件不变,改变超声辐射时间,以考察超声辐射时间对产品收率的影响,结果见图2.3.2 超声波强度对苯亚甲基苯乙酮产率的影响量取10%NaOH水溶液6.3 mL,95%EtOH 7.5 mL,保持n(苯乙酮):n(苯甲醛)=1:1,反应温度25◦C∼30◦C等条件不变,改变超声波强度,以考察超声波强度对产品收率的影响,结果见图3.可以看出,随着超声辐射功率的加强,产率收率有所增加.3.3 不同反应方式的对比从表1结果来看,超声波发生器促进的反应在40 min内能得到92%产率,而采用超声清洗器促进的方法在40 min内能得到88%产率.因此超声波促进的反应具有一定的优势,而且超声波辐射法降低了反应能耗,减少环境污染的目的,符合绿色化学的理念.3.4 反应物的摩尔比对产品收率的影响根据化学反应平衡原理,增大物质的量比有利于提高产品的收率,但会造成原料的浪费.本实验保持催化剂10%NaOH 6.3 mL,95%EtOH 7.5 mL,超声波辐射功率700 W,实验温度25◦C∼30◦C实验时间40 min等条件不变,改变苯甲醛的用量,考察苯乙酮与苯甲醛的摩尔比对产品收率的影响.结果见表2.结果显示,苯甲醛与苯乙酮的摩尔比为1:1得到最高的收率92%.图 2 超声辐射时间对苯亚甲基苯乙酮产率的影响图 3 超声波强度对苯亚甲基苯乙酮产率的影响表 1 不同反应方式对苯亚甲基苯乙酮产率的影响?3.5 催化剂用量的影响催化剂的用量对产品的收率有很大的影响.为考察催化剂用量对产品收率的影响,保持苯乙酮3 mL,苯甲醛2.5 mL,超声功率700 W,反应时间40 min,反应温度25◦C∼30◦C等条件不变,改变催化剂10%NaOH的用量,结果见表3.表 2 苯乙酮与苯甲醛的摩尔比对苯亚甲基苯乙酮产率的影响?表 3 催化剂用量对苯亚甲基苯乙酮产率的影响?由表3可知,随着催化剂用量的增加,产品收率显著提高,当催化剂用量为6.3 mL时,收率达到92%,再继续加大催化剂用量,产品收率并没有明显的升高.故选择催化剂用量6.3 mL为宜.4 结论1.本实验利用超声波辐射技术,以苯乙酮和苯甲醛为原料,10%氢氧化钠为催化剂合成了苯亚甲基苯乙酮,通过条件优化以高达92%收率获得了苯亚甲基苯乙酮.2.通过对超声波清洗器与超声波合成仪的对比,表明此方法具有催化剂价廉易得、催化效果好、合成路线短、反应条件温和、提纯操作简单,且超声波合成仪具有更为高效和符合绿色经济的优点.参考文献:[1]郑洪伟,牛新文,朱君,等.查尔酮类化合物生物活性研究进展[J].中国新药杂志,2007,16(18):1445-1449.[2]由业诚,张晓辉,郭明,等.微波辐射KF-Al2O3催化合成查尔酮的研究[J].化学研究与应用,2000,12(2):186-188.[3]郭宏雄,臧庶声,李文科,等.查耳酮的制备I[J].兰州医学院学报,1998,24(2):12213.[4]武汉大学化学与分子科学学院实验中心编.有机化学实验[M].武汉:武汉大学出版社,2004,241-242.[5]北京大学化学学院有机化学研究所编.有机化学实验:2版[M].北京:北京大学出版社,2002,168-169.[6]李兆陇,银金香,林天舒.有机化学实验[M].北京:清华大学出版社,2000,128-129.[7]李霁良.微型半微型有机化学实验[M].北京:高等教育出版社,2003,207-208.[8]胡晓允,周忠强,单自兴.苯亚甲基苯乙酮合成方法的改进[J].广州化工,2013,41(3):50-51.[9]王春山,吴浩浩,谭亚军,等.查尔酮及氮杂查尔酮的机械法合成[J].南通大学学报(自然科学版),2013,12(1):40-44.[10]胡晓允,韦丽艳,钟诗诗,等.功能化离子液体催化合成苯亚甲基苯乙酮[J].实验室科学,2015,18(3):48-50.[11]刘兴利,赵志刚,曾碧涛,等.微波干法合成查尔酮[J].化学研究与应用,2007,19(5):574-576.[12]张国喜,杨金凤,姬广军,等.微波辅助合成查尔酮衍生物的工艺[J].石河子大学学报(自然科学版),2011,29(6):785-788.[13]廖九中,杨慧文,潘育方.延胡索生物碱超声法提取工艺的研究[J].广东药学院学报,2012,28(2):153-155.[14]李记太,臧洪俊.超声波应用于有机合成方面的新进展[J].河北大学学报(自然科学版),2000,20(1):96-102.[15]赵新海,姬红,刘晨江.氨基磺酸铵:一种“一锅法”合成3,4-二氢嘧啶-2(1H)-(硫)酮的有效催化剂[J].新疆大学学报(自然科学版),2010,27(2):132-135. [16]黄丹,江国庆.超声技术在查尔酮合成中的应用研究[J].有机化学,2002,22(12):1057-1059.[17]贾兆海,陈馥衡,谢毓元.超声波在有机合成中的应用[J].化学进展,1998,10(1):63-73.[18]周先波,周赛春,王永红,等.在有机合成实验教学中超声波应用初探[J].实验科学与技术,2007,5(6):107-108.。
苯亚甲基苯乙酮合成方法的改进

( 1 Co l l e g e o f C h e mi s t r y a n d Ma t e r i a l s ,S o u t h—C e n t r a Un i v e r s i t y f o r Na t i o n a l i t i e s ,Hu b e i Wu h a n 4 3 0 0 7 4;
苯 亚 甲基 苯 乙 酮 ,又称 查 尔 酮 ,在 医 药 和 日用 化 学 品 领 域
有广泛的应用。苯亚甲基苯 乙酮 的传 统合成方法 是 以乙醇为反 应溶 剂 ,1 0 % 的氢氧化钠水溶液催化苯 乙酮和苯 甲醛发生 羟醛 缩合 脱水而得。现行的有机化 学实验 教材 。 - 4 1 ~般都选用 这种 方法 合成苯亚甲基苯乙酮 ,其具 体方法 是 :往苯 乙酮 、乙醇及 1 0 %氢氧化钠水溶液 的混合体 系中缓 慢滴加 苯 甲醛 ,控制 滴加 速度使 反应温度控 制在 2 5~ 3 0℃ ,滴加 完后继 续搅 拌至 有 晶
体析 } { I ,一 般 需 1 . 5~ 2 h ,收率 5 7 . 7 % 一8 7 . 3 %。
文章 编号 :1 0 0 1 — 9 6 7 7 ( 2 0 1 3 ) 0 3 — 0 0 5 0 — 0 2
An I mp r o v e d Me t h o d f o r P r e p a r a t i o n o f Ch a l c o n e
HU Xi a o—y u n ,ZHOU Zh o n g ~q i a n g ,S HAN Zi—x i n g
2 C o l l e g e o f C h e m i s t y r a n d M o l e c u l a r S c i e n c e s , Wu h a n U n i v e r s i t y ,H u b e i Wu h a n 4 3 0 0 7 2, C h i n a )
苯亚甲基苯乙酮

R-CH2CH=O + R-CH-CH=O
OH H2O
R-CH2 -CH-CH-CH=O O R
R-CH2-CH-CHCH=O OH R
R-CH2-CH=CH-C=O R
3)交叉羟醛缩合反应 交叉羟醛缩合反应
C6H5CHO + CH 3CHO OH
[
C6H5-CH-CH2-CHO ] OH
粗产物用95%乙醇重结晶(每克产物约需4-5[实际 粗产物用95%乙醇重结晶( 每克产物约需4 95 3-4] mL溶剂),若溶液颜色较深可加少量活性炭脱色, mL溶剂) 若溶液颜色较深可加少量活性炭脱色, 溶剂 得浅黄色片状结晶6-7克,熔点56-57℃。 得浅黄色片状结晶6 熔点56-57℃ 56
二、实验原理
羟醛缩合反应是制备α 羟醛缩合反应是制备 α , β- 不饱和醛酮的重要方 法。 活泼氢的芳醛可与有α 无α-活泼氢的芳醛可与有α-活泼氢的醛酮发生 的交叉的羟醛缩合反应又称为claisen-schmidt反应 。 反应。 的交叉的羟醛缩合反应又称为 反应 缩合产物自发脱水生成稳定的共轭体系α 缩合产物自发脱水生成稳定的共轭体系 α , β- 不饱 和醛酮。 和醛酮。它是合成侧链上含两种官能团的芳香族化合 物及含几个苯环的脂肪族体系中间体的一条重要途径。 物及含几个苯环的脂肪族体系中间体的一条重要途径。
苯亚甲基苯乙酮 (查尔酮) 查尔酮) Benzal acetophenone
主 要 内 容
一、目的要求 二、实验原理 三、试剂及仪器 四、实验装置图 五、操作步骤 六、注意事项 七、问题 八、结果要求
一、目的与要求
1、掌握羟醛缩合反应的原理和机理 、 2、学会查尔酮的合成方法 、 3、掌握机械搅拌器、复习恒压滴液 、掌握机械搅拌器、 漏斗的规范操作 4、学会如何控制反应温度的操作 、
2020有机化学实验2-5苯亚甲基苯乙酮

10%氢氧化钠水溶液5mL 5mL 95% C2H5OH 2.2mL苯乙酮
实验步骤
1.加料、反应: (2)开动电磁搅拌器,并加热至20℃(微热)时 滴加1.84mL苯甲醛,保温(20~25℃) 搅 拌 20min(滴加苯甲醛不宜过快,因该反应为放热反 应);再在冰水浴中搅拌30 min,有黄色晶体生成 (若没有晶体析出的话,可加入苯亚甲基苯乙酮晶 种,促进晶体析出)。
实验步骤
2. 抽滤: • (1)抽滤; • (2)用水洗涤产品至中性(由于产品不溶于水,
因此可用H2O洗涤) • (3)压紧,抽干,得粗产品。
实验步骤
3. 重结晶:
(1)将粗产品转移至25mL锥形瓶中,在锥形瓶 上装上直型水冷凝管,加入7.5mL95% C2H5OH (分批滴加,边滴加边加热),在50~55℃热水浴 中加热(水浴温度不应超过55℃,因产品的熔点 为 57℃ ) , 粗 产 品 溶 解 后 , 再 多 加 3mL 95% C2H5OH。
• 4.本实验中,重结晶操作应注意哪些问题?
1) 为使结晶和重结晶地收率高,溶剂的量尽可能少, 故在开始加入的溶剂量不足以将欲纯化的化学试剂全部溶 解,在加热的过程中可以小心的补加溶剂,直到沸腾时固 体物质全部溶解为止
• 2) 以及为了便于重复,固体和溶剂都应予以称量和计量。
• 3) 在使用混合溶剂进行结晶和重结晶时,最好将欲纯化 的化学试剂溶于少量溶解度较大的溶剂中,然后趁热慢 慢地分小份加入溶解度较小的第二种溶剂,直到它触及 溶液的部位有沉淀生成但旋即有溶解为止。
3. 由于产物熔点低(57℃),重结晶回流时,有时产品呈熔 融状,需加溶剂使其成均相,且温度不能超过55℃。
注意事项
4. 粗产品重结晶时用回流装置制备饱和溶液。 5. 某些人对本产品过敏,皮肤触及时发痒,使用时应注意。
苯亚甲基苯乙酮-4-氯苯甲酰腙的合成、晶体结构及荧光性质

2 结果与讨论
2 1 红外 光谱 分析 .
在 40 0~ 0 m 范 围 内测定 了标 题 化合 物 0 4 0 c 的红外光谱 。I R分析 表 明 , 3 10c 在 5 m 处 有较 强
冷却。滴完后 , 维持此温度继续搅拌 3 i, 0mn 再在室 温下搅拌 15h 有晶体析出。停止搅拌 , . , 以冰浴冷 却1 i, 结 晶完 全 。抽 滤 , 集 产 物 , 水 充 分 5mn使 收 用 洗涤 至洗 出液呈 中性 , 后 用 约 1 . 然 0 0 mL冰 乙醇 洗
= .2 (ldt) G F= .6 。荧光光谱表 明, 02 67 a aa , O 0 9 8 l 该化合物 的荧光性能较好 , 以作为一种潜在的光 活性材料 。 可
关键词 : 酰腙 ; 合成 ; 晶体结 构 ; 荧光
中 图分 类 号 : Q0 12 T 5 . 2 T 3 . ; Q0 0 4 2 文 献标 识 码 : A 文 章 编 号 :6 1— 2 6 2 1 )2— 18— 3 17 30 ( 0 1 1 23 0
的吸 收 峰 , 属 于 化 合 物 中 ( 一N — N ) 1 归 H 一 的 J ( — H) 在 l64c 处 出现强 而 尖锐 的 吸收 峰 , N ; 5 m 其 归 属 于 化 合 物 中一 C N 一 的 v( C-O ) 收 O H  ̄ - 吸 峰 ; 1 8 m 附 近 出 现 的 吸 收 峰 归 属 为 在 59 c
实验室常用毒、麻、精、放药品

实验室常用毒、麻、精、放药品目录:1 毒品:西药类:金属砷、三氧化二砷(亚砷酸)、流化砷、三流化砷(雌黄)、五流化钾(雄黄)、砷酸甲、亚砷酸钾、亚酸砷钠、亚砷酸钙、砷酸硼、二氧化硒、偏钒酸钠、砒石(红矾)王氧化二钒、白砒、亚砒酸、苯巴比妥(鲁米钠)巴比妥酸、流代巴比妥酸(TBA)、巴比妥钠、巴比妥、戊巴比妥钠、苯巴比妥钠、阿米妥钠、阿片粉、去水吗啡、盐酸乙基吗啡、盐酸吗啡、盐酸吗啡针、海洛因、吗啡阿托品、氢溴酸后吗托品、磷酸可待因、盐酸可卡因、盐酸普罗卡因、硝酸士的年、马钱子碱、硝基马钱子硷、马钱子丁碱、硝酸毛果云香碱、氢溴酸东芭苍碱、Cauehaviein、 Pricaine、毒毛旋花素K、箭毒、盐酸毒箭毒、氯化简箭毒、水杨酸毒扁豆碱、印防己毒素、盐酸佐旋麻黄素、红色氧化汞、黄色氧化汞、氯化汞、溴化汞、碘化汞、黄硫化汞、黑硫化汞、硝酸汞、硝酸亚汞、对氯汞苯甲酸、乙酸汞、乙酸亚汞、乙酸第二水银、水杨酸汞、流氰化汞、流氰酸汞、汞、汞碘化银、流氰酸汞铵、偏钒酸铵、氰化钾、氰化钠、氰化铜、氰化亚铜、氰氢酸、溴化氰、氯化钡、三氧化锑、三氧化二锑、饿酸。
中药类:砒石、砒霜、水银、生马钱子、生传乌、生草乌、生白附子、生附子、生半夏、生南星、生巴豆、斑蝥、青娘虫、红娘虫、生甘遂、生狼毒、生藤黄、生千金子、生天仙子、闹羊花、雪上枝蒿、白降丹、蟾酥、洋金花、红粉、轻粉、雄黄。
2 麻醉品: (1)阿片类 (2)阿片生物碱类 (3)可卡因 (4)吗啡代用品(5)大麻类3 精神药品: 吗啡、杜冷丁、强痛定、安钠咖、咖啡因、复方樟脑西丁等4 放射性药品:3H 14C 32S 35P 45Ca 51Cr 68Ga 59Fe 86Rb 125I 131I 99m Tc附件四实验室常用易燃、易爆化学试剂目录:1 苯类: 苯、联苯、异丙苯、乙基苯、丁基苯、135三甲苯、碘代苯、氯苯、对二氯苯、邻二氯本、间二氯苯、对硝基氯代苯、2,4二硝基氯代苯、对硝基溴代苯、六氢代苯、邻溴氯苯、第二丁基苯、第三丁基苯、偶氮苯、聚氯羟苯、硝基苯、间二硝基苯、甲苯、二甲苯、对二甲苯、1,2,4,5四甲基苯、三氯甲苯、3,4二氯甲苯、间溴甲苯、间硝基甲苯、2,4二硝基甲苯,2,4一二硝基氟苯,二乙烯苯,过氧化羟异丙苯。
实验室常用毒、麻、精、放药品目录

实验室常用毒、麻、精、放药品目录1. 毒品:西药类:金属砷、三氧化二砷(亚砷酸)、硫化砷、三硫化砷(雌黄)、五硫化钾(雄黄)、砷酸钾、亚砷酸钾、亚酸砷钠、亚砷酸钙、砷酸硼、二氧化硒、偏钒酸钠、砒石(红矾)五氧化二钒、白砒、亚砒酸、苯巴比妥(鲁米钠)巴比妥酸、硫代巴比妥酸(TBA)、巴比妥钠、巴比妥、戊巴比妥钠、苯巴比妥钠、阿米妥钠、阿片粉、去水吗啡、盐酸乙基吗啡、盐酸吗啡、盐酸吗啡针、海洛因、吗啡阿托品、氢溴酸后吗托品、磷酸可待因、盐酸可卡因、盐酸普罗卡因、硝酸士的年、马钱子碱、硝基马钱子硷、马钱子丁碱、硝酸毛果云香碱、氢溴酸东芭苍碱、Cauehaviein、Pricaine、毒毛旋花素K、箭毒、盐酸毒箭毒、氯化简箭毒、水杨酸毒扁豆碱、印防己毒素、盐酸佐旋麻黄素、红色氧化汞、黄色氧化汞、氯化汞、溴化汞、碘化汞、黄硫化汞、黑硫化汞、硝酸汞、硝酸亚汞、对氯汞苯甲酸、乙酸汞、乙酸亚汞、乙酸第二水银、水杨酸汞、流氰化汞、流氰酸汞、汞、汞碘化银、流氰酸汞铵、偏钒酸铵、氰化钾、氰化钠、氰化铜、氰化亚铜、氰氢酸、溴化氰、氯化钡、三氧化锑、三氧化二锑、饿酸。
中药类:砒石、砒霜、水银、生马钱子、生传乌、生草乌、生白附子、生附子、生半夏、生南星、生巴豆、斑蝥、青娘虫、红娘虫、生甘遂、生狼毒、生藤黄、生千金子、生天仙子、闹羊花、雪上枝蒿、白降丹、蟾酥、洋金花、红粉、轻粉、雄黄。
2.麻醉品:(1)阿片类(2)阿片生物碱类(3)可卡因(4)吗啡代用品(5)大麻类3.精神药品:吗啡、杜冷丁、强痛定、安钠咖、咖啡因、复方樟脑西丁等4.放射性药品:3H、14C、32P、35S、45Ca、51Cr、68Ga、59Fe、86Rb、125I、131I、99mTc等附件四:实验室常用易燃、易爆化学试剂目录1.苯类:苯、联苯、异丙苯、乙基苯、丁基苯、135三甲苯、碘代苯、氯苯、对二氯苯、邻二氯本、间二氯苯、对硝基氯代苯、2,4二硝基氯代苯、对硝基溴代苯、六氢代苯、邻溴氯苯、第二丁基苯、第三丁基苯、偶氮苯、聚氯羟苯、硝基苯、间二硝基苯、甲苯、二甲苯、对二甲苯、1,2,4,5四甲基苯、三氯甲苯、3,4二氯甲苯、间溴甲苯、间硝基甲苯、2,4二硝基甲苯,2,4一二硝基氟苯,二乙烯苯,过氧化羟异丙苯。
苯乙酮MSDS

苯乙酮第一部分:化学品名称化学品中文名称:苯乙酮化学品英文名称:phenyl methyl ketone中文名称2:乙酰苯英文名称2:acetyl benzene技术说明书编码:1730CAS No.:98-86-2分子式:C8H8O分子量:120.14第二部分:成分/组成信息有害物成分含量CAS No.苯乙酮98-86-2第三部分:危险性概述危险性类别:侵入途径:健康危害:人吞服本品可发生麻醉和止痛作用。
对人的危害主要是对眼和皮肤的刺激作用,可引起皮肤局部灼伤和角膜损害。
除热蒸气外,一般吸入和在工业操作过程中不会引起中毒危害。
环境危害:对环境有危害,对大气可造成污染。
燃爆危险:本品可燃,具刺激性。
第四部分:急救措施皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗至少15分钟。
就医。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。
就医。
吸入:脱离现场至空气新鲜处。
如呼吸困难,给输氧。
就医。
食入:饮足量温水,催吐。
就医。
第五部分:消防措施危险特性:遇明火、高热可燃。
若遇高热,容器内压增大,有开裂和爆炸的危险。
有害燃烧产物:一氧化碳、二氧化碳。
灭火方法:消防人员须佩戴防毒面具、穿全身消防服,在上风向灭火。
灭火剂:雾状水、泡沫、干粉、二氧化碳、砂土。
第六部分:泄漏应急处理应急处理:隔离泄漏污染区,限制出入。
切断火源。
建议应急处理人员戴防尘面具(全面罩),穿防毒服。
用砂土、蛭石或其它惰性材料吸收。
收集于干燥、洁净、有盖的容器中,转移至安全场所。
若大量泄漏,收集回收或运至废物处理场所处置。
第七部分:操作处置与储存操作注意事项:密闭操作,局部排风。
操作人员必须经过专门培训,严格遵守操作规程。
建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,穿防毒物渗透工作服,戴橡胶耐油手套。
远离火种、热源,工作场所严禁吸烟。
使用防爆型的通风系统和设备。
避免与氧化剂、酸类接触。
搬运时要轻装轻卸,防止包装及容器损坏。
配备相应品种和数量的消防器材及泄漏应急处理设备。
乙酸乙酯与苯乙酮的碳谱峰区间位置解读

乙酸乙酯与苯乙酮的碳谱峰区间位置解读乙酸乙酯(ethyl acetate)和苯乙酮(phenylacetone)是常见的有机化合物,在碳谱分析中表现出一系列特征性的峰。
本文将对乙酸乙酯和苯乙酮在碳谱中的峰区间位置进行解读,以帮助读者更好地理解这两种化合物的结构和定性分析方面的应用。
乙酸乙酯的碳谱峰区间位置解读乙酸乙酯的分子式为C4H8O2,它包含两个乙基基团和一个乙酸基团。
在碳谱分析中,乙酸乙酯的峰区间位置可以提供关于化合物各个碳原子的信息。
以下是乙酸乙酯常见的碳谱峰区间位置及其对应的化学位移值:1.舒尔特环(Schiff base):124-135 ppm该峰位于碳谱的较低频率区间,是乙酸乙酯结构中甲基羰基碳原子的化学位移值。
这个碳原子与乙酸基团相连,形成一个C=O官能团。
2.甲基醚(methyl ether):52-58 ppm该峰位于碳谱的中等频率区间,对应乙酸乙酯结构中两个甲基基团上的碳原子。
甲基基团是乙酸乙酯的一个重要结构特征。
3.亚甲基(methylene):30-35 ppm该峰位于碳谱的较高频率区间,对应乙酸乙酯结构中两个亚甲基基团上的碳原子。
亚甲基基团是乙酸乙酯的另一个重要结构特征。
4.乙酸基团(acetyl):166-174 ppm该峰位于碳谱的较高频率区间,对应乙酸乙酯结构中的乙酸基团上的碳原子。
乙酸基团是乙酸乙酯的另一个重要结构特征。
苯乙酮的碳谱峰区间位置解读苯乙酮的分子式为C9H10O,它有一个苯环和一个丙酮基团。
苯乙酮的碳谱峰区间位置可以提供有关苯环和丙酮结构的信息。
以下是苯乙酮常见的碳谱峰区间位置及其对应的化学位移值:1.苯环(benzene ring):115-150 ppm该峰位于碳谱的较低频率区间,对应苯乙酮结构中苯环上的碳原子。
苯环是苯乙酮分子结构的重要组成部分。
2.丙酮基团(acetone group):190-210 ppm该峰位于碳谱的较高频率区间,对应苯乙酮结构中丙酮基团上的碳原子。
苯乙酮

谢谢观看
注意事项
安全术语 风险术语
危险性概述 急救措施
泄漏应急处理
消防措施
操作处置与储存
S26:In case of contact with eyes, rinse immediately with plenty of water and seek medical advice.
不慎与眼睛接触后,请立即用大量清水冲洗并征求医生意见
应用
用于制造香皂和纸烟。也用作有机化学合成的中间体、纤维树脂等的溶剂和塑料的增塑剂。用于调配樱桃、 番茄、草莓、杏等食用香精,也可用于烟用香精中。在最终加香食品中的建议用量为0.6~20mg/kg 。
作溶剂使用时,有沸点高、稳定、气味愉快等特点。溶解能力与环己酮相似,能溶解硝化纤维素、乙酸纤维 素、乙烯树脂、香豆酮树脂、醇酸树脂、甘油醇酸树脂等。常与乙醇、酮、酯以及其他溶剂混合使用。
苯乙酮
有机化合物
01 理化性质
目录
02 分子结构数据
03 计算化学数据
04 制备
05 应用
06 注意事项
苯乙酮,分子式为C8H8O,是一种有机化合物,为无色或淡黄色液体,不溶于水,易溶于多数有机溶剂。
理化性质
物理性质
ห้องสมุดไป่ตู้化学性质
熔点:19.6℃ 密度:1.03g/cm3 沸点:202.3℃ 分子式:C8H8O 分子量:120.14 饱和蒸气压(kPa):0.133(15℃) 闪点:82.2℃ 折光率:1.512 logP:1.66 外观:无色或淡黄色油状液体 溶解性:不溶于水,易溶于多数有机溶剂
甲苯乙酮结构

甲苯乙酮结构
一、介绍甲苯乙酮的基本信息
甲苯乙酮(Acetophenone)是一种有机化合物,分子式为C8H8O,分子量为120.15 g/mol。
它是一种无色液体,有芳香味。
甲苯乙酮可以用于制造香精、树脂、橡胶等化工产品。
二、甲苯乙酮的结构式
甲苯乙酮的结构式如下:
CH3
|
C=O
|
C6H5
三、甲苯乙酮的物理性质
1. 外观:无色液体。
2. 气味:芳香味。
3. 熔点:-15°C。
4. 沸点:202°C。
5. 密度:1.03 g/cm³。
6. 折射率:1.529。
四、甲苯乙酮的化学性质
1. 酸碱性:中性物质,不溶于水,易溶于有机溶剂。
2. 氧化还原反应:可以被氢气还原为环己醇;可以被硝酸银氧化为对羟基苯甲酮;可以和亚硝酸钠反应生成对硝基苯甲酮。
3. 反应活性:可以和乙酸酐反应生成苯乙酮;可以和苯乙烯反应生成二苯基乙烯。
五、甲苯乙酮的用途
1. 香精制造:甲苯乙酮是制造香精的重要原料之一,可以用于制造花香、果香等不同种类的香精。
2. 树脂制造:甲苯乙酮可以用于合成各种树脂,如聚丙烯腈树脂、聚丁二烯树脂等。
3. 橡胶制造:甲苯乙酮可以作为橡胶生产中的溶剂和活性剂。
4. 医药化学:甲苯乙酮可以作为医药中间体,如合成抗癌药物、镇静剂等。
六、安全注意事项
1. 甲苯乙酮易燃,避免接触明火。
2. 甲苯乙酮有刺激性气味,避免长时间吸入高浓度气体。
3. 甲苯乙酮有一定毒性,避免误食或皮肤接触。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
3、粗产物分离
减压抽滤收集产物,用水充分洗涤,至洗涤液 对PH试纸显中性。然后用少量冷乙醇(5-6 mL)洗 涤结晶,挤压抽干,得苯亚甲基苯乙酮粗品。
4、粗产物提纯
粗产物用95%乙醇重结晶(每克产物约需 4-5[实际 3-4] mL溶剂),若溶液颜色较深可加少量活性炭脱色, 得浅黄色片状结晶6-7克,熔点56-57℃。
苯亚甲基苯乙酮 (查尔酮) Benzal acetophenone
主 要 内 容
一、目的要求 二、实验原理 三、试剂及仪器 四、实验装置图 五、操作步骤 六、注意事项 七、问题 八、结果要求
一、目的与要求
1、掌握羟醛缩合反应的原理和机理 2、学会查尔酮的合成方法 3、掌握机械搅拌器、复习恒压滴液 漏斗的规范操作 4、学会如何控制反应温度的操作
2、合成
所有试剂用量减半
依次加入25mL10%氢氧化钠溶液、15 mL乙醇和6 mL苯乙 酮,搅拌下由滴液漏斗滴加5 mL苯甲醛,控制滴加速度保持 反应温度在 25-30℃之间,必要时用冷水浴冷却。滴加完毕 后,继续保持此温度搅拌 0.5h[1 h 要搅拌充分 ] 。然后加几 粒苯亚甲基苯乙酮的晶种,室温下继续搅拌 1-1.5h,即有固 体析出。反应结束后将三颈瓶置于冰水浴中冷却 15-30min, 使结晶完全。
二、实验原理
羟醛缩合反应是制备α,β- 不饱和醛酮的重要方 法。
无α-活泼氢的芳醛可与有α-活泼氢的醛酮发生
的交叉的羟醛缩合反应又称为 claisen-schmidt 反应。 缩合产物自发脱水生成稳定的共轭体系α,β- 不饱 和醛酮。它是合成侧链上含两种官能团的芳香族化合 物及含几个苯环的脂肪族体系中间体的一条重要途径。
NaOH O CC6H5 H
O [ C6H5-CH-CH2CC6H5 ] OH
-H O 2
反应机理:
H2O
CH2COC6H5 + C6H5CH=O OH C6H5CH CH2COH5
OH
CH2COC6H5 O
O CH2=CC6H5 ] C6H5CH CH2COC6H5
六、注意
1、搅拌器要装正 2、温度计不能装,会打碎;稀碱最好新配(浓 度要够) 3、一定要按顺序加入试剂,因为可抑制副反应 发生过多 4、控制好温度,参见注释1 5、滴加完苯甲醛搅拌时间最好1 h,见注释2 6、洗涤时要充分,转移至烧杯中进行 7、重结晶时一定要使产物完全溶解,呈均相, 若为油水 分离状不行,见注释4 8、产物对某些人皮肤过敏,注意尽量不与皮肤 接触
OH H2O
R-CH2 -CH-CH-CH=O O R
R-CH2-CH-CHCH=O OH R
R-CH2-CH=CH-C=O R
3)交叉羟醛缩合反应
C6H5CHO + CH3CHO OH
[
C6H5-CH-CH2-CHO ] OH
H2O
C6H5CH=CHO
本实验的主反应:
o
C6H5CHO + CH3CC6H5 H C6H5 C=C
七、问题
1、什么是羟醛缩合反应? 2、交叉羟醛缩合反应又是一人名反应,称为什 么? 3、本反应中若将稀碱换成浓碱可以吗?为什么? 4、先加苯甲醛,后加苯乙酮可以吗?为什么? 5、用水洗的目的是什么?用醇洗的目的呢? 6、用有机溶剂重结晶的一般步骤有哪些?与用水 重结晶的操作有哪些不同? 7、本实验中可能有哪些副反应,如何采取措施避 免?
H2O OH
C6H5CH =CHCOC6H5
三、主要试剂的物化常数
苯甲醛 苯乙酮 乙醇 10%氢氧化钠
四、装置
合成装置(三颈瓶的中口上装搅拌器, 左口上装滴液漏斗,从右口 加入试剂,不装温度计) 抽滤装置 有机溶剂重结晶的一套装置
五、实验操作步骤
1、安装仪器
在三颈瓶上安装机械搅拌、恒压滴液漏斗,检查搅拌 器能否正常运转
反应机理: (1)α-活泼氢的反应
H
C-C=O + B
碳负离子的形成
-C=C-O-)
H B + -C-C = O (共振式 -C-C=O
(2)有α-活泼氢的醛酮在稀碱催化下,可发生自身缩合反应
R-CH2CH=O
OH H2O
[R-CH-CH=O
R-CH=CH-O ]
H2O OH
R-CH2CH=O + R-CH-CH=O
