第十章 醚和环氧化合物
合集下载
第十章 醚和环氧化合物

9
例如:合成
(CH3)2CH O CH2Ph
X
(CH3)2CHCl + NaO CH2
(CH3)2CHONa + Cl CH2
(CH3)2CHOH Na
(CH3)2CHONa
CH3
Cl2 hν
CH2Cl
(CH3)2CHONa
(CH3)2CH O CH2Ph
10
◆ 芳香醚的合成:
O ONa + CH3OSOCH3 O
R
+
.. O ..
R' + HCl
R
O
+
R' + Cl
pKb≈ 17.5
H
醚还可以与缺电子的Lewis酸形成络合物:
R
.. O .. .. O ..
R' + BF3
R R'
O
R R' O
BF3
X Mg R" O R R'
16
R
R' + R"MgX
2. 醚键的断裂 醚在HI或HBr的作用下,C–O键断裂,生成醇与卤代烷等
第十章 醚和环氧化合物
1
1 结构和命名
通式为R—O—R,两个烃基相同时称为简单醚,不相
同时称为混合醚。
烃基可以是芳香烃基,也可以是脂肪烃基,两个烃基 可以彼此相连形成环醚。 醚和碳原子数目相同的醇互为同分异构体。 CH3OCH3 CH3CH2OH
2
H O H
R O R'
醚
CH3CH2OCH2CH3
R ONa + R' L
用于混醚、环醚、芳香醚的合成
例如:合成
(CH3)2CH O CH2Ph
X
(CH3)2CHCl + NaO CH2
(CH3)2CHONa + Cl CH2
(CH3)2CHOH Na
(CH3)2CHONa
CH3
Cl2 hν
CH2Cl
(CH3)2CHONa
(CH3)2CH O CH2Ph
10
◆ 芳香醚的合成:
O ONa + CH3OSOCH3 O
R
+
.. O ..
R' + HCl
R
O
+
R' + Cl
pKb≈ 17.5
H
醚还可以与缺电子的Lewis酸形成络合物:
R
.. O .. .. O ..
R' + BF3
R R'
O
R R' O
BF3
X Mg R" O R R'
16
R
R' + R"MgX
2. 醚键的断裂 醚在HI或HBr的作用下,C–O键断裂,生成醇与卤代烷等
第十章 醚和环氧化合物
1
1 结构和命名
通式为R—O—R,两个烃基相同时称为简单醚,不相
同时称为混合醚。
烃基可以是芳香烃基,也可以是脂肪烃基,两个烃基 可以彼此相连形成环醚。 醚和碳原子数目相同的醇互为同分异构体。 CH3OCH3 CH3CH2OH
2
H O H
R O R'
醚
CH3CH2OCH2CH3
R ONa + R' L
用于混醚、环醚、芳香醚的合成
第十章 醚和环氧化合物(修改)

O
O
4.命名
普通命名法: 甲醚 ; 甲乙醚; 乙醚; 烯丙基乙炔基醚.
O
O
O
O
系统命名法
1-甲氧基丁烷; 乙氧基乙烯 1,4-环氧丁烷
O
O
O
二.一般制法
(1)一般用于制备对称醚 产率10>20>30 (30易脱水成烯) (2)可用于制备伯烷基叔烷基醚
OH
+
OH
con.H2SO4 O
叔烷基醚还可以这样制备:
1.乙醚 乙醚通常用于从水中萃取有机物的原因: ① 乙醚微溶于水; ② 乙醚能溶解大多数有机物; ③ 沸点低.
环氧乙烷及其它1,2-环氧化物
制备 ① 烯烃氧化
C C
+
RCO3H Ag
C C O
(过过过过过)
CH2 CH2
+
O2
250℃
CH2 O
CH2
(催过过过)
② β-卤代醇与碱作用
C C X OH
+
CH3 C O C CH3
H
+
CH3 CH3 C CH3
H O
+
CH3 C CH3 CH3
(CH3)3COH CH3 CH3 C CH2
CH3 _ H+
CH3 CH3 C O CH3 CH3
H
+
CH3 CH3 C CH3
H O
+
CH3 CH3 CH3 C+
+
CH3OH CH3 CH3 C CH2
CH3 _ H+
OH
+
H2SO4 O
2. Williamson醚合成法 醚合成法 特点:a.可制混合醚; b.不能用20RX、30RX。
第十章-醚和环氧化合物

检查过氧化物的方法:使湿的淀粉/KI试纸变蓝或使FeSO4 /KSCN显红色。 除去过氧化物的方法:用FeSO4洗涤(还原破坏)
四、克莱森(Claisen)重排
烯丙基芳基醚在高温下可以重排为邻烯丙基酚或对烯丙基酚, 称为克莱森重排。
OC* H2CH=CH2 200oC
OH CH2CH=C* H2
若邻位已被占领,烯丙基经两次连续重排迁移到对位。
CH3
OCH2CH=C* H2 CH3
CH3
OH CH3
CH2CH=C* H2
αβγ
O CH2CH=CHCH3
CH3
CH3
重排机理:经历环状过渡态
CH3
OH CH3
CH2CH=CHCH3
α βγ
* O
* O
O
OH
H CH2CH=C*H2 互变异构
CH2CH=C* H2
如何制备?
OH
CHCH2CH3 C6H5 CH3
KOH 160 ~180oC
CH2=CH O C2H5
汞盐催化下醇对炔烃的亲电加成反应
CH3C CH + HOR Hg2+
CH2C=CH2 OR
第四节 醚的化学性质
醚是一类不活泼的化合物,对稀酸、碱、金属钠、催化氢 化、氧化剂、还原剂等都很稳定,与强酸可以发生反应。
一 烊盐的形成 二 醚键的断裂 三 生成过氧化物 四 克莱森重排
OR C
OR
H3O+
C O + ROH
ROH
H3O+
H+
O
O OR
四氢吡喃醚
+ ROH
O OH
常用于保护羟基
4* 含芳基的混合醚,醚键总是优先在脂肪烃基一边断裂。
第十章 醚和环氧化合物

sp3杂化
2. 环氧化合物的结构
10.3 醚和环氧化合物的制法 1. 醚和环氧化合物的工业合成
乙醇Байду номын сангаас硫酸催化下,加热脱水生成乙醚。
乙烯催化氧化得环氧乙烷。
浓 H2SO4
2 CH3CH2OH
CH3CH2OCH2CH3 Ag
H2C CH2
+
1/2 O2
oC 280~300
1~2MPa
H2C CH2 O
R
OH
+
H3C
C
CH2
CH3
用于醇的保护和脱保护
• 烯基醚
R' C R" CH OR R"
H2O/ H+
R' CH CH O + HOR
醛(或酮) 总是在烯基醚键处开裂
醇
3. 环氧化合物的酸性开环——亲核取代反应SN1机理
环氧化合物的碱性开环——SN2机理
O O + NH3 HOCH2CH2NH2 一乙醇胺 O HOCH2CH2NHCH2CH2OH 二乙醇胺 HOCH2CH2 HOCH2CH2 HOCH2CH2 三乙醇胺 N
第十章
醚和环氧化合物
主要学习内容
掌握醚的分类及其命名法。 掌握氢键对沸点、水溶性等物理性质的影响。 理解醚的结构特点。 掌握醚和环氧化合物的化学性质 理解醚和环氧化合物的制备方法
一.醚(Ether)和环氧化合物的分类及命名
分类
O O O O O
O R R'
R
O
R'
(CH2)n O
• 叔烷基醚按SN1 机理
CH3 CH3 CH3 I H O C CH3 CH3 CH3 O H CH3 C CH3 I CH3 I C CH3 CH3 I OH + CH3 C CH3
第十章 醚及环氧化合物.

Boiling Points of Ethers and the Isomeric 1-Alkanols
Ether CH3OCH3 CH3OCH2CH3 (CH3CH2)2O Name Methoxymethane (Dimethyl ether) b.p. (oC) -23.0 1-Alkanol CH3CH2OH CH3CH2CH2OH CH3(CH2)3OH CH3(CH2)7OH b.p. (oC) 78.5 82.4 117.3 194.5
反应的动力:亲核试剂强的亲核性,开环后张力减小 2 碱性开环方向
SN2:从位阻小的方向进攻
31
3 碱性开环的立体化学
SN2:从离去基团的背面进攻
32
Summary
环氧化合物在酸性与碱性条件下都可以开环: (1) 酸性开环,为SN2机理,但具有部分SN1的性质, 不对称的 环氧化合物开环时, 开环反应的比较复杂。 (2) 碱性下开环,同样为SN2机理,但不对称的环氧化合物开 环时,开环方向由空间效应所决定,亲核试剂加在取代 少的环碳上。 (3) 无论酸性或是碱性开环,亲核试剂从氧桥的反面进攻中 心碳原子,符合SN2反应的立体化学特征。
§5 冠醚(Crown ether)
高度稀释
18-Crown-6
23
选择性识别
相转移催化-PTC(Phase Transfer Catalysis)
24
§6 环氧化合物的反应
分子内部存在张力,易开环
一、酸性开环
25
1 酸性开环机理:一般SN2
削弱C-O键
2 酸性开环方向
SN2机理但具有部分SN1的性质
Why?
10
二、Williamson Ether Synthesis
第十章 醚和环氧化合物

NH3 ① CH
CH3 CH CH2NH2 OH + CNa ② H3O CH3 CH CH2C CH OH
OH
冠醚
O O O O O
O O O O O O
O O O O O O
15-冠-5
O O K+ O O
18-冠-6
二环己并-18-冠-6
O O
O Li+ O
O O
冠醚通常用Williamson法制备
-
醚可以溶于浓的强无机酸形成 盐,如浓盐酸、浓硫酸。 用冷水稀释可以得到醚,可用于醚的分离、纯化。 醚可以和lewis酸形成加合物或络合物。 R R
O R
R O R
BF3
R R'MgX R
O R
O R Mg X
BF3
R O R
2、 醚键的断裂:
CH3CH2CH2OCH3 HI
H CH3CH2CH2OCH3
环氧乙烷由于存在较大角张力,性质活泼, 容易与亲核试剂(如H2O、HX、ROH、 NH3、RMgX等)发生亲核取代反应而开环。
① n C6H13MgBr,乙醚 n C6H13CH2CH2OH + ② H 3O CH2 CH2 O H+/H2O or HO /H2O H+/ROH or RO-/ROH
Pederson 1904年生于韩国,1927年在马萨诸塞州工科 大学硕士,1927-1969年杜邦公司研究员。 Cram1919年生于佛蒙特州,1942年Nebraska大 学学士,1947年哈福大学博士。1956年起任加利福尼 亚大学教授。 Lehn 1939年生于法国,于斯特拉斯堡大学获博士学 位,后为该校教授。
环氧化合物 (Epoxides)
有机化学-第十章 醚与环氧化合物-文档资料

Oxonium salt
17
10.5.2 酸催化醚键断裂
例如: (1) 对称醚键的断裂: 两侧醚键断裂均等
18
(2) 甲基伯烷基醚:醚键断裂在甲基一侧
(3) 叔烷基醚:醚键断裂在叔丁基一侧
(4) 芳基醚:醚键断裂在烷基一侧
19
醚键开裂机理
甲基伯烷基醚:SN2机理(主要考虑位阻影响为主)
叔烷基醚:SN1机理(主要考虑碳正离子稳定性)
11
(3) 立体专一性反应——邻基参与作用
12
10.3.3 不饱和烃与醇的反应
该反应是可逆反应,可利用异丁烯与醇反应生成的叔 丁基醚保护醇羟基。
13
10.4 醚的物理性质和波谱性质
IR:
C–O
Байду номын сангаас
1200 ~ 1050cm-1
14
10.4 醚的物理性质和波谱性质
δ 3.4 ~ 4.0
1H
NMR:
20
两类较易水解的醚类化合物
• 叔丁基醚
用于醇的保护和脱保护
• 烯基醚
21
烯基醚的水解机理
22
10.5.3 环氧化合物的开环反应
稀酸介质 HX溶液
23
反应机理
不对称环氧化物的酸性下开环
反应取向:在取代基多的一端开环,具有SN1性质。
立体化学: 反式开环。
酸的醇溶液
碱性条件下的环氧化物开环
2
。
10.1 醚和环氧化合物的分类
单醚:
乙醚 甲基叔丁醚
醚
混醚: 环醚:
四氢呋喃(THF)
1,4-二氧六环
环氧化合物:
环氧乙烷
3
10.1 醚和环氧化合物的命名 1. 单醚: “二”+“烃基 + 醚”
17
10.5.2 酸催化醚键断裂
例如: (1) 对称醚键的断裂: 两侧醚键断裂均等
18
(2) 甲基伯烷基醚:醚键断裂在甲基一侧
(3) 叔烷基醚:醚键断裂在叔丁基一侧
(4) 芳基醚:醚键断裂在烷基一侧
19
醚键开裂机理
甲基伯烷基醚:SN2机理(主要考虑位阻影响为主)
叔烷基醚:SN1机理(主要考虑碳正离子稳定性)
11
(3) 立体专一性反应——邻基参与作用
12
10.3.3 不饱和烃与醇的反应
该反应是可逆反应,可利用异丁烯与醇反应生成的叔 丁基醚保护醇羟基。
13
10.4 醚的物理性质和波谱性质
IR:
C–O
Байду номын сангаас
1200 ~ 1050cm-1
14
10.4 醚的物理性质和波谱性质
δ 3.4 ~ 4.0
1H
NMR:
20
两类较易水解的醚类化合物
• 叔丁基醚
用于醇的保护和脱保护
• 烯基醚
21
烯基醚的水解机理
22
10.5.3 环氧化合物的开环反应
稀酸介质 HX溶液
23
反应机理
不对称环氧化物的酸性下开环
反应取向:在取代基多的一端开环,具有SN1性质。
立体化学: 反式开环。
酸的醇溶液
碱性条件下的环氧化物开环
2
。
10.1 醚和环氧化合物的分类
单醚:
乙醚 甲基叔丁醚
醚
混醚: 环醚:
四氢呋喃(THF)
1,4-二氧六环
环氧化合物:
环氧乙烷
3
10.1 醚和环氧化合物的命名 1. 单醚: “二”+“烃基 + 醚”
第十章醚和环氧化合物

《有机化学》授课教案
第十章
授课内容
授课对象
学时安排
醚和环氧化合物
应用化学专业本科
2学时
教学内容
10-1醚和环氧化合物的命名;
10-2醚和环氧化合物的结构;
10-3醚和环氧化合物的制法;
10-4醚的物理性质;
10-5醚的波谱性质;
10-6醚和环醚的化学性质;
10-7冠醚。
教学重点
醚和环氧化合物的结构;醚的制法;醚的波谱性质;醚和环醚的化学性质。
2.《有机化学》徐寿昌等,高等教育出版社
3.叶孟兆,《有机化学》中国农业出版社2000年5月
备注
教学难点
醚和环氧化合物的结构;醚和环醚的化学性质。
要求
1.了解醚和环氧化合物的命名、醚的物理性质;
2.掌握醚和环氧化合物的结构;
3.掌握醚和环氧化合物的制法;
4.掌握醚的波谱性质;
5.掌握醚和环醚的化学性质;
6.、9。
参考书
1.《基础有机化学》邢其毅等,高等教育出版社
第十章
授课内容
授课对象
学时安排
醚和环氧化合物
应用化学专业本科
2学时
教学内容
10-1醚和环氧化合物的命名;
10-2醚和环氧化合物的结构;
10-3醚和环氧化合物的制法;
10-4醚的物理性质;
10-5醚的波谱性质;
10-6醚和环醚的化学性质;
10-7冠醚。
教学重点
醚和环氧化合物的结构;醚的制法;醚的波谱性质;醚和环醚的化学性质。
2.《有机化学》徐寿昌等,高等教育出版社
3.叶孟兆,《有机化学》中国农业出版社2000年5月
备注
教学难点
醚和环氧化合物的结构;醚和环醚的化学性质。
要求
1.了解醚和环氧化合物的命名、醚的物理性质;
2.掌握醚和环氧化合物的结构;
3.掌握醚和环氧化合物的制法;
4.掌握醚的波谱性质;
5.掌握醚和环醚的化学性质;
6.、9。
参考书
1.《基础有机化学》邢其毅等,高等教育出版社
大学有机化学醚和环氧化合物PPT课件

大学有机化学醚和环氧化 合物ppt课件
• 有机化学醚的介绍 • 环氧化合物的介绍 • 醚和环氧化合物的比较 • 有机化学醚和环氧化合物的实际应用 • 有机化学醚和环氧化合物的未来发展
01
有机化学醚的介绍
醚的定义和结构
醚的定义
醚是一类由醇或酚与卤素或硫酸反 应生成的化合物,其结构通式为RO-R',其中R和R'为烃基。
醚和环氧化合物的应用比较
醚的应用
醚在工业上主要用于溶剂、麻醉剂、农药等。
环氧化合物的应用
环氧化合物主要用于合成树脂、聚合物、涂料等高分子材料。
应用比较
醚和环氧化合物的应用领域不同,醚主要用于化学试剂、农药等; 而环氧化合物主要用于高分子材料合成。
04
有机化学醚和环氧化合物的实际应用
醚在医药领域的应用
THANKS
感谢观看
一些醚类化合物具有杀虫、杀 菌或除草活性,可以直接用作 农药,如杀螨醚、苯氧威等。
醚类化合物还可以作为农药的 增效剂,与其他农药混合使用, 以提高防治效果并减少农药的 使用量。
环氧化合物在材料科学领域的应用
环氧化合物可以通过聚合反应制备高 分子材料,如环氧树脂、环氧橡胶等, 这些材料具有优异的力学性能、电绝 缘性能和耐腐蚀性能。
醚和环氧化合物的性质比较
醚的性质
醚是较为稳定的化合物,对酸、 碱都有较好的稳定性。醚的沸点 较低,容易挥发。
环氧化合物的性质
环氧化合物对酸、碱都敏感,容 易发生开环反应。环氧化合物的 沸点较高,不易挥发。
性质比较
醚和环氧化合物的性质差异较大, 醚较为稳定,沸点低;而环氧化 合物对酸、碱敏感,沸点较高。
详细描述
环氧化合物具有多种化学性质,包括亲核性、亲电性、开环反应等。在一定条件下,环氧化合物可以 与多种试剂发生反应,如醇、酚、胺等。其中,开环反应是环氧化合物最重要的反应类型之一,可以 通过与氢离子、金属离子等反应打开环氧环。
• 有机化学醚的介绍 • 环氧化合物的介绍 • 醚和环氧化合物的比较 • 有机化学醚和环氧化合物的实际应用 • 有机化学醚和环氧化合物的未来发展
01
有机化学醚的介绍
醚的定义和结构
醚的定义
醚是一类由醇或酚与卤素或硫酸反 应生成的化合物,其结构通式为RO-R',其中R和R'为烃基。
醚和环氧化合物的应用比较
醚的应用
醚在工业上主要用于溶剂、麻醉剂、农药等。
环氧化合物的应用
环氧化合物主要用于合成树脂、聚合物、涂料等高分子材料。
应用比较
醚和环氧化合物的应用领域不同,醚主要用于化学试剂、农药等; 而环氧化合物主要用于高分子材料合成。
04
有机化学醚和环氧化合物的实际应用
醚在医药领域的应用
THANKS
感谢观看
一些醚类化合物具有杀虫、杀 菌或除草活性,可以直接用作 农药,如杀螨醚、苯氧威等。
醚类化合物还可以作为农药的 增效剂,与其他农药混合使用, 以提高防治效果并减少农药的 使用量。
环氧化合物在材料科学领域的应用
环氧化合物可以通过聚合反应制备高 分子材料,如环氧树脂、环氧橡胶等, 这些材料具有优异的力学性能、电绝 缘性能和耐腐蚀性能。
醚和环氧化合物的性质比较
醚的性质
醚是较为稳定的化合物,对酸、 碱都有较好的稳定性。醚的沸点 较低,容易挥发。
环氧化合物的性质
环氧化合物对酸、碱都敏感,容 易发生开环反应。环氧化合物的 沸点较高,不易挥发。
性质比较
醚和环氧化合物的性质差异较大, 醚较为稳定,沸点低;而环氧化 合物对酸、碱敏感,沸点较高。
详细描述
环氧化合物具有多种化学性质,包括亲核性、亲电性、开环反应等。在一定条件下,环氧化合物可以 与多种试剂发生反应,如醇、酚、胺等。其中,开环反应是环氧化合物最重要的反应类型之一,可以 通过与氢离子、金属离子等反应打开环氧环。
《醚和环氧》课件

威廉姆逊合成法
醇盐与卤代烃在碱的作用下发 生取代反应,生成醚。
酚烷基化
酚与卤代烃在酸性条件下发生 烷基化反应,生成醚。
烯烃与卤代烃反应
烯烃与卤代烃在酸性条件下发 生取代反应,生成醚。
醚的反应类型
醚的裂解
醚在酸性条件下发生裂 解,生成醇或烷烃。
醚的氧化
醚在氧化剂的作用下发 生氧化,生成过氧化物
。
醚的烷基化
环氧的还原
环氧可以通过还原剂如氢气、金属催化剂等还原成醇或烃,其还原产物取决于还原剂和反应条件。
醚和环氧的加成反应比较
醚的加成
醚在加成反应中通常作为溶剂或反应介质,其本身不参与加成反应。
环氧的加成
环氧可以与水、醇、氨等发生加成反应,生成相应的加成产物。
06
醚和环氧的实际应用
醚在工业生产中的应用
醚和环氧在其他领域的应用
醚在化学反应中的应用
醚类化合物可以作为反应溶剂和反应物参与 各种化学反应,如烷基化、酰基化、酯化等 。醚类化合物在有机合成中具有重要的地位 ,为化学工业提供丰富的化合物原料。
环氧在建筑领域的应用
环氧树脂在建筑领域中主要用于地坪涂装、 混凝土加固和粘接材料等方面。其优良的耐 久性和装饰性能使环氧树脂成为现代建筑中 不可或缺的材料之一。
THANKS
感谢观看
醚在酸性条件下发生烷 基化反应,生成新的醚
。
醚的水解
醚在碱性条件下发生水 解,生成醇。
醚在有机合成中的应用
01
02
03
作为溶剂
醚类化合物常用作有机合 成中的溶剂,如乙醚、四 氢呋喃等。
作为反应介质
醚类化合物可以作为有机 合成中的反应介质,如醇 与卤代烃的取代反应、酚 烷基化等。
有机化学(高鸿宾第四版)第十章醚和环氧化合物

AgI 沉淀
根据生成碘化银的量,计算出甲氧基含量。此反 应用于天然的复杂有机化合物分子中甲氧基的测定。
当混醚中的一个烃基是芳基时,由于p、π-共轭效应的影响, 芳环与氧原子相连的键比较牢固,与氢碘酸反应时,发生烷氧 键(R-O)断裂,生成碘代烷和酚。
O C H 25H + I S N 2
O H C + H C 3 H 2 I
C H 3 O C H 3
甲醚
O
二苯醚
H 2 C H C O C H C H 2
二乙烯基醚
(2) 混醚:“烃基”+“烃基”+ “醚”,较
优基团
置后,但芳基置前:
C H 3O C 2H 5
O C H 3
甲乙醚
苯甲醚
methyl ethyl ether (茴香醚)
(3)对于结构复杂的醚: 较大的烃基作为母体,烃氧基作为取代基 。
① 乙 醚
M g B r+H 2 C O C HC H 3② H 3 O +
C H 2 C HC H 3 O H
(60%)
例:
C H 2 = C H 2 C H 3 C H 2 C H 2 C H 2 O H
CH3CH2-MgCl +
O
-Mg(OH)Cl H2O
C H 3 C H 2 C H 2 C H 2 O M g C l
但可以和水分子形成氢键, 小分子醚有一定水溶性。
易燃易爆 使用小分子醚时,应避免明火。
乙醚,它遇到火星就有发生燃烧爆炸的危险。其蒸气能 从远处将明火引来起火。
醚长期放置受热或碰撞可发生爆炸。
三、醚的化学性质
{稳定,不和除酸之外的试剂反应。
在空气中会慢慢氧化成过氧化物。
根据生成碘化银的量,计算出甲氧基含量。此反 应用于天然的复杂有机化合物分子中甲氧基的测定。
当混醚中的一个烃基是芳基时,由于p、π-共轭效应的影响, 芳环与氧原子相连的键比较牢固,与氢碘酸反应时,发生烷氧 键(R-O)断裂,生成碘代烷和酚。
O C H 25H + I S N 2
O H C + H C 3 H 2 I
C H 3 O C H 3
甲醚
O
二苯醚
H 2 C H C O C H C H 2
二乙烯基醚
(2) 混醚:“烃基”+“烃基”+ “醚”,较
优基团
置后,但芳基置前:
C H 3O C 2H 5
O C H 3
甲乙醚
苯甲醚
methyl ethyl ether (茴香醚)
(3)对于结构复杂的醚: 较大的烃基作为母体,烃氧基作为取代基 。
① 乙 醚
M g B r+H 2 C O C HC H 3② H 3 O +
C H 2 C HC H 3 O H
(60%)
例:
C H 2 = C H 2 C H 3 C H 2 C H 2 C H 2 O H
CH3CH2-MgCl +
O
-Mg(OH)Cl H2O
C H 3 C H 2 C H 2 C H 2 O M g C l
但可以和水分子形成氢键, 小分子醚有一定水溶性。
易燃易爆 使用小分子醚时,应避免明火。
乙醚,它遇到火星就有发生燃烧爆炸的危险。其蒸气能 从远处将明火引来起火。
醚长期放置受热或碰撞可发生爆炸。
三、醚的化学性质
{稳定,不和除酸之外的试剂反应。
在空气中会慢慢氧化成过氧化物。
10-醚和环氧化合物
O C H 3 + N aC I
C I + C H 3O N a
不反应
制备含苯基的醚时须采用酚钠,否则反应很难发生 (2) 合成环醚
OH (C H 2 ) n CH2 X OH H 2O O (C H 2 ) n X CH2 X (C H 2 ) n + 1 O
k3 > k5 > k6 > k4 > k7 > k8 (kn 为速率常数,n 为生成环醚环的节点数)
D 2O
D C H 2C H 2C H 2O
C CH3
D C H 2C H 2C H 2O H + C H 3
C
CH2
四、醚的物理性质
醚分子极性小,分子间作用力小,沸点低。但醚可与水形成氢键,故醚 微溶于水。
五、醚的波谱性质
IR: C-O 伸缩振动吸收峰在 1200-1050 cm-1
1H
NMR:
CH 3 X + (CH 3 ) 3 CONa
CH3 H 3C C X C H 3 + C H 3O N a
(CH 3 ) 3 C O
CH3 H 3C C
CH 3
C H 2 + N aX + C H 3 O H
制备有叔烃基的混醚时,应采用叔醇钠与伯卤烷作用,否则得不到醚
O N a + C H 3C I
CH
O
质子化学位移在 3.4 - 4.0 ppm
六、醚和环醚的化学性质
1. 佯盐的生成
R O R + HCl R + O H 佯盐
R + Cl
生成的佯盐可溶于浓强酸中,用冷水稀释则重新析出醚层。利用这一性 质可分离提纯醚
第十章 醚及环氧化合物

-CH3COOH
(CH3)3CCHCH2HgOOCCH3 OC2H5
NaBH4 OH-
(CH3)3CCHCH3 + Hg + -OOCCH3 OC2H5
反应遵循马氏规则:氢加在含氢较多的碳上,烷氧 基加在含氢较少的碳上。 优点:反应快,操作方便,产率高,一般不发生重排和消除。 如果用叔醇和烯烃制备相应的醚,由于空间位阻, 用Hg(OOCCF3)2来代替Hg(OOCCH3)2,效果较好。
α O H3C
α β γ H C 3 CH3 β O γ CH3 H3C O CH3 γ β α
OH H3C CH3 H3C H
O CH3 β α γ
α
β γ
在有机合成上可用于制备邻位带有某些烃基的酚类化合物。
脂肪乙烯基烯丙醚的重排:
1O 2 HC CH2 3 CH2 1 CH 2 CH2 3 O1 HC 2 CH2 3 1 CH2 2 CH CH2 3
-Cl-
O
二、 醇分子间失水---制备简单醚
CH3CH2OH
H+
CH3CH2OH + CH3CH2—OH2
+
+
-H2O
SN2
-H+
CH3CH2OCH2CH3 H
CH3CH2OCH2CH
3
醇在浓H2SO4作用下可以制得对称的醚。 1oROH制醚产率好。
三、 烯烃的烷氧汞化-脱汞法
(CH3)3CCH=CH2 + Hg(OOCCH3)2 + C2H5OH
(CH3)3C
+ O CH3 + H
(CH3)3C
O CH3 H
SN1
(CH3)3C+ + CH3OH I(CH3)3CI
10 第十章_醚和环氧化合物

醚的分类
醚 (Ether)
单醚:
乙醚
环醚:
四氢呋喃(THF)
水
醇
混醚:
叔丁基甲基醚
环氧化合物:
环氧乙烷
1,4-二氧六环
10.1 醚和环氧化合物的命名
单醚: “二”+“烃基” + “醚” “二”字和“基”字有时可省略,但不饱和醚习 惯上保留“二”字。
(二)乙(基)醚 乙醚
diethyl ether
1,2–二甲氧基乙烷 (乙二醇二甲醚)
1,2-dimethoxyethane
环醚的命名
环醚: 按杂环化合物命名为“氧杂环某烷”, 三元环醚习惯称为“环氧某烷”。
环氧乙烷 (氧杂环丙烷)
1,2-epoxyethane (oxirane)
2–(氯甲基)氧杂环丙烷 (环氧氯丙烷)
2-(chloromethyl)oxirane (1,2-epoxy-3-chloropropane)
有机化学 Organic Chemistry
第十章 醚和环氧 化合物
第十章 醚和环氧化合物
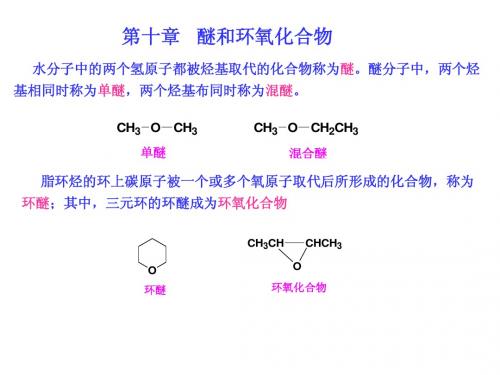
水分子中的两个氢原子都被烃基取代的化合物称为醚 。脂环烃的环上碳原子被一个或多个氧原子取代后所形 成的化合物,称为环醚;其中三元环醚称为环氧化合物 。
醚和环氧化合物的分类、命名、制法 醚和环氧化合物的物理性质和波谱性质 醚键的断裂 环氧化合物的开环反应 环氧化合物与 Grignard 试剂的反应 Claisen 重排 冠醚
醚键开裂机理:
SN2机理
位阻影响
SN1机理
中间体稳定性
10.5.3 环氧化合物的开环反应
环氧乙烷酸性条件下开环:
不对称环氧化合物酸性条件下开环
反应取向: 亲核试剂优先进攻取代较多的碳原子, 类SN1。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
醚也可以和lewis酸形成络合物:
BF3 R O R' + AlCl3 Mg
lewis 碱
R O R' R O R' R O R'
BF3 AlCl3 Mg R" X
R" X
lewis 酸
10.6.2 酸催化碳氧键断裂
醚与HBr、HI作用,可使醚链断裂:
CH3OCH2CH3 + HI
CH3I + CH3CH2OH (定量进行)
第十章
醚和环氧化合物
水分子中的两个H被烃基R取代形成的化合物叫做醚。
醚键(C-O-C)
C2H5OC2H5
CH3OC2H5 CH2 CH2 O
O CH3
单醚
混醚
环醚
芳醚
10.1
醚和环氧化合物的命名
① 习惯命名法:(常用,适用于简单醚)
¥ ´ Ñ º µ ¿ Ã £ CH3CH2OCH2CH3 (¶ )Ò Ã þ Ò Ñ
(CF3COO)2Hg (CH3)3COH
OC(CH3)3 HgOOCCF3
NaBH4 OH -
OC(CH3)3
(CH3)3C CH=CH2
(1) Hg(OAc)2,CH3OH (2) NaBH4,OH -
(CH3)3C CH CH3 OCH3
P368习题10.2
10.4
① ②
醚的物理性质
相对密度、沸点较低,因为醚分子间不能形成氢键。 水中溶解度与同碳数醇差不多,因醚分子与水分子可形成分子间 氢键:
10.6.4 环氧乙烷与Grignard试剂的反应
环氧乙烷与格氏试剂反应,得到多两个碳的伯醇:
O
+ R-MgX
ÅÅ
RCH2CH2OMgX
纯醚 H2O H+
H2O/H+
RCH2CH2OH
à ö Ä ® ¼ ¶ 2· Cµ ² ´
例如:CH =CHCH MgBr + 2 2
O
CH2=CHCH2 CH2CH2 OH
乙醚是重要的有机溶剂,在工业上,可用醇脱水的方法制取:
2CH3CH2OH
浓H2SO4
CH3CH2
O CH2CH3
环氧乙烷是重要的有机化工原料,是制备非离子表面活性剂的重要 原料。工业上,可由乙烯催化氧化制取环氧乙烷:
Ag 1 CH2=CH2 + O2 o 2 300 C , 1~2Mpa
CH2 O
3-氯-1,2-环氧丙烷 (简称为环氧氯丙烷)
O O 1,4-环氧丁烷 (或四氢呋喃)
1,4-二氧六环 (或二 口 烷) 恶
P368习题10.1
10.2
醚和环氧化合物的结构
10.2.1 醚的结构 饱和醚分子中的氧原子采取不等性sp3杂化,醚键键角接近于109.5°
不等性sp3杂化 O CH3
o
0.142nm
CH2OH OH CH3
(1) NaH/CH2Cl2 (2) TsCl/CH2Cl2
CH2 O-
OTs O
- OTs-
CH3
90%
环保型新反应:
绿色 化学
O OCH3 + CH OH + CO 3 2 碳酸二甲酯 可循环使用 O 无毒, 可代替有毒的硫酸二甲酯( CH3O S OCH3 传统的甲基化试剂) O
AgNO 3
AgI
根据AgI的重量可推算出原来分 子中 -OCH 3 的含量。(Zeisel法)
伯烷基醚与HI作用时,按SN2机理进行:
HI SN2
CH3CH2CH2I
CH3CH2CH2
O CH3
小
H+
I-
CH3CH2CH2
O CH3 S 2 N H
CH3CH2CH2OH + CH3I
小O
O
OH
六元环状过渡态
(H) R O-CH-CH=CH 2
a b c
OH
例:
CH 2-CH=CH-R c b a (H)
c b a
O-CH 2-CH=CH 2 R-C=CH-R'
a
b
c
O CH2-CH=CH 2 R-C-CH-R'
10.6.1
盐的生成
R O + ÅHCl(ÅÅH 2SO4Å ¨ ò ¨ R'
î ¼ á Ë
R + O H ClR' (HSO4-)
Å Ñ ò ÅÎ
盐必须在浓HCl、浓硫酸作用下才能生成,因为 盐在浓酸下才能稳定 存在,一遇水即水解!利用此性质可分离提纯醚。 例:用简单的化学方法除去正溴丁烷中少量的正丁醇、正丁醚、1-丁烯? 答案:用浓硫酸洗。
OH + CH O C OCH 3 3
(2) 合成环醚 — 分子内的Williamson合成反应
OH (CH2)n CH2 X
OH-
O(CH2)n CH2 X
- X-
(CH2)n+1 O
• 为避免分子间的Williamson反应,可采用溶剂,在稀释条件下合成环醚。
• 环的大小与反应速率的关系: k3 ≥ k5 ≥ k6≥ k4 ≥ k7≥ k8 (k为速率常数,n为生成环醚环的节点数) • Why?熵变和环张力共同作用的结果。 n太大,不利于氧负离子进攻卤原子的α–C,不利于环醚的生成; n太小,产物环张力大,不稳定,也不利于环醚的生成
C ONa CH3
O Na
+ Br CH2CH3
OCH2CH3
注意:不能用叔卤烷做原料!
叔卤烷在碱性条件下易消除:
CH3 CH3-C-Br + CH3CH2ONa CH3
CH3 CH3C=CH2 + CH3CH2OH + NaBr
使用磺酸酯、硫酸酯、碳酸酯等代替卤代烷进行Williamson合成 反应,也可得到相应的醚(相当于把离去基团由Cl-换成OTs-等):
H2SO 4
CH 3 BrCH 2CH 2CH 2O-C-CH 3 CH 3
Mg 干醚
D 2O
H2SO 4
CH 3 DCH 2CH 2CH 2OH + CH 3-C=CH 2
环氧化合物在酸催化下可开环加成,生成2-取代乙醇:
H 2O CH2 CH2 + C2H5OH O HBr
H+
CH2 OH
D2O H2SO4
CH3 BrCH2CH2CH2O C CH3 CH3
Mg 纯醚
DCH2CH2CH2O C CH3 CH3
H2SO4
CH3 DCH2CH2CH2OH + CH3 C CH2
(2) 乙烯基醚的合成
由于乙烯醇不存在,不能采用Williamson合成法制备乙烯醚, 而是利用乙炔的亲核加成来制备乙烯醚:
CH3- CH O
CH2
Nu
CH3
CH O-
Nu CH2
(似S N2)
C 空间障碍:1 < C2 ,
例如:
Nu更容易从背面进攻C1
H3C
C CH CH3 CH ONa,CH OH H3C C 3 3 H3C O O
CH3O-
CH3 CHCH3 OCH3
CH3OH
CH3 H 3C C CHCH3 OH OCH3
(HOCH2CH2)3N
三乙醇胺
例2:
CH2 CH2 + HO O
R
烷基酚
OH
-
OH CH2CH2O
乙二醇烷基酚醚
R
O
OH -
HOCH2CH2OCH2CH2O
二乙二醇烷基酚醚
R
n-1 O
OH -
HO(CH2CH2O)n CH2CH2O
聚乙二醇烷基酚醚 乳化剂-OP
R
反应是按照SN2机理进行的,在取代基较少的碳原子上引入新的取代基:
不对称环氧化合物与格氏试剂反应时,易按SN2机理进行,
在取代基较少的碳原子上引入新的取代基:
MgBr +
CH3 纯醚 O
H2O H+
CH2CHCH3 OH
10.6.5
Claisen重排
苯基烯丙基醚及其类似物在加热时,经六元环状过渡态生成C-烯丙 基酚或酮的重排反应,称为Claisen重排。
混合醚: CH3OCH2CH3 甲乙醚 (CH3)3COCH3 甲叔丁醚 OCH3 苯甲醚
(芳基命在前面)
O (¶ )±Ã þ ½ Ñ
(小的R命在前面)
②
系统命名法:(不常用,适用于复杂醚) 将RO-或ArO-当作取代基,以烃为母体:
CH3CH2CH2CHCH2CH3 OCH3 3-甲氧基己烷
CH3OCH CHCH2CH3
20% KOH水溶液 , P NaOH 160~180 C
o
CH CH + CH3OH
CH2=CH OCH3
CH CH + C2H5OH
CH2=CH OC2H5
(3) 烯烃的溶剂汞化-脱汞法 与烯烃经羟汞化-脱汞反应制醇相似。烯烃与三氟乙酸汞 (或乙酸汞)在醇的存在下反应,首先生成烷氧基有机汞,然 后用硼氢化钠还原,脱汞生成醚。
CH3 CH3 CH3CH C
CH3
-H+
OH HOCH3
10.6.3 碱催化碳氧键断裂
一般情况下,醚对碱稳定。但环氧化合物却在碱性条件下发生开环加成。
例1:
CH2 CH2 + NH3 O O
OH -
OH -
HOCH2CH2NH2
乙醇胺
