有机化学-第十六章 糖类
单糖和多糖-糖类

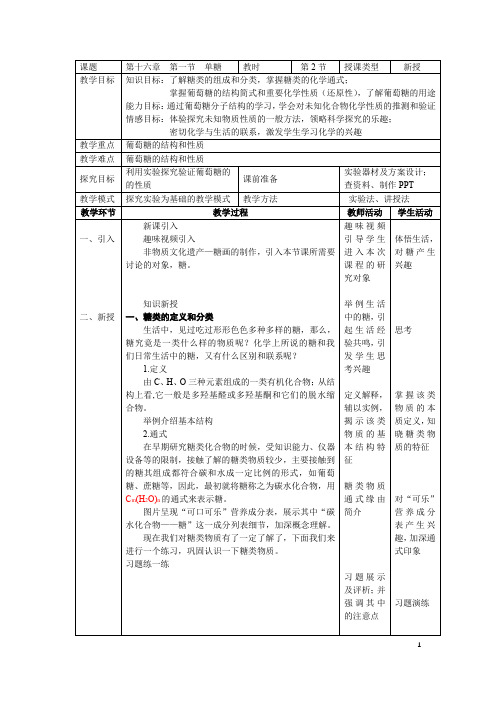
生成同一种糖脎。
果糖脎
葡萄糖脎
有机化学(第9版)
四、化学性质
(四)差向异构化反应
有机化学(第9版)
四、化学性质
(五)氧化反应
1. 与碱性弱氧化剂反应
碱性弱氧化剂:Tollens试剂, Fehling试剂, Benedict试剂。单糖被氧化成
糖酸,并生成银镜或Cu2O沉淀(砖红色)。
有机化学(第9版)
α -D-甲基葡萄糖苷
有机化学(第9版)
四、化学性质
(三)成脎反应
单糖与过量的苯肼一起加热作用,生成难溶于水的黄色结晶物质,叫做糖脎。
葡萄糖腙
有机化学(第9版)
四、化学性质
(三)成脎反应
葡萄糖脎
有机化学(第9版)
四、化学性质
(三)成脎反应
两种糖的成脎反应均发生在C1、C2两原子上,且成脎后两种糖的差别消失,
第十六章
糖 类
第一节 单糖
第二节 双糖和多糖
重点难点 掌握 单糖的定义、分类、结构、构型和开链结构、变旋 光现象和环状结构;单糖的化学性质。
熟悉
常见双糖的结构与性质;常见多糖的结构与特性。
了解
糖类化合物的来源及重要的生物功能。
第一节
单 糖
有机化学(第9版)
糖类(saccharide)又称碳水化合物(carbohydrate)。早期发现糖类组成符
有机化学(第9版)
二、变旋光现象和环状结构
Haworth式
D-葡萄糖发生变旋光现象的内在原因是两种端基异构体与开链结构之间处于
动态平衡。
有机化学(第9版)
三、物理性质
某些单糖的物理常数 糖 熔点(℃) 87 90 比旋光度 -23.7º -59º
生物化学糖类化学

核酮糖
木酮糖
阿洛酮糖
2021/8/11
山梨糖
塔格糖
10
第一节
概述
二. 糖 的 分 类
糖类物质是一大类物质的总称,它分为单糖、寡 糖、多糖和结合糖、衍生糖五类
根据能否水解和水解后的产物将糖类分为: 糖类
单糖
寡糖
多糖
2021/8/11
11
糖类化合物
单糖 :不能水解的最简单糖类,是多羟基的 醛或酮的衍生物(醛糖或酮糖)
2021/8/11
34
(二).分类
醛糖 按功能基分:
酮糖
2021/8/11
丙糖
按碳原子数分:
丁糖 戊糖
己糖
…… ……
35
第二节 单糖
一
(二).分类
.
定
最简单的单糖
义
(含三个碳原子)
和
O
分
C-H H-C-OH
类
CH2OH
CH2OH C=O CH2OH
甘油醛(醛糖)
二羟丙酮(酮糖)
2021/8/11
性
和 开
甘油醛异构体的比旋光度数值相等,但方向相反,
分别记为左旋 l( - ) 、与右旋 d ( + )
链 外消旋体:等量的对映(差向、旋光)异构体混合
结 时,则旋光性相互抵消,无旋光性的混合体。记为d
构
l(±)2021/8/11
41
第二节 单糖
二 (一).旋光性
.
单 糖 注意!
的
旋
旋光物的构型D或L与实际旋光性d
链
结 (4).旋光异构体的性质:化学性质和大部分物理性质相同,
构
只对偏202振1/8/光11 影响不同。
有机化学《单糖》教案
基于选项C提示注意点:注意:1、有些糖不符合通式,如:鼠李糖(C6H12O5);2、有些符合通式的却不属于糖类,例如:甲醛(CH2O)、乙酸(C2H4O2)基于选项D,那该类物质如何分类呢?3.分类下面我们进入本次课的重点,认识并学习一下最简单的糖。
二、单糖(一)重要的单糖自然界分布最广的单糖:葡萄糖和果糖,存在来源简介;●物理性质(样品呈现,认识葡萄糖)观察样品,归纳葡萄糖物理性质,呈现糖类相对甜度表,了解单糖的甜度。
●分子结构分子式:C6H12O6结构简式:(葡萄糖结构简式略)乙醛糖(果糖结构简式略)己酮糖两种单糖,葡萄糖的性质更为丰富和重要,因此本节单糖我们以葡萄糖的学习为主,那葡萄糖的结构中都有哪些基团呢?可能的性质有哪些呢?(二)葡萄糖的化学性质1.氧化反应有机物多数可以燃烧,葡萄糖也是可以的,完全燃烧可转化为CO2和H2O,化学方程式展示。
C6H12O6 + 6O2→6CO2 + 6H2O葡萄糖注意:书写化学方程式时,若以分子式表示糖类物质,需在糖分子下标注糖的名称,以免混淆。
生命体内,1mol葡萄糖约可以释放出2804kJ的能量2.与碱性弱氧化剂的反应(1)与银氨溶液反应呈现实验步骤,提问过程中银氨溶液配制时的现象变化。
观察实验现象,记录反应方程式CH2OH(CHOH)4CHO+2Ag(NH3)2OH→CH2OH(CHOH)4COONH4+2Ag↓+3NH3 +H2O(2)与新制Cu(OH)2反应呈现实验步骤,观察实验现象CH2OH(CHOH)4CHO+2Cu(OH)2+ NaOH→CH2OH(CHOH)4COONa + Cu2O↓ + 3H2O还原糖定义:可以被碱性弱氧化剂氧化的糖。
注意:果糖虽然是酮糖,但也可以被碱性弱氧化剂氧化,也是还原糖。
上述均是发生的氧化反应,那和氧化相对应的是什么反应呢?葡萄糖可以被还原吗?3.加成反应葡萄糖分子在一定条件下,可以被还原为己六醇。
那么果糖可以被还原吗?习题练一练练习2对应的是醛基的性质,练习3对应的是羟基和羧基的性质,因为葡萄糖结构中存在羟基,同样可以发生酯化反应。
有机化学基础知识点糖类与多糖的命名与性质

有机化学基础知识点糖类与多糖的命名与性质糖类与多糖是有机化学中重要的基础知识点,它们在生物学、化学工程等领域具有广泛的应用。
本文将针对糖类与多糖的命名与性质进行探讨。
一、糖类的命名与性质1. 单一糖类的命名与性质单糖是由单个糖分子组成的简单糖类化合物,常见的单糖有葡萄糖、果糖和半乳糖等。
单糖的命名主要通过其分子结构确定,如葡萄糖的分子式为C6H12O6。
在命名单糖时,需要根据糖醇为主链的形式,指定它们的立体构型。
单糖的性质表现出溶解性强、呈甜味、具有旋光性等特点。
此外,不同单糖的甜度和旋光性也存在一定差异,这与它们的分子结构和立体构型有关。
2. 糖苷与糖醛的命名与性质糖苷是由糖分子与非糖分子(如苷、甾类等)通过醚键连接而成的化合物。
糖苷的命名方式为:首先指定非糖部分的名称,其次通过连接符号将糖部分的名称写在后面,如乙酰葡萄糖。
糖醛是以羟基代替甲基的糖类衍生物。
其命名方式为:首先指定糖醛的名称,然后加上醛前缀,如葡萄庚糖醛。
糖苷和糖醛在生物体内具有重要的生理功能和药理作用。
3. 糖醇的命名与性质糖醇是糖类中去除一个或多个氧原子后形成的醇类化合物,也称为糖醇或醇糖。
常见的糖醇有山梨醇、甘露醇等。
糖醇的命名方式为:以相应糖类的名称为前缀,后缀加上醇,如葡萄糖醇。
糖醇具有甜味、溶解性好、相对稳定等性质。
它们在医药、食品工业等领域中广泛应用,如山梨醇被用作低热值甜味剂。
二、多糖的命名与性质1. 多糖的命名与结构多糖是由多个糖分子通过糖苷键连接而成的大分子化合物,包括两种主要类型:寡糖和多糖。
寡糖由2-10个糖分子组成,而多糖由数十到数百个糖分子组成。
多糖的命名方式主要是通过糖分子的种类、数量以及它们之间的连接方式进行描述。
例如,淀粉是由α-D葡萄糖分子通过α-1,4-糖苷键和α-1,6-糖苷键连接而成的多糖。
2. 多糖的性质多糖具有高分子量、溶解性较差、具有胶凝能力等特点。
它们在生物体内发挥着结构支持、能量储存和信息传递等重要作用。
有机化学糖类ppt课件

糖类化合物的降解过程及关键酶
单糖降解
单糖在细胞内通过糖酵解途径降解为丙酮酸,进而生成ATP和还原力(NADH)。此过 程中的关键酶包括己糖激酶、磷酸果糖激酶和丙酮酸激酶。
双糖和多糖降解
双糖和多糖在相应酶的催化下分解为单糖,如蔗糖酶、淀粉酶和纤维素酶等。随后,单 糖按照糖酵解途径进行降解。多糖的降解对于生物体获取能量和维持血糖水平具有重要
单糖、双糖与多糖分类
01
02
03
单糖
不能水解的最简单的糖, 如葡萄糖(醛糖)、果糖 (酮糖)。
双糖
由两个单糖分子脱水缩合 而成,如蔗糖、麦芽糖。
多糖
由多个单糖分子脱水缩合 而成的高分子化合物,如 淀粉、纤维素。
还原性糖与非还原性糖
还原性糖
分子中含有游离醛基或酮基的单糖和含有游离醛基的二糖都具有还原性,如葡萄糖、果糖、麦芽糖等 。
有机化学糖类ppt课件
• 糖类概述与分类 • 单糖结构与性质 • 双糖结构与性质 • 多糖结构与性质 • 糖类化合物的合成与降解 • 糖类在生物体内的代谢与调控
01
糖类概述与分类
糖类的定义及重要性
糖类的定义
糖类是多羟基醛、多羟基酮以及能水解而生成多羟基醛或多羟基酮的有机化合物 。
糖类的重要性
糖类是自然界中广泛分布的一类重要的有机化合物。日常食用的蔗糖、粮食中的 淀粉、植物体中的纤维素、人体血液中的葡萄糖等均属糖类。糖类在生命活动过 程中起着重要的作用,是一切生命体维持生命活动所需能量的主要来源。
生物识别
多糖在生物体内还具有重要的识别功能。例如,细胞膜表 面的糖蛋白和糖脂中的多糖部分可参与细胞间的识别和信 号传导过程。此外,多糖还可作为病原体相关分子模式( PAMPs)被免疫系统识别,从而引发免疫反应。
糖类化学知识点总结

糖类化学知识点总结糖类是一类重要的有机化合物,其化学结构和性质的研究对于生物学和食品工业具有重要的意义。
糖类包括单糖、双糖、多糖等多种类型,它们具有不同的分子结构和特性。
本文将对糖类的化学结构、命名方法、性质以及在生物体内和食品工业中的应用进行系统的总结和阐述。
一、单糖的化学结构和命名方法1. 单糖的分类单糖是由碳、氢、氧三种元素组成的糖类化合物,它们的分子结构中含有一个或多个羟基和一个或多个醛基或酮基。
根据它们的化学结构,单糖可分为醛糖和酮糖两类。
醛糖的分子中含有一个醛基,酮糖的分子中含有一个酮基。
2. 单糖的化学结构单糖的化学结构可以用希尔德-奥斯特公式来表示,其中n代表碳原子数,希尔德-奥斯特公式的结构为(CH2O)n。
单糖的分子结构包括直链结构和环状结构两种形式。
直链结构是单糖分子直接相连形成的链状结构,而环状结构是由直链结构转变而来的,其中含有环氧醇化合物。
3. 单糖的命名方法根据单糖分子中羟基的位置不同,可以分为各种不同的单糖,比如葡萄糖、果糖、半乳糖等,并且还可以根据立体构型的不同将它们分为L-型和D-型两种立体异构体。
二、双糖和多糖的化学结构和性质1. 双糖的化学结构和性质双糖是由两个单糖分子通过糖苷键连接而成的化合物,根据单糖分子的组成不同,双糖可分为蔗糖、麦芽糖、乳糖等多种类型。
双糖具有不同的甜度和溶解度,它们在食品工业中具有广泛的应用。
2. 多糖的化学结构和性质多糖是由多个单糖分子通过糖苷键连接而成的化合物,它们的分子结构复杂,包括淀粉、纤维素、半乳聚糖等多种类型。
多糖在生物体内具有重要的功能,如淀粉是植物体内储存能量的重要物质,而纤维素是植物细胞壁结构的主要组成部分。
三、糖的生物合成和降解1. 糖的生物合成糖类在生物体内是通过一系列酶促反应进行合成的,主要包括糖异生和糖原合成两个过程。
糖异生是指通过葡萄糖及其衍生物的代谢途径来合成其他单糖,而糖原合成是指通过多糖合成反应来合成淀粉和糖原。
高中有机化学--糖类.ppt

A、乙醇萄糖
合理膳食
健
经常运动
康 寄
保持身体健康
语
让爱你的人放心
一.糖类的概念及分类 1 .定义: 糖类是指 多__羟_基__醛 多__羟_基_酮_ 以 及能水解生成它们的物质。
说明:(1)糖类是绿色植物光合作用的产
物,糖类不都是甜的。我们食用的蔗糖是甜的, 它只是糖类中的一种。淀粉、纤维素均不甜,但 它们也属于糖类。有些有甜味的物质,如糖精, 不属于糖类。
(3) 葡萄糖的用途
1. 营养 物质
3. 制药 工业
2. 镀银 工业
4、 制酒 工业
【乐于关注】
糖尿病称为现代 疾病中仅次于癌症的 第二杀手,全世界糖 尿病患者约有1.25亿 人,我国的糖尿病患 者已超过4000万人。
防治糖尿病的关 键在哪里?
【善于思考】
合理膳食是防治糖尿 病的关键。
糖尿病人是否就不能 吃甜食了呢?
②此通式适用于大多数糖类化合物,而
对少数糖类物质不适合,如鼠李糖化学式为 ___C_6_H_1_2_O_5____,脱氧核糖化学式为_C__5_H___1_0_O___4_ 。 有些符合此通式的物质并不是糖类,如
__甲__醛___C__H_2_O__,,乙__酸___C_2_H__4O__2_,
___乳__酸___C_3_H__6O__3__等。
③
葡萄糖与新制氢氧化铜反应生 成绛蓝色溶液,加热产生砖红 色沉淀。
分子中含有一个醛 基,且有多个羟基
④ 在一定条件下,1. 80 g (0.01mol) 葡萄糖与0.05mol乙酸完全酯化。
每个分子中含 有5个羟基
⑤ 葡萄糖可以被还原为直链己六醇 6个碳排成直链
关于葡萄糖分子结构的结论:
糖类—单糖(药学有机化学课件)

O C CH CH CH CH CH2OH H OH OH OH OH
u有4个手性碳原子,共有16种对映异构体(8 对)
u构型采用D、L构型标记法
D、L构型法的定义
CHO
H
OH
CH2OH
D-甘油醛
CHO
H
OH
HO
H
H
OH
H
OH
CH2OH
D-葡萄糖
CHO
HO
H
CH2OH
L-甘油醛
CHO
H
H OHale Waihona Puke HO HH OH CH2OH
D-(-)-艾杜糖
CHO H OH H OH HO H H OH
CH2OH
D-(-)-古罗糖
CHO HO H HO H
H OH H OH
CH2OH
D-(+)-甘露糖
CHO H OH H OH H OH H OH
CH2OH
D-(+)-阿洛糖
CHO H OH HO H HO H H OH
CH2OH
D-葡萄糖
CHO HO H HO H
H OH H OH
CH2OH
D-甘露糖
CH2OH CO HO H H OH H OH CH2OH
D-果糖
(二)成脎反应
反应试剂:单糖,过量苯肼
反应方程式:
CHO H OH HO H H OH H OH
CH2OH
H2N NH C6H5
HC N NH C6H5
CH2OH
H5
O OH
H 4 OH H
1
OH 3 H
2H OH
CH2OH
O OH
chap.15 糖类(有机化学)

常 用
chapter 15
8
单糖的开链结构和构型
D型糖与L型糖是对映体,根据D型糖可写出相应的L型糖
CHO H HO H H OH H OH OH CH2OH HO H HO HO CHO H OH H H CH2OH
O C HO H H CH2OH L-(-)-甘油醛
D-葡萄糖
L-葡萄糖
chapter 15
1)用斐林试剂、托伦试剂、班氏试剂氧化
CHO H HO H H OH H OH OH CH2OH Tollens Fehling Benedict' H HO H H COOH OH H OH OH CH2OH
D-葡萄糖
D-葡萄糖酸
还原糖——能与托伦试剂、班氏试剂或费林试剂反应的糖称为还 原糖。(所有的单糖、具有变旋作用的二糖) 非还原糖——不能与上述试剂反应的糖为非还原糖
21
成苷反应
糖苷中,非糖部分叫配糖基,连接配糖基与糖苷基的键叫苷键
CH2OH O O-CH3 OH OH OH
配糖基
苷键 不同的苷键(α-苷键和β-苷键) 需用不同的酶水解
chapter 15
22
糖苷的特点
无色无味晶体,味苦,水溶性大,有旋光性 无变旋现象,不能成脎反应,无还原性 与醚的性质类似,在碱性条件下稳定,在酸性 或酶的催化下易水解 由α-半缩醛羟基形成的苷键称为α- 苷键 由β-半缩醛羟基形成的苷键称为β-苷键 不同的苷键需不同的酶水解
葡萄糖的六元环Haworth结构并不能解释为什么它的两种异 构体在平衡体系中含量不同。吡喃糖六元环与环己烷相似, 分子不是平面结构,椅式构象是稳定构象。
不等性sp3杂化
O
吡喃环
大一有机化学糖类知识点

大一有机化学糖类知识点糖类是生物体内重要的有机化合物,主要由碳、氢、氧三种元素组成。
在大一有机化学课程中,糖类是一个重要的知识点。
本文将介绍大一有机化学中常见的糖类结构、性质以及在生物体内的重要作用。
一、糖类结构糖类按照其所含的单糖分子种类和数量可以分为单糖、双糖和多糖三类。
1. 单糖单糖是由一个单糖分子构成的糖类,常见的单糖有葡萄糖、果糖和核糖等。
这些单糖的结构都是由多个碳原子、氢原子和氧原子组成的环状结构,其中一个碳原子上带有羟基(OH)。
2. 双糖双糖是由两个单糖分子通过酸催化下的缩合反应形成的糖类,常见的双糖有蔗糖、乳糖和麦芽糖等。
双糖的结构由两个单糖分子通过一个氧原子相连形成。
3. 多糖多糖是由多个单糖分子通过缩合反应形成的糖类,常见的多糖有淀粉和纤维素等。
多糖的结构由许多单糖分子通过缩合反应形成的复杂结构。
二、糖类性质1. 溶解性糖类在水中具有良好的溶解性,尤其是单糖和双糖。
这是因为糖类分子中带有许多羟基,使得其与水分子之间能够形成氢键。
2. 光学活性糖类分子中存在手性碳原子,使得糖类具有光学活性。
葡萄糖是最常见的具有光学活性的糖类分子,其有两个立体异构体,分别为D-葡萄糖和L-葡萄糖。
3. 还原性糖类中的单糖具有还原性,可以与硝酸银等强氧化剂反应。
这是因为单糖分子含有还原末端,可以将银离子还原为银颗粒。
三、糖类在生物体内的作用糖类在生物体内起着重要的能量供应和结构支持的作用。
1. 能量供应糖类在细胞内通过糖酵解产生能量。
葡萄糖是细胞内最主要的能量来源,通过糖酵解可以产生大量的三磷酸腺苷(ATP),提供细胞所需的能量。
2. 结构支持糖类在生物体内也起到结构支持的作用。
例如,纤维素是植物细胞壁的重要成分,能够增加植物细胞的稳定性和机械强度。
此外,糖类还参与到DNA、RNA的合成以及免疫反应等生物过程中。
总结:糖类是生物体内重要的有机化合物,在大一有机化学课程中是一个重要的知识点。
我们学习了糖类的结构、性质以及在生物体内的重要作用。
有机化学第16章糖类资料

5
CHO CHOH CH2OH
丙醛糖(甘油醛)
CH2OH CO CH2OH
丙酮糖
CHO CHOH CHOH CHOH CH2OH 戊醛糖
CH2OH CO CHOH CHOH CH2OH 戊酮糖
CHO CHOH CHOH CH2OH
15
β - D-吡喃-果糖
链状费歇尔投影式转变成哈沃斯式 通用写法:
a. 吡喃型
O
O
呋喃型
氧在右上角 碳原子顺时针排列
b.将标准费歇尔式碳键右侧基团或原子写在哈沃斯式环
平面的下方;左侧基团或原子写在环平面上方。
c. D-型糖 ,-CH2OH 环上;半缩醛羟基在环下α,环上β d. L-型糖 ,-CH2OH 环下;半缩醛羟基在环上α,环下β
6
CH2OH O
OH
1
CH2OH
H H
H6
H
5
H
1
O CH2OH
OH 2
5H
OH 2
H4
3 OH
OH
H
α - D-呋喃-果糖
6
CH2OH O
OH
5H
OH 2
H4 OH
3 C1H2OH H
β -D-呋喃-果糖
OH
4
OH
3
OH H
α - D-吡喃-果糖
H
H6
H
5
H
1
O CH2OH
OH 2
OH
4
OH
3
OH H
丁醛糖 CHO CHOH CHOH CHOH CHOH CH2OH 已醛糖
有机化学《糖类》课件

可能存在的形式
鉴别方法
1、碳碳双键 2、醛基 3、羰基
使溴水或高锰酸钾溶液褪色 使溴水褪色、发生银镜反应等
不能发生银镜反应
4、羧基
具有酸的通性,能使指示剂变色
5、酯基 6、环状结构
使含酚酞的NaOH溶液逐渐褪色 难以检测
[活动与探究] P90
实验事实
结论
1 1.80 g葡萄糖完全燃烧,只得到 2.64g二氧化碳和1.08 g水
甜味 甜
甜
甜
不甜 不甜
结构 多羟基醛 多羟基醛 多羟基酮 n个葡萄糖单元
关系
同分异构
不是同分异构
拓展视野:单糖的立体异构
1、什么叫手性?
物质与其镜象的关系,与人的左手、右手一样,非常相似 但不能叠合,因此我们把物质的这种特性称为手性。
2、什么叫对映异构?
结构相同,构型不同并且互呈镜象对映关系的立体异 构现象称为对映异构。
水,等于口服营养液
学以致用
不宜吃糖的时机:
• 饭前吃糖降低食欲 • 睡前吃糖,易形成酸性物质,形成龋齿 • 饱食后再吃糖,会使人发胖,促发糖尿病 • 牙病者吃糖会诱发牙痛 • 糖吃得过多,一部分转化为丙酮酸,使血液显
酸性,人体为了保持弱碱性,要动用钙等碱性 物质去中和过量的酸,可能导致人体缺钙
学以致用
(B )
2.能说明葡萄糖是一种还原性糖,依据是( B)D A.与H2加成生成六元醇 B.能发生银镜反应 C.能发生酯化反应 D.能与新制Cu(OH)2悬浊液共热生成红色沉
淀
3、下列关于葡萄糖的叙述错误的是( B )
A.葡萄糖的分子式是C6H12O6 B.葡萄糖是碳水化合物,因其分子是由6
个碳原子和6个H2O构成 C.葡萄糖是一种多羟基醛,所以既有醇的
化学 糖类知识点总结

化学糖类知识点总结一、基本概念糖是指含有醛基或酮基的碳水化合物。
它们通常是多元醇,也就是含有多个羟基的化合物。
根据碳水化合物的结构特点,糖类可分为单糖、双糖、寡糖和多糖四大类。
1. 单糖单糖是由3-7个碳原子组成的简单碳水化合物,通式为(CH2O)n。
根据其醛基或酮基的位置和数量,单糖又可分为醛糖和酮糖两类。
常见的单糖包括葡萄糖、果糖、半乳糖等。
2. 双糖双糖是由两个单糖分子经由缩合反应形成的碳水化合物,通常由α-1,4-糖苷键或β-1,4-糖苷键连接。
蔗糖、乳糖、麦芽糖等均为常见的双糖。
3. 寡糖寡糖是由3-10个单糖分子经由糖苷键连接而成的碳水化合物,它们具有较复杂的结构和多样的生物活性。
低聚果糖、低聚葡萄糖等都是寡糖的代表。
4. 多糖多糖是由数十至上百个单糖分子经由糖苷键连接而成的碳水化合物,是生物体内最广泛的一类糖类。
淀粉、纤维素、糖原等都属于多糖。
二、分类根据单糖的类型和数量,糖类可分为脱氧糖、醛糖和酮糖三大类。
1. 脱氧糖脱氧糖是指在单糖分子中某些羟基被氢或其他基团所取代,从而形成一种脱氧的糖类。
常见的脱氧糖包括脱氧核糖、脱氧賖和氨基葡萄糖等。
2. 醛糖醛糖是指单糖分子中含有醛基的糖类,通常以醛基为末端。
葡萄糖、半乳糖等都属于醛糖。
3. 酮糖酮糖是指单糖分子中含有酮基的糖类,通常以酮基为末端。
果糖就是一种典型的酮糖。
三、生物学功能糖类在生物体内具有多种重要的生物学功能,主要包括提供能量、构建细胞壁、储存能量和作为通讯信号等。
1. 提供能量糖类是生物体内主要的能量来源之一。
通过细胞代谢途径,单糖分子可以氧化分解成ATP,从而为细胞提供能量。
葡萄糖是最重要的能量来源之一,它在有氧条件下可以完全被氧化分解,释放出大量的能量。
2. 构建细胞壁在植物细胞和真菌细胞中,糖类起着构建细胞壁的重要作用。
纤维素是由葡萄糖分子通过β-1,4-糖苷键连接而成的多糖,在细胞壁中起着支撑和保护细胞的作用。
3. 储存能量动物体内的肝脏和肌肉组织中可以储存糖原,植物体内的叶绿器中可以储存淀粉。
有机化学课后题答案chapter16

第十六章 多步骤有机合成习题解答习题16-1和习题16-2(略)习题16-3OH (1)OH +MgBrH O +BrMg a bab对比a ,b 两种可能的合成途径,b 途径的原料比较难获得,因此,路径a 比较好。
(2)OH ababMgBr+O+BrMg Oc cO+CH 3MgI三种途径中a 途径最佳,原料最大简化。
(3)OHOBr O+MgBr+Oab两种途径都比较简化,反应条件都有无水条件下进行的,因此两条路径相当。
习题16-4所列反应均不能实现。
理由如下:(1)主要形成O(2)缩酮将水解O O或(3)分子内反应为主,生成O O(4)醇将脱水(5)羰基也将被还原OH(6) 醇羟基存在下无法制备格氏试剂(7)醇将水解BrCOO习题16-5机理:OOHR16-6R NH COOH ROHR C OH2OHH- H COHOH R2+CHOOHOH这里相当于一个酰胺水解。
一般总成本在酸性条件下也能进行羰基质子化和接受H2O 的进攻,但烃基是难以离去的。
习题16-7(略)习题16-8(A) H OHCH3CH2CH3Br HCH32CH3PBr3(S)-2-丁醇(R)-2-三溴丁烷(B) H OHCH32CH3H OTsCH32CH3AcO HCH32CH3 TsClpyridineCH3COO(S)-2-丁醇TsO HCH3CH2CH3H BrCH3CH2CH3(1)H2O+OH PBr3习题16-9CH3CH2C CH NaNH2BrCH2CH3CH3CH2C C NaCH3CH2C CCH2CH3HH3CH2C HCH2CH3HH3CH2C CH2CH3H习题16-10(略)习题16-11(P664)(书中题号为16-8)ONO(1)CH 3MgBr 3+习题16-12(P668)(书中题号为16-9)(以R 代表支链)O RCr OO HO 铬酸酯(连氧碳上无H)重排OHOHO Cr OO++H 3O习题16-13(P671)(书中题号为16-10)COOHPhCOOEtPhCH 3COOMe2COOMePh(交叉酯缩合)MeOHSSH2CH 2CH 2COOMePhh vEtO习题16-14(P671)(书中题号为16-11)(逆向思考)1 231'2'3'1233'2'1'OH习题16-15(P671)(书中题号为16-12)OH O+OHTetrahedron Letters, 1993, 34(2), 247~250Tara J. Spules, Jason D. Galpin and Dwight MacdonaldChange-accelerated cope rearrangements of 3-amino-1,5-dienes显然,上述桥环化合物更容易合成得到,可见,重排反应使后一个化合物的合成简化。
有机化学大一糖类知识点

有机化学大一糖类知识点糖类是一类在生物界中广泛存在的有机化合物,它们是构成生物体的重要成分,也是能量的重要来源。
在大一有机化学的学习中,糖类作为一个重要的知识点,需要我们了解其结构、分类和一些重要的反应。
本文将介绍有机化学大一糖类知识点的主要内容。
一、糖类的结构糖类的结构非常多样化,但它们都由一个或多个单糖单元组成。
单糖是最简单的糖类,由3-7个碳原子和伴随的羟基组成。
常见的单糖包括三碳糖丙酮糖、五碳糖葡萄糖和六碳糖果糖等。
多糖是由许多单糖单元通过糖苷键连接而成,如葡聚糖和淀粉等。
二、糖类的分类根据单糖的化学性质,糖类可以分为单糖、双糖和多糖三个类别。
单糖是由一个单糖单元组成,双糖则由两个单糖单元通过糖苷键连接而成,多糖则由许多单糖单元组成。
三、糖类的重要反应1. 缩醛反应:糖类中的部分羟基在酸性条件下可以发生缩醛反应,生成醛酮官能团,这是糖类重要的识别反应之一。
2. 试剂检验:糖类可以通过加入试剂进行检验。
比如用硝酸银试剂检测存在于糖中的醛基,形成银镜反应,可以判断糖的还原性,如果糖和葡萄糖是还原糖。
3. 水解反应:多糖可以通过水解反应将多个单糖单元分解为单糖,如酶催化下的淀粉水解。
酶催化水解是生物体分解多糖的主要途径。
4. 光学活性:糖类中的单糖和双糖分子可以存在手性中心,因而具有旋光性质。
通过旋光仪可以测定旋光度,来判断糖类的旋光性质。
四、糖类在生物体中的作用糖类在生物体中具有重要的作用。
首先,糖类是生物体的主要能量来源,通过糖酵解和呼吸作用释放能量。
其次,糖类参与细胞膜的结构,并参与了生物粘附和识别过程。
此外,糖类还是核酸和脂肪的结构单位,为生物体提供了重要的物质基础。
总结:有机化学大一糖类知识点主要包括糖类的结构、分类和一些重要的反应。
糖类是生物体的重要成分之一,对于生命过程具有重要的作用。
通过学习糖类的知识,我们可以更好地理解生物体的结构和功能,为进一步研究生命科学奠定基础。
以上就是有机化学大一糖类知识点的主要内容。
糖类的化学性质

糖类的化学性质糖是一种广泛存在于自然界的重要有机化合物,它们的化学性质与其结构密切相关。
糖包含羟基、醛基、酮基等官能团,因此在化学反应中极易发生氧化、还原、酸碱水解、缩合等反应。
本文将从这些方面来探讨糖的化学性质。
一、氧化还原反应糖具有重要的还原性质。
在存在比它们还原性更强的还原剂时,糖可以发生氧化反应,同时还原剂被还原成较弱的物质。
对于单糖来说,它们可以在碱性条件下与空气中的氧气发生氧化反应,生成羧酸和醛。
例如,葡萄糖在碱性条件下可被氧化为葡萄糖酸,下面是反应式:C6H12O6 + O2 → C6H10O7 + H2O另一方面,糖还具有重要的还原性质,可以被强氧化剂还原为醇或糖醇。
例如,葡萄糖在浓硝酸的作用下可以被还原为甘露醇:C6H12O6 + 6 HNO3 → C6H14O6 + 6 NO2 + 3 H2O二、酸碱水解糖在弱酸或弱碱条件下可以发生水解反应。
这种水解反应被称为糖水解或糖分解。
在酸性条件下,糖分解产生分子量较小的产物,如果糖和葡萄糖。
在碱性条件下分解,产物主要是己糖和戊糖。
下面是葡萄糖的酸性水解反应:C6H12O6 + H2O → C5H10O5 + C6H12O6在碱性条件下,葡萄糖的水解反应的产物为:C6H12O6 + 2 NaOH → C6H10O5Na2 + 2 H2O三、缩合反应糖分子的羟基和醛基在缩合反应中可以发挥重要作用。
缩合反应是一种重要的糖化学反应,它可以合成二糖、三糖、多糖等复杂化合物。
常见的缩合反应有糖醛基在酸性条件下与羟基缩合形成的糖苷键和异构糖在碱性条件下与羟基缩合形成的糖苷键等。
下面是葡萄糖和果糖缩合形成蔗糖的反应:C6H12O6 + C6H12O6 → C12H22O11 + H2O四、其他反应除以上三类反应之外,还有一些其他的反应也体现了糖的化学性质。
例如,在存在酸催化剂下,葡萄糖和果糖可以发生环化反应,形成半乳糖、伊莫球碱、凝集素等化合物。
此外,还可以通过糖转移酶催化的反应,形成糖链分子,构成多种多样的糖蛋白和糖类化合物。
有机化学基础知识点糖类的结构和性质

有机化学基础知识点糖类的结构和性质糖类是有机化合物中最常见的一类物质,广泛存在于自然界和生物体内。
它们不仅是重要的营养物质,也在生物体内担任着重要的功能角色。
本文将就糖类的结构和性质进行详细的讨论。
一、糖类的结构糖类的基本结构可以归纳为单糖、双糖和多糖三种类型。
单糖是最简单的糖类,包括三种常见的单糖:葡萄糖、果糖和半乳糖。
它们的分子式均为C6H12O6,但它们的结构却有所不同。
葡萄糖和果糖都是环状的结构,而半乳糖则是线性结构。
双糖是由两个单糖分子通过缩合反应形成的,比如蔗糖和乳糖。
多糖是由多个单糖分子缩合而成,常见的有淀粉和纤维素。
二、糖类的性质1. 溶解性: 糖类常用作食品中的添加剂,如砂糖和蜂蜜。
它们具有良好的溶解性,尤其是在水中能够迅速溶解。
这也是为什么糖类常被用于制作饮料、甜点等食品的原因。
2. 甜味: 糖类具有独特的甜味,是许多食物中不可或缺的调味品。
这是由于糖类分子中含有许多羟基,能够与味蕾上的受体相结合,从而引起甜味感觉。
3. 反应性: 糖类具有一定的反应性,可以与其他物质产生化学反应。
例如,糖类能够与氨基酸缩合形成糖基化合物,这在生物体内起着重要的作用。
此外,糖类还可以与氧化剂反应发生糖的焦糖化反应,生成焦糖色素。
4. 发酵性: 糖类可以被微生物发酵产生酒精和二氧化碳。
这也是为什么糖类常被用于酿造过程中的原因。
在酵母菌的作用下,糖类可以转化为乙醇和二氧化碳,并且在此过程中释放能量。
5. 构象异构性: 糖类分子的立体结构存在构象异构性。
例如,在溶液中,葡萄糖分子可以存在α型和β型两种构象。
这种构象异构性对于糖类的生物活性和化学性质都有一定的影响。
综上所述,糖类作为有机化合物的一类,其结构和性质的研究对于我们了解生物体内的基本过程和化学反应机制具有重要意义。
通过对糖类结构和性质的深入研究,我们可以更好地理解糖类在生物体内的作用,从而为相关领域的研究和应用提供基础支持。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
糖类
作者 :
单位 :
目录
第一节 单糖 第二节 双糖和多糖
重点难点
掌握 单糖的定义、分类、结构、构型和开链结构、变旋 光现象和环状结构;单糖的化学性质。
熟悉 常见双糖的结构与性质;常见多糖的结构与特性。
了解 糖类化合物的来源及重要的生物功能。
第一节
单糖
有机化学(第9版)
糖类(saccharide)又称碳水化合物(carbohydrate)。早期发现糖类组成符 合Cn(H2O)m,但随着对糖类研究的深入发现有不少糖类化合物不符合此经验 化学式,如鼠李糖;有些符合此经验式的化合物并不属于糖类,如甲醛、醋酸、 乳酸。
葡萄糖、果糖、蔗糖与 Fehling试剂反应结果
有机化学(第9版)
三、多糖
(一)淀粉
直链淀粉:约占淀粉的20%,能溶于热水,遇碘显蓝色。由D-葡萄
糖经α-1,4΄糖苷键连接。 淀 粉 支链淀粉:约占淀粉的80%,在热水中溶胀成糊状,遇碘显紫红色。
由D-葡萄糖经α-1,4΄和α-1,6΄糖苷键连接。
(一)成酯反应
有机化学(第9版)
四、化学性质
(二)成苷反应
环状糖的半缩醛羟基在酸的催化下,与另一分子中的羟基、氨基或硫羟 基(活泼氢)等失水,生成的失水产物称为糖苷。
D-葡萄糖
苷键
苷键
β-D-甲基葡萄糖苷
α-D-甲基葡萄糖苷
有机化学(第9版)
四、化学性质
(三)成脎反应
单糖与过量的苯肼一起加热作用,生成难溶于水的黄色结晶物质,叫做糖脎。
在化学结构上,糖指多羟基醛(酮),或能水解产生多羟基醛(酮)的化 合物。根据糖类化合物的水解情况,可将其分为单糖、双糖、寡糖和多糖。单 糖指不能被水解的多羟基醛(酮);水解后产生两分子单糖者称为双糖;水解 后生成3~10个单糖的称为寡糖或称低聚糖;完全水解后生成10个以上单糖的 称为多糖。
有机化学(第9版)
D D
有机化学(第9版)
四、化学性质
(六)酸性条件下的脱水反应
有机化学(第9版)
四、化学性质
(六)酸性条件下的脱水反应
第二节
双糖和多糖
有机化学(第9版)
一、双糖
(一)麦芽糖(maltose)
麦芽糖由淀粉水解得到,由D-葡萄糖经α-1,4΄糖苷键连接,具有还原性
及变旋光现象,在酸或酶作用下可水解为葡萄糖。
D-甘油醛 D-glyceraldehyde
L-甘油醛 L-glyceraldehyde
D-(+)-葡萄糖 D-(+)- glucose
L-(-)-葡萄糖 L-(-)- glucose
有机化学(第9版)
D-醛糖系列
有机化学(第9版)
一、构型和开链结构
糖的相对构型 仅有一个手性碳构型不同的非对映异构体,称为差向异构体。
单糖的分类
单糖 官能团
碳数
醛
酮
糖
糖
丙丁 戊己 糖糖 糖糖
醛糖 aldose
费歇尔投影式
己醛糖
己酮糖
戊醛糖
有机化学(第9版)
一、构型和开链结构
糖的相对构型 Fischer投影式中距羰基最远的手性碳的构型为糖的绝对构型,羟基向右为
D型,向左为L型。
C2差向异构 C4差向异构
D
D
D
D
D
D
有机化学(第9版)
二、变旋光现象和环状结构
变旋光现象
+
同一物质的两种晶体比旋光度不同,混合后比旋光度发生变化的现象称为变旋 光现象(mutarotation)。
有机化学(第9版)
二、变旋光现象和环状结构
Haworth式
有机化学(第9版)
二、变旋光现象和环状结构
动态平衡。
有机化学(第9版)
三、物理性质
糖 D-核糖 D-2-去氧核糖 D-葡萄糖 D-果糖 D-半乳糖 D-甘露糖
某些单糖的物理常数
熔点(℃) 87 90 146 104 167 132
比旋光度 -23.7º -59º +52.7º -92.4º +80.2º +14.6º
有机化学(第9版)
四、化学性质
1. 与碱性弱氧化剂反应
碱性弱氧化剂:Tollens试剂, Fehling试剂, Benedict试剂。单糖被氧化成 糖酸,并生成银镜或Cu2O沉淀(砖红色)。
有机化学(第9版)
四、化学性质
(五)氧化反应
2. 与溴水反应(醛糖)
D D
有机化学(第9版)
四、化学性质
(五)氧化反应
3. 与稀硝酸反应
有机化学(第9版)
一、双糖
(一)麦芽糖(maltose)
有机化学(第9版)
一、双糖
(二)纤维二糖(cellobiose)
由D-葡萄糖经β-1,4΄糖苷键连接,具有还原性及变旋光现象,在酸或酶作
用下可水解为葡萄糖。人体内缺乏催化β-1,4΄糖苷键水解的酶,不能将纤维二糖 转变为葡萄糖。
有机化学(第9版)
葡萄糖腙
有机化学(第9版)
四、化学性质
(三)成脎反应
葡萄糖脎
有机化学(第9版)
四、化学性质
(三)成脎反应
两种糖的成脎反应均发生在C1、C2两原子上,且成脎后两种糖的差别消失, 生成同一种糖脎。
果糖脎
葡萄糖脎
有机化学(第9版)
四、化学性质
(四)差向异构化反应
有机化学(第9版)
四、化学性质
(五)氧化反应
为葡萄糖,为生理活动提供能量。糖原存在于动物肝脏和肌肉中,肝脏中含量达 10% ~ 20%,肌肉中含量约4%。易溶于热水成透明胶体。
有机化学(第9版)
三、多糖
(一)淀粉
直链淀粉
淀粉分子与碘作用示意图
有机化学(第9版)
三、多糖
(一)淀粉
支链淀粉
有机化学(第9版)
三、多糖
(一)淀粉
淀粉酶 淀粉
麦芽糖
麦芽糖酶 葡萄糖
有机化学(第9版)
三、多糖
(二)糖原
由D-葡萄糖经α-1,4΄和α-1,6΄糖苷键连接,是动物体内糖的贮存形式,可降解
Haworth式
β-D-吡喃葡萄糖
α-D-吡喃葡萄糖
β-D-glucopyranose α-D-glucopyranose
半缩醛羟基在环平面上方(与C6羟甲基位于同侧)的称为β-异构体,在环 平面下方的称为α-异构体。
有机化学(第9版)
二、变旋光现象和环状结构
Haworth式
D-葡萄糖发生变旋光现象的内在原因是两种端基异构体与开链结构之间处于
一、双糖
(三)乳糖(lactose)
由半乳糖和葡萄糖经β-1,4΄糖苷键连接,具有还原性及变旋光现象。乳 糖存在于动物乳汁中,牛乳中含4 % ~ 5% ,人乳中含5 % ~ 8% ,甜味只 有蔗糖的70%。
有机化学(第9版)
一、双糖
(四)蔗糖
由葡萄糖和果糖经α,β-1,2΄糖苷键连接,不具有还原性 及变旋光现象。
